大学课程《物理化学》各章节知识点汇总
物理化学知识点(全)
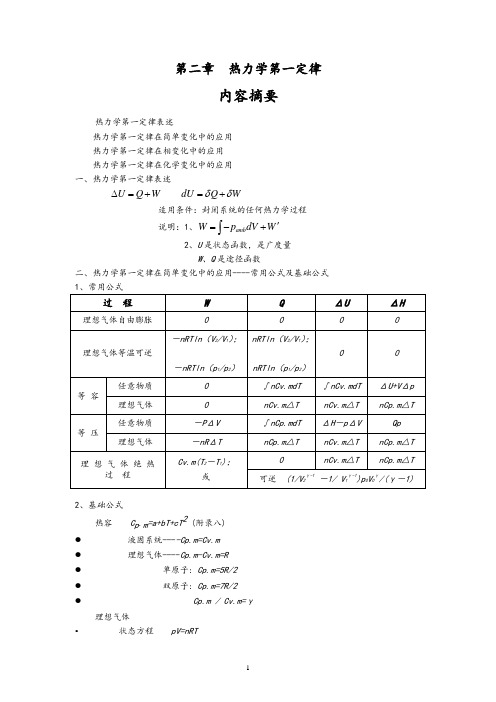
第二章热力学第一定律内容摘要热力学第一定律表述热力学第一定律在简单变化中的应用 热力学第一定律在相变化中的应用 热力学第一定律在化学变化中的应用 一、热力学第一定律表述U Q W ∆=+ dU Q W δδ=+适用条件:封闭系统的任何热力学过程 说明:1、amb W p dV W '=-+⎰2、U 是状态函数,是广度量W 、Q 是途径函数 二、热力学第一定律在简单变化中的应用----常用公式及基础公式 过 程WQΔUΔH理想气体自由膨胀理想气体等温可逆-nRTln (V 2/V 1); -nRTln (p 1/p 2) nRTln (V 2/V 1);nRTln (p 1/p 2)0 0等 容任意物质0 ∫nCv.mdT ∫nCv.mdT ΔU+V Δp 理想气体 0 nCv.m △T nCv.m △T nCp.m △T 等 压任意物质-P ΔV ∫nCp.mdT ΔH -p ΔV Qp 理想气体-nR ΔT nCp.m △TnCv.m △T nCp.m △T 理 想 气 体 绝 热过 程 Cv.m(T 2-T 1);或nCv.m △TnCp.m △T可逆 (1/V 2γ-1-1/ V 1γ-1)p 0V 0γ/(γ-1)2、基础公式热容 C p .m =a+bT+cT 2 (附录八) ● 液固系统----Cp.m=Cv.m ● 理想气体----Cp.m-Cv.m=R ● 单原子: Cp.m=5R/2 ● 双原子: Cp.m=7R/2 ● Cp.m / Cv.m=γ理想气体• 状态方程 pV=nRT• 过程方程 恒温:1122p V p V = • 恒压: 1122//V T V T = • 恒容: 1122/ / p T p T =• 绝热可逆: 1122 p V p V γγ= 111122 T p T p γγγγ--=111122 TV T V γγ--= 三、热力学第一定律在相变化中的应用----可逆相变化与不可逆相变化过程1、 可逆相变化 Q p =n Δ相变H m W = -p ΔV无气体存在: W = 0有气体相,只需考虑气体,且视为理想气体ΔU = n Δ相变H m - p ΔV2、相变焓基础数据及相互关系 Δ冷凝H m (T) = -Δ蒸发H m (T)Δ凝固H m (T) = -Δ熔化H m (T) Δ凝华H m (T) = -Δ升华H m (T)(有关手册提供的通常为可逆相变焓)3、不可逆相变化 Δ相变H m (T 2) = Δ相变H m (T 1) +∫Σ(νB C p.m )dT 解题要点: 1.判断过程是否可逆;2.过程设计,必须包含能获得摩尔相变焓的可逆相变化步骤;3.除可逆相变化,其余步骤均为简单变化计算.4.逐步计算后加和。
物理化学的知识点总结

物理化学的知识点总结一、热力学1. 热力学基本概念热力学是研究能量转化和传递规律的科学。
热力学的基本概念包括系统、环境、热、功、内能、焓、熵等。
2. 热力学第一定律热力学第一定律描述了能量守恒的原理,即能量可以从一个系统转移到另一个系统,但总能量量不变。
3. 热力学第二定律热力学第二定律描述了能量转化的方向性,熵的增加是自然界中不可逆过程的一个重要特征。
4. 热力学第三定律热力学第三定律表明在绝对零度下熵接近零。
此定律是热力学的一个基本原理,也说明了热力学的某些现象在低温下会呈现出独特的特性。
5. 热力学函数热力学函数是描述系统状态和性质的函数,包括内能、焓、自由能、吉布斯自由能等。
二、化学热力学1. 热力学平衡和热力学过程热力学平衡是指系统各个部分之间没有宏观可观察的能量传输,热力学过程是系统状态发生变化的过程。
2. 能量转化和热力学函数能量转化是热力学过程中的一个重要概念,热力学函数则是描述系统各种状态和性质的函数。
3. 热力学理想气体理想气体是热力学研究中的一个重要模型,它通过状态方程和理想气体定律来描述气体的性质和行为。
4. 热力学方程热力学方程是描述系统热力学性质和行为的方程,包括焓-熵图、温度-熵图、压力-体积图等。
5. 反应焓和反应熵反应焓和反应熵是化学热力学研究中的重要参数,可以用来描述化学反应的热力学过程。
三、物质平衡和相平衡1. 物质平衡物质平衡是研究物质在化学反应和物理过程中的转化和分配规律的一个重要概念。
2. 相平衡相平衡是研究不同相之间的平衡状态和转化规律的一个重要概念,包括固相、液相、气相以及其之间的平衡状态。
3. 物质平衡和相平衡的研究方法物质平衡和相平衡的研究方法包括热力学分析、相平衡曲线的绘制和分析、相平衡图的绘制等。
四、电化学1. 电解质和电解电解质是能在水溶液中发生电离的化合物,电解是将电能转化为化学能或反之的过程。
2. 电化学反应和电势电化学反应是在电化学过程中发生的化学反应,电势是描述电化学系统状态的一个重要参数。
物理化学各章知识点总结-86页

经此过程,所有状态函数的变量均为零。
4. 功和热
注意:
W pambdV
• 不论是膨胀还是压缩,体积功都用- pambdV
计算,公式中的压力都用外压
• 公式中的pamb不能随便写到积分号外,只有 常数才行
• 只有- pambdV这个量才是体积功,pambV或 Vdpamb都不是体积功。
不同过程功的计算分析:W p amb V
W pamb dV
(1)环境为真空态(自由膨胀):
pamb= 0,W = 0
(2)恒外压过程(pamb恒定): W = -pambΔV = -pamb(V2-V1)
(3)恒压过程(pamb=p=定值):
W=-p△V
(4)恒容过程(△V =0):
W=0
例如:在298.15 K时
1 2
H2
(g,
p
)
1 2
Cl2
(g,
p
)
HCl(
g,
p
)
反应焓变为:
r
H
m
(298
.15
K
)
92.31kJ.mol 1
这就是HCl(g)的标准摩尔生成焓:
f Hm (HCl, g,298.15K) 92.31kJ.mol1
10.可逆过程与可逆体积功
可逆过程:系统内部及系统与环境之间在无限接近平 衡条件下进行的过程,称为可逆过程,否则称为不可 逆过程。
生成物来表示反应进行的程度,所得的值都是相
同的,即:
d dnD dnE dnF dnG D E F G
当反应按所给反应式的系数比进行了一个单位的化 学反应时,即 nB / mol B,这时反应进度就是1mol。
《大学物理化学》知识点总结

第一章 理想气体1、理想气体:在任何温度、压力下都遵循PV=nRT 状态方程的气体。
2、分压力:混合气体中某一组分的压力。
在混合气体中,各种组分的气体分子分别占有相同的体积(即容器的总空间)和具有相同的温度。
混合气体的总压力是各种分子对器壁产生撞击的共同作用的结果。
每一种组分所产生的压力叫分压力,它可看作在该温度下各组分分子单独存在于容器中时所产生的压力B P 。
P y P B B =,其中∑=BBB B n n y 。
分压定律:∑=BB P P道尔顿定律:混合气体的总压力等于与混合气体温度、体积相同条件下各组分单独存在时所产生的压力的总和。
∑=BB V RT n P )/(3、压缩因子ZZ=)(/)(理实m m V V 4、范德华状态方程 RT b V V ap m m=-+))((2 nRT nb V Van p =-+))((225、临界状态(临界状态任何物质的表面张力都等于0)临界点C ——蒸气与液体两者合二为一,不可区分,气液界面消失; 临界参数:(1)临界温度c T ——气体能够液化的最高温度。
高于这个温度,无论如何加压 气体都不可能液化;(2)临界压力c p ——气体在临界温度下液化的最低压力; (3)临界体积c V ——临界温度和临界压力下的摩尔体积。
6、饱和蒸气压:一定条件下,能与液体平衡共存的它的蒸气的压力。
取决于状态,主要取决于温度,温度越高,饱和蒸气压越高。
7、沸点:蒸气压等于外压时的温度。
8、对应状态原理——处在相同对比状态的气体具有相似的物理性质。
对比参数:表示不同气体离开各自临界状态的倍数 (1)对比温度c r T T T /= (2)对比摩尔体积c r V V V /= (3)对比压力c r p p p /= 9、rr r c r r r c c c T Vp Z T V p RT V p Z =⋅=10、压缩因子图:先查出临界参数,再求出对比参数r T 和r p ,从图中找出对应的Z 。
物理化学知识点总结

第一章 热力学第一定律一、基本概念系统与环境,状态与状态函数,广度性质与强度性质,过程与途径,热与功,内能与焓。
二、基本定律热力学第一定律:ΔU =Q +W 。
焦耳实验:ΔU =f (T ) ; ΔH =f (T ) 三、基本关系式1、体积功的计算 δW = -p e d V恒外压过程:W = -p e ΔV可逆过程:1221ln ln p p nRT V V nRT W ==2、热效应、焓等容热:Q V =ΔU (封闭系统不作其他功) 等压热:Q p =ΔH (封闭系统不作其他功) 焓的定义:H =U +pV ; d H =d U +d(pV )焓与温度的关系:ΔH =⎰21d p T T T C3、等压热容与等容热容热容定义:V V )(T U C ∂∂=;p p )(T H C ∂∂=定压热容与定容热容的关系:nR C C =-V p 热容与温度的关系:C p =a +bT +c’T 2 四、第一定律的应用1、理想气体状态变化等温过程:ΔU =0 ; ΔH =0 ; W =-Q =⎰-p e d V 等容过程:W =0 ; Q =ΔU =⎰T C d V ; ΔH =⎰T C d p 等压过程:W =-p e ΔV ; Q =ΔH =⎰T C d p ; ΔU =⎰T C d V 可逆绝热过程:Q =0 ; 利用p 1V 1γ=p 2V 2γ求出T 2,W =ΔU =⎰T C d V ;ΔH =⎰T C d p不可逆绝热过程:Q =0 ; 利用C V (T 2-T 1)=-p e (V 2-V 1)求出T 2,W =ΔU =⎰T C d V ;ΔH =⎰T C d p2、相变化可逆相变化:ΔH =Q =n Δ_H ;W=-p (V 2-V 1)=-pV g =-nRT ; ΔU =Q +W3、热化学物质的标准态;热化学方程式;盖斯定律;标准摩尔生成焓。
摩尔反应热的求算:)298,()298(B H H m f B m r θθν∆=∆∑反应热与温度的关系—基尔霍夫定律:)(])([,p B C T H m p BB m r ∑=∂∆∂ν。
物理化学知识点归纳

第二章热力学第一定律一、热力学基本概念1.状态函数状态函数,是指状态所持有的、描述系统状态的宏观物理量,也称为状态性质或状态变量。
系统有确定的状态,状态函数就有定值;系统始、终态确定后,状态函数的改变为定值;系统恢复原来状态,状态函数亦恢复到原值。
2.热力学平衡态在指定外界条件下,无论系统与环境是否完全隔离,系统各个相的宏观性质均不随时间发生变化,则称系统处于热力学平衡态。
热力学平衡须同时满足平衡(△T=0)、力平衡(△p=0)、相平衡(△μ=0)和化学平衡(△G=0)4个条件。
二、热力学第一定律的数学表达式1.△U=Q+W或dU=ΔQ+δW=δQ-p amb dV+δW`规定系统吸热为正,放热为负。
系统得功为正,对环境做功为负。
式中p amb为环境的压力,W`为非体积功。
上式适用于封闭系统的一切过程。
2.体积功的定义和计算系统体积的变化而引起的系统和环境交换的功称为体积功。
其定义式为:δW=-p amb dV(1) 气体向真空膨胀时体积功所的计算 W=0(2) 恒外压过程体积功 W=p amb (V 1-V 2)=-p amb △V 对于理想气体恒压变温过程 W=-p △V=-nR △T (3) 可逆过程体积功 W r =⎰21p V V dV(4)理想气体恒温可逆过程体积功 W r =⎰21p V V dV =-nRTln(V 1/V 2)=-nRTln(p 1/p 2)(5)可逆相变体积功 W=-pdV三、恒热容、恒压热,焓 1.焓的定义式H def U + p V 2.焓变(1)△H=△U+△(pV)式中△(pV)为p V 乘积的增量,只有在恒压下△(pV)=p(V 2-V 1)在数值上等于体积功。
(2)△H=⎰21,T T m p dT nC此式适用于理想气体单纯p VT 变化的一切过程,或真实气体的恒压变温过程,或纯的液、固态物质压力变化不大的变温过程。
3. 内能变 (1)△U=Qv式中Qv 为恒热容。
物理化学复习知识点归纳

第二章热力学第一定律1. 系统①隔离系统(孤立系统):没有物质和能量交换 ②封闭系统:只有能量交换③敞开系统(开放系统):既有物质交换,又有能量交换 2. 状态函数分类①广度量(广度性质):与物质数量成正比,有加和性,数学上是一次齐函数 ②强度量(强度性质):与物质数量无关的性质,不具有加和性 *任何两个广度性质之比得出的物理量则为强度量 3.过程分类①恒温过程:T=T 环境=定值②恒压过程:P=P 环境=定值(过程中压强均相等且不变) ③等压过程:P 1 = P 2 = P amb = 常数 ④恒容过程:V=定值⑤绝热过程:系统与环境无热交换,Q=0⑥循环过程:系统从始态出发经一系列变化又回到始态的过 ⑦自由膨胀过程(向真空膨胀):P amb (环境压强)=0 ,δW=0⑧可逆过程:将推动力无限小、系统内部及系统与环境之间在无限接近平衡条件下进行的过程。
即P amb =P 系统+dp ,且d p ≈0 4.功和热 (1)功:途径函数①体积功 W=⎰-2V1V am b dV p ,系统得到环境所作功,W >0;系统对环境作功,W <0②可逆功W=⎰-2V 1V pdV(2)热:途径函数,若系统从环境吸热,Q >0;若系统向环境放热,Q <05.热力学能(内能):指系统内部的所有粒子全部能量的总和,包括系统内分子平动、转动、振动能和势能等,即内能,用U 表示,U=f (T,V ),则有:dV )VU(dT )T U (dU T V ∂∂+∂∂= *理想气体时,U=f (T ),恒温过程,0)VU(T =∂∂,即△U=05.热力学第一定律封闭体系:△U=Q+W 或dU=δQ +δW6.焓 H=U+pV , △H=△U+△(pV )=△U+△(nRT ),H=f (p,T ),则有:dp )PH(dT )T H (dH T p ∂∂+∂∂=, ①凝聚态变化过程时,因△(pV )≈0,故△U ≈⎰=∆2T 1T m ,p dT C n H②理想气体时,H=f (T ),恒温过程,0)VH(T =∂∂,即△U=0 7.恒容热、恒压热①恒容热:Q V =△U 或δQ V = dU (dV=0,W ′=0),即系统进行恒容且无非体积功的过程中与环境交换的热,Q V 只取决于系统的始、末态②恒压热:Q p =△H 或δQ p = dH (恒压dp=0或等压,W ′=0),即系统进行恒压且无非体积功的过程中与环境交换的热,Q V 只取决于系统的始、末态 8.摩尔热容①摩尔定容热容(C V ,m ) 定义式:C V ,m =v m v v )TU ()T U (n 1dT Q n 1∂∂=∂∂=δ,单位:J ·mol -1·K -1应用:理想气体单纯pVT 变化过程dU=dT nC dT )TU(m ,v V =∂∂或⎰=∆2T 1T m,v dT Cn U当恒容时,Q V =⎰=∆2T 1T m ,v dT C n U②摩尔定压热容(C p ,m ) 定义式:C p ,m =p m p p )TH ()T H (n 1dT Q n 1∂∂=∂∂=δ,单位:J ·mol -1·K -1应用:理想气体单纯pVT 变化过程dH=dT nC dT )TH(m ,p p =∂∂或⎰=∆2T 1T m,p dT CnH当恒压时,Q p =⎰=∆2T 1T m ,p dT C n H③C V ,m 与C p ,m 关系C p ,m -C V ,m =p m T m m T V p V U ⎪⎭⎫⎝⎛∂∂⎥⎥⎦⎤⎢⎢⎣⎡+⎪⎪⎭⎫ ⎝⎛∂∂,理想气体:C p ,m -C V ,m =R 常温下,理想气体,单原子C V ,m =R 23,双原子C V ,m =R 259.相变焓①摩尔相变焓:(恒压无非体积功)m ,p m Q H =∆βα;纯物质两相平衡,T 、P 一定,)T (f H m =∆βα同一种物质、相同条件下互为相反的两种相变过程,m m H H αββα∆-=∆②摩尔相变焓随温度的变化:⎰∆+∆=∆TT m ,p 0m m dTC )T (H )T (H βαβαβα10.化学反应焓 (1)反应进度:BBn νξ∆=(2)摩尔反应焓B B m r H H ν∑=∆,)p ,T (f H m r =∆ (3)标准摩尔反应焓①标准态:气态,任意T ,kPa 100p =Θ下表现出理想气体性质的纯气体状态 液体或固体,任意T ,kPa 100p =Θ的纯液体或纯固体状态②标准摩尔反应焓)T ,,B (H )T ,,B (H )T (f )T (H )T (H mC B m f B B B m r βνβννΘΘΘΘ∆∑-=∆∑==∑=∆ 【说明】)T ,,B (H m f βΘ∆摩尔生成热,即1B =ν,稳定相态的单质的)T ,,B (H mf βΘ∆=0 )T ,,B (H mc βΘ∆摩尔燃烧热,即1B -=ν,自然燃烧产物为C →CO 2(g)、H →H 2O (l )、N →N 2(g )、S →SO 2(g ),所以产物CO 2(g)、H 2O (l )、N 2(g )、SO 2(g )等的)T ,,B (H mc βΘ∆=0 ③RT Q Q )g (B m ,v m ,p ν∑=-④)T (f )T (H m r =∆Θ——基希霍夫公式:⎰∆+∆=∆ΘΘTK15.298m ,p r mr m r dT C )K 15.298(H )T (H 或m ,p r m r C dT)T (H d ∆=∆Θ⑤非恒温反应过程热(最高温度)计算恒压燃烧所能达到的最高火焰温度计算依据:Q p =△H=0(恒压、绝热) 恒容燃烧(爆炸)反应所能达到的最高温度依据:Q V =△H=0(恒容、绝热) 11.可逆体积功可逆过程有,P amb =P 系统+dp ≈P 系统 (dp ≈0) 所以 ⎰⎰-=-=2V 1V 2V 1V amb r pdV dV P W①理想气体恒温可逆体积功:21122V 1V 2V 1V r ,T P Pln nRT V V ln nRT dV V nRT pdV W -=-=-=-=⎰⎰②理想气体绝热可逆体积功:理气绝热可逆过程方程式1TV-γ=常数、γpV =常数、γγ-1Tp=常数⎪⎪⎭⎫⎝⎛--=-=--⎰1112112V 1V r ,a V 1V 11V p pdV W λγγγ或)T T (nC U W 12m ,V r ,a -=∆= 12.节流膨胀与焦耳-汤姆逊实验①焦耳-汤姆逊实验:绝热条件下,气体的始末态压力分别保持恒定不变情况下的膨胀过程,称节流膨胀②节流膨胀的热力学特征:节流膨胀为恒焓过程,足够低压的气体(可视为理气)经节流膨胀后温度基本不变。
大学物理化学知识点归纳只是分享

⼤学物理化学知识点归纳只是分享⼤学物理化学知识点归纳第⼀章⽓体的pvT 关系⼀、理想⽓体状态⽅程pV=(m/M )RT=nRT(1.1)或pV m =p (V/n )=RT (1.2)式中p 、V 、T 及n 的单位分别为P a 、m 3、K 及mol 。
V m =V/n 称为⽓体的摩尔体积,其单位为m 3·mol 。
R=8.314510J ·mol -1·K -1称为摩尔⽓体常数。
此式适⽤于理想,近似于地适⽤于低压下的真实⽓体。
⼆、理想⽓体混合物1.理想⽓体混合物的状态⽅程(1.3)pV=nRT=(∑BB n )RTpV=mRT/M mix (1.4)式中M mix 为混合物的摩尔质量,其可表⽰为M mix def∑BByM B(1.5)M mix =m/n= ∑BB m /∑BBn(1.6)式中M B 为混合物中某⼀种组分B 的摩尔质量。
以上两式既适⽤于各种混合⽓体,也适⽤于液态或固态等均匀相混合系统平均摩尔质量的计算。
2.道尔顿定律p B =n B RT/V=y B p (1.7)P=∑BB p(1.8)理想⽓体混合物中某⼀种组分B的分压等于该组分单独存在于混合⽓体的温度T 及总体积V 的条件下所具有的压⼒。
⽽混合⽓体的总压即等于各组分单独存在于混合⽓体的温度、体积条件下产⽣压⼒的总和。
以上两式适⽤于理想⽓体混合系统,也近似适⽤于低压混合系统。
3.阿马加定律V B *=n B RT/p=y B V (1.9)V=∑V B *(1.10)V B *表⽰理想⽓体混合物中物质B 的分体积,等于纯⽓体B 在混合物的温度及总压条件下所占有的体积。
理想⽓体混合物的体积具有加和性,在相同温度、压⼒下,混合后的总体积等于混合前各组分的体积之和。
以上两式适⽤于理想⽓体混合系统,也近似适⽤于低压混合系统。
三、临界参数每种液体都存在有⼀个特殊的温度,在该温度以上,⽆论加多⼤压⼒,都不可能使⽓体液化,我们把这个温度称为临界温度,以T c 或t c 表⽰。
物理化学各章节总结

物理化学每章总结第1章 热力学第一定律及应用1.系统、环境及性质热力学中把研究的对象〔物质和空间〕称为系统,与系统密切相关的其余物质和空间称为环境。
根据系统与环境之间是否有能量交换和物质交换系统分为三类:孤立系统、封闭系统和敞开系统。
性质⎩⎨⎧容量性质强度性质2.热力学平衡态系统的各种宏观性质不随时间而变化,则称该系统处于热力学平衡态。
必须同时包括四个平衡:力平衡、热平衡、相平衡、化学平衡。
3.热与功 (1) 热与功的定义热的定义:由于系统与环境间温度差的存在而引起的能量传递形式。
以Q 表示,0>Q 表示环境向系统传热。
功的定义:由于系统与环境之间压力差的存在或其它机、电的存在引起的能量传递形式。
以W 表示。
0>W 表示环境对系统做功。
(2) 体积功与非体积功功有多种形式,通常涉及到是体积功,是系统体积变化时的功,其定义为:V p W d δe -=式中e p 表示环境的压力。
对于等外压过程 )(12e V V p W --= 对于可逆过程,因e p p =,p 为系统的压力,则有V p W V V d 21⎰-=体积功以外的其它功,如电功、外表功等叫非体积功,以W ′表示。
4.热力学能热力学能以符号U 表示,是系统的状态函数。
假设系统由状态1变化到状态2,则过程的热力学增量为 12U U U -=∆对于一定量的系统,热力学能是任意两个独立变量的状态函数,即 ),(V T f U = 则其全微分为V V U T T U U TVd d d ⎪⎭⎫ ⎝⎛∂∂+⎪⎭⎫ ⎝⎛∂∂=对一定量的理想气体,则有0=⎪⎭⎫⎝⎛∂∂TV U 或 U =f 〔T 〕 即一定量纯态理想气体的热力学能只是温度的单值函数。
5.热力学第一定律及数学表达式 (1) 热力学第一定律的经典描述① 能量可以从一种形式转变为另一种形式,但在转化和传递过程中数量不变。
② “不供应能量而可连续不断做功的机器称为第一类永动机,第一类永动机是不可能存在的。
物理化学复习重点

物理化学总复习 第一章 热力学第一定律δWe= - p e d V d U =δQ +δW基本要求1 熟悉基本概念,系统与环境、状态与状态函数、过程与途径、热和功、准静态过程与可逆过程、能与焓等。
2 掌握各种过程Q 、W 、U ∆和H ∆的计算。
3 掌握应用Hess 定律、生成焓及燃烧焓计算反应热的方法。
4 熟悉反应热与温度的关系,能用基尔霍夫定律求算各温度的反应热。
容提要第二节 热力学基本概念1系统与环境:敞开系统、封闭系统、孤立系统。
2系统的性质 3热力学平衡态 4状态函数与状态方程 5过程与途径 6热和功第三节 热力学第一定律1热力学第一定律 2 热力学能3 热力学第一定律的数学表达式第四节 可逆过程与体积功1体积功 2功与过程 3可逆过程 第五节 焓1焓的定义H=U+ pV2恒容热效应和恒压热效应V Q U =∆ p Q H =Δ 第六节 热容1 热容的定义。
2 定容热容与定压热容V C p C 第七节 热力学第一定律的应用1 热力学第一定律应用于理想气体 2理想气体的C p 与V C 之差 3 理想气体的绝热过程 第八节 热化学1化学反应的热效应 2 反应进度 3 热化学方程式第九节 化学反应热效应的计算1Hess 定律2生成焓和燃烧焓 O mf H ∆ Om c H ∆3反应热与温度的关系——基尔霍夫定律第二章 热力学第二定律d 0Q S Tδ-≥2221,,1112ln ln ln ln V m p m T V T p S nC nR nC nR T V T p ∆=+=+基本要求1理解热力学第二定律的建立过程,S 的引入及引入F 和G 的原因; 2掌握克劳修斯不等式,过程可逆性判断; 3掌握∆S 、∆F 、∆G 在各种变化过程中的计算;变化过程单纯状态函数变化相变化学变化恒温过程恒压过程恒容过程绝热过程恒温恒压可逆相变恒压过程恒容过程可逆过程不可逆过程4理解热力学第三定律及规定熵,掌握在化学变化中标准状态函数的计算;5 掌握吉布斯-亥姆霍兹公式; 容提要第一节自发过程的特征 第二节 热力学第二定律克劳修斯表述“热量由低温物体传给高温物体而不引起其它变化是不可能的”。
大学物理化学知识点总结归纳

大学物理化学知识点总结归纳第一章气体的pvT关系一、理想气体状态方程pV=(m/M)RT=nRT(1.1)或pVm=p(V/n)=RT(1.2)式p、V、T及n的单位分别为P a 、m3、K及mol。
Vm=V/n称为气体的摩尔体积,其单位为m3·mol。
R=8.314510J·mol-1·K-1称为摩尔气体常数。
此式适用于理想,近似于地适用于低压下的真实气体。
二、理想气体混合物1.理想气体混合物的状态方程(1.3)pV=nRT=(∑Bn)RTpV=mRT/Mmix(1.4)式Mmix为混合物的摩尔质量,其可表示为Mmix def ∑BBy M B(1.5)Mmix=m/n=∑BBm/∑Bn(1.6)式MB为混合物某一种组分B的摩尔质量。
以上两式既适用于各种混合气体,也适用于液态或固态等均匀相混合系统平均摩尔质量的计算。
2.道尔顿定律pB=nBRT/V=yBp(1.7)P=∑Bp(1.8)理想气体混合物某一种组分B的分压等于该组分单独存在于混合气体的温度T及总体积V的条件下所具有的压力。
而混合气体的总压即等于各组分单独存在于混合气体的温度、体积条件下产生压力的总和。
以上两式适用于理想气体混合系统,也近似适用于低压混合系统。
3.阿马加定律V B *=nBRT/p=yBV(1.9)V=∑V*(1.10)VB*表示理想气体混合物物质B 的分体积,等于纯气体B在混合物的温度及总压条件下所占有的体积。
理想气体混合物的体积具有加和性,在相同温度、压力下,混合后的总体积等于混合前各组分的体积之和。
以上两式适用于理想气体混合系统,也近似适用于低压混合系统。
三、临界参数每种液体都存在有一个特殊的温度,在该温度以上,无论加多大压力,都不可能使气体液化,我们把这个温度称为临界温度,以Tc 或tc表示。
我们将临界温度Tc时的饱和蒸气压称为临界压力,以p表示。
在临界温度和临界压力下,物质的摩尔体积称为临界摩尔体积,以Vm,c 表示。
大学课程《物理化学》各章节知识点汇总

1. 自由膨胀过程(即外压等于零):
W pedV
W
V2 V1
pedV
0
5
2. 恒定外பைடு நூலகம்膨胀(压缩)过程
a. 一次膨胀过程
p2
p2
膨胀
p1, V1
p2 , V2
p1
W
V2 V1
pedV
p2
p2 (V2 V1)
V1
V2
a ' .一次压缩过程
p1 p1
p2 , V2
压缩
p1, V1 p1
W
A (p1V1)
p
D
A S1(等 温)C S2 (等容) B
S
S1
S2
nR ln
p1
T
T
T
V1
p2
可逆相变过程的熵变
S Qr Qp H TT T
20
变温过程中熵变的计算
Q CdT
dS Q C dT
T
T
等容过程:
dT dS CV T
或
S
C T2
T1 V
dT T
等压过程:
dS
Cp
dT T
或
S
C T2
T1 p
dT T
压力、体积、温度都发生 变化的过程
U QV
T2 T1
CV
dT
等压热效应(p1 p2 pe ) U Q W
U U2 U1 Qp pe (V2 V1)
(U2 p2V2 ) (U1 p2V2 ) Qp
H2 H1 H Qp
dH Qp
Cp
Qp
dT
H T
p
pH Qp
T2 T1
C
物理化学重要知识点总结及其考点说明

第一章气体的pvT关系⑴波义尔定律:当n、T一定时,PV=常数⑵盖-吕萨克定律:当n、P一定时,V/T=常数⑶阿伏伽德罗定律:当T、P一定时,V/n=常数●⑷理想气体状态方程:PV=(m/M)RT= nRT或者或PVm=p(V/n)=RTR=8.314mol-1·K-1称为摩尔气体常数;T为华氏温度⑸摩尔分数:X B=n B/n总●⑹道尔顿定律:P B=P总X B;P总=P分⑺实际气体状态方程:PV=znRT(z为压缩因子)●⑻理想气体特征:①分子间无相互作用力②分子本身不占有体积第二章热力学第一定律热力学第一定律(能量守恒定律)●⑴系统:①隔离系统:无能量、无物质交换②★封闭系统:有能量、无物质交换(热力学基础;热力学研究对象)③敞开系统:有能量、有物质交换●⑵状态函数:P、V、T、U、H、G、A、S (P、T、C p, m、C V,m 为强度量,其他均为广度量) 状态函数特征:①有可微分性,能计算②只与始末状态有关●途径函数:Q、W●⑶热:系统从环境中吸热(Q>0);系统对环境做功(W<0)●⑷热力学能:△U=Q+W(封闭系统);U只是温度T的函数;只与首末有关非体积功的计算①气体向真空膨胀时体积功所的计算W=0②恒外压过程体积功W=-p(V2-V1)=-p△V③对于理想气体恒压变温过程W=-p△V=-nR△T④可逆过程体积功W=-p(v2-v1)●⑤理想气体恒温可逆过程体积功 W=-p(v2-v1)或者W=-nRTln(V1/V2)或者W=nRTln(p2/ p1)⑥理想气体绝热可逆过程体积功W=-p(v2-v1)=(-)γ= C p, m /C V,m(双原子气体为1.4)T2/T1=(V1/V2) 的γ-1次方;T2/T1=(P1/P2)的(γ-1)/γ次方;P2/P1=(V1/V2)的γ次方●⑦恒温膨胀可逆功最大,系统对环境作最大功;恒温可逆压缩,环境对系统做最小功⑧可逆相变体积功W=-pdV恒热容、恒压热,焓⑴焓定义:H=U + PV⑵焓变:△H=△U+△(pV)式中△(pV)为p V乘积的增量,只有在恒压下△(pV)=p(V2-V1)在数值上等于体积功。
大学物理化学笔记总结

⼤学物理化学笔记总结第⼀章物理化学的定义,相变化(物质在熔点沸点间的转化)物理化学的基本组成:1化学热⼒学(⽅向限度)2化学动⼒学(速率与机理)3结构化学物理化学的研究⽅法、热⼒学⽅法、动⼒学⽅法、量⼦⼒学⽅法系统、环境的定义。
系统的分类:开放系统,封闭系统,隔离系统系统的性质:强度性(不可加),⼴延性(可加)。
系统的状态状态函数及其性质:1单值函数2仅取决于始末态3全微分性质。
热⼒学能、热和功的定义热分:潜热,显热。
功分:膨胀功、⾮膨胀功。
热⼒学第⼀定律的两类表述:1第⼀类永动机不可制成。
2封闭体系:能量可从⼀种形式转变为另⼀种形式,但转变过程中能量保持不变。
、恒容热、恒压热,焓的定义。
PV U H def+≡恒容热:①封闭系统② W f =0 ③W e =0 恒压热:①封闭系统②W f =0 ③d p =0 理想⽓体的热⼒学能和焓是温度的函数。
C, C V , C V,m , C P , C P,m 的定义。
△u =n C V,m (T 2-T 1) △H=n C P,m (T 2-T 1) C V,m =a+bT+cT 2+…/ a+bT -1+cT -2+… 单原⼦分⼦C V,m =23R C P,m =25R 双原⼦分⼦C V,m =25R C P,m =27R γ单=35 γ双=57 C P,m - C V,m =R R=·mol -1·k-1可逆过程定义及特点:①阻⼒与动⼒相差很⼩量②完成⼀个循环⽆任何功和热交换③膨胀过程系统对环境做最⼤功,压缩过程环境对系统做最⼩功可逆过程完成⼀个循环△u=0 ∑=0W ∑=0QW 、 Q 、△u 、△H 的计算①等容过程:W=0 Q=△u △u=n C V,m (T 2-T 1) △H=n C P,m (T 2-T 1)②等压过程:W=-Pe(V 2-V 1) Q=△H △u=n C V,m (T 2-T 1) △H=n C P,m (T 2-T 1) ③等温过程:W=-nRTln 12V V Q=-W △u=△H=0④绝热可逆过程:W=n C V,m (T 2-T 1) /??---1112111γγv v v p Q=0 △u=n C V,m (T 2-T 1)△H=n C P,m (T 2-T 1) 21p p =(12v v )γ 21T T =(12v v )1-γ 21T T=(21p p )γγ1-相变化过程中△H 及△u 的计算△u=△H-P △V=△H-nRT 见书1-10 化学计量系数ν化学反应进度??=BνBn ?(必与指定的化学反应⽅程对应)化学反应热效应定义,盖斯定律:⼀个化学反应,不管是⼀步完成或是经数步完成,反应的总标准摩尔焓变是相同的,即盖斯定律。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
pV K
'
TV
1
K
T p
1
K
''
第二章 热力学第二定律
W Q2
可逆热机效率
T2 T1 T1 1 T2 T2
B
熵函数
克劳修斯不等式:
S A B
A
Q
T
0
dS
Q
T
0
熵增加原理: 孤立体系:
nB X B ,m
B 1
i
化学势的定义
GB ,m
G B nB T , p ,n j B
G f (T , p, n1 , n2 , )
G G G G dG dn1 dn2 dp dT T p ,ni p T ,ni n1 T , p ,n j1 n2 T , p ,n j2
H B ,m GB ,m
S B ,m
偏摩尔量的集合公式
dX X1,m dn1 X 2,m dn2 X B,m dnB
B
dX X dn X dn
1, m 1 2, m
2
X i ,m dni
X n1 X1,m n2 X 2,m ni X i,m
可使系统和环境都复原,而没有任何耗散效应。是以无
限小的变化进行,系统始终无限接近平衡态。
第一定律的数学表达式
U Q W
对微小变化: dU Q W 等容热效应
dU Q W
W pdV 0
U QV ,
U QV CV dT
T1 T2
理想气体的绝热过程
Q 0, dU W pdV , dU CV dT
nRT pdV dV CV dT V
V2 T1 (C p CV ) ln CV ln V1 T2 V2 T1 ( 1) ln ln V1 T2
Cp / CV Cp,m / CV ,m
状态和状态函数
系统的一些性质,其数值仅取决于系统所处的状态,
而与系统的经历无关;它的变化值仅取决于系统的
始态和终态,而与变化的途径无关。具有这种特性
的物理量称为状态函数。
热:系统与环境之间因温差而传递的能量称为热, 用符号Q 表示。 系统吸热,Q >0;系统放热,Q <0。
功:系统与环境之间传递能量的方式有热和功,
S绝热 0
S孤立 0
B
自发过程方向的确定:
S系统 S B S A
Qr
T
S孤立=S系统 S环境 0
A
熵变的计算
总则
S环境
Q实际 T环境
理想气体等温过程的熵变
S S B S A
B
Qr
A
Q ( )r T T
Wmax Qr S T T
p1
压缩
W1 '
p2 , V2
压缩pLeabharlann , V 'p' , V '
p1 , V1
W W1 ' W2 '
p1
V1
p ' dV p1dV
V2 V'
V'
p'
p '(V ' V2 ) p1 (V1 V ')
p2
V1 V '
V2
3. 准静态过程
a. 在整个膨胀过程中,外压始终比体系压力小一个无限
《物理化学》 各章节重要知识点
第一章: 热力学第一定律 第二章: 热力学第二定律 第三章: 化学平衡 第四章: 相平衡 第五章: 电化学 第六章: 化学动力学
第一章 热力学第一定律
系统
在科学研究时必须先确定研究对象,把 研究的对象称为系统或体系。
环境 系统以外的与系统相联系的那部分物质 称为环境。
B
VB ,m
V nB T , p ,n jB
H nB T , p ,n jB G nB T , p ,n jB
U B ,m
U nB T , p ,n jB
S nB T , p ,n jB
U dU TdS pdV dnB nB S ,V ,n j B
dU TdS pdV
U U T, p S V ,ni V S ,ni
G U pV TS
dU dG pdV Vdp TdS SdT
p2
膨胀
p2
p2 , V2
p1
p1 , V1
V2
W pe dV
V1
p2
V1
p2 (V2 V1 )
V2
a ' .一次压缩过程
p1
压缩
p1
p1 , V1
p1
p2 , V2
W ' pe dV
V2
V1
p1 (V1 V2 )
p2
V1
V2
b. 多次膨胀过程
p'
p'
H Cp dT T p
T2 T1
15
Qp
p H Qp C p dT
理想气体
U ( )T 0 V
U ( )T 0 p
H H )T 0 ( )T 0 ( p V
理想气体Cp与CV关系
Cp CV nR
Cp,m CV ,m R
S p V T T V
dF SdT pdV
dG SdT Vdp
S V T p p T
理想气体等温变化的ΔG
dG SdT Vdp dG Vdp
G Vdp
p1
p2
p2 p1
p2 nRT dp nRT ln p p1
可逆相变过程的ΔG
dG SdT Vdp
不可逆相变过程的ΔG
G 0
G H2O( g, T , p1 ) H2O(l , T , p1 )
G1
G G1 G2 G3
G3
G2 H2O( g, T , p2 ) H2O(l, T , p2 )
dG SdT Vdp
G G V S , T p ,ni p T , ni
dG SdT VdP B dnB
B
30
U f (S ,V , n1 , n2 , )
U U U U dU dn1 dn2 dS dV S V ,ni V S ,ni n1 S ,V ,n j1 n2 S ,V ,n j2
p2 dp
p2 , V2
压缩
p1
p1 , V1
p1
p2
V1
V2
V1
2
W pe dV
V2
V1
( pi dp)dV V pi dV
V1 V2
三、可逆过程
某系统经一系列的过程后,如果系统回到初始状态叫做
系统的复原;环境在经历一些的变化后,如果既没有功
的得失也没有热的得失就叫做环境的复原。 某系统经一过程由状态1变为状态2之后,如果能使系统
除热以外的其它能量都称为功,用符号W表示。
功可分为体积功和非体积功两大类。 环境对系统作功 W >0 系统对环境作功 W <0
Q和W都不是状态函数,其数值与变化途径有关。
§1-4 可逆过程和体积功
一、体积功
因系统的体积变化而引起的系统与环境之间交换的功称 为体积功。
pe
W Fe dl ( pe A)dl
A (p1V1)
压力、体积、温度都发生 变化的过程 p
D
S1 (等温) S2 (等容) A C B
B (p2V2)
T2
C
T1 V
S S1 S2 nR ln
V2 dT CV V1 T1 T
T2
S '1 (等温) S '2 (等压) A D B
偏摩尔量
X B ,m
X nB T , p ,n jB
X X dX dp X B ,m dnB dT T p ,ni B p T ,ni
等温等压下:
dX X1,m dn1 X 2,m dn2 X B,m dnB
pe d ( Al )
A
dl
pi
pe dV
二、功与过程
功不是状态函数,其数值与过程有关。系统由同一始态
经不同的过程变化到同一终态,则体统对环境或环境对
体系所作的功不同。 1. 自由膨胀过程(即外压等于零):
W pe dV
W pedV 0
V1
5
V2
2. 恒定外压膨胀(压缩)过程 a. 一次膨胀过程
p2
p2
W1
p1 , V1
膨胀
W2
p' , V '
p ', V '
膨胀
p2 , V2
W W1 W2
p1
V2
p ' dV p2dV
V1 V'
V'
p'
p '(V 'V1 ) p2 (V2 V ')
p2
V1 V '
