工业流程题的解题方法
化学工业流程题技巧

化学工业流程题技巧
化学工业流程题是化学工程专业的重要内容,解题的关键在于
掌握一定的技巧和方法。
首先,要熟练掌握化学工业流程的基本原
理和流程图,理解各个单元操作的作用和原理。
其次,要注重细节,特别是对于流程中的关键步骤和关键参数要有深入的了解。
另外,
要善于运用化学工程学的知识,如热力学、物质平衡、能量平衡等
原理,结合具体的流程条件进行分析。
此外,需要注意化学工业流
程中的安全、环保、节能等方面的考虑,这些因素也是解题的重要
依据。
最后,要多做练习,通过大量的题目练习,不断总结经验,
提高解题能力。
在解题过程中,要注意分析问题,理清思路,抓住关键,避免
在细节上纠缠。
对于复杂的流程题,可以采用逐步分析的方法,先
从整体上把握流程的主要特点和关键环节,然后再深入到细节部分
进行分析。
同时,要善于利用图表等工具,直观地展现流程的变化
和关系,有助于理清思路和解题思路。
总之,掌握化学工业流程题的技巧需要全面的化学工程知识作
为基础,结合细致的分析和逻辑思维,多做练习,不断总结经验,
才能在解题过程中游刃有余。
工业流程题解题技巧

高中化学工业流程题也让一部分同学很头疼,除杂,分离提纯等等明明知道这些知识,但是做题却想不起来,不知道该怎样运用它们解题,其实,我们除了了解这些基本知识以外更应该熟悉一些解题技巧,知识不难,主要是考题比较开放,可以联系实际应用进行考察,所以同学们才觉得这些题很难,那么今天小编就给大家总结一些工艺流程题目的解题技巧,觉得好的同学不要忘记分享哦!工艺流程题解题技巧一,除杂、分离、提纯类工艺流程题本质就是对混合物的除杂、分离、提纯。
①首先,找出要得到的主要物质是什么,混有哪些杂质;②然后,认真分析当加入某一试剂后,能与什么物质发生反应,生成了什么产物;③最后,思考要用什么样的方法才能将杂质除去。
这样才能每一步所加试剂或操作的目的。
二、物质制备类工艺流程题①先是确定要制备什么物质,从题干或问题中获取有用信息,了解产品的性质(具有某些特殊性质的产物,要采取必要的措施来避免在生产过程中产生其它杂质,比如:产品受热易分解,可能要低温烘干、减压烘干、减压蒸发等);②分析流程中的每一步骤,从几个方面了解流程:反应物是什么?反应方程式是什么?该反应造成了什么后果?对制造产品有什么作用?③从问题中获取信息,帮助解题。
标准化问题要标准化回答。
题目中的信息往往是制备该物质的关键所在。
产物如果具有某些特殊性质,则要采取必要的措施来避免在生产过程中产生其它杂质。
如:⑴如果在制备过程中出现一些受热易分解的物质或产物,则要注意对温度的控制。
⑵如果产物是一种会水解的盐,且水解产物中有挥发性的酸产生时,则要加相对应的酸来防止水解。
如:制备FeCl3、AlCl3、MgCl2、Cu(NO3)2等物质时,要蒸干其溶液得到固体溶质时,都要加相应的酸或在酸性气流中干燥来防止它水解,否则得到的产物分别是Fe2O3、Al2O3、MgO、CuO;而像Al2(SO4)3、NaAlO2、Na2co3等盐溶液,虽然也发生水解,但产物中Al(OH)3、H2so4、NaHCO3、NaOH都不是挥发性物质,在蒸发时,抑制了盐的水解,最后得到的还是溶质本身。
专题四化学工艺流程题的突破
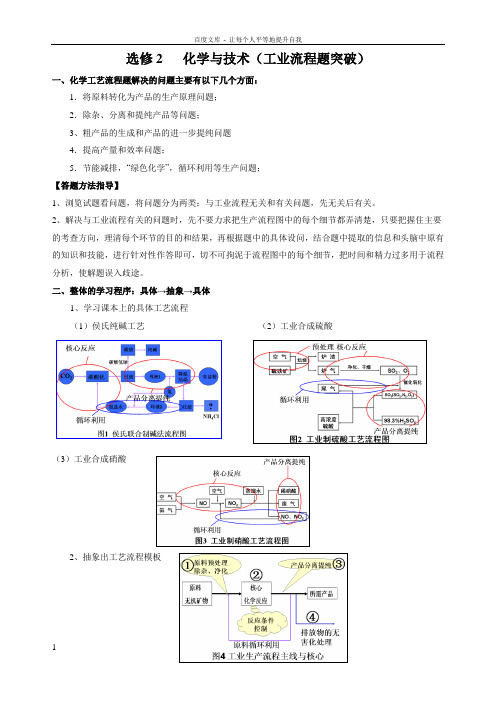
选修2 化学与技术(工业流程题突破)一、化学工艺流程题解决的问题主要有以下几个方面:1.将原料转化为产品的生产原理问题;2.除杂、分离和提纯产品等问题;3、粗产品的生成和产品的进一步提纯问题4.提高产量和效率问题;5.节能减排,“绿色化学”,循环利用等生产问题;【答题方法指导】1、浏览试题看问题,将问题分为两类:与工业流程无关和有关问题,先无关后有关。
2、解决与工业流程有关的问题时,先不要力求把生产流程图中的每个细节都弄清楚,只要把握住主要的考查方向,理清每个环节的目的和结果,再根据题中的具体设问,结合题中提取的信息和头脑中原有的知识和技能,进行针对性作答即可,切不可拘泥于流程图中的每个细节,把时间和精力过多用于流程分析,使解题误入歧途。
二、整体的学习程序:具体→抽象→具体1、学习课本上的具体工艺流程(1)侯氏纯碱工艺(2)工业合成硫酸(3)工业合成硝酸2、抽象出工艺流程模板H 2SO 4浸取滤渣A除铁Fe 2(SO 4)3Fe 屑还原滤渣B浓缩结晶FeSO 47H 2O空气FeOOH除重金属物质C 滤渣DZnSO 47H 2O闪锌矿副产品3、分析以下工业流程的主线和核心步骤,在分析过程中关注以下几个方面:(1) 明确实验的目的 (2) 抓住几条线索 阶段线索 考查侧重 主要目的 1、原料的预处理阶段: 原料、产品 核心化学反应 产物又多又纯 2、杂质的分离与提纯 杂质 分离提纯方法杂质分离彻底 3、粗产品的提取产品产品提取方法及物质循环利用产品的获取【例题】1、(16分)工业上用闪锌矿(主要成分为ZnS ,还含有CdS 、Fe 2O 3等杂质)为原料生产ZnSO 4·7H 2O 的工艺流程如下:(己知Cd 的金属活动性介于Zn 和Fe 之间)2、电镀污泥中含有NiO CuO ZnO O Al OH Cr 、、、、323)(等物质,工业上通过“中温焙烧—钠氧化法”回收722O Cr Na 等物质。
2023年高考山东卷化学解题模型及真题变式题(工业流程题)

高考化学无机化工流程题的解题策略一、解题指导类型一物质制备类化工流程题1. 熟悉常用的操作方法及其作用(1)对原料进行预处理的常用方法及其作用:①研磨——减小固体的颗粒度,增大固体与液体或气体间的接触面积,加快反应速率。
②水浸——与水接触反应或溶解。
③酸浸——与酸接触反应或溶解,使可溶性金属进入溶液,不溶物通过过滤除去。
④灼烧——除去可燃性杂质或使原料初步转化,如从海带中提取碘时的灼烧就是为了除去可燃性杂质。
⑤煅烧——改变结构,使一些物质能溶解。
并使一些杂质在高温下氧化、分解,如煅烧高岭土。
(2)常用的控制反应条件的方法:①调节溶液的pH。
常用于使某些金属离子形成氢氧化物沉淀。
调节pH 所需的物质一般应满足两点:a. 能与H+反应,使溶液pH 增大;b. 不引入新杂质。
例如:若要除去Cu²+中混有的Fe³+, 可加入CuO、Cu(OH)₂、Cu₂(OH)₂CO₃等物质来调节溶液的pH, 不可加入NaOH 溶液、氨水等。
②控制温度。
根据需要升温或降温,改变反应速率或使平衡向需要的方向移动。
③趁热过滤。
防止某物质降温时会析出。
④冰水洗涤。
洗去晶体表面的杂质离子,并减少晶体在洗涤过程中的溶解损耗。
2. 识别流程图化工流程中箭头指出的是投料(反应物),箭头指向的是生成物(包括主产物和副产物),返回的箭头一般是被“循环利用”的物质。
类型二提纯类化工流程题1. 明确常用的提纯方法(1)水溶法:除去可溶性杂质。
(2)酸溶法:除去碱性杂质。
(3)碱溶法:除去酸性杂质。
(4)氧化剂或还原剂法:除去还原性或氧化性杂质。
(5)加热灼烧法:除去受热易分解或易挥发的杂质。
(6)调节溶液的pH 法:如除去酸性溶液中的Fe³+等。
2. 明确常用的分离方法(1)过滤:分离难溶物和易溶物,根据特殊需要采用趁热过滤或者抽滤等方法。
(2)萃取和分液:利用溶质在互不相溶的溶剂里的溶解度不同提取分离物质,如用CCl₄或苯萃取溴水中的溴。
高中化学-化学工业流程图题解题技巧

高中化学-化学工业流程图题解题技巧高中化学化学工业流程图题解题技巧在高中化学的学习中,化学工业流程图题是一类常见且具有一定难度的题型。
这类题目通常以工业生产为背景,将化学知识与实际生产过程相结合,考查同学们对化学原理、实验操作、物质转化等多方面知识的理解和应用能力。
要想在这类题目中取得好成绩,掌握一些有效的解题技巧是至关重要的。
一、认真审题,把握整体拿到一道化学工业流程图题,首先要做的就是认真审题,仔细观察流程图的结构和走向。
了解题目所涉及的工业生产背景,明确生产的目的和主要产品。
同时,注意题目中的文字说明、数据、条件等信息,这些都是解题的关键线索。
在审题过程中,要对整个流程有一个大致的认识,搞清楚原料是什么,经过了哪些主要的反应和操作步骤,最终得到了什么样的产物。
通过这样的整体把握,可以为后续的解题思路奠定基础。
二、分析流程中的关键环节1、原料预处理原料往往需要经过一系列的预处理,如粉碎、溶解、除杂等。
思考这些预处理步骤的目的是什么,比如粉碎可以增大反应物的接触面积,提高反应速率;溶解是为了使反应物在溶液中更好地进行反应;除杂则是为了除去可能影响反应进行或产品质量的杂质。
2、化学反应流程图中会涉及多个化学反应,要弄清楚每个反应的反应物、生成物以及反应条件。
判断反应的类型(如氧化还原反应、酸碱中和反应等),并运用化学平衡、化学反应速率等知识分析反应的进行情况。
3、分离提纯在工业生产中,得到的产物往往需要进行分离提纯,以获得高纯度的产品。
常见的分离提纯方法有过滤、结晶、蒸馏、萃取等。
要理解每种方法的适用条件和原理,根据题目中的具体情况判断应该采用哪种方法。
4、循环利用注意流程图中是否存在物质的循环利用。
循环利用可以提高原料的利用率,降低生产成本,减少废弃物的排放。
分析哪些物质可以循环利用以及循环利用的途径。
三、关注题目中的设问题目中的设问通常是有针对性的,要根据设问的要求有重点地分析流程图。
如果是问某一步骤的作用,就要结合前后的步骤和相关的化学知识进行回答;如果是计算某种物质的含量或产率,就要找出相关的化学反应方程式,利用题目中给出的数据进行计算。
高中有机化学工业流程题解题技巧 -回复

高中有机化学工业流程题解题技巧 -回复
高中有机化学工业流程题解题技巧主要包括以下几点:
1. 理解化学反应机理:在解决有机化学工业流程题时,首先要理解每个化学反应的机理。
这包括了反应物与产物之间的变化过程以及反应条件对反应的影响等内容。
通过理解反应机理,可以把握整个化学过程,有助于解决工业流程题。
2. 熟悉化学反应条件:在工业流程中,许多有机化学反应都需要特定的条件才能进行。
这些条件可能包括温度、催化剂、压力等。
熟悉这些条件并能正确运用它们,对于解题很重要。
3. 分析原料和产品之间的关系:在有机化学工业流程题中,通常会给出一系列原料和产物,要求你找出它们之间的转化关系。
这时,可以通过分析原料和产物之间的相似性和差异性,推测出可能的转化途径。
常用的转化途径包括酸碱中和、氧化还原、取代反应等。
4. 运用有机化学知识:解决有机化学工业流程题,需要熟练掌握有机化学的基本概念和相关知识。
比如,了解官能团的性质及转化途径、认识常用的有机反应等。
有机化学的知识储备越丰富,解题能力就越强。
5. 注重实际应用:有机化学工业流程题主要考察的是解决实际问题的能力。
因此,在解题过程中,要注重从实际角度出发,考虑生产成本、环保性等方面的因素,合理选择合适的反应条件和方法。
总之,解决有机化学工业流程题需要综合运用化学知识、分析能力和实际应用能力。
通过多做练习,提高对有机化学原理的理解和应用能力,就能更好地解决这类题目。
浅析工业流程题解题策略

浅析工业流程题解题策略工业流程题是高中化学中重要的一部分,与其他生物化学和有机化学知识一样,需要掌握具有一定难度的应用能力。
针对工业流程题,我们可以采用以下几点策略来进行解题:1.梳理工业过程全流程工业流程题要求我们对工业生产全过程进行梳理,理解每个步骤的化学意义及操作工艺。
在解决问题过程中,对于生产过程中可能出现的中间化合物及产物,需要掌握其化学性质和物理性质,这有助于我们判断唯一答案的正确性并作出正确的决策。
2.注意反应物和副产物在工业流程中,反应物和副产物可能相当复杂,涉及各种元素、化合物及物质。
针对不同工业生产,如烟气净化、纺织染色等,反应物和副产物都有不同。
在解题过程中,充分了解不同反应物及副产物的性质特点,判断与目标产品的连接程度、反应量、反应时间等,有助于我们准确预估工业生产结果。
3.考虑实际操作的复杂性在工业生产中,可能涉及多种机械、化学和物理操作系统,从各操作部门的安装、调试管理及维修,到操作人员的安全培训和生产工艺的应用细节。
针对实际操作略有复杂性的工业生产工艺,需要加强计算和分析能力,以便系统化地理解实际工业生产的机制及效果。
4.尽可能使用常见化学知识工业流程题本质上是对有机化学、物理化学、生化学等化学知识点的实际应用。
因此,我们需要运用自己具有的化学知识,尽可能少地引入未知资源,以达到精确和可靠的答案。
在解决问题过程中,要有充分的时间和耐心积累,将不断加深思考能力。
工业流程题解题策略不局限于以上四点,面对不同工业生产的需求,应用和掌握不同的化学知识及操作细节是成功解决这一类化学题目的关键。
在实际解题中,我们还可以根据具体情况自由发挥,从而获得更多精彩的思维和探索价值。
初中化学专题三_工业流程图题

为主线,物质随着操作发生变化。
(2)此外,这类题目中通常还包含简单的实验设计,且实验 一般为制备或对样品的定性定量分析实验。
三、化工流程图题型的结构、解题方法和思路 1.化工流程图题型的结构 题头(引入信息)→题干(提取信息,应用解题)→题尾(得出结 论或产品)。
2.解题方法和思路
3.具体操作 (1)关注“箭头”:箭头进入的是投料(即反应物),出去的是
题型 3
化工实验废液
5.兴趣小组的同学在开展“废物利用、减少污染”的活动 中,取某工厂合金废料(含铝、铁、铜)进行如下实验:
过滤 ;该操作需用到的铁制仪器为 (1)操作Ⅰ的名称是________
铁架台(带铁圈) 。 ________________
铁、铜(或 Fe、Cu) ;操作Ⅱ反应的化学 (2)固体 A 的成分是__________________ Fe+H2SO4===FeSO4+H2↑ 。 方程式为:____________________________
高温、高压
(5)将沸点不同的气体分离开来,常采用液化分离法。如控
制温度在-183 ℃时,可将空气中 N2 与 O2 分离。根据下表中物
质的沸点判断,要将产物 NH3 与 N2、H2 分离开来,最适宜的温 - 33.35 ℃。 度应该控制在 ______ 物质 沸点/℃
H2 -252
N2 -195.8
(合理即可 ) (填名称)高温煅烧而得, (2)生石灰可以由碳酸钙 __________ __________
CaCO3=====CaO+CO2↑ 其反应的化学方程式为:______________________________ 。
高温
(3)操作②的名称是蒸发浓缩 ________;结晶得到的固体烧碱中可能
工艺流程题解题技巧专题

工艺流程题解题技巧专题一、【考点分析】无机化工题实际上是考查考生运用化学反应原理及相关知识来解决工业生产中实际问题的能力。
解此类型题目的基本步骤是:①从题干中获取有用信息,了解生产的产品②分析流程中的每一步骤,从几个方面了解流程:A.反应物是什么B.发生了什么反应C.该反应造成了什么后果,对制造产品有什么作用。
抓住一个关键点:一切反应或操作都是为获得产品而服务。
③从问题中获取信息,帮助解题。
了解流程后着手答题。
对反应条件的分析可从以下几个方面着手:对反应速率有何影响?对平衡转化率有何影响?对综合生产效益有何影响?如原料成本,原料来源是否广泛、是否可再生,能源成本,对设备的要求,环境保护(从绿色化学方面作答)。
二、【工业流程题中常用的关键词】原材料:矿样(明矾石、孔雀石、蛇纹石、大理石、锂辉石、黄铜矿、锰矿、高岭土,烧渣),合金(含铁废铜),药片(补血剂),海水(污水)灼烧(煅烧):原料的预处理,不易转化的物质转化为容易提取的物质:如海带中提取碘酸:溶解、去氧化物(膜)、调节pH促进水解(沉淀)碱:去油污,去铝片氧化膜,溶解铝、二氧化硅,调节pH促进水解(沉淀)氧化剂:氧化某物质,转化为易于被除去(沉淀)的离子氧化物:调节pH促进水解(沉淀)控制pH值:促进某离子水解,使其沉淀,利于过滤分离煮沸:促进水解,聚沉后利于过滤分离;除去溶解在溶液中的气体,如氧气趁热过滤:减少结晶损失;提高纯度三、【工业流程常见的操作】(一)原料的预处理①溶解:通常用酸溶。
如用硫酸、盐酸、浓硫酸等。
含有Al2O3的用碱溶解。
②灼烧:如从海带中提取碘③煅烧:如煅烧高岭土改变结构,使一些物质能溶解。
并使一些杂质高温下氧化、分解④研磨:适用于有机物的提取如苹果中维生素C的测定等。
(二)控制反应条件的方法①控制溶液的酸碱性使其某些金属离子形成氢氧化物沉淀——pH值的控制。
调节pH所需的物质一般应满足两点:能与H+反应,使溶液pH值增大不引入新杂质。
高中化学-化学工业流程图题解题技巧

高中化学-化学工业流程图题解题技巧1、工业流程图题做题原则:(1)、首先快速审题,明确实验目的,解决“干什么”(2)、“怎么做”:迅速把握文字材料和方框中有效信息,仔细分析每一步发生的反应及得到的产物。
把产物或得到的滤液、滤渣等成分写在流程图相应位置上。
(3)、遇到不懂的信息或问题可以跳过去,到时再说,有些提供的信息可能在问题中根本没及,有些信息则可以结合问题帮助理解。
(4)、可以在问题中寻找一些相对独立的问题作答,节约审题时间。
2、在化学工业中应考虑的问题,可以归纳如下:①化学反应原理——化学原理在实际工业上是否可行②成本要低——原料的选取使用、设备的损耗等,这是整个过程都需考虑的问题③原料的利用率要高——利用好副产品、循环使用原料、能量尽可能利用④生产过程要快——化学反应速率⑤产率要高——化学平衡⑥产品要纯——产品的分离、提纯⑦环保问题——反应物尽可能无毒无害无副作用,“三废”的处理3、由此,化工题常考查的知识点则总结如下:①化学反应原理——化学(离子)方程式的书写、无机物的性质及制备②化学反应速率原理③化学平衡原理④水解理论⑤化学反应与能量——热量的计算(盖斯定律),电化学(电解、电镀)⑥物质制备和分离的知识——基础实验⑦绿色化学的观点4、工业流程题目在流程上一般分为3个过程:原料处理→分离提纯→获得产品(1)原料处理阶段的常见考点与常见名词①加快反应速率②溶解:通常用酸溶。
如用硫酸、盐酸、浓硫酸等水浸:与水接触反应或溶解浸出:固体加水(酸)溶解得到离子酸浸:在酸溶液中反应使可溶性金属离子进入溶液,不溶物通过过滤除去的溶解过程③灼烧、焙烧、煅烧:改变结构,使一些物质能溶解,并使一些杂质高温下氧化、分解④控制反应条件的方法(2)分离提纯阶段的常见考点①调pH值除杂a.控制溶液的酸碱性使其某些金属离子形成氢氧化物沉淀b.调节pH所需的物质一般应满足两点:能与H+反应,使溶液pH值增大;不引入新杂质。
化学工业流程题解题方法

化学工业流程题解题方法化学工业流程题是近几年高考的热点,在2018年高考化学试题中占分14分,所占分值比较高。
但由于该题目对学生能力要求较大,而且题目考察的内容较多,所以这道题每年的得分情况都不是很乐观。
今天,学姐就说一下我在做工业流程题时总结的一些方法,纯干货,让你的工业流程题轻松拿满分。
做题之前的思想建设工业流程题看名字就知道,你面对的是工厂式生产,不是实验室那种精细的操作流程。
工厂式生产就意味着原料的纯度不高,也就是原料中有杂质,所以,你在做题的时候一定要考虑杂质的存在。
工厂式生产还避免不了的就是成本问题,化工生产不是做实验,化工生产量都比较大,当然是怎么便宜怎么来。
所以做题的时候需要考虑如何实现成本最低,母液的循环再利用和热量的循环再利用等也要考虑进去,一定要实现利益最大化。
另外,你还要知道,化工生产的步骤一定要尽量少,越简单粗暴越好。
这些思想建设是做好工业流程题的基础,你都要知道,但是不用在每次做题之前都乱七八糟想这么一大堆,了解就行。
下面正式进入知识点重新梳理:首先要了解高考化学工业流程题型特点:1.化学工艺流程题由题引、题干和题设三部分构成。
(1)制备型题型特点(2)提纯型题型特点题引一般简单介绍该工艺生产的原材料和生产的目的、产品(包括副产品);题干以工业生产为主要背景,以文字、工艺流程图、表格相结合的形式呈现;题设主要是根据生产过程中涉及的化学知识步步设问,形成与化工生产紧密联系的化工工艺试题,主要涉及原料的选择、循环利用、绿色化学、环境保护、分离提纯、反应原理、实验操作、产率计算等。
2.试题陌生度高,以陌生的新物质为背景,贴近工业生产(如会出现更多的工业术语和设备名称等),试题文字信息量大,综合性强,对能力要求高。
给大家写一些突破技巧:1.解题思路(1)粗读题干,挖掘图示关注关键字,弄懂流程图,但不必将每一种物质都推出,只需问什么推什么。
如制备类无机化工题,可粗读试题,知道题目制取什么、大致流程和有什么提示等。
工业流程题解题技巧

高中化学工业流程题也让一部分同学很头疼,除杂,分离提纯等等明明知道这些知识,但是做题却想不起来,不知道该怎样运用它们解题,其实,我们除了了解这些基本知识以外更应该熟悉一些解题技巧,知识不难,主要是考题比较开放,可以联系实际应用进行考察,所以同学们才觉得这些题很难,那么今天小编就给大家总结一些工艺流程题目的解题技巧,觉得好的同学不要忘记分享哦!工艺流程题解题技巧一、除杂、分离、提纯类工艺流程题本质就是对混合物的除杂、分离、提纯。
①首先,找出要得到的主要物质是什么,混有哪些杂质;②然后,认真分析当加入某一试剂后,能与什么物质发生反应,生成了什么产物;③最后,思考要用什么样的方法才能将杂质除去。
这样才能每一步所加试剂或操作的目的。
二、物质制备类工艺流程题①先是确定要制备什么物质,从题干或问题中获取有用信息,了解产品的性质(具有某些特殊性质的产物,要采取必要的措施来避免在生产过程中产生其它杂质,比如:产品受热易分解,可能要低温烘干、减压烘干、减压蒸发等);②分析流程中的每一步骤,从几个方面了解流程:反应物是什么?反应方程式是什么?该反应造成了什么后果?对制造产品有什么作用?③从问题中获取信息,帮助解题。
标准化问题要标准化回答。
题目中的信息往往是制备该物质的关键所在。
产物如果具有某些特殊性质,则要采取必要的措施来避免在生产过程中产生其它杂质。
如:⑴如果在制备过程中出现一些受热易分解的物质或产物,则要注意对温度的控制。
⑵如果产物是一种会水解的盐,且水解产物中有挥发性的酸产生时,则要加相对应的酸来防止水解。
如:制备FeCl3、AlCl3、MgCl2、Cu(NO3)2等物质时,要蒸干其溶液得到固体溶质时,都要加相应的酸或在酸性气流中干燥来防止它水解,否则得到的产物分别是Fe2O3、Al2O3、MgO、CuO;而像Al2(SO4)3、NaAlO2、Na2CO3等盐溶液,虽然也发生水解,但产物中Al(OH)3、H2SO4、NaHCO3、NaOH 都不是挥发性物质,在蒸发时,抑制了盐的水解,最后得到的还是溶质本身。
高中化学工业流程题答题技巧

高中化学工业流程题答题技巧化学作为一门实践性很强的科学,是高中化学教学中非常重要的一个部分。
在高考中,经常会遇到关于化学工业流程的问题,这种题型对学生的实际动手操作能力以及对化学原理的理解有着较高的要求。
下面,我将介绍一些高中化学工业流程题答题技巧,希望能对广大学生有所帮助。
首先,我们需要掌握化学工业流程的基本模式。
一般来说,化学工业流程可以分为输入物质、反应过程和产物三个部分。
解答化学工业流程题时,需要关注这三个方面。
输入物质通常是反应物和催化剂,反应过程则涉及到反应条件和反应机理,最后产物则是反应得到的化合物。
其次,答题时要注重分析问题的关键点。
在化学工业流程题中,往往会强调某个特定的条件、催化剂或反应物的选择。
我们需要准确地理解这些关键点,并将其应用到题目中。
同时,要注意题目中可能存在的隐含信息,例如反应过程中可能涉及到的催化剂的选择、反应物的摩尔比等。
另外,建议学生们在解答化学工业流程题时养成绘制反应示意图和计算所需物质摩尔比的习惯。
绘制反应示意图可以帮助学生更加清晰地理解整个反应过程,并减少因错误包括或漏掉某些物质而引起的错误。
计算所需物质摩尔比则是解答化学工业流程题的关键步骤,要准确地根据化学方程式和所给条件计算所需物质的摩尔比。
此外,学生们还要学会应用化学原理来解答化学工业流程题。
例如,根据颜色的变化判断某个物质是否进入反应,根据气体的生成确定产物等。
对于有机合成反应,要熟悉常见的有机反应机理和反应条件,以便在解答题目时能够准确地推断产物和判断反应条件。
最后,多做习题是提高解答化学工业流程题能力的有效方法。
通过多做习题,可以加深对化学工业流程的理解,熟悉不同类型题目的解题思路和解题技巧。
同时,还可以发现自己的不足和问题,并及时进行总结和反思,进一步提高自己的解题能力。
总之,化学工业流程题在高中化学考试中占据着重要的地位。
通过掌握化学工业流程的基本模式,注重分析问题的关键点,掌握化学原理,绘制示意图和计算摩尔比,以及多做习题等技巧,可以帮助学生提高解答化学工业流程题的能力,更好地应对高考化学试题。
初三化学九年级下册一模复习《工业流程图专题》知识点归纳学案与练习题专题

工艺流程图专题一、工艺流程路线示意图箭头:进入的是投料(即反应物),出去的是生成物(包括主产物和副产物)。
出线、进线:表示物料流向或操作流程;反向线:表示物质循环使用;方框:表示经过反应或操作后剩余的物质。
二、工艺流程题的解题方法与策略1.一般采用首尾分析法,明确原始物质及目标产物2.读流程,观其大略,找出流程主线(即从流程开始到达产品或是达成实验目的的为主线,其他的是支线,如上图)。
3.常考的操作术语及目的:(1)对原料进行预处理的常用方法及其作用①粉碎(研磨):增大反应物的,加快或使反应。
②灼烧(煅烧):使固体在高温下分解或使杂质在高温下氧化、分解等。
使反应充分进行或增大转化率。
(2)明确常用的分离方法①过滤:和的分离。
所需仪器有铁架台(带铁圈)、滤纸、。
洗涤:尽量除去晶体表面的杂质或干扰物质。
干燥:除去固体中的水。
4.答题技巧:(1)所设问题一般都是孤立的,在解答时不要求流程全看懂后再解答,看不懂的地方先跳过去,继续解答后面的问题。
有时候可以直接使用“节点法”进行解题,即进入“节点”的物质是反应物,流出“节点”的是生成物。
(2)抓住一个关键点:一切反应或操作都是为了获得产品或是达成实验的目的。
(3)推断流程图某一步中的物质,可以从上一步操作中反应物可能发生的反应入手进行分析,同时需注意所加试剂是否有过量(剩余),要关注物质在流程“节点”中转移情况(三大转移):反应产物转移;不反应物质转移和过量物质转移。
(4)陌生化学方程式的书写:根据箭头方向,箭头进入的是投料(即反应物),出去的是生成物(包括主产物和副产物);若从已知信息中找出的反应物和生成物不满足质量守恒定律,可以在反应物或生成物中加上水,然后进行配平,还应注意反应条件的有关信息;若在空气中煅烧或通入空气则还需考虑空气中的氧气是否参与反应。
(5)循环利用的物质:某物质不在流程的主线上而在流程的支线上,它是某一步骤中的产物同时也是另一步骤中的原料,它即是这个流程中的循环利用物质。
高中化学无机化工业流程题的高考命题特点和解题方

高中化学无机化工业流程题的高考命题特点和解题方法!无机化工流程题的特点:规律:主线主产品、分支副产品、回头为循环。
核心考点:物质的分离操作、除杂试剂的选择、生产条件的控制。
1. 流程的呈现主要有以物质转化为主线,以操作过程为主线,甚至有时候会以设备为主线。
2. 这类题常围绕以下几个知识点进行设问:⑴反应速率与平衡理论的运用反应物颗粒大小:反应速率、原料的利用率等温度:反应速率、物质的稳定性、物质的结晶等⑵氧化还原反应的判断、化学方程式或离子方程式的书写;⑶利用控制pH分离除杂;⑷化学反应的能量变化;⑸实验基本操作:除杂、分离、检验、洗涤、干燥等;⑹流程中的物质转化和循环,资源的回收和利用;⑺环境保护与绿色化学评价。
01原料处理的方法和作用对原料进行预处理的常用方法及其作用:1. 粉碎、研磨:减小固体的颗粒度,增大固体与液体或气体间的接触面积,加快反应速率。
2. 水浸:与水接触反应或溶解。
3. 酸浸:通常用酸溶,如用硫酸、盐酸、浓硫酸等,与酸接触反应或溶解,使可溶性金属离子进入溶液,不溶物通过过滤除去。
近年来,在高考题出现了“浸出”操作。
在化工生产题中,矿物原料“浸出”的任务是选择适当的溶剂,使矿物原料中的有用组分或有害杂质选择性地溶解,使其转入溶液中,达到有用组分与有害杂质或与脉石组分相分离的目的。
4. 浸出率:固体溶解后,离子在溶液中含量的多少(更多转化)。
5. 灼烧:除去可燃性杂质或使原料初步转化,如从海带中提取碘时的灼烧就是为了除去可燃性杂质,将有机碘转化为碘盐。
6. 灼烧、焙烧、煅烧:改变结构和组成,使一些物质能溶解;并使一些杂质在高温下氧化、分解,如煅烧高岭土和石灰石。
02掌握核心化学反应1. 元素及其化合物知识:化工生产将原料转变成产品的过程,也是物质经。
工业流程题解题方法

工业流程题解题方法一、熟悉工业流程的几个常用的关键词1、浸出:固体加入水或酸溶解得到离子。
2、酸浸:指在酸溶液中反应使可溶金属离子进入溶液,不溶物通过过滤除去溶解的过程。
3、水洗:水洗通常是为了除去水溶性的杂质。
有机物洗涤:减少晶体损失4、灼烧(煅烧):原料的预处理,不易转化的物质转为容易提取的物质:如海带中提取碘等5、酸作用:溶解、去氧化物(膜)、调节PH促进水解(沉淀)6、碱作用:去油污,去铝片氧化膜,溶解铝、二氧化硅,调节PH促进水解(沉淀)7、氧化剂:氧化某物质,转化为易于被除去(沉淀)的离子8、控制PH值:促进某离子水解,使其沉淀,利于过滤分离9、煮沸:促进水解,聚沉后利于过滤分离;除去溶解在溶液中的气体,如氧气10、趁热过滤:减少结晶损失;提高纯度二、工业流程中的主要操作:结晶、重结晶、洗涤、干燥、灼烧、分液、重复操作2-3次等如结晶的几种方法:(1)、当溶液是单一溶质时①、所得晶体不带结晶水(如NaCl、K NO3):蒸发、结晶②、所得晶体带结晶水:蒸发浓缩(至有晶膜出现为止),冷却结晶,过滤(2)当溶液中有两种或以上溶质时要得到溶解度受温度影响小的溶质:浓缩(结晶),趁热过滤要得到溶解度受温度影响大的:蒸发浓缩,冷却结晶1、首尾分析法:对一些线型流程工艺(从原料到产品为一条龙生产工序)试题,首先对比分析生产流程示意图中的第一种物质原材料与最后一种物质产品,从对比分析中找出原料与产品之间的关系,弄清生产流程过程中原料转化为产品的基本原理和除杂分离提纯产品的化工工艺,然后再结合题设的问题,逐一推敲解答.例1、(09上海)实验室用大理石等原料制取安全无毒的杀菌剂过氧化钙。
大理石的主要杂质是氧化铁,以下是提纯大理石的实验步骤:(1)、溶解大理石时,用硝酸而不同硫酸的原因是。
(2)、操作Ⅱ的目的是,溶液A(溶质是共价化合物)是。
(3)、写出检验滤液中是否含铁离子方程式:。
(4)、写出加入碳酸铵所发生反应的离子方程式:。
高中化学工业流程题答题技巧_概述说明以及解释

高中化学工业流程题答题技巧概述说明以及解释1. 引言1.1 概述本文主要讨论高中化学工业流程题的解题技巧和方法。
在高中化学考试中,工业流程题占据了重要位置,需要阐述化学反应、原理和实践应用等多个方面的知识。
因此,掌握正确的答题技巧对于提高成绩至关重要。
1.2 文章结构本文分为五个部分。
首先是引言部分,概述文章的主要内容以及目的。
接下来是高中化学工业流程题答题技巧的详细阐述,包括了解基本概念、掌握常见化学反应方程式和理解工业流程原理等。
第三部分解释了高中化学工业流程题的重要性,包括实践意义、考试应用性以及对个人学习的促进作用等方面。
然后是解答高中化学工业流程题的技巧和方法,其中包括抓住关键信息点、利用知识链条思维法和考虑实际情境因素进行推理与解答等内容。
最后是结论部分,总结了要点和技巧应用意义,并鼓励读者进行更多实践与训练以提高解题能力和熟练度,并展望了未来的应用前景和发展趋势。
1.3 目的本文旨在帮助高中化学学习者掌握解答高中化学工业流程题的技巧和方法。
通过详细阐述基本概念、常见化学反应方程式和工业流程原理,读者将能够更好地理解和分析工业流程的各个环节。
此外,我们将解释这类题目的重要性,并提供相关技巧和方法,希望能够有效促进读者在考试中取得更好的成绩。
最后,本文还将对未来高中化学工业流程题的应用前景和发展趋势进行展望,为读者进一步深入研究该领域提供参考。
2. 高中化学工业流程题答题技巧2.1 了解基本概念在回答高中化学工业流程题时,首先需要对相关的基本概念有一定的了解。
这包括了解不同化学反应的类型(如酸碱反应、氧化还原反应等)以及它们的特点和条件。
此外,还应熟悉常见元素和化合物的性质、结构和用途等基本知识。
2.2 掌握常见化学反应方程式高中化学工业流程题通常会涉及一系列的化学反应,因此掌握常见的化学反应方程式是非常重要的。
这样可以帮助我们理解不同反应之间的关系,并更好地分析和解决问题。
2.3 理解工业流程原理对于高中化学工业流程题,了解其背后的工业原理也很关键。
化学工业流程题解题方法

化学工业流程题解题方法化学工业流程题是近几年高考的热点,在2018年高考化学试题中占分14分,所占分值比较高。
但由于该题目对学生能力要求较大,而且题目考察的内容较多,所以这道题每年的得分情况都不是很乐观。
今天,学姐就说一下我在做工业流程题时总结的一些方法,纯干货,让你的工业流程题轻松拿满分。
做题之前的思想建设工业流程题看名字就知道,你面对的是工厂式生产,不是实验室那种精细的操作流程。
工厂式生产就意味着原料的纯度不高,也就是原料中有杂质,所以,你在做题的时候一定要考虑杂质的存在。
工厂式生产还避免不了的就是成本问题,化工生产不是做实验,化工生产量都比较大,当然是怎么便宜怎么来。
所以做题的时候需要考虑如何实现成本最低,母液的循环再利用和热量的循环再利用等也要考虑进去,一定要实现利益最大化。
另外,你还要知道,化工生产的步骤一定要尽量少,越简单粗暴越好。
这些思想建设是做好工业流程题的基础,你都要知道,但是不用在每次做题之前都乱七八糟想这么一大堆,了解就行。
下面正式进入知识点重新梳理:首先要了解高考化学工业流程题型特点:1.化学工艺流程题由题引、题干和题设三部分构成。
(1)制备型题型特点(2)提纯型题型特点题引一般简单介绍该工艺生产的原材料和生产的目的、产品(包括副产品);题干以工业生产为主要背景,以文字、工艺流程图、表格相结合的形式呈现;题设主要是根据生产过程中涉及的化学知识步步设问,形成与化工生产紧密联系的化工工艺试题,主要涉及原料的选择、循环利用、绿色化学、环境保护、分离提纯、反应原理、实验操作、产率计算等。
2.试题陌生度高,以陌生的新物质为背景,贴近工业生产(如会出现更多的工业术语和设备名称等),试题文字信息量大,综合性强,对能力要求高。
给大家写一些突破技巧:1.解题思路(1)粗读题干,挖掘图示关注关键字,弄懂流程图,但不必将每一种物质都推出,只需问什么推什么。
如制备类无机化工题,可粗读试题,知道题目制取什么、大致流程和有什么提示等。
工业流程题方法

工业流程题方法我跟你说啊,工业流程题这事儿,我一开始也是瞎摸索。
我就看着那题里一堆箭头啊,物质啊,反应啊,脑袋直发懵。
最初我就死记硬背,想着把那些常见的工业流程都背下来,什么制硫酸的流程啦,炼铁炼钢的流程啦。
结果一到考试,稍微变点样我就傻了,这方法真不咋靠谱。
后来我就试着从物质的转化入手。
就好比你这有一堆原材料,假如是一堆矿石,要把里面有用的金属弄出来,就像从一堆果壳里把果仁取出来一样。
我就先找流程开始的物质,看看它都能变成啥。
比如说一块铁矿石,你得知道它可能在高温下被还原剂还原,那就得知道什么样的还原剂合适,反应会生成什么副产物。
这个时候我就会在草稿纸上把可能的反应一个个写下来,就算不完全对,但至少自己思路清晰许多。
我还犯过一个错误呢,就是光看那些主要的反应物,忽略了杂质。
有一回做一道关于提纯啥物质的题,我光顾着计算主要物质的一系列反应了,完全没把其中的杂质考虑进去。
结果最后答案跟实际差了十万八千里。
这就告诉我啊,工业流程题一定要看清楚有没有杂质,那些杂质在流程里可能会参与什么反应,是要被除掉啊,还是会产生什么影响。
流程中的反应条件也特别重要。
就像做菜,不同的菜需要不同的火候和调料一样,化学物质之间的反应也需要合适的条件。
我现在做工业流程题,都会特别留意反应是在高温下,还是常温下,有没有催化剂啥的。
因为这个往往会直接影响反应能不能发生,还有产物是什么。
再比如,有的反应需要在酸性或者碱性条件下进行,这既是解题的线索,也是需要注意的点,要是在流程里看到什么酸或者碱的加入,就得琢磨琢磨是为啥了。
还有哦,关于工业流程题里的循环物质。
这要是没弄明白,损失可就大了。
我记得有一种流程是生产某种碱,中间产生的二氧化碳可以回用,这回用的部分既节省成本又环保。
你要是没看到这个循环利用的部分,整个计算或者流程分析可能就错了。
所以做工业流程题的时候,一定要睁大眼睛,看看有没有哪个物质打了个回流箭头,又回来重新参与反应了。
工业流程题技巧

工业流程题技巧今天来聊聊工业流程题的一些实用技巧。
我当年上学的时候,工业流程题可把我给愁坏了。
就像面对一个特别复杂的迷宫,到处都是弯弯绕绕,完全不知道从哪儿下手。
有一次考试,遇到一道关于金属冶炼的工业流程题,我一看题就懵了,结果那道题得分特别低。
这之后我才下定决心研究一下这类题的解法技巧。
首先呢,做这类题目你得有个整体的思路,就跟搭房子似的,先要有一个框架。
看工业流程题一定要先看清楚原料和目标产物是什么。
这就好比你要做饭,先得清楚你有什么食材,要做出什么菜。
比如说原料是某种矿石,目标产物是某种金属单质,那你就要顺着这个思路,思考中间可能需要的化学反应。
对了,还有个事儿要说。
在看流程的时候,要特别关注那些“进出口物质”,就像家里的大门一样,进进出出的东西肯定重要。
某个物质进来后变成了什么?或者发生了什么变化才产生新的物质出去?这往往就是解题的关键。
这里我有个小教训,有次做题没注意进口物质在流程中发生了很细微的变化,结果纠缠了半天还是选错了答案。
说到这里,我想起在分析化学反应的时候啊,那些陌生方程式的书写常常让人头疼。
其实呢,你可以根据流程里的信息写出主要产物和反应物,就像填空一样。
比如说看到一种物质和酸反应了,那很可能会有盐和水之类的产物,再根据元素守恒和化合价啥的去调整系数。
这就像拼拼图一样,一块一块找到合适的地方塞进去。
不过呢,实话讲,这些技巧也有局限性。
有时候遇到特别复杂的流程,光是理清楚思路还不够,可能还需要对工业上的一些特殊知识有所了解。
要是碰到这样的情况,那你可以把它记下来当作知识储备,或者联想你之前做过的类似题目有没有相似的细节。
你可能会问,如果遇到完全没见过的流程怎么呢?这时候不要慌,就从最基础的物质性质开始分析。
比如说这种物质是酸性的还是碱性的,能不能和其他物质发生反应,把自己当成一个小发明家去想象反应的可能性。
工业流程题的解题是有章可循的,但也需要不断积累。
要是你也有什么特别的解题小妙招,欢迎交流哦,咱们可以互相学习。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
海水 制卤素
性质探究
氯气 性质
钠的 性质
镁的 性质
碳酸钠 性质
溴、碘 性质
实际应用
生产和生活等领域的应用
精品
工业制备
电解 铝
铁的 冶炼
铜的 精炼
硅的 制备
性质探究
铝 氧化铝 氢氧化铝
铁 Fe3+ Fe2+
硅
铜
二氧化硅
硅酸盐
社会应用
生产和生活等领域的应用
精品
27.硼及其化合物在工业上有许多用途。以 铁硼矿(主要成分为Mg2B2O5·H2O和Fe3O4,还 有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原 料制备硼酸(H3BO3)的工艺流程如图所示:
(一) 反应原理 •氧化还原反应 •离子反应 •反应速率 •化学平衡 •溶液中离子平衡
精品
(二)物质(离子)性质和反应 •氧化性、还原性 •酸、碱性 •特性 (三)混合物的分离 •分离方法 •分离装置 •实验操作……
精品
(四)关注课本内的工业生产原型 1.天然水的净化和软化 2.海水的综合利用 • 海水制盐 • 氯碱工业 • 海水提溴 • 海水提镁 3.石油和煤的综合利用 • 石油的分馏 • 煤的干馏
SO2与H2O反应 SO2与O2反应 O2、S、SO2、 浓H2SO4的氧化 性;H2S、 Na2SO3的还原 性;O3、H2O2 的性质
Cl2与H2O 反应
X2的氧化性,X的还原性; HClO的漂白 性,F2与H2O 反应
平衡移 动原理
代表物 的典型 反应
电解 质 溶液
H2CO3的电离 CO32-、HCO3的水解 CH3COOH 为一元弱酸
精品
回答下列问题: (1)写出 与硫酸反应的化学方程式 。为提 高浸出速率,除适当增加硫酸浓度外,还可采 取的措施有 (写出两条)。 (2)利用 的磁性,可将其从“浸渣”中分 离。“浸渣”中还剩余的物质是 。(写化学 式) (3)“净化除杂”需先精品加 溶液,作用是 。
(4)“粗硼酸”中的主要杂质是 (填名 称)。 (5)以硼酸为原料可制得硼氢化钠(NaBH4 ), 它是有机合成中的重要还原剂,其电子式为 。 (6)单质硼可用于生产具有优良抗冲击式表示制备过程 。
金属的冶炼、废物回收利用
水资源 工艺
海水综合利用、污水处理
精品
整理所学教材上涉及的相关工业
海水综合利用 必修2第页
精品
精品
碳族
氮族
氧族
卤素
备注
化学 平衡
氧化 还原 反应
CO2与H2O反 应
C、CO、CO2 三角关系 提纯硅; 水煤气
合成氨; 氨溶于水
NH3的还原性 NO2与水反应 HNO3的强氧 化性
NH4+水解 NH3·H2O为 一元弱碱
S2-、SO32-的水 解,H2SO4、 NaHSO4强酸 性,H2SO3的电 离
HClO的电离
重点是 电离、 水解
周期 各族元素周期表的位置、主要化合价、原子半径、核外电子排布、性质的相 律 似性和递变性。
精品
工业生产
电解 食盐水
电解 氯化钠
海水 提镁
侯氏 制碱
关注——反应条件的控制 •温度 •压强 •催化剂 •原料配比 •溶液的pH调节 •溶剂的选择
精品
关注——流程图或题目中前后物质状态和成分 的变化
精品
四、核心考点
• 混合物分离操作 • 除杂试剂的选择 • 有关转化或分离的反应 • 有关反应原理的问题
精品
五、解决问题的能力
• 课内知识的迁移思维 • 逻辑思维 • 发散思维和收敛思维 • 综合能力
工业流程题的解题方法
高三
精品
• 工业题——是关注与化学有关的科学技术、 社会经济和生态环境。以化工为背景素材, 将工业生产中的真实情况以信息的形式给 出,运用中学化学中涉及到的元素化合物 知识、化学反应原理、化学实验技能、化 学计算等来解决化工生产实际问题的综合 类题型
精品
一、基础知识和基本技能
精品
(二)掌握工业中主要物质的分类和性质 1.物质的分类 2.物质性质
精品
(三)生产中的关键过程
1.浸出:水洗、酸洗、碱洗 2.分离: • 过滤分离 • 蒸馏分离 • 分液分离 • 结晶分离 3.转化: • 氧化法——加氧化剂 • 还原法——加还原剂 4.富集
精品
(四)了解工业流程的方法和常用术语
1、原料预处理(初步分离)的常用工艺 •研矿——增大接触面积,使反应充分,提高速率 •浸出——通常用酸溶或碱溶形成溶液,有时加热 •焙烧——加热的一种方法,如海带中提取碘 •灼烧或煅烧——使一些物质高温下氧化,分解;
结构改变更易溶解酸浸出 •吹出——利用空气吹出溶液中的气体
精品
2、沉淀的生成的常用方法 • 加入沉淀剂——利用离子反应 • 调pH——利用酸碱性 3.利用平衡原理 • 化学平衡原理 • 溶液中的离子平衡原理
精品
4.工业制硫酸、硝酸的反应原理 5.合成氨工业的原理 • 反应原理 • 化学平衡原理(反应条件) 6.纯碱的生产 • 侯氏制碱法的原理 • 土法制碱法 7.材料 • 无机非金属材料、新型材料 • 有机高分子合成材料
精品
整理所学教材上涉及的相关工业
化工生 产工艺
氯碱、硝酸、纯碱等
物质提 取工艺
精品
精品
二、解题方法
第一步:明确目的 第二步:物质分类 •无机物按组成的树状分类 •有机物按官能团的分类 第三步:原料和产物的转化原理和过程(主线) •氧化还原反应原理转化 •酸碱性反应与原理转化
精品
第三步:分离原理和方法(副线) •酸浸或碱浸(溶解) •除杂 •提纯 •富集 •结晶……
精品
三、审题要点
