实验02严梦
关于高中学生生物实验设计与操作比赛复赛的通知.doc
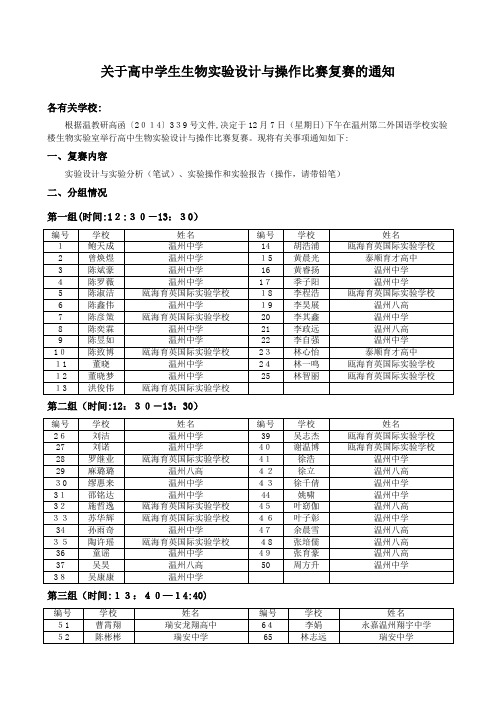
关于高中学生生物实验设计与操作比赛复赛的通知
各有关学校:
根据温教研高函〔2014〕339号文件,决定于12月7日(星期日)下午在温州第二外国语学校实验楼生物实验室举行高中生物实验设计与操作比赛复赛。
现将有关事项通知如下:
一、复赛内容
实验设计与实验分析(笔试)、实验操作和实验报告(操作,请带铅笔)
二、分组情况
第一组(时间:12:30-13:30)
第二组(时间:12:30-13:30)
第三组(时间:13:40—14:40)
第四组(时间:13:40-14:40)
第五组(时间:14:50-15:50)
第六组(时间:14:50—15:50)
三、其它事项
1.请有关学校安排辅导教师带队,按时参加,注意交通安全。
2.本次活动由温州第二外国语学校承办。
差旅费等回原单位报销。
温州市教育教学研究院
2013年12月4日。
明度差别阈限实验报告

明度差别阈限实验报告一、实验目的本实验旨在通过测量不同颜色之间的明度差别阈限,探究个体对颜色明度的敏感度和分辨能力,进一步了解颜色视觉感知的生理和心理机制。
二、实验原理明度差别阈限是指个体能够分辨的最小明度差异。
本实验采用双盲法,通过对比不同颜色之间的明度差异,测量个体对颜色明度的敏感度和分辨能力。
三、实验步骤1. 准备实验材料:红、绿、蓝、黄四种颜色的色卡,每种颜色25张,从浅到深排列。
2. 选取10名实验参与者,年龄在18-40岁之间,视力正常,无色盲等视觉障碍。
3. 将参与者分为4组,每组5人,每组测试一种颜色。
4. 实验开始前,向参与者介绍实验目的、原理和步骤,并确保他们了解实验要求。
5. 实验过程中,要求参与者对比相邻两张色卡,判断两张色卡之间的明度差异是否能够被察觉。
若能够察觉,则继续比较下两张色卡;若不能察觉,则停止比较。
记录参与者在能够察觉到的最小明度差异时所对应的色卡序号。
6. 重复以上步骤,直至所有参与者完成所有颜色测试。
7. 将所有参与者的实验结果汇总,计算每种颜色的明度差别阈限。
四、实验结果根据实验结果,我们可以得出以下结论:1. 在红色和绿色色卡测试中,参与者的明度差别阈限较低,说明他们对这两种颜色的明度变化较为敏感。
2. 在蓝色和黄色色卡测试中,参与者的明度差别阈限相对较高,说明他们对这两种颜色的明度变化相对不敏感。
3. 在不同颜色测试中,女性参与者的明度差别阈限普遍低于男性参与者,说明女性对颜色明度的敏感度更高。
4. 年龄对参与者的明度差别阈限影响较小,但随着年龄的增长,参与者的明度差别阈限会有一定程度的提高。
关于碳酸钾的实验报告

一、实验目的1. 了解碳酸钾的物理性质和化学性质。
2. 掌握碳酸钾的检验方法。
3. 通过实验验证碳酸钾的化学性质。
二、实验原理碳酸钾(K2CO3)是一种白色结晶性粉末,具有弱碱性。
在水中,碳酸钾可溶解,并发生水解反应,生成碳酸氢钾和氢氧化钾。
碳酸钾与酸反应可生成二氧化碳气体、水和相应的钾盐。
本实验通过观察碳酸钾的溶解性、与酸反应的现象,以及检验二氧化碳气体的产生,来验证碳酸钾的性质。
三、实验器材与试剂1. 实验器材:试管、烧杯、玻璃棒、酒精灯、铁架台、胶头滴管、量筒、pH试纸等。
2. 试剂:碳酸钾固体、稀盐酸、澄清石灰水、酚酞指示剂等。
四、实验步骤1. 碳酸钾的溶解性实验(1)取少量碳酸钾固体放入试管中,加入适量蒸馏水,振荡溶解。
(2)观察碳酸钾是否溶解,记录溶解现象。
2. 碳酸钾的水解实验(1)取少量碳酸钾溶液于试管中,加入几滴酚酞指示剂。
(2)观察溶液颜色变化,记录现象。
3. 碳酸钾与酸反应实验(1)取少量碳酸钾溶液于试管中,加入稀盐酸。
(2)观察是否有气泡产生,记录现象。
4. 二氧化碳气体的检验(1)将上述实验中产生的气体通入澄清石灰水中。
(2)观察澄清石灰水是否变浑浊,记录现象。
五、实验现象与结论1. 碳酸钾溶解性实验:碳酸钾固体在蒸馏水中溶解,形成无色溶液。
2. 碳酸钾水解实验:碳酸钾溶液加入酚酞指示剂后,溶液颜色变为粉红色,说明溶液呈碱性。
3. 碳酸钾与酸反应实验:碳酸钾溶液加入稀盐酸后,产生大量气泡,说明碳酸钾与酸反应生成二氧化碳气体。
4. 二氧化碳气体的检验:将产生的气体通入澄清石灰水中,石灰水变浑浊,说明二氧化碳气体与澄清石灰水反应生成碳酸钙沉淀。
六、实验讨论1. 通过本实验,我们了解到碳酸钾是一种白色结晶性粉末,易溶于水,呈碱性。
2. 碳酸钾与酸反应生成二氧化碳气体,可用于检验碳酸钾的存在。
3. 二氧化碳气体与澄清石灰水反应生成碳酸钙沉淀,可用于检验二氧化碳气体的产生。
七、实验总结本实验通过观察碳酸钾的溶解性、与酸反应的现象,以及检验二氧化碳气体的产生,验证了碳酸钾的性质。
+1.3+跨学科实践:降落伞++---2024-2025学年教科版物理八年级上学期

新课教学
比较第2、4两组数据可知,在其他条件一定的情况下,降 落伞在空中滞留的时间与伞的形状无关。 比较第4、5两组数据可知,在其他条件一定的情况下,降落 伞在空中滞留的时间与伞的伞绳长无关。
比较第5、6两组数据可知,在其他条件一定的情况下,降落 伞在空中滞留的时间与伞高度有关,伞的高度越高,伞在空 中滞留的时间越长。
当堂训练 完成课堂8分钟
课后作业 教材课后练习题+课后练习册
导入新课
举办降落伞比赛。
导入新课
• 探究问题: 降落伞在空中的滞留时间与什么因素有关?
新课教学
进行猜想: A.可能与降落伞的伞绳长有关 B.可能与降落伞的形状有关 C.可能与降落伞的面积有关 D.可能与降落伞开始下落高度有关 E.可能与降格
实验 降落伞 降落伞 降落伞 降落伞 降落伞 降落伞滞 次数 伞绳长 的形状 的面积 的高度 总重量 留的时间
降落伞滞 留的时间
3.67s
5.82s 4.91s 5.82s 5.82s 9.24s
新课教学
实验数据分析及结论:
比较第1、 2两组数据可知,在其他条件一定的情况下,降落 伞在空中滞留的时间与伞的面积有关,伞的面积越大,伞在空 中滞留的时间越长。 比较第2、3两组数据可知,在其他条件一定的情况下,降落 伞在空中滞留的时间与伞的总重量有关,伞的总重量越大,伞 在空中滞留的时间越短。
教科版 八年级物理上册
第1章 走进实验室
第3节 跨学科实践:降落伞
授课老师:张老师
学习目标
1.学生体验自主探究活动过程,领悟“控制变量”等科学研究 方法;经历长度、时间与面积的测量过程,体会物理测量的 基本方法,会根据测量对象选择适当的仪器。 2.通过经历探究过程,树立善于参与讨论与交流,勇于发表自 己的观点与成果的意识。通过参与探究活动,培养尊重事实 的科学态度,以及善于与他人合作的精神。
成村学校2011年中考实验分组情况
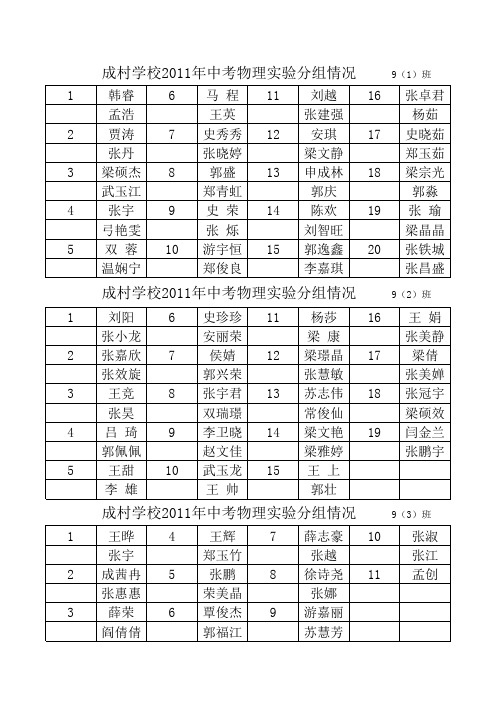
王 娟 张美静 梁倩 张美婵 张冠宇 梁硕效 闫金兰 张鹏宇
成村学校2011年中考物理实验分组情况
1 2 3 4 5 6 7 8 9 10 11
9(ቤተ መጻሕፍቲ ባይዱ)班
张淑 张江 孟创
9(1)班
张卓君 杨茹 史晓茹 郑玉茹 梁宗光 郭淼 张 瑜 梁晶晶 张铁城 张昌盛
9(2)班
成村学校2011年中考物理实验分组情况
1 2 3 4 5 刘阳 张小龙 张嘉欣 张效旋 王竞 张昊 吕 琦 郭佩佩 王甜 李 雄 王晔 张宇 成茜冉 张惠惠 薛荣 阎倩倩 6 7 8 9 10 史珍珍 安丽荣 侯婧 郭兴荣 张宇君 双瑞璟 李卫晓 赵文佳 武玉龙 王 帅 王辉 郑玉竹 张鹏 荣美晶 覃俊杰 郭福江 11 12 13 14 15 杨莎 梁 康 梁璟晶 张慧敏 苏志伟 常俊仙 梁文艳 梁雅婷 王 上 郭壮 薛志豪 张越 徐诗尧 张娜 游嘉丽 苏慧芳 16 17 18 19
成村学校2011年中考物理实验分组情况
1 2 3 4 5 韩睿 孟浩 贾涛 张丹 梁硕杰 武玉江 张宇 弓艳雯 双 蓉 温娴宁 6 7 8 9 10 马 程 王英 史秀秀 张晓婷 郭盛 郑青虹 史 荣 张 烁 游宇恒 郑俊良 11 12 13 14 15 刘越 张建强 安琪 梁文静 申成林 郭庆 陈欢 刘智旺 郭逸鑫 李嘉琪 16 17 18 19 20
实验2实验报告

实验2实验报告在我们探索知识的道路上,实验就像是一个个神秘的冒险,每一次都充满了未知和惊喜。
今天,我要和大家分享的就是实验 2 的奇妙之旅。
这次实验的主题是关于具体实验主题。
为了能顺利完成这个实验,我们可是做了充分的准备。
老师提前给我们讲解了实验的原理和步骤,让我们心里有了个底。
实验开始啦!我紧张又兴奋地摆弄着实验器材,就像一个即将出征的战士在检查自己的武器装备。
我小心翼翼地拿起实验器材名称,眼睛紧紧盯着它,生怕一个不小心就出了差错。
旁边的小伙伴也都全神贯注,教室里安静得只能听到我们紧张的呼吸声。
按照预定的步骤,我先进行了第一步操作。
这一步看起来简单,可真做起来还真不容易。
我得控制好操作的关键因素,稍微有一点偏差,可能就会影响整个实验结果。
我深吸一口气,告诉自己要稳住。
经过几次尝试,终于成功地完成了这一步,心里不禁小小地欢呼了一下。
接下来的步骤越来越复杂,我感觉自己的大脑在飞速运转。
在进行关键步骤名称的时候,我遇到了一个大难题。
怎么都达不到预期的效果,我急得满头大汗。
这时,我想起老师说过的话:“遇到问题不要慌,要冷静思考。
”于是,我停下手中的动作,重新审视了一遍实验步骤,仔细观察了其他同学的操作,终于发现了自己的错误。
原来是我在错误的具体方面上出了岔子。
找到问题所在后,我迅速调整,终于顺利地度过了这个难关。
在整个实验过程中,我和小伙伴们互相帮助,互相鼓励。
当有人遇到困难时,大家都会停下自己的工作,一起出谋划策。
这种团队合作的氛围让我感到特别温暖,也让我明白了在学习的道路上,我们不是一个人在战斗。
经过一番努力,实验终于接近尾声。
当看到最终的实验结果时,那种成就感简直无法用言语来形容。
我们的努力没有白费,实验成功啦!通过这次实验,我不仅学到了知识,还锻炼了自己的动手能力和解决问题的能力。
更重要的是,我明白了做任何事情都要有耐心、细心,遇到困难不能轻易放弃。
这就是我的实验 2 之旅,充满了挑战和收获。
预实习实验报告

一、实验背景随着科学技术的飞速发展,实验室成为了科学研究和技术创新的重要阵地。
为了提高我国高等教育的实践教学质量,许多高校都开设了预实习课程,旨在让学生提前接触实验室环境,了解科研工作流程,培养学生的实践能力和创新精神。
本报告将对我校化学与材料学院预实习课程中的实验部分进行总结和分析。
二、实验目的1. 了解实验室的基本操作规程和安全规范。
2. 掌握实验仪器的使用方法和操作技巧。
3. 学习实验数据的处理和分析方法。
4. 培养严谨的实验态度和团队合作精神。
三、实验内容本次预实习实验共分为三个部分:无机化学实验、有机化学实验和物理化学实验。
(一)无机化学实验1. 实验名称:溶液的配制2. 实验目的:学习溶液的配制方法,掌握物质的量浓度、质量分数等基本概念。
3. 实验原理:根据物质的量浓度计算所需溶质的质量或体积,再通过称量或量取配制一定浓度的溶液。
4. 实验步骤:(1)计算所需溶质的质量或体积;(2)称量或量取溶质;(3)将溶质溶解于溶剂中;(4)转移溶液至容量瓶中,定容至刻度线;(5)摇匀溶液。
(二)有机化学实验1. 实验名称:苯甲酸的制备2. 实验目的:学习有机合成实验的基本操作,掌握苯甲酸的制备方法。
3. 实验原理:利用苯甲酸的酰基化合物与水反应,生成苯甲酸和相应的酸。
4. 实验步骤:(1)称量苯甲酰氯和催化剂;(2)将苯甲酰氯溶解于溶剂中;(3)加入催化剂,混合均匀;(4)反应一段时间后,冷却溶液;(5)过滤、洗涤、干燥,得到苯甲酸。
(三)物理化学实验1. 实验名称:电导率的测定2. 实验目的:学习电导率的测定方法,掌握电导率与溶液浓度、温度等的关系。
3. 实验原理:利用电导率仪测定溶液的电导率,根据电导率计算溶液的离子浓度。
4. 实验步骤:(1)将待测溶液注入电导率池;(2)打开电导率仪,设定测量条件;(3)读取电导率值;(4)根据电导率值计算溶液的离子浓度。
四、实验结果与分析1. 无机化学实验:通过配制不同浓度的溶液,验证了物质的量浓度、质量分数等基本概念的正确性,掌握了溶液的配制方法。
高锰酸钾_氧气实验报告

一、实验目的1. 了解高锰酸钾制取氧气的原理和实验步骤。
2. 掌握实验室制取氧气的操作方法。
3. 观察氧气的性质,加深对氧气性质的理解。
二、实验原理高锰酸钾在加热条件下会分解生成氧气、二氧化锰和锰酸钾。
其化学反应方程式为:2KMnO4 → K2MnO4 + MnO2 + O2↑三、实验仪器和药品1. 仪器:大试管、酒精灯、铁架台、铁夹、集气瓶、水槽、玻璃导管、胶塞、玻璃片、棉花。
2. 药品:高锰酸钾。
四、实验步骤1. 组装实验装置:将大试管固定在铁架台上,用铁夹夹住试管管口1/3处。
将玻璃导管一端插入胶塞,另一端插入集气瓶。
将集气瓶倒置于水槽中,并用玻璃片盖住瓶口。
2. 装入药品:将高锰酸钾放入试管底部,用棉花塞住试管口。
3. 加热:点燃酒精灯,用外焰加热试管底部,观察高锰酸钾的变化。
4. 收集氧气:当试管内产生气泡时,逐渐将导管伸入集气瓶中,待集气瓶内充满氧气后,将导管从水槽中取出。
5. 停止加热:当氧气收集完毕后,熄灭酒精灯。
6. 实验结束:整理实验器材,清洗试管、集气瓶等。
五、实验现象1. 加热过程中,高锰酸钾由紫红色变为黑色,试管内产生气泡。
2. 随着气泡的产生,集气瓶内水面逐渐上升,最终充满氧气。
六、实验结果与分析1. 高锰酸钾在加热条件下分解生成氧气、二氧化锰和锰酸钾,符合实验原理。
2. 通过排水法收集氧气,观察到氧气密度比空气大,能够上升至集气瓶中。
3. 实验过程中,高锰酸钾分解产生的氧气使集气瓶内水面上升,说明氧气具有膨胀性。
七、实验注意事项1. 实验过程中,注意安全操作,防止烫伤。
2. 加热试管时,注意观察试管内药品的变化,避免加热过度。
3. 收集氧气时,注意观察集气瓶内水面上升情况,避免氧气泄漏。
4. 实验结束后,及时整理实验器材,清洗试管、集气瓶等。
八、实验总结本次实验成功制取了氧气,通过观察氧气性质,加深了对氧气性质的理解。
实验过程中,掌握了实验室制取氧气的操作方法,提高了实验技能。
大学生对虚拟仪器了解的研究

认真学 ,体台 拟 仪器的特点
址 奉 r解 虚拟 仪 器 不 太 想 做 , 只 想 了解 了解
仅仅旁现,或者放弃
86 %
( )调查 结果 分析 二
从 五 个 调 查 内 容来 看 , 并 结 合 我们 的 访 谈 的结 果 , 我 们 可 清 楚 地 得 到 以下 五 点 结 论 :
器有充分的 了解 ,特别是虚拟仪器在 自动测量中的了解 ,以
达 到 全 面 培 养 学 生 的 目的 。虽 然 , 从 这 次 简 单 的调 查 中得 到
( )对调查 结果 的思考 三
从 我 们 的 调 查 分 析 中可 以看 到 了 一 种 新 的 教 学 现 象 ,虽
许多有意义的结论,但还有许 多问题有待进一步调查 ,以期
21 0 1年第 5期 【 总第 1 1期 ) 4
大 众 科 技
DA ZHO NG Kቤተ መጻሕፍቲ ባይዱJ
No 5。 0 1 . 2 1
( mu t eyN .4 ) Cu l i l o1 1 av
大 学 生 对 虚 拟 仪 器 了解 的 研 究
严 梦 飞 石 竹 玉 张 婧 朱 俊
的 角度 出 发 ,虚 拟 仪 器 引 入 实验 教 学不 仅 避 免 了传 统 仪 器 带 来 的各 种 弊 病 , 而且 为学 生 提 供 更 大 的 开 放 空 间 ,便 于学 生 随 时随 地 进 行创 新实 验 。 我 们 知 道 虚 拟 仪 器 不 能 代 替 真 实 仪 器 , 但 从 实 际 教学 的 角 度 出发 ,适 当开 设 虚 拟 仪 器 的 相 关 课 程 , 让 学 生对 虚 拟 仪
显然 ,我们认为在实验教学 中引入虚拟 仪器是有必要的。这
模拟实训实验报告

一、实验目的通过本次模拟实训实验,使学生熟悉实验室的安全操作规程,掌握实验仪器的使用方法,提高学生的实验技能和动手能力,培养学生的科学思维和创新能力。
二、实验内容1. 实验仪器:实验台、试管、酒精灯、镊子、滴管、试管架、烧杯、天平、pH试纸等。
2. 实验材料:稀盐酸、氢氧化钠、硫酸铜溶液、氯化钠溶液、硫酸锌溶液、酚酞指示剂等。
三、实验步骤1. 实验室安全操作(1)穿戴实验服、实验手套、护目镜等防护用品。
(2)了解实验室的安全操作规程,严格遵守。
(3)实验过程中,注意避免化学品接触皮肤和眼睛。
2. 实验仪器操作(1)熟悉实验仪器的使用方法,掌握操作技巧。
(2)正确使用酒精灯、滴管、试管等实验仪器。
3. 实验操作(1)取一定量的稀盐酸、氢氧化钠、硫酸铜溶液、氯化钠溶液、硫酸锌溶液,分别置于试管中。
(2)用滴管向每个试管中加入酚酞指示剂。
(3)观察颜色变化,记录实验结果。
(4)重复实验,分析实验现象。
四、实验结果与分析1. 实验结果(1)稀盐酸、氢氧化钠溶液分别呈酸性、碱性,酚酞指示剂变色。
(2)硫酸铜溶液与氢氧化钠溶液反应,产生蓝色沉淀。
(3)氯化钠溶液与酚酞指示剂混合,无明显变化。
(4)硫酸锌溶液与氢氧化钠溶液反应,产生白色沉淀。
2. 实验分析(1)酚酞指示剂在酸性溶液中无色,在碱性溶液中呈红色,可用于判断溶液的酸碱性。
(2)硫酸铜溶液与氢氧化钠溶液反应,生成氢氧化铜沉淀,反应方程式为:CuSO4 + 2NaOH → Cu(OH)2↓ + Na2SO4。
(3)氯化钠溶液与酚酞指示剂混合,无明显变化,说明氯化钠溶液呈中性。
(4)硫酸锌溶液与氢氧化钠溶液反应,生成氢氧化锌沉淀,反应方程式为:ZnSO4 + 2NaOH → Zn(OH)2↓ + Na2SO4。
五、实验结论1. 通过本次模拟实训实验,学生掌握了实验室的安全操作规程,提高了实验技能和动手能力。
2. 学生熟悉了实验仪器的使用方法,了解了实验原理和操作步骤。
高三二统班级成绩
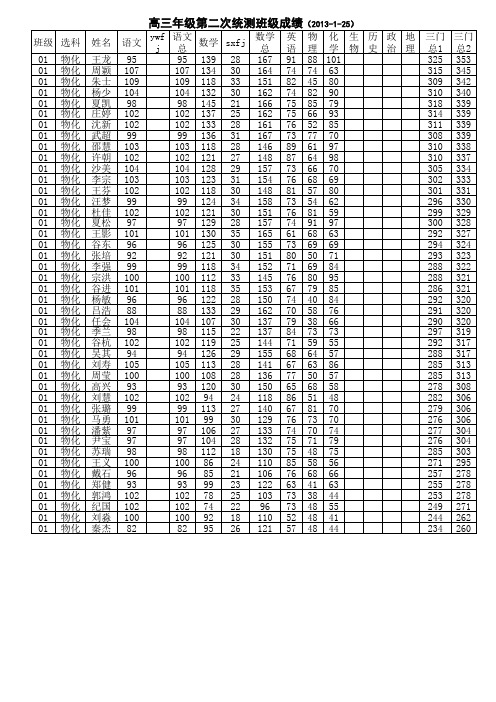
班级 选科 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 02 姓名 语文 ywfj语文总 数学 sxfj 数学总 英语 物理 化学生物历史政治地理 115 103 92 101 91 93 91 94 108 94 105 100 101 96 100 93 103 105 103 101 102 101 107 93 103 102 100 104 92 93 81 102 94 102 88 102 84 96 94 91 94 95 103 96 94 85 95 90 91 98 88 124 136 128 123 133 125 134 126 99 129 111 118 112 122 102 114 93 105 120 96 104 114 93 103 99 86 106 100 105 110 119 112 105 94 109 76 112 97 92 79 98 77 78 104 82 87 74 86 84 89 77 31 36 31 28 36 32 35 34 26 31 32 27 32 24 30 30 33 34 21 27 27 30 27 31 27 26 30 27 27 21 34 25 27 30 28 26 25 22 28 29 22 28 31 17 25 29 26 19 11 20 21 155 172 159 151 169 157 169 160 125 160 143 145 144 146 132 144 126 139 141 123 131 144 120 134 126 112 136 127 132 131 153 137 132 124 137 102 137 119 120 108 120 105 109 121 107 116 100 105 95 109 98 86 71 89 82 74 82 70 71 86 65 66 68 68 70 79 72 78 63 62 82 73 61 78 76 73 87 65 69 76 75 64 58 70 70 70 86 68 70 70 85 66 77 65 57 70 69 74 73 79 58 67 63 42 70 60 62 43 51 55 53 64 53 34 46 48 50 70 28 62 58 62 45 50 64 53 25 47 54 47 18 39 83 42 32 51 59 33 44 57 34 45 50 24 56 48 54 25 31 38 29 57 51 75 69 59 92 75 71 73 87 64 81 63 66 48 78 58 77 54 61 65 65 67 68 74 71 60 63 82 80 72 64 85 77 49 79 72 66 49 63 68 62 67 45 57 64 65 53 56 43 61 57 64 物生 杨颖 115 物生 李慧敏 103 物生 管倩 92 物生 田丽娟 101 物生 李振华 91 物生 徐慧 93 物生 单仁邦 91 物生李蕴旋捷 94 物生 李颖 108 物生 张兴 94 物生 邱亚 105 物生 孟洁 100 物生 王建锐 101 物生 孙义 96 物生 朱树翠 100 物生 陈旺 93 物生 郎娜 103 物生 周杰 105 物生 王月 103 物生 崔小雨 101 物生 徐纤 102 物生 吴霞 101 物生 张凯云 107 物生 高敏 93 物生 王蒙蒙 103 物生 朱琳 102 物生 吴萍 100 物生 刘奔 104 物生 黄卫梦 92 物生 严梦甜 93 物生 侍邦耀 81 物生 徐大帅 102 物生 成文辉 94 物生 陈婷婷 102 物生 史雅婷 88 物生 马云 102 物生 李珊 84 物生 杜雅芝 96 物生 蒋林倩 94 物生 朱盈云 91 物生 周筛 94 物生 牛莹 95 物生 李少豪 103 物生 何宗恒 96 物生 王静 94 物生 陶勐 85 物生 祁青青 95 物生 庄梦雨 90 物生 李香 91 物生 成勇 98 物生 谷容容 88 三门 三门 总1 总2 325 356 310 346 309 340 306 334 298 334 300 332 295 330 291 325 293 319 288 319 282 314 286 313 281 313 288 312 281 311 279 309 274 307 273 307 285 306 279 306 279 306 276 306 278 305 272 303 275 302 275 301 271 301 273 300 273 300 278 299 264 298 272 297 269 296 266 296 267 295 264 290 264 289 263 285 256 284 255 284 258 280 249 277 246 277 257 274 246 271 241 270 243 269 249 268 254 265 245 265 232 253
中小学课题申报书:智慧学习空间构建与教学应用策略研究

智慧学习空间构建与教学应用策略研究学科分类:基础教育课题类别:重点课题关键词:智慧学习空间、教学应用策略、基础教育预期研究成果:研究报告课题设计论证一、问题的提出、课题界定、国内外研究现状述评、选题意义与研究价值。
(一)问题的提出2019年6月,中共中央国务院颁布的《关于深化教育教学改革全面提高义务教育质量的意见》中提到:要促进信息技术与教育教学融合应用,推进“教育+互联网”发展,建立覆盖义务教育各年级各学科的数字教育资源体系[1]。
2018年教育部印发的《教育信息化2.0行动计划》中也明确指出要“构建智慧学习支持环境……大力推进智能教育,开展以学习者为中心的智能化教学支持环境建设”[2]。
这种国家层面的支持,为我国的教育,特别是基础教育的发展提供了强有力的政策保障,同时也促使广大教育工作者积极投身到教育信息化的实践以及研究工作中来。
在教育信息化的众多应用领域中,“智慧学习空间”近年来逐渐被引入基础教育的教学实践,并取得了一定成效。
通过“智慧教室”、“创客空间”以及“虚拟网络学习空间”等新颖的教学形式和技术手段,学生的学习积极性和创造性获得了明显提升。
但我们也应该注意到,目前各学校“智慧学习空间”建设的发力点还较为分散,对于其中的“物理空间”、“教学资源空间”以及“网络学习空间”等子空间尚未完全打通,不能发挥其合力作用。
为了更好地促进其在基础教育中的应用,本课题以小学教育为背景,拟对智慧学习空间的构建进行研究,并就相关教学应用策略展开实践探讨。
(二)课题的界定1.智慧学习空间对于教学过程而言,学习空间是教与学两种活动发生的载体与支撑[3]。
在“互联网”、“大数据”以及“人工智能”技术蓬勃发展的背景下,“学习空间”与各种“智慧”技术相结合的产物即是“智慧学习空间”,它是信息技术与教育教学深度融合的产物。
鉴于表现形式的不同,“智慧学习空间”可理解为包含若干子空间,如“物理空间”、“教学资源空间”、“网络学习空间”等,它们的共同特点是以智慧化的方式衔接“教”与“学”的活动。
锰氧化性_实验报告

一、实验目的1. 验证二氧化锰(MnO2)的氧化性。
2. 探究MnO2在不同反应条件下的氧化效果。
二、实验原理MnO2是一种具有较强氧化性的化合物,在酸性条件下,MnO2可以将还原剂氧化,自身被还原。
本实验通过观察MnO2与不同还原剂反应的现象,来验证其氧化性。
三、实验材料1. 实验仪器:试管、烧杯、酒精灯、镊子、滴管、滤纸等。
2. 实验药品:MnO2固体、稀盐酸、硫酸铜溶液、碘化钾溶液、淀粉溶液、硫酸铁溶液、KSCN溶液等。
四、实验步骤1. 验证MnO2的氧化性(1)取一支试管,加入少量MnO2固体,滴加少量稀盐酸,观察是否有气泡产生。
(2)将反应后的溶液过滤,取滤液,加入少量淀粉溶液,观察溶液颜色变化。
2. 探究MnO2在不同反应条件下的氧化效果(1)取两支试管,分别加入少量MnO2固体,一支加入稀盐酸,另一支加入硫酸铜溶液,观察反应现象。
(2)取两支试管,分别加入少量MnO2固体,一支加入碘化钾溶液,另一支加入硫酸铁溶液,观察反应现象。
(3)取一支试管,加入少量MnO2固体,滴加KSCN溶液,观察溶液颜色变化。
五、实验结果与分析1. 验证MnO2的氧化性实验结果显示,在加入稀盐酸的试管中,有气泡产生,说明MnO2与稀盐酸反应生成气体。
加入淀粉溶液后,溶液颜色未发生变化,说明MnO2氧化稀盐酸后未生成淀粉溶液变色的物质。
2. 探究MnO2在不同反应条件下的氧化效果(1)在加入稀盐酸的试管中,MnO2与稀盐酸反应生成气体,说明MnO2具有氧化性。
在加入硫酸铜溶液的试管中,MnO2与硫酸铜溶液反应,生成蓝色沉淀,说明MnO2在酸性条件下可以氧化铜离子。
(2)在加入碘化钾溶液的试管中,MnO2与碘化钾溶液反应,溶液颜色变深,说明MnO2在酸性条件下可以氧化碘离子。
在加入硫酸铁溶液的试管中,MnO2与硫酸铁溶液反应,溶液颜色未发生变化,说明MnO2在此条件下未发生氧化还原反应。
(3)在加入KSCN溶液的试管中,MnO2与KSCN溶液反应,溶液颜色未发生变化,说明MnO2在此条件下未发生氧化还原反应。
二氧化锰的溶胶凝胶实验报告

二氧化锰的溶胶凝胶实验报告二氧化锰的溶胶凝胶实验报告一、引言二氧化锰是一种重要的功能材料,具有广泛的应用领域。
溶胶凝胶是一种制备纳米材料的有效方法,能够控制材料的形貌和性能。
本实验旨在通过溶胶凝胶法合成二氧化锰纳米颗粒,并研究其形貌和晶体结构。
二、实验方法1. 实验材料和设备:(1) 无水乙醇(2) 甘油(3) 高纯度硝酸钾(4) 无水氯化锰(5) 恒温槽(6) 离心机2. 实验步骤:(1) 在250 mL三口烧瓶中加入10 mL无水乙醇和5 mL甘油,充分混合。
(2) 将10 g高纯度硝酸钾溶解在50 mL无水乙醇中,得到硝酸钾溶液。
(3) 将硝酸钾溶液缓慢滴加到烧瓶中,并同时加入适量的无水氯化锰。
(4) 在恒温槽中保持温度为60℃,并用离心机将烧瓶中的溶液离心10分钟。
(5) 将沉淀洗涤至中性pH值,然后离心收集沉淀。
(6) 将沉淀置于干燥箱中,在60℃下干燥24小时。
(7) 得到二氧化锰溶胶凝胶样品。
三、实验结果1. 形貌观察:通过扫描电子显微镜(SEM)观察,发现二氧化锰溶胶凝胶样品呈现出均匀的颗粒分布和较为光滑的表面。
2. 晶体结构分析:利用X射线衍射(XRD)仪器对二氧化锰溶胶凝胶样品进行分析。
从XRD图谱可以看出,二氧化锰溶胶凝胶样品具有结晶性,呈现出与标准晶体相符合的特征峰。
四、讨论1. 形貌观察结果说明通过溶胶凝胶法制备的二氧化锰纳米颗粒具有良好的分散性和较小的颗粒尺寸。
这对于提高材料的表面积和活性具有重要意义。
2. XRD分析结果表明二氧化锰溶胶凝胶样品具有良好的晶体结构,与标准晶体相符合。
这说明溶胶凝胶法能够制备出结晶度较高的二氧化锰纳米颗粒。
3. 实验中使用的无水乙醇和甘油起到了溶剂和表面活性剂的作用,有助于控制溶液中二氧化锰纳米颗粒的形成过程。
五、结论通过溶胶凝胶法成功合成了二氧化锰纳米颗粒。
通过形貌观察和晶体结构分析发现,该样品具有均匀分布、光滑表面和良好的晶体结构特征。
【2018-2019】奇妙的身体实验-范文模板 (1页)

【2018-2019】奇妙的身体实验-范文模板本文部分内容来自网络整理,本司不为其真实性负责,如有异议或侵权请及时联系,本司将立即删除!== 本文为word格式,下载后可方便编辑和修改! ==奇妙的身体实验奇妙的身体实验王晨衔杭州市西湖区求是(和家园)小学二年级指导老师:天然学园张燕今天一上课,张老师就让我们做实验,一共做了两个实验。
我们先做了铅笔亲嘴。
王晨铭和严悦齐上去试,严悦齐用右手大拇指和食指握在铅笔被削过的地方,右手弯曲,左手蒙着左眼留出右眼。
而王晨铭却握在笔杆表面上。
他们碰来碰去就是碰不着,犹如两个拳击高手在试探对方,却不肯出招。
王晨铭想了想,就换了一个握手电筒的姿势,可笔尖碰来碰去还是碰不到。
王晨铭心急了,手在发抖,又换了个姿势,跟严悦齐一样握笔,终于碰到了,他们总算松了口气。
张老师让我们自己试试,我和沙靖皓一组很快就成功了,看来还是我俩厉害。
张老师又让我们做捡橡皮,游戏规则是:屁股不能离墙,双腿不能弯曲。
老师先让崔文旭去试,他一开始就一只手向下,一只手高举,像大雁飞行的样子。
突然,他“啊”的一声惊叫,差点摔倒,屁股差点离墙,我们哄堂大笑起来。
他走了一步,可还是捡不到橡皮,时间到了他还没拿到,他觉得很可惜,满脸遗憾地下了台。
第二次是沙靖皓和程博文,他们都很努力,可像崔文旭一样没成功。
后来张老师让我们也试了试,我跟其他人一样没成功。
最后=后张老师就告诉我们游戏的奥秘:第一个实验,一只眼睛笔尖不容易碰在一起,是因为一只眼睛看东西没有立体的感觉。
第二个实验,膝盖不弯,身体就不能保持平衡。
原来是这样啊。
小小的实验还有奇妙的道理。
空气氧气浓度实验报告

一、实验目的1. 了解空气中氧气的浓度。
2. 掌握测定空气中氧气浓度的方法。
3. 分析影响氧气浓度的因素。
二、实验原理氧气是空气中的一种重要成分,其浓度对生物体的生存和化学反应具有很大影响。
本实验采用燃烧法测定空气中氧气的浓度,利用红磷燃烧消耗氧气,使集气瓶内压强减小,通过测量进入集气瓶内水的体积来计算氧气的浓度。
三、实验器材1. 集气瓶2. 烧杯3. 燃烧匙4. 红磷5. 乳胶管6. 橡皮塞7. 导管8. 止水夹9. 酒精灯10. 水平仪四、实验步骤1. 将集气瓶容积划分为5等份,并做好标记。
2. 将集气瓶倒置于烧杯中,将导管一端插入烧杯底部,另一端连接乳胶管。
3. 将红磷放入燃烧匙中,点燃后迅速放入集气瓶内,立即塞紧橡皮塞。
4. 观察集气瓶内水面上升情况,待水面上升至一定高度后,打开止水夹,观察水面下降情况。
5. 待集气瓶内水面下降至标记位置时,关闭止水夹,记录此时进入集气瓶内水的体积。
6. 重复上述步骤3-5,进行三次实验,求平均值。
五、实验现象1. 红磷燃烧产生大量白烟。
2. 集气瓶内水面上升,随后下降至标记位置。
六、实验数据实验次数 | 水的体积(mL)-------------------1 | 502 | 483 | 52平均体积 | 50七、实验结果与分析1. 根据实验数据,计算空气中氧气的浓度:氧气体积 = 集气瓶体积× 水的体积 / 平均体积氧气体积= 500mL × 50mL / 50mL = 500mL氧气浓度 = 氧气体积 / 集气瓶体积× 100%氧气浓度= 500mL / 500mL × 100% = 100%2. 分析影响氧气浓度的因素:(1)红磷量:红磷量过少,无法消耗足够氧气,导致氧气浓度测量值偏低。
(2)装置气密性:装置漏气,外界空气进入集气瓶,导致氧气浓度测量值偏低。
(3)燃烧速度:红磷燃烧速度过慢,导致氧气浓度测量值偏低。
高锰酸钾制取氧气实验报告

高锰酸钾制取氧气实验报告一、实验目的1、掌握用高锰酸钾制取氧气的实验原理和操作方法。
2、了解氧气的性质和检验方法。
3、培养实验操作能力和观察能力。
二、实验原理高锰酸钾在加热的条件下分解生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO₄=△= K₂MnO₄+ MnO₂+ O₂↑三、实验用品1、仪器:大试管、酒精灯、铁架台(带铁夹)、水槽、集气瓶、玻璃片、导气管、棉花、火柴。
2、药品:高锰酸钾。
四、实验步骤1、检查装置气密性先将导气管的一端浸入水槽中,用手紧握试管外壁,如果导管口有气泡冒出,松开手后,导管内形成一段水柱,说明装置气密性良好。
2、装药品将少量高锰酸钾粉末用纸槽或药匙小心地送到试管底部,然后在试管口塞上一团棉花,防止加热时高锰酸钾粉末进入导管。
3、固定装置将试管固定在铁架台上,铁夹应夹在距试管口约 1/3 处,试管口略向下倾斜,防止冷凝水回流到热的试管底部,使试管炸裂。
4、加热先预热,然后集中在药品部位加热。
5、收集气体当气泡连续均匀地冒出时,开始收集氧气。
氧气不易溶于水,可用排水法收集。
将集气瓶装满水,倒扣在水槽中,当气泡从集气瓶口向外冒出时,表明氧气已收集满。
6、验满将带火星的木条放在集气瓶口,如果木条复燃,说明氧气已满。
7、停止加热先把导管移出水面,然后熄灭酒精灯,防止水槽中的水倒吸入试管,使试管炸裂。
五、实验现象1、加热时,试管内的固体逐渐由紫红色变为黑色。
2、收集到的气体能使带火星的木条复燃。
六、注意事项1、装药品前必须检查装置气密性。
2、试管口要略向下倾斜,防止冷凝水回流炸裂试管。
3、试管口要塞一团棉花,防止高锰酸钾粉末进入导管。
4、加热时要先预热,然后集中在药品部位加热。
5、用排水法收集氧气时,要等气泡连续均匀冒出时再收集。
6、实验结束时,先把导管移出水面,再熄灭酒精灯。
七、氧气的性质检验1、把带火星的木条伸入集气瓶中,木条复燃,说明氧气能支持燃烧。
2、将一根燃着的木条伸入集气瓶中,木条燃烧更旺,说明氧气具有助燃性。
浅谈高中化学教学中学生实验探究能力的培养

浅谈高中化学教学中学生实验探究能力的培养
周嵩程
【期刊名称】《中学课程辅导(教学研究)》
【年(卷),期】2021()3
【摘要】结合素质教育理念的具体要求,高中化学教师在指导学生学习时,应充分认识到本学科对培养学生实践探究能力和科学精神的重要作用,应运用更精细、更多元的教学方法,优化教学过程,创新教学方案,以促进学生化学综合素养的全面发展和全面提高。
【总页数】1页(P0132-0132)
【作者】周嵩程
【作者单位】浙江省温州市第二外国语学校,浙江温州325000
【正文语种】中文
【中图分类】G633.8
【相关文献】
1.探讨高中化学教学中学生实验探究能力的培养策略
2.浅析高中化学教学中学生实验探究能力的培养
3.浅谈高中化学教学中学生实验探究能力的培养
4.高中化学教学中学生实验探究能力的培养策略
5.高中化学教学中学生实验探究能力的培养途径
因版权原因,仅展示原文概要,查看原文内容请购买。
高中化学探究性实验有效教学探析

高中化学探究性实验有效教学探析江苏省前黄高级中学(圆员猿员远员) 高晓军●摘 要:化学教学是一门理论与实验相结合的学科.尤其是高中阶段的学习,它对于学生今后的发展是至关重要.本文将通过对探究性实验有效教学如何在高中化学课堂中的应用来进行讨论,致力于高效课堂的打造.关键词:高中化学教学;探究性实验;实施策略中图分类号:G632 文献标识码:B 文章编号:1008-0333(2016)21-0081-01 近些年来,随着在新课改的不断深入,教师们越来越重视课堂效率的提高.因此,如何打造高效课堂也就成了当下最为重要的教育问题.高中化学作为一门理论与实验相结合重要学科,知识也很细碎,不论是教师,还是学生在化学的学习问题上都在进行着探究,希望找到一套合适的、有效的方法.为了更好的将探究性实验教学应用于化学课堂,接下来笔者就将对这种教学方式的应用策略进行分析.一、高中化学探究性实验有效教学存在的问题1.教学理念受到传统教育模式的影响我国传统的教学模式更注重学生是否有好的学习成绩,而忽略了对学生能力的培养.但随着社会的不断进步,社会的发展需要的是综合素质能力比较强的人才.由于在树立教学目标的过程中已经出现了偏差,这就会使整个教育理念在实践的过程中受到影响.教师作为学生学习时的引路人,对学生的影响是极大的.比如说,现在有很大一部分教师在进行教学的过程中依旧使用的是原来的教学方式,只是单一的依照考试大纲的要求来制定教学目标和教学任务,而不是联系实际,将学生作为主体,把因材施教的教育理念贯彻落实到教学工作中,他们只是将历年考试的考点整理出来,然后针对这部分知识采用题海战术的方式让学生进行练习,从而取得高分.这样一来,固然学生的学习成绩都不错,但对学生自身的发展是十分不利的,它会使学生在学习过程中对老师逐渐产生依赖心理,缺少对知识的深入理解,形成思维定式,缺少创新意识,从而使课堂效率逐渐降低.2.还没有树立正确的学习意识在教育工作的实施程中,不论是学校的领导者还是教师,都应该正确的认识到教育的真正意义,而不是单一的追求高分,这样会很容易让学生在学习的过程中出现高分低能的现象,不利于教学工作的开展.如果学校的领导能够正确的认识到探究性实验教学的重要性,就能够更合理的对教学资源进行划分,避免出现实验设备不足的尴尬局面.如果教师能够意识到探究实验教学对化学教学效果的提高作用,就会制定出更加合理化、高效化的教学计划,在潜移默化中培养学生正确的学习态度,激发学生的学习热情,使学生的学习效果有更加明显的提高.二、高中化学实验探究性教学的实施策略1.树立正确理念,提高教育认识教师是施教者,学生是受教者,教师和学生都应该正确的认识到自己在教学过程中的地位,树立正确的教育理念.笔者认为,高中化学是一种半文半理的学科,它包含着许多细碎的知识点,需要进行大量的记忆,但是也会牵涉到一些计算,需要学习者有较好的逻辑思维.总的来说,在化学的学习过程中,不论是理论知识的记忆,还是逻辑思维的推断,都离不开对知识的理解.化学是一门需要实验的学科,在实验的过程中,能够使学生更好的掌握所学内容,加深对知识的理解.在化学教学的过程中,如果能够正确的使用实验进行教学,就会使教学效果事半功倍.比如,教师可以在课前备课的时候,对教学过程中需要用到的实验提前进行研究,在网上查找一些相关的实验资料,对实验过程中可能出现的问题,进行总结,然后再将实验巧妙的与课堂结合,使学生在学习的过程中可以学习到更为全面的知识.这样不仅可以使教师及时的帮助学生解决问题,大大的减少对课堂有效教学时间的浪费,使课堂环节设置能够环环相扣,而且能够以深入浅出的教学方法,使学生取得更好的学习效果,打造高效课堂.2.强化实验分析,力求举一反三在典型实验上下功夫,注重总结反思相结合,清晰的实验目的,优化的流程设计,效果一定可想而知.再由典型实验为引子,加强对学生实验能力的夯实,将知识进行内化.比如学习用二氧化锰、浓盐酸混和加热来制取氯气,我首先要求学生想想实验室里制取氧气的实验,对此进行归纳:仪器选取,连接,固定,装置气密性的检查及药品的取用等.对这些操作的理论根椐进行强调,从而引导得出制取氯气的发生装置、收集方法等.最后得出《氨气的实验室制法》的有关设计思路、操作等.3.进行有效实验,培养创新能力首先要引导学生设计实验,选取实验仪器.其次要让学生留心观察现象,通过分析得出一定的结论,从中感受到成功的快乐,如有不足要进行反思.另外要学会正确面对实验中的困难,如:在进行“铁丝在氧气中燃烧”实验中,有的小组未看到四射的火星,此时教师要抓住契机,引领学生分析,反思,寻找失败原因,这个过程经实验本身更重要.因此,在化学课堂教学中,进行探究性实验教学很有必要,会使课堂效率最大化.当然,这也要求我们教者在课前做好充分的准备,尽可能的对各种可能发生的状况考虑周全,这样才能保证实验教学在化学教学过程中的顺利实施.参考文献[1]李建,车延平.高中化学实验探究方法的案例分析[J].现代阅读,2011(12):105[2]丁莹.高中化学实验探究教学模式初探[J].高等函授学报,2009(8):61~62[3]夏彬彬.加强高中化学实验改革提高教学效率[J].基础教育,2010:304~306—18—All Rights Reserved.。
发酵罐的操作流程

发酵罐的操作流程(总7页)--本页仅作为文档封面,使用时请直接删除即可----内页可以根据需求调整合适字体及大小--一.目的:为了确保发酵产品安全正常生产,建立50L发酵罐设备标准操作规程。
二.适用范围:50L发酵罐的操作三.责任人:1、实验员:负责生产现场水、电、气及生产设备的正常使用;使用生产用原辅料及检测设施。
2、指导老师:指导学生了解发酵设备结构,熟悉掌握发酵操作规程,安全使用发酵罐系统。
3、操作者:遵守安全管理规定,严格按照标准操作规程操作。
四、操作步骤发酵罐内部构造示意图第一步、准备工作1.检查压力表是否为零,若不是则开对应的阀门调零。
2.检查阀门是否为关闭状态,若不是则顺时针旋转关闭。
3.检查蒸汽发生器上的压力表不得低于。
4.检查空压机的压力表不得低于。
5.校正温度和pH电极:温度用沸水或冰水校正,pH用标准溶液校正。
6.检查发酵罐的密封性:关F21,F16,开F11,F15,使发酵罐的压力表为,保持5min,再关F11,F15。
第二步、空气管道的消毒打开F3,F14,微开F12,F13(转两圈),等到F4均匀的蒸汽时,关闭F13,F12,微开F14,调节F3,使空气管道的压力表维持在,30min,关F14,F3。
开F11,F14,使空气管道压力保持在,当有F14干燥冷空气排出时,微开F14,调节F11,使空气管道的压力保持在。
第三步、空消开F4,F22,排冷凝水,当F22有均匀蒸汽排出时,关F22,开F21,F16,排空气,当F16有均匀蒸汽排出时,发酵罐的压力为。
微开F16,调节F21(关F21或F4),使发酵罐压力保持在。
30min.关F21、F4,大开F16进行泄压,使发酵罐压力到微正压~,再关F16.第四步投料第五步、实消1.开F2,F37(排污管),F16,打开手动搅拌,当发酵罐内温度达到80—90度时,关F2,F37,手动搅拌。
2.开F4,F22,排冷凝水,当F22有均匀蒸汽出现时,关F22,开F21。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
《数学实验》实 验 报 告02
实验名称 数学建模初步 实验日期 李夏明
班级 文正12信计学号 07 姓名 严梦 成绩
一、实验目的
通过解决简化的实际问题,学习初步的数学建模方法,培养建模意识.
二、实验内容
1.与蛛网模型有差别的模型。
设第k +1与第k 时段商品上市数量之差是第k 时段价格的线性增函数,系数为a ; 第k +1与第k 时段商品价格之差是第k 时段数量的线性减函数,系数为b 。
又知当商品数量为500、价格为200时,处于平衡状态。
建立差分方程模型描述商品数量和价格的变化规律,对以下情况作图讨论其变化趋势。
(1) 设a = 0.2,b = 0.1,开始时商品数量和价格分别在500和100附近;
(2) 利用特征根讨论变化趋势。
提示:k x 表示第k 时段的数量,k y 表示第k 时段的价格
10100.2,0.1k k k k k
k x x ay a a y y bx b b ++-=+=⎧⎧⎨⎨-=-+=⎩⎩;500200x y =⎧⎨=⎩是平衡点,代入方程组得到 004050a b =-⎧⎨=⎩。
00
500100x y =⎧⎨=⎩是起始点,递推出11x y =⎧⎨=⎩,22x y =⎧⎨=⎩,。
2.书本
提示:先把速度v 化到单位:m/s ,距离d=2
12k v k v + <==> d = [k1,k2] * [v;v^2];调用语句k=d/[v;v^2]可以估计出系数k
三、实验结果(包括所用命令、程序,运行结果等)
1.(1)x0=500;y0=200;x1=510;beta=5;n=500;a=0.2;b=0.1;
x(1)=x1;
for k=1:n-1
x(k+1)=x(k)+a*y(k)+a0;
y(k+1)=y(k)-b*x(k)+b0;
end
y(n)=y(n-1)-b*x(n)+b0;
plot(x); grid; gtext('x(k)');
gtext(a,beta,'FontSize',20); pause
plot(y); grid; gtext('y(k)');
gtext(a,beta,'FontSize',20); pause
end (2)(2)由方程组⎩⎨⎧+=-+=-++++010112a ay x x a ay x x k k k k k k ,将两式相减,
得到
代入,把01112),(2b bx y y y y a x x x k k k k k k k k +-=-+=+-++++
得到
),
(
2
1
2
b
bx
a
x
x
x
k
k
k
k
+
-
=
+
-
+
+
即
,0
1
2-
)
1(
22
,0
1
2
=
+
+
=
+
+
-
+
+
λ
λ
λ)
(
特征方程ab
ab
x
ab
x
x
k
k
k
特征根
ab
ab
-
+
=
+
-
±
=1
2
)
1(4
4
2
2,1
λ
当
.
,1
1
,
1
2,1
2,1
不稳定
模长为
时,特征根是复数>
+
=
±
=
>ab
abi
abλ
λ
当ab<0时,特征根方程是实数
.
,1
1
1
,
1
2,1
不稳定
>
-
+
=
-
±
=ab
abλ
λ
所以当ab≠0时,平衡点不稳定.
2先列出实际的速度和距离的数据,画出图像,再通过理论计算出速度和距离,将两张图放在一起做出对比。
v=[20000/3600 40000/3600 60000/3600 80000/3600 100000/3600 120000/3600 140000/3600];
d=[6.5 17.8 33.6 57.1 83.4 118.0 153.5];
plot(v,d,'bo',v,d,'g-');hold on;
k=d/[v;v.^2]
d1= k * [v;v.^2]; [v',d',d1']
plot(v,d1,'r+');
k =
0.6522 0.0853
ans =
5.5556
6.5000 6.2553
11.1111 17.8000 17.7748
16.6667 33.6000 34.5584
22.2222 57.1000 56.6062
27.7778 83.4000 83.9181
33.3333 118.0000 116.4941
38.8889 153.5000 154.3343
四、问题讨论(实验心得与体会)
本次的实验题目要看清,思路要理清,在没有弄清题目的情况下感觉不知道要做什么。
所以,还是要上课听讲的。
此外,对于输入特殊的符号感觉也很困难,需要多加锻炼。
