生物化学课件 第六章 生物氧化
合集下载
人民卫生出版社《生物化学》第六章 生物氧化

⊿Gº’ = -nF ⊿Eº'
n:传递电子数;F:法拉第常数
➢ 合成1摩尔ATP 需能量约30.5kJ
偶联部位
NADH~CoQ CoQ~Cytc Cyta-a3~O2
电位变化 (∆E0')
0.36V 0.21V 0.53V
自由能变化 (∆G0')
69.5KJ/mol 40.5KJ/mol 102.3KJ/mol
三、NADH和FADH2是呼吸链的电子供体
1、NADH氧化呼吸链 NADH →复合体Ⅰ→CoQ →复合体Ⅲ→Cyt c →复合体Ⅳ→O2
2、琥珀酸氧化呼吸链 琥珀酸 →复合体Ⅱ →CoQ →复合体Ⅲ→Cyt c →复合体Ⅳ→O2
呼吸链各组分的排列顺序的实验依据
➢ 标准氧化还原电位 ➢ 特异抑制剂阻断 ➢ 还原状态呼吸链缓慢给氧 ➢ 将呼吸链拆开和重组
生物氧化与体外氧化之不同点
生物氧化
➢ 反应环境温和,酶促反应逐步进 行,能量逐步释放,能量容易捕 获,ATP生成效率高。
体外氧化
➢ 能量突然释放。
➢ 通过加水脱氢反应使物质能间接 获得氧;脱下的氢与氧结合产生 H2O,有机酸脱羧产生CO2。
➢ 物质中的碳和氢直接氧 结合生成CO2和H2O 。
生物氧化的一般过程
胞液侧 4H+
2H+ 4H+ Cyt c
+
+++++ +
++
+
Q
Ⅰ
--
NADH+H+
NAD+
Ⅱ
-
延胡索酸
琥珀酸
Ⅳ
Ⅲ- - -
基础生物化学-生物氧化

内膜约含 80%的蛋白质,包括电子传递链和氧 化磷酸化的有关组分,是线粒体功能的主要 担负者 。 线粒体 的内腔 充满半流动的基质 (衬质),其中包含大量的酶类以及线粒体 DNA和核糖体。 线粒体基质酶类包括 TCA酶类、脂肪酸-氧化 酶类和氨基酸分解代谢酶类。
哺乳动物线粒体 DNA 为环状分子,编码包括 细胞色素氧化酶、细胞色素 b 和 F0 疏水亚基 在内的10多种蛋白质,约占内膜总蛋白质的 20%,其余的蛋白质均由核基因编码,在细 胞质中合成后运入线粒体。 线粒体内膜的内表面有一层排列规则的球形颗 粒,通过一个细柄与构成嵴的内膜相连接, 这就是ATP合酶(偶联因子F1-F0)。
6.1.1.3 生物氧化中CO2和H2O的生成 ① CO2的生成 代谢底物在酶的作用下经一系列脱氢、加水等 反应,转变为含羧基的化合物,经脱羧反应 生成CO2,包括直接脱羧和氧化脱羧。
② H2O的生成 生物氧化中底物脱下的氢与氧结合生成水。
6.1.2 生物氧化的自由能变化 6.1.2.1 自由能概念 生物体不能直接利用热能做动,在生命活动过 程中所需的能量都来自体内生化反应释放的 自由能。 自由能(free energy) :在恒温、恒压条件下一 个体系可用于做有用功的能量。又称Gibbs自 由能,以G表示。
②黄素蛋白(flavoproteins) 与电子传递链有关的黄素蛋白有两种,分别以 FMN和FAD为辅基。
在FAD、FMN分子中的异咯嗪部分可进行可逆 的脱氢加氢反应。氧化型黄素辅基从NADH接 受两个电子和一个质子,或从底物(如琥珀酸) 接受两个电子和两个质子而还原: NADH+H++FMN=NAD++FMNH2 琥珀酸+FAD=延胡索酸+FADH2
生物化学第六章 生物氧化(共77张PPT)

O O- P
O-
O O P O-
O-
NH2
N
N
焦磷酸
ATP(三磷酸腺苷) 千卡/摩尔
O O- P
O-
O O- P
O-
O O- P
O-
NN OCH2 O
HH
H
H
OH OH
(3)烯醇式磷酸化合物
COOH O CO PO CH2 O
磷酸烯醇式丙酮酸
千卡/摩尔
2.氮磷键型
O
NH
PO
C NH O
N CH3 C H 2C O O H
利用专一性电子传递抑制剂选择性的阻断呼吸 链中某个传递步骤,再测定链中各组分的氧化-还原 状态情况,是研究电子传递中电子传递体顺序的一 种重要方法。
2、常用的几种电子传递抑制剂及其作用部位
(1)鱼藤酮、安密妥、杀粉蝶菌素:其作用是阻断电子在NADH— Q还原酶内的传递,所以阻断了电子由NADH向CoQ的传递。
3.生成二氧化碳的氧化反应
(1)直接脱羧作用 氧化代谢的中间产物羧酸在脱羧酶的催化下,直接
从分子中脱去羧基。例如丙酮酸的脱羧。 (2)氧化脱羧作用
氧化代谢中产生的有机羧酸(主要是酮酸)在氧化脱
羧酶的催化下,在脱羧的同时,也发生氧化(脱氢)作用。 例如苹果酸的氧化脱羧生成丙酮酸。
第二节、生物能及其存在形式
4、复合体Ⅳ: 细胞色素c氧化酶
功能:将电子从细胞色素c传递给氧
复合体IV
还原型Cytc → CuA→a→a3→CuB
→O2
其中Cyt a3 和CuB形成的活性部位将电子交给O2。
复 合 体 Ⅳ 的 电 子 传 递 过 程
Cytc
e-
胞液侧
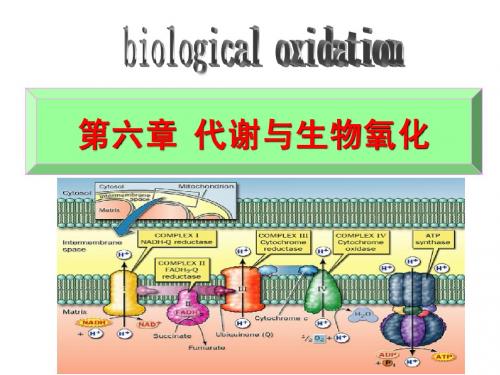
第六章 代谢与生物氧化
一、新陈代谢
第 六 章 代 谢 与 生 物 氧 化 4. 代谢
——完成某一代谢过程的一组相互衔接的酶 完成某一代谢过程的一组相互衔接的酶 促反应。 促反应。 特点: 特点:
没有完全可逆的代谢途径; 没有完全可逆的代谢途径; 的代谢途径 代谢途径形式是多样 形式是多样的 代谢途径形式是多样的; 代谢途径有确定的细胞定位 确定的细胞定位; 代谢途径有确定的细胞定位; 代谢途径是相互沟通的; 代谢途径是相互沟通 相互沟通的 能量关联; 代谢途径之间有能量关联 代谢途径之间有能量关联; 代谢途径的流量可调控 可调控。 代谢途径的流量可调控。
能
在高能化合物分子中, 在高能化合物分子中 , 被水解断裂时释放出大量 自由能的活泼共价键。 高能键常用符号“ 表示 表示。 自由能的活泼共价键。 高能键常用符号“ ~ ”表示。
“高能键”≠“键能高” 高能键” 高能键 键能高”
茶学与生物系-生物化学
代谢中的能量物质
第 六 章
根据分子结构和高能键的特征,高能化合物可分为: 根据分子结构和高能键的特征,高能化合物可分为: 焦磷酸化合物: (1) 焦磷酸化合物:如ATP
(C~S)型 型
茶学与生物系-生物化学
二、生物氧化
第 六 章 代 谢 与 生 物 氧 化 1.定义 定义
糖类、脂肪、 糖类、脂肪、蛋白质等有机物质在细胞中进行脱 加氧等氧化分解生成CO2和H2O,并释放出能量 氢、加氧等氧化分解生成 , 的过程称为生物氧化 生物氧化(biological oxidation)。 的过程称为生物氧化 。 其实质是需氧细胞在呼吸代谢过程中所进行的一 系列氧化还原反应过程,故又可称细胞呼吸 细胞呼吸。 系列氧化还原反应过程,故又可称细胞呼吸。
• 新陈代谢 一 新陈代谢一 物质 和 能量 转变
生物化学 生物氧化(6)

基质 嵴 内膜
外膜
外膜 膜间腔 F1-F0复合体
内膜
F1亚基 F0亚基
膜间腔
线粒体结构模式图
线粒体嵴的分子组成
2020/6/11
27
线粒体的结构
2020/6/11
呼吸链
28
二、电子传递链的组成及电子传递顺序
1、电子传递中有四个复合体参与:
OO CH3 C O P O-
O-
乙酰磷酸
O
O
RC O P O A
O
O
O-
H3N+ C O P OO-
酰基腺苷酸
O
O
氨甲酰磷酸 RCH C O P O A
N+H3
O-
氨酰基腺苷酸
(B) 焦磷酸化合物
OO
O- P O P O-
O-
O-
焦磷酸
O O- P
O-
ATP(三磷酸腺苷)
7.3千卡/摩尔
O O- P
O-
O O- P
O-
NH2
N
N
NN OCH2 O
HH
H
H
OH OH
(C)烯醇式磷酸化合物
COOH O CO PO CH2 O
磷酸烯醇式丙酮酸 14.8千卡/摩尔
(2) 氮磷键型
O
O
NH
PO
NH
PO
C NH O N CH3 CH2COOH
C NH O N CH3 NH2 CH2CH2CH2CHCOOH
CH2 H3C S+ A
3.最重要的高能化合物ATP (三磷酸腺苷)
NH2
N
N
~ ~ O-
Oγ
P O-
生物化学第六章生物氧化

(还原剂) (氧化剂)
可写成 A2+ B3+
A3+
B2+
2019/11/23
生物化学教研室
9
第三节 生成ATP的氧化体系
一、呼吸链的概念
代谢物脱下的成对氢原子(2H)通过多种酶和辅酶所 催化的连锁反应逐步传递,最终与氧结合生成水。由 于此过程与细胞呼吸有关,所以将传递链称为呼吸链, 也叫电子传递呼吸链。
氧化酶,而其它均为不需氧脱氢酶。其中a与 a3很难分开,常写为aa3。
在微粒体中主要为细胞色素b5、p450。p450作用 与aa3类似 。
2019/11/23
生物化学教研室
19
细胞色素的结构
2019/11/23
生物化学教研室
20
呼吸链复合体
人线粒体呼吸链通过上述5大类成分形成4个复合体。
2019/11/23
P/O比值:每消耗1摩尔原子氧所消耗的无机磷 原子的摩尔数。
2019/11/23
生物化学教研室
39
2、氧化磷酸化的偶联机制
内模胞浆侧
化 学 渗 透 学 说内膜基侧2019/11/23
生物化学教研室
40
ATP合酶(复合体Ⅴ)
由F1和F0组成。 F1 在线粒体内膜基质 侧形成颗粒状突起, 催化ATP的生成。 F膜0镶中嵌。在当线H+粒顺体浓内度 梯度经回流时,γ 亚基发生旋转,3个 β 亚基构象变化, 由紧密结合型变为 开放型,释放ATP。
根据呼吸链各组分的标准氧化还原电位测定(电位越 低越容易失去电子)、利用呼吸链特异性的阻断剂测 定其氧化和还原状态的吸收光谱及离体线粒体各组分 的氧化顺序等实验,确定了呼吸链各组分的排列顺序, 并发现体内存在两条主要的呼吸链。
第6章 生物氧化

其作用是催化电子从琥珀酸转至泛醌,但不转 移质子。 至少由4条肽链组成,含有黄素蛋白(FAD), 铁硫蛋白和细胞色素(cytochrome,Cyt)b560。 电子传递的方向为:琥珀酸→FAD→Fe-S→Q。 反应结果为:琥珀酸+Q→延胡索酸+QH2
生物化学与分子生物学教研室
FMN的结构
黄素蛋白中的FAD的结构
1、复合体Ⅰ—— NADH脱氢酶
其作用是催化NADH的2H传递至泛醌(辅酶Q), 同时将4个质子由线粒体基质(M侧)转移至膜 间隙(C侧)。 动物的复合物Ⅰ由42条肽链组成,呈L型,含有 黄素蛋白(FMN为辅酶)和铁硫蛋白(铁硫簇为 辅酶),分子量接近1MD,以二聚体形式存在。 电子传递的方向为:NADH→FMN→Fe-S→Q,总 的反应结果为:NADH + 5H+M + Q→NAD+ + QH2 + 4H+C
生物化学与分子生物学教研室
线粒体结构
生物化学与分子生物学教研室
(一) 呼吸链的组成
用胆酸、脱氧胆酸处理线粒体内膜,可以得到 四个具有电子传递功能的酶复合体和1个ATP合酶。
辅酶Q和细胞色素C 不属于任何一种复合物。辅 酶Q溶于内膜、细胞色素C位于线粒体内膜的外侧, 属于膜的外周蛋白。
生物化学与分子生物学教研室
(Fe-S)
O2
-
NDP
-
ATP
寡霉素
生物化学与分子生物学教研室
2、ADP的调节作用:ADP增多,促进磷酸化。 3、甲状腺激素:促进氧化磷酸化;使偶联蛋白 基因表达增加,引起耗氧和产热增加。 4、线粒体DNA突变
生物化学与分子生物学教研室
四、ATP
(一)高能化合物与ATP
生物化学与分子生物学教研室
FMN的结构
黄素蛋白中的FAD的结构
1、复合体Ⅰ—— NADH脱氢酶
其作用是催化NADH的2H传递至泛醌(辅酶Q), 同时将4个质子由线粒体基质(M侧)转移至膜 间隙(C侧)。 动物的复合物Ⅰ由42条肽链组成,呈L型,含有 黄素蛋白(FMN为辅酶)和铁硫蛋白(铁硫簇为 辅酶),分子量接近1MD,以二聚体形式存在。 电子传递的方向为:NADH→FMN→Fe-S→Q,总 的反应结果为:NADH + 5H+M + Q→NAD+ + QH2 + 4H+C
生物化学与分子生物学教研室
线粒体结构
生物化学与分子生物学教研室
(一) 呼吸链的组成
用胆酸、脱氧胆酸处理线粒体内膜,可以得到 四个具有电子传递功能的酶复合体和1个ATP合酶。
辅酶Q和细胞色素C 不属于任何一种复合物。辅 酶Q溶于内膜、细胞色素C位于线粒体内膜的外侧, 属于膜的外周蛋白。
生物化学与分子生物学教研室
(Fe-S)
O2
-
NDP
-
ATP
寡霉素
生物化学与分子生物学教研室
2、ADP的调节作用:ADP增多,促进磷酸化。 3、甲状腺激素:促进氧化磷酸化;使偶联蛋白 基因表达增加,引起耗氧和产热增加。 4、线粒体DNA突变
生物化学与分子生物学教研室
四、ATP
(一)高能化合物与ATP
中职生物化学课件第6章

子,使氧激活成为氧
离子,故又被称为细 胞色素氧化酶。
Cyta与Cyta3结合紧密很难分开,常被称为 细胞色素aa3(Cytaa3)
一、呼吸链的组成
❖在呼吸链组成成分中,除了少数游离存在 外,大部分以复合体的形式存在。线粒体 内膜中含有四种具有传递电子功能的酶复 合体,这些复合体主要通过上述酶和辅酶 组分发挥其传递氢或电子的功能。
三、ATP的生成与能量的利用和转移
(二)ATP的生成方式
ATP的生成方式
底物水平磷酸化
氧化磷酸化
三、ATP的生成与能量的利用和转移
(二)ATP的生成方式
1. 底物水平磷酸化 代谢过程中,代谢物由于脱氢或脱水引起分
子内部能量重新排布,形成高能键,然后把高能 键的能量转移给ADP形成ATP的过程称为底物水 平磷酸化。如:
❖(二)脱氢酶 需氧脱氢酶: 如黄嘌呤氧化酶 不需氧脱氢酶:如乳酸脱氢酶
三、生物氧化过程中CO2的生成
❖ 体内二氧化碳的生成来自于有机酸的脱羧作用, 而不是碳和氧的直接化合。根据有机酸脱去羧基 的位置不同可分为-脱羧和-脱羧,又根据脱羧 是否伴随氧化,分为氧化脱羧和单纯脱羧。
三、生物氧化过程中CO2的生成
一、呼吸链的组成
表6-1 四种人线粒体呼吸链复合体
复合体 复合体Ⅰ
酶名称 NADH-泛醌还原酶
辅基 FMN, Fe-S
复合体Ⅱ
琥珀酸-泛醌还原酶
FAD, Fe-S
复合体Ⅲ 复合体Ⅳ
泛醌-细胞色素c还原酶 细胞色素c氧化酶
铁卟啉,Fe-S 铁卟啉,Cu
二、呼吸链中氢和电子的传递顺序
❖ 实验证实,线粒体呼吸链有两条:一条是NADH 氧化呼吸链;另一条是琥珀酸氧化呼吸链。
离子,故又被称为细 胞色素氧化酶。
Cyta与Cyta3结合紧密很难分开,常被称为 细胞色素aa3(Cytaa3)
一、呼吸链的组成
❖在呼吸链组成成分中,除了少数游离存在 外,大部分以复合体的形式存在。线粒体 内膜中含有四种具有传递电子功能的酶复 合体,这些复合体主要通过上述酶和辅酶 组分发挥其传递氢或电子的功能。
三、ATP的生成与能量的利用和转移
(二)ATP的生成方式
ATP的生成方式
底物水平磷酸化
氧化磷酸化
三、ATP的生成与能量的利用和转移
(二)ATP的生成方式
1. 底物水平磷酸化 代谢过程中,代谢物由于脱氢或脱水引起分
子内部能量重新排布,形成高能键,然后把高能 键的能量转移给ADP形成ATP的过程称为底物水 平磷酸化。如:
❖(二)脱氢酶 需氧脱氢酶: 如黄嘌呤氧化酶 不需氧脱氢酶:如乳酸脱氢酶
三、生物氧化过程中CO2的生成
❖ 体内二氧化碳的生成来自于有机酸的脱羧作用, 而不是碳和氧的直接化合。根据有机酸脱去羧基 的位置不同可分为-脱羧和-脱羧,又根据脱羧 是否伴随氧化,分为氧化脱羧和单纯脱羧。
三、生物氧化过程中CO2的生成
一、呼吸链的组成
表6-1 四种人线粒体呼吸链复合体
复合体 复合体Ⅰ
酶名称 NADH-泛醌还原酶
辅基 FMN, Fe-S
复合体Ⅱ
琥珀酸-泛醌还原酶
FAD, Fe-S
复合体Ⅲ 复合体Ⅳ
泛醌-细胞色素c还原酶 细胞色素c氧化酶
铁卟啉,Fe-S 铁卟啉,Cu
二、呼吸链中氢和电子的传递顺序
❖ 实验证实,线粒体呼吸链有两条:一条是NADH 氧化呼吸链;另一条是琥珀酸氧化呼吸链。
复旦大学生化课件生物氧化

(2)催化:RH + O2 R + H2O 作用产物之一是H2O,不是H2O2;包括两种类型:金 属蛋白,如抗坏血酸氧化酶,含铜 L-抗坏血酸 + O2 脱氢抗坏血酸 + H2O
另一类是细胞色素氧化酶,催化: 4 Cyt c-Fe2+ + O2 4 Cyt c-Fe3+ + H2O
ቤተ መጻሕፍቲ ባይዱ
过氧化物酶(Peroxidase)
O
O
-酮 酸 脱 羧 酶
H 3C C COOM H g2+TPP H 3C C H+ C 2
2. -直 接 脱 羧
O
O
H2
丙酮酸脱羧酶
HOOC C C COOH
H3C C CO+OHC2
草 酰 乙 酸
丙 酮 酸
氧化脱羧基作用
(Oxidative decarboxylation)
1. -氧化脱羧
O
The matrix contains the enzymes that are responsible for the citric acid cycle, oxidation, AA oxidation and etc. The matrix also contains dissolved O2, H2O, CO2, the recyclable intermediates that serve as energy shuttles, and much more. Because of the folds of the cristae, no part of the matrix is far from the inner membrane. Therefore matrix components can quickly reach inner membrane complexes and transport proteins.
另一类是细胞色素氧化酶,催化: 4 Cyt c-Fe2+ + O2 4 Cyt c-Fe3+ + H2O
ቤተ መጻሕፍቲ ባይዱ
过氧化物酶(Peroxidase)
O
O
-酮 酸 脱 羧 酶
H 3C C COOM H g2+TPP H 3C C H+ C 2
2. -直 接 脱 羧
O
O
H2
丙酮酸脱羧酶
HOOC C C COOH
H3C C CO+OHC2
草 酰 乙 酸
丙 酮 酸
氧化脱羧基作用
(Oxidative decarboxylation)
1. -氧化脱羧
O
The matrix contains the enzymes that are responsible for the citric acid cycle, oxidation, AA oxidation and etc. The matrix also contains dissolved O2, H2O, CO2, the recyclable intermediates that serve as energy shuttles, and much more. Because of the folds of the cristae, no part of the matrix is far from the inner membrane. Therefore matrix components can quickly reach inner membrane complexes and transport proteins.
生物化学课件-生物氧化

26
1、不需传递体体系∶ 是最简单的生物氧化体系。从底物脱下来的氢不需传递, 直接在酶作用下与分子氧结合。这种酶可分为∶
2021/4/8
27
(1) 氧化酶类催化的反应模式∶
(见P310)
氧化酶类∶ 它是含Cu++或Fe++的金属蛋白,不能从底物上脱氢,只
能夺取底物上的电子对(2e),用于激活分子氧(O2),从而促 进氧与底物的化合。氰化物、硫化氢对氧化酶有抑制作用。
三羧酸 循环
2021/4/8
大分子降解 成基本结构 单位
小分子化合物 分解成共同的 中间产物(如 丙酮酸、乙酰
CoA等)
共同中间物进 入三羧酸循环, 氧化脱下的氢由 电子传递链传递 生成H2O,释放 出大量能量,其 中一部分通过磷 酸化储存在ATP 中。
5
二、中间代谢
1、酶抑制剂的应用 2、利用遗传缺陷症研究代谢途径 3、气体测量法 4、同位素示踪法
R为气体常数,其值为8.314J·K-1 ·mol-1,F为法拉第常数, 其值为96.485kJ /(V. mol ), T为热力学温度,当T = 298K时
Eφ’ =EφΘ0’ +
2.03.0033RTlg ca[(电氧 子化 受体型 ] )
nF
cg([还 电子原 供体型 ] )
2021/4/8
16
ADP + Pi
生物氧化过程中 释放出的自由能
ATP + H2O
2021/4/8
49
一、ATP 的生成
类别:底物水平磷酸化 电子传递水平磷酸化
2021/4/8
50
二、电子传递过程中自由能的变化
呼吸链中电子传递时自由能的下降
第06章生物氧化1

➢ 复合体Ⅲ每传递2个电 子向内膜胞浆侧释放4 个H+,复合体Ⅲ也有 质子泵作用。
➢ Cyt c是呼吸链唯一水 溶性球状蛋白,不包含 在复合体中。将获得的 电子传递到复合体Ⅳ。
目录
4. 复合体Ⅳ: 细胞色素c氧化酶
亚基:13条 辅酶/辅基:Cu+/Cu2+(含Cu多肽:CuA)
Fe2+/Fe3+(细胞色素aa3) Cu+/Cu2+(含Cu多肽:CuB)
血红素c 血红素a,a3,
CuA, CuB
含结合位点
NADH(基质侧) CoQ(脂质核心) 琥珀酸(基质侧) CoQ(脂质核心) Cyt c(膜间隙侧)
Cyt c1, Cyt a Cyt c(膜间隙侧)
➢ 泛醌不包含在上述四种复合体中。
目录
4H+
Ⅱ
琥珀酸
胞液侧
延胡索酸
Ⅰ
基质侧
QH2 Q
NADH+H+
目录
人线粒体呼吸链复合体
复合体
酶名称
复合体Ⅰ NADH-泛醌 还原酶
复合体Ⅱ 琥珀酸-泛醌 还原酶
复合体Ⅲ 泛醌-细胞色 素C还原酶
细胞色素c
复合体Ⅳ 细胞色素C氧 化酶
质量 (kD) 850
140
250
13 162
多肽 链数
39
4
11
1ห้องสมุดไป่ตู้13
功能辅基
FMN,Fe-S
FAD,Fe-S
血红素bL, bH, c1, Fe-S
目录
生物氧化与体外氧化之不同点
生物氧化
体外氧化
➢ 反应环境温和,酶促反应逐步 进行,能量逐步释放,能量容 易捕获,ATP生成效率高。
➢ Cyt c是呼吸链唯一水 溶性球状蛋白,不包含 在复合体中。将获得的 电子传递到复合体Ⅳ。
目录
4. 复合体Ⅳ: 细胞色素c氧化酶
亚基:13条 辅酶/辅基:Cu+/Cu2+(含Cu多肽:CuA)
Fe2+/Fe3+(细胞色素aa3) Cu+/Cu2+(含Cu多肽:CuB)
血红素c 血红素a,a3,
CuA, CuB
含结合位点
NADH(基质侧) CoQ(脂质核心) 琥珀酸(基质侧) CoQ(脂质核心) Cyt c(膜间隙侧)
Cyt c1, Cyt a Cyt c(膜间隙侧)
➢ 泛醌不包含在上述四种复合体中。
目录
4H+
Ⅱ
琥珀酸
胞液侧
延胡索酸
Ⅰ
基质侧
QH2 Q
NADH+H+
目录
人线粒体呼吸链复合体
复合体
酶名称
复合体Ⅰ NADH-泛醌 还原酶
复合体Ⅱ 琥珀酸-泛醌 还原酶
复合体Ⅲ 泛醌-细胞色 素C还原酶
细胞色素c
复合体Ⅳ 细胞色素C氧 化酶
质量 (kD) 850
140
250
13 162
多肽 链数
39
4
11
1ห้องสมุดไป่ตู้13
功能辅基
FMN,Fe-S
FAD,Fe-S
血红素bL, bH, c1, Fe-S
目录
生物氧化与体外氧化之不同点
生物氧化
体外氧化
➢ 反应环境温和,酶促反应逐步 进行,能量逐步释放,能量容 易捕获,ATP生成效率高。
生物氧化—氧化呼吸链(生物化学课件)

(二)氧化呼吸链组分的排列顺序
1、NADH氧化呼吸链
NADH →复合体Ⅰ→Q →复合体Ⅲ→Cyt c → 复合体Ⅳ→O2
2、琥珀酸氧化呼吸链
琥珀酸 →复合体Ⅱ →Q →复合体Ⅲ→Cyt c → 复合体Ⅳ→O2
NADH
琥珀酸
FAD (Fe-S)
FADH2氧化呼吸链
(琥珀酸、α-磷酸甘油、脂酰CoA)
➢ 电子传递过程: CoQH2→(Cyt bL→Cyt bH) →Fe-S
→Cytc1→Cytc
➢复合体Ⅲ每传递2个电子向内膜胞浆侧 释放4个H+,复合体Ⅲ也有质子泵作用。
细胞色素(cytochrome, Cyt)
细胞色素是一类含血红素样辅基(铁卟啉) 的电子传递蛋白,其中的铁原子可进行Fe2+ Fe3++e 反应传递电子,为单电子传递体。
➢ 每传递2个电子可将4个H+从内膜基质侧泵到 胞浆侧,复合体Ⅰ有质子泵功能。
(1)NAD+和NADP+的结构 R=H: NAD+; R=H2PO3: NADP+
NAD+(NADP+)和NADH(NADPH)相互转变
氧化还原反应时变化发生在五价氮和三价氮之间。 双电子传递体。
(2)FMN和FAD的结构
氧化还原对 Cyt c1 Fe3+ /Fe2+ Cyt c Fe3+ /Fe2+ Cyt a Fe3+ /Fe2+ Cyt a3 Fe3+ /Fe2+
1/2O2 /H2O
E0‘(V) 0.22 0.254 0.29 0.35 0.816
电子传递链
O
H 3C 5
第六章 生物氧化

E0‘(V)
-0.32 -0.219 -0.219
氧化还原对
Cyt c1 Fe3+ /Fe2+ Cyt c Fe3+ /Fe2+ Cyt a Fe3+ /Fe2+
E0‘(V)
0.22 0.254 0.29
Cyt bL(bH) Fe3+/Fe2+
Q10 /Q10H2
0.05(0.10)
0.06
Cyt a3 Fe3+ /Fe2+
FMN(FAD)的结构:
CH2OPO32H H H C C C CH2 H3C N N O OH OH OH
N H3C N
异 咯 嗪
O
异咯嗪环的作用:
FMN/FAD
FMNH /FADH
FMNH 2/FADH
2
(氧化型)
(还原型)
铁硫蛋白 铁硫蛋白(Fe-S)共有
9种同工蛋白;分子中
含有由半胱氨酸残基硫
目录
泛醌从复合体Ⅰ、Ⅱ募集还原当量和电子并穿 梭传递到复合体Ⅲ。
电子传递过程:CoQH2→(Cyt bL→Cyt bH)
→Fe-S →Cytc1→Cytc
目录
细胞色素类:
这是一类以铁卟啉为辅基的酶。在生物氧 化反应中,其铁离子可为+2价亚铁离子,也可 为+3价高铁离子,通过这种转变而传递电子。
R=H: NAD+;
R=H2PO3: NADP+
目录
NAD+(NADP+)和NADH(NADPH)相互转变
氧化还原反应时变化发生在五价氮和三价氮之间。
目录
FMN结构中含核黄素,发挥功能的部位是异 咯嗪环,氧化还原反应时不稳定中间产物是 FMNH· 。在可逆的氧化还原反应中显示3种分子状 态,属于单、双电子传递体。
生物化学:生物氧化 ppt课件

➢ 复合体Ⅳ 抑制剂:CN-、N3-紧密结合氧化型 Cyt a3,阻断电子由Cyt a到CuB- Cyt a3间传递。 CO与还原型Cyt a3结合,阻断电子传递给O2。
化学渗透示意图及各种抑制剂对电子传递链的影响
各种呼吸链抑制剂的阻断位点
抗霉素A 二巯基丙醇
CO、CN-、 N3-及H2S
×
×
×
化学渗透假说
要点: 1、线粒体内膜上电子传递链中的递电子体和递
氢体间隔排列,形成三个回路,回路有质子泵 的作用,可将质子( H+ )泵出线粒体基质。
2、递氢体从基质接受底物的氢原子,将电子交
给下一个递电子体,而将H+留在基质外胞液中。
化学渗透假说
要点: 3、整个过程中,仅有2个电子传递,并排出6个
H+,H+不能自由出入内膜,导致了内膜两侧的 H+浓度梯度和跨膜电位差,储存了一定的电化 学势能。
4、当内膜外侧的H+通过ATP合酶,顺电化学梯度
回流时,由ATP合酶底部进入线粒体基质时,将 储存的势能释放出来,推动ATP合酶的F1亚基利 用势能将ADP合成 ATP。
三、影响氧化磷酸化的因素
(一)有3类氧化磷酸化抑制剂
ATP
3-磷酸甘油酸 胞液
ATP
丙酮酸
GDP+Pi
(3)琥珀酸单酰COA GTP + ADP
GTP
线
琥珀酸 + HSCOA 粒
GDP + ATP 体
(一)确定氧化磷酸化偶联部位的实验依据
氧化磷酸化偶联部位:复合体Ⅰ、Ⅲ、Ⅳ
➢ 根据P/O比值 ➢ 自由能变化: ⊿Gº'=-nF⊿Eº'
1、P/O 比值 指氧化磷酸化过程中,每消耗1/2摩尔O2所生
化学渗透示意图及各种抑制剂对电子传递链的影响
各种呼吸链抑制剂的阻断位点
抗霉素A 二巯基丙醇
CO、CN-、 N3-及H2S
×
×
×
化学渗透假说
要点: 1、线粒体内膜上电子传递链中的递电子体和递
氢体间隔排列,形成三个回路,回路有质子泵 的作用,可将质子( H+ )泵出线粒体基质。
2、递氢体从基质接受底物的氢原子,将电子交
给下一个递电子体,而将H+留在基质外胞液中。
化学渗透假说
要点: 3、整个过程中,仅有2个电子传递,并排出6个
H+,H+不能自由出入内膜,导致了内膜两侧的 H+浓度梯度和跨膜电位差,储存了一定的电化 学势能。
4、当内膜外侧的H+通过ATP合酶,顺电化学梯度
回流时,由ATP合酶底部进入线粒体基质时,将 储存的势能释放出来,推动ATP合酶的F1亚基利 用势能将ADP合成 ATP。
三、影响氧化磷酸化的因素
(一)有3类氧化磷酸化抑制剂
ATP
3-磷酸甘油酸 胞液
ATP
丙酮酸
GDP+Pi
(3)琥珀酸单酰COA GTP + ADP
GTP
线
琥珀酸 + HSCOA 粒
GDP + ATP 体
(一)确定氧化磷酸化偶联部位的实验依据
氧化磷酸化偶联部位:复合体Ⅰ、Ⅲ、Ⅳ
➢ 根据P/O比值 ➢ 自由能变化: ⊿Gº'=-nF⊿Eº'
1、P/O 比值 指氧化磷酸化过程中,每消耗1/2摩尔O2所生
相关主题
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
为体内各种生理活动提供能量,形成磷酸酯类中间 代谢物参与酶的共价修饰。
高能磷酸键与高能磷酸化合物 高能磷酸键:水解时释放的能量大于30.5KJ/mol的
磷酸酯键,常表示为 P。
高能磷酸化合物:含有高能磷酸键的化合物
(第二货币)
各种高能磷酸化合物的生成:
二磷酸核 苷酸激酶
CDP CTP
组成:黄素蛋白(Flavoprotein)
含FMN 铁硫蛋白(Iron-sulfur protein) 含铁硫簇
FMN:黄素单核苷酸(Flavin mononucleotide)
铁硫簇(Iron-sulfur cluster, Fe-S)
NAD+的结构和作用
NAD+的结构和作用
氧化还原反应时氮原子在五价和三价之间变换
ATP
ADP
肌酸
磷酸肌酸
ATP的生成和利用
ATP
肌酸
磷酸 肌酸
氧化磷酸化 底物水平磷酸化
~P
机械能(肌肉收缩) 渗透能(物质主动转运) 化学能(合成代谢) 电能(生物电) 热能(维持体温)
ADP
~P
五、通过线粒体内膜的物质转运
线粒体外膜通透性高,线粒体对物质通过的选择性 主要依赖于内膜中不同转运载体对各种物质的转运。
各种细胞色素的结构:
复合体 III (Complex III)
细胞色素c是移动的电子载体
4. 复合体Ⅳ------细胞色素C氧化酶
功能:将电子从细胞色素C传递给氧 组成:Cyta, Cyta3 (含2个铁卟啉辅基和2个铜原 子)
Cu+
Cu2+ + e-
功能:将电子从细胞色素C传递给氧
细胞色素
定义:细胞色素是一类含有血红素的电子传递蛋白的总称。 分 类:根据吸收光谱不同,参与呼吸链组成的细胞色素 有Cyta、 Cytb、Cytc三类,每一类又因其最大吸收 峰的细微差别再分为几种亚类。 特 点:以铁卟啉为辅基,催化电子传递, 均有特殊吸收光谱而呈现颜色。
Cyta: Cyta、Cyta3 Cytb: Cytb562 、Cytb566 Cytc: Cytc、 Cytc1
2. 呼吸链成分的排列顺序
呼吸链成分的排列顺序试验依据
(Ⅰ) 根据呼吸链各组分的标准氧化还原电位
(Ⅱ) 利用呼吸链特异的抑制剂阻断某一组分的电子传递,阻断
部位前组分为还原态,后面组分为氧化态,根据吸收光谱改变 进行检测
还原态
氧化态
2、呼吸链类型
NADH氧化呼吸链:
由复合体Ⅰ、Ⅲ、Ⅳ组成。
代谢物脱下的氢经一定顺序排列的氢递体或电子递 体传递,与O2 结合生成H2O的完整体系,也称电子 传递链(Electron transfer chain)。
组 成:
递氢体、电子传递体
1. 呼吸链的组成
四种酶复合体
复合体
复合体Ⅰ 复合体Ⅱ 复合体Ⅲ 复合体Ⅳ
酶名称
NADH-泛醌还原酶 琥珀酸-泛醌还原酶
ATP ADP
UDP GDP GTP ATP UTP ADP
腺苷酸激酶 (adenylate kinase)
ATP ADP
ADP + ADP AMP + ATP
磷酸肌酸激酶 (Creatine phosphate,CP)
H
NH2 C NH H3C N CH2 COOH
N PO3H2 C NH H3C N CH2 COOH
谷草转氨酶
谷草转氨酶
2.ATP-ADP载体(ATP-ADP carrier) 2. 腺苷酸载体(adenine nucleotide transporter)
3. 线粒体蛋白的跨膜转运
线粒体外膜上的解折叠酶使蛋白质 空间结构松散
外膜受体识别,再被转移到总插入蛋白
总插入蛋白使蛋白质前体从氨基端 开始通过线粒体外膜与内膜之间的接触 点转运至线粒体基质 基质中的加工肽酶切除蛋白质前体 中含有导向信息的氨基端前导序列,生 成成熟的基质蛋白质
区段
电位变化 (⊿E°′)
自由能变化
⊿G°′=-nF⊿E°′
能否生成ATP
(⊿G°′是否大于30.5KJ)
NAD+~CoQ CoQ ~Cytc Cytaa3~O2
0.36V 0.21V 0.53V
69.5KJ/mol 40.5KJ/mol 102.3KJ/mol
能 能 能
氧化磷酸化偶联部位
ATP
ATP
ATP
2. 氧化磷酸化的偶联机制
化学渗透假说(Chemiosmotic
hypothesis)
电子经呼吸链传递时,释放的
能量可将质子(H+)从线粒体内膜的基 质侧泵到内膜外侧,产生膜内外质子 电化学梯度(H+ 浓度梯度和跨膜电 位差)。当质子顺浓度梯度回流时驱 动ADP与Pi生成ATP 。
外
F1与F0之间柄部的寡霉素敏感蛋白。
寡霉素
2. ADP的调节作用
ADP浓度增高,氧化磷酸化速度加快;
ADP不足,氧化磷酸化速度减慢。
呼吸控制率(Respiratory control ratio , RCR)
用离体线粒体实验,当有过量底物存在时,加入ADP 后的耗氧速率与仅有底物时的耗氧速率之比。
生物氧化的一般过程:
NADH+H+ or FADH2
ATP是能量生成和能量利用系统的桥梁
ATP
ADP
第一节 生成ATP的氧化体系
线 粒 体 氧 化 体 系
线粒体 (Mitochondria)
呼吸链(Respiratory chain)
一、呼吸链(Respiratory chain)
定义:
4,生物氧化生成的H2O是代谢物脱下的氢与氧 结合产生,H2O也直接参与生物氧化反应; CO2由有机酸脱羧产生,氧化过程中脱下来的氢 质子和电子,通常由各种载体,如NADH等传 递到氧并生成水。 5,生物氧化的速度由细胞自动调控。
部位:在真核生物细胞内,生物氧化都是在线 粒体内进行,原核生物则在细胞膜上进行。
呼吸链抑制剂:阻断呼吸链中某些部位电子传递
鱼藤酮(rotenone)、粉蝶霉素A(piericidin A)、异戊巴比妥 (amobarbital)等与复合体Ⅰ中的铁硫蛋白结合
抗霉素A(antimycin A)、二巯基丙醇(dimercapto-propanol) 抑制复合体Ⅲ中Cytb与Cytc1间的电子传递
P/O 比值: 物质氧化时,每消耗1摩氧原子所消耗的无机磷 的摩尔数(或ADP摩尔数),即生成ATP的摩尔数。
实验:
抗坏血酸 β-羟丁酸 P/O=2.4~2.8 生成2.5ATP P/O=1.7 生成1.5ATP P/O=0.88 生成1ATP 细胞色素C(Fe2+) P/O=0.61 ~0.68 生成0.5ATP
位于棕色脂肪组织中的线粒体中,主要有UCP-1、2、3、 4、5五种。
解偶联蛋白作用机制(棕色脂肪组织线粒体)
下丘脑感受冷刺激 交感神经 去甲肾上腺素
三酰甘油
目前,解偶联蛋白药物可用于治疗肥胖
氧化磷酸化抑制剂: 对电子传递及ADP磷酸化均有 抑制作用
例:寡霉素(oligomycin) 结合ATP合酶
生物化学
Biochemistry
CHAPTER 7
生物氧化
Biological oxidation
生物氧化的概念
物质在生物体内进行氧化称生物氧化,主要指糖、脂肪、
蛋白质等在体内分解时逐步释放能量,最终生成CO2 和 H2O
的过程。 糖
脂肪
蛋白质
O2
CO2和H2O
ADP+Pi 能量 ATP
热能
生物氧化的特点
由NAD+接受多种代谢产物脱氢得到的产物。 NADH所携带的高能电子是线粒体呼吸链主要 电子供体之一。
异咯嗪环
FAD
FMN
FMN的递氢作用
铁 硫 蛋 白
Fe
Fe2பைடு நூலகம்2
Fe4S4
空 间 构 象
Fe2+
Fe3+ + e
泛醌的递氢作用
复合体Ⅰ的功能
2.复合体Ⅱ------琥珀酸-泛醌还原酶
氧自由基的产生与消除
线粒体缺陷(母系遗传居多)与衰老等退行性疾 病有关,包括帕金森氏病和阿茨海默病等。
谷胱甘肽过氧化物酶与GSH还原酶
超氧化物歧化酶与过氧化氢酶
四、能量货币ATP
ATP的结构
N NH2
O HO P OH O
O P OH O
O P OH OH OH O CH2 N O N
N
ATP的功能
琥珀酸氧化呼吸链(FADH2氧化呼吸链): 由复合体Ⅱ、Ⅲ、Ⅳ组成。
FADH2氧化呼吸链
NADH氧化呼吸链
二、 氧化磷酸化 (oxidative phosphorylation)
定义:代谢物脱下的氢经呼吸链传递,逐步释放能量 使ADP磷酸化生成ATP的过程称氧化磷酸化。
1.确定偶联部位的实验及数据
解偶联剂(Uncoupler) 使氧化与磷酸化偶链过程脱离
基本作用机制:
使呼吸链传递电子过程中泵出的H+ ,不经ATP合酶的F0 质子通道回流,而通过线粒体内膜中其他途径返回线粒体基 质,从而破坏了内膜两侧的电化学梯度,使ATP的生成受到 抑制,由电化学梯度储存的能量以热能形式释放。
举例:
二硝基苯酚(Dinitrophenol, DNP) 解偶联蛋白(Uncoupling protein )
辅基
FMN,Fe-S FAD,Fe-S 铁卟啉,Fe-S 铁卟啉,Cu
泛醌-细胞色素C还原酶
细胞色素C氧化酶
