2020多发性骨髓瘤首次复发评估与治疗(完整版)
中国多发性骨髓瘤诊断和治疗指南(2020年版)

第2 位常见恶性肿瘤,多发于老年,目前仍无法
治愈。随着新药不断问世及检测手段的提高,
MM 的诊断和治疗得以不断改进和完善。本次指
南修订中增加了达雷妥尤单抗联合治疗部分及相
关注意事项,在难治复发性MM 部分增加了嵌合
抗原受体T 细胞免疫疗法,强调自体造血干细胞
移植对于适合移植患者仍然具有不可替代的地位。
肾功能正常[肌酐清除率>40ml/min或血清肌酐水平<177umol/L(2.0mg/dl)] 肾功能不全[肌酐清除率≤40ml/min或血清肌酐水平≥177umol/L(2.0mg/dl)]
中国多发性骨髓瘤诊治指南(2020 年修订)
本次指南修订中增加了达雷妥尤单抗联合治疗部 分及相关注意事项,在难治复发性MM 部分增加了嵌合 抗原受体T 细胞(chimeric antigen receptor T cell, CAR-T)免疫疗法,强调自体造血干细胞移植 (autologous hematopoietic stem cell transplantation, ASCT)对于适合移植患者仍然具有不可替代的地位。 本文是对该指南分析解读,供同行学习
·标准与讨论·
中国医师协会血液科医师分会
中华医
学会血液学分会
中国医师协会多发性
骨髓瘤专业委员会
通信作者:黄晓军,北京大学人民医院 北京大学
血液病研究所 国家血液系统疾病临床医学研究中
心100ห้องสมุดไป่ตู้44,Email:xjhrm@
【提要】 多发性骨髓瘤(MM)是一种克隆浆细
胞异常增殖的恶性疾病,在很多国家是血液系统
【关键词】 多发性骨髓瘤; 指南; 诊断; 治疗
一:临床表现
骨髓瘤相关器官功能损害 “CRAB”症状 C——血钙增高 R——肾功能损害(轻链管型肾病,蛋白尿,肌酐清除率下降) A——贫血(常为单纯正细胞正色素性贫血,少数伴白细胞、血小板减 少) B——骨病(骨痛、局部肿块、病理性骨折) 其他——免疫力下降、高粘滞血症、淀粉样病变等
2022中国多发性骨髓瘤诊治指南修订诊断部分解读全文

2022中国多发性骨髓瘤诊治指南修订诊断部分解读(全文)摘要《中国多发性骨髓瘤诊治指南(2022年修订)》版再次和大家见面。
今年的指南〃诊断部分〃有较大修订,包括首次纳入高危冒烟型骨髓瘤的诊断标准、删除蛋白鉴定〃的界定,及增加罕见骨髓瘤类型的内容,体现了〃诊断标准制定更精准、诊断定义细节更规范、罕见类型诊断更全面〃的三大特点,本文对诊断部分的更新进行了详细解读。
多发性骨髓瘤(multiple myeloma z MM )是一种好发于老年人的恶性浆细胞肿瘤,1844年由Solly医生首次报道。
目前随着全球人口老龄化趋势,MM发病率逐年增高。
随着对骨髓瘤疾病的认识深入,新疗法的不断涌入,检测技术的快速发展,MM诊治指南更需更新迭代,因此《中国多发性骨髓瘤诊治指南》2022年修订版与大家如约而至。
本版指南〃诊断部分〃有较大修订,本着力求推进科学化、规范化,全面提高我国MM诊治水平的宗旨,在诊断部分体现了〃诊断标准制定更精准、诊断定义细节更规范、罕见类型诊断更全面〃的三大特点,具体解读如下。
一、诊断标准制定更精准本次诊断标准表2进行了精简,更加直观的展示了意义未明单克隆免疫球蛋白增多症monoclonal gammopathy of undetermined significance , MGUS )、冒烟型骨髓瘤(smoldering multiple myeloma , SMM )和活动性MM ( active multiple myeloma , aMM )的标准,尤为重要的是首次纳入高危冒烟型骨髓瘤(SMM )的诊断标准和删除M蛋白鉴定的诊断条件。
1.首次纳入高危冒烟型骨髓瘤(SMM)的诊断标准:高危冒烟型骨髓瘤的诊断标准国际上有不同的定义,从2007年的PETHEMA到2018年Mayo Clinic z 2020年国际骨髓瘤工作组(IMWG )所提出的标准,包括M蛋白量、骨髓浆细胞比例、受累轻链数值,PETCT结果,或者细胞遗传学(FISH )高危因素等特征,并且基于不同因素高危SMM的积分各有不同。
2020 ASH 多发性骨髓瘤AL淀粉样变性新进展

2020 ASH 多发性骨髓瘤/AL淀粉样变性新进展受COVID-19疫情影响,第62届美国血液学年会(ASH)将首次以线上形式于2020年12月5日-8日召开。
一年一度的ASH年会可谓是全球最顶级的血液学领域国际盛会,是全球上百个国家的上万名血液学专家获悉领域最新进展、交流学习的盛大平台。
今年ASH年会上在多发性骨髓瘤和轻链(AL)淀粉样变性领域将有哪些研究成果精彩亮相呢?1. CARTITUDE-1:Cilta-cel治疗复发/难治性多发性骨髓瘤(R/R MM)的Ib/II期临床研究摘要号:177Cilta-cel(LCAR-B38M;JNJ-68284528)是一种靶向B细胞成熟抗原的嵌合抗原受体T(CAR-T)细胞疗法。
在中国的LEGEND-2 I期研究中,Cilta-cel对患有R/R MM的患者产生了深度、持久的缓解,并具有可控的安全性。
本研究报告了来自Ib期的部分更新数据以及II 期的初始数据。
截至2020年5月20日,97例R/R MM患者接受了Cilta-cel治疗(29例Ib期,68例II期)。
中位随访时间为8.8个月。
总缓解率(Overall Response Rate,ORR,主要终点)为94.8%(95%CI 88.4–98.3),严格意义的完全缓解(sCR)率为55.7%(95%CI 45.2-65.8),非常好的部分缓解(VGPR)率为32.0%(95%CI 22.9–42.2),部分缓解(PR)率为7.2%(95%CI 3.0–14.3)。
所有患者的M蛋白水平均降低。
至首次缓解(第一次达到≥PR)的中位时间为1.0个月(范围0.9-5.8;80.4%≤1.0个月),至大于等于完全缓解(≥CR)的中位时间为1.8个月(范围0.9-12.5;74.1%≤3.0个月)。
缓解深度随着时间而加深,中位缓解持续时间未达到(NR)。
在52例微小残留病(MRD)可评估的患者中,94.2%的患者MRD阴性(阈值为10-5)。
骨髓瘤指南共识解读:多发性骨髓瘤的疗效评估(全文)

骨髓瘤指南共识解读:多发性骨髓瘤的疗效评估(全文)MM疗效评估指标概述多发性骨髓瘤(MM)的疗效评估体系最初是来自欧洲骨髓移植协作组(EBMT)的疗效标准,之后,国际骨髓瘤工作组(IMWG)采纳了这一标准,并做了一定程度的修订。
中国多发性骨髓瘤诊治指南也基本上参考IMWG的疗效标准,并且原则上建议在治疗期间,每隔30-60天进行一次疗效评估。
骨髓瘤的疗效评估相比白血病要复杂很多,主要是因为骨髓瘤的生物学特点比较特殊,骨髓瘤细胞在骨髓里面的分布是局灶性的,它的评估指标大体上可以分为三个部分,肿瘤细胞分泌产物、肿瘤细胞、整体影像学。
肿瘤细胞分泌产物看M蛋白,治疗以后M蛋白数量下降,下降的比例可作为疗效评估的一个重要基石。
但是精确检测M蛋白并不容易,因为会有多克隆正常浆细胞分泌的免疫球蛋白混杂其中。
M蛋白的检测方法进行M蛋白定量最常见的方法就是免疫比浊法,其原理是当可溶性抗原与相应抗体特异结合,二者比例合适时,在特殊的缓冲液中它们快速形成一定大小的抗原抗体复合物,使反应液体出现浊度。
利用现代光学测量仪器对浊度进行测定从而检测抗原含量。
它的优点是简便、快速。
缺点是测得的结果为免疫球蛋白的总量,所以没有办法区分它是单克隆的,还是多克隆的免疫球蛋白。
而血清蛋白电泳能够克服这一缺点,测定时可以进行M蛋白比例的计算。
对于IgG型MM,如果在血清蛋白电泳上出现M蛋白条带,M 蛋白条带的定义是高与底之比大于2,就可以认为它是M蛋白的片段,即单克隆的免疫球蛋白。
计算血清M蛋白就是用总蛋白乘以M蛋白在整体当中所占的比例。
对于轻链型MM,轻链分子量较小,容易进入尿液,所以轻链型MM疗效判断应该着重进行尿液检测,它的计算跟血中M蛋白类似,先测得24小时尿的总蛋白量,然后再乘以尿蛋白电泳当中M蛋白片段的比例,即得出24小时尿M蛋白的量。
有的中心不能进行尿蛋白电泳的检测,可测定替代尿M蛋白的量进行评估,即受累型尿轻链浓度,乘以24小时总尿量,得出来替代尿M蛋白的量。
中国多发性骨髓瘤诊治指南(2020年修订)

定义及背景 诊断标准、分型、分期 鉴别诊断 预后评估与危险分层 疗效评估 治疗与随访
疗效评估
✓参考2016年IMWG疗效标准,分为传统的疗效标准和MRD疗效标准,在治疗 中先进行传统的疗效评估,在临床研究中当患者进入完全缓解后再进行 MRD疗效评估。
✓微小缓解(minimal response,MR)、疾病稳定(stable disease,SD)仅用 于难治复发或临床试验中患者的疗效评估。
定义及背景 诊断标准、分型、分期 鉴别诊断 预后评估与危险分层 疗效评估 治疗与随访
鉴别诊断
✓MM需与可出现M蛋白的下列疾病鉴别:意义未明的单克隆丙种球蛋白病 (MGUS)、华氏巨球蛋白血症、AL型淀粉样变性、孤立性浆细胞瘤(骨 或骨外)、POMES综合征。
✓此外,还需与反应性浆细胞增多症、转移性癌的溶骨性病变、浆母细胞性淋 巴瘤、单克隆免疫球蛋白相关肾损害(MGRS)等鉴别,其中MGRS是由于 单克隆免疫球蛋白或其片段导致的肾脏损害,其血液学改变更接近MGUS, 但出现肾功能损害,需要肾脏活检证明是M蛋白或其片段通过直接或间接作 用所致。
诊断标准
(二)有症状(活动性)多发性骨髓 瘤诊断标准(需满足第1条及第2条, 加上第3条中任何1项)
分型
✓依照M蛋白类型分为:IgG型、IgA型、IgD型、IgM型、IgE型、轻链型、双 克隆型以及不分泌型。进一步可根据M蛋白的轻链型别分为κ型和λ型。
Durie-Salmon分期系统
国际分期系统(ISS)及修订的国际分期系统(R-ISS)
传统的IMWG疗效标准
4. 部分缓解(partial response,PR):(1)血清M 蛋白减少≥50%,24 h尿M蛋白减 少≥90%或降至<200 mg/24h;(2)若血清和尿中M 蛋白无法检测,要求受累与非受 累血清FLC之间的差值缩小≥50%;(3)若血清和尿中M蛋白以及血清FLC都不可测 定,且基线骨髓浆细胞比例≥30%时,则要求骨髓内浆细胞数目减少≥50%;(4)除 了上述标准外,若基线存在软组织浆细胞瘤,则要求可测量病变最大垂直径乘积之和 (sum of products of greatest diameters,SPD)缩小≥50%。以上血清学和尿M蛋白指 标均需连续2次评估,同时应无新的骨质病变发生或原有骨质病变进展的证据。 5.MR(仅用于难治/复发MM的评价):血清M蛋白减少25%~49%并且24 h尿轻链减 少50%~89%。若基线存在软组织浆细胞瘤,则要求可测量病变SPD缩小25%~49%。 溶骨性病变的数量和大小没有增加(可允许压缩性骨折的发生)。 6. SD:不符合CR、VGPR、PR、MR 及疾病进展(progressive disease,PD)标准。 同时无新的骨质病变或原有骨质病变进展的证据。
2024高危多发性骨髓瘤诊断与治疗专家共识要点(全文)

2024高危多发性骨髓瘤诊断与治疗专家共识要点(全文)过去的二十余年,由千新治疗策略的引入,多发性骨髓瘤(MM)患者的生存期得到显著延长。
但MM是一组生物学和临床高度异质性的肿瘤,仍有部分患者(15%~20%)从目前的治疗模式中获益较小。
这部分患者临床特征往往为侵袭性,表现为早期复发或原发难治,称之为高危多发性骨髓瘤(High risk multi p le myel om a, HR M M)。
临床医师应该及早识别出HRMM,给予个体化治疗。
为提高中国医师对HRMM的诊断及治疗水平,中国抗癌协会(C A C A)血液肿瘤专业委员会和中国临床肿瘤学会(CSCO)多发性骨髓瘤专家委员会组织相关专家经过多次讨论,制定了本版HRMM诊断与治疗中国专家共识。
一、HRMM的定义目前缺乏对HRMM的准确定义,参考国际骨髓瘤工作组(IMWG)对HRMM定义,专家委员会认为在规范治疗的情况下,接受auto-HSCT 的MM患者总生存(OS)期<3年或未接受auto-HSCT的MM患者OS 期<2年定义为HRMM患者,接受auto-HSCT的MM患者OS期<2年则定义为超高危MM(Ultra-high risk MM, UHRMM)患者。
二、根据预后因素识别HRMM由千高危患者从目前标准治疗模式中获益较少,因此根据预后因素识别此类患者非常重要,其中MM肿瘤细胞的生物学特征和治疗反应是识别HRMM的决定性因素。
(-) MM的静态预后因素1.遗传学高危因素:细胞遗传学异常是MM危险分层体系中的核心指标,但目前对高危细胞遗传学异常(H igh i sk cy o gen et i cs abnor m al i i es, H RCAs)的定义仍然存在一定的争议。
2016年IMWG指南将t(4;14)、t(14;16)、t(14;20)、del (17 /17p)、lq21获得/扩增、非超二倍体核型、核型del(13)、高危基因表达谱归为HRCAs。
复发难治性多发性骨髓瘤治疗研究新进展

复发难治性多发性骨髓瘤治疗研究新进展陈卫琼ꎬ莫祖艳ꎬ王珊珊ꎬ黄勃ꎬ王晓桃(桂林医学院第二附属医院血液内科ꎬ广西桂林541100)㊀㊀DOI:10 3969/j issn 1006 ̄2084 2020 06 011基金项目:国家自然科学基金(81460038)通信作者:王晓桃ꎬEmail:wxttjl@126.com中图分类号:R733.3㊀㊀㊀㊀㊀文献标识码:A㊀㊀㊀㊀㊀文章编号:1006 ̄2084(2020)06 ̄1097 ̄07㊀㊀摘要:多发性骨髓瘤是一种以浆细胞异常克隆为特征的异质性恶性肿瘤ꎬ几乎所有的患者最终都会出现复发或者难治ꎮ随着近年来的深入研究ꎬ复发难治性多发性骨髓瘤(RRMM)的临床治疗从传统的联合化疗发展到免疫疗法㊁细胞疗法等治疗方式ꎮ现已逐渐出现或正处于临床试验阶段的新的蛋白酶体抑制剂㊁免疫调节药物㊁单克隆抗体㊁组蛋白去乙酰化酶抑制剂等新型药物以及嵌合抗原受体T细胞免疫疗法㊁造血干细胞移植等治疗策略可改善患者的生存期ꎮ在未来ꎬ明确RRMM的发病机制㊁开发新型靶向治疗药物及细胞治疗可能成为RRMM的研究方向和重点ꎮ关键词:复发难治性多发性骨髓瘤ꎻ新型药物ꎻ嵌合抗原受体T细胞免疫疗法ꎻ造血干细胞移植NewProgressinTreatmentofRelapsedandRefractoryMultipleMyelomaCHENWeiqiongꎬMOZuyanꎬWANGShanshanꎬHUANGBoꎬWANGXiaotaoDepartmentofHematologyꎬtheSecondAffiliatedHospitalofGuilinMedicalUniversityꎬGuilin541100ꎬChinaCorrespondingauthor:WANGXiaotaoꎬEmail:wxttjl@126.comAbstract:Multiplemyelomaisakindofheterogeneousmalignanttumorcharacterizedbyabnormalplasmacellcloneꎬandalmostallofthepatientswillrelapseordevelopintorefractoryconditioneventually.Withthedeepeningresearchinrecentyearsꎬtheclinicaltreatmentofrelapsedandrefractorymultiplemyeloma(RRMM)recurrenceprogressesfromtradi ̄tionalcombinedchemotherapytoimmunetherapyandcelltherapy.Atpresentꎬproteasomeinhibitorsꎬimmunomodulatorydrugsꎬmonoclonalantibodiesꎬhistonedeacetylaseinhibitorsandchimericantigenreceptor ̄Tcellimmunotherapyꎬhemato ̄poieticstemcelltransplantationandothertherapeuticstrategieshavegraduallyemergedorareinclinicaltrialsꎬwhichmaysignificantlyimprovethesurvivalofpatients.InthefutureꎬidentifyingthepathogenesisofRRMMꎬdevelopingnewtargetedtherapeuticdrugsandcelltherapymaybecometheresearchdirectionandfocusofRRMM.Keywords:RelapsedandrefractorymultiplemyelomaꎻNewdrugꎻChimericantigenreceptor ̄TcelltherapyꎻHemato ̄poieticstemcelltransplantation㊀㊀多发性骨髓瘤(multiplemyelomaꎬMM)是一种血液系统恶性肿瘤ꎬ占血液系统恶性肿瘤的10%ꎬ主要发病年龄为63~70岁[1]ꎮMM是一种异质性疾病ꎬ主要通过促进恶性浆细胞的克隆扩增㊁刺激新生血管生成和激活破骨细胞等共同作用ꎮMM细胞过度表达CD54㊁淋巴细胞功能相关分子和CD56等表面抗原ꎬ使恶性浆细胞与骨髓微环境相互作用ꎬ促进旁分泌细胞因子的分泌ꎬ从而维持肿瘤细胞存活[2]ꎮ目前MM仍无法治愈ꎬ治疗目标在于控制疾病进展ꎬ改善总体反应率(overallresponserateꎬORR)㊁无进展生存期(progressionfreesurvivalꎬPFS)和总生存期(overallsurvivalꎬOS)ꎬ但大多数患者最终发展成为复发性或难治性的MM[3]ꎮ复发难治性多发性骨髓瘤(relapsedandrefractorymultiplemyelomaꎬRRMM)患者是指疗效达到微小反应及以上后出现的复发并且需进行补救的治疗者ꎬ或距最近一次治疗60d内疾病出现进展者[4]ꎮ客观实验室和放射学标准为:血清M蛋白增加ȡ25%或尿液中的单克隆蛋白绝对增加量必须ȡ200mg/24h及相关和未受影响的血清游离轻链之间的差异ȡ25%ꎬ新裂解性骨病变或软组织浆细胞瘤的新生㊁现有骨病变或软组织浆细胞瘤的大小显著增加ꎬ在非分泌性疾病患者中ꎬ复发MM定义为骨髓浆细胞百分比的增加(ȡ10%)[5 ̄6]ꎮ近年来ꎬ国内外不少学者对RRMM患者的治疗进行了深入的研究ꎮ现就RRMM的治疗进展予以综述ꎮ1㊀药物治疗1.1㊀蛋白酶体抑制剂1.1.1㊀Carfilzomib㊀Carfilzomib是一种四肽环氧酮蛋白酶体抑制剂ꎬ可与蛋白酶体亚基p5和低相对分子质量免疫蛋白酶体的亚基(LMP7)不可逆结合ꎬ并且比硼替佐米的亲和力更大ꎬ作为一种新型蛋白酶体抑制剂ꎬCarfilzomib适用于接受至少两种治疗的RRMM患者[7 ̄10]ꎮCarfilzomib单药治疗RRMM患者的ORR为23.7%ꎬPFS为7.8个月ꎬ中位OS为15.6个月[11]ꎮDimopoulos等[12]的Ⅲ期研究在RRMM患者中进行了Carfilzomib联合地塞米松与硼替佐米联合地塞米松的效果比较ꎬ结果显示ꎬCarfilzomib联合地塞米松组ORR优于硼替佐米联合地塞米松组(77%比63%)ꎬ且Carfilzomib联合地塞米松组不仅表现出更长的PFS(18.7个月比9.4个月)ꎬ并能显著阻碍疾病进展ꎬ降低死亡风险ꎬCarfilzomib联合地塞米松组血液不良事件发生率高于硼替佐米联合地塞米松组ꎬ主要表现为贫血㊁血小板减少ꎬ但神经病变低于硼替佐米联合地塞米松组ꎻ研究还发现ꎬCarfilzomib患者耐受性较硼替佐米好ꎬ其周围神经病变发生率较低ꎬ治疗效果好ꎬ不受其他药物的影响ꎬ在长期治疗中ꎬ成为治疗方案中的有吸引力的蛋白酶体抑制剂ꎮ在Stewart等[13]进行的一项Ⅲ期研究中ꎬ将复发MM患者随机分为Carfilzomib联合Lenalidomide及地塞米松组与Lenalidomide联合地塞米松组ꎬ结果ORR分别为87%和67%ꎬPFS分别为26.3个月和17.6个月ꎬ完全缓解分别为31.8%和9.3%ꎬ两组的不良事件相似ꎬCarfilzomib联合Lenalidomide及地塞米松组心血管事件发生率较Lenalidomide联合地塞米松组增加ꎮ由此可见ꎬCar ̄filzomib三联体治疗效果优于双联体联合治疗ꎬ双联体治疗效果优于单药治疗ꎮ故Carfilzomib三联体治疗未来可考虑作为至少接受一次治疗MM患者的长期临床方案[14]ꎮ1.1.2㊀Ixazomib㊀Ixazomib是第二代蛋白酶体抑制剂ꎬ并且是第一个口服蛋白酶体抑制剂ꎬ相比硼替佐米ꎬIxazomib具有较低的多发性神经病变风险ꎬ美国食品药品管理局(FoodandDrugAdministrationꎬFDA)已批准Ixazomib联合Lenalidomide和地塞米松用于治疗RRMM[7 ̄10]ꎮMateos等[15]研究中ꎬ将RRMM患者随机分为Ixazomib联合Lenalidomide及地塞米松组和安慰剂联合Lenalidomide及地塞米松组ꎬ结果显示ꎬIxazomib联合Lenalidomide及地塞米松组的PFS㊁ORR㊁完全缓解率均优于安慰剂联合Lenalidomide及地塞米松组(PFS:20.6个月比14.7个月ꎻORR:78%比72%ꎻ完全缓解率:12%比7%)ꎬIxazomib联合Lenalidomide及地塞米松组与安慰剂联合Lenalidomide及地塞米松组相比ꎬ最常见的不良事件为中性粒细胞减少症(22%比24%)㊁血小板减少症(19%比9%)及贫血(9%比13%)等ꎮ值得注意的是ꎬIxazomib所致血小板减少的药物不良反应呈周期性及短暂性[16]ꎮ研究发现ꎬIxazomib在年轻MM患者自体干细胞移植后和老年患者标准诱导后的维持治疗中可延长患者的生存期ꎬ提高生活质量[17]ꎮ1.1.3㊀Marizomib㊀Marizomib是一种正在研究的蛋白酶体抑制剂ꎬ与20S蛋白酶体的3个催化亚基不可逆结合ꎮMarizomib与20S蛋白酶体的不可逆结合是其细胞毒性增加㊁作用时间延长以及在硼替佐米耐药细胞系中保持活性的机制[18]ꎮⅠ期临床试验(NPI ̄0052 ̄107)研究中ꎬ用Marizomib㊁Pomalidomide和低剂量地塞米松治疗RRMMꎬ纳入38例患者ꎬ所有患者均已接受过Lenalidomide和硼替佐米治疗ꎬ结果显示ꎬORR为53%ꎬ完全缓解率为64%ꎬ最常见3级及以上的血液不良事件为中性粒细胞减少症(29%)㊁贫血(11%)和血小板减少症(11%)[19]ꎮ临床前研究表明ꎬMarizomib通过穿过血脑屏障ꎬ抑制大脑中的蛋白酶体活性ꎬ并在颅内胶质瘤异种移植模型中具有抗肿瘤作用[20]ꎮBadros等[21]报道ꎬMarizomib在RRMM中表现出令人鼓舞的活性ꎬ在胶质瘤中也有新的临床活性ꎬ因此Mmarizomib成为一种潜在的中枢神经系统MM治疗干预手段ꎮ1.1.4㊀Oprozomib㊀Oprozomib(ONX0912)是一种新型口服不可逆蛋白酶体抑制剂ꎬ其作用机制与Marizomib相似ꎬ主要通过抑制蛋白酶体的糜蛋白酶样活性发挥作用ꎮ目前研究发现ꎬOprozomib在体内和体外表现出类似的抗血管生成作用ꎬ激活胱天蛋白酶(caspase) ̄8㊁caspase ̄9㊁caspase ̄3和poly(ADP)核糖聚合酶ꎬ抑制MM细胞迁移[22]ꎮOprozomib的Ⅰb/Ⅱ期单药开放标签研究ꎬ共有106例患者参与ꎬ其中68例MM患者在多次治疗后复发ꎬ结果显示ꎬcarfilzomib难治性组的反应率为27%ꎬ硼替佐米难治性组的反应率(n=12)为25%[23]ꎮ在临床相关浓度下ꎬOprozomib在体外直接抑制破骨细胞的形成和促进骨吸收ꎬ同时增强成骨分化和基质矿化[24]ꎮ在MM小鼠模型中ꎬ含环氧酮基的蛋白酶体抑制剂可降低小鼠5TGM1和人RPMI ̄8226的肿瘤负荷ꎬ防止骨丢失[25]ꎮ这些数据表明ꎬ除了抗骨髓瘤的特性外ꎬOprozomib可以有效地将骨微环境从分解代谢状态转变为合成代谢状态ꎬ并且与硼替佐米类似ꎬ可以减少MM的骨骼并发症发生ꎮ在临床应用中ꎬOprozomib可提高MM骨病患者生活质量[26]ꎮ1.2㊀免疫调节剂1.2.1㊀Lenalidomide㊀Lenalidomide是一种免疫调节剂ꎬ其主要作用机制包括减少肿瘤坏死因子 ̄α㊁白细胞介素(interleukinꎬIL) ̄1β㊁IL ̄6和IL ̄12的产生ꎬ增加IL ̄2和γ干扰素的合成ꎬ增强抗原呈递功效的树突状细胞对肿瘤抗原的摄取ꎬ抑制T调节细胞ꎬ并增强自然杀伤T细胞的活性[27 ̄28]ꎮ在MyelomaXI研究中ꎬ符合移植条件组和不符合移植组RRMM患者接受Lenalidomide单药维持治疗ꎬ结果显示ꎬ符合移植条件组PFS显著优于不符合移植组(60.3个月比25.7个月)[29]ꎮ值得注意的是ꎬ该研究中的一部分患者(包括移植合格和移植不合格)通过流式细胞术进行微小残留(minimalresidualdiseaseꎬMRD)测试ꎬ56%达到MRD阴性ꎬ此外ꎬ32%维持治疗初期MRD阳性患者使用Lenalidomide维持治疗期间MRD转为阴性ꎬLenalidomide为这一人群提供了有价值的维持治疗选择[30]ꎮ目前FDA已批准Lenalidomide联合地塞米松㊁Daratumumab联合Lenalidomide及地塞米松㊁Elotuzumab联合Lenalidomide及地塞米松3种方案治疗RRMM患者[31]ꎮ研究还发现ꎬ对于新诊断的MM患者ꎬ自体干细胞移植后Lenalidomide维持治疗直至病情进展可延长PFS和OS[32]ꎮ此外ꎬvanBeurden等[33]针对RRMM的治疗方案进行荟萃分析ꎬ结果显示ꎬDaratumumab联合Lenalidomide及地塞米松的治疗效果最佳(12个月PFS为83.3%ꎻORR为92.9%)ꎮ1.2.2㊀Pomalidomide㊀Pomalidomide是新一代口服免疫调节剂ꎬ具有体外抗增殖和促凋亡作用ꎬ在RRMM患者中获得了比较好的疗效[34]ꎮ在随机Ⅲ期试验(MM ̄003)中ꎬRRMM患者随机分为Pomalidomide联合低剂量地塞米松组和Pomalidomide联合高剂量地塞米松组ꎬ中位随访10个月后ꎬ低剂量地塞米松组的PFS㊁OS均优于高剂量组(PFS:4个月比1.9个月ꎻOS:12.5个月比8.1个月)[35]ꎮPomalidomide联合低剂量地塞米松治疗对硼替佐米和Lenalidomide双重抵抗的患者ꎬ中性粒细胞减少发生率升高ꎬ大剂量Pomalidomide可能伴随骨髓抑制增加ꎬ但Pomalidomide治疗过程中所伴随的大部分血液学毒性可通过停药得以解决ꎬ而Pomalidomide是如何克服对Lenalidomide及硼替佐米耐药的骨髓瘤细胞基因的机制仍需要进一步研究[34ꎬ36]ꎮ研究还发现ꎬPomalidomide还用于免疫球蛋白轻链型淀粉样变性㊁骨髓纤维化㊁小细胞肺癌及其他晚期实体肿瘤的治疗ꎬ并且取得了较好的疗效[37]ꎮ2013年ꎬFDA和欧洲药品管理局已批准Pomalidomide单独或联合地塞米松治疗至少接受两个以上方案包括Lenalidomide和硼替佐米组合耐药的RRMM患者[35]ꎮ1.3㊀单克隆抗体1.3.1㊀Daratumumab㊀Daratumumab是一种针对CD38的人免疫球蛋白G1的单克隆抗体ꎬCD38是一种细胞表面蛋白ꎬ作为细胞内钙信号的调节因子ꎬ参与调控细胞凋亡㊁存活和增殖等信号通路[38]ꎮ在SIRIUS研究中ꎬRRMM患者接受16mg/kg的Daratumumab单药治疗ꎬ结果显示ꎬORR为29.2%ꎬPFS为7.4个月ꎬ完全缓解率为2.8%ꎬ非常好部分缓解率为12.2%ꎬ部分缓解率为29.2%ꎬ最常见血液不良事件为贫血(33%)和血小板减少(25%)[39]ꎮDaratumumab联合疗法会产生更强的效果ꎬ在POLLUX试验中ꎬRRMM患者随机分为Daratumumab联合Lenalidomide及地塞米松组和Lenalidomide联合地塞米松组ꎬ结果显示ꎬDaratumumab联合Lenalidomide及地塞米松组的PFS㊁ORR均优于Lenalidomide联合地塞米松组(12个月PFS:83.3%比60.1%ꎻORR:92.9%比76.4%)ꎬ常见的血液不良事件为中性粒细胞减少症(59%比43%)等[40]ꎮ此外ꎬ在EQUULEUS研究中ꎬDaratumumab联合Pomalidomide及地塞米松的疗效也较为显著ꎬORR为66%ꎬPFS为9.9个月[41]ꎮCASTOR研究中ꎬDaratumumab联合硼替佐米及地塞米松的PFS为26.2个月ꎬORR为85%[42]ꎮ根据以上试验结果分析得出ꎬDaratumumab三联用药方案FPS㊁ORR显著优于Daratumumab单药[43]ꎮBlommestein等[44]分析得出ꎬDaratumumab联合Lenalidomide及地塞米松方案治疗RRMM的PFS㊁ORR㊁OS均较显著ꎮ由于这些试验在RRMM治疗环境中具有宝贵的安全性和令人鼓舞的疗效数据ꎬDaratumumab目前正在Ⅲ期随机试验中进行测试ꎬ其中Daratumumab被添加到符合移植条件和不符合移植条件患者的前期治疗方案中ꎬ一旦证明有效ꎬ单克隆抗体可能成为前期治疗的标准部分[45]ꎮ1.3.2㊀Elotuzumab㊀Elotuzumab是针对CS1(cell ̄surfaceglycoproteinCD2subset1)的人源化免疫球蛋白G1单克隆抗体ꎮ临床前研究表明ꎬElotuzumab与蛋白酶体抑制剂和免疫调节剂具有协同作用ꎬⅠ期试验证明了Elotuzumab的安全性ꎬ并为其临床疗效提供了依据[46]ꎮ在RRMM患者中ꎬElotuzumab与Lenalidomide及地塞米松的联合治疗显示出良好的安全性和令人鼓舞的反应率ꎬELOQUENT2期研究中ꎬ将RRMM患者随机分为Elotuzumab联合Lenalidomide及地塞米松组和Lenalidomide联合地塞米松组ꎬ结果显示ꎬElotuzumab联合Lenalidomide及地塞米松组的总反应率㊁PFS㊁ORR均优于Lenalidomide联合地塞米松组(总反应率:79%比66%ꎻPFS:19.4个月比14.8个月ꎻORR:79%比66%)[47]ꎮZhang等[48]的荟萃分析结果显示ꎬElotuzuma单一疗法在RRMM患者中几乎没有疗效ꎬ三联方案的ORR为73%ꎬ其中Elotuzumab联合Lenalidomide及地塞米松方案的PFS㊁ORR较为显著ꎮ因此ꎬElotuzumab联合方案在RRMM中产生了满意的临床效果ꎬ可作为该类患者连续治疗的适宜选择[48 ̄49]ꎮ1.3.3㊀Indatuximab㊀Indatuximab是一种嵌合抗CD138单克隆抗体ꎮCD138在恶性浆细胞上的过度表达量很大ꎬ是MM中最特异性的靶抗原之一ꎮ抗CD138与美登木素生物碱类药物DM4的联合作用可使细胞毒素靶向传递至骨髓瘤细胞ꎬIndatuximab在细胞表面内化ꎬ将DM4释放到细胞质中ꎬ其抗微管蛋白作用可促进细胞死亡[17]ꎮ目前ꎬIndatuximab已经被批准在体外和临床上开展抗骨髓瘤药物联合研究[50]ꎮJagannath等[51]的研究中ꎬRRMM患者(n=34)接受不同剂量的Indatuximab单药治疗ꎬ结果显示5.9%的患者出现部分缓解(80mg/m2和140mg/m2)ꎬ超过75%的患者病情稳定或好转ꎬ14.7%的患者发生了轻微和部分反应ꎬ中位进展时间为3个月ꎬ中位OS为26.7个月ꎮ临床前研究表明ꎬIndatuximab和Lenalidomide之间存在相当大的协同作用ꎬ两者联合治疗可能产生更好的疗效ꎬ目前还处于临床试验研究中[8]ꎮ1.4㊀组蛋白去乙酰化酶(histonedeacetylaseꎬHDACi)Panobinostat是一种有效的pan ̄HDACiꎬ它通过调节组蛋白乙酰化和组蛋白去乙酰化水平ꎬ参与MM细胞基因转录ꎬ诱导氧化应激和DNA损伤ꎬ促进细胞周期停滞ꎬ诱导细胞凋亡ꎬ抑制聚集体及血管形成[45ꎬ52]ꎮLiu等[50]报道ꎬ共有700例RRMM患者接受Panobinostat治疗ꎬ汇总分析显示ꎬORR为45%(31%~59%)ꎬ临床获益率为56%(36%~76%)ꎬ疾病稳定率为29%(18%~41%)ꎬ疾病进展率为8%(4%~12%)ꎬPanobinostat与蛋白酶体抑制剂联合或不联合地塞米松的亚组分析中ꎬORR为52%ꎬ最常见的3/4级血液学不良事件为血小板减少症(48%)㊁中性粒细胞减少症(37%)㊁淋巴细胞减少症(33%)和贫血(16%)ꎬ非血液学不良事件包括腹泻(14%)㊁疲劳(12%)㊁肺炎(8%)和恶心(4%)等ꎮPanobinostat联合蛋白酶体抑制剂似乎对RRMM患者具有良好的耐受性和有效性[53]ꎮHDACis与其他抗骨髓瘤药物的联合治疗具有较好的临床效果ꎬ对于既往硼替佐米或Lenalidomide耐药的患者ꎬ联合HDACis为较好的选择ꎬ但是HDACis等多药联合的血液不良事件发生率也相对增加ꎮ鉴于此ꎬ深入探索HDACis在体内的药动学㊁组织分布㊁作用靶点和生物学作用的复杂性ꎬ有助于提高抗肿瘤效应并减少不良反应发生ꎬ为RRMM的治疗和预后带来更多的可能[45]ꎮ2㊀嵌合抗原受体T细胞免疫疗法细胞疗法是一种快速发展的骨髓瘤治疗方法ꎬ它独特的作用机制具有克服耐药性和有助于长期缓解的潜力[54]ꎮ目前正在研究两种主要的方法ꎬ即非基因修饰策略(依赖于内源性的抗骨髓瘤T细胞库)和基因修饰策略(引入新的T细胞受体或嵌合抗原受体以赋予新的抗原特异性)ꎮ其中B细胞成熟抗原 ̄嵌合抗原受体T细胞免疫疗法(chimericantigenreceptorT ̄cellimmunotherapyꎬCAR ̄T)㊁CD19㊁CD38㊁CD138和SLAMF7在内的多种抗原靶点正被用于骨髓瘤的研究ꎬ其中B细胞成熟抗原是最有希望的[55]ꎮ来自B细胞成熟抗原CAR ̄T细胞的四项Ⅰ期研究(每项研究使用不同的CAR结构ꎬ涉及90例RRMM患者)的初步数据显示ꎬ在有效剂量(>108CAR阳性细胞)的条件下ꎬ反应率为60%~100%ꎬ包括MRD阴性完全缓解ꎬ而且ꎬ在最近的两项研究中ꎬ中位随访时间为6~10个月ꎬ大多数患者仍无进展[56 ̄57]ꎮCAR ̄T细胞毒性与CD19CAR ̄T细胞相似ꎬ包括细胞因子释放综合征和神经毒性ꎬ这些毒性是可逆的ꎮ目前B细胞成熟抗原CAR ̄T细胞多项研究正在进行中ꎮ未来的研究方向包括与免疫调节药物或其他CAR ̄T细胞的联合应用ꎬ以及使用基因编辑的细胞产品来增强CAR ̄T细胞的安全性和有效性[58]ꎮ3㊀造血干细胞移植3.1㊀自体造血干细胞移植㊀有研究表明ꎬ新型药物联合自体造血干细胞移植可显著提高MM患者的完全缓解率及PFSꎬ提高患者生活质量[59]ꎬ但新药目前无法完全替代自体干细胞移植ꎮ美国国家综合癌症网络推荐ꎬ对于初治65岁以下的MM患者ꎬ在诱导治疗4个周期后ꎬ若疾病不处于进展阶段ꎬ无明确移植禁忌证ꎬ应行自体造血干细胞移植治疗[60]ꎮVeltri等[61]回顾性分析中ꎬ将接受首次自体造血干细胞移植的RRMM患者(n=233)分为双重难治性骨髓瘤组(n=105)和非双重难治性骨髓瘤(n=128)ꎬ结果显示ꎬ大多数患者能够获得疗效ꎬ并且一部分患者能够达到完全缓解ꎬ在存活患者的中位随访时间(42个月)中ꎬORR为80%ꎬ完全缓解率为22%ꎬ部分缓解率为40%ꎬ非双重难治性骨髓瘤组的PFS㊁OS㊁2年总生存率优于双重难治性骨髓瘤组(PFS:18.2个月比14.4个月ꎻOS:56.6个月比38.9个月ꎻ2年总生存率:76%比71%)ꎮ在常规化疗基础上进行自体造血干细胞移植能显著提高多发性骨髓瘤的完全缓解率㊁非常好部分缓解率ꎬ自体造血干细胞移植治疗的长期生存显著优于传统化疗ꎮ3.2㊀异基因造血干细胞移植㊀异基因造血干细胞移植由于移植物中无肿瘤细胞污染ꎬ并且移植物有抗骨髓瘤效应ꎬ从而进一步清除患者体内残存肿瘤细胞ꎬ成为目前唯一有可能治愈MM的方法[62]ꎮFranssen等[63]将147例MM患者分为异基因造血干细胞移植一线治疗组(n=58)和RRMM组(n=89)ꎬ中位随访时间为88.8个月中ꎬ结果显示ꎬ异基因造血干细胞移植治疗组完全缓解率㊁PFS㊁OS优于RRMM组(完全缓解率:48.3%比30.3%ꎻPFS:30.2个月比8.0个月ꎻOS:NR比28.7个月)ꎬ而RRMM组非常好部分缓解率㊁部分缓解率高于异基因造血干细胞移植治疗组(非常好部分缓解率:37.1%比31.0%ꎻ部分缓解率:20.2%比8.6%)ꎮGiralt等[64]指出ꎬ对于初次自体移植术后24个月内复发的患者ꎬ异基因造血干细胞移植应被认为是最合适的治疗方法ꎮ但在复发/难治性情况下ꎬ异基因造血干细胞移植的效果欠佳ꎬ特别是对于自体移植后早期复发的患者ꎮ在这方面ꎬ应探索最佳诱导ꎬ维持治疗和异基因后造血干细胞移植免疫治疗的价值ꎮ4㊀小㊀结RRMM的发病机制尚未完全阐明ꎬ相关信号通路的研究应针对这些通路的靶向药物开发ꎬ包括Venetoclax(ABT ̄199)㊁单克隆抗体Isatuximab㊁XPO ̄1抑制剂Selinexor㊁细胞毒性T淋巴细胞相关蛋白4抑制剂Ipilimumab和抗程序性细胞死亡1抑制剂Pembrolizumab等ꎮ目前RRMM的新型药物联合使用和CAR ̄T细胞疗法㊁造血干细胞移植等治疗方式取得了很好的疗效ꎮ随着越来越多的新型靶向药物的研发及临床上的不断探索以及对肿瘤干细胞认识的不断深入ꎬ将会给RRMM患者带来新的希望ꎮ参考文献[1]㊀BrennerHꎬGondosAꎬPulteD.Recentmajorimprovementinlong ̄termsurvivalofyoungerpatientswithmultiplemyeloma[J].Bloodꎬ2008ꎬ111(5):2521 ̄2526.[2]㊀KumarSKꎬRajkumarSVꎬDispenzieriAꎬetal.Improvedsurvivalinmultiplemyelomaandtheimpactofnoveltherapies[J].Bloodꎬ2008ꎬ111(5):2516 ̄2520.[3]㊀KyleRAꎬRajkumarSV.Criteriafordiagnosisꎬstagingꎬriskstratifica ̄tionandresponseassessmentofmultiplemyeloma[J].Leukemiaꎬ2009ꎬ23(1):3 ̄9.[4]㊀SonneveldPꎬBroijlA.Treatmentofrelapsedandrefractorymultiplemyeloma[J].Haematologicaꎬ2016ꎬ101(4):396 ̄406. [5]㊀AndersonKCꎬKyleRAꎬRajkumarSVꎬetal.Clinicallyrelevantendpointsandnewdrugapprovalsformyeloma[J].Leukemiaꎬ2008ꎬ22(2):231 ̄239.[6]㊀RajkumarSVꎬHarousseauJLꎬDurieBꎬetal.Consensusrecom ̄mendationsfortheuniformreportingofclinicaltrials:ReportoftheInternationalMyelomaWorkshopConsensusPanel1[J].Bloodꎬ2011ꎬ117(18):4691 ̄4695.[7]㊀ManasanchEEꎬOrlowskiRZ.Proteasomeinhibitorsincancertherapy[J].NatRevClinOncolꎬ2017ꎬ14(7):417 ̄433. [8]㊀ChhabraS.Novelproteasomeinhibitorsandhistonedeacetylaseinhibitors:Progressinmyelomatherapeutics[J].Pharmaceuticals(Basel)ꎬ2017ꎬ10(2).pii:E40.[9]㊀NaymagonLꎬAbdul ̄HayM.Novelagentsinthetreatmentofmultiplemyeloma:Areviewaboutthefuture[J].JHematolOncolꎬ2016ꎬ9(1):52.[10]㊀DouQPꎬZonderJA.Overviewofproteasomeinhibitor ̄basedanti ̄cancertherapies:Perspectiveonbortezomibandsecondgenerationproteasomeinhibitorsversusfuturegenerationinhibitorsofubiquitin ̄proteasomesystem[J].CurrCancerDrugTargetsꎬ2014ꎬ14(6):517 ̄536.[11]㊀SiegelDSꎬMartinTꎬWangMꎬetal.Aphase2studyofsingle ̄agentcarfilzomib(PX ̄171 ̄003 ̄A1)inpatientswithrelapsedandrefractorymultiplemyeloma[J].Bloodꎬ2012ꎬ120(14):2817 ̄2825.[12]㊀DimopoulosMAꎬMoreauPꎬPalumboAꎬetal.Carfilzomibanddexamethasoneversusbortezomibanddexamethasoneforpatientswithrelapsedorrefractorymultiplemyeloma(ENDEAVOR):Arandomisedꎬphase3ꎬopen ̄labelꎬmulticentrestudy[J].LancetOncolꎬ2016ꎬ17(1):27 ̄38.[13]㊀StewartAKꎬRajkumarSVꎬDimopoulosMAꎬetal.Carfilzomibꎬlenalidomideꎬanddexamethasoneforrelapsedmultiplemyeloma[J].NEnglJMedꎬ2015ꎬ372(2):142 ̄152.[14]㊀LandgrenOꎬSonneveldPꎬJakubowiakAꎬetal.Carfilzomibwithimmunomodulatorydrugsforthetreatmentofnewlydiagnosedmultiplemyeloma[J].Leukemiaꎬ2019ꎬ33(9):2127 ̄2143. [15]㊀MateosMVꎬMassziTꎬGrzaskoNꎬetal.Impactofpriortherapyontheefficacyandsafetyoforalixazomib ̄lenalidomide ̄dexam ̄ethasonevs.placebo ̄lenalidomide ̄dexamethasoneinpatientswithrelapsed/refractorymultiplemyelomainTOURMALINE ̄MM1[J].Haematologicaꎬ2017ꎬ102(10):1767 ̄1775.[16]㊀MoreauPꎬMassziTꎬGrzaskoNꎬetal.Oralixazomibꎬlenalido ̄mideꎬanddexamethasoneformultiplemyeloma[J].NEnglJMedꎬ2016ꎬ374(17):1621 ̄1634.[17]㊀NijhofISꎬvandeDonkNWCJꎬZweegmanSꎬetal.CurrentandNewTherapeuticStrategiesforRelapsedandRefractoryMultipleMyeloma:AnUpdate[J].Drugsꎬ2018ꎬ78(1):19 ̄37. [18]㊀AllegraAꎬAlonciAꎬGeraceDꎬetal.Neworallyactiveproteasomeinhibitorsinmultiplemyeloma[J].LeukResꎬ2014ꎬ38(1):1 ̄9. [19]㊀SpencerAꎬHarrisonSꎬZonderJꎬetal.Aphase1clinicaltrialevaluatingmarizomibꎬpomalidomideandlow ̄dosedexamethasoneinrelapsedandrefractorymultiplemyeloma(NPI ̄0052 ̄107):Finalstudyresults[J].BrJHaematolꎬ2018ꎬ180(1):41 ̄51. [20]㊀DiKꎬLloydGKꎬAbrahamVꎬetal.Marizomibactivityasasingleagentinmalignantgliomas:Abilitytocrosstheblood ̄brainbarrier[J].NeuroOncolꎬ2016ꎬ18(6):840 ̄848.[21]㊀BadrosAꎬSinghZꎬDhakalBꎬetal.Marizomibforcentralnervoussystem ̄multiplemyeloma[J].BrJHaematolꎬ2017ꎬ177(2):221 ̄225.[22]㊀RajanAMꎬKumarS.Newinvestigationaldrugswithsingle ̄agentactivityinmultiplemyeloma[J].BloodCancerJꎬ2016ꎬ6(7):e451.[23]㊀GelfandETꎬBasualdoCAꎬCallaghanJC.Carcinoidtumorofthethymusassociatedwithrecurrentpericarditis[J].Chestꎬ1981ꎬ79(3):350 ̄351.[24]㊀ZhouHJꎬAujayMAꎬBennettMKꎬetal.Designandsynthesisofanorallybioavailableandselectivepeptideepoxyketoneprotea ̄someinhibitor(PR ̄047)[J].JMedChemꎬ2009ꎬ52(9):3028 ̄3038.[25]㊀SpuntSLꎬGruppSAꎬVikTAꎬetal.PhaseⅠstudyoftemsirolimusinpediatricpatientswithrecurrent/refractorysolidtumors[J].JClinOncolꎬ2011ꎬ29(21):2933 ̄2940.[26]㊀HurchlaMAꎬGarcia ̄GomezAꎬHornickMCꎬetal.Theepoxyketone ̄basedproteasomeinhibitorscarfilzomibandorallybioavailableoprozomibhaveanti ̄resorptiveandbone ̄anabolicactivityinadditiontoanti ̄myelomaeffects[J].Leukemiaꎬ2013ꎬ27(2):430 ̄440. [27]㊀SzalatRꎬMunshiNC.NovelAgentsinMultipleMyeloma[J].CancerJꎬ2019ꎬ25(1):45 ̄53.[28]㊀ChimCSꎬKumarSKꎬOrlowskiRZꎬetal.Correction:Managementofrelapsedandrefractorymultiplemyeloma:Novelagentsꎬantibodiesꎬimmunotherapiesandbeyond[J].Leukemiaꎬ2019ꎬ33(4):1058 ̄1059.[29]㊀MorganGJꎬGregoryWMꎬDaviesFEꎬetal.Theroleofmainte ̄nancethalidomidetherapyinmultiplemyeloma:MRCMyelomaIXresultsandmeta ̄analysis[J].Bloodꎬ2012ꎬ119(1):7 ̄15. [30]㊀ZagouriFꎬTerposEꎬKastritisEꎬetal.Anupdateontheuseoflenalidomideforthetreatmentofmultiplemyeloma[J].ExpertOpinPharmacotherꎬ2015ꎬ16(12):1865 ̄1877.[31]㊀GormleyNJꎬKoCWꎬDeisserothAꎬetal.FDADrugApproval:ElotuzumabinCombinationwithLenalidomideandDexamethasonefortheTreatmentofRelapsedorRefractoryMultipleMyeloma[J].ClinCancerResꎬ2017ꎬ23(22):6759 ̄6763.[32]㊀RichardsonPGꎬHolsteinSAꎬSchlossmanRLꎬetal.Lenalidomideincombinationoraloneasmaintenancetherapyfollowingautolo ̄gousstemcelltransplantinpatientswithmultiplemyeloma:Areviewofoptionsforandagainst[J].ExpertOpinPharmacotherꎬ2017ꎬ18(18):1975 ̄1985.[33]㊀vanBeurden ̄TanCHYꎬFrankenMGꎬBlommesteinHMꎬetal.SystematicLiteratureReviewandNetworkMeta ̄AnalysisofTreatmentOutcomesinRelapsedand/orRefractoryMultipleMyeloma[J].JClinOncolꎬ2017ꎬ35(12):1312 ̄1319. [34]㊀EngelhardtMꎬAjayiSꎬReinhardtHꎬetal.Pomalidomide[J].RecentResultsCancerResꎬ2018ꎬ212:169 ̄185.[35]㊀DimopoulosMAꎬPalumboAꎬCorradiniPꎬetal.Safetyandefficacyofpomalidomidepluslow ̄dosedexamethasoneinSTRATUS(MM ̄010):Aphase3bstudyinrefractorymultiplemyeloma[J].Bloodꎬ2016ꎬ128(4):497 ̄503.[36]㊀LudwigHꎬSonneveldP.Diseasecontrolinpatientswithrelapsedand/orrefractorymultiplemyeloma:Whatistheoptimaldurationoftherapy?[J].LeukResꎬ2012ꎬ36(Suppl1):S27 ̄34. [37]㊀LaroccaAꎬMontefuscoVꎬBringhenSꎬetal.Pomalidomideꎬcyclo ̄phosphamideꎬandprednisoneforrelapsed/refractorymultiplemye ̄loma:Amulticenterphase1/2open ̄labelstudy[J].Bloodꎬ2013ꎬ122(16):2799 ̄2806.[38]㊀DimopoulosMAꎬOriolAꎬNahiHꎬetal.Daratumumabꎬlenalido ̄mideꎬanddexamethasoneformultiplemyeloma[J].NEnglJMedꎬ2016ꎬ375(14):1319 ̄1331.[39]㊀LonialSꎬWeissBMꎬUsmaniSZꎬetal.Daratumumabmonotherapyinpatientswithtreatment ̄refractorymultiplemyeloma(SIRIUS):Anopen ̄labelꎬrandomisedꎬphase2trial[J].Lancetꎬ2016ꎬ387(10027):1551 ̄1560.[40]㊀XuXSꎬDimopoulosMAꎬSonneveldPꎬetal.PharmacokineticsandExposure ̄ResponseAnalysesofDaratumumabinCombinationTherapyRegimensforPatientswithMultipleMyeloma[J].AdvTherꎬ2018ꎬ35(11):1859 ̄1872.[41]㊀ChariAꎬSuvannasankhaAꎬFayJWꎬetal.Daratumumabpluspomalidomideanddexamethasoneinrelapsedand/orrefractorymultiplemyeloma[J].Bloodꎬ2017ꎬ130(8):974 ̄981. [42]㊀PalumboAꎬChanan ̄KhanAꎬWeiselKꎬetal.DaratumumabꎬBortezomibꎬandDexamethasoneforMultipleMyeloma[J].NEnglJMedꎬ2016ꎬ375(8):754 ̄766.[43]㊀BlairHA.Daratumumab:AReviewinRelapsedand/orRefractoryMultipleMyeloma[J].Drugsꎬ2017ꎬ77(18):2013 ̄2024. [44]㊀BlommesteinHMꎬvanBeurden ̄TanCHYꎬFrankenMGꎬetal.Efficacyoffirst ̄linetreatmentsformultiplemyelomapatientsnoteligibleforstemcelltransplantation:Anetworkmeta ̄analysis[J].Haematologicaꎬ2019ꎬ104(5):1026 ̄1035.[45]㊀RoyceSGꎬVerverisKꎬKaragiannisTC.Histonedeacetylaseinhibi ̄tors:Canweconsiderpotentanti ̄neoplasticagentsforthetreatmentofasthma?[J].AnnClinLabSciꎬ2012ꎬ42(3):338 ̄345. [46]㊀LonialSꎬDimopoulosMꎬPalumboAꎬetal.Elotuzumabtherapyforrelapsedorrefractorymultiplemyeloma[J].NEnglJMedꎬ2015ꎬ373(7):621 ̄631.[47]㊀GrosickiSꎬBarchnickaA.Elotuzumab:Anovelimmune ̄stimula ̄tingtherapytotreatmultiplemyeloma[J].ExpertRevHematolꎬ2016ꎬ9(7):621 ̄628.[48]㊀ZhangTꎬWangSꎬLinTꎬetal.Systematicreviewandmeta ̄analysisoftheefficacyandsafetyofnovelmonoclonalantibodiesfortreat ̄mentofrelapsed/refractorymultiplemyeloma[J].Oncotargetꎬ2017ꎬ8(20):34001 ̄34017.[49]㊀TaiYTꎬDillonMꎬSongWꎬetal.Anti ̄CS1humanizedmonoclonalantibodyHuLuc63inhibitsmyelomacelladhesionandinducesantibody ̄dependentcellularcytotoxicityinthebonemarrowmilieu[J].Bloodꎬ2008ꎬ112(4):1329 ̄1337.[50]㊀LiuJDꎬSunCYꎬTangLꎬetal.EfficacyandSafetyofPanobinostatinRelapsedor/andRefractoryMultipleMyeloma:MetaAnalysesofClinicalTrialsandSystematicReview[J].SciRepꎬ2016ꎬ6:27361[51]㊀JagannathSꎬHeffnerLTJrꎬAilawadhiSꎬetal.IndatuximabRavtansine(BT062)MonotherapyinPatientsWithRelapsedand/orRefractoryMultipleMyeloma[J].ClinLymphomaMyelomaLeukꎬ2019ꎬ19(6):372 ̄380.[52]㊀AtadjaP.Developmentofthepan ̄DACinhibitorpanobinostat(LBH589):Successesandchallenges[J].CancerLettꎬ2009ꎬ280(2):233 ̄241.[53]㊀RichardsonPGꎬHungriaVTꎬYoonSSꎬetal.Panobinostatplusbortezomibanddexamethasoneinpreviouslytreatedmultiplemyeloma:Outcomesbypriortreatment[J].Bloodꎬ2016ꎬ127(6):713 ̄721.[54]㊀AbbasiJ.AmidFDAapprovalfilingsꎬanotherCAR ̄Ttherapypatientdeath[J].JAMAꎬ2017ꎬ317(22):2271.[55]㊀AliSAꎬShiVꎬMaricIꎬetal.Tcellsexpressingananti ̄B ̄cellmaturationantigenchimericantigenreceptorcauseremissionsofmultiplemyeloma[J].Bloodꎬ2016ꎬ128(13):1688 ̄1700. [56]㊀BaumeisterSHꎬMuradJꎬWernerLꎬetal.PhaseITrialofAutolo ̄gousCARTCellsTargetingNKG2DLigandsinPatientswithAML/MDSandMultipleMyeloma[J].CancerImmunolResꎬ2019ꎬ7(1):100 ̄112.[57]㊀CohenADꎬGarfallALꎬStadtmauerEAꎬetal.Bcellmaturationantigen ̄specificCARTcellsareclinicallyactiveinmultiplemyeloma[J].JClinInvestꎬ2019ꎬ129(6):2210 ̄2221. [58]㊀XuJꎬWangQꎬXuHꎬetal.Anti ̄BCMACAR ̄Tcellsfortreatmentofplasmacelldyscrasia:CasereportonPOEMSsyndromeandmultiplemyeloma[J].JHematolOncolꎬ2018ꎬ11(1):128. [59]㊀DhakalBꎬSzaboAꎬChhabraSꎬetal.AutologousTransplantationforNewlyDiagnosedMultipleMyelomaintheEraofNovelAgentInduction:ASystematicReviewandMeta ̄analysis[J].JAMAOncolꎬ2018ꎬ4(3):343 ̄350.[60]㊀LemieuxEꎬHulinCꎬCaillotDꎬetal.Autologousstemcelltrans ̄plantation:Aneffectivesalvagetherapyinmultiplemyeloma[J].BiolBloodMarrowTransplantꎬ2013ꎬ19(3):445 ̄449. [61]㊀VeltriLWꎬMiltonDRꎬDelgadoRꎬetal.Outcomeofautologoushematopoieticstemcelltransplantationinrefractorymultiplemyeloma[J].Cancerꎬ2017ꎬ123(18):3568 ̄3575.[62]㊀HtutMꎬDᶄSouzaAꎬKrishnanAꎬetal.Autologous/AllogeneicHematopoieticCellTransplantationversusTandemAutologousTransplantationforMultipleMyeloma:ComparisonofLong ̄TermPostrelapseSurvival[J].BiolBloodMarrowTransplantꎬ2018ꎬ24(3):478 ̄485.[63]㊀FranssenLEꎬRaymakersRAꎬBuijsAꎬetal.Outcomeofallogeneictransplantationinnewlydiagnosedandrelapsed/refractorymultiplemyeloma:Long ̄termfollow ̄upinasingleinstitution[J].EurJHaematolꎬ2016ꎬ97(5):479 ̄488.[64]㊀GiraltSꎬGarderetLꎬDurieBꎬetal.AmericanSocietyofBloodandMarrowTransplantationꎬEuropeanSocietyofBloodandMarrowTransplantationꎬBloodandMarrowTransplantClinicalTrialsNetworkꎬandInternationalMyelomaWorkingGroupConsensusConferenceonSalvageHematopoieticCellTransplantationinPatientswithRelapsedMultipleMyeloma[J].BiolBloodMarrowTransplantꎬ2015ꎬ21(12):2039 ̄2051.收稿日期:2019 ̄06 ̄09㊀修回日期:2019 ̄10 ̄26㊀编辑:郑雪。
中国多发性骨髓瘤诊治指南(2020年修订完整版)

中国多发性骨髓瘤诊治指南(2020年修订完整版)摘要多发性骨髓瘤(MM)是一种克隆浆细胞异常增殖的恶性疾病,在很多国家是血液系统第2位常见恶性肿瘤,多发于老年,目前仍无法治愈。
随着新药不断问世及检测手段的提高,MM的诊断和治疗得以不断改进和完善。
本次指南修订中增加了达雷妥尤单抗联合治疗部分及相关注意事项,在难治复发性MM部分增加了嵌合抗原受体T细胞免疫疗法,强调自体造血干细胞移植对于适合移植患者仍然具有不可替代的地位。
多发性骨髓瘤(multiple myeloma,MM)是一种克隆浆细胞异常增殖的恶性疾病,在很多国家是血液系统第2位常见恶性肿瘤[1,2],多发于老年,目前仍无法治愈。
随着新药不断问世及检测手段的提高,MM的诊断和治疗得以不断改进和完善。
本次指南修订中增加了达雷妥尤单抗联合治疗部分及相关注意事项,在难治复发性MM部分增加了嵌合抗原受体T 细胞(chimeric antigen receptor T cell,CAR-T)免疫疗法,强调自体造血干细胞移植(autologous hematopoietic stem cell transplantation,ASCT)对于适合移植患者仍然具有不可替代的地位。
每2~3年1次的中国MM诊治指南的更新对于提高我国MM的诊治水平具有重要意义。
临床表现MM常见的症状包括骨髓瘤相关器官功能损伤的表现,即"CRAB"症状[血钙增高(calcium elevation),肾功能损害(renal insufficiency),贫血(anemia),骨病(bone disease)]以及继发淀粉样变性等相关表现。
诊断标准、分型、分期一、诊断所需的检测项目(表1[3])对于临床疑似MM的患者,应完成基本检查项目。
在此基础上,有条件者可进行对诊断病情及预后分层具有重要价值的项目检测。
二、诊断标准综合参考美国国家综合癌症网络(National Comprehensive Cancer Network,NCCN)及国际骨髓瘤工作组(International Myeloma Working Group,IMWG)的指南[4],诊断无症状(冒烟型)骨髓瘤和有症状(活动性)骨髓瘤的标准如下。
多发性骨髓瘤化疗方案

多发性骨髓瘤化疗方案第1篇多发性骨髓瘤化疗方案一、方案背景多发性骨髓瘤(Multiple Myeloma,MM)是一种起源于B淋巴细胞的恶性浆细胞病,其特征为骨髓内单一浆细胞株异常增生。
本化疗方案旨在为多发性骨髓瘤患者提供规范化、个体化的治疗,提高患者生存质量,延长生存期。
二、治疗目标1. 缓解病情,降低肿瘤负荷;2. 控制病情进展,延长患者无进展生存期;3. 降低并发症发生率,改善患者生存质量;4. 提高患者整体治疗效果。
三、治疗方案1. 初治患者:(1)诱导治疗:诱导治疗旨在迅速降低肿瘤负荷,为后续治疗创造条件。
方案如下:- 采用VAD(长春新碱+多柔比星+地塞米松)方案,每4周为1个周期,共4-6个周期;- 或采用VRD(硼替佐米+长春新碱+地塞米松)方案,每4周为1个周期,共4-6个周期。
(2)巩固治疗:巩固治疗旨在进一步降低肿瘤负荷,提高治疗效果。
方案如下:- 采用高剂量化疗联合自体造血干细胞移植(HDT-ASCT),或异基因造血干细胞移植(Allo-HSCT);- 或采用免疫调节剂(如来那度胺)联合化疗。
(3)维持治疗:维持治疗旨在延长患者无进展生存期,降低复发风险。
方案如下:- 采用免疫调节剂(如来那度胺)单药治疗;- 或采用低剂量化疗。
2. 复发/难治性患者:针对复发/难治性多发性骨髓瘤患者,可根据患者病情、前期治疗及药物耐受情况,选用以下方案:- 采用新药(如帕博西尼、卡非佐米等)联合化疗;- 或采用二线免疫调节剂(如沙利鲁米、伊沙佐米等)单药或联合化疗;- 或参加临床试验,寻求新的治疗手段。
四、治疗监测与评估1. 诱导治疗期间:- 每2周进行一次血常规、肝肾功能、血清蛋白电泳、免疫固定电泳等检查;- 每4周进行一次骨髓穿刺检查;- 每8周进行一次全身骨骼显像、PET-CT等影像学检查;- 根据病情变化,调整治疗方案。
2. 巩固/维持治疗期间:- 每3个月进行一次血常规、肝肾功能、血清蛋白电泳、免疫固定电泳等检查;- 每6个月进行一次骨髓穿刺检查;- 每12个月进行一次全身骨骼显像、PET-CT等影像学检查;- 根据病情变化,调整治疗方案。
骨髓瘤的治疗方案

骨髓瘤的治疗方案第1篇骨髓瘤的治疗方案一、背景骨髓瘤(Multiple Myeloma,MM)是一种起源于骨髓浆细胞的恶性肿瘤,其特征为恶性浆细胞在骨髓中克隆性增生,导致骨骼破坏、贫血、肾功能损害等症状。
随着我国人口老龄化,骨髓瘤的发病率逐年上升。
本方案旨在为骨髓瘤患者提供一套合法合规的治疗方案,以提高患者生存质量,延长生存期。
二、治疗原则1. 个体化治疗:根据患者的年龄、病情、体能状态、并发症等因素,制定个性化的治疗方案。
2. 综合治疗:采用多种治疗手段,包括药物治疗、放疗、手术治疗、支持治疗等,以达到最佳治疗效果。
3. 随访评估:治疗过程中密切监测病情变化,及时调整治疗方案。
4. 合法合规:确保治疗方案符合国家相关法规和诊疗指南。
三、治疗方案1. 初期治疗(1)药物治疗:采用基于硼替佐米、来那度胺、沙利度胺等药物的多药联合化疗方案。
根据患者病情和体能状态,选择合适的药物组合和剂量。
(2)放疗:针对局部骨骼破坏、疼痛等症状,可采用姑息性放疗。
(3)支持治疗:包括纠正贫血、改善肾功能、预防感染等。
2. 持续治疗(1)药物治疗:根据病情变化,调整药物组合和剂量,可采用口服药物、皮下注射等方式。
(2)定期随访:每3个月进行一次全面评估,包括血常规、尿常规、肾功能、影像学检查等。
(3)维持治疗:病情稳定后,可采用低剂量药物治疗,以维持病情稳定。
3. 疾病进展后的治疗(1)更换药物:针对病情进展,更换敏感药物,重新制定化疗方案。
(2)加强支持治疗:针对并发症,加强相应治疗。
(3)评估治疗效果:每3个月进行一次全面评估,根据病情变化调整治疗方案。
四、注意事项1. 治疗过程中,密切监测药物不良反应,及时处理。
2. 加强患者教育,提高患者对疾病的认识和自我管理能力。
3. 遵循国家相关法规,确保治疗方案的合法合规。
4. 定期参加专业培训,提高治疗团队的专业水平。
五、总结骨髓瘤的治疗方案应遵循个体化、综合化、合法合规的原则。
《中国多发性骨髓瘤诊治指南(2020年修订)》解读

《中国多发性骨髓瘤诊治指南(2020年修订)》解读摘要《中国多发性骨髓瘤诊治指南(2020年修订)》关于微小残留病(MRD)疗效标准部分仍参照2016年发表在《柳叶刀》上的国际骨髓瘤工作组(IMWG)多发性骨髓瘤(MM)疗效和MRD评估共识。
大量研究证实MM治疗后的MRD转阴与患者的长期无进展生存(PFS)密切相关,而且越来越多的学者建议在临床试验中将MRD作为PFS的替代终点。
因此,应用二代流式细胞仪、二代测序等方法检测MRD,对于MM患者预后预测、分层治疗等具有重要意义。
由于新药治疗的出现以及各种检测方法自身存在的不足,MRD疗效评估尚存在一些问题,需要血液科医生高度关注。
《中国多发性骨髓瘤诊治指南(2020年修订)》关于微小残留病(minimal residual disease,MRD)疗效标准部分仍参照2016年发表在《柳叶刀》上的国际骨髓瘤工作组(International Myeloma Working Group,IMWG)多发性骨髓瘤(multiple myeloma,MM)疗效和MRD评估共识[1,2]。
大量研究证实MM治疗后的MRD转阴与患者的长期无进展生存(progression-free survival,PFS)密切相关[1,2,3],而且越来越多的学者建议在临床试验中将MRD作为PFS的替代终点。
因此,应用二代流式细胞(new generation flow,NGF)、二代测序(new generation sequencing,NGS)等方法检测MRD对于MM患者预后预测、分层治疗等具有重要意义[4,5,6,7,8,9]。
由于新药治疗的出现以及各种检测方法自身存在的不足,MRD疗效评估尚存在一些问题,需要血液科医生高度关注[4,5,6,7,8,9]。
一、新药治疗对多参数流式细胞仪(multiparameter flow cytometry,MFC)检测MRD的影响MFC检测MRD针对MM表面抗原的骨干抗体,包括CD38、CD138、CD45、CD56以及CD19等。
多发性骨髓瘤的化疗方案

多发性骨髓瘤的化疗方案引言多发性骨髓瘤(Multiple Myeloma,MM)是一种常见的血液恶性肿瘤,主要起源于骨髓中的浆细胞。
该病的发病率在全球范围内呈上升趋势,同时也是造成恶性血液肿瘤死亡的主要原因之一。
化疗是多发性骨髓瘤的主要治疗方法之一,本文将详细介绍多发性骨髓瘤的化疗方案。
化疗方案1. 第一线化疗方案第一线化疗方案是指初次诊断多发性骨髓瘤的患者接受的第一疗程治疗。
常用的第一线化疗方案包括:(1)联合化疗方案:联合化疗是多发性骨髓瘤的常用治疗方法之一,常用药物包括多柔比星、长春新碱、环磷酰胺等。
这些药物可以通过抑制癌细胞的增殖和促使其凋亡来达到治疗的效果。
(2)高剂量化疗方案:高剂量化疗是指给予高剂量化疗药物的治疗方案。
常用的药物包括甲氨蝶呤、长春新碱等。
高剂量化疗可以增加药物对癌细胞的杀伤作用,但同时也会对正常细胞造成一定的损伤。
2. 第二线化疗方案第二线化疗方案是指初次治疗失败或复发的多发性骨髓瘤患者接受的治疗方案。
常用的第二线化疗方案包括:(1)靶向药物治疗:靶向药物是指能够选择性地作用于癌细胞特定分子靶点的药物。
常用的靶向药物有替吉奥尼布(Thalidomide)、依达拉滨(Lenalidomide)等。
这些药物通过抑制癌细胞的增殖和促使其凋亡来起到治疗的效果。
(2)自体干细胞移植:自体干细胞移植是指从患者体内采集干细胞,经过化疗后再将其重新植入患者体内的治疗方法。
该方法可以恢复正常造血功能,并提高患者对化疗的敏感性。
(3)免疫治疗:免疫治疗是指利用免疫系统抗击肿瘤的治疗方法。
常用的免疫治疗方法包括免疫细胞疗法、肿瘤疫苗等。
这些治疗方法可以增强患者的免疫力,提高对肿瘤的抵抗能力。
3. 维持治疗方案维持治疗是指在第一线治疗和移植后继续进行的治疗方案,旨在延缓疾病的进展和提高患者的生存率。
常用的维持治疗药物包括替吉奥尼布、依达拉滨等靶向药物,以及地塞米松等激素类药物。
此外,也可以采用定期化疗的方式进行维持治疗。
多发性骨髓瘤疗效评价标准
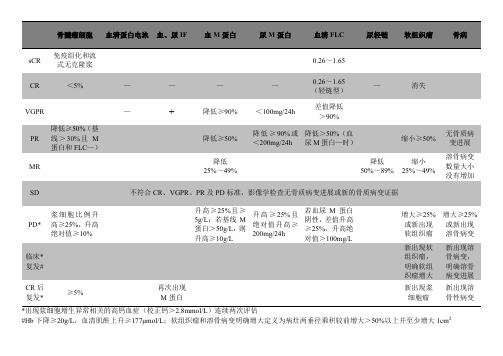
sCR 免疫组化和流式无克隆浆0.26~1.65CR<5%————0.26~1.65(轻链型)—消失VGPR—+降低≥90%<100mg/24h差值降低>90%PR 降低≥50%(基线>30%且M蛋白和FLC—)降低≥50%降低≥90%或<200mg/24h降低>50%(血尿M蛋白—时)缩小≥50%无骨质病变进展MR降低25%~49%降低50%~89%缩小25%~49%溶骨病变数量大小没有增加SD不符合CR、VGPR、PR及PD标准,影像学检查无骨质病变进展或新的骨质病变证据PD*浆细胞比例升高≥25%,升高绝对值≥10%升高≥25%且≥5g/L;若基线M蛋白>50g/L,则升高≥10g/L升高≥25%且绝对值升高≥200mg/24h若血尿M蛋白阴性,差值升高≥25%,升高绝对值>100mg/L增大≥25%或新出现软组织瘤增大≥25%或新出现溶骨病变临床*复发#新出现软组织瘤,明确软组织瘤增大新出现溶骨病变,明确溶骨病变进展CR后复发*≥5%再次出现M蛋白新出现浆细胞瘤新出现溶骨性病变*出现浆细胞增生异常相关的高钙血症(校正钙>2.8mmol/L)连续两次评估#Hb下降≥20g/L,血清肌酐上升≥177μmol/L;软组织瘤和溶骨病变明确增大定义为病灶两垂径乘积较前增大>50%以上并至少增大1cm2。
多发性骨髓瘤化疗方案

多发性骨髓瘤化疗方案多发性骨髓瘤化疗方案引言多发性骨髓瘤(Multiple Myeloma,MM)是一种恶性浆细胞克隆增生性疾病,它通常表现为骨髓浆细胞的异常增生并导致骨骼破坏。
化疗是多发性骨髓瘤的常规治疗方法之一,其目的是减轻疾病症状、延缓疾病进展并提高患者的生存率。
本文将对多发性骨髓瘤的化疗方案进行介绍。
1. 初诊患者的化疗方案对于初诊的多发性骨髓瘤患者,常规的化疗方案通常包括以下几个阶段:阶段一:诱导治疗诱导治疗的目的是迅速减少肿瘤负荷、控制病情并提高患者的存活率。
常用的诱导治疗方案包括:- 环磷酰胺(Cyclophosphamide)+ 哌嗪(Bortezomib)+地塞米松(Dexamethasone)- 环磷酰胺+莫西沙星(Lenalidomide)+地塞米松- VAD方案(长春新碱(Vincristine)、哌嗪和地塞米松)阶段二:移植前维持治疗移植前维持治疗的目的是控制病情、减少肿瘤负荷,并为后续的造血干细胞移植做准备。
常用的移植前维持治疗方案包括:- 莫西沙星+地塞米松- 瓦莫方案(哌嗪、莫西沙星和地塞米松)阶段三:造血干细胞移植造血干细胞移植是多发性骨髓瘤的重要治疗手段之一。
移植前常采用化疗方案进行预处理,常用的预处理方案包括:- 高剂量长春新碱(Vincristine)、哌嗪和地塞米松- 高剂量环磷酰胺2. 复发/难治性患者的化疗方案对于多发性骨髓瘤的复发/难治性患者,常规的化疗方案如下:阶段一:复发治疗复发治疗的目的是控制病情、减少肿瘤负荷,并延迟病情进展。
常用的复发治疗方案包括:- GVd方案(长春新碱、哌嗪和地塞米松)- 哌嗪+地塞米松+他法兰(Thalidomide)- BCD方案(S-101、长春新碱和高剂量他法兰)阶段二:维持治疗维持治疗的目的是维持疾病的控制稳定,并提高患者的生存率。
常用的维持治疗方案包括:- 莫西沙星+地塞米松- 他法兰- 莫达非尼(Pomalidomide)+地塞米松3. 化疗的不良反应管理化疗治疗多发性骨髓瘤时,患者可能会出现一些不良反应,包括恶心呕吐、造血抑制、神经毒性等。
中国多发性骨髓瘤诊断和治疗指南(2020年版)

1处或多处溶骨性病变
有症状(活动性)多发性骨髓瘤诊断标准
8
(2)无靶器官损害表现,但出现以下1项或多项指标异常(sLiM) [ S ] 骨髓单克隆浆细胞比例≥60%d [ Li ] 受累/非受累血清游离轻链比≥100e [M ] MRI检查出现>1处5mm以上局灶性骨质破坏
传统的IMWG 疗效标准
21
9.CR 后复发:符合以下之一: (1)免疫固定电泳证实血或尿M 蛋白再次出现; (2)骨髓浆细胞比例≥5%; (3)出现以上PD 的标准之一。
15
意义未明的单克隆丙种球蛋白病(MGUS) 华氏巨球蛋白血症
AL 型淀粉样变性 孤立性浆细胞瘤(骨或骨外)
POMES 综合征 反应性浆细胞增多症
转移性癌的溶骨性病变
浆母细胞性淋巴瘤
单克隆免疫球蛋白相关肾损 害(MGRS):MGRS是由于单克隆免疫球蛋 白或其片段导致的肾脏损害,其血液学改变更接近MGUS,但出现肾功能 损害,需要肾脏活检证明是M蛋白或其片段通过直接或间接作用所致。
中国多发性骨髓瘤诊断和治疗指南(24020年版)
共识更新
5
二、诊断标准
6
(一)无症状(冒烟型)骨髓瘤诊断标准 (需满足第3 条+ 第1 条/第2 条)
• 1.血清单克隆M 蛋白≥30 g/L,24 h 尿轻链≥0.5 g • 2.骨髓单克隆浆细胞比例10%~59% • 3.无相关器官及组织的损害(无SLiM-CRAB等终末器官损害表现)
多发性骨髓瘤患者首次治疗部分缓解时NLR、MLR_与预后的关系

多发性骨髓瘤患者首次治疗部分缓解时NLR 、MLR 与预后的关系王豪言,孙晓白,李梦一,牛俊伟,白炎亮,孙恺郑州大学人民医院 河南省人民医院血液科,郑州450003摘要:目的 探讨多发性骨髓瘤(MM )患者首次治疗部分缓解时中性粒细胞/淋巴细胞比值(NLR )、单核细胞/淋巴细胞比值(MLR )与预后的关系。
方法 经治疗后首次部分缓解的MM 患者106例,随访观察患者生存情况,计算无进展生存期(PFS )和总生存期(OS )。
采用受试者工作特征(ROC )曲线分析首次部分缓解时NLR 和MLR 预测患者预后的效能并获取最佳截断值,将患者分为高NLR 组、低NLR 组和高MLR 组、低MLR 组,分别比较高NLR 组与低NLR 组、高MLR 组与低MLR 组患者的PFS 和OS 。
收集首次部分缓解时患者的年龄、性别、血红蛋白、白/球蛋白比值、乳酸脱氢酶、β2-微球蛋白、血清钙、胱抑素C 、轻链类型、NLR 、MLR 资料,纳入Cox 回归分析模型,分析MM 患者PFS 、OS 的影响因素。
结果 106例患者随访至2022年10月,死亡27例,总生存率为74.5%。
患者中,高NLR 组(NLR>2.14) 49例、低NLR 组(NLR≤2.14) 57例和高MLR 组(MLR>0.36) 46例、低MLR 组(MLR≤0.36) 60例。
低NLR 组尿酸<283.5 μmol /L 者比例高于高NLR 组,低MLR 组Hb≥96 g /L 者比例高于高MLR 组(P 均<0.05)。
高NLR 组中位PFS 和中位OS 低于低NLR 组,高MLR 组中位OS 低于低MLR 组(P 均<0.05)。
首次部分缓解时NLR 是MM 患者PFS 的独立影响因素,白球比和NLR 是OS 的独立影响因素(P 均<0.05)。
结论 MM 患者首次治疗部分缓解时的NLR 、MLR 与预后有关,其中NLR 是预后的独立影响因素,NLR 升高提示预后不良,NLR 可作为MM 诱导治疗中间阶段评估预后的指标。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2020多发性骨髓瘤首次复发评估与治疗(完整版)
我们之前梳理了首次复发多发性骨髓瘤的治疗原则与方案选择,尤其对二代口服蛋白酶体抑制剂伊沙佐米的方案做了推荐和阐述(详见盘点国内外指南,看首次复发MM如何应对!)。
本文则简述首次复发多发性骨髓瘤患者治疗前的全局评估。
过去的数十年,随着新药如蛋白酶体抑制剂(PIs)、免疫调节剂(IMiDs)和单克隆抗体(MoAbs)等的引入,多发性骨髓瘤(MM)患者的5年总生存有了较大改善。
尽管如此,MM仍然无法治愈,大多数患者最终都会复发而需进一步治疗。
问题是,由于新药可及性的提高,复发MM患者的管理发生了显著变化,治疗方案增多的同时,治疗选择的复杂性、作出不适当的治疗决策的风险也随之增加。
尤其对于MM首次复发患者,在此重要关口,如何调整治疗是极为关键的,而在诊疗决策前的疾病评估,则是确立新方案的重中之重!
在此背景下,意大利专家小组提出了《MM首次复发合理评估的专家共识》[1]。
多发性骨髓瘤首次复发时,
评估要关注以下五点
这项共识提出,当MM患者出现首次复发时,为了后续制定适当的治疗策略,应关注和评估以下几项:患者特征、病史、既往治疗毒性、复发类型、患者偏好及其他因素。
1评估病史:该共识推荐三联方案
病史评估包括细胞遗传学特征,既往治疗是什么,既往治疗反应情况,缓解持续时间,前线治疗毒性等。
国际骨髓瘤工作组(IMWG)的指南认为,对于既往标准治疗后缓解持续时间达24个月,或自体造血干细胞移植(ASCT)且无维持治疗患者的缓解持续时间达18-24个月,再或ASCT序贯维持治疗的缓解持续时间达36-48个月的首次复发患者,可采用之前的治疗方案或在这个方案中添加其他药物进行治疗。
该共识认为,鉴于三联疗法的治疗优势,同方案再治疗并不是最佳选择。
例如如果一线接受基于硼替佐米方案治疗的患者,复发时可接受基于来那度胺的三联方案,如可以用含口服蛋白酶体抑制剂伊沙佐米的IRd全口服方案(伊莎佐米-来那度胺-地塞米松)等。
2评估既往治疗毒性:应对周围神经病变
在诱导治疗期间发生的不良反应中,对复发后选择治疗方案有明显影响的是硼替佐米诱发的周围神经病变(PN)。
对于PN患者,不建议使用基于硼替佐米的方案,可谨慎使用其他PIs。
目前中国上市的PIs 有两款,硼替佐米和伊沙佐米,意味着对此类患者可换用伊莎佐米。
3确定临床复发类型:侵袭性还是非侵袭性
复发分类有助于临床医生选择适当的治疗方案,以减少治疗复杂性。
根据IMWG标准,MM复发分为生化复发和临床复发。
在此基础上,该共识认为,临床复发可分为侵袭性和非侵袭性复发。
区分标准为:如果MM复发满足以下条件中至少一项,应视为侵袭性复发;反之,若不符合以下任何一项,
则视为非侵袭性复发(图1):
存在肾功能损害或高钙血症:肾功能损害定义为肌酐清除率<40 mL/min或血清肌酐>177 mmol/L(>2 mg/dL);高钙血症定义为血清钙水平>2.75 mmol/L(11 mg/dL)或相比正常上限增加>0.25 mmol/L(1 mg/dL)。
存在髓外浆细胞瘤(EMP):
包括新发软组织浆细胞瘤、已有浆细胞瘤明显增大(≥50%),其可通过CT、MRI、PET扫描等检出。
乳酸脱氢酶(LDH)>正常水平:
LDH水平高于正常上限提示疾病侵袭性增加、细胞增殖率高和/或肿瘤存在[2]。
骨相关并发症:骨病通常伴有剧烈疼痛或相关并发症(如骨折),需手术和/或放疗进行治疗。
骨骼X线、MRI或PET-CT检查示至少1处≥5 mm局灶性骨病变是提示骨髓瘤需要治疗的指标之一。
外周血浆细胞存在:
在不符合浆细胞白血病诊断标准(绝对浆细胞计数≥2×109/L、负荷>白细胞总数的20%)的患者中,循环浆细胞存在被视为侵袭性、快速进展疾病的标准。
M蛋白水平快速升高(在2个月内翻倍):
达到血清M蛋白≥1 g/dl、尿M蛋白≥0.5 g/24h。
浆细胞增殖指数高:浆细胞增殖指数是反映浆细胞增殖速率的一个指标,高指数提示侵袭性疾病。
注:PB:外周血;ULN:正常上限
图1 侵袭性与非侵袭性复发评估的决策树
对于首次复发MM患者,也应先确认是生化复发还是临床复发,其中临床复发患者要区分是侵袭性还是非侵袭性复发。
针对不同类型复发患者的治疗思路,在IMWG推荐基础上,该共识给出的建议是:
(1)不符合IMWG治疗标准的生化复发,应每2个月或更短时间内随访1次;
(2)符合IMWG治疗标准的生化复发,应按非侵袭性临床复发治疗;(3)对于临床复发,应在前线治疗方案基础上辨别侵袭性或非侵袭性,然后调整治疗方案(图2)。
注:Dara:daratumumab;Elo:elotuzumab;IMiD:免疫调节剂;I:伊沙佐米;K:卡非佐米;d:地塞米松;R:来那度胺;V:硼替佐米。
图2 复发MM管理的决策树
《中国多发性骨髓瘤诊治指南(2020年修订)》关于生化复发的治疗原则与前述略有不同。
其中指出,对于无症状的生化复发患者,受累球蛋白上升速度缓慢,仅需观察,不需要立即开始治疗,建议3个月随访1次;若患者出现单克隆球蛋白增速加快,如3个月内增加1倍时,应开始治疗[3]。
4患者特征:推荐进行虚弱评分
患者特征评估包括年龄、体能状态评分、合并症、虚弱评分等。
年龄、体能状态评分和合并症是影响治疗相关毒性和治疗结果的已知因素。
IMWG虚弱评分被认为是预测毒性、治疗停止和结果的最佳工具,既往这个评分工具是用于新诊断MM患者的,该共识认为IMWG 的虚弱评分对于首次复发MM患者同样适用(IMWG虚弱评分介绍见文末)。
5需顾及生活质量/患者选择空间/看护者情况/旅行的可能性
MM首次复发后的治疗应考虑到患者的生活质量、患者的选择空间、看护者情况以及是否有外出或旅行。
对于所有MM复发患者,均强烈建议找到治疗策略与生活质量之间的平衡,防止因治疗不连贯或不规范造成的病情进展。
全面良好的评估决定了治疗策略的正确性
总体来说,为首次复发MM制定治疗策略时,考虑和评估患者疾病特征、个人状况以及初始治疗情况非常重要。
在可选药物增多的情况下,对于一线治疗获得持久、高质量缓解的患者,首次复发时使用相同方案再治疗是可行的,不过换用其他类别的药物或许是更好的办法。
区分临床复发是侵袭性还是非侵袭性,并做出相应的治疗选择,也是该共识的亮点。
另外,在目前中国MM药物的可及范围内,全口服的IRd方案是首次复发MM的重要治疗选择之一。
附:IMWG虚弱评分
虚弱评分系统基于年龄、合并症、认知和身体状况而开发(表1),旨在评估患者的虚弱情况并提供更为合适的治疗策略。
根据虚弱评分(范围:0-5分)可将患者分为3组:
状态良好(分值为0)
状态中等(分值为1)
虚弱(分值≥2)(表2)[4]。
表1 虚弱评分所涉及变量的评分情况
表2 虚弱评分分组。
