碳负离子的反应
13 碳负离子的反应

(
)
O
O
(1) C2H5ONa (2) H
1. OH
H5C2OC(CH2)4COC2H5
(
)
2. H
+
(
)
CH3COCH2COOC2H5
1)NaH 2)C6H5COCl
1)OH
(
)
2)H /
+
(
)
O
O
(1) NaH (2) H
CH3CCH3 + CH3(CH2)3CH2COC2H5
(
)
CH2CH2COOC2H5 H3C CH CH2CH2COOC2H5
取代甲基酮( 取代甲基酮 应用广泛)
取代乙酸
O H CH3 C C CH3 CH2CH2CH3
CH3 O H O (1) C2 H5ONa 2 C C C OC2H5 (2) CH3CH2CH2 Br (1) C2H5 ONa (2) CH3I (1) OH-/H2O (2) H3O+ TM
取代环烷基甲基酮
O
O
CH3CCH2COC2H5
OH
-
OOH
O
O CH3COOH + -CH2COC2H5
CH3C-CH2COC2H5
O CH3COO- + CH3COC2H5
OH-
H+
2 CH3COOH + C2H5OH
• 在合成上的应用
O CH3CCH2COOC2H5 C2H5ONa O CH3CH2CH2Br CH3CCHCOOC2H5
CH2(CO2C2H5)2
(1) C2H5ONa (2) CH3CH2 CH2Br
(1) C2H5ONa (2) CH3I
第十二章 碳负离子的反应

2014/5/31第十二章 碳负离子的反应一、克莱森酯缩合反应 1.举例2. 克莱森酯缩合反应特点 (1)α‐C上有两个H,反应易进行. (2) 用强碱催化,如醇钠、叔丁醇钠或NaH.乙酰乙酸乙酯 简称“三乙”(3) 反应产物:一分子酯羰基C与另一分子酯的α‐C 相连, 失去一分子醇. 产物:β‐ 羰基酸酯;C=O 与酯基处1,3 位. (4) 延长碳链的反应.克莱森酯缩合反应五步骤: 3.克莱森酯缩合反应机理 1. 一分子酯形成C‐ 2. C‐对另一分子酯的羰基亲核 加成形成O‐ 3. O‐ 消除RO‐ β‐羰基酸酯 4. 中和反应成盐 5. 盐酸化成酯缩合反应的动力:中和反应酯缩合反应不能用NaOH催化的原因1. 在NaOH作用下,酯易水解. 2. 中和反应不发生,反应无动力.4. 交叉酯缩合 一个酯有α‐H,另一个酯没有α‐H用极强的碱,可使带一个α‐H的酯反应实验中控制,使有α‐H的反应物浓度始终最小 (向反应体系中滴加)12014/5/31举例α‐C上引入酯基 草酸二乙酯无α‐H的酯有α‐H的酯醛酮可与酯进行缩合,醛酮的α‐H酸性较强, 可在碱性条件下形成C‐.如果是二元酸酯,可形成五员或六员环, 属分子内酯缩合。
例1.设计路线:1,3‐双官能 团化合物 分子内酯缩合,又称Dieckmann缩合,形成 五元或六元环状化合物。
主要适用制备: 1,6‐二羧酸酯,1,7‐二羧酸酯。
例2.另加上一个‐OC2H5 例3.例4. 思路 步骤: 思路: 步骤:例5.22014/5/31二、乙酰乙酸乙酯 1、制备 (1)实验室制备:克莱森酯缩合反应 (2)工业制备2、性质 1、与HCN,NaHSO3,NH2OH,PhNHNH2 反应,证明有CH3C=O 三乙 2、与反应显蓝紫色,证明有C=C‐OH 3、在Br2/CCl4中褪色,证明有C=C(1)酮式‐烯醇式互变异构三乙烯醇式含量多于丙酮的原因: 1、双键与形成共轭体系 2、OH与C=O形成六元环的氢键,使三乙烯 醇式结构增加 如体系中共轭体系延长,则烯醇结构增大。
《碳负离子的反应》课件

防护措施
禁止事项
应急处理
废弃物处理
实验时需佩戴实验服、 护目镜等防护装备。
禁止在实验过程中饮食 、吸烟等行为。
熟悉实验中可能发生的 意外情况及处理方法。
按规定正确处理实验废 弃物。
实验废弃物的处理
分类处理
根据废弃物的性质进行分类, 如有机废弃物、无机废弃物等
。
回收利用
部分废弃物可进行回收利用, 以节约资源。
副产物的生成。
06
碳负离子反应的实验操作 与安全注意事项
实验操作规程
01
02
03
04
实验前的准备
确保实验室环境整洁,检查实 验器材是否齐全、完好。
试剂取用
按照需求适量取用,避免浪费 或不足。
操作步骤
按照规定的顺序进行实验操作 ,不可省略或颠倒。
数据记录
实时记录实验数据,确保准确 无误。
安全注意事项
安全处置
对于无法回收利用的废弃物, 需按照规定进行安全处置。
记录存档
对废弃物的处理过程进行记录 ,并存档备查。
THANKS
感谢观看
自由基反应
总结词
自由基反应是碳负离子与自由基的反 应,通常发生在碳负离子的未共用电 子对被自由基的空轨道接收的过程中 。
详细描述
在自由基反应中,碳负离子与自由基 相互作用,形成新的碳-碳键或碳-自 由基键。这种反应通常在高温或光照 条件下进行,有利于自由基的形成和 反应。
光化学反应
总结词
光化学反应是碳负离子在光的作用下发 生的化学反应,通常需要特定波长的光 照射。
β-羟基酸酯的合成
总结词
β-羟基酸酯是有机合成中的一种特殊结构, 碳负离子可以用于合成β-羟基酸酯。
碳负离子-缩合反应

研究背景和意义
随着生物医药和材料科学的发展,对具有特定结构和功能的有机化合物的需求不断 增加。
碳负离子-缩合反应作为合成这些化合物的重要手段,其研究具有重要的实际意义和 应用价值。
目前,尽管已有许多关于碳负离子-缩合反应的研究,但仍存在许多挑战和未解决的 问题,需要进一步探讨和深入研究。
02 碳负离子
碳负离子作为反应物
碳负离子是一种重要的有机反应 中间体,在缩合反应中常被用作
反应物。
碳负离子可以与多种亲电试剂如 醇、硫醇、酚等发生缩合反应, 生成相应的醚、硫醚、酚醚等化
合物。
碳负离子作为反应物的优点在于 其反应活性高,选择性好,可以
有效地避免副反应的发生。
碳负离子在有机合成中的应用
碳负离子在有机合成中有着广泛的应 用,可以用于合成多种有机化合物。
对未来研究的建议
加强机理研究的深度和广度,深入了解反应过 程中的电子转移和键合变化等微观机制。
将碳负离子-缩合反应与其他有机合成方法相结合, 探索其在复杂分子合成和天然产物全合成等领域的应
用潜力。
进一步探索碳负离子-缩合反应在不同底物和反 应条件下的应用范围,以拓展其在有机合成领 域的应用。
结合计算化学和实验手段,研究反应过程中的动 态行为和过渡态结构,为优化反应条件和提高反 应效率提供理论指导。
碳负离子的定义
碳负离子是一种具有负电荷的碳原子,通常与一个或多个正 电荷共享。
碳负离子是许多有机化学反应的重要中间体,尤其在缩合反 应中。
碳负离子的性质
碳负离子具有很强的反应活性,容易与其它分子或离子发 生反应。
由于碳负离子具有不稳定性,通常需要在特定的条件下保 存和操作。
碳负离子的形成
碳负离子可以通过多种方式形成,如 取代反应、氧化反应、还原反应等。
碳负离子的反应

官能团转化反应
卤代烃的水解反应
卤代烃在碱性条件下生成碳负离 子,与水发生亲核取代反应生成 醇。
酯的水解反应
酯在碱性条件下生成碳负离子, 与水发生亲核取代反应生成羧酸 和醇。
立体选择性反应
烯烃的顺反异构化反应
在光照或加热条件下,烯烃与卤素发生 加成反应生成卤代烷,卤代烷在碱性条 件下生成碳负离子,再与另一分子烯烃 发生亲核加成反应,生成具有立体选择 性的顺反异构体。
碳负离子的反应
汇报人:XX
• 碳负离子概述 • 碳负离子的反应类型 • 碳负离子在有机合成中的应用 • 碳负离子的反应机理与动力学 • 碳负离子的实验方法与检测技术 • 碳负离子的应用前景与挑战
01
碳负离子概述
定义与性质
定义
碳负离子是指带有负电荷的碳原子, 通常表示为$C^-$。它是许多有机化 学反应中的重要中间体。
自由基反应
自由基引发
在某些条件下,如高温或过氧化物存在下,碳负离子可以引发自由基链式反应。通过均裂产生自由基,进而引发 后续的自由基传递和终止步骤。
自由基加成
碳负离子可以作为自由基受体,与自由基发生加成反应。例如,在烯烃的自由基加成反应中,碳负离子与烯烃中 的双键发生加成,生成新的自由基中间体。
电化学反应
性质
碳负离子具有亲核性,可以与亲电试 剂发生反应。它的稳定性取决于其所 处的化学环境,如溶剂、温度、pH值 等。
结构与稳定性
结构
碳负离子的结构通常是一个或多个碳 原子通过共价键与其他原子或基团相 连,并带有一个负电荷。这个负电荷 可以通过共振结构进行分散,从而提 高其稳定性。
稳定性
碳负离子的稳定性与其结构密切相关 。一般来说,具有较大共轭体系或能 够通过共振稳定化的碳负离子更稳定 。例如,苯基负离子比甲基负离子更 稳定。
碳负离子的反应

含有α氢原子的酮与酯之间也可以进行缩合 反应主要产物为β-二酮。
例如:
第二节 β-二羰基化合物的烷基化、酰基 化及其在合成中的应用
两个羰基被一个碳原子隔开的化合物称 为β-二羰基化合物。
β-二羰基化合物一般泛指β-二酮、β-酮 酸酯、丙二酸酯等含活泼亚甲基化合物 。
这类化合物主要的反应类型是亚甲基碳 上的烷基化、酰基化反应。
一、乙酰乙酸乙酯
无色,具有水果香味,沸点118℃, 微溶于水,易溶于多种有机溶剂。
反应可在不同的酯之间进行,称为交叉 酯缩合。
Claisen 缩合举例
混合酯缩合
反应机理
狄克曼(Dieckmann)缩合(也叫酯分子内 缩合)
含6个或7个碳的二元酸酯,在碱性催化 剂作用下环化生成五元或六元环为主的 -酮酯称为狄克曼反应。
分子内羟醛缩合
羟醛缩合反应不仅可以在分子间进行,含有α-氢原子的 二元醛或酮也可以进行分子内缩合,生成环状化合物, 是制备5~7元环化合物的常用方法之一。
ห้องสมุดไป่ตู้
β-羟基醛在加热时即失去一分子水,生成 α,β-不饱和醛
常用的碱性催化剂除了氢氧化钠、氢氧化钾外,还有叔 丁醇铝、醇钠等。 由此可见,通过羟醛缩合反应可以制备α,β-不饱和醛,进 一步还可以转变为其它化合物。所以羟醛缩合反应是有 机合成中用于增长碳链的重要方法之一。
含有α-氢原子的酮在稀碱作用下也 可以发生类似反应,即羟酮缩合反应, 但是反应的平衡偏向反应物一侧,例如 ,丙酮在氢氧化钡催化下,发生反应。
碳负离子的结构与碳正离子或碳自由基 不同,因为带负电荷的碳原子最外层有3对 成键电子和1对未成键电子,这样的4对电子 需要采取相互远离的方式排列,因此碳负离 子采用sp3杂化轨道成键,未成键电子对与3 个共价键形成一个四面体结构。碳正离子、 碳自由基和碳负离子的结构对比如下图所示 。
碳负离子的反应

(二)克脑文格尔反应
定义:在弱碱性催化剂作用下,醛或酮与具 有活泼亚甲基的化合物的缩合反应,称为克 脑文格尔反应. 常用的碱性催化剂有吡啶、哌啶、胺等。 反应通式:
R R
/
C O + CH2
Y Y/
R R/ C C
Y Y/
Y或 Y/ = COR COOR COOH CN
NO 2 等
反应机理
Y H2C Y
CH2 — C
CH2—CH2
C2H5ONa -C2H5OH
-
CH2 — C CH2 CH2 CH2—CH2
=
CH2 CH2 — C CH-COOC2H5 CH2 CH2—CH2 O
Oຫໍສະໝຸດ ==反 应 特 征
反应物:具有H,并能够形成五、六元环的二元羧酸酯。 催化剂:C2H5ONa 产 物:环状-酮酸酯 过 程:-C2H5OH
抗变态反应药物曲尼司特中间体3-(3,4-二甲氧 苯基丙烯酸的合成.
CHO 丙二酸
CH = CHCOOH
CH = CHCONH COOH
OCH3 吡啶/哌啶 OCH3
OCH3 OCH3 91%
OCH3 OCH3 曲尼司特
3-(3,4-二甲氧苯基)丙烯酸
酮一般不与丙二酸与丙二酸酯作用,但可与活性 更强的氰乙酸酯反应,缩合产物经水解、脱羧也可制 得不饱和酸。
(三)达琴反应
定义:在強碱(醇钠、氨基钠)作用下,醛、酮与α-卤代 酸酯反应,生成α,β-环氧酸酯的反应称为达琴反应。 通式:
R R/(H) C=O +
ClCH2COOC2H5
C2H5O Na
R
R/(H)
O C - CHCOOC2H5
碳负离子反应

穿戴防护装备:实验过程中必须穿戴防护 服、手套、护目镜等防护装备。
实验环境:实验应在通风良好的实验室中 进行避免在密闭空间内进行。
实验材料:实验材料应妥善保管避免接触 皮肤和眼睛。
实验操作:实验过程中应严格按照实验 步骤进行操作避免操作不当导致危险。
实验废弃物:实验结束后应妥善处理实验 废弃物避免环境污染。
碳负离子反应是合 成有机化合物的重 要方法之一广泛应 用于药物合成、材 料科学等领域。
碳负离子反应的机 理包括亲核加成、 亲核取代、亲核消 除等。
碳负离子反应的分类
碳负离子反应可以分为两类:亲核碳负离子反应和亲电碳负离子反应 亲核碳负离子反应是指碳负离子作为亲核试剂与亲电试剂发生反应 亲电碳负离子反应是指碳负离子作为亲电试剂与亲核试剂发生反应 碳负离子反应在合成化学中具有广泛的应用如合成有机化合物、药物合成等
碳负离子反应的特点
碳负离子是一种重要的有机合成中间体 碳负离子反应具有高度选择性和立体选择性 碳负离子反应可以生成多种类型的有机化合物 碳负离子反应在合成化学中具有广泛的应用
碳负离子反应的原理
碳负离子反应的化学键特征
碳负离子反应是一种化学反应其中 碳原子失去电子形成负离子。
碳负离子反应的化学键特征还与反 应条件、反应物浓度等因素有关。
碳负离子反应的研究趋势和展望
研究热点:碳负离子反应在材料科学、化学合成等领域的应用 研究方法:理论计算、实验验证相结合的研究方法 研究挑战:如何提高碳负离子反应的效率和选择性 研究展望:未来可能会在能源、环保等领域取得突破性进展
碳负离子反应的研究方法和手段
实验方法:通过实验观察碳负离子反应的过程和结果 理论研究:通过理论推导和计算来研究碳负离子反应的机理和规律 模拟计算:通过计算机模拟来研究碳负离子反应的条件和影响因素 合作研究:与其他研究机构或企业合作共同推进碳负离子反应的研究
一、碳负离子的产生二、碳负离子的烃基化反应三、碳负离子的酰基化
第三章 碳负离子反应
三、碳负离子的 酰基化反应
1 基本反应
1 基本反应 12
为使酯缩合反应顺利进行,可在反应过程中,不断将 生成的醇去除,使平衡移动。 合成位阻大的-酮酸酯,须用强碱。
2 反应实例
酯分子之间的缩合 分子内酯缩合 酯的混和缩合 酮与酯的缩合 碳负离子与草酸酯 碳负与甲酸酯碳酸酯 烯醇镁盐及其反应
1
Department of Material and Engineering, Soochow University
第三章 2 碳负离子的结构 12
碳负离子反应 碳负离子在有机合成中的应用
一、碳负离子的产生
1 碳负离子的生成
2 碳负离子的结构 3 动力学控制和
热力学控制
Department of Material and Engineering, Soochow University
3 双负离子的生成
第三章 碳负离子反应
二、碳负离子的 烃基化反应
1 基本反应实例
3 双负离子的生成
Department of Material and Engineering, Soochow University
12
-酮醛、-酮酸酯等-二羰基化合物亦可发生类似反应。
2 烃基化试剂
3 双负离子的生成
当两种不同的酯发生交叉Claisen缩合时,必须有一种 不含-H,否则会有四种可能产物,合成意义不大。
常用的不含-H的酯有草酸二乙酯、甲酸酯、碳酸二乙 酯、苯甲酸酯。这些酯在酰化反应中可分别引入- COCOOEt,-CHO,-COOEt,-COPh基团。
第三章 2 反应实例 碳负离子反应
1 碳负离子的生成
2 碳负离子的结构 3 动力学控制和
有机化学碳负离子的反应
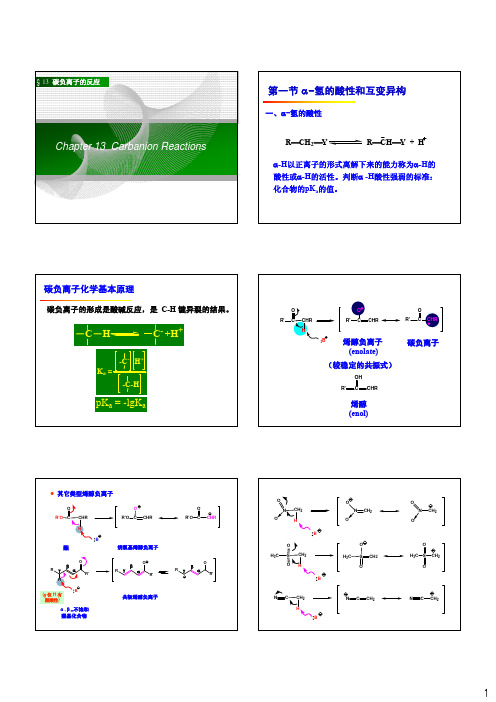
O R'O C
CHR
H
B
酯
O R'O C CHR
烷氧基烯醇负离子
O
β
Rγ
α
R'
H
B (γ 位 H 有
弱酸性)
α,β-不饱和 羰基化合物
β
O
Rγ
α
R'
共轭烯醇负离子
O R'O C CHR
O β
Rγ
α
R'
O
N CH2
O
H
B
O H3C S CH2
OH
B
N C CH2 H B
O N CH2
O
O
H3C
S CH2 O
¾芳醛中羰基化合物的反应活性受电子效应和空间结 构位置的影响,空间位阻较大时它将起主要的作用。
¾当苯环上为烷基时,由于烷基是给电子的基团,又 有位阻使反应物羰基活性下降,反应难以进行,产率 也低。
¾邻位甲基的位阻十分明显,导致不发生反应。
¾当苯环上有吸电子基团时有利于反应进行,不仅反 应的速度加快,并且产率也大大增加。
新型强碱
z 1. LDA 二异丙基胺锂 z 2. LHMDS六甲基二硅胺锂 z 3. LATMP四甲基哌啶锂
特点: z 1. 碱性强pKa大于33 z 2. 能溶解于非极性溶剂 z 3. 位阻大亲核性差
二、互变异构
O R' C CHR
H
O R' C CHR
B 烯醇负离子 (enolate)
(较稳定的共振式)
COOH
−CH=O + H2C
COOH
NH3,C2H5OH -H2O
COOH −CH=CHC
碳负离子的经典反应.

DESIGN BY2014.12
经典反应
碳负离子 碳原子的性质 在有机化合物中, 碳原子常采取SP、SP2和SP3三种杂化形式。我们知道与P轨道 相比较S轨道更靠近原子核, 所以S轨道中的电子离核较近,受原子核束缚的较紧, 因此当杂化轨道S 成份增加时, 其吸电子的能力增强, 电负性增大, 接纳负离子中的电子的能力增加, 从而导致负离子 的稳定性增大。
O
O
该反应的净结果是二甲氨甲基取代了α-H ,故又称为氨甲基化反应,产物 为β-氨基酮。
=
=
C C H3 + HC HO + (C H3)2NH
HCl
C C H2 C H2N(C H 3)2 HC l
Mannich反应机理
(i)
R O C H CHR' H R OH C CHR' H R OH C CHR'
O
-
ClCH2CH2COEt
CH3C-CH-COOEt CH2CH2COOC2H5 O
OH H2O
-
H
+
- CO2
O
CH3CCH2CH2CH2COH
O O CH3CCH2CH2CH2CCH3
O EtO O
O
CH3CCH2COEt
-
ClCH2CH2CCH3
O CH3C-CH-COOEt CH2CH2CCH3 O
OH H2O
-
H
+
- CO2
O
O
CH3CCH2CH2CH2CCH3 + CH3COOH
用乙酰乙酸乙酯合成二羰基化合物
O O O CH3CCH2COC2H5 NaOC2H5 O O
《碳负离子的反应》课件

2 碳负离子反应多种多样,具有重要的应用价值
碳负离子可以发生取代、消除和加成等多种反应,广泛应用于有机合成、制药化工和生 物化学领域。
3 进一步研究碳负离子反应的机理和应用前景具有重要意义
对碳负离子反应的深入研究有助于理解有机化学反应的机制,并且为新型反应的发展提 供了契机。
有机合成
碳负离子反应在有机合成中起 着至关重要的作用,可以用于 合成复杂的有机分子结构。
制药化工
许多药物和化工品的制备都离 不开碳负离子反应,它们成为 了现代化工领域的重要工具。
生物化学
碳负离子反应在生物化学研究 中也有广泛应用,有助于揭示 生命活动中的关键反应过程。
总结
1 碳负离子是有机化学中重要的反应中间体
《碳负离子的反应》PPT 课件
欢迎大家来到本课程的《碳负离子的反应》PPT课件。在本课程中,我们将深 入探讨碳负离子的概念,不同类型的反应以及它们的应用。让我们一起开始 这段知识之旅吧!
碳负离子的概念简介
定义
碳负离子是带有负电荷的碳 离子,作为重要的有机化学 反应中间体存在。
特性
碳负离子具有高度活泼性, 容易发生取代、消除和加成 等多种反应。
形成方式
碳负离子可以通过电子捐赠 基团的取代反应或者临近负 电荷基团的裂解而形成。
碳负离取代反应是碳负离子最常见的反应类型,包括单取代和多取代反应。
2
消除反应
碳负离子也可以发生β-消除反应,生成双键或三键化合物。
3
加成反应
加成反应是碳负离子与亲电性试剂形成新键,包括1,2-加成和1,4-加成。
碳负离子反应的实例
单取代反应的例子
碳负离子的反应-文档资料

Y
ArCHO + CH2
N
Ar
Z or
N H
Y、Z 为吸电子集团如:
COOH CH2
COOH
COOEt CH2
COOEt
O
CCH3 CH2
CCH3 O
Y CH C
Z
CN CH2
COOEt
O O
例如:
COOH
CHO + CH2
N
COOH
CH C(COOH)2
CH3O
CHO + CH2(COOH)2 N CH3O
C6H5CH
CHCOOH
+ CH3COOH
通式:
O
肉桂酸
R ArCHO +
R
CH2 CH2
C O
C
O
RCH2COOK or K2CO3
ArCH C COOH R
α,β-不饱和酸
+ RCH2COOH
反应机理:
OO
OO
OO
H2C H
O CH3
H2C
O
CH3
Ph CH O
O CH3Ac
O
O O
乙酰乙酸乙酯是以酮式—烯醇式平衡混合物的形式同时共存。
OO
CH3-C-CH2-C-OC2H5
酮式
能与: NaHSO3 HCN 苯肼等加成
OH O CH3-C=CH-C-OC2H5
烯醇式
又可: Na作用 H2↑ 使Br2/CCl4退色 与FeCl显色3
乙酰乙酸乙酯的制备(-羰基酯类化合物的制 备)---酯缩合反应
碳负离子的反应
-氢与碳负离子的关系
X
RX CH2Y
有机合成课件第4章稳定化碳负离子的缩合反应

REPORTING
• 引言 • 稳定化碳负离子 • 缩合反应 • 稳定化碳负离子的缩合反应 • 实验操作与注意事项 • 课程总结与展望目录源自PART 01引言
REPORTING
课程背景
有机合成是化学领域中的重要分 支,涉及到复杂有机化合物的合
成和制备。
酯化反应
羧酸中的羧基与醇中的羟基发生质子转移,生成酯和水。
烯醇化反应
烯醇中的碳碳双键与另一分子醇中的羟基发生加成反应, 生成β-羟基酮。
PART 04
稳定化碳负离子的缩合反 应
REPORTING
稳定化碳负离子在缩合反应中的应用
碳负离子作为重要的中间体, 在有机合成中广泛应用于缩合 反应。
稳定化碳负离子能够降低碳负 离子的反应活性,使其在缩合 反应中更加可控,提高反应的 选择性和产率。
步骤一
在干燥的烧杯中加入稳定化碳 负离子和适量的溶剂,搅拌均
匀。
步骤二
缓慢滴加催化剂,观察反应变 化。
步骤三
在恒温水浴中加热反应混合物 ,保持温度恒定。
步骤四
反应结束后,冷却至室温,进 行后处理。
实验注意事项与安全
安全警示
避免直接接触化学试剂,穿戴实验服和化学 防护眼镜。
环境保护
废液应妥善处理,避免对环境造成污染。
稳定化碳负离子的形成通常涉及离去基团(如卤素、烷基等)的离去, 这有助于提高碳负离子的稳定性。
PART 05
实验操作与注意事项
REPORTING
实验前的准备
实验材料
稳定化碳负离子、反应溶剂、催 化剂等。
实验设备
搅拌器、恒温水浴、滴定管、称量 纸等。
碳负离子反应

CH3COONH4
CH3C CHCOOH CH3
Dazen 反应
在强碱(醇钠、氨基钠等)作用下,醛、酮 与α-卤代酸酯反应,生成α,β-环氧酸酯
R O C CHCOOC2H5 (H)R'
R C O + ClCH2COOC2H5 (H)R'
C2H5ONa
O C2H5O + H CH COC2H5 Cl
缩合反应机理:
R CH2 CHO + HO-
O R CH2 C H
O
R
CH CHO + H2O
O
+ R
CH CHO
R CH2
C CH CHO H R
H2O
R CH2 C CH CHO H R
R CH 2
OH C CH H R CHO
+ OH-
2 羟醛缩合反应的衍生类型
(1) Peking 反应
(2)Knoevennagel 反应 (3)Dazen 反应
O
OC2H5
O O C OC2H5
交叉酯缩合反应
不同的具α -H 的酯进行酯缩合时,可能有四种 产物,在合成上无意义
CH3COOC2H5 和 CH3CH2COOC2H5
不具有α-氢的酯可以提供羰基,与具有α-氢的酯 进行酯缩合反应时,可得到较纯的产物。这种缩合 称为交叉酯缩合(crossed ester condensation)。
R-X R CH
COOC2H5 COOC2H5
H2 R C COOH
1. H2 2. H3+O,heat
O,OH-
1.EtONa EtOH 2.R’-X
O R CHC R' OH
有机化学中的重排反应合成方法

有机化学中的重排反应合成方法重排反应是有机化学中一类非常重要的反应类型,通过此类反应可以有效地合成复杂的有机化合物。
本文将介绍有机化学中常见的重排反应及其合成方法。
一、醇重排反应醇重排反应是指醇分子在一定条件下发生内部原子或官能团重排,从而生成具有不同结构的醇化合物。
常见的醇重排反应有醇的断裂与迁移重排、氧化重排和氧杂环重排等。
1. 醇的断裂与迁移重排醇的断裂与迁移重排是指醇分子中的C-O键发生断裂与迁移,生成具有不同碳骨架的醇化合物。
常见的醇的断裂与迁移重排反应包括β-消除重排、E1cb机理的重排和Pinacol重排等。
2. 氧化重排氧化重排是指醇分子在氧化剂的作用下发生内部重排,生成具有不同碳骨架的醇化合物。
常见的氧化重排反应有Baeyer-Villiger氧化重排和尤格催化剂氧化重排等。
3. 氧杂环重排氧杂环重排是指含氧杂环化合物在一定条件下发生内部重排,生成具有不同结构的醇化合物。
常见的氧杂环重排反应包括Pummerer重排和Beckmann重排等。
二、烯重排反应烯重排反应是指具有烯丙基结构的有机化合物在一定条件下发生结构重排,生成具有不同结构的化合物。
常见的烯重排反应包括烯醇重排、烯丙基重排和烯烃转位等。
1. 烯醇重排烯醇重排是指烯醇分子在一定条件下发生内部重排,生成具有不同碳骨架的化合物。
常见的烯醇重排反应有脱醇重排和β-取代基迁移等。
2. 烯丙基重排烯丙基重排是指具有烯丙基结构的化合物在一定条件下发生结构重排,生成具有不同碳骨架的化合物。
常见的烯丙基重排反应有烯丙醇重排和烯丙基迁移等。
3. 烯烃转位烯烃转位是指具有烯烃结构的有机化合物在一定条件下发生结构转位,生成具有不同碳骨架的化合物。
常见的烯烃转位反应包括Cope重排和Claisen重排等。
三、碳负离子重排反应碳负离子重排反应是指碳负离子化合物在一定条件下发生内部重排,生成具有不同碳骨架的化合物。
常见的碳负离子重排反应有甲基重排、氢负离子迁移和羰基碳负离子重排等。
α—碳负离子的亲核加成及在有机合成中的应用

α—碳负离子的亲核加成及在有机合成中的应用α—碳负离子是有机化学中非常重要的化学物质,因为它可以通过亲核加成反应参与各种重要的有机合成反应。
接下来将分步骤阐述α—碳负离子的亲核加成及在有机合成中的应用。
一、α—碳负离子的生成α—碳负离子是指由于有机化合物中的氢离子(H+)的存在而产生的负离子,这个离子是指有机化合物中处于α位(与一个碳原子相连的那个碳原子)的碳离子。
α—碳负离子的产生通常是由于酸或碱性条件下的质子化或去质子化反应所引起的。
二、α—碳负离子的亲核加成α—碳负离子是亲核试剂,可以与合适的亲电试剂结合,进行亲核加成反应。
亲核加成是指亲核试剂中的亲核离子攻击亲电试剂中的电子缺陷区域的过程。
在α—碳负离子的加成反应中,通常是通过其攻击相邻碳原子上的亲电性的双键而实现的。
这种反应通常需要酸性催化剂的存在。
例如,α-烷基化反应是α-羧酸反应的一种形式,该反应可以通过α—碳负离子的亲核加成反应完成。
三、α—碳负离子在有机合成中的应用α—碳负离子在有机合成中的应用非常广泛。
通过α—碳负离子的亲核加成反应,可以完成许多有机合成反应,例如米氏反应、爱菲纳—佩特里反应等。
在米氏反应中,α—碳负离子作为亲核试剂参与反应,与成环的分子中的亲电性的碳原子发生亲核加成反应。
这种反应可以用于生成螺环化合物和其他复杂的有机分子结构。
在爱菲纳—佩特里反应中,即酚醛缩合反应,α—碳负离子作为亲核试剂与酚或醛结合,生成醇或烯醇醛。
此反应可以用于构造多个键和环。
总之,α—碳负离子的亲核加成反应在有机合成中发挥着不可或缺的作用。
它为化学家们提供了一种新的方法,可以合成多种许多复杂的天然产物和药物。
随着合成化学的不断发展,更多的有机合成反应将利用α—碳负离子的亲核加成反应,为有机合成提供更多的可能性。
碳负离子反应

NaH
pKa
20 ~ 24
最好仍用 PhCOOEt, HCOOEt 等无 -H 的酯
2013-8-9
碳负离子反应
31
• C-烃化程度: RI > RBr > RCl > ROTs • 原因:软硬酸碱理论 亲核中心中,O- 较 C- 硬
离去基中, I-很软,OTs-较硬
• 根据软-软、硬-硬作用原理,RI 优先与 C-反应,ROTs 优先进攻 O-。
2013-8-9
碳负离子反应
32
C C O N C N C C O
另: H Cl C Cl Cl
R S C O
2013-8-9
碳负离子反应
3
一. 碳氢键的酸度
• 酸度表示:pKa (以该物质在水中的解离度Ka求得-logKa)
2013-8-9
碳负离子反应
4
活性亚甲基化合物及其它一般试剂的酸性
化合物 CH3COOH NCCH2COOC2H5 CH2(COCH3)2 CH3NO2 CH3COCH2COOC2H5 CH2(COOC2H5)2 CH3OH C2H5OH (CH3)3COH pKa 5 9 9 10 11 13 16 18 19 化合物 C6H5COCH3 CH3COCH3 CH3SO2CH3 CH3SO2C2H5 CH3COOEt CH3CN C6H5NH2 (C6H5)3CH CH3SOCH3 pKa 19 20 ~23 ~24 ~24 ~25 ~30 ~40 ~40
O H3C S CH2 Ph3C NH2
CH3 H3C O CH3
其共轭酸 pKa ~ 40 (CH3CH2)2N
2013-8-9
碳负离子反应
9
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
——β-二羰基化合物§ α-H 的酸性和互变异构α-H 的酸性 1、-H 的酸性在有机化学中,与官能团直接相连的碳原子均称为-C ;-C 上的氢原子均称为-H 。
-H 以质子形式解离下来的能力,即为-H 的活性或-H 的酸性。
因此烃也可叫做氢碳酸。
表14-1-1 常见化合物-H 的p K a 值羧酸衍生物中的-H 的活性一般比醛酮为弱,但酰氯中由于氯原子与羰基的共轭程度差且吸电子效应强,反而使其-H 的酸性增强。
酸性大小: 酰氯>醛、酮>酯>酰胺Cl :吸电子诱导>给电子共轭O :给电子共轭>吸电子诱导 2、影响-H 的酸性的因素1)-C 所连接的官能团及其官能团的吸电子能力。
总的吸电子能力越强,-H 的酸性就越大; 2)取决于氢解离后生成的碳负离子(carbanion)结构的稳定性。
负离子上电子的离域范围越大越稳定;3)分子的几何形状、介质的介电常数、溶剂等都有关系。
3、β-二羰基化合物α-H 的活性分析乙酰乙酸乙酯是一个典型的1,3-二羰基化合物,由于受两个羰基的吸电子作用,亚甲基上的H 特别活泼,和碱作用形成稳定的负离子。
负离子特别稳定是因为负离子可以同时和两个羰基发生共轭作用,具有比较广泛的离域范围。
烯醇负离子其他1,3-二羰基化合物情况相似,其他的吸电子基团如硝基、氰基等与羰基作用相同在含有氢的碳原子上连有两个吸电子基团的化合物都含有一个活泼的亚甲基,它们统称为含活泼亚甲基(氢 )的化合物。
β-二酮 β-羰基酸酯 丙二酸酯 氰乙酸酯 硝基乙酸酯 活泼氢化合物的双重反应性能:碳负离子 烯醇负离子 氧负离子一般情况下,这些物质在反应时可以看作是碳负离子对其它官能团的亲核加成反应。
酮式和烯醇式的互变异构两个羰基被一个碳原子隔开的化合物;当同一碳原子上连有两个吸电子基团时,这样的可以看作是活泼H 可以在α-C 和羰基O 之间来回移动。
1、酸碱对互变平衡的影响痕量的酸、碱甚至是玻璃仪器都能促使平衡的快速建立。
(1)酸催化过程在酸催异构化过程中,酸首先与羰基氧原子作用形成 盐,其共轭碱——水再夺取-H 形成烯醇。
(2)碱催化过程碳可以直接和α-H 结合,同时形成一个碳负离子。
通过电子对的转移,碳上的负电荷转移到氧上,形成烯醇负离子。
2、化合物的结构对互变平衡的影响通常,单羰基化合物中的烯醇式异构体含量很少。
-二羰基结构的化合物,在平衡状态下其烯醇式的含量较高。
通常以平衡混合物的形式存在。
例:乙酰乙酸乙酯(三乙)酮式 % 烯醇式 % .=41℃(267Pa) .=33℃(267Pa)这类化合物的烯醇式异构体具有较大稳定性的原因有二: ①通过分子内氢键,形成稳定的六元环状化合物;②羟基氧上的未共用电子对,可以通过p-π共轭发生离域,使分子内能降低。
在一些含氮化合物中也常发生互变异构现象:4、异构化对化学性质的影响(1)与FeCl 3的显色反应(烯醇式含量多的物质);(2)与溴的四氯化碳溶液加成; (3)-H 氘代(快速确定-H 的个数);(4)构型变化。
如-C 是手性中心并且手性碳上有氢原子,会发生外消旋化。
如-C 不是手性中心则不会发生外消旋化。
酮式中碳氧π键比烯醇式中碳碳π键更稳定!碳负离子形成及其基本原理1、碳负离子的形成及其稳定性碳负离子是以一个带有负电荷的碳为中心原子的中间体,是有机化学反应中常见的活性中间体。
如甲基负离子、烯丙基负离子、苄基负离子、三苯甲基负离子等。
碳负离子可以通过金属有机化合物异裂而产生。
碳氢键的碳原子上存在吸电子基时易形成碳负离子。
如:(1)内部条件能形成碳负离子的化合物从结构上讲,至少含有一个氢的碳原子的邻位要有一个活化基团,一些带有双键或叁键的吸电子基团C=O、NO2、SO2、CN、C≡C等都是活化基团。
活化基团的作用:①由于其吸电子作用,使氢碳酸的酸性增加,而容易脱质子化;②使形成的CӨ的负电荷离域而趋于稳定。
活化基团的强弱顺序:-NO2>-C=O>-SO2>-COOR>-CN>-C≡CH>-C6H5>-CH=CH2>-R除了要有一个活化基团外,分子中的其它基团的空间效应和电子效应对C—的形成和稳定性也有影响,其中空间阻碍影响最大。
(2)外部条件有了一个带有活化基团的化合物后,还必须加入碱,才能把α-H交换下来,形成碳负离子。
选择强度适合的碱,酸性弱的α-H要用强碱,反之用较弱的碱。
在选择碱的时候,还要分清哪些碱是强亲质子性的(与质子结合的能力),哪些碱是强亲核性的(与碳正离子的结合能力),哪些是两种都有的。
这是因为在形成CӨ的过程中,碱可能进攻碳原子,也可能进攻质子氢。
一般来说,亲核试剂的亲核性能大致与其碱性的强弱次序相对应。
对具有相同进攻原子的亲核试剂,碱性愈强者,亲核性愈强。
下面列出常用碱的性能:(1)具有强亲质子和强亲核能力的碱:HOӨ,CH3OӨ,C2H5OӨ,RSӨ,CNӨ等;(2)具有强亲质子弱亲核能力的碱:HӨ,NH2Ө;(3)具有强亲质子相当弱亲核性的碱:Et2NӨ,C6H5NӨ,Me3Si-NӨ。
在形成碳负离子的外部因素中,还应指出的是溶剂的影响。
假如溶剂的酸性比氢碳酸强的多的话,就不能产生很多的CӨ,因为刚形成的碱性很强的CӨ夺取溶剂的质子,又成为原来的化合物(内返作用)。
一般应采用极性大但酸性弱的溶剂,即非质子溶剂。
有以下几种配合:(1)t-BuOH,溶剂用t-BuOH或DMSO、THF;(2)NaNH2,溶剂用液氨或醚、苯、甲苯、1,2-二甲氧基烷苯等;(3)NaH 、LiH ,溶剂为苯、醚、THF 等; (4)(C 6H 5)3CNa ,溶剂为苯基醚、液氨等。
如:2、碳负离子的反应C Ө形成后(虽然是共振稳定的)具有很高的能量,可以发生多种亲核加成反应,重要的四类反应用通式表示如下: (1)与含羰基的化合物(2)酰基化反应:与羧酸及其衍生物的羰基发生亲核加成接着失去RO Ө或Z Ө形成β-酮酯或β-二酮,这是酯缩合型反应,总的结果是在C Ө上带上一个酰基。
(3)与烷基卤化物的反应(4)与活泼烯烃的加成反应§ 缩合反应Ⅰ——羟醛缩合见第11章《醛与酮》 α-H 的反应§ 缩合反应Ⅱ——Mannich 反应Mannich 反应甲醛与仲胺在弱酸性介质中亲核加成,再脱水形成正碳离子与醛(酮)、羧酸、酯、硝基化合物、腈的α-C ,以及端炔、酚的邻、对位等具有负碳离子性质的位置偶联,称为Mannich 反应,又称胺甲基化反应。
1、反应通式2、Mannich 反应机理3、Mannich 反应举例Mannich 反应在合成上的应用1、合成β-氨基酮衍生物【例1】写出合成路线2、制备,-不饱和酮【例2】甲基乙烯基酮的制备通过Mannich碱产生§缩合反应Ⅲ卤代反应——见第11章《醛与酮》α-H的反应 3、卤仿反应酯的缩合反应1、Claisen缩合(两个相同酯之间的缩合)具有-活泼氢的酯,在碱的作用下,两分子酯相互作用,生成-羰基酯,同时失去一分子醇的反应。
其它常用碱:NaH,NaNH2,LDA,Ph3CNa,t-BuOK(弱亲核性强碱);碱用量对反应的影响催化量:反应可逆大于化学计量:反应完全Claisen缩合举例:Claisen缩合机理(1)交叉酯缩合(两个不同酯之间的缩合)混合酯缩合举例:2、Dieckmann缩合(分子内酯缩合)二元酸酯若分子中的酯基被四个以上的碳原子隔开时,就发生分子内的酯缩合反应,形成五元环或六元环的酯,这种分子内的环化酯缩合反应称为狄克曼酯缩合。
对称二羧酸酯的Dieckmann 缩合例:Dieckmann 缩合的可逆性在合成上的应用如两个酯基间只隔有三个或三个以下的碳原子时,就不能发生分子内的缩合。
但这种二酸酯可以发生分子间缩合,或与不含-H的酯缩合,也均能得到环状羰基酯。
如丁二酸二乙酯间的缩合:3、酮的酰基化(酮酯缩合)【反应机理】不对称酮的酰基化4、β-二羰基化合物的互变异构现象5、酮或酯的酰基化反应在合成上的应用——制备β-二羰基型化合物( 1, 3-二羰基化合物)1, 3-二羰基型化合物的反合成分析【例 1】(反合成分析)【例 2】(反合成分析)【例 3】(反合成分析)合成路线6、酮和酯类化合物α位的烷基化反应应予以考虑的问题:(1)反应的活性问题(一般酮和酯类化合物α氢的酸性不够强,须强碱作用,反应条件较为苛刻);(2)反应的区位选择性问题(不对称酮有两种反应位置);(3)酮或酯的自身缩合问题(醇醛缩合和Claisen缩合)。
【例1】【例2】【例3】1, 3 -二羰基化合物的烷基化反应【例4】§缩合反应Ⅳ【复习】1、羰基α位的反应——酰基化(Claisen缩合,交叉酯缩合,Dieckmann缩合)和烷基化本节重点:羰基α位的酰基化和烷基化在合成上的应用2、酮式水解和酸式水解乙酰乙酸乙酯的制备及在合成中的应用合成等价物丙酮1、乙酰乙酸乙酯的合成乙酰乙酸乙酯−−−−→2、在合成中的应用(1)制备取代丙酮(甲基酮)类化合物扩展:制备环烷基甲基酮(2)制备甲基二酮类化合物扩展:制备2, 5-己二酮(3)通过酰基化制备β-二酮类化合物丙二酸二酯的制备及在合成中的应用合成等价物丙酮1、丙二酸二酯的合成丙二酸二酯−−−−→2、在合成中的应用(1)制备取代乙酸扩展:制备环烷基乙酸(2)制备二元羧酸3、乙酰乙酸乙酯和丙二酸酯合成法举例小结羰基α位酯基的作用——活化、定位、引导断键例:比较以下两条合成路线,你认为哪种较好,为什么?【例 1】分析并写出合成路线合成线路a合成线路b【例 2】分析并写出合成路线§缩合反应ⅤMichael加成碳负离子与,-不饱和羰基化合物发生的1,4-加成反应,叫做Michael反应。
这是形成碳碳键的重要方法之一。
1、反应通式2、反应机理3、Michael 加成举例一些羰基化合物α位的缩合反应归纳Robinson成环Micheal加成后,再发生分子内的羟醛缩合(或酯酮缩合),形成六元环状α,β不饱和酮(或1,3-环己二酮)。
1、反应通式2、Robinson成环举例5元环状烯酮和1, 4-二羰基化合物的合成一些特殊结构羰基化合物的合成方法小结(1)1, 3-二羰基(2)1, 4-二羰基(3)1, 5-二羰基(4)六元环状1, 3-二羰基(5)六元环状烯酮§缩合反应ⅥKnoevenagel反应在弱碱性催化下,醛酮与具有活泼亚甲基的化合物的缩合反应。
常用的碱性催化剂有吡啶、哌啶、胺等。
1、反应通式2、反应特点类似Aldol缩合;双活化基团的羰基化合物为烯醇负离子供体;弱碱催化(一般为胺类化合物或吡啶)。
3、反应机理由于使用的是弱碱避免了醛酮自身的缩合,扩大了醛酮的使用范围。
4、Knoevenagel反应举例Perkin反应(类似Aldol缩合)碱催化下,芳醛和酸酐反应生成-芳基-,-不饱和羧酸的反应。
