医疗器械经营企业记录表格本汇总
医疗器械经营企业记录表格验收用完整版
专业资料
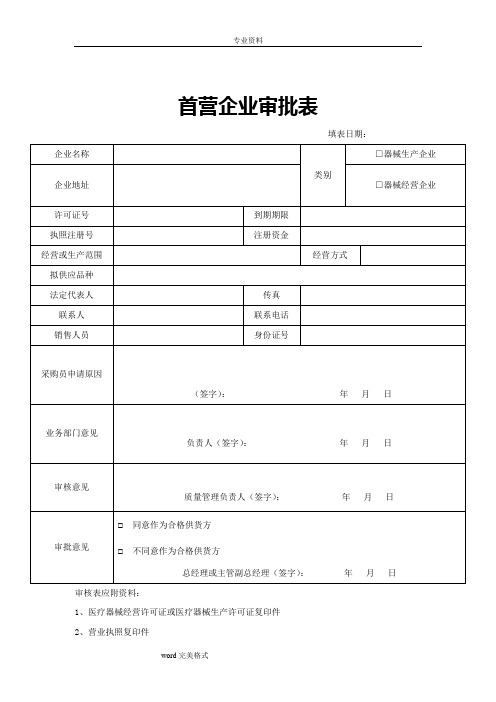
首营企业审批表
填表日期:
审核表应附资料:
1、医疗器械经营许可证或医疗器械生产许可证复印件
2、营业执照复印件
专业资料
3、委托书原件
首营品种审批表
编号:
注:附医疗器械生产/经营企业许可证、营业执照、医疗器械产品注册证、质量标准、出厂检验报告、委托书及业务员身份证复印件、样品、价格批文等资料。
验收单
日期:页次:质检部:
在库养护、检查表日期:页次:养护:
不合格品处理记录表
不合格医疗器械报损审批表
退回产品记录
日期:页次:质检部:
质量信息汇总表
质量问题追踪表
不良事件报告记录
质量事故报告记录
质量查询、投诉的报告处理记录
(反馈信息单)
方法:□信函□电话□附送样品□其他序号:年月日
质量(管理)档案
年至____ __
用户反馈质量记录
质量信息汇总表
退货记录
日期:页次:质检部:
质量事故报告记录
不良事件报告记录
质量问题跟踪表
设施和设备及定期检查、维修、保养档案
计量器具管理档案
用户档案
年度培训记录表
员工健康检查档案
质量管理制度执行情况检查和考核记录
记录表格目录
记录表格目录
医疗器械采购记录
供货单位:购进日期:年月日编号:
word完美格式
word完美格式
购货人:医疗器械召回情况记录表
word完美格式医疗器械销售记录表
word完美格式。
医疗器械经营企业质量管理体系全套记录表格

医疗器械经营企业质量管理体系全套记录表格内部审核与管理制度实施考核检查记录使用部门:NO: QMST-QR-001召回计划实施情况报告NO: QMST-QR-002文件发放/回收记录表文件更改申请审批记录表NO: QMST-QR-004购进(采购)记录文件作废/保留/销毁单NO: QMST-QR-006合格供方名单NO: XX-QR-007首营企业审批表首营品种审批表注:附生产企业许可证、营业执照、批准文件、质量标准、出厂检验报告、样品、价格批文、GSP证书及临床总结报告等资料.NO: QMST-QR-009质量验收记录养护档案表NO: QMST-QR-011设备报废单NO: QMSTXX-QR-012仪器设备维修保养记录NO: QMST-QR-013仪器设备台帐NO: QMST-QR-014设备日常保养点检表NO: QMST-QR-015计量器具检定记录卡取样记录养护设备使用记录库存质量养护记录在库检查记录部门:质量管理部检验员:审核:NO: QMST-QR-020年月库区:表号:温度范围℃适宜相对湿度范围%注:冷库温度:2-8℃,相对湿度:45-75%NO: QMST-QR-021NO: QMST-QR-022销售记录(清单)出库复核记录不合格产品报损审批表报告单位:报告日期:报损台帐不合格台帐(销毁记录)编号:说明:来源指不合格的来源部门或门店或客户名称NO: QMST-QR-027NO: QMST-QR-028NO: QMTS-QR-029顾客投拆查询质量台帐人员培训考核记录表NO: QMST-QR-032顾客质量投诉及处理记录NO: QMST-QR-033客户资格审核表NO: XX-QR-034质量记录处理(销毁)记录单号:NO: XX-QR-035采购计划编制:日期:批准:日期:NO: QMST-QR-036产品质量保证协议书甲方:公司乙方:公司为认真贯彻医疗器械等产品的法律法规,保证产品质量,明确质量责任,甲、乙双方本着平等、互利的原则,经协商,达成如下协议:一、乙方保证向甲方提供最新版本的供应商和产品资料,并保证所提供资料的真实性、合法性,并有责任及时更新已经过期、变更的资料,其中包括:1.合法有效、加盖公章的《营业执照》、许可证(按许可证管理的)复印件;2.合法有效、加盖公章的强制认证证书或其他有特别管理要求的文件复印件;3.产品的有效及合法批件复印件。
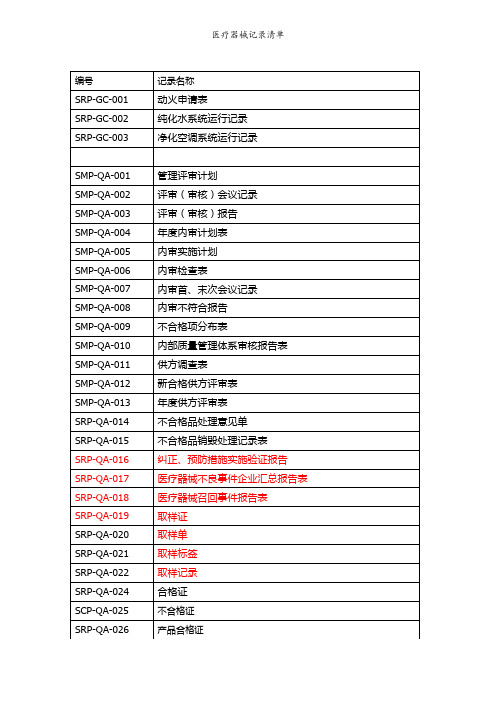
医疗器械记录清单
SRP-RY-007
试用期考核审批表
SRP-RY-008
员工转正申请
SRP-RY-009
上岗证
SRP-RY-010
人员健康档案
SRP-RY-011
员工身体不良情况记录
SRP-RY-012
信息联络单
SRP-RY-013
会议记录SRP-RY-014会议计划表SRP-RY-015
会议通知
SRP-RY-016
SRP-QA-015
不合格品销毁处理记录表
SRP-QA-016
纠正、预防措施实施验证报告
SRP-QA-017
医疗器械不良事件企业汇总报告表
SRP-QA-018
医疗器械召回事件报告表
SRP-QA-019
取样证
SRP-QA-020
取样单
SRP-QA-021
取样标签
SRP-QA-022
取样记录
SRP-QA-024
编号
记录名称
SRP-GC-001
动火申请表
SRP-GC-002
纯化水系统运行记录
SRP-GC-003
净化空调系统运行记录
SMP-QA-001
管理评审计划
SMP-QA-002
评审(审核)会议记录
SMP-QA-003
评审(审核)报告
SMP-QA-004
年度内审计划表
SMP-QA-005
内审实施计划
SMP-QA-006
内审检查表
SMP-QA-007
内审首、末次会议记录
SMP-QA-008
内审不符合报告
SMP-QA-009
不合格项分布表
SMP-QA-010
内部质量管理体系审核报告表
III类医疗器械经营企业质量管理全套表格
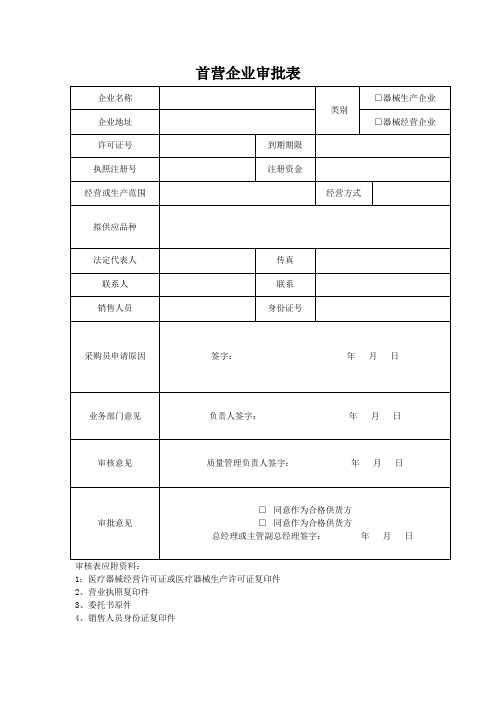
1:医疗器械经营许可证或医疗器械生产许可证复印件2、营业执照复印件3、委托书原件4、销售人员身份证复印件营业执照;2、医疗器械生产许可证或医疗器械经营许可证;3、企业法定代表人的委托授权书原件,委托授权书应明确授权范围及有效期;4、销售人员身份证明;5、医疗器械产品注册证书及附件;6、产品合格证明;7、产品质量标准;8、检验报告书;9、质量保证协议;10包装、标签、说明书批件和实样;以上资料除不能提供原件外,复印件需加盖原单位红色印章医疗器械购进记录年度医疗器械验收、入库记录年度出库单保管员:复核员:入库单制单日期:产品出库、复核记录产品销售记录质量查询、投诉、抽查情况记录医疗器械在库养护、检查记录温湿度记录表年月库区:常温库适宜温度范围:0~30℃适宜相对湿度范围40~80%温湿度记录表年月库区:阴凉库适宜温度范围:0~20℃适宜相对湿度范围40~80%售后服务登记表编号:医疗器械售后服务反馈登记表编号:质量跟踪处置情况质量事故调查处理记录年度员工培训记录不合格品处理记录表不良事件报告记录医疗器械销售产品召回记录质量管理制度执行情况和考核记录质量管理制度执行情况和考核记录质量管理制度执行情况和考核记录质量管理制度执行情况和考核记录质量管理制度执行情况和考核记录计量器具使用、检定记录年度员工培训计划可疑医疗器械不良事件报告表报告日期:年月日编码:报告来源:生产企业经营企业使用单位单位名称:联系地址: 邮编:联系:员工健康体检汇总表备注:员工健康档案还应包括每名员工的每年度的体检报告复印件也可,应尽量在本市二级以上医院进行体检;授权委托书____________:兹委托我公司员工____身份证号码________负责______区域销售我公司所经营医疗器械产品______________注明名称、规格型号,多品种的请附表;请贵公司予以接洽;有效期年月日至年月日_______公司加盖企业公章加盖法人章年月日设施和设备及定期检查、维修保养记录质量管理制度执行情况检查和考核记录医疗器械经营企业质量管理授权书授权为质量管理受权人;受权人根据企业负责人授权,行使以下质量管理权项:一、组织建立和完善本企业经营质量管理体系,对该体系进行监控,确保其有效运行;二、定期对本企业经营质量管理体系进行监督检查,检查结果直接上报所在地食品药品监管部门;三、对企业购进、销售、运输过程中涉及的可能影响产品质量等问题行使决定权;四、对企业的购销资质证明文件包括许可证、法人委托书、身份证明、检验报告、批签发等、产品标签说明书、合同、票据包括随货同行、汇款单位、产品来源及真伪等进行审查和甄别;确认合格的,出具确认合格报告书;凡没有经过确认的产品,不得采购和销售;五、受权人在行使职权时,企业其他人员必须予以配合和服从;六、授权人应加强对受权人的监督;受权人在行使职权期间发生的质量责任问题,除追究受权人的责任外,授权人应承担连带责任;七、本授权书于年月日起生效;受权人签名:年月日。
医疗器械质量记录(全套表格)

医疗器械质量管理记录1、文件修订申请表32、文件发放记录表43、文件回收记录表54、文件销毁申请表65、文件销毁记录表76、质量管理体系问题改进和措施跟踪记录87、医疗器械群体不良事件基本信息表98、医疗器械不良反应/事件报告表109、质量查询、投诉、服务记录1010、质量事故调查、处理表1111、医疗器械质量投诉处理记录1212、质量事故处理跟踪记录1313、员工健康档案表1514、员工健康检查汇总表1615、年度质量培训计划表1716、培训签到表1817、培训实施记录表1918、员工个人培训教育档案1919、设施设备台帐2120、设施设备运行维护使用记录2221、计量器具检定记录2222、医疗器械养护质量情况分析季度报表2423、医疗器械质量信息反馈表2424、医疗器械质量信息传递处理单2525、医疗器械召回记录2726、医疗器械追回记录2827、不合格医疗器械台帐2928、不合格医疗器械报损审批表3029、不合格医疗器械报损销毁审批表3030、质量管理制度执行情况自查及整改记录表3131、质量管理制度执行情况检查和考核记录表3232、医疗器械采购记录.3433、医疗器械收货记录3534、医疗器械验收记录3235、医疗器械出库记录3736、温湿度记录表3237、计算机系统权限授权审批记录表3238、车辆日常保养及卫生检查表4039、月卫生检查记录表4140、设施设备检修维护记录4241、医疗器械质量监控检查记录3242、医疗器械质量复查报告单3243、医疗器械停售通知单3244、医疗器械解除停售通知单3245、医疗器械拒收通知单3246、合格供货方档案表3247、储存作业区来访人员登记表3248、首营企业审批表5049、首营品种审批表3250、全体人员情况表3251、供货企业质量体系评定表3252、质量保证体系调查表3253、医疗器械质量档案表3254、医疗器械质量信息汇总表561、文件修订申请表2、文件发放记录表编号:JYBN—QXJL-002—013、文件回收记录表4、文件销毁申请表5、文件销毁记录表6、质量管理体系问题改进和措施跟踪记录编号:JYBN—QXJL-006-017、医疗器械群体不良事件基本信息表编号:JYBN-QXJL—007—01报告日期:年月日8、医疗器械不良反应/事件报告表编号:JYBN—QXJL-008—01首次报告□跟踪报告□报告类型:新的□严重□一般□报告单位类别:医疗机构□经营企业□生产企业□个人□其他□9、质量查询、投诉、售后服务记录10、质量事故调查、处理表审批人:11、医疗器械质量投诉处理记录12、质量事故处理跟踪记录13、员工健康档案表编号:JYBN-QXJL—013-01注:应将历次体检结果证明文件存入档案14、员工健康检查汇总表编号:JYBN—QXJL—014-011615、年度培训计划表质管部:行政部:审批人:1716、培训签到表17、培训实施记录表18、员工个人培训教育档案编号:JYBN—QXJL-018-0119记录人:2019、设施设备台帐20、设施设备运行维护使用记录21、计量器具检定记录22、医疗器械养护情况汇总分析季度报表养护员:汇总日期: 年月日23、医疗器械质量信息反馈表24、医疗器械质量信息传递处理单25、医疗器械召回记录2726、医疗器械追回记录2827、不合格医疗器械台帐2928、不合格医疗器械报损审批表29、不合格医疗器械报损销毁审批表30、质量管理制度执行情况自查及整改记录表编号:JYBN—QXJL—030-0131、质量管理制度执行情况检查和考核记录表编号:JYBN—QXJL—031-0132、医疗器械采购记录编号:JYBN—QXJL-032-013433、医疗器械收货记录编号:JYBN—QXJL—033-0135编号:JYBN—QXJL-034-01363736、温湿度记录表编号:JYBN-QXJL—036-01年月37、计算机系统权限授权审批记录表编号:JYBN—QXJL—037-0138、车辆日常保养及卫生检查表编号:JYBN—QXJL—038-0139、月卫生检查记录表编号:JYBN—QXJL—039—01检查日期:年月日符合或不符合的□内打√.检查人:40、设施设备检修维护记录编号: JYBN—QXJL—040—0141、医疗器械质量监控检查记录编号: JYBN—QXJL—041-0142、医疗器械质量复查报告单编号: JYBN—QXJL—042-0143、医疗器械停售通知单44编号:JYBN—QXJL—043—0144、医疗器械解除停售通知单45编号:JYBN—QXJL-044—014645、医疗器械拒收通知单编号:JYBN—QXJL—045-0146、合格供货方档案表编号:JYBN—QXJL—046—01建档时间:47、储存作业区来访人员登记表编号:JYBN—QXJL—047—014948、首营企业审批表编号:JYBN—QXJL-048-01。
医疗器械质量记录(全套表格)

医疗器械质量记录(全套表格)医疗器械质量管理记录表格包括以下内容:1.文件修订申请表这个表格记录了对文件进行修订的申请。
在这个表格中,可以记录申请的原因、修订的内容以及修订的日期等信息。
这个表格可以帮助管理者追踪文件修订的历史和原因。
2.文件发放记录表这个表格记录了向哪些人员发放了文件。
在这个表格中,可以记录发放的日期、发放的人员、发放的文件名称等信息。
这个表格可以帮助管理者追踪文件的流向和发放情况。
3.文件回收记录表这个表格记录了哪些文件被回收了。
在这个表格中,可以记录回收的日期、回收的人员、回收的文件名称等信息。
这个表格可以帮助管理者追踪文件的回收情况。
4.文件销毁申请表这个表格记录了对哪些文件进行销毁的申请。
在这个表格中,可以记录申请的原因、销毁的文件名称、销毁的日期等信息。
这个表格可以帮助管理者追踪文件销毁的历史和原因。
5.文件销毁记录表这个表格记录了哪些文件被销毁了。
在这个表格中,可以记录销毁的日期、销毁的人员、销毁的文件名称等信息。
这个表格可以帮助管理者追踪文件的销毁情况。
6.质量管理体系问题改进和措施跟踪记录这个表格记录了质量管理体系中出现的问题和采取的措施。
在这个表格中,可以记录问题的描述、解决方案、实施时间等信息。
这个表格可以帮助管理者追踪质量管理体系中的问题和解决情况。
13、员工健康档案表员工健康档案表是一份重要的文档,它记录了员工的健康状况和医疗史。
在这个表格中,我们需要填写员工的个人信息、体检记录、病史、药物过敏史等内容。
这些信息对于企业管理者来说非常重要,因为它们可以帮助我们更好地了解员工的身体状况,为员工提供更好的保健服务。
14、员工健康检查汇总表员工健康检查汇总表是一份汇总员工体检结果的文档。
在这个表格中,我们需要记录员工的体检项目、检查结果、医生建议等内容。
这些信息可以帮助企业管理者更好地了解员工的身体状况,及时发现健康问题,采取措施预防疾病,保障员工的身体健康。
医疗器械经营企业记录表格验收用完整版
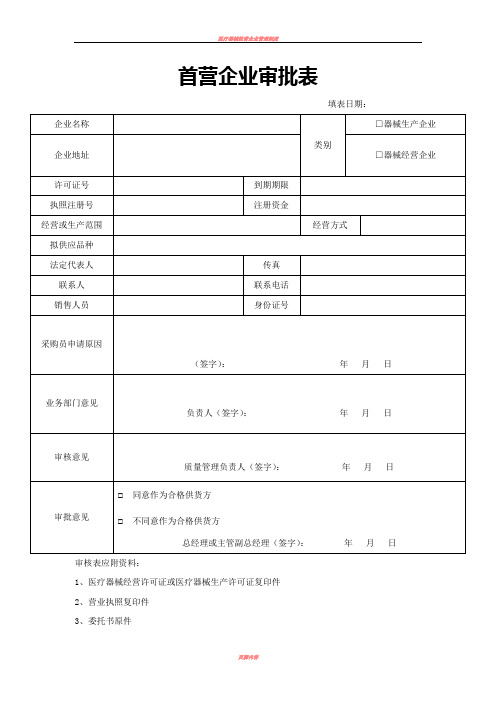
填表日期:
企业名称
类别
□器械生产企业
企业地址
□器械经营企业
许可证号
到期期限
执照注册号
注册资金
经营或生产范围
经营方式
拟供应品种
法定代表人
传真
联系人
联系电话
销售人员
身份证号
采购员申请原因
(签字): 年 月 日
业务部门意见
负责人(签字): 年 月 日
审核意见
质量管理负责人(签字): 年 月 日
许可证号:
电话:
医疗器械性能、用途、外观、质量情况审核
注册证号
质量标准
装箱规格
有效期
储存条件
采购员意见
负责人签字:日期:
质检员意见
负责人签字:日期:
经理审批意见
□同意进货 □不同意进货
负责人签字:日期:
注:附医疗器械生产/经营企业许可证、营业执照、医疗器械产品注册证、质量标准、出厂检验报告、委托书及业务员身份证复印件、样品、价格批文等资料。
维修记录
保养记录
备注
计量器具管理档案
计量器具名称
使用部门(管理人)
使用情况
备注
用户档案
用户名称
使用产品名称规格
质量反馈
年度培训记录表
培训日期
主讲人
培训内容
培训人员
员工健康检查档案
序号
姓名
性别
年龄
学历
或职称
岗位
体检日期
备注
质量管理制度执行情况检查和考核记录
项目
部门
检查记录
考核记录
质量方针和目标管理
各部门
质检
养护
医疗器械记录表格(出库、销售、退货、验收、采购等记录表)

医疗器械记录表格(出库、销售、退货、
验收、采购等记录表)
XXX医疗器械出库复核记录表:
出库日期商品名称数量规格/型号生产企业注册证号批号有效期购货企业复核
医疗器械销售记录:
日期商品名称规格/型号生产企业注册证号数量单价有效期购货企业经营地址联系电话
医疗器械退货记录:
产品名称生产企业规格/型号注册证号批号有效期退货单位退货日期退货数量退货原因处理结果
医疗器械售后服务及质量跟踪记录表:
购买日期购货方产品名称生产厂家规格/型号批号产品质量处理购货方联系人联系方式员工签字结果
洛阳XX医疗器械有限公司库房养护检查记录:
日期商品名称规格/型号注册证号生产厂商供货企业批号有效期养护员养护数量结论签字备注
XXX医疗器械采购记录表:
购货日期供货单位产品名称生产厂商规格/型号注册证号产品批号数量单价金额经办人
医疗器械质量复检通知单:
序号到货日期复检产品名称生产企业规格/型号注册证号批号有效期验收员意见质管部复检意见
医疗器械质量查询、投诉、抽查情况记录:
日期客户名称投诉产品生产厂家注册证号批号有效期投诉内容处理结果
设施和设备安装、维修、调试及定期检查、保养记录:
序号日期设施、设备名称定期检查保养情况清洁记录维修记录设备状态记录人
XX医疗器械有限公司医疗器械购进验收记录:
商品数型号/规格验收合格数验收员日期生产厂商供货企业注册证号批号有效期验收结论备注。
医疗器械内审记录表格模板
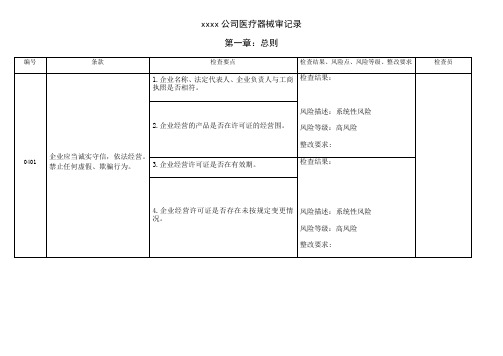
xxxx公司医疗器械审记录第一章:总则
xxxx公司医疗器械审记录第二章:职责与制度
xxxx公司医疗器械审记录第二章:职责与制度
xxxx公司医疗器械审记录第二章:职责与制度
xxxx公司医疗器械审记录第二章:职责与制度
xxxx公司医疗器械审记录第二章:职责与制度
xxxx公司医疗器械审记录第二章:职责与制度
xxxx公司医疗器械审记录第二章:职责与制度
xxxx公司医疗器械审记录
第二章:职责与制度
xxxx公司医疗器械审记录第二章:职责与制度
xxxx公司医疗器械审记录第二章:职责与制度
xxxx公司医疗器械审记录第三章:人员与培训
xxxx公司医疗器械审记录第三章:人员与培训
xxxx公司医疗器械审记录第四章:设施与设备
xxxx公司医疗器械审记录第四章:设施与设备
xxxx公司医疗器械审记录第四章:设施与设备
xxxx公司医疗器械审记录第四章:设施与设备
xxxx公司医疗器械审记录第四章:设施与设备
xxxx公司医疗器械审记录第四章:设施与设备
xxxx公司医疗器械审记录第四章:设施与设备
xxxx公司医疗器械审记录第五章:采购、收货与验收
xxxx公司医疗器械审记录第五章:采购、收货与验收
xxxx公司医疗器械审记录第五章:采购、收货与验收
xxxx公司医疗器械审记录第六章:入库、储存与检查
xxxx公司医疗器械审记录第六章:入库、储存与检查
xxxx公司医疗器械审记录第六章:入库、储存与检查
xxxx公司医疗器械审记录
第七章:销售、出库与运输。
医疗器械分销企业记录表格

医疗器械分销企业记录表格介绍医疗器械分销企业记录表格用于记录医疗器械分销企业的相关信息和活动。
该表格旨在帮助企业管理医疗器械的分销过程,并提供完整的记录以便将来参考和审查。
记录表格内容记录表格包括以下几个主要部分:1. 企业信息- 企业名称:记录医疗器械分销企业的名称。
- 注册资本:记录企业的注册资本金额。
- 法定代表人:记录企业的法定代表人姓名。
- 联系人:记录企业的联系人姓名。
- 联系记录企业的联系电话。
2. 分销产品信息- 产品名称:记录被分销的医疗器械的名称。
- 产品批准文号:记录医疗器械的批准文号。
- 生产企业:记录医疗器械的生产企业名称。
- 分销价格:记录医疗器械的分销价格。
- 分销数量:记录医疗器械的分销数量。
3. 分销渠道- 分销渠道:记录医疗器械的分销渠道,如分销商、代理商等。
- 分销区域:记录医疗器械的分销区域范围。
4. 分销时间- 分销开始时间:记录医疗器械的分销开始时间。
- 分销结束时间:记录医疗器械的分销结束时间。
使用指南使用医疗器械分销企业记录表格时,应按照以下步骤进行操作:1. 填写企业信息:填写医疗器械分销企业的相关信息。
2. 填写分销产品信息:填写被分销的医疗器械的相关信息。
3. 填写分销渠道:填写医疗器械的分销渠道信息。
4. 填写分销时间:记录医疗器械的分销时间信息。
请注意,为保证记录的准确性和完整性,应在每次分销活动发生时及时更新该记录表格。
结论医疗器械分销企业记录表格是一种方便管理和记录医疗器械分销信息的工具。
通过使用该表格,企业可以实时了解分销情况,并保留详细的记录以备将来参考和审查之用。
医疗器械经营企业质量管理记录

医疗器械经营企业质量管理记录首营企业审批表企业名称:企业地址:社会统一信用代码:许可证号:有效期限:法定代表人:联系人:销售人员:传真:联系身份证号:注册资金:发证日期:经营方式:类别:器械生产企业 / 器械经营企业(生产企业略)经营或生产范围:拟购进品种:采购意见(签字):年月日审核意见:质量负责人(签字):年月日审批意见:法人或企业负责人(签字):年月日审批表应附资料(均应加盖供方原印章):1、医疗器械经营许可证(第二类经营备案凭证)或医疗器械生产许可证(第一类生产备案凭证)复印件;2、营业执照复印件;3、销售人员授权书原件;4、销售人员身份证复印件;5、供货方随货同行单样本。
首营品种审批表产品名称:型号规格:产品性能:结构及组成:产品适用范围:产品禁忌症:生产企业名称:生产地址:供货企业名称:业务联系人:法定代表人:联系法定代表人:联系注册证号(备案凭证号):储运条件:供货企业生产或经营范围:采购意见(签字):年月日审核意见:审批意见:审批表应符资料(均应加盖供货方原印章):1、医疗器械产品注册证(变更文件)或备案凭证;2、产品外包装、标签、说明书;3、样品或宣传彩页;4、采购合同或协议(含质量保证协议);法人或企业负责人(签字):年月日质量负责人(签字):年月日医疗器械采购记录序号购货日期名称规格(型号)产品注册证号或(备案凭证编号)单位数量单价金额供货单位生产厂家备注医疗器械验收记录年度有效期或失效期生产企业供货者到货数量到货日期验收合格数量验收结果验收人员验收日期备注序号名称规格(型号)注册证号或备案凭证号批号或序列号生产日期医疗器械在库养护、检查记录年度检查日期名称规格(型号)注册证号或备案凭证号批号或序列号生产日期有效期或失效期生产企业数量外观是否完好包装有无破损处理结果养护员签字备注医疗器械出库、复核记录年度出库日期购货者名称规格型号注册证号或备案凭证编号批号或序列号生产日期有效期或失效期生产企业数量质量状况复核员备注医疗器械运输记录年度序号送货日期购货者送货地址销售清单(随货同行单)号出发时间送达时间送货车辆接收人送货人备注日期供货者购货者名称号(备案凭证编号)退货原因备注医疗器械销售记录(批发)年度008:本文记录了医疗器械批发销售的详细信息,包括销售日期、名称、规格、型号、注册证号或备案凭证编号、数量、单价、金额、批号或序列号、生产许可证、有效期、生产企业号或备案凭证编号、经营许可证、购货者名称号(备案凭证编号)、经营地址联系方式等。
医疗器械经营企业记录表格完整版本

首营企业审批表
填表日期:
首营品种审批表
编号:1
注:附医疗器械生产企业许可证、营业执照、医疗器械产品注册证、质量标准、出厂检验报告、委托书及业务员身份证复印件、样品、价格批文等资料。
验收单
日期:页次:质检部:
在库养护、检查表
不合格品处理记录表
不合格医疗器械报损审批表
日期: 页次: 质检部: 退回产品记录
进货日不合格不合
药监局信息行业信息
质量信息汇总表
质量冋题追踪表
不良事件报告记录
质量事故报告记录
质量查询、投诉的报告处理记录(反馈信息单)
方法:□信函□电话□附送样品□其他序号:年
月日
质量(管理)档案
年至 ______
用户反馈质量记录
质量信息汇总表
退货记录
日期:页次:质检部:
质量事故报告记录
不良事件报告记录
质量冋题跟踪表
设施和设备及定期检查、维修、保养档案
计量器具管理档案
眼镜顾客配镜记录表
地址:TEL: FAX:
顾客地址:手机:
用户档案
培训计划
_________ 年度培训记录表
员工健康检查档案
质量管理制度执行情况检查和考核记录。
最新人民医院医疗器械管理制度及记录表格

x市人民医院医疗器械管理条目一、质量管理规定1、医疗器械质量管理程序2、医疗器械进货检查验收制度3、医疗器械使用前质量检查制度4、医疗器械使用管理制度5、医疗器械储存、保管、养护制度6、医用耗材库房管理制度7、仓库温湿度管理制度8、一次性无菌医疗器械使用及用后销毁制度9、医疗器械不良反应报告制度10、一次性使用无菌医疗器械购进、验收、使用管理制度11、一次性使用无菌医疗器械用后销毁制度12、消毒产品进货验收、使用管理、储存制度二、各类附表1、医疗器械质量管理委员会职责及名单2、一次性医疗器械入库登记表3、试剂验收管理规定条目表4、库存医疗器械定期检查记录表5、益阳市人民医院医疗设备维护保养记录表6、医疗设备维护保养记录表医疗器械质量管理程序一、医疗器械质量验收程序1.目的:为保证医疗器械入库前的质量,规范验收过程的操作,特制定本程序。
2.范围:医疗器械入库前的质量控制。
3.职责:采购员、验收员负责按本程序的规定操作。
4.程序:4.1产品到货后,采购员接收并核对产品数量,初验合格后通知验收员验收。
4.2来货产品进入待验库/区,验收员核对基本信息:来货实物与合同、发货单、产品注册(备案)证的品名、注册(备案)证号、规格、数量、生产厂商、产品批号、有效期、供货单位等信息是否一致;进口医疗器械还必须核对海关报关单或相关部门的基本信息是否一致。
4.3依据有关标准及质量保证协议对来货产品质量进行逐批验收。
4.4检查说明书、标签、包装、批准文号、合格证、外观性状等是否符合规定。
4.5合格医疗器械办理入库手续,作好验收记录。
4.6对信息不一致,质量异常、标志模糊、漏液等不符合验收标准的产品应拒收,并填写《拒收报告单》,报质量管理机构负责人审核并签署处理意见,通知采购员处理。
二、医疗器械入库储存程序1.目的:为保证入库储存医疗器械质量,规范入库储存过程的操作,特制定本程序。
2.范围:所有入库、在库医疗器械及入库储存的过程。
医疗器械质量记录(全套表格)

医疗器械质量管理记录1、文件修订申请表 (3)2、文件发放记录表 (4)3、文件回收记录表 (5)4、文件销毁申请表 (6)5、文件销毁记录表 (7)6、质量管理体系问题改进和措施跟踪记录 (8)7、医疗器械群体不良事件基本信息表 (9)8、医疗器械不良反应/事件报告表 (10)9、质量查询、投诉、服务记录................................................ 错误!未定义书签。
10、质量事故调查、处理表................................................... 错误!未定义书签。
11、医疗器械质量投诉处理记录............................................... 错误!未定义书签。
12、质量事故处理跟踪记录................................................... 错误!未定义书签。
13、员工健康档案表......................................................... 错误!未定义书签。
14、员工健康检查汇总表..................................................... 错误!未定义书签。
15、年度质量培训计划表..................................................... 错误!未定义书签。
16、培训签到表............................................................. 错误!未定义书签。
17、培训实施记录表......................................................... 错误!未定义书签。
医疗器械质量记录(全套表格)

医疗器械质量管理记录1、文件修订申请表32、文件发放记录表43、文件回收记录表54、文件销毁申请表65、文件销毁记录表76、质量管理体系问题改进和措施跟踪记录87、医疗器械群体不良事件基本信息表98、医疗器械不良反应/事件报告表109、质量查询、投诉、服务记录1210、质量事故调查、处理表1311、医疗器械质量投诉处理记录1412、质量事故处理跟踪记录1513、员工健康档案表1714、员工健康检查汇总表1815、年度质量培训计划表1916、培训签到表2017、培训实施记录表2118、员工个人培训教育档案2219、设施设备台帐2320、设施设备运行维护使用记录2421、计量器具检定记录2522、医疗器械养护质量情况分析季度报表2623、医疗器械质量信息反馈表2724、医疗器械质量信息传递处理单2825、医疗器械召回记录2926、医疗器械追回记录3027、不合格医疗器械台帐3228、不合格医疗器械报损审批表3329、不合格医疗器械报损销毁审批表3430、质量管理制度执行情况自查及整改记录表3531、质量管理制度执行情况检查和考核记录表3632、医疗器械采购记录。
3433、医疗器械收货记录3534、医疗器械验收记录3635、医疗器械出库记录3736、温湿度记录表3637、计算机系统权限授权审批记录表3638、车辆日常保养及卫生检查表4039、月卫生检查记录表4140、设施设备检修维护记录4241、医疗器械质量监控检查记录3642、医疗器械质量复查报告单3643、医疗器械停售通知单3644、医疗器械解除停售通知单3645、医疗器械拒收通知单3646、合格供货方档案表3647、储存作业区来访人员登记表3648、首营企业审批表5049、首营品种审批表3650、全体人员情况表3651、供货企业质量体系评定表3652、质量保证体系调查表3653、医疗器械质量档案表3654、医疗器械质量信息汇总表561、文件修订申请表编号:JYBN-QXJL—001—012、文件发放记录表编号:JYBN-QXJL-002-013、文件回收记录表编号:JYBN—QXJL-003-014、文件销毁申请表编号:JYBN—QXJL—004-015、文件销毁记录表编号:JYBN-QXJL—005-01。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
首营企业审批表
填表日期:
首营品种审批表
编号:1
注:附医疗器械生产企业许可证、营业执照、医疗器械产品注册证、质量标准、出厂检验报告、委托书及业务员身份证复印件、样品、价格批文等资料。
验收单
在库养护、检查表
不合格品处理记录表
不合格医疗器械报损审批表
退回产品记录
日期:页次:质检部:
质量信息汇总表
质量问题追踪表
不良事件报告记录
质量事故报告记录
质量查询、投诉的报告处理记录(反馈信息单)
方法:□信函□电话□附送样品□其他序号:年月日
质量(管理)档案
年至
用户反馈质量记录
质量信息汇总表
退货记录
日期:页次:质检部:
质量问题跟踪表
设施和设备及定期检查、维修、保养档案
计量器具管理档案
————眼镜顾客配镜记录表地址:: :
顾客地址: 手机:
眼部健康
检查情况
隐形眼镜
配戴情况
配镜后
复查情况
产品基
本情况
用户档案
培训计划
年度培训记录表
员工健康检查档案
质量管理制度执行情况检查和考核记录。
