氢氯噻嗪杂质经验总结分享
厄贝沙坦氢氯噻嗪片剂有关物质的方法学研究

医药科研厄贝沙坦氢氯噻嗪片剂有关物质的方法学研究王雪平 (海南省食品药品检验所儋州分所,海南儋州 571700)摘要:目的:建立HPLC法测定厄贝沙坦氢氯噻嗪片有关物质的方法。
方法:色谱柱:Agilent ZORBAX SB-CN柱(5μm,4.6×250 mm);流动相:磷酸盐缓冲液(取磷酸二氢钾1.36g,加水900mL,加入三乙胺2mL,用磷酸调pH值至3.0,加水稀释至1000mL)-甲醇-乙腈(44:34:22);流速:1.5mL/min;检测波长:220nm。
结果:主峰位置未受杂质影响,主峰和杂质峰能较分离。
结论:本法测定厄贝沙坦氢氯噻嗪片剂有关物质,方法简便、快速、结果准确,专属性好,适用于厄贝沙坦氢氯噻嗪片的质量控制。
关键词:高效液相色谱法;厄贝沙坦氢氯噻嗪片;有关物质高血压是引起冠心病、心梗、脑梗等多种心脑血管疾病的危险因素[1]。
厄贝沙坦氢氯噻嗪片是由血管紧张素-Ⅱ受体拮抗剂厄贝沙坦和噻嗪类利尿药氢氯噻嗪组成的复方制剂,比其中任何单一药物成分的降压作用都更有效,用于原发性高血压的治疗,特别是单一治疗疗效不佳的高血压[2~3]。
两种药物的降压机制不同,组成固定剂量的复方制剂后可以协同降压、增强降压效果,且能互相补充其不足,减少或抵消单药长期用药可能出现的不良反应。
因此,两种药物组成复方制剂具有较多优势。
高效液相色谱法具有操作简便、专属性强、灵敏度高、重复性好等优点,因此选择高效液相色谱法测定厄贝沙坦氢氯噻嗪片的有关物质,药品分析方法的质量直接影响着药品标准的质量。
故建立有关物质测定方法之后,仍需通过一系列的试验来验证该方法的可行性[4~5],从而为厄贝沙坦氢氯噻嗪片在治疗人类疾病中保证其安全性、有效性和可控性提供科学的依据。
1实验仪器与试药Agilent 1100高效液相色谱仪(美国安捷伦公司);电子天平CPA225D(梅特勒-托利多公司);厄贝沙坦(批号:100607-201202,中国食品药品检定研究院)、氢氯噻嗪(批号:100309-201404,中国食品药品检定研究院)、厄贝沙坦有关物质A和氢氯噻嗪有关物质A对照品均由齐鲁制药(海南)有限公司提交提供;厄贝沙坦氢氯噻嗪片(齐鲁制药(海南)有限公司,批号为C1L1308004、C1L1308005、C1L1308006)。
高效液相色谱法测定氢氯噻嗪原料的含量

高效液相色谱法测定氢氯噻嗪原料的含量【摘要】目的:成立氢氯噻嗪原料药的含量测定方式。
方式:采纳C18柱(250 mm× mm,5 μm),以 mol/L磷酸二氢钠乙腈(9∶1)(用磷酸调剂pH值至)为流动相,检测波长271 nm,流速 mL/min,柱温30 ℃。
结果:氢氯噻嗪浓度在~ mg/mL浓度范围内与峰面积线性关系良好(r=,n=7),加样回收率%,RSD=%。
结论:该方式专属性强,灵敏度高,重复性好,操作简便,适用于氢氯噻嗪原料的质量操纵。
【关键词】氢氯噻嗪高效液相色谱法含量测定HPLC Determination of HydrochlorothiazideZENG Tan, ZHOU Lin(Chongqing Institute for Drug Control, Chongqing 400121, China)[Abstract] Objective:To develop an HPLC method for the determination of Hydrochlorothiazide. Methods: The chromatographic separation was performed on a C18 column (250 mm × mm, 5 μm) held in the oven of 30 ℃. The mobile phaseconsisted of a degassed mixture of mol/L monobasic sodium phosphate and acetonitrile (9:1), adjusted with phosphoric acid to a pH of . The flow rate was mL/min and UV detection wavelength was 271 nm. Results: The calibration of the responses of hydrochlorothiazide ranged from to mg/mL with a correlation coefficient of , recovery rate of % and RSD=%. Conclusions: The method proves to be quick, simple and sensitive. It could be applied into the quality control of hydrochlorothiazide.[Key words] Hydrochlorothiazide; High performance liquid chromatography; Determination of content氢氯噻嗪是一种临床应用十分普遍的药物,要紧抑制髓袢升支皮质部对Na+和Cl的重吸收,使肾脏对氯化钠的排泄增加而产生利尿作用,常与其他降压药物配合作用医治高血压。
HPLC法测定复方卡托普利片中氢氯噻嗪的含量

HPLC法测定复方卡托普利片中氢氯噻嗪的含量陈玉璞【摘要】目的建立测定复方卡托普利片中氢氯噻嗪含量的方法.方法采用HPLC 法,C18柱(150 mm×6.0 mm,5 μm);流动相为磷酸盐缓冲液(O.01 mol·L-1磷酸二氢钾溶液,用磷酸调节pH至3.0)-甲醇-水(4:30:66);检测波长为272nm.结果氢氯噻嗪质量浓度在4.48~44.80 mg·L-1范围内线性关系良好(r=0.999 9),平均回收率为98.9%,RSD为0.7%.结论方法简便、快速,结果准确,专属性强,可作为复方卡托普利片中氢氯噻嗪的含量测定方法.【期刊名称】《西北药学杂志》【年(卷),期】2010(025)001【总页数】2页(P14-15)【关键词】HPLC法;复方卡托普利片;氢氯噻嗪【作者】陈玉璞【作者单位】焦作市食品药品检验所,河南焦作454000【正文语种】中文【中图分类】R927.2高血压是常见病,由于该病死亡率很高,因此,降血压药的研制越来越受到人们的重视。
复方卡托普利片为常用降压药,主要成分有卡托普利和氢氯噻嗪,其中氢氯噻嗪具有利尿、降压等作用。
复方卡托普利片现行国家药品标准中氢氯噻嗪含量测定为紫外分光光度法[1]。
笔者参考文献[2]建立用HPLC法测定其中氢氯噻嗪的含量,作为复方卡托普利片质量控制指标,为控制药品质量提供了一种简单、灵敏、快速、准确的检测方法。
1 仪器与试药1.1 仪器 UVIKONXL型紫外分光光度计(法国);AE-240双量程电子天平(瑞士梅特勒公司);岛津HPLC仪(LC-10ADVP泵;SPD-10AVP紫外检测器;CS-Light PotrunA nalysis数据处理系统)。
1.2 试药氢氯噻嗪对照品(中国药品生物制品检定所,批号10309-0001,供含量测定用,含量99.4%);复方卡托普利片(天津药业焦作有限公司,批号09040421,08041621,08101421,07111421,09091521);水为纯净水;甲醇为一级色谱纯。
流化床颗粒包衣法制备替米沙坦氢氯噻嗪片

氢氯噻嗪的药理作用及不良反应分析

氢氯噻嗪的药理作用及不良反应分析发表时间:2018-04-09T14:14:53.460Z 来源:《航空军医》2018年1期作者:夏洋[导读] 氢氯噻嗪是噻嗪类中常用的利尿剂,近年来,氢氯噻嗪对于治疗高血压应用广泛。
(双鸭山市食品药品不良反应监测中心黑龙江双鸭山 155100)摘要:氢氯噻嗪是噻嗪类中常用的利尿剂,近年来,氢氯噻嗪对于治疗高血压应用广泛。
氢氯噻嗪口服吸收迅速但不完全,进食能增加吸收量,作用平稳持续,与其他抗高血压药物联合应用能显著增加疗效,可降低心血管病的患病率和死亡率,而且费用低廉,依从性好,为降压治疗的起始药和维持药。
但长期应用可出现乏力、倦怠、眩晕、食欲缺乏、恶心、呕吐、腹泻及血压降低等症状,减量或调节电解质失衡后症状即可消失。
有时可出现较严重反应,应加注意。
关键词:氢氯噻嗪;药理作用;不良反应氢氯噻嗪又名双氢氯噻嗪、双氢克尿噻、双氢氯消疾、双氢氯散疾。
为白色结晶性粉末,无臭,味微苦,为临床常用噻嗪类利尿降压药。
利尿作用主要是抑制髓袢升支的皮质段和远端小管前段对钠、氯离子的重吸收,起排钠利尿作用。
降压作用与增加钠从尿中排泄有关,也可能是增加了胃肠道对Na+的排泄。
抗利尿作用机制尚不十分明确,其能减少肾原性尿崩症的尿量有时达50%。
本品主要用于治疗各型水肿,对心性和肾性水肿疗效较好;也可单独或与其他降压药联合应用于治疗原发性高血压;还可治疗中枢性或肾性尿崩症及预防含钙盐成分形成的结石等。
氢氯噻嗪的大多不良反应与剂量和疗程有关。
1 药动学氢氯噻嗪口服能迅速吸收,血药浓度在会1~2小时达峰值,血浆半清除时间是10~17小时,血浆浓度与口服剂量呈正相关,进入血液后经肾脏迅速代谢,血浆蛋白结合率为67.9%,75~97%从尿液排出。
服药2小时后产生利尿作用,达峰时间为4小时,3~6小时后产生降压作用,作用持续时间6~12小时。
本品部分与血浆蛋白结合,蛋白结合率为40%,另外部分进入红细胞、胎盘内。
HPLC法测定复方制剂厄贝沙坦氢氯噻嗪片有关物质

第51卷第1期 辽 宁 化 工 Vol.51,No.1 2022年1月 Liaoning Chemical Industry January,2022收稿日期: 2021-10-21HPLC法测定复方制剂厄贝沙坦氢氯噻嗪片有关物质赵翠,徐宝燕,兰公剑(南京正大天晴制药有限公司, 江苏 南京 210046)摘 要:目的:建立厄贝沙坦氢氯噻嗪片有关物质检测方法。
方法:采用Phenomenex Luna®3μm CN 100A (4.6 mm×150 mm,3 μm)为色谱柱;以0.01 mol·L-1的磷酸二氢钾缓冲液(取磷酸二氢钾1.36 g,加水1 000 mL 溶解,加入2 mL三乙胺,用磷酸调节pH值至3.0)为流动相A,以甲醇-乙腈(5∶1)为流动相B,线性梯度洗脱0~5 min,流动相B 18%;5~22min,流动相B 18%~45%;22~27 min,流动相B 45%;27~28 min,流动相B 45%~18%;流速为1.0 mL·min-1,检测波长为220 nm。
结果:各已知杂质在限度质量分数10%~200%范围内线性关系良好,r ≥0.999 9,各杂质及主峰与相邻杂质分离良好;各已知杂质的回收率在98.0%~110.6%范围内,RSD均小于2.0%(n=12);溶液在24 h内稳定;精密度和重复性RSD均小于5.0%。
结论:方法精密度好、准确度高,可用于本品的有关物质检测。
关 键 词:厄贝沙坦氢氯噻嗪片;有关物质;高效液相色谱仪法(HPLC)中图分类号:O657.7 文献标识码: A 文章编号: 1004-0935(2022)01-0146-03高血压是危害人类健康的常见的心血管疾病之一,心脏和血管是高血压的主要靶器官,长期高血压可影响重要脏器尤其心、脑、肾的结构和功能,最终导致这些器官的功能衰竭,迄今仍是心血管疾病死亡的主要原因之一[1-3]。
复方地巴唑氢氯噻嗪胶囊工艺改进和磷酸氯喹的质量研究

中图分类号:R97 文献标识码:B DOI:10.19613/ki.1671-3141.2018.46.062
本 文 引 用 格 式: 赵 军 霞 . 复 方 地 巴 唑 氢 氯 噻 嗪 胶 囊 工 艺 改 进 和 磷 酸 氯 喹 的 质 量 研 究 [J]. 世 界 最 新 医 学 信 息 文 摘 ,2018,18(46):98-99.
1 磷酸氯喹的含量测定方法 磷酸氯喹的含量测定方法是参照中国国家食品药品监
督管理局颁布标准及中国药典 HPLC 法相关要求制定。 具体方法如下: 1.1 仪 器 与 试 药。 高 效 液 相 色 谱 仪(Agilent LC-1100 美国)。复方地巴唑氢氯噻嗪胶囊(福州辰星药业有限 公司生产);维生素 B1 对照品、维生素 B6 对照品、盐 酸异丙嗪对照品(均由中国食品药品生物制品检定所提 供);磷酸氯喹对照品(福建省食品药品检验所提供 含 量 99.8%)、硫酸胍生对照品(福建省食品药品检验所提 供 含量 99.4%)、地巴唑对照品。甲醇和乙腈为色谱纯; 水为实验室制作的超纯水;其他试剂为分析纯 [1]。 1.2 色谱条件。色谱柱(C18 2504.65 Welch Materials); 流动相组成为:pH3.5 缓冲液(称取 1.35 g 己烷磺酸钠, 溶解到适量的水中,加入 10 mL 冰醋酸,再加水到 1000 mL,用三乙胺调节 pH=3.5):甲醇:乙腈 =55:24:21;流 速为 1.0;柱温 40 摄氏度;检测波长是 275;样品进量量
98
World Latest Medicne Information (Electronic Version) 2018 Vo1.18 No.46
·药物研究·
复赵军霞
(河南中帅医药科技股份有限公司,河南 郑州 450001)
氢氯噻嗪

[修订]氢氯噻嗪QinglüsaiqinHydrochlorothiazide书页号:2005年版二部-406[修订]第2行“按干燥品计算,含C7H8ClN3O4S2应为98.5%~101.5%”改为“按干燥品计算,含C7H8ClN3O4S2应为98.0%~102.0%”。
【检查】氯化物取本品1.0g,加水20ml,振摇,滤过,分取滤液10ml,依法检查(附录Ⅷ A ),与标准氯化钠溶液5.0ml制成的对照液比较,不得更浓(0.01%)。
炽灼残渣不得过0.1%(附录Ⅷ N)。
【含量测定】照高效液相色谱法(附录Ⅴ D)测定。
色谱条件与系统适用性试验用十八烷基硅烷键合硅胶为填充剂;0.1mol/L磷酸二氢钠-乙腈(9∶1)(用磷酸调节pH值至3.0±0.1)为流动相;检测波长为271nm,流速为每分钟1.5ml;柱温30℃。
取氢氯噻嗪和氯噻嗪对照品,用流动相溶解并稀释制成每1ml含0.04mg的溶液,作为系统适用性试验溶液。
氢氯噻嗪和氯噻嗪峰的分离度应大于2.0。
测定法取本品约20mg,精密称定,置100ml量瓶中,加甲醇-乙腈(1∶1)5ml,振摇使溶解,用流动相稀释至刻度,摇匀,精密量取5ml,置25ml量瓶中,用流动相稀释至刻度,摇匀,作为供试品溶液。
取10 l注入液相色谱仪,记录色谱图;另取氢氯噻嗪对照品适量,精密称定,同法制成每1ml约含0.04mg的溶液,作为对照品溶液。
同法测定,按外标法以峰面积计算,即得。
[删去]【鉴别】(1)、(3)【检查】芳香第一胺[增订]【鉴别】(1) 取本品50mg,置100ml量瓶中,用0.1mol/L氢氧化钠溶液10ml溶解,再加水稀释至刻度,摇匀,取该溶液2ml,置100ml量瓶中,用0.01mol/L氢氧化钠溶液稀释至刻度,摇匀,照紫外-可见分光光度法(附录ⅣA),在250nm~350nm波长范围内测定吸光度,在273nm和323nm波长处有最大吸收,在273nm和323nm波长处的吸光度比值为5.4~5.7。
氢氯噻嗪

氢氯噻嗪百科名片氢氯噻嗪为利尿药、抗高血压药。
主要适用于心原性水肿、肝原性水肿和肾性水肿:如肾病综合征、急性肾小球肾炎、慢性肾功能衰竭以及肾上腺皮质激素与雌激素过多引起的水肿;高血压;尿崩症。
长期应用时宜适当补充钾盐。
目录药品概述药物分析药理毒理药代动力学适应症用法用量1不良反应儿童用药1老年患者用药注意事项药物相互作用药物过量药物贮藏生产企业增加2010版中国药典修订增订内容展开编辑本段药品概述通用名:氢氯噻嗪结构式化学名:6-氯-3,4-二氢-2H-1,2,4-苯并噻二嗪-7-磺酰胺-1,1-二氧化物拼音名:QINGLUSAIQIN 英文名:HYDROCHLOROTHIAZIDE CAS No.:58-93-5 结构式:分子式:C7H8ClN3O4S2 分子量:297.74 规格:(1)10mg (2)25mg 别名:双氢氯噻嗪,双氢克尿塞,双氢氯消疾,DCT,噢列特(Oretic),Richlyn,Dichlotride,Esidrix,Hydrodiuril。
类别:利尿药、抗高血压药。
剂量:口服,一次25~100mg。
制剂:①片剂:25mg、50mg、100mg。
②溶液剂:50mg/5ml。
性状:本品为白色结晶性粉末;无臭,味微苦。
本品在丙酮中溶解,在乙醇中微溶,在水、氯仿或乙醚中不溶;在氢氧化钠溶液中溶解。
熔点:本品的熔点为265~273℃,熔融时同时分解。
氢氯噻嗪编辑本段药物分析方法名称:氢氯噻嗪的测定—中和滴定法应用范围:本方法采用滴定法测定氢氯噻嗪的含量。
本方法适用于氢氯噻嗪。
方法原理:供试品加二甲基甲酰胺溶解后,加偶氮紫指示液,在氮气流中,用甲醇钠滴定液(0.1mol/L)滴定至溶液恰显蓝色。
读出甲醇钠滴定液使用量,并将滴定结果用空白试验校正,每1mL甲醇钠滴定液(0.1mol/L)相当于14.89mg的C7H8ClN3O4S2。
试剂: 1. 水(新沸放置至室温) 2. 甲醇钠滴定液(0.1mol/L) 3. 偶氮紫指示液 4. 无水甲醇 5.基准苯甲酸 6. 二甲基甲酰胺仪器设备:试样制备: 1. 甲醇钠滴定液(0.1mol/L)配制:取无水甲醇(含水量0.2%以下)150mL,置于冰水冷却的容器中,分次加入新切的金属钠2.5g,使完全溶解后,加无水苯(含水量0.02%以下)适量,使成1000mL,摇匀。
缬沙坦氢氯噻嗪片有关物质测定方法研究

定缬 沙坦 氢氯噻嗪 片的有 关物质 。
关 键 词 : 沙 坦 氢 氯噻 嗪 片 ; 关 物 质 ; 校 正 因子 的主 成 分 对 照 法 缬 有 加 中图 分 类 号 : 9 7 1 文 献 标 识 码 : 文章 编 号 :6 2—7 3 2 1 ) 4—0 1 0 R2.1 A 17 7 8(0 2 O 2 4— 3
0 9 9 9 T e l e rr n e o as ra a . 1~9 7 g・mL~ , . 9 . h i a a g fv l t n w s0 8 n a .2 r=0. 9 . n l s o T i t o s c n e i n , c 9 9 9 Co cu i n h s meh d wa o v n e t a — c r t o h ee i ain o lt d s b tn e n Va s r n Hy r c lr t izd a l t. u a e frt e d t r n t fr ae u sa c s i la t d o ho o ha ie T b es m o e a Ke r s Vas r n Hy r c lr t izd a lt ; l td s b tn e ; i o o e t ef o a ewi ai r t n fc y wo d : lat d o h o oh a i e T b es Reae u sa c s Ma n c mp n n l —c mp t c l ai a — a s r h b o
氢氯噻嗪杂质汇总
5784-45-2
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
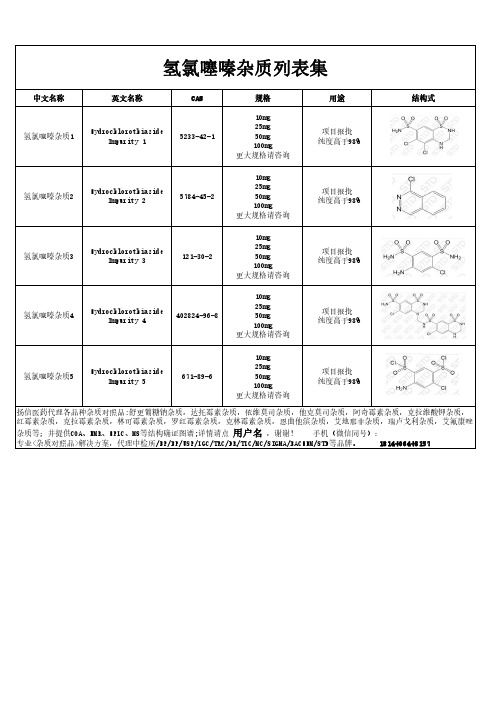
氢氯噻嗪杂质3
Hydrochlorothiazide Impurity 3
121-30-2
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
氢氯噻嗪杂质4
Hydrochlorothiazide
氢氯噻嗪杂质列表集
中文名称
英文名称
CAS
氢氯噻嗪杂质1
Hydrochlorothiazide Impurity 1
5233-42-1
规格
10mg 25mg 50mg 100mg 更大规格请咨询
用途
项目报批 纯度高于98%
结构式
氢氯噻嗪杂质2
Hydrochlorothiazide Impurity 2
Impurity 4
402824பைடு நூலகம்96-8
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
氢氯噻嗪杂质5
Hydrochlorothiazide Impurity 5
671-89-6
10mg 25mg 50mg 100mg 更大规格请咨询
项目报批 纯度高于98%
扬信医药代理各品种杂质对照品:舒更葡糖钠杂质,达托霉素杂质,依维莫司杂质,他克莫司杂质,阿奇霉素杂质,克拉维酸钾杂质, 红霉素杂质,克拉霉素杂质,林可霉素杂质,罗红霉素杂质,克林霉素杂质,恩曲他滨杂质,艾地那非杂质,瑞卢戈利杂质,艾氟康唑
杂质等;并提供COA、NMR、HPLC、MS等结构确证图谱;详情请点 用户名 ,谢谢! 手机(微信同号):
专业<杂质对照品>解决方案,代理中检所/EP/BP/USP/LGC/TRC/DR/TLC/MC/SIGMA/BACHEM/STD等品牌。 1814+064+3157
氢氯噻嗪

氢氯噻嗪编辑氢氯噻嗪为利尿药、抗高血压药。
主要适用于心原性水肿、肝原性水肿和肾性水肿:如肾病综合征、急性肾小球肾炎、慢性肾功能衰竭以及肾上腺皮质激素与雌激素过多引起的水肿;高血压;尿崩症。
长期应用时宜适当补充钾盐。
1药品概述中文名称:氢氯噻嗪化学名:6-氯-3,4-二氢-2H-1,2,4-苯并噻二嗪-7-磺酰胺-1,1-二氧化物拼音名:qīng lǜ saì qín英文名:HYDROCHLOROTHIAZIDECAS No.:58-93-5 结构式:分子式:C7H8ClN3O4S2分子量:297.74规格:⑪10mg ⑫25mg别名:双氢氯噻嗪,双氢克尿塞,双氢氯消疾,DCT(DHCT),噢列特(Oretic),Richlyn,Dichlotride,Esidrix,Hydrodiuril。
类别:利尿药、抗高血压药。
剂量:口服,一次25~100mg。
制剂:①片剂:25mg、50mg、100mg。
②溶液剂:50mg/5ml。
性状:该品为白色结晶性粉末;无臭,味微苦。
该品在丙酮中溶解,在乙醇中微溶,在水、氯仿或乙醚中不溶;在氢氧化钠溶液中溶解。
熔点:该品的熔点为265~273℃,熔融时同时分解。
2安全术语S22:Do not inhale dust.;S24/25:Avoid contact with skin and eyes.;3药物分析氢氯噻嗪方法名称:氢氯噻嗪的测定—中和滴定法应用范围:该方法采用滴定法测定氢氯噻嗪的含量。
该方法适用于氢氯噻嗪的含量测定。
方法原理:供试品加二甲基甲酰胺溶解后,加偶氮紫指示液,在氮气流中,用甲醇钠滴定液(0.1mol/L)滴定至溶液恰显蓝色。
读出甲醇钠滴定液使用量,并将滴定结果用空白试验校正。
试剂:⒈水(新沸放置至室温)⒉甲醇钠滴定液(0.1mol/L)⒊偶氮紫指示液⒋无水甲醇⒌基准苯甲酸⒍二甲基甲酰胺仪器设备:试样制备:⒈甲醇钠滴定液(0.1mol/L)配制:取无水甲醇(含水量0.2%以下)150mL,置于冰水冷却的容器中,分次加入新切的金属钠 2.5g,使完全溶解后,加无水苯(含水量0.02%以下)适量,使成1000mL,摇匀。
