立体化学PPT课件
合集下载
有机化学第三章立体化学

一、 含两个取代不同手性碳原子的对映异构
HO Cl COOH H H COOH ( I ) (2R,3R)
2-羟基-3-氯丁二酸总共有几种立体异构体?
COOH H HO Cl H COOH (I) (2R,3R)
COOH H OH H Cl COOH I) (I (2S,3S)
COOH H HO H Cl COOH I I) (I (2R,3S)
COOH C H CH3 镜象
分子式和构造相同:
C3H6O3
CH3CHCOOH OH
Locating a Stereocenter (Chiral Carbon)
标出手性碳
H N
*
CH 2 CH 2
CH 3
毒芹碱
判断下列化合物是否有手性碳? 是否是手性分子?
有两个手性碳却不是手性分子!
含一个手性碳原子的分子一定是个手性分子。 含多个手性碳原子的分子不一定是个手性分子.
标记: H
OH CH3 (a)
C
根据次序规则:OH>COOH>CH3>H
直接从Fischer投影式判断R/S构型
概括地说:“横变竖不变”
补充:各构型式间转换: (1)透视式或纽曼投影式改写成费歇尔投影式时,先把交叉式构象 旋转成重叠式构象,然后按投影要求写出相应的费歇尔投影式。 (2)判断每一个手性碳的R,S构型。
有旋光性的必要条件。
对映异构体
--互为实物与镜象的两个构型异构体.又称对 映体。它们构造相同。互相对映却不能叠合。
COOH H3C OH H 实物 C HO 镜子
COOH C CH3 H 镜象
乳酸分子的一对对映体
不对称碳原子
——与四个不同的原子或原子团相连的碳原子。 用“ * ”号标出。又叫手性碳。 例 手性碳
HO Cl COOH H H COOH ( I ) (2R,3R)
2-羟基-3-氯丁二酸总共有几种立体异构体?
COOH H HO Cl H COOH (I) (2R,3R)
COOH H OH H Cl COOH I) (I (2S,3S)
COOH H HO H Cl COOH I I) (I (2R,3S)
COOH C H CH3 镜象
分子式和构造相同:
C3H6O3
CH3CHCOOH OH
Locating a Stereocenter (Chiral Carbon)
标出手性碳
H N
*
CH 2 CH 2
CH 3
毒芹碱
判断下列化合物是否有手性碳? 是否是手性分子?
有两个手性碳却不是手性分子!
含一个手性碳原子的分子一定是个手性分子。 含多个手性碳原子的分子不一定是个手性分子.
标记: H
OH CH3 (a)
C
根据次序规则:OH>COOH>CH3>H
直接从Fischer投影式判断R/S构型
概括地说:“横变竖不变”
补充:各构型式间转换: (1)透视式或纽曼投影式改写成费歇尔投影式时,先把交叉式构象 旋转成重叠式构象,然后按投影要求写出相应的费歇尔投影式。 (2)判断每一个手性碳的R,S构型。
有旋光性的必要条件。
对映异构体
--互为实物与镜象的两个构型异构体.又称对 映体。它们构造相同。互相对映却不能叠合。
COOH H3C OH H 实物 C HO 镜子
COOH C CH3 H 镜象
乳酸分子的一对对映体
不对称碳原子
——与四个不同的原子或原子团相连的碳原子。 用“ * ”号标出。又叫手性碳。 例 手性碳
《立体化学教学》课件

手性来源
手性主要来源于碳原子的四个单键,使得碳 原子在形成有机分子时,可能形成两种不同 的空间排列方式,从而产生手性。
手性判断
判断一个分子是否具有手性,可以通过查看 其是否具有手性碳原子,即连接四个不同基 团的碳原子。
对映体
01
02
03
对映体定义
对映体是指通过镜面对称 的方式无法重合的两个立 体异构体。
02
它涉及到有机化学、无机化学、 物理化学等多个学科领域,是化 学学科的一个重要分支。
立体化学的重要性
立体化学对于理解分子性质、化学反 应机制以及药物设计等方面具有重要 意义。
通过了解分子的三维结构,可以更好 地理解其物理性质和化学性质,预测 其反应行为,为新材料的开发和药物 的设计提供理论支持。
动态立体化学的应用
动态立体化学在药物设计和合成、催 化剂设计等领域有广泛应用,了解分 子构型的变化有助于优化化学反应过 程和开发新的化学技术。
04
立体化学的教学策略与技巧
利用模型进行立体展示
总结词
通过实物模型展示分子结构,帮助学生理解立体化学的概念。
详细描述
利用分子模型展示分子的三维结构,让学生直观地观察分子中原子在空间中的排列方式。通过对比不同结构的分 子模型,解释立体化学中的概念,如顺反异构、手性等。
旋光性测定的教学案例
总结词
演示旋光性测定的实验操作和数据分析
详细描述
介绍旋光性测定的基本原理和实验操作,包 括旋光仪的构造和工作原理、样品的制备和 测量步骤等。通过具体的旋光性测定实验, 演示实验操作过程和数据分析方法,包括旋 光度的测量、图谱解析和误差分析等。同时 ,强调旋光性测定在化学、生物和医学等领 域的重要应用。
第三章 立体化学

H CH3
CH3
1
H
2
CH3
3
R
(三)螺旋型手性分子
H H
hexahelicene
trans-cyclooctene
(四)其它手性分子
CH3 CO2H
HO2C (CH2)10
Fe
HO2C
H Fe(CO)4
H
CO2H
3-1-4 具有多个手性中心的分子
(一)具有两个手性中心 例:
V U X
R R
V W Z W Z
例1:aspartic acid
in H2O [α] D20= + 4.36o 例2:
CH3 HO2CCH2C CO2H C2H5
[α]
HO2C
* CO2H NH2
[α] D 90 -1.86o =
25 =-5.0 o D 25
(C 16.5g/100ml, CHCl3)
[α] D =-0.7 o (C 10.6g/100ml, CHCl3)
¡ £
NaN3
¡ £
(S)-(+)-乳酸
(S)-(+)-丙氨酸
(三)生物化学方法:类似化合物同酶作用时, 酶进攻具有相同构型的化合物(利用了 酶的反应专一性)。 (四)光学比较法:同系物中,相同构型常具 有相同的旋光方法。 (五)特殊的x-ray晶体衍射方法。
手性化合物都具有光学活性
但是没有光学活性的物质不一定是非手性化合物
3-1-2 光学活性分子的判断
对称平面 (σ):
将分子平均分成互成实物与镜象关系的平面
H2O, NH3, CH4的对称面?
CH3
对称中心 (i):分子中的一个点,由该分子中任一 部分向该中心画出的直线以等距离延长到另一 侧时会遇到相同部分
高等有机化学第三章立体化学

高等有机化学第三章立体化学
contents
目录
• 立体化学基本概念 • 碳原子立体化学 • 手性分子结构与性质 • 立体化学在有机合成中应用 • 立体化学在药物设计中的应用 • 实验方法与技巧
01
立体化学基本概念
立体异构现象
立体异构体
分子式相同,但空间排列不同的化合 物,具有不同的物理和化学性质。
碳原子手性判断
对称面与对称中心
若一个分子中存在一个对称面或对称中心,则该分子不具有旋光性。对称面是指能将分子分为两个互为镜像的部 分的平面;对称中心是指能将分子中任意一点与另一点重合的点。
潜手性与非对映异构体
潜手性是指分子中某些基团可以围绕单键旋转而产生手性的现象。非对映异构体是指具有相同分子式、不同结构 且不能通过旋转操作相互转化的立体异构体。
感谢观看
。
化学性质差异
手性分子在化学反应中可能表 现出不同的反应速率和选择性
。
生物活性差异
许多生物活性物质都是手性的 ,其生物活性与手性密切相关 ,不同手性分子的生物活性可
能存在显著差异。
手性识别与拆分方法
手性识别
通过对手性分子的结构和性质进行分析,确定其手性特征。常见的方法包括X射线晶体学、圆二色光 谱、核磁共振等。
构型与构象
构型
分子中原子或基团在空间中的相 对位置关系,是固定的空间排列
。
构象
由于单键旋转而产生的不同空间排 列,是动态的空间排列。
构型与构象的关系
构型是构象的基础,构象是构型的 动态表现。不同的构型可能产生不 同的构象,而同一构型也可能产生 多种不同的构象。
02
碳原子立体化学
碳原子杂化类型
sp杂化
03
contents
目录
• 立体化学基本概念 • 碳原子立体化学 • 手性分子结构与性质 • 立体化学在有机合成中应用 • 立体化学在药物设计中的应用 • 实验方法与技巧
01
立体化学基本概念
立体异构现象
立体异构体
分子式相同,但空间排列不同的化合 物,具有不同的物理和化学性质。
碳原子手性判断
对称面与对称中心
若一个分子中存在一个对称面或对称中心,则该分子不具有旋光性。对称面是指能将分子分为两个互为镜像的部 分的平面;对称中心是指能将分子中任意一点与另一点重合的点。
潜手性与非对映异构体
潜手性是指分子中某些基团可以围绕单键旋转而产生手性的现象。非对映异构体是指具有相同分子式、不同结构 且不能通过旋转操作相互转化的立体异构体。
感谢观看
。
化学性质差异
手性分子在化学反应中可能表 现出不同的反应速率和选择性
。
生物活性差异
许多生物活性物质都是手性的 ,其生物活性与手性密切相关 ,不同手性分子的生物活性可
能存在显著差异。
手性识别与拆分方法
手性识别
通过对手性分子的结构和性质进行分析,确定其手性特征。常见的方法包括X射线晶体学、圆二色光 谱、核磁共振等。
构型与构象
构型
分子中原子或基团在空间中的相 对位置关系,是固定的空间排列
。
构象
由于单键旋转而产生的不同空间排 列,是动态的空间排列。
构型与构象的关系
构型是构象的基础,构象是构型的 动态表现。不同的构型可能产生不 同的构象,而同一构型也可能产生 多种不同的构象。
02
碳原子立体化学
碳原子杂化类型
sp杂化
03
有机化学Chapter8(立体化学)

—— 设 想 分 子 中 有 一 条 直 线 , 当 分 子 以 此 直 线 为 轴 旋 转 360º /n 后 , 再用一个与此直线垂直的平面进行反映 ( 即作出 镜象),如果得到的镜象与原来的分子完全相同,这条直线就 是交替对称轴. 4
(Ⅰ) 旋转90º 后得(Ⅱ), (Ⅱ)作镜象得(Ⅲ), (Ⅲ)等于(Ⅰ) 有4重交替对称轴的分子
相同,但在空间的排列方式不同。
构象异构 顺反异构
CH3 H C C CH3 H
CH3 H C C H CH3
C异构:本章学习
8.1 手性和对映体 生活中的对映体 (1)-镜象
沙漠胡杨
生活中的 对映体(2) -镜象
左右手互为镜象
桂林风情
镜象与手性Chirality的概念
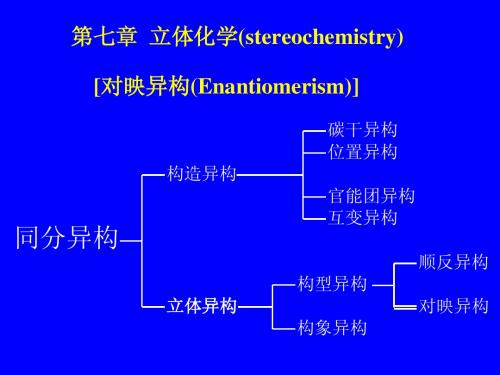
同分异构现象
碳链异构(如:丁烷/异丁烷) 构造异构 官能团异构(如:醚/醇) constitutional 位臵异构(如:辛醇/仲辛醇)
同分异构 isomerism
立体异构 Stereo-
构型异构 configurational 对映非对映异构 构象异构 conformational
顺反,Z、E异构
[α]λ =
t
α ρ l· B
式中t表示温度,λ表示所用光的波长。 若所测的旋光物质为纯液体,只要把ρB换成液体的密
度ρ即可。
比旋光度只决定于物质的结构。
各种化合物的比旋光度是它们各自特有的物理常数.
乳酸
CH3CHCOOH OH
*
右旋体
α ° [ ] 20 D = + 3.8
α ° ] 20 左旋体 [ D = - 3.8
构造异构,分子中原子互相联接的方式和次序
不同而产生的异构现象。
(Ⅰ) 旋转90º 后得(Ⅱ), (Ⅱ)作镜象得(Ⅲ), (Ⅲ)等于(Ⅰ) 有4重交替对称轴的分子
相同,但在空间的排列方式不同。
构象异构 顺反异构
CH3 H C C CH3 H
CH3 H C C H CH3
C异构:本章学习
8.1 手性和对映体 生活中的对映体 (1)-镜象
沙漠胡杨
生活中的 对映体(2) -镜象
左右手互为镜象
桂林风情
镜象与手性Chirality的概念
同分异构现象
碳链异构(如:丁烷/异丁烷) 构造异构 官能团异构(如:醚/醇) constitutional 位臵异构(如:辛醇/仲辛醇)
同分异构 isomerism
立体异构 Stereo-
构型异构 configurational 对映非对映异构 构象异构 conformational
顺反,Z、E异构
[α]λ =
t
α ρ l· B
式中t表示温度,λ表示所用光的波长。 若所测的旋光物质为纯液体,只要把ρB换成液体的密
度ρ即可。
比旋光度只决定于物质的结构。
各种化合物的比旋光度是它们各自特有的物理常数.
乳酸
CH3CHCOOH OH
*
右旋体
α ° [ ] 20 D = + 3.8
α ° ] 20 左旋体 [ D = - 3.8
构造异构,分子中原子互相联接的方式和次序
不同而产生的异构现象。
第七章 立体化学
标出手性碳(Chiral Carbon)
O CH
3
* CH
OH
C
OH
L a c 乳酸 id tic a c
O CH
3
H
CH
3
*
H
HO
C
CH
H N CH CH CH
2
*
2
3
CH
3
毒芹碱(Coniine)
CH
3
O-Acetyl-b-boswellic Acid
H 3C
* *
CH
3
邻乙酰基--乳香酸
CH CH
*
3
*
*
3
H
*
CH
3
*
O
*
*
*
H 3C C O H 3C
*
COOH
有多少个手性碳原子?
应该有11个
对映体
(Enantiomers)
镜面
一对对映体(互为镜像关系)
对映体
C H 2C H 3 C Cl H I
镜面
C H 2C H 3 C Cl H II
H 3C
CH3
二、分子的手性和对称因素
C H 2C H 3 C Cl H I
镜面
C H 2C H 3 C Cl H II
H 3C
CH3
左旋体、右旋体及外消旋体
一对对映体中:使平面偏振光向左旋的称为左旋体, 用“(–)”或“ l‖表示。 使平面偏振光向右旋的称 为右旋体,用“(+)”或“d‖表示。 外消旋体:左旋体与右旋体,旋光度相同、旋光方向 相反。等量的左旋体与右旋体的混合物。无旋光性。 外消旋体用 (±) 或 (RS) 或 (dl) 或 DL表示。
第六章 立体化学

解
Cl
>
CBr3
>
CHCl2 C6H5
>
COCl CH2CH3
>
COOH
>
CONH2
>
CHO
>
CH2OH
>
>
24
A. 三维结构:
(a>b>c>d)
25
OH
C2H5 H CH3
R
方法:站在最小基团d的对面,然后按先后次序观察 其他三个基团。从最大的a经b到c,若是顺时针的, 则为“R”;反之,标记为“S”。(a>b>c>d)
六、环状化合物的立体异构
有两个碳原子各连有一个取代基,就有顺反异构。 如环上有手性碳原子,则有对映异构现象。 环状化合物手性碳原子的判断: 看要考察的碳原子所在的环左右 是否具有对称性,若无对称性则 相当于两个不一样的官能团,则 该碳原子是手性碳原子。如有所 示结构中:
几个*?几 个光学异 构体?
HOOC
HOOC NO2
COOH O 2N
2,2‘-二羧基-6,6’-二硝基联苯分子的一对对映体
基团的阻转能力大小:
I>Br>Cl>CH3>NO2>COOH>NH2>OCH3>OH>F>H
结论:联苯型化合物只要同一苯环上所连的基团不同, 分子就具有手性。
50
指出下列化合物有无光活性
CHO Br (1) CN Br (2) N CH3 H2N N C2H5 C2H5 CH3 HOOC (3) CONH2 CH2 CH
(5)
CH3 CH
CH Cl
(6)
有机化学《立体化学》课件

Van’t Hoff 认为含有不对称碳的分子具有旋光性。
Stereocenter
优点:使用方便 缺点:很多例外
有些分子中存在不对称碳,但却无手性:
H
H
H
H3C Cl
CH3 Cl
H3C Cl
有些分子中没有不对称碳,但却有手性:
A A
Pc
a
b
5.1.3 Symmetric element
C2
C3
C3
H
4
H
H
H3 2H
H
1H
H
H H
H H
H
H H
H
C2
C3
8
C
对称面
:假如有一个平面可以将分子分割成两部分,而其中一部分正好 是另一部分的镜象,这个平面就是分子的对称面。
H
HCH
H
σ
Four planes of symmetric in the molecule
Br H Br H
5.3.1 Molecule with two same asymmetric carbons
5.3.2 Optical activity and conformation 5.3.3 Molecule with two different
充分且必要
1874 Newzealand Van’t Hoff
The carbon atom linking four different groups or atoms is called an “asymmetric carbon”.
不对称碳原子:与四个互不相同 的一价基团相连接的碳原子。
加“ * ”表示
CO OH
Br Cl H
Stereocenter
优点:使用方便 缺点:很多例外
有些分子中存在不对称碳,但却无手性:
H
H
H
H3C Cl
CH3 Cl
H3C Cl
有些分子中没有不对称碳,但却有手性:
A A
Pc
a
b
5.1.3 Symmetric element
C2
C3
C3
H
4
H
H
H3 2H
H
1H
H
H H
H H
H
H H
H
C2
C3
8
C
对称面
:假如有一个平面可以将分子分割成两部分,而其中一部分正好 是另一部分的镜象,这个平面就是分子的对称面。
H
HCH
H
σ
Four planes of symmetric in the molecule
Br H Br H
5.3.1 Molecule with two same asymmetric carbons
5.3.2 Optical activity and conformation 5.3.3 Molecule with two different
充分且必要
1874 Newzealand Van’t Hoff
The carbon atom linking four different groups or atoms is called an “asymmetric carbon”.
不对称碳原子:与四个互不相同 的一价基团相连接的碳原子。
加“ * ”表示
CO OH
Br Cl H
最新第三章立体化学(Stereochemistry)PPT

一、不对称碳、手性碳、 手性分子、对映体
1. 不对称碳:饱和碳原子上连有互不相同的 四个原子或原子团(用*表示)。
2. 手性:物质的分子和它的镜像不能重叠。
3. 手性分子:具有手性的分子。
4. 对映体:互为镜像关系,但不能完全重合 的一对异构体,互为对映体。他们都具有 旋光性。
LIYING
2021/1/20
OH L a c tic a c id 乳酸
第三章立体化学(Stereochemistry)
Locating a Stereocenter
Br
* C3HC2HC2HC2HC2HC C2HC2HC2HC3H
H
LIYING
2021/1/20
第三章立体化学(Stereochemistry)
Locating a Stereocenter
1848年
酒 石 酸 钠 铵 晶
巴斯德
体
LIYING
2021/1/20
Crystals of Sodium Ammonium Tartrate
第三章立体化学(Stereochemistry)
对映体 (Enantisomers)
❖Isomers that are non-superimposable
LIYING
2021/1/20
(+)
表示
[t
cl
右旋, (-) 表示 左旋
:旋光度;[]:比旋光度;t:温 度;:光波长;c:样品浓度,单 位g/ml;l:样品管长度,单位dm
第三章立体化学(Stereochemistry)
第二节 对映异构现象与 分子结构的关系
LIYING
2021/1/20
第三章立体化学(Stereochemistry)
有机化学PPT第五章 立体化学基础课件

凡是连有4个不同的原子或基团的碳原子称为手 性碳原子, 也可称为手性中心。
南京医科大学康达学院化学教研室 有机化学
南京医科大学康达学院 博学至精 明德至善
含有一个手性碳原子的化合物,在空间有2种不同构
型, 它们彼此构成一对对映体。
CH3C* HCOOH
COOH
OH
乳酸
HO C H
CH3
COOH H C OH
CH3
有一个手性碳的化合物必定 是手性化合物,只有一对对映体。
南京医科大学康达学院化学教研室 有机化学
南京医科大学康达学院 博学至精 明德至善
问题:下列化合物哪些含手性碳原子?
1. CH2Cl2
2. CHCl3 3.CH3CHClCH2CH3
4. CH3-CH-CH2CH3 CH2CH3
H
6.
CH3 7.
南京医科大学康达学院化学教研室 有机化学
南京医科大学康达学院 博学至精 明德至善
第一节 手性分子和对映体
一、手 性
观察自己的双手, 左手与右手有什么联系和区别?
南京医科大学康达学院化学教研室 有机化学
南京医科大学康达学院 博学至精 明德至善
左右手互为镜像与实物关系(称为对映关 系),彼此又不能重合的现象称为手性。
H
2 COOH
H3C3 1Cl
H 1OH
2 CH2CH3
3CH3
竖,顺,R南-京型医科大学康达学院化学教横研室,有逆机化,学 R-型
南京医科大学康达学院 博学至精 明德至善
课堂练习:根据Fischer投影式命名。
2
CO2H
H
OH 1
3 CH3 R-(-)-乳酸
HOCH2 3
南京医科大学康达学院化学教研室 有机化学
南京医科大学康达学院 博学至精 明德至善
含有一个手性碳原子的化合物,在空间有2种不同构
型, 它们彼此构成一对对映体。
CH3C* HCOOH
COOH
OH
乳酸
HO C H
CH3
COOH H C OH
CH3
有一个手性碳的化合物必定 是手性化合物,只有一对对映体。
南京医科大学康达学院化学教研室 有机化学
南京医科大学康达学院 博学至精 明德至善
问题:下列化合物哪些含手性碳原子?
1. CH2Cl2
2. CHCl3 3.CH3CHClCH2CH3
4. CH3-CH-CH2CH3 CH2CH3
H
6.
CH3 7.
南京医科大学康达学院化学教研室 有机化学
南京医科大学康达学院 博学至精 明德至善
第一节 手性分子和对映体
一、手 性
观察自己的双手, 左手与右手有什么联系和区别?
南京医科大学康达学院化学教研室 有机化学
南京医科大学康达学院 博学至精 明德至善
左右手互为镜像与实物关系(称为对映关 系),彼此又不能重合的现象称为手性。
H
2 COOH
H3C3 1Cl
H 1OH
2 CH2CH3
3CH3
竖,顺,R南-京型医科大学康达学院化学教横研室,有逆机化,学 R-型
南京医科大学康达学院 博学至精 明德至善
课堂练习:根据Fischer投影式命名。
2
CO2H
H
OH 1
3 CH3 R-(-)-乳酸
HOCH2 3
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
一、分子的对称因素和手性 (3)手性膦、手性氮与手性砜类化合物
一、分子的对称因素和手性
(4)含手性轴的化合物:分子的轴上原子
不是对称的被取代,而使分子具有手性。
一、分子的对称因素和手性
a. 丙二烯衍生物 (具手性轴)
C6H5
C6H5
C CC
a-C10H7
C10H7- a
CH3
CH3
C CC
H
H
反应停事件
O H
N
O
NH
O
O
(S)-thalidomide
O H
N
O
O
O NH
(R)-thalidomide
1984年荷兰药理学家Ariens极力提倡手性药物以单一对 映体上市, 抨击以消旋体形式进行药理研究以及上市。 他的一系列论述的发表,引起药物部门广泛的重视。
1992年,美国食品和医药管理局提出法规,申报手性药 物时,必须对不同对映体的作用叙述清楚。
2001年诺贝尔化学奖授予了3位美日科学家,表彰他们 在手性催化氢化反应和手性催化氧化反应领域所做出的 重大贡献。
目前,研究和发展新的手性技术,借此获得光学纯的手 性药物,已成为许多实验室和医药公司追求的目标。
构造: 分子中各原子间相互结合的顺序(连接顺序) 构型:原子或基团在空间的排列方式 构象:具有一定构型的分子由于单键旋转使分子内的 原子或原子团在空间产生不同的排列。 问题: 二甲基环己烷有多少构造异构体? 1,3-二甲基环己烷是否存在构型异构体? 其中顺式构型是否存在构象异构体?
同分异构
碳架异构
构造异构 官能团异构 位置异构
互变异构
构型异构 顺反异构
立体异构
对映异构
构象异构
立体化学是研究分子中原子或基团在空间的 排列状况,以及不同的排列对分子的物理、化学、 生理性质所产生的影响。
异构现象:
• 立体化学起源于1848年, 法国化学家巴斯德(Pasteur) 将外消旋的酒石酸铵钠的结晶,分离成左旋体和右旋 体,从而发现了对映异构现象。
三、外消旋体
外消旋体(racemic mixture 或racemate): 一对对映体的等量混合物,常用(±)或 dl表示。
外消旋体是否显旋光性?为什么?
• 立体化学是研究化合物分子在三维空间的立体形象与 其物理性质,反应性能以及生理活性之间的关系的科 学。
• 立体化学已成为化学学科的一个重要分支,研究分子 的立体结构与性能之间的关系已成为化学的一项重要 内容。
反应停事件:
20世纪50年代中期,反应停(沙利度胺,Thalidomide) 作为镇静剂,有减轻孕妇清晨呕吐的作用而被广泛应 用。结果在欧洲导致1.2万例胎儿致 残,即海豹婴。 于是1961年该药从市场上撤消。后来发现沙利度胺R 型具有镇静作用,而S型却是致畸的罪魁祸首。研究 人员进一步研究发现沙利度胺任一异构体在体内都能 转变为相应对映体,因此无论是S型还是R型,作为 药物都有致畸作用。
二、旋光性和手性的关系
当偏振光通过一个分子对称的介质时,两种圆偏 振光受到分子的作用相同,以相同的速度通过这种介 质,偏振光原来的偏振面不变,即对称分子无旋光活 性。如果偏振光通过由手性分子组成的介质,则右旋 圆偏振光从右边接近分子,左旋圆偏振光从左边接近 分子,由于分子的不对称性,这两种圆偏振光所遇到 的基团不同,不同基团的极化度不相同,所以两种圆 偏振光的折射率不同,即两种圆偏振光经过手性分子 时所遇到的阻力不同,从而使二者传播的速度不同。
b. 联芳基型化合物(具手性轴)
CH3 H3C
NH2 H2N
一、分子的对称因素和手性
NO2 HOOC
O2N COOH
O2N COOH
联苯型
N2O HOOC
A
A
B C==C==C
B
A
A
C==C==C B
B
丙二烯型
一、分子的对称因素和手性
(5) 手性面分子(分子中无手性中心, 无手性轴)
(CH2)8
一、分子的对称因素和手性
判断分子具有手性的充分必要条件: 分子既没有对称面,没有对称中心,也没有四重 交替对称轴。一般情况下,只要分子中既没有对 称面也没有对称中心,即可判断它是手性分子。
手性分子的几种情况: ⑴分子含有手性中心即不对称碳原子(连接四个 不同取代基的碳原子) ⑵非碳手性中心(Si,N,S,P As以及B等);非碳 原子所形成的不对称四面体(或三角锥体)化合 物也有对映异构现象。
O
O
HOOC
取代对苯二酚双环醚衍生物。
一、分子的对称因素和手性
下列哪些化合物为手性分子
判断下列分子是否有手性:
NO2 HOOC
a
非N手O性2 H分O子OC
CH3
H
b
CCC
H
H
非手性分子
CH3
H
c
CCC
H
CH3
CH3
d
H
含手性轴,手性分子
COOH
C H
手性分子的生物作用
手性分子的立体结构与受体的立体结构(受 体靶位有互补关系时,其活性部位才能进入受 体的靶位,产生应有的生理作用。而一对对映 体只有其中一个适合进入一个特定受体靶位, 产生生理活性。
手性分子与手性生物受体之间的相互作用
例如:
HO
COOH HOOC
OH
H NH2 HO
(+)-多巴 (无生理效应)
H2N H OH
(-)-多巴 (抗帕金森病)
你认为下列阐述中哪些是正确的?哪些是 错误的?为什么?
一对对映体总有实物与镜影关系。 所有手性分子都有非对映体。
所有具有手性碳的化合物都是手性分子。 具有R构型的手性化合物必定有右旋的旋 光方向。
对映异构体:
互为镜象的两种构型异构体。
手性:一个物体若与自身镜象不能叠合, 具有手性。
不能与镜象叠合的分子叫手性分子;手性 分子都具有旋光性。
能与镜象叠合的分子叫非手性分子。 分子的手性是存在对映异构体的必要和充
分条件。
2-1 对映异构 旋光性物质(光活性物质):能使偏
振光旋转的物质。
光学活性的物质总是成对出现,一个 左旋,一个右旋,互为对映体;
如果一个化合物没有对称面,它必然是手 性的。
二、旋光性和手性的关系
CH3
H
OH
H
H3C
HO
H
H
图4-5 乙醇分子对偏振光无净旋光
无旋光性
两个圆偏振光重叠所产生的平面偏振光
二、旋光性和手性的关系
例如,一束平面偏振光在右旋光活性的物 质中传播,其右旋圆偏振光比左旋圆偏振光传 播的速度快,于是在通过这种物质之后,透射 出来的两种圆偏振光重新组合成的平面偏振光 的偏振面就向右旋转了一个角度。
