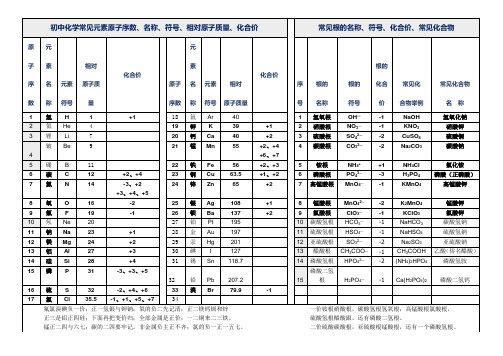
化学必背20种元素和化合价表(中考)
初三常见化合价背诵表
10
氖
Ne
20
27
铂
Pt
195
10
碳酸氢根
HCO3—
-1
NaHCO3
碳酸氢钠
11
钠
Na
23
+1
28
金
Au
197
11
硫酸氢根
HSO4—
-1
NaHSO4
硫酸氢钠
12
镁
Mg
24
+2
29
汞
Hg
201
12
亚硫酸根
SO32—
-2
Na2SO3
亚硫酸钠
13
铝
Al
27
+3
30
碘
I
127
13
醋酸根
CH3COO—
-1
-1、+1、+5、+7
34
氟氯溴碘负一价;正一氢银与钾钠;氧的负二先记清;正二镁钙钡和锌
一价铵根硝酸根,碳酸氢根氢氧根;高锰酸根氯酸根,
正三是铝正四硅;下面再把变价归;全部金属是正价;一二铜来二三铁。
硫酸氢根醋酸跟,还有磷酸二氢根。
锰正二四与六七;碳的二四要牢记。非金属负主正不齐;氯的负一正一五七。
铜
Cu
63.5
+1、+2
6
磷酸根
PO43—
-3
H3PO4
磷酸(正磷酸)
7
氮
N
14
-3、+2
+3、+4、+5
24
锌
Zn
65
+2
7
高锰酸根
MnO4—
-1
常见元素化合价归纳整理

化学根本知识归纳整理一、常见元素化合价口诀与原那么一价氢氯钾钠银二价氧钙镁钡锌三铝四硅五价磷二三铁、二四碳一至五价都有氮铜汞二价最常见正一铜氢钾钠银正二铜镁钙钡锌三铝四硅四六硫二四五氮三五磷一五七氯二三铁二四六七锰为正碳有正四与正二再把负价牢记心。
所有单质中元素化合价为零,化合物中各元素化合价代数和为零。
二、常见原子团的化合价+1价:铵根离子〔NH4+〕;-1价: 氢氧根离子〔OH-〕硝酸根离子〔NO3-〕碳酸氢根离子〔HCO3-〕硫酸氢根离子〔HSO4-〕高猛酸根离子〔MnO4-〕氯酸根离子〔ClO3-〕次氯酸根离子〔ClO-〕醋酸根离子〔CH3COO-〕偏铝酸根离子〔AIO2-〕-2价:碳酸根离子〔CO32-〕硫酸根离子〔SO42-〕亚硫酸根离子〔SO32-)三、常见物质的化学式非金属单质:氢气碳氮气氧气磷硫氯气H2 C N2 O2 P S Cl2金属单质:钠镁铝钾钙铁锌铜钡钨汞Na Mg Al K Ga Fe Zn Cu Ba W Hg常见氧化物:水一氧化碳二氧化碳五氧化二磷氧化钠二氧化氮二氧化硅H2O CO CO2P2O5 Na2O NO2SiO2二氧化硫三氧化硫一氧化氮氧化镁氧化铜氧化钡氧化亚铜SO2 SO3 NO MgO CuO BaO Cu2O 氧化亚铁三氧化二铁〔氧化铁或铁红〕四氧化三铁三氧化二铝三氧化钨FeO Fe2O3 Fe3O4 Al2O3 WO3氧化银氧化铅二氧化锰Ag2O PbO MnO2氯化物/盐酸盐:氯化钾氯化钠(食盐) 氯化镁氯化钙氯化铜氯化锌氯化钡氯化铝KCl NaCl MgCl2CaCl2CuCl2ZnCl2 BaCl2 AlCl3氯化亚铁氯化铁氯化银FeCl2FeCl3 AgCl常见的酸:硫酸盐酸硝酸磷酸硫化氢溴化氢碳酸H2SO4 HCl HNO3 H3PO4 H2S HBr H2CO3常见的盐:硫酸铜硫酸钡硫酸钙硫酸钾硫酸镁硫酸亚铁硫酸铁CuSO4 BaSO 4 CaSO4K2SO4 MgSO4FeSO4 Fe2 (SO4)3硫酸铝硫酸氢钠硫酸氢钾亚硫酸钠硝酸钠硝酸钾硝酸银Al2(SO4)3NaHSO4 KHSO4Na2SO3 NaNO3 KNO3 AgNO3硝酸镁硝酸铜硝酸钙亚硝酸钠碳酸钠碳酸钙碳酸镁Mg(NO3)2 Cu(NO3)2Ca(NO3)2NaNO2 Na2CO3 CaCO3 MgCO3常见的碱: 氢氧化钠氢氧化钙氢氧化钡氢氧化镁氢氧化铜氢氧化钾氢氧化铝NaOH Ca(OH)2 Ba(OH)2 Mg(OH)2Cu(OH)2KOH Al(OH)3氢氧化铁氢氧化亚铁Fe(OH)3 Fe(OH)2常见有机物: 甲烷乙炔甲醇乙醇乙酸 (醋酸)CH4C2H2CH3OH C2H5OH CH3COOH常见结晶水合物:碱式碳酸铜石膏熟石膏明矾Cu2(OH)2CO3 CaSO4•2H2O 2 CaSO4•H2O KAl(SO4)2•12H2O绿矾蓝矾碳酸钠晶体常见化肥: FeSO4•7H2O CuSO4•5H2O Na2CO3•10H2O尿素硝酸铵硫酸铵碳酸氢铵磷酸二氢钾CO(NH2)2NH4NO3(NH4)2SO4 NH4HCO3KH2PO4四、常见物质中重点元素的化合价H: HCl NaH CaH2。
初三化学化合价表

初三化学化合价表化合价是化学中用来表示元素与其他元素结合的能力或价电子数的概念。
它是化学反应和化学方程式中的重要指标之一。
化合价的大小决定了元素与其他元素形成化合物时的电子转移或共用情况,进而影响化合物的性质和稳定性。
化合价表是一张记录元素化合价的表格,它依据元素的电子结构和化学性质,列出了常见元素的化合价范围。
下面我们将逐一介绍常见元素的化合价。
1. 氢(H):氢原子只含有一个电子,其化合价为+1。
2. 氧(O):氧原子含有六个电子,主要倾向于接受两个电子,其化合价为-2。
3. 碳(C):碳原子含有四个电子,主要倾向于共用四个电子,其化合价为+4。
4. 氮(N):氮原子含有七个电子,主要倾向于接受三个电子,其化合价为-3。
5. 硫(S):硫原子含有十六个电子,主要倾向于接受两个电子,其化合价为-2。
6. 氯(Cl):氯原子含有十七个电子,主要倾向于接受一个电子,其化合价为-1。
7. 钠(Na):钠原子含有十一个电子,主要倾向于失去一个电子,其化合价为+1。
8. 铁(Fe):铁原子含有二十六个电子,其化合价可以是+2或+3。
9. 铜(Cu):铜原子含有二十九个电子,其化合价可以是+1或+2。
10. 氟(F):氟原子只含有七个电子,其化合价为-1。
11. 锌(Zn):锌原子含有三十个电子,其化合价为+2。
12. 铝(Al):铝原子含有十三个电子,其化合价可以是+3。
13. 硅(Si):硅原子含有十四个电子,主要倾向于共用四个电子,其化合价为+4。
14. 磷(P):磷原子含有十五个电子,主要倾向于接受三个电子,其化合价为-3。
15. 锰(Mn):锰原子含有二十五个电子,其化合价可以是+2、+4、+7。
以上是初三化学化合价表中常见元素的化合价。
需要注意的是,化合价并不是固定不变的,它受到许多因素的影响,如元素的电子结构、电负性以及化合物的性质等。
因此,在具体的化学反应中,元素的化合价可能会有一定的变化。
初中常见物质化学式与元素化合价

盐酸
HCl
硫酸
H2SO4
硝酸
HNO3
氯离子
Cl-
硫酸根离子
SO4-2
硝酸根离子
NO-
元素化合价
-1
原子团化合价
-2
原子团化合价
-1
氯化钠
NaCl
硫酸钠
Na2SO4
硝酸钠
NaNO3
氯化钾
KCl
硫酸钾
K2SO4
硝酸钾
KNO3
氯化银
AgCl
硫酸银
AgSO4
硝酸银
AgNO3
氯化铵
ClNH4
硫酸铵
NH4SO4
3.常见有机化合物
常见有机化合物
甲烷
CH4
甲醇
CH3OH
葡萄糖
C6H12O6
乙烷
C2H6
乙醇
C2H5OH
果糖
C6H12O6
丙烷
C3H8
丙醇
C3H7OH
麦芽糖
C12H22O11·H2O
丁烷
C4H10
丁醇
C4H9OH
淀粉
C6H12O6n
戎烷
C5H12
戎醇
C5H11OH
…
己烷
C6H14
己醇
C6H13OH
庚烷
硝酸亚铁
FeNO₃₂
氯化铁
FeCl3
硫酸铁
Fe2SO43
硝酸铁
FeNO33
氯化铝
AlCl3
硫酸铝
Al2SO43
硝酸铝
AlNO33
续表
碳酸
H2CO3
氢氧根离子
OH
氢氧化铁
FeOH23
初中常见元素或原子团化合价口诀汇总

初中常见元素或原子团化合价口诀汇总
一、常见元素的主要化合价
化合价口诀一:
氟氯溴碘负一价;正一氢银与钾钠。
氧的负二先记清;正二镁钙钡和锌。
正三是铝正四硅;下面再把变价归。
全部金属是正价;一二铜来二三铁。
非金属有正也有负;碳的二四要牢记。
氮磷负三与正五;不同磷三氮二四。
硫有负二正四六;边记边用就会熟。
化合价口诀二
一价氢氯钾钠银;二价氧钙钡镁锌,
三铝四硅五氮磷;二三铁二四碳,
二四六硫都齐全;铜以二价最常见。
化合价口诀三:
钾钠氢银正一价,钙镁锌钡正二价,
氟氯溴碘负一价,通常氧是负二价,
铜正一二铝正三,铁有正二和正三,
碳有正二和正四,硫有负二正四六。
化合价口诀四:
一价氯氢钾钠银;二价氧镁钙钡锌(~~羊没盖背心);三铝四硅五价磷;二三铁,二四碳;二四六硫应记全。
化合价口诀五:
氢钠钾银正一价,钙钡镁锌正二价,一二铜,二三铁,
二四六硫二四碳,三铝四硅三五磷,变价还有锰氯氮。
化合价口诀六:
一价氯氢钾钠银,二价氧钡钙镁锌,三铝四硅五氮磷,
二三铁,二四碳,二四六硫价齐全,铜汞二价最常见。
化合价要记清,莫忘单质价为零!
二、常见原子团的化合价
化合价口诀一:
一价铵根硝酸根;二价硫酸碳酸根。
暂记铵根为正价;负三有个磷酸根。
化合价口诀二:
负一硝酸氢氧根,负二硫酸碳酸根。
负三记住磷酸根;正一价的是铵根。
初中化学化合价口诀表

初中化学化合价口诀表一、概述化学化合价是指元素在化合物中的价态或化合物中各元素的正、负电荷的比例关系。
初中化学中,我们需要掌握一些常见元素的化合价,能够通过化合价口诀来快速准确地确定元素的化合价。
本文将介绍常见元素的化合价口诀表,供初中化学学习者参考。
二、主要元素的化合价1. 碱金属元素(IA族元素)•氢(H):氢化物(H-)中氢的化合价为-1。
•钾(K)、钠(Na):一价阳离子,其化合价为+1。
2. 碱土金属元素(IIA族元素)•铍(Be):二价阳离子,其化合价为+2。
•镁(Mg):二价阳离子,其化合价为+2。
3. 铜、银、金(IB、IIB、VIB族元素)•铜(Cu):由于具有两种化合价态,可根据具体情况确定。
–铜在阳离子中的化合价为+2。
–铜在氧化物中的化合价为+1。
•银(Ag)、金(Au):由于只有一种化合价态,其化合价分别为+1。
4. 卤素元素(VIIA族元素)•氟(F):一种化合价态,其化合价为-1。
•氯(Cl)、溴(Br)、碘(I):均为一价阴离子,其化合价为-1。
5. 第16、17、18族元素•氧(O):一种化合价态,其化合价为-2。
•硫(S):根据实际情况可有多种化合价态,一般为2、4、6。
•氮(N):根据实际情况可有多种化合价态,一般为-3、+3、+5。
6. 第1、2、13、14族元素•氢(H):正离子时,氢的化合价为+1。
•碳(C)、硅(Si):根据实际情况可有多种化合价态。
三、化合价口诀表化合价口诀表是帮助我们记忆元素化合价的一种方法。
下面是常见元素的化合价口诀表:1.氢除负一,银金加一。
2.氧氟氯溴碘,氧负二级加一线。
3.金银铜铁,只有单一态。
4.碱土金属被二抹,除铬锌盖球袋。
5.氨氮亏三只脚,邦硅磷锡老大巧。
6.钙锶镭四两铺,吃饭就来氧边走。
通过这些简洁的句子,我们可以快速记忆常见元素的化合价,辅助我们在化学计算和化学式写法中省去繁琐的查阅过程。
四、小结初中化学化合价口诀表是学习初中化学中化合价的有效辅助工具之一。
中考化学元素周期表必背内容

中考化学元素周期表必背内容化学元素周期表是我们学习化学的重要工具,对于中考的同学们来说,掌握其中的一些关键内容是非常必要的。
首先,我们要了解元素周期表的基本结构。
元素周期表是按照元素的原子序数递增的顺序排列的。
横行称为周期,纵行称为族。
原子序数等于核电荷数等于质子数等于核外电子数。
这是一个非常重要的概念,同学们一定要牢记。
在元素周期表中,前20 号元素是必须要熟练背诵的。
它们分别是:氢(H)、氦(He)、锂(Li)、铍(Be)、硼(B)、碳(C)、氮(N)、氧(O)、氟(F)、氖(Ne)、钠(Na)、镁(Mg)、铝(Al)、硅(Si)、磷(P)、硫(S)、氯(Cl)、氩(Ar)、钾(K)、钙(Ca)。
我们可以通过一些口诀来帮助记忆,比如“氢氦锂铍硼,碳氮氧氟氖,钠镁铝硅磷,硫氯氩钾钙”。
接下来,让我们分别了解一下这些元素的一些基本性质。
氢元素是宇宙中最常见的元素之一,通常以单质氢气(H₂)的形式存在。
氢气具有可燃性,在空气中燃烧生成水。
氦元素是一种惰性气体,化学性质非常稳定。
锂是一种银白色的金属,在电池制造中有着重要的应用。
铍是一种硬度较高的金属。
硼在自然界中通常以化合物的形式存在。
碳元素是构成有机物的基础,有多种同素异形体,如金刚石、石墨和 C₆₀等。
氮元素在空气中含量最多,氮气(N₂)化学性质稳定,但在一定条件下可以和其他物质发生反应。
氧元素是维持生命活动必不可少的,氧气(O₂)支持燃烧和呼吸。
氟是最活泼的非金属元素之一,氟气具有很强的氧化性。
氖也是一种惰性气体,常用于霓虹灯。
钠是一种活泼的金属,与水剧烈反应生成氢氧化钠和氢气。
镁在空气中燃烧会发出耀眼的白光。
铝具有良好的延展性和导电性。
硅是半导体材料的重要组成部分。
磷有白磷和红磷两种常见的同素异形体。
硫在空气中燃烧产生淡蓝色火焰。
氯是一种黄绿色的气体,具有强氧化性。
氩是惰性气体,一般不参与化学反应。
钾是一种活泼的金属,与水反应比钠更剧烈。
钙在人体骨骼和牙齿中含量较多。
化学中化合价口诀

化学中化合价口诀
初中常用1:
一价氯氢钾钠银
二价氧钙钡镁锌
三铝四硅三五磷
二三铁,二四碳
二四六硫要记全
铜汞二价最常见
锰有二四六七价
常用元素铭记心
一价氢氧铵原子团二硫碳根
初中常用2:
一价氯氢钾钠银
二价氧镁钙钡锌
亚铁二铝铁三
铜汞二价最常见
一价氢氧硝酸根
二价硫酸碳酸根
只有正一是铵根
初中的3
一价钾钠氯氢银(氯是负一价)
二价钙镁氧钡锌(氧是负二价)
三铝四硅五氮磷
二三铁二四碳
二四六硫要记清
铜汞二价最常见
锰有四价二四六七
负一还有氟溴碘
4
一价氯氢钾钠银
二价氧钙钡镁锌
三铝四硅三五磷
二三铁,二四碳
二四六硫要记全
铜汞二价最常见
锰有二四六七价
常用元素铭记心
一价氢氧铵原子团二硫碳根
5.
我的不用记正负价
一价钾钠氯银,
二价钡镁钙锌,
三铝四硅五价磷,
六硫七锰八为零,
一铜二铁加亚名,
单质为零,
氢正一,氧负二,
氢氧优先,不变价优先,
遇正必负。
绝对有效,分给我吧,我也在学,用了这个口诀很轻松,轻松上98。
