异丙醇—环己烷双液系相图
异丙醇-环己烷双液系相图

渤海大学学生实验报告课程名称:任课教师:实验室名称:物理化学实验室(二)房间号实验时间: 2013 年月日学院化学化工与食品安全学院专业班级姓名学号同组人实验项目异丙醇-环己烷双液系相图组别实验成绩一、实验目的1、了解物理化学实验中常用的物理方法-光学方法的基本原理2、绘制异丙醇-环己烷双液系的沸点-组成图,确定其沸点组成及衡沸温度3、进一步理解分馏原理4、掌握阿贝折射计的原理及使用方法二、实验原理在常温下两种液态以任意比例相互溶解所组成的体系称之为完全互溶双液系。
在恒定压力下,表示溶液沸点与组成关系的图称之为沸点-组成图。
本实验利用回流及分析的方法来绘制相图。
取不同组成的溶液在沸点仪中回流,测定其沸点及其气液组成。
沸点数据可由温度计获得,气-液相组成可通过测其折射率,然后由组成-折射率曲线中最后确定。
三、仪器与试剂沸点测定仪阿贝折射仪吸液管调压变压器温度计移液管(1ml 10ml 25ml) 异丙醇环己烷四、实验装置渤海大学实验报告用纸(第页共页)五、实验步骤1.已知浓度溶液折射率的测定取异丙醇和环己烷以及环己烷摩尔分数分别为0.2、0.4、0.6、0.8四种组成的溶液在25℃下,逐次用阿贝折射计测定其折射率,绘制组成-折射率的关系曲线;2,溶液沸点及气液组成的测定(1)取25ml异丙醇于沸点测定仪之蒸馏瓶内,连好路线,打开回流冷却水,接通电源加热至沸腾。
待温度恒定后,记下温度将调压变压器调至零处,停止加热充分冷却后取样,用阿贝折射计分别测定气相和液相冷凝液的折射率,按上述步骤分别测各液体的沸点及气相冷凝液和液相折射率;(2)将蒸馏瓶内的溶液倒入回馏瓶中,并用环己烷清洗蒸馏瓶,然后取25ml环己烷于蒸馏瓶内,按(1)的操作步骤进行,以后分别加入异丙醇0.2ml,0.3ml,0.5ml,1ml,4ml,5ml,测定其沸点及气相冷凝液和液相折射率。
六、数据记录和处理大气压:大气压:101.56kpa; 压力校正因素:溶液沸点与大气压有关沸点校正:△t=t/10 *(101.325-p)/101.325 tb=t+△t编号项目1 2 3 4 5 6 7 8t0c 66.4 64.6 63.9 64.1 64.3 64.6 65.7 71.6气相ny1 1.4029 1.4027 1.4012 1.4005 1.3995 1.3988 1.3962 1.38422 1.4027 1.4028 1.4010 1.4007 1.3994 1.3987 1.3964 1.3843平均 1.4028 1.4027.5 1.4011 1.4006 1.39945 1.39875 1.3963 1.38425xg41.4 42.2 45.0 45.8 47.9 49.6 61.4 69.0液相nx1 1.4212 1.4191 1.4119 1.4106 1.3891 1.3831 1.3751 1.36372 1.4211 1.4190 1.4120 1.4108 1.3890 1.3832 1.3750 1.3635平均 1.42115 1.41905 1.41195 1.4007 1.38905 1.38315 1.37505 1.3636xl5.8 10.0 25.0 46.1 63.8 70.4 80.0 94.8 △t -0.0154 -0.0150 -0.0148 -0.0149 -0.0149 -0.0150 -0.0152 -0.0166tb66.3846 64.585 63.8852 64.0851 64.2851 64.585 65.6848 71.5834恒沸温度校正前63.95 后63.94 恒沸组成xg = xl=45.7渤海大学实验报告用纸(第页共页)七结果讨论与分析1.产生误差的原因:a.温度计的水银球应一半在液体中,一半在气相中,以确保气液达平衡,否则将影响实验结果。
2-双液系相图

3、实验步骤
1.已知浓度溶液折射率的测定 .
取异丙醇和环己烷以及环己烷摩尔 分数分别23.31%、45.85%、58.94%、 、 分数分别 、 、 74.80%四种组成的溶液,逐次用阿贝 四种组成的溶液, 四种组成的溶液 折射计测定其折射率。 折射计测定其折射率。 绘制组成一折射率的关系曲线 组成一折射率的关系曲线。 绘制组成一折射率的关系曲线。
2、基本原理
两种液态物质混合而成的二组分体系称为双液系 液体的蒸气压与外界压力相等时的温度—沸点 一定压力下,双液系的沸点与组成的T-x相图一般 有下列三种情况
完全互溶的双液系的沸点完全互溶的双液系的沸点-组成图
利用回流及分析的方法来绘制相图。 利用回流及分析的方法来绘制相图。取不同组成 的溶液在沸点仪中回流,测定其沸点及气、 的溶液在沸点仪中回流,测定其沸点及气、液相组 成。沸点数据可直接由温度计获得; 沸点数据可直接由温度计获得 数据可直接由温度计获得; 气、液相组成可通过测其折射率,然后由组成—— 折射率曲线中最后确定。 。
电阻丝不能露出液面,一定要浸没于溶液中,以 免通电红热后引起有机溶剂燃烧。电阻丝两端电 压不能过大,过大会引起有机溶剂燃烧或烧断电 阻丝。 测量过程中一定要达到气液平衡状态,即体系的 温度保持稳定,才能测定其沸点及气相冷凝液和 液相的折射率。
在测定其气相冷凝液和液相的折射率时要保持 温度一致。 使用阿贝折射仪 阿贝折射仪时,棱镜上不能接触硬物,擦 拭棱镜时需用擦镜纸等柔软的纸。 测定折射率时,动作要迅速,避免样品中易 挥发组分的损失
4. 数据记录和处理
1、绘制 ℃时的组成 、绘制25℃ 一折射率关系曲线 标准曲线) (标准曲线) 2、沸点值进行校正。假定 、沸点值进行校正。 特鲁顿( 特鲁顿(Trouton)规则适 ) 用于溶液井应用克劳修斯 一克拉贝龙方程则有
异丙醇-环己烷双液系相图

校园 一角
实验一 自制植物酸碱指示剂
指导教师 张婷
实验一自制植物酸碱指示剂
一 实验目的
1.了解指示剂的指示原理、指示剂的种 类以及有关指示剂选择的方法。
六 拓展资料
大多数植物花卉的色素,都能在酸溶液和碱溶液中 有显著的变色现象,所以一般可以用来作为酸碱指示剂。 特别是带红色、紫色的鲜花,如红玫瑰、状元红、一串 红等花的色素,对酸碱指示剂的效果特别最好。
大多数色花经揉烂后用水浸取即可,仅有个别色花 (如一串红、天竹葵、指甲花等)要用酒精、食盐水浸 取;大多数植物色素用冷水浸取即可,象旱菜则要加少 量食盐在沸水中浸取;大多数浸取液在空气中放置,部 分有色成分会被空气氧化,色泽会明显减褪,但对酸碱 的指示效果仍很理想;少数浸取液,如旱菜汁在空气中 却相当稳定,存放十天半个月,也不见色泽减褪。
旱菜、红玫瑰、 胭脂萝卜、95% 酒精溶液、稀 盐酸、稀NaOH 溶液
四 实验步骤
1.从胭脂萝卜中提取酸碱指示剂 将胭脂萝卜切碎后放到研钵中捣烂,再加入少量的蒸
馏水(或者纯净水),并玻璃棒搅动,浸出色素。几分 钟后,用纱布滤出色汁。在三支试管中分别滴入3ml稀盐 酸、稀NaOH溶液、蒸馏水,然后分别滴入3滴胭脂萝卜 色素的提取液,观察现象。
四 实验步骤
2.从旱菜中提取酸碱指示剂 取100克旱菜,洗净后切碎,放到烧杯中,加水浸没1
/2菜叶,并加入少量食盐,加热煮沸8分钟,并不断搅拌 菜叶,把煮后的旱菜菜汁滤入一只小烧杯中。在在三支试 管中分别滴入3ml稀盐酸、稀NaOH溶液、蒸馏水,然后 分别滴入3滴旱菜菜汁滤液,观察现象。
实验四异丙醇—环己烷双液系相

可编辑ppt
10
• 3.在测定其气相冷凝液和液相的折射率时 要保持温度一致。
• 4.使用阿贝折射仪时,棱镜上不能接触硬 物,擦拭棱镜时需用擦镜纸等柔软的纸。
可编辑ppt
11
阿贝折射仪的使用
1.阿贝折射仪 的构造原理
可编辑ppt
12
• 2.阿贝折射仪的使用方法 • (1)仪器安装: • (2)加样:顺单一方向轻擦镜面 (不可来回擦) • (3)调光明暗的界面恰好同十字线交叉处重合 • (4)读数 折射率 • 0~95% 糖溶液的百分数
分别测定气相冷凝液和液相的折射
率。按上述操作步骤分别测定加人
环已烷为1ml、 2ml、3ml、4ml、
5ml 、 10ml 时 各 液 体 的 沸 点 及 气 相
冷凝液和液相折射率。
可编辑ppt
6
(2)将蒸馏瓶内的溶液倒 人回收瓶中,并用环已烷 清洗蒸馏瓶。然后取25ml
环己烷注入蒸馏瓶内,按 (1)的操作步骤进行。以 后分别加人异丙醇0.2ml、 0.3ml、0.5ml、1.0ml、 4ml、5ml,测定其沸点及 气相冷凝液和液相折射率。
可编辑ppt
3
为了绘制沸点—组成图,可采取不同的方 法。比如取该体系不同组成的溶液,用化学分 析方法分析沸腾时该组成的气、液组成,从而 绘制出完整的相图。在本实验中的折射率的测 定,就是一种间接获取组成的办法。它具有简 捷、准确的特点。
本实验就是利用回流及分析的方法来绘制 相图。取不同组成的溶液在沸点仪中回流,测 定其沸点及气、液相组成。沸点数据可直接由 温度计获得;气、液相组成可通过测其折射率, 然后由组成—折射率曲线中最后确定。
实验四、 异丙醇—环己烷 双液系相图
可编辑ppt
环己烷-异丙醇双液系相图的绘制

宜宾学院 化学与化工学院
实验中心
实验目的
1 .了解物理化学实验手段中常用的物理方法— —光学方法的基本原理; 2.绘制异丙醇一环己烷双液系的气-液平衡相图, 了解相图和相律的基本概念; 3.进一步理解分馏原理; 4. 掌握测定双组分液体的沸点及正常沸点的方 法; 5.掌握阿贝折射计的原理及使用方法。
操作步骤
1.已知浓度溶液折 射率的测定(略)
取异丙醇和环己烷以 及环己烷摩尔分数分 别 23.31% 、 45.85% 、 58.94% 、 74.80% 四种 组成的溶液,逐次用 阿贝折射仪测定其折 射率。绘制组成一折 射率的关系曲线。
沸点仪结构图
2.溶液沸点及气、液相组成的测定
(1)取25mL异丙醇置于沸点测定仪之蒸馏瓶内。按图连 接好线路,打开回流冷却水,通电并调节变压器使液体加 热至沸腾,回流并观察温度计的变化,待温度恒定记下沸 腾温度。然后将调压变压器调至零处。停止加热,充分冷 却后,用吸液管分别从冷凝管上端的分馏液取样口及加液 口取样,用阿贝折射计分别测定气相冷凝液和液相的折射 率。按上述操作步骤分别测定加人环已烷为2mL、3mL、 4mL、5mL、10mL时各液体的沸点及气相冷凝液和液相折 射率。 (2)将蒸馏瓶内的溶液倒人回收瓶中,并用环已烷清洗蒸 馏瓶。然后取25mL环己烷注入蒸馏瓶内,按(1)的操作 步骤进行。以后分别加人异丙醇0.3mL、0.5mL、1.mL、 4mL、5mL,测定其沸点及气相冷凝液和液相折射率。
数据记录和处理
1、绘制环己烷-异 丙醇体系的组成一 折射率关系曲线 (工作曲线)略
1.44 1.43 1.42 1.41 1.4
1.39
1.38
异丙醇-环己烷双液系相图 - 烟台大学—环境与材料工程学院

二组分合金系统相图的绘制
杜伟
一 实验目的
1. 用热分析步冷曲线法绘制铋-镉二组分金属 相图 2. 掌握热分析法的测量技术 3.了解纯物质的步冷曲线和混合物的步冷曲 线的形状有何不同,其相变点的温度应如何 确定。
二 基本要求
(1)学会用热分析法测绘Bi-Cd二组 分金属相图。
(2)了解热电偶测量温度和进行热电 偶校正的方法。
三 实验原理
用几何图形来表示多相平衡体系中有哪些相、 各相的成分如何,不同相的相对量是多少,以及它 们随浓度、温度、压力等变量变化的关系图,叫相 图。 绘制相图的方法很多,其中之一叫热分析法。 在定压下把体系从高温逐渐冷却,作温度对时间变 化曲线,即步冷曲线。体系若有相变,必然伴随有 热效应,即在其步冷曲线中会出现转折点。从步冷 曲线有无转折点就可以知道有无相变。测定一系列 组成不同样品的步冷曲线,从步冷曲线上找出各相 应体系发生相变的温度,就可绘制出被测体系的相 图。
五 实验步骤
图3 步冷曲线测量装置 1.加热炉 2.不锈钢管 3.套管 4.热电偶
六、 注意事项
1.用电炉加热样品时,温度要适当,温度过高样 品易氧化变质;温度过低或加热时间不够则样品 没有完全熔化,步冷曲线转折点测不出。 2.热电偶热端插到样品中心部位,管内注入少量 的石腊油,热电偶浸入油中。搅拌时注意勿使热 端离开样品,金属熔化后常使热电偶套管浮起, 这些因素都会导致测温点变动。
当熔融体系在均匀冷却过程中无相变时,温 度将连续均匀下降得一平滑的步冷曲线;当体系 内发生相变则因体系产生的相变热与自然冷却时 体系放出的热量相抵消,步冷曲线就会出现转折 或水平线段,转折点对应的温度,为该组成体系 的相变温度。利用步冷曲线所得到的一系列组成 和所对应的相变温度数据,以横轴表示混合物的 组成,纵轴上标出开始出现相变的温度,把这些 点连起来,就可绘出相图。二元简单低共熔体系 的冷却曲线具有如下图所示的形状
实验 异丙醇—环己烷双液系相图

实验 异丙醇—环己烷双液系相图一、实验目的1.了解物理化学实验手段中常用的物理方法——光学方法的基本原理。
2. 绘制异丙醇-环己烷双液系的沸点-组成图,确定其恒沸物组成及恒沸温度。
3. 进一步理解分馏原理。
4. 掌握阿贝折射计的原理及使用方法。
二、实验背景根据相律绘制相图,通过相图的分析加深对所研究体系的认识,是热力学方法研究多相平衡体系的重要内容之一。
相平衡是物理化学的重要教学内容,其中气液平衡是最常见,也是讨论最多的内容之一。
各体系相图的绘制为生产和科研实践中对某些液体混合物的分离、提纯与精制、蒸馏、精馏等具有一定的指导意义。
完全互溶双液系的T-x图,按曲线的特征,体系可以分为三大类,理想体系,正偏差体系和负偏差体系。
其中,当偏差足够大时,会出现极大点和极小点,分别对应最大负偏差和最大正偏差,对应的极值点称为恒沸点,所对应的溶液称为恒沸混合物。
考虑综合因素,一般实验都选择具有最低恒沸点的异丙醇—环己烷或乙醇—环己烷体系,本实验选异丙醇—环己烷体系。
根据相平衡原理,对二组分体系,当压力恒定时,当气液两相平衡时,体系的自由度为1。
当体系的温度确定时,气液两相的组成也确定。
反过来,当气液两相的组成确定时,体系的平衡温度也确定。
沸点仪就是根据这个原理设计的。
本实验中气液相的组成通过测定对应样品的折射率来确定,因而两组分的折射率相差越大越好,同时为了避免组分因挥发而造成测量误差,还要求两组分的饱和蒸汽压相差越小越好。
目前实验教学中最常用的沸点仪如图8-2所示,结构简单,容易操作,但达到平衡时间较长。
另外一类型测定装置叫平衡釜,有陆志虞平衡釜、爱立斯平衡釜、罗斯平衡釜等,平衡釜结构比较复杂。
还有一种多功能沸点测定仪,具有沸点测定仪和平衡釜的双重功能,测定范围较广,除常规的气液平衡数据的测定外,还可用于含盐体系和部分互溶体系气液平衡的测定。
三、实验原理在常温下,任意两种液体混合组成的体系称为双液体系。
若两液体能按任意比例相互溶解,则称完全互溶双液体系;若只能部分互溶,则称部分互溶双液体系。
异丙醇-环己烷气液平衡相图
实验七 异丙醇-环己烷气液平衡相图一、实验目的1. 了解绘制双液系相图的基本原理和方法;2. 采用回流冷凝法测定不同浓度的异丙醇-环己烷体系的沸点和气液两相平衡成分,绘制常压下环己烷-异丙醇双液系的T-x图,并找出恒沸点混合物的组成和最低恒沸点;3.学会使用阿贝折射仪。
二、实验原理 在常温下,任意两种液体混合组成的体系称为双液体系。
若两液体能按任意比例相互溶解,则称完全互溶双液体系;若只能部分互溶,则称部分互溶双液体系。
液体的沸点是指液体的蒸气压与外界大气压相等时的温度。
在一定的外压下,纯液体有确定的沸点。
而双液体系的沸点不仅与外压有关,还与双液体系的组成有关。
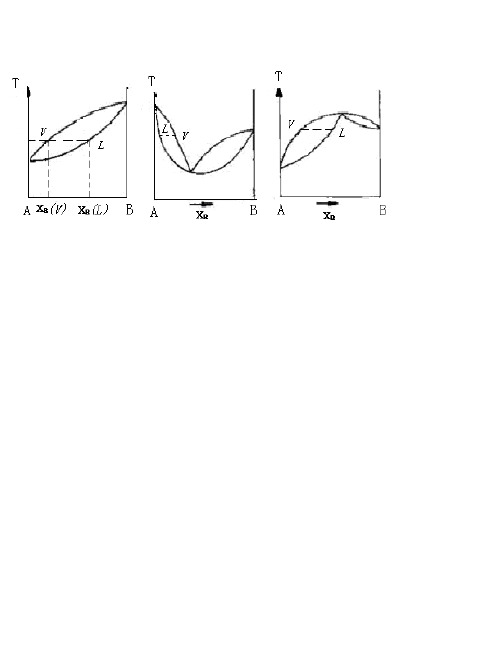
图17-1(a)是一种最简单的完全互溶双液系的T-x图(像苯与甲苯)。
图中纵轴是温度(沸点)T,横轴是液体B的摩尔分数xb (或质量百分组成),上面一条是气相线,下面一条是液相线,对应于同一沸点温度的二曲线上的两个点,就是互相成平衡的气相点和液相点,其相应的组成可从横轴上获得。
因此如果在恒压下将溶液蒸馏,测定气相馏出液和液相蒸馏液的组成就能绘出T-x图。
某些完全互溶的双液体系近似遵循拉乌尔定律,其正(或负)偏差不大,在T-x图上溶液的沸点介于A、B二纯液体的沸点之间(见图17-1(a)),如甲醇与水、二硫化碳与四氯化碳等。
大多数实际溶液由于A、B二组分的相互影响,常会与拉乌尔定律有较大偏差,在T-x图上会有最高或最低点出现,如图17-1(b)、(c)所示。
这些点称为恒沸点,其相应的溶液称为恒沸点混合物。
恒沸点混合物蒸馏时,所得的气相与液相组成不变,靠蒸馏无法改变其组成。
如HCl与水、丙酮与氯仿、硝酸与水等的体系具有最高恒沸点,苯与乙醇、异丙醇与环己烷、水与乙醇等的体系则具有最低恒沸点。
具有恒沸点的双液系与理想溶液或偏差很小的近似理想溶液的双液系的根本区别在于,体系处于恒沸点时气液两相的组成相同,因而也就不能像前者那样通过反复 蒸馏而使双液系的两个组分完全分离,因为对这样的溶液进行简单的反复蒸馏智能获得某一纯组分和组成为恒沸点的混合物。
异丙醇-环己烷气液平衡相图

实验七 异丙醇-环己烷气液平衡相图一、实验目的1. 了解绘制双液系相图的基本原理和方法;2. 采用回流冷凝法测定不同浓度的异丙醇-环己烷体系的沸点和气液两相平衡成分,绘制常压下环己烷-异丙醇双液系的T-x图,并找出恒沸点混合物的组成和最低恒沸点;3.学会使用阿贝折射仪。
二、实验原理 在常温下,任意两种液体混合组成的体系称为双液体系。
若两液体能按任意比例相互溶解,则称完全互溶双液体系;若只能部分互溶,则称部分互溶双液体系。
液体的沸点是指液体的蒸气压与外界大气压相等时的温度。
在一定的外压下,纯液体有确定的沸点。
而双液体系的沸点不仅与外压有关,还与双液体系的组成有关。
图17-1(a)是一种最简单的完全互溶双液系的T-x图(像苯与甲苯)。
图中纵轴是温度(沸点)T,横轴是液体B的摩尔分数xb (或质量百分组成),上面一条是气相线,下面一条是液相线,对应于同一沸点温度的二曲线上的两个点,就是互相成平衡的气相点和液相点,其相应的组成可从横轴上获得。
因此如果在恒压下将溶液蒸馏,测定气相馏出液和液相蒸馏液的组成就能绘出T-x图。
某些完全互溶的双液体系近似遵循拉乌尔定律,其正(或负)偏差不大,在T-x图上溶液的沸点介于A、B二纯液体的沸点之间(见图17-1(a)),如甲醇与水、二硫化碳与四氯化碳等。
大多数实际溶液由于A、B二组分的相互影响,常会与拉乌尔定律有较大偏差,在T-x图上会有最高或最低点出现,如图17-1(b)、(c)所示。
这些点称为恒沸点,其相应的溶液称为恒沸点混合物。
恒沸点混合物蒸馏时,所得的气相与液相组成不变,靠蒸馏无法改变其组成。
如HCl与水、丙酮与氯仿、硝酸与水等的体系具有最高恒沸点,苯与乙醇、异丙醇与环己烷、水与乙醇等的体系则具有最低恒沸点。
具有恒沸点的双液系与理想溶液或偏差很小的近似理想溶液的双液系的根本区别在于,体系处于恒沸点时气液两相的组成相同,因而也就不能像前者那样通过反复 蒸馏而使双液系的两个组分完全分离,因为对这样的溶液进行简单的反复蒸馏智能获得某一纯组分和组成为恒沸点的混合物。
异丙醇一环己烷双液系相图

3、利用组成一折 、 射率关系曲线所 确定的气、 确定的气、液相 组成, 组成,以及校正 后的各组成下的 沸点数据绘制沸 沸点数据绘制沸 点一组成图, 点一组成图,确 定该体系的恒沸 定该体系的恒沸 温度与恒沸组成。 温度与恒沸组成
实验注意事项
电阻丝不能露出液面,一定要浸没于溶液 中,以免通电红热后引起有机溶剂燃烧。 电阻丝两端电压不能过大,过大会引起有 机溶剂燃烧或烧断电阻丝。 测量过程中一定要达到气液平衡状态,即 体系的温度保持稳定,才能测定其沸点及 气相冷凝液和液相的折射率。 在测定其气相冷凝液和液相的折射率时要 保持温度一致。 使用阿贝折射仪时,棱镜上不能接触硬物, 擦拭棱镜时需用擦镜纸等柔软的纸。
操作步骤
1.已知浓度溶液折 射率的测定
取异丙醇和环己烷以 及环己烷摩尔分数分 别 23.31% 、 45.85% 、 58.94% 、 74.80% 四 种 组成的溶液,逐次用 阿贝折射仪测定其折 射率。绘制组成一折 射率的关系曲线。 射率的关系曲线。
沸点仪结构图
溶液沸点及气、 2.溶液沸点及气、液相组成的测定
为了绘制沸点一组成图, 为了绘制沸点一组成图,可采取不同的方 比如取该体系不同组成的溶液, 法。比如取该体系不同组成的溶液,用化学分 析方法分析沸腾时该组成的气、液组成, 析方法分析沸腾时该组成的气、液组成,从而 绘制出完整的相图。在本实验中的折射率 折射率的测 绘制出完整的相图。在本实验中的折射率的测 就是一种间接获取组成的办法。 定,就是一种间接获取组成的办法。它具有简 准确的特点。 捷、准确的特点。 本实验就是利用回流及分析的方法来绘制 相图。取不同组成的溶液在沸点仪中回流,测 相图。 取不同组成的溶液在沸点仪中回流, 定其沸点及气、液相组成。沸点数据可直接由 定其沸点及气、液相组成。 沸点数据可直接由 液相组成可通过测其折射率 可通过测其折射率, 温度计获得; 温度计获得;气、液相组成可通过测其折射率, 然后由组成一折射率曲线中最后确定。 然后由组成一折射率曲线中最后确定。
环己烷-异丙醇双液系相图

环⼰烷-异丙醇双液系相图2.6 环⼰烷-异丙醇双液系相图2.6.1 实验⽬的1.了解物理化学实验⼿段中常⽤的物理⽅法—光学⽅法的基本原理。
2.绘制环⼰烷-异丙醇双液系的沸点~组成图,并找出恒沸点及恒沸点混合物的组成。
3.进⼀步理解分馏原理。
4.掌握阿贝折射仪的原理及使⽤⽅法。
2.6.2 实验原理单组分液体在⼀定的外压下沸点为⼀定值。
把两种完全互溶的挥发性液体(组分A和B)混合后,在⼀定的温度下,平衡共存的⽓液两相组成通常并不相同。
因此在恒压下将溶液蒸馏,测定馏出物(⽓相)和蒸馏液(液相)的组成,就能找到平衡时⽓、液两相的成分并绘出T—x图,即所谓的相图。
完全互溶双液系在恒定压⼒下的沸点~组成图可分为三类:(1)液体与拉乌尔定律的偏差不⼤,沸点介于A、B两纯组分沸点之间(图6⼀1),如苯~甲苯体系。
(2) A、B两纯组分混合后与拉乌尔定律有较⼤的正偏差,溶液存在最低沸点(图6⼀2),如⽔~⼄醇;苯~⼄醇等体系。
(3)实际溶液由于A、B两纯组分相互影响,常与拉乌尔定律有较⼤负偏差,溶液存在最⾼沸点(图6⼀3),如盐酸~⽔体系;丙酮~氯仿体系。
图6—1 偏差不⼤的体系图6—2 正偏差很⼤的体系图6—3 负偏差很⼤的体系对(2)、(3)类体系有时被称为具有恒沸点的双液系。
它与(1)类的根本区别在于,体系处于恒沸点时⽓、液两相的组成相同。
因⽽也就不能象(1)类那样通过反复蒸馏⽽使双液系的两个组分完全分离。
对(2)、(3)类的溶液进⾏简单的反复蒸馏只能获得某⼀纯组分和组成为恒沸点的相应组成的混合物。
如要获得两纯组分,需采取其他⽅法。
体系的最低或最⾼恒沸点即为恒沸温度,恒沸温度对应的组成为恒沸组成。
环⼰烷-异丙醇双液系属于具有最低恒沸点⼀类。
为了绘制沸点~组成图,可采取不同的⽅法。
⽐如取该体系不同组成的溶液,⽤化学分析⽅法分析沸腾时该组成的⽓、液组成,从⽽绘制出完整的相图。
可以想象,对于不同的体系要⽤不同的化学分析⽅法来确定其组成,这种⽅法是很繁杂的。
对异丙醇_环己烷双液系相图实验条件改进的讨论

∑ 对 211 中结果: n1=
—
35, x 1=
68126℃,
S
2 1
=
(x 1i-
—
x1
)
2
n1- 1 = 015683
∑ 对 212 中结果: n2=
—
9, x 2=
68187℃,
S
2 2
=
(x 2i-
—
x2
)
2
n2- 1 = 011507
查 t 分布表有: tΑ(n1+ n2- 2) = = t01025 (42) 210181,
2 结果与讨论
211 方法一: 按教材〔6〕中方法, 仅将组成由摩尔分数改为用环己烷体积百分数来表示。 每次加入的
第二组分的体系按书上所述进行操作, 抽取 35 名学生的实验结果, 求得对应于最低恒沸点的温度及 组成分别是: (67160, 6110)、(69150, 6818)、(68160, 6010)、(68150, 6210)、(68150, 6110)、(68100,
×100◊
=
0139◊
, 是一很小值, 说明 T b,m in测量的准确度很好, 实验测得的 V 环己烷◊
的相
对误差为6411647-11677117 ×100◊ = - 4151◊ , 有一定的误差存在, 但仍属正常误差范围之内。 这主要 是由于被测体系有一定的挥发性, 同时所用试剂异丙醇和环己烷均没有经过精制, 这都使得在组成的
1 问题的提出
根据相律绘制相图, 通过对相图的分析加深对所研究体系的认识, 是热力学方法研究多相平衡体 系的重要内容之一。 经过本世纪初以来对完全互溶双液系的研究, 使这一类相图日趋完善, 以至于使 “完全互溶双液系相图”的实验作为一个经典实验而纳入了许多物理化学实验的教材中〔1, 2, 3, 4, 5〕。在这 些教材中, 大多是以苯—甲醇或苯—乙醇为测定体系。 考虑到苯有一定的毒性, 东北师范大学等校编 的《物理化学实验》第二版中〔6〕, 将此体系改为异丙醇—环己烷体系, 此教材即是我系学生正在使用的 教材。异丙醇——环己烷体系是一个可以以任意比例相互混溶的完全互溶双液系。由相律, f= C- 5 + 2, 这里相数 5 m in= 1, 组分数 C = 2, 故此体系自由度 fmax = 3, 即要完整描述此双液系相图需要用三 维坐标。但通常是在某个限制条件下进行的, 如可以是定温下的压力——组成图, 但更方便、更常用的 是定压下的温度——组成图, 此时体系的条件自由度 f3 = C - 5 + 1= 2, 用二维平面图形即可描述此 体系相图。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
异丙醇—环己烷双液系相图
————————————————————————————————作者:————————————————————————————————日期:
实验四异丙醇—环己烷双液系相图
一、实验目的:
1.了解物理化学实验手段中常用的物理方法—光学方法的基本原理。
2.绘制异丙醇—环己烷双液系的沸点—组成图,确定其恒沸组成及恒沸温度。
3.进一步理解分馏原理。
4.掌握阿贝折射计的原理及使用方法。
二.基本原理:
根据相律:f + φ = c + 2 ,对二组分体系:f = 4 - φ,f max = 3 (T,P,x)。
对于二组分体系,常常保持一个变量为常量,而得到立体图形的平面截面图。
这种平面图可以有三种:p-x图,T-x图,T-p图。
常用的是前两种。
在平面图上,f*=3-φ,f*max=2,同时共存的相数φmax=3。
单组分的液体在一定外压下,它的沸点是一定值,把两种完全互溶的挥发性液体(组分A和B)互相混合后,在某一定温度下,平衡共存的气液两相的组成,通常并不相同,因此如果在恒压下将溶液蒸馏,测定馏出物(气相)和蒸馏液(液相)的折射率,就能找出平衡时气液两相的成分,并绘出沸点—组成(T—x)图线,在常温下,两种液态物质以任意比例相互溶解所组成的体系称之为完全互溶双液系。
完全互溶双液系在恒定压力下的沸点—组成图可分为三类:
(1)溶液沸点介于两纯组分沸点之间(如图1),(2)溶液存在最低沸点(图2)和(3)溶液存在最高沸点(图3)。
(2)、(3)被称为具有恒沸点的双液系,即体系处于恒沸点时气、液两相的组成相同,其相应的溶液称为恒沸点混合物。
此时对恒沸点混合物进行蒸馏,所得气相与液相组成相同,因此我们不能用普通蒸馏方法获得任一纯组分。
异丙醇—环己烷双液系属于具有最低恒沸点一类的体系。
T—x图在进行蒸馏或分馏时是必不可少的,而分馏在提纯溶剂和石油工业中也得到广泛应用,所以这种图是具有很大的实用价值的。
本实验的目的就是要绘制异丙醇—环己烷的T—x图并找出恒沸点混合物的组成。
1.沸点—组成图的绘制
为了绘制沸点—组成图,可采取不同的方法。
在本实验中,我们采用的是一种物理方法—通过折射率的测定,来间接的获取溶液组成,它具有简捷、准确的特点。
本实验就是利用回流及分析的方法来绘制相图。
取不同组成的溶液在沸点仪中回流,测定其沸点及气、液相组成。
沸点数据可直接由温度计获得,气、液相组成可通过测其折射率,然后由组成—折射率曲线中最后确定。
以沸点对组成作图,将所有的气、液相组成连起来,即成相图。
2.阿贝折射计的原理与使用
原理:利用折射率的原理制成的。
参考图7.7。
使用:
(1)将超级恒温槽调到测定所需要之温度(20),并将此恒温水通入阿贝折射计的两棱镜恒温夹套中,检查棱镜上的温度计的读数。
如被测样品浑浊或有较浓的颜色时,视野较暗,可打开基础棱镜上的圆窗进行测量。
(2)阿贝折射计置于光亮处,但避免阳光直接照射,调节反射镜,使白光射入棱镜。
(3)打开棱镜,滴1~2滴无水乙醇(或乙醚)在镜面上,用擦镜纸轻轻擦干镜面,再将棱镜轻轻合上。
(4)测量时,用滴管取待测试样,由位于两棱镜上方的加液孔将此被测液体加入两棱镜间的缝隙间,旋紧锁钮,务使被测物体均匀覆盖于两棱镜间镜面上,不可有气泡存在,否则重新取样进行操作。
(5)转棱镜使目镜中能看到半明半暗现象,让明暗界线落在目镜里交叉法线交点上,如有色散现象,可调节消色补偿器,使色散消失,得到清晰的明暗界限。
(6)测完后用擦镜纸擦干棱镜面。
简单可表示为:
仪器安装—加样—对光—左下按钮粗调明暗面—右上按钮细调消色散—读数—仪器校正(纯水的n D20=1.3325)
三.实验装置图:
四.实验步骤:
1. 将超级恒温槽恒温至20 C,安装好仪器。
2.在干净的烧杯中加入20~30ml所测溶液,从移取液相的瓶口倒入,温度计的水银球一半浸在液体中,一半在气相中,水银球离电热丝2-3mm,打开回流冷凝管,插上14V直流电源加热。
(注意:在没有加入液体之前,一定不要通电,以防烧坏电阻丝)
3.加热沸腾后,用小电源加热(换12V),沸腾一段时间后看温度稳定后停止加热,(注意:一定要拔下电源插头),记下此时的温度(即沸点),其间倾倒2-3次气相组成液。
用盛水的大烧杯冷却后用抹布擦干,防止水进入试样。
4.分别从液相(烧瓶底部)和气相(冷凝管底部)用滴管吸取液体,(注意:滴管一定要干燥,每次要用电吹风机吹干;另外取气相液时滴管要垂直;)测其折射率。
(注意:每测一次样品,都要用搽镜纸将镜面搽干净,镜面上的液体要均匀,不可有气泡)。
每做完一个样品,要将剩余液体倒回原瓶,不要倒错。
按照上述步骤再做下一个。
通过折射率—组成工作曲线
(给出,不需做实验)得到相应温度下气液相的组成。
五.数据记录:
异丙醇—环己烷一定组成溶液的折射率
异丙醇重量百分数(%)0.00 7.85 15.15 22.02 32.62 41.66 51.72 74.01 100.00 溶液的折射率 1.4263 1.4210 1.4168 1.4130 1.4077 1.4029 1.3983 1.3882 1.3773
溶液沸点、折射率及组成
溶液沸点73.30 70.20 69.00 69.70 71.30 78.20
气相冷凝液
折射率 1.4121 1.4098 1.4072 1.4062 1.4050 1.3942 组成(%)24.93 29.67 35.03 37.09 39.56 61.81
液相折射率 1.4241 1.4187 1.4071 1.3989 1.3908 1.3810 组成(%)0.21 11.33 35.23 52.13 68.82 89.01 恒沸温度:69.4o C 恒沸组成:异丙醇%=32 气压:p o
六.实验注意事项:
1. 沸点仪没加液体,不得加热,防止电热丝烧断。
2.测试样品前一定要断电,用自来水冷却半分钟,然后用抹布擦干。
防止水进入试样。
取气相液滴需要垂直,做完后试样倒回原瓶,不要倒错,重做下一个。
3.低压直流电14伏。
4.在分馏液取样口处应加一干燥设备。
5.气液相反复倾倒2~3次,以确保气液达平衡。
倾倒时,速度要快,防止电热丝被烧断。
6.温度计的水银球应一半在液体中,一半在气相中(气液平衡)。
7.盛气相冷凝液的部位不可太大,只需盛一滴即可,若太大,不易达平衡。
8.滴管一定要干燥,用吹风机吹干。
9.滴水后,调下旋钮有色彩,调上旋钮消色散。
调明暗界限恰好通过十字线交点。
(蒸馏水n D20=1.3331)
10.读数镜筒太暗,可调旁边窗口盖成45o角。
七.结果讨论:
1.气液相应反复倾倒2~3次,以确保气液达平衡。
2.温度计的水银球应一半在液体中,一半在气相中,以确保气液达平衡,否则将影响实验结果。
3.滴管一定要用吹风机吹干,否则由于滴管上的残留液,而影响气相或液相的组成。
4.恒温槽中的水的温度应始终保持恒定,否则将影响气相或液相的折光率,从而影响气相或液相的组成。
5.气相或液相的折光率的测定准确与否,将直接影响实验结果。
八.思考题:
1.操作步骤中,在加入不同数量的各组分时,如发生了微小的偏差,对相图的绘制有无影响?为什么?
答:加入各组分时,如发生了微小的偏差,对相图的绘制无影响,因为最终液体的组成是通过对折光率的测定,在工作曲线上得出,所以无影响。
2.折射率的测定为什么要在恒定温度下进行?
答:因为折射率与温度有关,所以在测量时要在两棱镜的周围夹套内通入恒温水,保持恒温。
3.影响实验精度的因素之一是回流的好坏。
如何使回流进行好?它的标志是什么?
答:要使回流进行好,必须使气液多次充分接触,所以玻璃陶管不可缺,这样沸腾时才能不断撞击水银球,使气液两相平衡。
它的标志是温度指示数恒定。
4.对应某一组成测定沸点及气相冷凝液和液相折射率,如因某中原因缺少其中某一个数据,应如何处理?它对相图的绘制是否有影响?
答:沸点的数据不能少,其它可以少。
对于缺少的数据,可由它们的趋势找出其它点。
5.正确使用阿贝折射仪要注意些什么?(课本P87)
6.由所得相图,讨论某一组成的溶液在简单蒸馏中的分离情况?
答:若组成在0~x之间,蒸馏会得到A和C;若组成在x~1之间,蒸馏将会得到C和B。
若组成为x,则蒸馏只会得到恒沸混合物C。
