高二化学乙酸和羧酸2
2022学年上学期高二化学人教版(2019)选择性必修3第三章第三节课时1羧酸

第三节羧酸酯第1课时羧酸[学习目标定位] 1.知道羧酸的结构特点及简单分类。
2.能够以乙酸为代表物质,掌握羧酸的性质及用途。
1.乙酸的组成与结构乙酸的分子式为C2H4O2,结构式为,结构简式为CH3COOH,官能团是—COOH。
2.乙酸的性质(1)乙酸俗名醋酸,是一种无色液体,具有强烈刺激性气味,易溶于水和乙醇。
(2)乙酸是一种弱酸,其酸性比碳酸的强,具有酸的通性。
在水中可以电离出H+,电离方程式为CH3COOH CH3COO-+H+。
①与酸碱指示剂作用,能使石蕊试液变红。
②与Mg反应的化学方程式为Mg+2CH3COOH===(CH3COO)2Mg+H2↑。
③与CaO反应的化学方程式为CaO+2CH3COOH===(CH3COO)2Ca+H2O。
④与Cu(OH)2反应的化学方程式为Cu(OH)2+2CH3COOH===(CH3COO)2Cu+2H2O。
⑤与Na2CO3反应的化学方程式为Na2CO3+2CH3COOH===2CH3COONa+CO2↑+H2O。
探究点一羧酸1.写出下列各种酸的结构简式,并填空:①乙酸:CH3COOH;②硬脂酸:C17H35COOH;③苯甲酸:C6H5COOH;④油酸:C17H33COOH;⑤乙二酸:HOOC—COOH。
(1)从上述酸的结构可以看出,羧酸可以看作是由羧基和烃基相连而构成的化合物。
其通式可表示为R—COOH,官能团为—COOH。
(2)按不同的分类标准对羧酸进行分类:若按羧酸分子中烃基的结构分类,上述物质中的①②④属于脂肪酸,③属于芳香酸。
若按羧酸分子中羧基的数目分类,上述物质中的①②③④属于一元酸,⑤属于二元酸。
2.羧酸可以表示为(1)当①键断裂时,羧酸电离出H+,因而羧酸具有酸的通性。
(2)当②键断裂时,—COOH中的—OH被取代,例如发生酯化反应时,羧酸脱去—OH而生成相应的酯和水。
[归纳总结]醇、酚、羧酸的结构中均有—OH,由于这些—OH所连的基团不同,—OH受相连基团的影响就不同。
【化学】乙酸--羧酸解析
结构特点:既有羧基又有醛基 H—C—O—H
化学
醛基 氧化反应 银镜反应、碱性新制Cu(OH)2
还原反应 与H2加成
性质
羧基
酸性 酸的通性 酯化反应 与醇发生酯化反应
P84 问题解决
浓硫酸
HCOOH + HOCH2CH3 △ HCOOCH2CH3 + H2O
甲酸乙酯
HCHO + 4Cu(OH)2 + 2NaOH 水→浴 2Cu2O↓+ Na2CO3
⑶还原反应
+ 6H2O
HCHO
+
H2
Ni
加热加压
CH3OH
P80 观察与思考
OH
★
n
+
n
HCHO
催化剂 水浴
缩聚反应
OH
CH2 n + n H2O
单体
单体
酚醛树脂
醛基的检验
甲酸某酯
1、哪些有机物中含有—CHO? 醛类、HCOOH、HCOOR、葡萄糖、麦芽糖
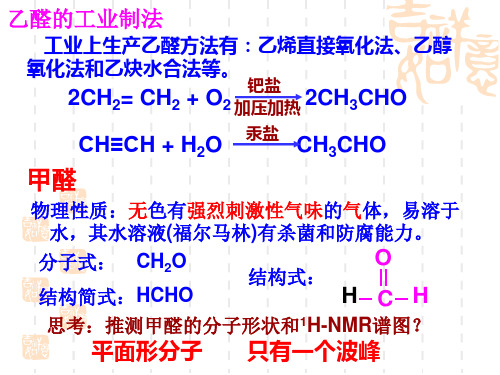
乙醛的工业制法
工业上生产乙醛方法有:乙烯直接氧化法、乙醇
氧化法和乙炔水合法等。
2CH2=
CH2
+
O2
钯盐 加压加热
2CH3CHO
CH≡CH + H2O 汞盐 CH3CHO
甲醛
物理性质:无色有强烈刺激性气味的气体,易溶于
水,其水溶液(福尔马林)有杀菌和防腐能力。
分子式: CH2O 结构简式:HCHO
O
D.用过量氢氧化钠溶液洗涤后分液
阅读 P83 信息提示 在可逆反应中,若改变化学平衡的条件,平衡会向削
弱这种改变的方向移动。
如:CH3COOH CH当3C达OO到- 化+ 学H+平衡时, 若此时中和掉H+离子,则H+浓度降低,平衡要削弱这 种改变,所以,平衡会向右移动,即继续电离出H+。
高二化学乙酸和羧酸PPT课件

CH3—C—O— H
OCH2
O
催化剂 加热
CH3—C—O—OCH2
O
+2H2O
CH3—C—O—OCH2
-
19
三三:、乙酸乙的化酸学性质的
化学性质小结
-
20
第五节酯
乙醛 第 乙 六酸
醛类化 章 的 第实 六验 节结 反 构 性 质
1、乙酸的酯化反应
制 法
应
-
21
观察实验 (1)、观察实验
(1)、
第五节乙 第乙 乙醛 六 酸 章的 第实 酸 六 验 醛类 节 结 羧 构 性 质
第六节 乙酸 羧酸
制 法
酸
重庆市涪陵实验中学 王俊明
-
1
第六节 乙酸 羧酸
知识点:
1、乙酸的酸性和酯化反应等化学性质,酯化反 应的概念。
2. 酯的水解;乙酸的酯化与乙酸乙酯的水解是 一对可逆反应。
3. 羧酸的简单分类,主要性质、用途;甲酸的 性质
重点:
乙酸的分子结构和化学性质
难点:
酯化反应的过程
-
2
第五节 第 一、
乙 六 乙
乙醛 章 酸 第的 酸 六 酸 节性
醛类 的
的 表
现
酸
一、乙酸的酸性
性
-
3
1、展示:乙酸 CH3COOH
无色、有刺激性气味、液体:
2、弱酸性:
A:紫色石蕊变红色
CH3COOH
CH3COO-+ H+
-
4
B、与Na反应:置换反应
R — COOH
羧酸
二元酸
有两个羧基 如:乙二酸
COOH
只有一个羧基
【襄樊五中】第13章《烃的衍生物》第6节《乙酸羧酸》第2课时

高二化学 第六章 烃的衍生物第六节 乙酸 羧酸(3课时)第2课时【说明】:本练习配套人教版化学读本,题目有一定的难度,适合省级示范高中或一些学校的优生使用,也可以作为高三第一轮复习的资料适用。
完成本练习的时间为30分钟,如果是高三第一轮复习,完成时间为20分钟。
后面有配套的标准答案,是经过认真审查的。
【习题内容】1 下列物质中,属于同系物的是( )A 硬脂酸和软脂酸B HCHO 和CH 3COOHC CH 2=CH —COOH 与CH 3(CH 2)2COOHD C 6H 5—OH 和C 6H 5—CH 2OH 2 下列物质中,属于同分异构体是是( )A 乙醇和乙醚B 丙醛和丙酮C 乙酸和甲酸甲酯D 硬脂酸和软脂酸 3 用分液漏斗可以分离的一组物质是( )A CH 3COOH 和C 2H 5OHBC 6H 5—OH 和C 2H 5OH C C 6H 6和NaAc 溶液D 植物油和乙酸乙酯 4 下列每组中各有三对物质,它们都能用分液漏斗分离的是( )A 乙酸乙酯和水、酒精和水、苯酚和水B 二溴乙烷和水、溴苯和水、硝基苯和水C 甘油和水、乙醛和水、乙酸和乙醇D 油酸和水、甲苯和乙醇、己烷和水5 下列物质既能使蓝色的石蕊试纸变红,又能被酸性高锰酸钾溶液氧化,还能使溴水褪色的是()A 乙烯B 甲酸乙酯C 福尔马林D 丙烯酸6 能将甲酸、石炭酸、NaOH、硫氰化铵溶液鉴别开的一种试剂是()A 溴水B 新制的Cu(OH)2溶液 C FeCl3溶液 D KMnO4溶液7 某有机物和过量的钠反应得气体VA 升,另一份等质量的该有机物和纯碱反应得气体VH升(同温同压下)若VA >VH,则该有机物可能是:()A HO(CH2)2COOH B 对羟基苯甲酸 C 乙二酸 D 乙二醇8 下列各组混合物中,各组可以任何比例混和,只要总质量固定,经过燃烧后产生的CO2的量为一恒量的是()A 甲醛和甲酸甲酯B 乙醛和乙酸C 丙醇和乙醇D 乙炔和苯9 标准状况下11.2L甲醛与33.6L氧气混和点燃后,又恢复到标况下,混和物体积为(D)A 16.8LB 22.4LC 28LD 33.6L10 可用来鉴别甲酸和乙酸的方法是()A 用石蕊试液加以鉴别B 加入乙醇及浓硫酸加热C 用碱中和后加入银氨溶液用水浴加热D 加入氢氧化钠溶液鉴别11下列物质中既显酸性,又能发生酯化反应和消去反应的是()①CH3CH2CH2Br ②CH3CH(OH)COOH③(CH3)2COHCOOCH3④(CH3)3CCHOHCOOHA 只有②B 只有②④C 只有③④D 只有①③12 巴豆酸结构简式为CH3—CH==CH—COOH,它在适当的条件下,能与下列哪些物质反应,①HCl②溴水③ Na2CO3溶液④ 2—丁醇⑤酸性高锰酸钾溶液()A 只有②③④B 只有①③⑤C 只有①②④D ①②③④⑤13 已知酸性C6H5COOH>H2CO3>C6H5OH>HCO3-—OOCCH3—OH可行的方法是()A 与足量的NaOH溶液共热,再通入CO2B 与稀硫酸共热后,再通入足量的NaOH溶液C 加热该物质的溶液,再通入足量SO2D 与稀硫酸共热后,加入足量的NaHCO315 分子量与乙烷相等的醛是,这种醛在室温下呈态,它的加氢产物叫,分子量与乙醇相等的羧酸是,它可否发生银镜反应?16 物质A的结构简式为:HO—(CH2)3—COOH,在一定条件具有下列性质,请用结构简式填空:⑴与浓硫酸共热生成B,B能使溴水褪色,B为⑵在浓硫酸存在时生成是分子式为C4H6O2的环状化合物C则C⑶在特定条件下发生双分子缩合反应生成分子式为C8H12O4的D,则D为⑷在一定条件下发生多分子缩聚反应生成高分子化合物E,则E为17 某种含结晶水的羧酸A6.3g在适当条件下分解,生成CO22.2g ,CO1.4g和H2O2.7g,若中和0.252gA需消耗0.2mol/L的NaOH溶液20ml,若使0.005mol的A完全酯化,需要0.46克CH3CH2OH,求A的最简式,分子式,并写出A的无水物结构简式。
人教版高中化学必修2《乙酸》教学设计

人教版高中化学必修2《乙酸》教学设计《乙酸》教学设计一、设计思想食醋是日常生活必不可少的重要调味品, 又是重要的化工原料。
学生对醋是很熟悉的 , 从学生熟悉的醋引入本课, 学生易于接受 , 同时结合酒中的乙酸的产生,有利于前后联系 . 结合在初中已经学过的有关乙酸的知识(乙酸的分子式、物理性质及酸性), 通过乙酸弱酸性实验以及电离方程式的书写, 理解乙酸的酸性是源于乙酸分子中 O— H 键的断裂。
并通过实验探究酸与醇的酯化反应,利用同位素示踪法来解释酯化反应的实质,酯化反应生成物水中的水是由醇提供氢和羧酸提供羟基的。
二、教材分析1.教材的地位和作用本节内容选自人教版高中化学必修 2 第三章第三节。
从教材整体上看,乙酸既是很重要的烃的含氧衍生物,又是羧酸类物质的代表物,它和我们的生活生产密切相关。
从知识内涵和乙酸的分子结构特点上看,乙酸既是醇、酚、醛知识的巩固、延续和发展,又是学好脂类化合物的基础,具有承上启下的作用。
乙酸在生活中是一种非常重要的有机物,自古就有民以食为天,食以味为先,味以酸为首的说法,这体现着乙酸作为一种重要调料的社会价值,而进入现代社会乙酸又成为了一种重要的化工原料,渗透到我们生活的各个领域。
2.教学目标(1)了解乙酸的物理性质和化学性质(酸性和酯化反应),认识乙酸的结构和官能团。
(2)学习实验设计方法,学会动手操作实验技能。
(3)树立乙酸与人类的生活生产密切相关的价值观。
3.教学重难点重点:乙酸的酸性和酯化反应难点:从结构角度认识乙酸的酯化反应三、学情分析初中学生只知道乙酸是一种酸,到了高中必修阶段乙酸就是一种有机物,而选修阶段乙酸是一种烃的衍生物,学生对乙酸分类的认知呈上升变化。
从结构的角度来看,初中学生只知道乙酸能解离出 H+, 到了必修要知道有特定的官能团,而到了选修阶段还要了解断键方式,学生对结构决定性质的认知也是呈上升变化的。
学生已经学习了烃的基础知识和乙醇、苯、乙醛等内容,对有机物的学习有了一定的认识,能掌握常见的有机物反应类型,具备了一定的实验设计能力,有较强的求知欲,利于沟通。
高考有机化学 羧酸的性质和应用

④二元羧酸与二元醇之间的酯化反应。 此时反应有两种情况:
⑤羟基酸的自身酯化反应。 此时反应有两种情况[以乳酸( )为例]:
1.
、
分别与 CH3CH2OH 反应, ( B.前者小于后者 )
生成的酯的相对分子质量大小关系 A.前者大于后者
乙酸的结构与性质
1.物理性质
俗称 醋酸(纯净 的乙酸称
颜色 气味 状态 熔沸点 挥发性 刺激 性
溶解性 易溶于水和
有机溶剂 ________
__色 无
___ 液
___ 低
___ 易
为_______) 冰醋酸
2.组成与结构
分子式 (化学式)
结构式
结构简式
官能团 (特征基团) 结构简式
比例模型
C2H4O2
1.羟基氢原子的活泼性比较
含羟基的物质 醇 比较项目 羟基上氢原 子活泼性 在水溶液中 电离程度 极难 电离
逐渐增强 ――――――→
水
酚
羧酸
难电离
微弱电离 部分电离 很弱的酸 性
酸碱性
中性
中性
弱酸性
含羟基的物质 醇 比较项目 与Na反应 与NaOH 反应 与NaHCO3 反应 反应放 出 H2 反应放 出 H2 反应放 出 H2 反应放 出 H2 水 酚 羧酸
2.在同温同压下,某有机物和过量 Na 反应得到 V1 L 氢气,另 一份等量的有机物和足量的 NaHCO3 反应得 V2 L 二氧化碳, 若 V1=V2≠0,则此有机物可能是
A.
(
B.HOOC—COOH
)
C.HOCH2CH2OH D.CH3COOH 解析: Na 既能与羟基反应,又能与羧基反应。NaHCO3 只与
【知识解析】羧酸

羧酸1 羧酸的基本知识温故乙酸的分子式是C2H4O2,结构简式是CH3COOH,是由甲基(—CH3)与羧基(—COOH)相连而构成的有机化合物。
(1)概念:羧酸是由烃基(或氢原子)与羧基()相连而构成的有机化合物。
(2)官能团:羧基(或—COOH)。
(3)通式:饱和一元脂肪酸的通式为C n H2n O2(n≥1)或C n H2n+1COOH(n≥0)。
注意最简单的羧酸是甲酸,其结构简式为HCOOH(4)分类(5)命名注意对于芳香羧酸和脂环羧酸,可把苯环和脂环作为取代基来命名。
如的名称为3-苯基丙烯酸。
2 羧酸的物理性质物理性质规律举例溶解性分子中碳原子数较少的羧酸能够与水互溶甲酸、乙酸、乙二酸随着分子中碳原子数的增加,一元羧酸在水中的溶解度迅速减小,甚至不溶于水高级脂肪酸是不溶于水的蜡状固体沸点随着分子中碳原子数的增加,一元羧酸的沸点逐渐升高丙酸>乙酸>甲酸注意羧酸的沸点一般高于与其相对分子质量相当的其他有机化合物,原因是羧酸分子间可以形成氢键。
3 羧酸的化学性质羧酸的化学性质主要取决于羧基官能团。
由于受氧原子电负性较大等因素的影响,当羧酸发生化学反应时,羧基中C—O和O—H容易断裂:(1)酸性①羧酸是一类弱酸,具有酸的通性,羧酸的电离方程式为RCOOH RCOO-+H+。
表现酸性的反应如下:反应现象或化学方程式与酸碱指示剂作用羧酸能使紫色石蕊溶液变红与碱反应RCOOH+NaOH—→RCOONa+H2O与碱性氧化物反应CuO+2RCOOH—→(RCOO)2Cu+H2O与活泼金属反应2RCOOH+2Na—→2RCOONa+H2↑RCOOH+NaHCO3—→RCOONa+H2O+CO2↑与某些盐反应2RCOOH+Na2CO3—→2RCOONa+H2O+CO2↑②教材P73·探究比较乙酸、碳酸和苯酚的酸性强弱实验装置CH3COOH与Na2CO3反应,有气体生成;生成的气体经过装有饱和NaHCO3实验现象溶液的洗气瓶后通入苯酚钠溶液中,溶液变浑浊实验结论酸性:化学方程式名师提醒(1)羧基(—COOH)由羰基()和羟基(—OH)构成,由于二者之间的相互影响,羧基上的氢原子比醇羟基上的氢原子易电离,因此羧酸具有酸性。
高二化学重点笔记知识点整理

高二化学重点笔记知识点整理高二化学重点笔记知识点(一)1、乙酸的分子式:C2H4O2,简写为CH3COOH,(羧基),乙酸是无色液体,有强烈的刺激气味。
易溶于水和乙醇。
熔点:16.6℃,沸点:117.9℃。
无水乙酸又称冰醋酸。
在室温较低时,无水乙酸就会凝结成像冰一样的晶体。
乙酸含有的羧基官能团决定乙酸的主要化学性质:酸性、酯化反应。
2、羧酸:在分子里烃基跟羧基直接相连接的有机化合物叫做羧酸。
一元羧酸的通式:RCOOH,饱和一元羧酸的通式:CnH2nO2。
3、羧酸的分类:按羧基的数目:一元羧酸、二元羧酸、多元羧酸;根据分子里的烃基是否饱和:饱和羧酸、不饱和羧酸;按烃基不同:脂肪酸、芳香酸;按C 原子数目:低级脂肪酸、高级脂肪酸。
4、羧酸的同分异构现象:羧酸的同分异构现象较普遍,羧酸既存在同类的同分异构体,也存在羧酸与酯的同分异构体。
5、羧酸的化学性质:由于羧酸的分子里都含有羧基,羧基是羧酸的官能团,它决定着羧酸的主要化学特性,所以羧酸的主要化学性质有:酸的通性,酯化反应。
6、酯的结构特征:酯是羧酸分子羧基中的-OH被-OR取代后的产物。
酯的特征结构是-COO-,羧酸酯的一般通式为RCOOR由饱和一元醇和饱和一元酸酯化反应得到的酯,可以用通式CmH2m+1COOCnH2n+1(或CnH2nO2)表示。
与饱和一元羧酸为同分异构体。
7、酯的物理性质:低级酯是有芳香气味的液体,存在于各种水果和花草中,酯的密度一般比水小,难溶于水,易溶于乙醇和乙醚等有机溶剂。
8、酯的同分异构现象:酯的同分异构现象一般要比其他的烃的含氧衍生物的同分异构现象更复杂,除酯类产生同分异构体外,酯与羧酸等物质之间也能产生同分异构体。
如C4H8O2的一部分同分异构体:CH3CH2CH2COOH、HCOOCH2CH2CH3、CH3COOCH2CH3、CH3CH2COOCH39、酯的化学性质:乙酸的酯化反应是一个可逆反应,因此酯类的重要化学性质之一就是可以发生水解反应。
第六节 乙酸 羧酸

第六节乙酸羧酸一、乙酸1、分子结构分子式C2H4O2, 结构简式:CO O H3CHO HOC3CH或2、物理性质无色、强烈刺激性气味的液体,熔点为16.6℃,低于16.6℃凝结成冰状晶体,故无水乙酸又称冰醋酸。
能与水和乙醇任意比互溶。
3、化学性质由于羰基对羟基影响,使羟基活性增强。
(1)酸性:乙酸在水溶液里部分电离-++C O O3C HHC O O H3C H具有无机酸通性:①与指示剂反应,如使紫色石蕊试液变红色。
②与金属活动顺序表中排了H前金属反应生成乙酸盐和H2③与碱性氧化物反应生成盐和水④与碱反应生成盐和水⑤与某些弱酸盐或不稳定酸盐反应注意:CH3CH2OH、H、CH3COOH 酸性比较:乙醇:中性,能与活泼金属反应,不与盐和碱反应。
苯酚:弱酸性,不能使指示剂变色,能与强碱反应,不与NaHCO3反应(更不会产生CO2)。
乙酸:弱酸性,能使指示剂变色,能与NaOH反应,能与碳酸盐反应产生CO2。
故酸性:乙酸﹥碳酸﹥苯酚﹥乙醇(2)酯化反应:酸与醇作用生成酯和水的反应O2H5H2CO18OC3CH4SO2H5H2CO18HO HOC3CH+∆+浓注意:a)经同位素氧-18测定,乙酸与乙醇作用生成乙酸乙酯的反应原理是:乙酸脱去羧基上的羟基,乙醇脱去羟基上的氢原子。
b)反应中浓硫酸起催化、吸水作用。
c)吸收装置(如右图)中导管口不与液面接触是防止试管中液体倒吸入反应容器中。
d)试管中用饱和Na2CO3溶液收集乙酸乙酯,目的是中和蒸气中的乙酸,溶解乙醇,降低乙酸乙酯的溶解度。
e)酯与混合液分离:用分液漏斗分液,取上层油状液体得酯。
4、乙酸的制法(1)发酵法乙酸氧化乙醛发酵氧化乙醇酶发酵糖类淀粉−−−→−()((2)乙烯氧化法C O O H3CH 22O CHO 3CH 2CHO 3CH 22O 2CH 2CH 2−−−→−+−−−→−+=催化剂催化剂此法原料来源丰富,生产工艺流程简单 (3)烷烃直接氧化法—丁烷氧化法O 2H 2C O O H3CH 2O 53CH 2CH 2CH 3CH 2++5、乙酸的用途生产醋酸纤维 、合成维纶纤维 、作溶剂、制香料、染料、医药、农药等。
羧酸-高二化学系列教学课件(人教版选择性必修3)

A、使紫色石蕊试液变色
具有
B、与活泼金属反应
酸的
C、与碱性氧化物反应
通性
D、与碱反应
E、与某些盐(如碳酸盐,酸式碳酸盐)反应
上述方案哪些更为合理?(反应灵敏,现象明显)
【活动3】如果想进一步证乙酸是弱酸,该怎么设计方案? (1)取0.1 mol·L-1乙酸溶液,测pH。 (2)取乙酸钠溶液,测pH。 (3)取浓度相等的盐酸和乙酸溶液,加入烧杯,测其导电性。
(1)当和_______________反应时,可转化为
。 。
(2)当和______________反应时,可转化为
。
(3)当和_____________反应时,可转化为
。
[答案] (1)NaHCO3 (2)NaOH(或 Na2CO3) (3)Na
乙二酸
2-甲基丁二酸
丙烯酸
如何解释? 阅读P72第一段及表3-4,总结羧酸的物理性质及其递变规律。
甲酸、乙酸等分子中碳原子数较少的羧酸能够与水互溶。随着分子中 碳原子数的增加,一元羧酸在水中的溶解度迅速减小,甚至不溶于水。
高级脂肪酸是不溶于水的蜡状固体。 随着分子中碳原子数的增加 ,其沸点也逐渐升高。
O—H键断裂时,解离出H+,
C—O键断裂时,
【联想质疑】 (1)乙醇中含有羟基(-OH),乙酸中的羧基也含有(OH),为什么乙醇没有酸性,而乙酸有酸性; (2)醛和酮中的碳氧双键能和H2发生加成反应,乙酸中的羧基也含有碳 氧双键,能否和氢气发生加成反应?
受碳氧双键的影响:
受羟基的影响:
1、羧酸的酸性
如何解释?
(4)羧酸与相对分子质量相当的其他有机化合物相 比,沸点较高,这与羧酸分子间可以形成氢键有关。
乙酸、羧酸

(三)甲酸除具有酸的性质外, 还有醛的性质。
小结:几种衍生物之间的关系
乙酸、羧酸
乙酸乙酯的制取:
1.反应机理:醇脱氢原子,羧酸脱 羟基结合生成水。
2.酯化反应可看作是取代反应, 也可看作是分子间脱水)中和挥发出来的乙酸,生成醋酸 钠(便于闻乙酸乙酯的气味)。 (2) 溶解挥发出来的乙醇。 (3)抑制乙酸乙酯在水中的溶解度。
乙酸、羧酸
(二)主要物理性质:密度一般小于 水,并难溶于水,易溶于乙醇和乙醚 等有机溶剂。 (三)用途:可用溶剂,也可用制备 饮料和糖果的香料。
(四)水解反应: 1.在酸中的反应方程式:
2、在碱中反应方程式:
五、羧酸
(一)羧酸是羧基跟烃基直接相连的 脂肪酸和芳香酸。
(二)分类: 1.根据羧基相连的烃基不同分为:脂 肪酸、芳香酸。 2.根据羧酸分子中羧基的数目,羧酸 又可以分为:一元酸、二元酸(如乙 二酸HOOC—COOH)、多元酸。
2CH3COOH + Na2CO3 = 2CH3COONa + CO2↑+ H2O
2.与Mg反应
Mg + 2CH3COOH → (CH3COO)2Mg + H2↑
3、酸性比较:
CH3COOH > H2CO3 > C6H5OH
电离方程式:
CH3COOH
CH3COO— + H+
(二)酯化反应
定义:醇和含氧酸起作用,生成酯和水 的反应叫做酯化反应。
温馨提示:为更好地满足您的学习和使用需求,课件在下载后可以自由编辑,请您根据实际情况进行调整!Thank you for
4.硫酸的作用: 催化剂;吸水性,该反应是可逆反应, 加浓硫酸可促进反应向生成乙酸乙酯 的反应方向进行。
乙酸-羧酸

乙酸 羧酸 一、乙酸 羧酸1、 定义:分子中烃基(或氢原子)跟羧基()相连的化合物属于羧酸。
2、 物理性质:无色液体,易溶于水,随着碳原子数增多,水溶性降低。
具有弱酸性,随着碳原子数增多,酸性降低。
3、 饱和一元酸的通式_________________________ 二、乙酸(冰醋酸即无水乙酸) 1、 分子结构:分子式为___________,结构式为_______________,结构简式为_________________,俗称_______2、乙酸的化学性质 (1)酸性乙酸水溶液中存在以下电离方程式:CH 3COOH CH 3COO -+H +,故乙酸为弱酸,能体现酸的性质。
乙酸能与Na 、NaOH 、NaHCO 3、Na 2CO 3反应,酸性大于碳酸。
酸性比较:在某有机物A 的分子中,其结构简式如右图。
写出: A 跟NaOH 溶液反应的化学方程式是A 跟NaHCO 3溶液反应的化学方程式是A 在一定条件下跟Na 反应的化学方程式是:(2)酯化反应在一支试管中加入3 mL 乙醇,然后边摇动试管边慢慢加入2 mL 浓硫酸和2 mL 冰醋酸。
按图连接好装置用酒精灯小心均匀地加热试管3~5 min ,产生的蒸气经导管通到饱和的碳酸钠溶液的液面上。
可以看到碳酸钠饱和溶液的液面上有透明的油状液体产生,并可闻到香味。
生成乙酸乙酯的反应A 、这种有香味的无色透明油状液体就是乙酸乙酯,反应的化学方程式可以表示如下:+CH 3CH 2OH浓硫酸+H 2OCH 3COOH CH 3COOCH 2CH3反应类型:酯化反应(取代反应),反应规律:_______________________________酸和醇起作用,生成酯和水的反应叫做酯化反应,这里的酸是指像乙酸之类的有机酸和像硝酸之类的无机含氧酸。
如果用含氧的同位素188O 的乙醇与乙酸作用,请写出化学方程式:B 、乙酸乙酯是酯类化合物的一种,乙酸乙酯的密度约为0.9 g·cm -3,沸点77 ℃,易溶于乙醇等,微溶于水。
高中化学《乙酸》课件

处理技术
针对羧酸类化合物的污染问题, 可采用物理、化学或生物方法进 行处理,如吸附、氧化、生物降
解等。
资源回收
通过合适的分离和提纯技术,可 实现羧酸类化合物的回收利用,
降低资源浪费和环境污染。
2024/1/25
30
感谢您的观看
THANKS
2024/1/25
31
乙酸是合成许多有机化 合物的重要原料,如乙 酸乙酯、乙酸纤维等。
8
乙酸可用于治疗某些皮 肤疾病和作为消毒剂使
用。
02
乙酸制备方法与实验
2024/1/25
9
实验室制备乙酸方法及原理
乙醇氧化法
在实验室中,常用乙醇氧化法制备乙 酸。该方法利用乙醇在催化剂作用下 与氧气反应,生成乙酸和水。反应原 理为乙醇中的羟基被氧化为羧基。
2024/1/25
实例分析
以乙酸和乙醇的酯化反应为例,探讨反应条件、催化剂选择 、产物分离提纯等实验细节。
17
酸碱中和反应在乙酸中的应用
01
02
03
中和滴定
利用酸碱中和反应的原理 ,通过滴定方法测定乙酸 的浓度或含量。
2024/1/25
缓冲溶液配制
乙酸与乙酸钠按一定比例 混合可配制缓冲溶液,用 于维持溶液pH值的有机 化合物,具有刺激性气味和酸味 。
分子式
乙酸的分子式为C2H4O2,由两 个碳原子、四个氢原子和两个氧 原子组成。
4
物理性质与化学性质
物理性质
无色透明液体。
具有刺激性气味和酸味。
2024/1/25
5
物理性质与化学性质
易溶于水、乙醇等溶剂。
化学性质
实验注意事项
选择合适的反应条件如温度、时间等;注意催化 剂的选择和用量;对产物进行充分提纯以保证鉴 定结果的准确性。
高中化学高二化学PPT课件乙酸和羧酸共46页PPT

谢谢!
51、 天 下 之 事 常成 于困约 ,而败 于奢靡 。——陆 游 52、 生 命 不 等 于是呼 吸,生 命是活 动。——卢 梭
53、 伟 大 的 事 业,需 要决心 ,能力 ,组织 和责任 感。 ——易 卜 生 54、 唯 书 籍 不 朽。——乔 特
高中化学高二化学PPT课件乙酸和羧酸
21、没有人陪你走一辈子,所以你要 适应孤 独,没 有人会 帮你一 辈子, 所以你 要奋斗 一生。 22、当眼泪流尽的时候,留下的应该 是强 。 23、要改变命运,首先改变自己。
24、勇气很有理由被当作人类德性之 首,因 为这种 德性保 证了所 有其余 的德性 。--温 斯顿. 丘吉尔 。 25、梯子的梯阶从来不是用来搁脚的 ,它只 是让人 们的脚 放上一 段时间 ,以便 让别一 只脚能 够再往 上登。
55、 为 中 华 之 崛起而 读书。 ——周 恩来
高二化学乙酸和羧酸2

请同学们试说出几种可以检验醋酸具 有酸性的方法?
1.利用指示剂——石蕊试液(酸红碱蓝); 利用金属活动性顺序表中氢前的金属可以置换 H+为H2性质。
2.与碳酸钠反应生成CO2气体。 2CH3COOH + Na2CO3 = 2CH3COONa + CO2↑
3.将表面用砂纸磨过镁条插入乙酸溶液。观 察现象。
⑴反应机理:醇脱氢原子,羧酸脱羟基结合生成水 ⑵酯化反应可看作是取代反应,也可看作是分
子间脱水的反应。 ⑶饱和碳酸钠溶液的作用:
①中和挥发出来的乙酸,生成醋酸钠(便 于闻乙酸乙酯的气味)
②溶解挥发出来的乙醇。
③抑制乙酸乙酯在水中的溶解度。
⑷硫酸的作用:催化剂;吸水性,该反应是可 逆反应,加浓硫酸可促进反应向生成乙酸乙酯 的反应方向进行。
无色、有强烈刺激性气味的液体,易溶 于水和有机溶剂,凝固点较高,易凝结 成冰状固体,无水乙酸又叫“冰醋酸”。
三、乙酸的结构
请同学试写出乙酸的分子结构式,分子式。
三、乙酸的分子结构
2、取代(酯 化 )
O
1、酸 性 (无H不被 氧 化 )
H3C C O H
乙 酰基
乙酰基(强吸电子基)使—O—H键的极性大大增加, 使O—H键易断,表示出强的酸性(CH3COOH >H2CO3)
乙酸 羧酸
重庆市涪陵实验中学 王俊明
复习:
在下列关系式中,请同学们试写出各转化过程相关的 化学反应方程式。
一、羧酸的结构
分子里由烃基(或H)与羧基相连而生成
的有机物 叫羧酸。
O
一般通式为:RCOOH 或 R C OH
—COOH(羧基)官能团。包含—CO—和 —OH两部分。
高中化学高二化学PPT课件乙酸和羧酸共46页文档

16、人民应该为法律而战斗,就像为 了城墙 而战斗 一样。 ——赫 拉克利 特 17、人类对于不公正的行为加以指责 ,并非 因为他 们愿意 做出这 种行为 ,而是 惟恐自 己会成 为这种 行为的 牺牲者 。—— 柏拉图 18、制定法律法令,就是为了不让强 者做什 么事都 横行霸 道。— —奥维 德 19、法律是社会的习惯和思想的结晶 。—— 托·伍·威尔逊 20、人们嘴上挂着的法律,其真实含 义是财 富。— —爱献 生
ห้องสมุดไป่ตู้
谢谢!
61、奢侈是舒适的,否则就不是奢侈 。——CocoCha nel 62、少而好学,如日出之阳;壮而好学 ,如日 中之光 ;志而 好学, 如炳烛 之光。 ——刘 向 63、三军可夺帅也,匹夫不可夺志也。 ——孔 丘 64、人生就是学校。在那里,与其说好 的教师 是幸福 ,不如 说好的 教师是 不幸。 ——海 贝尔 65、接受挑战,就可以享受胜利的喜悦 。——杰纳勒 尔·乔治·S·巴顿
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
Hale Waihona Puke 老葡京国际游戏注册 [单选]下列哪项不是前列腺增生的并发症()A.尿毒症B.血尿C.感染D.肾结石E.腹股沟疝 [单选,A2型题,A1/A2型题]下列错误的是()。A.发绀见于缺氧,缺氧一定有发绀B.发绀是皮肤、黏膜呈青紫色C.发绀常见的部位为口唇、指(趾)、甲床D.血液中存在异常血红蛋白的绝对量也可出现发绀E.发绀是血液中还原血红蛋白增多所致 [问答题,案例分析题]阅读理解:1、某建筑物采用框架剪力墙结构,在一层共有8根编号为L1的梁,见图3-26。"结构设计总说明"中有如下说明:梁与剪力墙、柱交接处应设箍筋加密区,长度为1.5H(H为梁高)。(钢筋保护层25mm)。试计算各钢筋。图3-26L1梁配筋图已知:钢筋总重量按下列各 [单选]产后子宫恢复至非孕期大小约需().A.3周B.4周C.5周D.6周E.7周 [单选]焦炉煤气加热焦炉时,当空气量偏小时,火焰()。A.亮白短小B.暗.冒烟C.充满火道 [单选,A1型题]摄影效应检查主要是应用X线的哪个特性()A.穿透作用B.荧光效应C.感光效应D.离子效应E.损伤作用 [单选]教育培训培养人才具有()的特点,要求课程开发具有超前性A、前瞻性B、多元性C、实践性D、周期性 [单选]猝死抢救时,最先进行的基础心肺复苏包括()A.气管插管B.胸外按压C.除颤复律D.心脏起搏E.肾上腺素 [填空题]我国沙漠沙物质的机械组成:以()为主。从粒径分析及中值粒径。 [单选]下列哪项不属于高级心肺复苏的措施()A.人工呼吸B.气管插管C.电除颤D.建立静脉通路,维持循环E.药物 [判断题]《出口玩具质量许可证》的有效期为3年。()A.正确B.错误 [填空题]HIS门诊挂号程序应具备的功能()、()、()。 [单选]碳化液在较大的过饱和度下开始结晶时,由于成核速率与相应的晶体成长速率相比要(),因此所得成品粒度会()。A、快,大B、快,小C、慢,大D、慢,小 [单选,A2型题,A1/A2型题]下列化学发光酶免疫分析特点中错误的是()A.属于酶免疫测定范畴B.整个反应无需固相载体参加,完全液态化C.酶标记抗原或抗体结合稳定D.酶催化发光剂发出的光稳定,持续时间长E.最后一步将底物改为发光剂和测定的仪器为光信号检测仪 [单选]发展心理学是研究()的科学。A.认知发展规律B.心理的种族发展C.心理的种系发展D.心理发展规律 [单选,A2型题,A1/A2型题]我国法定的职业肿瘤是()A.紫外线所致皮肤癌B.电离辐射所致白血病C.氯甲醚所致肺癌D.苯胺所致膀胱癌E.镍和镍化合物所致肺癌 [单选,A1型题]膀胱镜检查术,以下错误的是()A.术前做好解释工作B.嘱患者多饮水C.检查前清洗外阴D.术后留置导尿管1周E.应用抗生素,预防感染 [多选]下列社会学家属于唯名论者的是()A.霍布斯(某哲学家)B.涂尔干C.帕森斯D.韦伯 [单选]基尔霍夫电流定律的数学表达式是()。A.∑E=∑UB.∑I=0C.∑E=0D.∑U=0 [单选]当年播种,当年开花结果,然后死亡的植株是()。A.一年生植物B.两年生植物C.多年生植物D.木本植物 [单选]管理信息系统有以下三个特点:在企业管理中全面使用计算机;采用决策模型解决结构化的决策问题和使用()。A、数据库技术B、数据库技术和计算机网络C、计算机网络技术D、通信技术 [单选]高层民用建筑的裙房应设()楼梯间。A.开敞楼梯间B.敞开楼梯间C.封闭楼梯间D.防烟楼梯间 [问答题,简答题]什么是干馏点? [单选,A2型题,A1/A2型题]在中暑的几种类型中,以哪种最为凶险()。A.热射病B.热痉挛C.热衰竭D.先兆中暑E.以上都不是 [单选,A2型题,A1/A2型题]糖耐量试验(耐糖曲线)用于诊断()A.严重糖尿病B.酮症酸中毒C.检查血糖回复到正常水平的时间D.隐性糖尿病E.临床常规糖尿病 [单选]艾滋病患者抗HIV治疗的药物中不包括下列哪种()A.叠氮胸苷B.双脱氧肌苷C.双脱氧胞苷D.5-氟脲嘧啶 [单选]出境、入境的交通运输工具离、抵口岸时,必须接受()A、边防检查B、船体检查C、梯口监护D、驻船监护 [判断题]闭路监控用的是射频线型号是SYWV75-5线。A.正确B.错误 [单选]价格低廉、使用寿命长,具有良好的耐腐蚀性、耐温性、耐压性,且无电化学腐蚀,可制成氯碱工业工艺管、污水处理及输送管、热能输送管、水电站压力水管等,此种管材为()。A.玻璃钢管B.硬聚氯乙烯管C.硬聚氯乙烯/玻璃钢复合管D.钢塑复合管 [单选]该病房楼内设有上下层相连通的走廊、敞开楼梯、自动扶梯、传送带等开口部位时,应按上下连通层作为一个防火分区,其允许最大建筑面积之和不应超过《高层民用建筑设计防火规范(2005年版)》(GB50045--1995)的规定。当上下开口部位设有()等分隔设施时,其面积可不叠加计算。 [问答题,简答题]比例泵的启动和停泵步骤? [单选]与蛋白质载体或高分子聚合物结合才具有免疫原性的物质称为()A.变应原B.完全抗原C.半抗原D.佐剂E.载体 [问答题,简答题]什么是精馏的原理? [填空题]平面填料的典型结构是三六瓣结构,即朝向气缸的一侧由()组成,背离气缸的一侧由()组成,每一块平面填料外缘绕有螺旋弹簧,起()作用。 [单选]在现代商业保险中,符合保险人承保条件的特定风险一般被称为()。ABCD [单选]下载文件使用的协议是()A.HTTPB.POP3C.FTPD.TCP/IP [单选,A1型题]公卫医师何某在取得医师资格证书和执业许可证后的一年里,擅自从事婚前医学检查、遗传病诊断和产前诊断,虽经卫生行政部门制止,仍不改正,并又施行终止妊娠手术。依据《母婴保健法》规定,应对何某给予的行政处罚是()A.处以罚款B.没收违法所得C.没收非法财物D.吊 [单选]当飞机绕重心的角加速度为零时,位于飞机尾部设备的过载()。A.大于飞机重心处的过载B.等于飞机重心处的过载C.小于飞机重心处的过载D.与飞机重心处的过载无关 [填空题]按工作介质的不同,流体机械可分为()、()和()。 [多选]专利权的客体包括()。A.技术秘密B.计算机软件C.发明D.实用新型E.外观设计
