元素周期律(第1课时)
元素周期律+第1课时+参考教案

元素周期律第1课时◆教学目标与核心素养宏观辨识与微观探析:从微观上理解同周期元素原子核外电子排布的相似性和递变规律,明确宏观上的元素性质与微观上的原子核外电子排布之间的关系,理解结构决定性质,性质反映结构的基本规律。
科学探究与创新意识:通过完成相应的同周期元素性质的探究实验,初步体验科学探究在化学学科的学习中的重要地位,了解科学探究的基本方法,培养初步的科学探究能力。
证据推理与模型认知:建立元素原子结构变化与其性质变化的的微观模型,理解根据该模型进行元素性质推理的科学思想。
◆教学重难点元素周期律的概念;理解其变化规律。
◆教学过程一、导入新课通过对碱金属元素、卤素的原子结构和性质的研究,我们已经知道元素周期表中同主族元素的性质有着相似性和递变性。
那么,周期表中同周期元素的性质有什么变化规律呢?二、讲授新课【板书】元素周期律一、元素性质的周期性变化规律【思考与讨论】观察下面表格中的数据,思考并讨论随着原子序数的递增,元素原子的核外电子排布、原子半径和化合价各呈现什么规律性的变化?【讲解】通过比较上面元素的原子核外电子排布,可以得到同周期元素的核外电子排布的规律:同周期由左向右,元素原子的最外层电子数逐渐增加(第一周期是1→2,第二周期和第三周期都是1→8)【讲解】再比较上面元素的原子半径(稀有气体的半径没有可比性,所以不列出),可以得到同周期元素的原子半径的变化规律:同周期由左向右,元素原子的半径逐渐减小(不包括稀有气体)【设疑】观察下图,判断同周期和同主族元素原子半径的变化规律【讲解】同主族元素由上向下元素原子的半径逐渐增大,同周期元素由左向右,元素原子的半径逐渐减小。
H是所有原子中半径最小的。
【设疑】短周期主族元素中,原子半径最大的是哪种元素?(Na)【讲解】再比较上面元素的常见化合价,可以得到同周期元素的化合价的变化规律:同周期由左向右,元素的最高正价逐渐升高(+1→+7,O和F无最高正价);元素的最低负价由ⅣA族的-4价逐渐升高至ⅦA族的-1价【过渡】根据上面的分析,我们可以看出随着元素的原子序数递增,元素原子的核外电子排布、原子半径、元素化合价都呈现了周期性的变化,那么元素的金属性和非金属性是否也随着原子序数的递增而呈现周期性变化呢?【思考与讨论】根据第三周期元素原子的核外电子排布规律,推测该周期元素金属性和非金属性具有怎样的变化规律?【讲解】第三周期元素:Na、Mg、Al、Si、P、S、Cl的电子层数相同,随着核电荷数的递增,原子半径逐渐减小,导致失电子能力逐渐减弱,得电子能力逐渐增强,因此,金属性逐渐减弱,非金属性逐渐增强。
苏教必修二1.1.2元素周期律(第一课时)
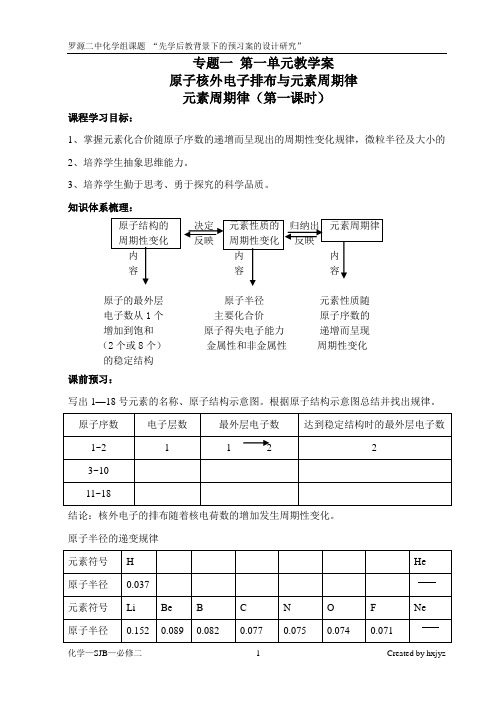
专题一第一单元教学案原子核外电子排布与元素周期律元素周期律(第一课时)课程学习目标:1、掌握元素化合价随原子序数的递增而呈现出的周期性变化规律,微粒半径及大小的2、培养学生抽象思维能力。
3、培养学生勤于思考、勇于探究的科学品质。
知识体系梳理:原子的最外层原子半径元素性质随电子数从1个主要化合价原子序数的增加到饱和原子得失电子能力递增而呈现(2个或8个)金属性和非金属性周期性变化的稳定结构课前预习:写出1—18号元素的名称、原子结构示意图。
根据原子结构示意图总结并找出规律。
结论:核外电子的排布随着核电荷数的增加发生周期性变化。
原子半径的递变规律总结:同一周期,随着原子序数的递增,元素原子半径逐渐减小,呈现周期性变化。
此处留白,学生填写预习中不明白的课前检测:1、比较Na、S原子半径的大小。
2、比较Na、O原子半径的大小。
课程达标检测:2.按粒子的半径从小到大顺序排列的是( )A.Cl,S,PB.N,O,FC.Al3+,Mg2+,Na+D.K,Na,Li3.下列各组微粒中,按微粒半径依次增大排列的是( )(A)Al3+,Al,Na,K (B)F,Cl,S2- ,S(C)S2-,Cl - ,K + ,Ca 2+ (D)Mg,Si,P,K4.a元素的阴离子,b元素的阴离子,c元素的阳离子具有相同的电子层结构,已知a的原子序数大于b的原子序数,则a,b,c三种离子半径大小的顺序是( )A.a>b>cB.b>a>cC.c>a>bD.c>b>a课后练习:。
4.2元素周期律(第1课时)教案
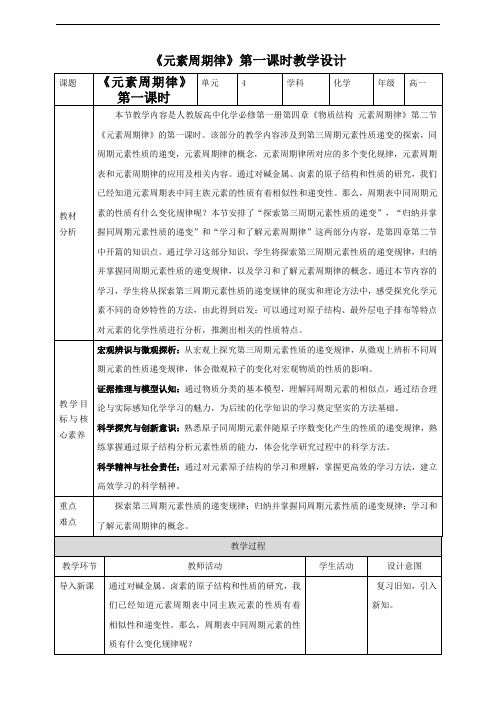
《元素周期律》第一课时教学设计讲授新课一、1~18号元素的特点1~18号元素的特点注:稀有气体元素的原子半径测定与相邻非金属元素的测定依据不同,数据不具有可比性,故不列出。
1~18号元素的特点1~18号元素的特点【设疑】观察下表,思考:随着原子序数递增,元了解同周期元素的原子半径大小及化合价,探索出规律。
素原子的核外电子排布、原子半径和化学价各呈现什么规律性变化?【设疑】观察下表,思考:随着原子序数递增,元素原子的核外电子排布、原子半径和化学价各呈现什么规律性变化?随着原子序数的递增,元素原子的核外电子排布、原子半径和化合价都呈现周期性变化。
核外电子层数相同,原子半径逐渐变小,化合价逐渐升高。
当K层为最外层时,最多能容纳2个电子数除了K层,其他各层为最外层时,多能容纳8个电子数。
【设疑】元素的金属性和非金属性是否也随着原子序数的递增而呈现周期性变化?第三周期元素性质的递变取一小段镁条,用砂纸除去表面的氧化膜,放到试管中。
向试管中加入2mL水,并滴入2滴酚酞溶液,观察现象。
观察表格,思考问题。
总结规律无明显现象。
因为镁和冷水不反应。
过一会儿,加热试管至液体沸腾,观察现象。
与钠和水的反应相比,镁和水的反应难易程度如何?生成了什么物质?有气体产生,溶液变成红色反应式:Mg + 2H2O ——Mg(OH)2 + H2↑钠的金属性要比镁大得多,所以与水反应钠比镁要剧烈得多。
所谓金属性就元素的原子失去电子的能力。
元素的金属性越强,越容易失电子被氧化。
第三周期元素性质的递变向试管中加入2mL 1mol/L AlCl3溶液,然后滴加氨水,直到不再产生白色絮状Al(OH)3沉淀为止。
将沉淀分装在两只试管中,向一支试管中滴加2mol 盐酸,向另一只试管中滴加2mol/LNaOH溶液。
边滴加边振荡,观察现象。
Al(OH)3在酸或强碱溶液中都能溶解,表明它既能与酸发生反应,又能与强碱溶液发生反应。
反应的离子方程式分别如下:Al(OH)3 + 3H+——Al3+ + 3H2OAl(OH)3 + OH-——AlO-2 + 2H2O金属元素的氢氧化物钠、镁、铝是金属元素,都能形成氢氧化物。
元素周期律第1课时

《必修Ⅱ第1章第2节元素周期律》(第1课时)【课标要求】1、了解原子核外电子的排布;2、掌握元素原子核外电子排布、原子半径、化合价的周期性变化3、学会总结、概括,体会结构决定性质的理念。
【重点难点】1、原子核外电子排布、原子半径、主要化合价周期性变化规律2、知道核外电子排布规律、原子、离子等微粒半径大小比较【新课导学】※一、原子核外电子的排布:1.原子核外的电子由于能量不同,它们运动的区域也不同。
通常能量低的电子在离核____的区域运动,能量高的电子在离核____的区域运动。
2.3.⑴按能量由低到高,即由内到外,分层排布。
①每层最多容纳____个电子②除K层外,其最外层中的电子数最多只能有____个(K层最多有__个)③除K层、L层为次外层时外,次外层不超过____个电子④倒数第三层不超过____个电子。
⑵根据核外电子排布的规律,能划出1-20号原子结构示意图。
完成教材P14科学探究。
二、化合价的周期性变化。
[结论:随着原子序数的递增,元素也呈现周期性变化。
总结:同一周期,随着原子序数的递增,元素原子半径逐渐,呈现周期性变化。
四、微粒半径大小的比较1、原子半径大小的比较同主族,从上到下,原子半径逐渐。
同周期,从左到右,原子半径逐渐。
2、离子半径大小的比较(1)具有相同电子层结构的离子半径大小的比较电子层数相同,随着核电荷数的增加,原子核对核外电子的吸引能力,半径。
比较微粒半径:O2-、F-、Na+、Mg2+比较微粒半径:S2-、Cl-、Na+、Mg2+(2)同主族离子半径大小的比较元素周期表中从上到下,电子层数逐渐,离子半径逐渐。
比较微粒半径:Li+、Na+、K+(3)同一元素的不同离子的半径大小比较同种元素的各种微粒,核外电子数越多,半径,高价阳离子半径低价离子半径。
比较微粒半径:Na、Na+ 比较微粒半径:Fe3+、Fe2+、Fe【自主探究】):①②③⑴半径最小的是________ ⑵具有最低负化合价的是___________⑶只有还原性的是______ ⑷只有氧化性的是_______【自我测试】1.核电荷数为16和核电荷数为4的元素的原子相比较,前者的下列数据是后者的4倍的是() A.电子数 B.最外层电子数 C.电子层数 D.次外层电子数2.下列数字为几种元素的核电荷数,其中原子核外最外层电子数最多的是( )A.8 B.14 C.16 D.173.某原子核外共有n个电子层(n>3),则(n一1)层最多容纳的电子数为 ( )A.8 B.18 C.32 D.2(n一1)24.A、B两原子,A原子L层比B原子M层少3个电子,B原子L层电子数恰为A原子L层电子数的2倍,则A、B分别是 ( )A.硅和钠 B.硼和氮 C.碳和氯 D.碳和铝5.某元素原子的最外层电子数为次外层电子数的3倍,则该元素原子核内质子数为()A.3 B.7 C.8 D.106.甲、乙两种微粒都只含有一个原子核,且核内具有相同数目的质子,这两种微粒一定是()A.同种原子 B.同种元素 C.互为同位素 D.具有相同的核外电子排布7.A、B两元素,元素A的核电荷数为a,且A3-与B n+的电子排布完全相同,元素B的核电荷数为() A.a—n一3 B.a +n+3 C.a+n一3 D.a—n+38.由短周期两种元素形成化合物A2B3,A3+比B2-少一个电子层,且A3+具有与Ne原子相同的核外电子层结构,下列说法正确的是 ( )A.A2B3是三氧化二铝 B.A3+与B2-最外层上的电子数相同C.A是第2周期第ⅢA族的元素 D.B是第3周期第ⅥA族的元素-1- -2-。
湖南名校集体备课教案 1.2元素周期律 第一课时

《元素周期律》教案第一课时一、三维目标(一)知识与技能1.原子半径、元素的化合价、元素的金属性和非金属性随着元素原子核外电子排布的周期性变化;2.掌握元素周期律的实质。
(二)过程与方法运用实验探究、结合有关数据认识元素周期律;模拟周期律的发现过程,体会科学发现的艰辛。
(三)情感态度与价值观引导学生树立由量变到质变以及“客观事物本来是相互联系的和具有内部规律的”辩证唯物主义观点。
三、教学重难点教学重点:原子半径、元素的化合价、元素的金属性和非金属性随着元素原子核外电子排布的周期性变化而呈周期性变化的规律。
教学难点:掌握元素周期律的实质。
四、教学过程【引入新课】我们已经知道,原子是由原子核和电子构成的,原子核的体积很小,仅占原子体积的几千亿分之一,电子在核外空间作高速的运动。
那么,电子的运动与宏观物体的运动有何不同?我们又怎样来描述核外电子的运动呢?核外电子又对元素性质有怎样的作用呢?【板书】元素周期律一、原子核外电子的排布1.核外电子运动特征【讨论】宏观物体的运动特征。
【总结】可以准确地测出它们在某一时刻所处的位置及运动的速度;可以描画它们的运动轨迹。
【讨论】微观粒子(电子)的特征:【投影】(1)电子的质量极微小(9.109×10-31 kg);(2)电子绕核运动是在原子这样极其微小的空间(原子的直径约10-10 m)中进行;(3)电子绕核作高速运动(运动的速度接近光速,约为108 m/s)【讨论】根据刚才介绍的情况,请问核外电子运动有什么显著特征呢?(引导学生讨论)【投影】电子绕核运动没有确定的轨道,不能精确测定或计算电子在任一时刻所在的位置,也不能描绘出其运动轨迹。
我们只能指出它在核外空间某处出现机会的多少。
【注意】电子绕核运动没有确定的轨道,但并不是说电子绕核运动没有什么规律。
【过渡】那么核外电子运动的规律是什么呢?【讲述】在含多个电子的原子中,有些电子能量较低,在离核较近的区域里运动;有些电子能量较高,在离核较远的区域里运动。
第一节 元素周期表(第一课时)

收集具代表性的由学生所编制的周期表,请 大家讨论交流周期表的编排,哪一种更为合 理呢?
周期表具有哪些编排原则?
(师生合作讨论)
1869年德米特里· 伊万诺维奇· 门捷 列夫在继承和分析了前人工作的基 础上,对大量实验事实进行了订正、 分析和概括,成功地对元素进行了 科学分类。 他总结出一条规律:元素(以及 由它所形成的单质和化合物)的 性质随着相对原子质量的递增而 呈现周期性的变化。这就是元素 周期。 他还预言了一些未知元素的性质 都得到了证实。但是由于时代的局 限,门捷列夫揭示的元素内在联系 的规律还是初步的,他未能认识到 形成元素性质周期性变化的根本原 因。
10 8
109
110
111
112
过渡元素
66 98 67 99 68 100 69 101 70 102 71 103
57 89
58 90
59 91
60 92
61 93
62 94
63 95
64 96
65 97
元素周期表的结构 —— 周期
第1周期:2 种元素
短周期
第2周期:8 种元素 第3周期:8 种元素 第4周期:18 种元素
七主七副一零一八
主族副族的对比
主
定 表 个 义 示 数
族
副
族
长短周期共同组成 IA、IIA、… 7
仅由长周期组成 IB、IIB、… 7
【思考与交流】
(一)、分二小组讨论 小组1:请你描述出Na、C、Al在周期表的位置, 并思考它们的化合价与原子结构有何关系?为什 么我们将稀有气体元素称为零族元素? 小组2:元素在周期表中的位置与原子结构有什么 关系?你觉得记住元素周期表重要吗?请 说说 原因。 (二)、选代表汇报,全班交流
元素周期律(第一课时)教案.doc

元素周期律(第一课时)教案教学内容元素周期律教学目标知识1.使学生了解元素原子的核外电子排布、原子半径、主要化合价的周期性变化规律2.认识元素性质的周期性变化是元素原子核外电子排布周期性变化的结果,从而理解元素周期律的实质。
能力通过元素周期律的推出及运用,初步培养学生抽象归纳以及演绎推理能力;在学习中提高自学能力和阅读能力德育结合元素周期律的学习,使学生初步掌握从大量的事实和资料中分析总结规律、透过现象看本质、宏观与微观相互转化等科学抽象方法。
教学重点原子的核外电子排布和原子半径变化的规律。
教学难点原子半径变化的规律,元素周期律的实质。
教师活动学生活动设计意图[课前情景]放映钟表,时间的周期性变化,的flash.[引入] 四季的轮回,年复一年,日复一日,这些描述时间的词语,都体现了时间变化的一个典型的特点——周期性,这节课,我们将通过元素周期律的学习来研究元素性质的变化特点,总结其规律。
[幻灯片]第二节元素周期律[讲述]为了更方便的研究元素的性质的变化规律,我们引入原子序数的概念[幻灯片]一、原子序数按照核电荷数有小到大的顺序给元素编号,这种编号,叫做原子序数。
[提问]根据原子序数的概念,思考:它与原子组成粒子的数量有什么关系?数值上原子序数=核电荷数=质子数意义上并不相同二、原子结构和性质的递变规律[练习)]写出1~18号元素的原子序数、元素名称、元素符号。
[幻灯片] 1~18号元素的原子序数、元素名称、元素符号。
请同学们对照,自己写得对不对。
[讲述]今天要讲的是元素性质的递变规律,我问什么要大家写原子结构是意图呢?这二者有什么关系呢?[学生回答]结构决定了元素的性质。
所以要研究性质必须先研究结构。
[总结学生的回答]很好,说得全面。
就构决定性质![提问]那么,现在为了研究元素的性质,我们一起来找找看元素的结构随着原子序数的增加有什么变化。
请同学们观察你们手中的原子结构够示意图,总结其变化规律。
新人教版高中化学必修2教案-元素周期律 (第1课时)

元素週期律教學目標1、瞭解元素原子核外電子排布,2、培養學學生分析問題,總結歸納的能力。
重點難點元素原子核外電子排布教學過程[引言]我們已學習了元素週期表的結構,那麼這張表又有何意義呢?我們能否從其中總結出元素的某些性質規律,以方便我們應用,解決新的問題呢?這就是我們本節課所要研究的內容。
[板書] 第二節元素週期律[教師]元素的性質是由組成該元素的原子結構決定的,因此我們討論性質之前,必須先來熟悉一下原子的結構。
[展示]電子層模型示意圖[講解]原子是由原子核和核外電子構成的,原子核相對於原子很小,即在原子內部,原子核外,有一個偌大的空間供電子運動。
如果核外只有一個電子,運動情況比較簡單。
對於多電子原子來講,電子運動時是否會在原子內打架呢?它們有沒有一定的組織性和紀律性呢?下麵我們就來學習有關知識。
[板書]一、原子核外電子的排布[講解]科學研究證明,電子的能量是不相同的,它們分別在能量不同區域內運動。
我們把不同的區域簡化為不連續的殼層,也稱作電子層,分別用n=1、2、3、4、5、6、7來表示從內到外的電子層,並分別用符號K、L、M、N、O、P、Q來表示。
通常,能量高的電子在離核較遠的區域運動,能量低的電子在離核較近的區域運動。
這就相當於物理學中的萬有引力,離引力中心越近,能量越低;越遠,能量越高。
[講解並板書]1、電子層的劃分電子層(n) 1、2、3、4、5、6、7電子層符號 K、L、M、N、O、P、Q離核距離近遠能量高低低高[設疑]由於原子中的電子是處於原子核的引力場中,電子總是盡可能的從內層排起當一層充滿後在填充下一層。
那麼,每個電子層最多可以排布多少個電子呢?核外電子的分層排布,有沒有可以遵循的規律呢?[思考]下麵請大家分析課本12頁表1-2,根據原子光譜和理論分析得出的核電荷數為1-20的元素原子核外電子層排布,看能不能總結出某些規律。
[學學生活動][講解並板書]2、核外電子的排布規律(1)各電子層最多容納的電子數是2n2個(n表示電子層)(2)最外層電子數不超過8個(K層是最外層時,最多不超過2個);次外層電子數目不超過18個,倒數第三層不超過32個。
元素周期律和元素周期表(第一课时)

全国“教学中的互联网搜索”优秀教案评选材料元素周期律和元素周期表(第一课时)【教案的背景】:我校实行368教学模式,创设优质高效课堂,高一化学教研组在学校368教学模式下,结合学科的特点,在小组合作学习的情况下,实行问题驱动型教学模式,其原理是将主干知识,以问题的形式展示出来。
学生通过小组合作讨论解答学案上设计的问题,将主干知识构建成统一体系。
【教学的课题】:《化学必修2》(鲁科版)2007年7月第3版2011年第13次印刷。
第一章第2节元素周期律和元素周期表(第一课时)元素周期律【教材的分析】:元素周期律和周期表是《化学必修2》第一章第2节内容。
本节教材在编写上特别注意培养学生的三维目标,通过本节课的学习,学生要学会总结归纳,具有一定的绘图和识图能力。
教材在设计材料时,注意让学生进行探究,然后总结归纳出元素的性质(最外层电子排布、原子半径、主要化合价)和原子结构的关系,随着原子序数变化的关系,最后归纳出元素周期律,揭示元素周期律的实质。
元素周期律是元素周期表编排的基础,元素周期律的学习要为元素周期表的学习打下基础,做好铺垫。
元素周期律学习对于第三节元素周期表的应用的学习也起重要的作用,在帮助学生建立“位-构-性”三者的关系,也具有一定的指导作用。
【教学方法】使用问题驱动,小组合作讨论,教师精讲点拨。
【学习过程】【预习学案】1、钠原子的原子结构示意图2、原子序数是 ,它与原子的核电荷数、质子数、核外电子数的关系。
3、随着原子序数的递增元素原子的、、均呈的变化,在大量科学研究基础上,人们归纳出一条规律,元素性质随元素原子序数的递增而呈现周期性的变化,这个规律叫其根本原因是核外电子排布的周期性变化。
3、1-18号元素①一般情况下,电子层数性同时,随着核外电荷数的递增原子半径逐渐②一般情况下,最外层电子数相同时,随着核电荷数的递增,原子半径逐渐③稀有气体原子半径与相邻原子半径比较,半径特别大。
4、1-18号元素的化合价随原子序数的增加有什么变化特征:(同一行即电子层相同)元素原子的最高化合价由逐渐增大到;最低负价由逐渐增大到最高正价数= 最高正价和最高负价的绝对值之和=【教学过程】元素周期律和元素周期律表(第一课时)【学习目标】(1)知识与技能目标掌握元素原子核外电子排布、原子半径、主要化合价的周期性变化,认识元素周期律的实质。
元素周期律(第一课时)教案

元素周期律(第一课时)教案一、教学目标本课时的教学目标是让学生了解元素周期律的基本思想和周期表的组成,掌握元素周期律的基本规律,同时也能够了解元素周期律的历史背景和发展过程。
二、教学重点和难点1. 教学重点:元素周期律的基本思想和周期表的组成,元素周期律的基本规律。
2. 教学难点:周期表对元素性质的预测和周期律的历史背景。
三、教学过程【导入】1. 通过图片展示和简单的活动,学生们了解有哪些元素以及它们分别的性质,引发学生们对于元素性质变化的思考,为引入元素周期律做铺垫。
2. 色码表的制作,让学生自行收集不同颜色的小球,为下一环节的分类打下基础。
【展开】1. 通过对于普朗克、门捷列夫、柯西和门德里夫提出的元素周期律做简单的介绍,引导学生理解周期律的基本思想和周期表的组成。
2. 解释周期表中元素的排列方式,回顾周期表中元素分类的基本方式和命名规律,让学生们掌握元素周期律的基本规律。
3. 进一步讲解元素周期律中元素性质的预测,让学生了解周期表的应用和实用价值。
4. 分组或自由活动,让学生们通过分析周期表中元素性质的变化以及不同元素之间的联系,探究元素周期律的更深层次的规律。
同时以简单易懂的例子,帮助学生理解元素周期规律。
【总结】1. 回顾教学目标,帮助学生梳理课程内容,巩固所学的知识和技能。
2. 对元素周期律在实际应用中的重要性做简单介绍。
四、教学反思在本课程的教学中,我重点强调了元素周期律的基本规律以及周期表的组成,同时也帮助学生理解了元素性质的预测和周期律的历史背景。
通过让学生进行分类活动和探究活动,培养了学生的合作能力和思考能力,并且让学生深入理解了元素周期律所涉及的知识点。
在未来的教学中,我会更注重教学重难点与生活联系的整合以及教学形式的多样化,保障学生更好的学习效果。
1.2.1元素周期律(第一课时教案)
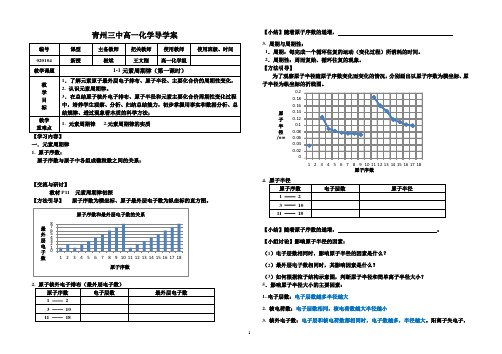
青州三中高一化学导学案编号 课型 主备教师 把关教师 使用教师 使用班级、时间020104 新授崔斌王文刚高一化学组教学课题 1-1元素周期律(第一课时)教 学 目 标 1.了解元素原子最外层电子排布、原子半径、主要化合价的周期性变化,2. 认识元素周期律。
3.在总结原子核外电子排布、原子半径和元素主要化合价周期性变化过程中,培养学生观察、分析、归纳总结能力,初步掌握用事实和数据分析、总结规律、透过现象看本质的科学方法; 教学 重难点1. 元素周期律2.元素周期律的实质【学习内容】 一.元素周期律 1. 原子序数:原子序数与原子中各组成微粒数之间的关系:【交流与研讨】教材P11 元素周期律初探【方法引导】 原子序数为横坐标、原子最外层电子数为纵坐标的直方图。
12345678123456789101112131415161718最外层电子数原子序数原子序数和最外层电子数的关系2. 原子核外电子排布(最外层电子数)原子序数 电子层数最外层电子数1 ——23 —— 10 11 —— 18【小结】随着原子序数的递增, 3. 周期与周期性:1.周期:每完成一个循环往复的运动(变化过程)所消耗的时间。
2.周期性:周而复始、循环往复的现象。
【方法引导】为了观察原子半径随原子序数变化而变化的情况,分别画出以原子序数为横坐标、原子半径为纵坐标的折线图。
4. 原子半径原子序数 电子层数原子半径1 ——23 —— 10 11 —— 18【小结】随着原子序数的递增, 。
【小组讨论】影响原子半径的因素:(1)电子层数相同时,影响原子半径的因素是什么? (2)最外层电子数相同时,其影响因素是什么?(3)如何根据粒子结构示意图,判断原子半径和简单离子半径大小?5.影响原子半径大小的主要因素: 1..电子层数:电子层数越多半径越大2. 核电荷数:电子层数相同,核电荷数越大半径越小3. 核外电子数:电子层和核电荷数都相同时,电子数越多,半径越大。
《主题一 第二节 元素周期律》教学设计

《元素周期律》教学设计方案(第一课时)一、教学目标1. 知识与技能:理解元素周期表的结构,掌握周期和族的含义,理解元素周期律的内容。
2. 过程与方法:通过观察、分析、归纳等学习方法,了解元素性质与核外电子排布的干系。
3. 情感态度与价值观:培养学生的观察能力及总结归纳能力,激发学生对化学学科的兴趣。
二、教学重难点1. 教学重点:理解元素周期表的结构,掌握周期和族的含义,理解元素周期律的内容。
2. 教学难点:通过观察、分析、归纳等学习方法,总结元素性质与核外电子排布的干系。
三、教学准备1. 准备教学用具:PPT课件、元素周期表、图片、实验器械等。
2. 准备教学内容:准备好相关的元素周期律的教学视频、案例及实验。
3. 预习要求:学生在课前预习元素周期表及元素周期律的相关知识,以便更好地参与教室讨论。
四、教学过程:(一)导入新课1. 回顾初中化学中学习过的元素,请学生列举出一些熟悉的元素及其化合物。
2. 提问:同砚们知道这些元素及其化合物之间存在哪些规律吗?3. 引入课题:元素周期律。
(二)新课教学1. 讲授元素周期表的结构和分类,让学生了解周期表中的横行代表周期,纵列代表族。
2. 介绍周期表中金属元素和非金属元素,并讲解同周期和同族元素之间的递变规律。
3. 结合周期表,讲解同周期元素原子核外电子层数和最外层电子数的变化规律,以及同主族元素原子最外层电子数和原子半径的变化规律。
4. 介绍元素金属性、非金属性以及原子得失电子的能力的观点和变化规律。
5. 通过实验演示,让学生观察金属钠与水反应的现象,并引导学生分析钠的性质和变化规律。
6. 引导学生自主探究其他元素的性质和变化规律,并尝试总结出元素周期律的普遍规律和特殊性。
7. 分组讨论:在周期表中某些区域的性质变化规律。
8. 请学生发言,分享自己的探究效果和总结,并由教师进行点评和补充。
(三)教室小结1. 回顾元素周期表的结构和分类。
2. 总结元素周期律的主要内容和变化规律。
元素周期律(第1课时)教学案

课题:第四章第二节元素周期律(第1课时)教学案课标要求1.通过对“同周期元素性质”的学习,培养科学探究和创新意识。
2.通过对“元素周期律内容和实质”的学习,建构微观原子结构特点决定宏观性质的探究思路和模式。
学习目标认识同周期元素的核外电子排布、主要化合价、原子半径等性质的周期性变化规律。
教学重难点同周期、同主族元素性质【情景导入】【问题探究1】原子结构的周期性变化决定反映元素性质的周期性变化归纳出反映元素周期律1.根据P、S、Cl在周期表中位置进行比较(1)H3PO4、H2SO4、HClO4酸性强弱。
(2)P3-、S2-、Cl-还原性强弱。
2.试根据同周期元素非金属性的变化规律,比较SiH4、PH3、H2S和HCl的稳定性。
探究提示:1.(1)非金属性:Cl>S>P,酸性:HClO4>H2SO4>H3PO4。
(2)非金属性:Cl>S>P,还原性:P3->S2->Cl-。
2.元素的非金属性越强,气态氢化物越稳定。
同周期元素,随着原子序数的递增,非金属性逐渐增强,故非金属性:Si<P<S<Cl,所以它们的氢化物的稳定性顺序为SiH4<PH3<H2S<HCl。
【问题探究2】1.第三周期元素的阳离子半径从左到右逐渐减小,对吗?提示:对。
第三周期元素的阳离子从左到右分别是钠离子、镁离子和铝离学习过程设计核外电子是处在一定的轨道上绕核运行的,正如太阳系的行星绕太阳运行一样;核外运行的电子分层排布,按能量高低而距核远近不同。
这个模型被称为“玻尔原子模型”。
现代物质结构理论在新的实验基础上保留了“玻尔原子模型”合理的部分,并赋予其新的内容。
你想知道核外电子是如何排布的吗?请让我们一起走进教材学习元素性质的周期性变化规律。
氢化物稳定性增强减弱还原性减弱增强最高价氧化物的水化物酸性增强减弱碱性减弱增强【归纳总结】(1)主族元素的最高正价=最外层电子数(O、F除外)。
(2)只有非金属才有负价,且|最低负价数值|+|最高正价数值|=8。
元素周期律第一课时

越小
如 Na > Mg > Al
F < O < N <C
⑶电子层数和核电荷数都相同 (同种元素)时,再看核外电子数
Mg
+12
+11
Na
(或最外层电子数),核外电子数
(或最外层电子数越多), 则半径 越大
Cl
+17
+17
Cl-
如 Cl < Cl-
下列各组微粒半径大小比较中,不正确的是( AB ) A. r(K+) > r(K) C.r(Na+) > r(Mg2+) > r(Al3+) B. r(Mg2+) > r(Na+) > r(F-) D.r(Cl -) > r(F-) > r(F)
4. B原子核外M层电子数是L层电子数的1/2,则B 是 。
科学探究一 元素核外电子排布情况 1—2号元素,从H到He只有1个
电子层,最外层电子数目由1 11—18号元素,从Na 到Ar有3个电子层, 个增加到到 2到 个,而达到稳定 3—10 号元素,从Li Ne有2个电子层, 随原子序数的增大,最外层电子数目由 随原子序数的增大,最外层电子数目 1个增加到结构 8个,而达到稳定结构
核外电子排布的一般规律
核外电子总是尽先排布在 能量最低 的电子 层里,排满一层后再排下一层;
1→2→3→ 4→ 5→6 → 7 K→L→M→N→O→P→Q 每层电子不能超过 2n2 个;
最外层电子不能超过 8 个(K层是最外层时不 超过 2 个),次外层电子不能超过 18 个,
倒数第三层电子不能超过
由1个增加到8个,而达到稳定结构
元素周期律(第一课时--推荐)教案--优秀.doc

元素周期律(第一课时)教案教学内容元素周期律教学目标知识1.使学生了解元素原子的核外电子排布、原子半径、主要化合价的周期性变化规律2.认识元素性质的周期性变化是元素原子核外电子排布周期性变化的结果,从而理解元素周期律的实质。
能力通过元素周期律的推出及运用,初步培养学生抽象归纳以及演绎推理能力;在学习中提高自学能力和阅读能力德育结合元素周期律的学习,使学生初步掌握从大量的事实和资料中分析总结规律、透过现象看本质、宏观与微观相互转化等科学抽象方法。
教学重点原子的核外电子排布和原子半径变化的规律。
教学难点原子半径变化的规律,元素周期律的实质。
教师活动学生活动设计意图[课前情景]放映钟表,时间的周期性变化,的flash.[引入] 四季的轮回,年复一年,日复一日,这些描述时间的词语,都体现了时间变化的一个典型的特点——周期性,这节课,我们将通过元素周期律的学习来研究元素性质的变化特点,总结其规律。
[幻灯片]第二节元素周期律[讲述]为了更方便的研究元素的性质的变化规律,我们引入原子序数的概念[幻灯片]一、原子序数按照核电荷数有小到大的顺序给元素编号,这种编号,叫做原子序数。
[提问]根据原子序数的概念,思考:它与原子组成粒子的数量有什么关系?数值上原子序数=核电荷数=质子数意义上并不相同二、原子结构和性质的递变规律[练习)]写出1~18号元素的原子序数、元素名称、元素符号。
[幻灯片] 1~18号元素的原子序数、元素名称、元素符号。
请同学们对照,自己写得对不对。
[讲述]今天要讲的是元素性质的递变规律,我问什么要大家写原子结构是意图呢?这二者有什么关系呢?[学生回答]结构决定了元素的性质。
所以要研究性质必须先研究结构。
[总结学生的回答]很好,说得全面。
就构决定性质![提问]那么,现在为了研究元素的性质,我们一起来找找看元素的结构随着原子序数的增加有什么变化。
请同学们观察你们手中的原子结构够示意图,总结其变化规律。
元素周期表(第一课时)

二、编排原则 1、按照原子序数(核电荷数)递增的顺序从左到右排列。 2、将电子层数相同的元素,按原子序数递增的顺序从 左到右排成一横行—周期。 3、把最外层电子数相同的元素,按电子层数递增的顺 序由上而下排成一纵行—族。
三、元素周期表的结构
1、周期 周期序数 = 电子层数
①元素周期表中具有相同的电子层数的元素,
N : +7 2 5
O : +8 2 6
F : +9 2 7 Ne : +10 2 8
Na : +11 2 8 1 Mg :+12 2 8 2 Al : +13 2 8 3 Si : +14 2 8 4
P : +15 2 8 5 S : +16 2 8 6 Cl : +17 2 8 7 Ar : +18 2 8 8
57
6 55 56 - 72 73 74 75 76 77 78 79 80 81 82 83 84 85 86
71
18 32
7 87
88
89103
104
105
106
107
108
109
110
111
112
【小结】对于ⅢA到ⅦA族, 同主族相邻元素的原子序数相差下一周期所容纳元素种。类
2、同主族相邻元素的原子序数之差:
8 5 6 7 8 9 10
III IV V VI VII
3 11 12 B B B B B
VIII
8 IB
II B
13 14 15 16 17 18
M L k
18 4 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36
2020-2021学年人教版新教材必修第一册 第4章第2节 元素周期律(第1课时) 课件(53张)

新知预习 一、原子结构的周期性变化
结合图1、图2、图3完成下表:
原子 电子 序数 层数
最外层 电子数
原子半径的变化(稀 有气体元素除外)
最高或最低化合价的变化
1~2
1
1~2
+1→0
3~10
__2___
___1_~__8__
三、元素周期律 1.内容:元素的性质随着原子序数的递增而呈周期性的变化。 2.实质:元素性质的周期性变化是原子的___核__外__电__子__排__布___的周期 性变化的必然结果。
预习自测
1.判断正误(正确的打“√”,错误的打“×”)。
(1)同周期元素,从左到右,原子半径逐渐减小,离子半径也逐渐减
与氢气反应
由难到易的顺序为_______S_i<_P__<_S_<_C_l_______
最高价氧化 物对应的水 化物的酸性
结论
H2SiO3: 弱酸
H3PO4:中强酸
H2SO4:强 HClO4:强
酸
酸
酸性:____H__C_l_O_4_>__H_2_S_O__4>__H__3_P_O_4_>__H__2S_i_O_3______
6.门捷列夫对化学这一学科发展的最大贡献在于发现了化学元素周
期律。下列事实不能用元素周期律解释的只有
(C )
A.碱性:KOH>Ca(OH)2>Mg(OH)2 B.稳定性:H2O>H2S>H2Se C.挥发性:HNO3>H3PO4>H2SO4 D.原子半径:P>S>Cl
解析:酸的挥发性是物质本身的特性,没有规律,所以选C。
课堂素能探究
知识点 一
元素周期律(第一课时)教案

元素周期律(第一课时)教案篇一:元素周期律(第一课时)教案必修2 第一章物质结构元素周期律第二节元素周期律(第一课时)一、教材分析:通过初三和必修I的学习,学生已经基本具备了一定的无机化学基础知识。
例如初三学习的原子的构成、核外电子排布、元素周期表简介等一些基本的物质结构知识,这些为本章的学习奠定了一定的基础。
在本章中,这些知识将更加细化,理论性更强,体系更加完整。
通过《物质结构元素周期律》的学习,可以使学生对于所学元素化合物等知识进行综合、归纳。
同时,作为理论指导,学生能更好的把无机化学知识系统化、网络化。
在物质结构的基础上,将元素周期表的学习和元素周期律的学习结合起来,将学生在初中和必修I中所学习的氧化还原反应和许多元素化合物的知识连汇贯通。
在第三节,通过化学键的学习,可以为今后有志深入学习化学的同学打下一定的基础。
总之,本章内容既是必修的重要理论内容,也是为选修内容的学习打下良好的基础。
二、教学目标:知识目标:1、知道元素原子核外电子排布规律;2、掌握元素原子核外电子排布、原子半径、主要化合价周期性变化。
能力目标:提高学生们归纳整理的能力。
情感、态度、价值观目标:学会总结,学会概括,体会结构决定性质的理念。
三.教学重点难点:重点:元素原子核外电子排布、原子半径、主要化合价周期性变化。
难点:知道元素原子核外电子排布规律。
四、学情分析:通过初三和必修I的学习,学生已经基本具备了一定的无机化学基础知识。
例如初三学习的原子的构成、核外电子排布、元素周期表简介等一些基本的物质结构知识,这些为本章的学习奠定了一定的基础。
五、教学方法:学案导学六、课前准备:学生学习准备:导学案- 1 -教师教学准备:投影设备七、课时安排:一课时八、教学过程:(一)、检查学案填写,总结疑惑点(主要以学生课前板书答案展示的方式)(二)、情景导入,展示目标:老师:原子结构大家在初中就已经了解了,刚才通过同学们对导学案的展示已经对原子结构了解的不成问题了,那么核外电子具体怎样排布?有什么规律特点,以及元素周期表能够体现出哪些结构规律,与元素性质规律有什么联系,是我们这节课要探讨的内容。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
云课堂核心理念:整合资源教自主合作学教师点拨导当堂分层练云课堂导学案....据此设计配套课件
正 价 最 低
负 价
结论2:随着原子序数的递增,元素 也呈现周期性变化。
[深入探究](1)分析原子序数为11~17的非金属元素的最高正化合价和最低负化合价的变化规律得出二者的关系________________________________________________
(2)原子序数为11~17的主族元素的最高正化合价和最低负化合价的数值与原子最外层电子数的关系是
_________ 3原子半径的周期性变化
规律:同一周期元素,随着原子序数的递增,元素原子半径逐渐 (___________外)。
结论3同一周期元素,随着原子序数的递增,元素____________________呈现周期性变化 归纳::随着______________的递增,元素原子的 ____ 、 _______ 、 ________________都呈现周期性变化。
元素符号 H He 原子半径nm 0.037 ─ 元素符号 Li
Be
B
C N
O
F
Ne
原子半径nm 0.152 0.089 0.082 0.077 0.075 0.074 0.071 ─ 元素符号 Na
Mg
Al
Si
P
S
Cl
Ar
原子半径nm
0.186 0.160 0.143 0. 117 0.110 0.102 0.099 ─
四、小结:本节课主要内容(重点展示): 同周期元素性质递变规律
D 、堂清训练卷(分ABC 三个等级,时值约15分钟)
基础巩固(A )
1下列微粒结构示意图表示的各是什么微粒?
A B C D
能力提升(B)
2.下列递变情况中不正确的是()
A.钠、镁、铝原子的最外层电子数依次增多
B.硅、磷、硫、氯元素的最高正化合价依次升高
C.碳、氮、氧、氟的原子半径依次增大
D.锂、钠、钾、铷的电子层数依次增多
思维拓展(C)
3.某元素原子核外有3个电子层,该元素最高正化合价与最低负化合价绝对值相等,则这种元素的名称是,元素符号为,最高价氧化物的化学式为,气态氢化物的化学式为。
E、日清测试卷(分ABC三个等级,时值约20分钟)
基础巩固(A)
1.下列有关原子核外电子排布说法错误的是()
A.在多电子原子中,电子的能量不同,电子分层排布
B.原子核外电子层由内到外能量越来越高
C.电子总是尽可能地先从内层排起,当一层充满后再填下一层
D每个电子层填充的电子数为2n2(n为电子层数)
知识点: 原子核外电子排布规律
2、某元素的原子核外有3个电子层,M层有4个电子,该原子核内的质子数为()
A、14
B、15
C、16
D、17
知识点: 原子核外电子排布规律
3.下列微粒结构示意图是否正确?如有错误,指出错误的原因。
知识点: 原子核外电子排布规律
4下列微粒结构示意图表示的各是什么微粒?
A B C D
知识点: 原子核外电子排布规律
5.最外层电子数为4的原子,其荷电核数可能为()
A.14
B.8
C.6
D.17
知识点: 原子核外电子排布规律
6.质量数为37的原子应该有()
A.18个质子,19个中子,19个电子
B.17个质子,20个中子,18个电子
C.19个质子,18个中子,20个电子
D.18个质子,19个中子,18个电子
知识点: 质量数与中子,电子、质子数之间关系。
7.和氖原子电子层结构相同的微粒是()
A.Na+
B.Cl-
C. K+
D.Ar
知识点: 原子核外电子排布规律
能力提升(B)
9从原子序数11依次增加到17,下列所叙递变关系错误的是( )
A.电子层数逐渐增多
B.原子半径逐渐增大
C.最高正价数值逐渐增大
D.从硅到氯负价从-4→-1
知识点:元素性质周期性变化规律
10原子序数为1~18的元素,随着核电荷数的递增而呈现周期性变化的是()A.电子层数 B.核外电子排布C .原子半径 D.元素主要化合价
知识点:元素性质周期性变化规律
11、下列元素中,原子半径最大的是()A.锂 B.钠 C.氟 D.氯
知识点:元素原子半径周期性变化规律
12、下列各组元素性质递变情况错误的是()
A.Li、Be、B原子最外层电子数依次升高
B.P、S、Cl元素最高正化合价依次升高
C. B、C、N、O、F原子半径依次升高
D. F 、Cl、Br的原子半径依次增大知识点:元素性质周期性变化规律
知识点:元素性质周期性变化规律
思维拓展(C)
13.以下说法正确的是()
A.原子序数越大,原子半径愈大
B.原子序数越大,原子半径愈小。
