金属的物理性质,和某些化学性质
实验活动4金属的物理性质和某些化学性质

1、某校化学活动小组为探究X、Y、Z三种金属与酸的反 应情况,进行了如下实验:取等质量的X、Y、Z分别与 足量的溶质质量分数相同的稀硫酸反应,都生成+2价金
属的硫酸盐,反应情况如图表示。下列对该图象理解的
叙述中,正确的是 (AD )多选
A、金属的活动性由强到弱:X、Z、Y B、金属的活动性由强到弱:X、Y、Z C、X、Y、Z依次可能是Mg、Zn、Fe D、相对原子质量的大小:Z > Y > X
实验活动4 金属的物理性质和某些化学性质
【实验用品】 试管、试管夹、酒精灯、电池、导线、 小灯泡、火柴。 镁条、锌粒、铝片、铁片、铁粉、铜 片、黄铜片(或白铜片)、稀盐酸、 稀硫酸、硫酸铜溶液、硝酸银溶液。
你还需要的实验用品:
.
【实验步骤】 1. 金属的物理性质 (1)观察并描述镁、铝、铁、铜的颜色和 光泽。
2. 金属的化学性质 (1)用坩埚钳夹取一块铜片,放在酒精 灯火焰上加热,观察铜片表面的变化。
铜片表面变黑
2Cu+ O2 == 2CuO
(2)向5支试管中分别放入少量镁条、铝片、 锌粒、铁片、铜片,然后分别加入5mL稀盐 酸(或稀硫酸),观察现象。如果有气体生 成,判断生成的气体是什么。
金属 镁 铝 锌 铁 铜
现象 迅速剧烈反应,产生大量的气泡 剧烈反应,产生大量的气泡 很快反应,产生大量的气泡 缓慢反应,有极少量气泡产生
没有明显变化
【问题与交流】 铁是银白色金属。在上述实验中,你观 察到的铁片和铁粉是什么颜色的?你有 什么问题?查阅资料,与同学交流。
铁粉:灰黑色 铁片:银白色
因为铁粉比较细,光学原因造成漫反射, 有很少的光可以进入我们的眼睛,所以 铁粉显黑色。
金属的物理化学性质

金属的物理性质1.金属光泽:(1)金属都具有一定的金属光泽,一般都呈银白色,而少量金属呈现特殊的颜色,如:金(Au)是黄色、铜(Cu)是红色或紫红色、铅(Pb)是灰蓝色、锌(Zn)是青白色等;(2)有些金属处于粉末状态时,就会呈现不同的颜色,如铁(Fe)和银(Ag)在通常情况下呈银白色,但是粉末状的银粉或铁粉都是呈黑色的,这主要是由于颗粒太小,光不容易反射。
(3)典型用途:利用铜的光泽,制作铜镜;黄金饰品的光泽也是选择的因素。
2.金属的导电性和导热性:(1)金属一般都是电和热的良好导体。
其中导电性的强弱次序:银(Ag)>铜(Cu)>铝(Al)(2)主要用途:用作输电线,炊具等3.金属的延展性:(1)大多数的金属有延性(抽丝)及展性(压薄片),其中金(Au)的延展性最好;也有少数金属的延展性很差,如锰(Mn)、锌(Zn)等;(2)典型用途:金属可以被扎制成各种不同的形状,金属金打成金箔贴在器物上4.金属的密度:(1)大多数金属的密度都比较大,但有些金属密度也比较小,如钠(Na)、钾(K)等能浮在水面上;密度最大的金属──锇,密度最小的金属──锂(2)典型用途:利用金属铝(Al)比较轻,工业上用来制造飞机等航天器5.金属的硬度:(1)有些金属比较硬,而有些金属比较质软,如铁(Fe)、铝(Al)、镁(Mg)等都比较质软;硬度最高的金属是铬(Cr);(2)典型用途:利用金属的硬度大,制造刀具,钢盔等。
6.金属的熔点:(1)有的金属熔点比较高,有的金属熔点比较低,熔点最低的金属是汞(Hg);熔点最高的金属是钨(W);(2)典型用途:利用金属锡(Sn)的熔点比较低,用来焊接金属金属的化学性质1.金属与氧气反应大多数金属在一定条件下,都能与氧气发生反应,生成对应的金属氧化物,也有少数金属很难与氧气发生化合反应。
如:“真金不怕火炼”,就是指黄金很难与氧气反应。
(1)金属镁与氧气发生反应实验现象:在空气中点燃镁带后,镁带剧烈燃烧,发出耀眼白光,放出白烟,生成一种白色固体。
《金属的物理性质和某些化学性质》教学设计

《金属的物理性质和某些化学性质》教学设计一、教学背景分析金属是化学元素中一类特殊的物质,具有独特的物理性质和化学性质。
在日常生活中,金属广泛应用于工业制造、建筑建设、电子设备等领域,对于学生了解金属的性质及其应用具有重要的意义。
二、教学目标1.了解金属的物理性质,包括导电性、导热性、延展性等;2.掌握金属的化学性质,如与酸、氧化剂等反应的特点;3.能够在实验中观察金属的性质变化,培养学生的实验操作能力和观察分析能力;4.培养学生的实验探究意识,激发学生对化学知识的兴趣。
三、教学内容和教学过程安排1.金属的物理性质(1)导电性、导热性:通过实验演示,让学生观察金属导电和导热的现象,引导学生讨论金属的导电性和导热性原理。
(2)延展性、塑性:让学生比较金属和非金属在延展性和塑性方面的差异,并进行实验验证。
2.金属的化学性质(1)与酸反应:演示金属与盐酸、硫酸等酸发生反应,观察产生气体和溶解现象,引导学生理解金属和酸的化学反应机理。
(2)与氧化剂反应:让学生观察金属与氧气或氯气等氧化剂的反应,了解金属氧化的过程及产物。
3.实验操作设计一系列实验,让学生自行操作实验装置,观察金属在不同条件下的性质变化,并记录实验现象和结论。
4.思考和讨论引导学生思考金属的性质是如何影响金属的应用和开发的,鼓励学生围绕金属的利用进行讨论和交流。
四、教学手段和教学资源1.实验仪器:导电仪、导热仪等。
2.实验药品:金属试样、酸、氧化剂等。
3.录像资料:展示金属的实验现象和化学反应过程。
4.课程材料:提供金属的物理性质和化学性质的相关知识点和实验步骤。
五、教学评价1.实验报告:要求学生按要求记录实验过程和结果,撰写实验报告。
2.课堂讨论:组织学生进行课堂讨论,评价学生对金属性质的理解和掌握程度。
3.作业考核:布置相关作业,考察学生对金属性质的掌握情况。
六、教学反思金属的物理性质和化学性质是化学教学中的重要内容,通过此次教学设计,我发现学生在实验中表现出极大的兴趣和积极性,并能够较好地理解和掌握金属的性质。
金属的化学性质和物理性质

金属的化学性质和物理性质金属是一类相对较常见的元素,它具有许多独特的化学和物理性质。
在本文中,我们将对金属的这些性质进行一些探讨和讨论,并进一步了解我们周围的世界。
一、金属的物理性质金属的物理性质包括密度、熔点、导电性、热导性、延展性和韧性等。
1. 密度金属的密度一般较高,具体数值因金属的种类不同而有所差异。
其中,铜的密度为8.96克/厘米立方,铁的密度为7.87克/厘米立方等,而同样是金属的碳密度则达到了2.23克/厘米立方。
总体来说,金属的密度比非金属要大得多,这与它们的原子结构有关。
2. 熔点金属的熔点通常很高,这是因为金属中的原子之间存在相对较强的金属键。
铁的熔点约为1538℃,铜则为1083℃,而金的熔点则更高,高达1064℃。
3. 导电性和热导性金属是优秀的导电体和热导体,这是因为它们的内部结构具有自由电子。
能够移动的自由电子可以在金属中自由流动,并且在电势差或温度梯度作用下,它们能够带动周围的离子发生运动。
这也是为什么金属制品比非金属制品更适合用作电线、电气设备和加热器等的原因。
4. 延展性和韧性大多数金属都具有出色的延展性和韧性。
它们能够被拉成长丝,压成薄片或弯曲而不会断裂或破碎。
这与金属中的原子的排列方式和结构有关。
二、金属的化学性质金属的化学性质也体现了本质上的一些特点,我们将以金属的腐蚀和氧化为例来探讨这些特点。
1. 腐蚀金属可以被氧气、水、酸和其他化学物质腐蚀,因为它们的表面容易被氧化或形成一层化学物质。
这点在日常生活中也有很多实例,比如生锈的铁器物、被腐蚀的铜器、年代久远的古币等等。
要避免这种情况,我们可以使用金属的保护措施,如电镀、镀金、涂漆等。
2. 氧化金属在遇到氧气时会发生氧化反应。
在这个过程中,金属会损失电子,被氧气氧化成离子的形式,它的表面也会形成一层氧化物。
这个过程可以被延缓或防止,例如使用保护剂,或者将金属的表面保持干燥、不受潮湿等等。
三、总结金属是具有广泛应用的一类元素,具有许多独特的物理和化学性质。
金属的物理性质和化学性质

金属的物理性质和化学性质金属是一类重要的物质,具有独特的物理性质和化学性质。
本文将就金属的这两个方面进行详细探讨。
一、金属的物理性质1. 密度和重量金属具有较高的密度,通常比非金属元素更重。
例如,铁的密度为7.87克/厘米立方(g/cm³),而氧气的密度仅为0.0013 g/cm³。
因此,金属在相同体积下比非金属更重。
2. 导电性和导热性金属是良好的导电体和导热体。
由于金属中的电子能在原子之间自由移动,所以金属能够很好地传导电流和热量。
这就解释了为什么金属常被用于电线、电路和散热器等电子设备中。
3. 延展性和铸造性金属具有较高的延展性和铸造性,能够以各种方式加工成不同形状的制品。
金属可以通过拉伸、锻造、挤压和压铸等方法改变其形状,使其适应各种需求。
这一特性使金属成为制造业中的重要材料。
4. 强度和韧性金属通常具有较高的强度和韧性。
强度指金属能够承受的外力,而韧性则是材料在受到外力时的变形程度。
金属的强度和韧性使其在建筑、机械和汽车等领域中得到广泛应用。
二、金属的化学性质1. 金属的活泼性金属常常具有较高的活泼性,容易与其他物质发生化学反应。
例如,钠是一种非常活泼的金属,在常温下可以与氧气反应生成氧化钠,并释放大量热量。
2. 金属的腐蚀性金属容易与氧气、水和酸等物质相互作用而发生腐蚀。
当金属表面暴露在湿氧气中时,会逐渐氧化生成金属氧化物,如铁锈。
为了防止金属的腐蚀,人们常采用涂层、镀层和防锈处理等方法。
3. 合金形成金属可以与其他金属或非金属元素形成合金。
合金是由两种或更多种金属混合而成的物质,具有优异的性质。
例如,铜与锌混合形成的黄铜具有较高的强度和耐腐蚀性。
总结:金属的物理性质和化学性质使其成为人类社会中不可或缺的重要材料。
金属的高密度、导电导热性、延展性和铸造性可满足各个领域的需求,而金属的活泼性、腐蚀性和合金形成等特性则赋予其更广泛的用途。
对金属的深入理解,有助于我们更好地利用和应用金属材料,推动科技和工业的发展。
实验活动4 金属的物理性质和某些化学性质 答案

1.铝、铜、铁、金四种金属具有相似的性质是()A.都是银白色的固体B.有导电性C.通常状况下能与氧气反应D.能和稀硫酸反应【解答】解:A、铝、铜、铁、金四种金属中,铝、铁是银白色的固体,铜是紫红色金属,金呈黄色,故选项说法错误.B、铝、铜、铁、金四种金属都具有良好的导电性,故选项说法正确.C、通常状况下铝、铜、铁能与氧气反应,金的化学性质不活泼,在高温时也不与氧气反应,故选项说法错误.D、位于氢前面的金属能置换出酸中的氢,铝、铁能与稀硫酸反应,铜、金不能与稀硫酸反应,故选项说法错误.故选:B.2.有甲、乙、丙三种金属,将甲、乙两种金属分别投入硫酸铜溶液中,甲的表面有红色物质析出,乙的表面没有明显变化.将丙投入甲的硫酸盐溶液中,有甲析出,则甲、乙、丙三种金属活动性顺序排列正确的是()A.甲>乙>丙B.甲>丙>乙C.乙>丙>甲D.丙>甲>乙【解答】解:由题意可知:将甲、乙两种金属分别投入硫酸铜溶液中,甲的表面有红色物质析出,乙的表面没有明显变化,说明甲>铜>乙;将丙投入甲的硫酸盐溶液中,有甲析出,说明丙>甲;则甲、乙、丙三种金属活动性顺序排列正确的丙>甲>乙;故选D.3.下列生活用品,主要利用金属具有良好导热性的是()A.铸铁炊具B.金属细丝C.铜制电缆D.铁锤【解答】解:A.因为铁能导热,所以可做成铁锅做饭;B.金属细丝利用了金属的延展性;C.铜制导线利用其导电性;D.铁锤利用了硬度大等性质.故选A.4.下列实验现象的描述错误的是()A.铁丝在氧气中燃烧火星四射B.镁条在空气中燃烧发出耀眼的强光C.铝丝伸入稀硫酸溶液中立即产生大量的气泡D.铜片投入稀硫酸中产生大量的气泡【解答】解:A、铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体,故说法正确;B、镁带在氧气中燃烧,发出耀眼的白光、放出大量的热、生成白色固体,故说法正确;C、铝能够和稀硫酸反应产生氢气,因此铝丝伸入稀硫酸溶液中立即产生大量的气泡,故说法正确;D、铜位于氢后,不能和稀硫酸反应,因此无现象,故说法错误;故选项为:D.5.在学习金属的化学性质时,老师给大家演示了如图所示的实验,下列说法正确的是()A.铜片表面始终没有明显变化B.一段时间后溶液由无色变为浅绿色C.反应后溶液中一定有硝酸铜,可能有硝酸银D.通过实验现象推测银和硫酸铜溶液也可以反应【解答】解:A、铜的表面有银白色物质生成,故A说法不正确;B、一段时间后溶液由无色变为蓝色,故B说法不正确;C、反应后溶液中一定有硝酸铜,可能有硝酸银,故C说法正确;D、通过实验现象推测铜比银活泼,银和硫酸铜溶液不可以反应,故D说法不正确.故选为:C.6.为了验证“Fe,Cu,Ag三种金属的活动性由强到弱”,小明设计了如图所示的实验,其中可以达到实验目的组合是()A.①②B.①③C.②④D.③④【解答】解:①中银不能与稀盐酸反应,说明银的金属活动性比氢弱,即H>银;②中铜不能与硫酸亚铁溶液反应,说明铜的金属活动性比铁弱,即Fe>Cu③中铁能与稀盐酸反应,说明铁的金属活动性比氢强,即Fe>H④铜能与硝酸银溶液反应,说明铜的金属活动性比银强,即Cu>Ag综合以上分析可知,②④的组合即可判断Fe,Cu,Ag三种金属的活动性由强到弱的顺序.故选C.7.等质量的甲、乙、丙三种金属的粉末,与足量的稀硫酸反应(反应后甲、乙、丙三种金属都显+2价),生成H2的质量与反应时间的关系如图所示,下列说法错误的是()A.三种金属的活泼性:乙>甲>丙B.生成氢气的质量:甲>乙>丙C.相对原子质量:甲>乙>丙D.消耗硫酸的质量:甲>乙>丙【解答】解:A、根据反应生成H2的质量与反应时间的关系图所示,当三种金属都在发生反应时,相同时间内乙放出氢气的质量大于甲、大于丙,可判断三种金属活动性顺序是乙>甲>丙,故说法正确;B、根据反应生成H2的质量与反应时间的关系图所示,在三种金属完全反应后,放出H2的质量是甲>乙>丙,故说法正确;C、三种金属的化合价、金属的质量都相等,完全反应放出氢气的质量与金属的相对原子质量成反比,即产生氢气多的相对原子质量小;根据反应生成H2的质量与反应时间的关系图所示,在三种金属完全反应后,放出H2的质量是甲>乙>丙,因此可判断相对原子质量是丙>乙>甲,故说法错误;D、金属与酸的反应生成氢气时,氢气来源于酸中的氢元素,所以生成的氢气与消耗的酸的多少顺序一致,消耗硫酸的质量:甲>乙>丙,故说法正确.故选C.8.请根据常见金属的活动性顺序回答:(1)在潮湿的空气中铁容易锈蚀而金不能,这是因为铁比金活泼(或铁的话动性比金强、金比铁稳定、在金属活动性顺序里铁排在金前面铁活泼、金稳定等合理即可);(2)在镁、铜、锌三种金属中.不能与稀硫酸发生置换反应的是铜(或Cu);(3)要比较铜和银的活动性,如果选用了铜,还需选用的一种盐溶液是硝酸银溶液(或AgNO3溶液、硝酸银、AgNO3).【解答】解:(1)铁的活动性比金强,容易与氧气反应,而金不容易与氧气反应,所以在潮湿的空气中铁容易锈蚀而金不能,所以本题答案为:铁比金活泼(或铁的话动性比金强、金比铁稳定、在金属活动性顺序里铁排在金前面,铁活泼、金稳定等合理即可);(2)在金属活动性顺序中,镁、铜、锌的活动性顺序为镁>锌>氢>铜,故铜不能与稀硫酸发生置换反应,所以本题答案为:铜(或Cu);(3)比较铜和银的活动性,可以采用金属与盐溶液反应的方法,选用了铜,则应该选择银的盐溶液,所以本题答案为:硝酸银溶液(或AgNO3溶液、硝酸银、AgNO3).9.回答下列与金属有关的问题.(1)铝合金和纯铝,硬度较大的是铝合金;(2)工业上,把赤铁矿冶炼成铁的主要反应原理是3CO+Fe2O32Fe+3CO2,其中Fe2O3发生了还原反应;(3)比较Mn、Pd(钯)、Cu三种金属的活动性顺序①将Mn片、Pd片分别加入到稀盐酸中,Mn片表面有气泡产生,Pd片没有变化.根据上述实验现象,得出的结论是Mn的活泼性比Pd强;②要确切得出这三种金属的活动性顺序,还需将Pd片加入到硫酸铜溶液中,观察现象.【解答】解:(1)一般说来合金的硬度一般比各成分金属大,合金的熔点一般低于组成它的成分金属的熔点.故填:铝合金;(2)根据高炉炼铁的原理:3CO+Fe2O32Fe+3CO2可知,在此反应中一氧化碳得氧发生了氧化反应,是还原剂;Fe2O3失氧发生了还原反应,是氧化剂;故填:Fe2O3(3)①将Mn片、Pd片分别加入到稀盐酸中,Mn片表面有气泡产生,Pd片没有变化,说明Mn的活泼性比Pd强.②要确切得出这三种金属的活动性顺序,还需将Pd片加入到铜盐中,如硫酸铜溶液中,观察Pd片表面是否有红色的金属铜出现,如有,说明Pd的活泼性比铜强,没有,则说明Pd的活泼性不如铜;故答案为:①Mn的活泼性比Pd强;②硫酸铜;10.如图,金属及金属材料在生产、生活中应用广泛.(1)铜可以拉成铜丝,这是利用金属的延展性.(2)铝具有很好的抗腐蚀性能,原因是4Al+3O2=2Al2O3(用化学方程式表示).(3)小明在学习金属的化学性质时,做了如下探究实验(金属片已打磨):①将铁片插入硫酸铜溶液中,铁片表面的现象是有紫红色的物质生成;②将铜片插入硝酸银溶液中,反应的化学方程式是Cu+2AgNO3=Cu(NO3)+2Ag.此探究实验的目的是探究铁、铜、银三种金属的活动性顺序.2【解答】解:(1)铜可以拉成铜丝,这是利用金属的延展性;(2)铝具有很好的抗腐蚀性能,原因是铝和氧气生成致密的氧化铝薄膜,化学方程式为4Al+3O2=2Al2O3;(3)①铁片和硫酸铜溶液反应生成铜和硫酸亚铁,所以将铁片插入硫酸铜溶液中,铁片表面的现象是有紫红色的物质生成;②铜片和硝酸银溶液生成银和硝酸铜,反应的化学方程式是Cu+2AgNO3=Cu(NO3)+2Ag.此探究实验的目的是探究铁、铜、银三种金属的活动性顺序.2故答案为:(1)延展性;(2)4Al+3O2=2Al2O3;(3)①有紫红色的物质生成;②Cu+2AgNO3=Cu(NO3)2+2Ag;探究铁、铜、银三种金属的活动性顺序.11.为探究锌、铜、镍三种金属的性质,某兴趣小组进行如下实验.【实验一】将三种金属丝分别与一节干电池和小电珠连接,小电珠发光.【实验二】取粗细、长短相同的锌丝、铜丝、镍丝均与50mL稀盐酸反应,实验记录如下:【实验三】金属锌、铜和稀盐酸构成如图所示的化学电池装置,观察到铜片表面有气泡(H2),小电珠发光.(1)实验一的现象说明三种金属都具有导电性.(2)镍与稀盐酸反应生成氯化镍(NiCl2)和氢气,反应的化学方程式是Ni+2HCl ═NiCl2+H2↑,铜不能与稀盐酸发生化学反应的原因是铜不活泼,在金属活动性顺序中排在氢的后面.(3)要判断三种金属活动性强弱,必须在实验二的基础上增补一个实验才能得出结论,其实验内容是把粗细、长短相同的锌丝、镍丝放入15%的50mL稀盐酸中,观察放出气泡的快慢.(4)金属活动性强弱是由金属物质的结构决定的,不会因某个实验而改变.下列关于实验三分析正确的是C(填选项).A.铜的金属活动性变得比锌强B.铜与稀盐酸发生了置换反应C.该装置将化学能转化为电能.【解答】解:(1)实验一的现象说明三种金属都具有导电性;(2)镍与稀盐酸反应生成氯化镍(NiCl2)和氢气,反应的化学方程式为:Ni+2HCl═NiCl2+H2↑;铜不能与稀盐酸发生化学反应的原因是:铜不活泼,在金属活动性顺序中排在氢的后面;(3)要判断三种金属活动性强弱,必须在实验二的基础上增补一个实验才能得出结论,其实验内容是:把粗细、长短相同的锌丝、镍丝放入15%的50mL稀盐酸中,观察放出气泡的快慢,放出气泡快并且多的金属活动性强;(4)A.铜的金属活动性比锌弱,该选项说法不正确;B.铜不能和稀盐酸反应,该选项说法不正确;C.该装置将化学能转化为电能,该选项说法正确.故填:导电;Ni+2HCl═NiCl2+H2↑;铜不活泼,在金属活动性顺序中排在氢的后面;把粗细、长短相同的锌丝、镍丝放入15%的50mL稀盐酸中,观察放出气泡的快慢;C.12.为探究Fe、Cu、Ag的金属活动性强弱,某兴趣小组做了如下实验:(1)实验前需将金属丝打磨,目的是除去金属表面的氧化膜.(2)甲实验中发生反应的化学方程式为Cu+2AgNO3═2Ag+Cu(NO3)2;乙实验中观察到的现象为铁丝的表面有一层红色物质,溶液由蓝色逐渐变为浅绿色.(3)通过甲、乙实验探究,可得出三种金属活动性由强到弱的顺序为Fe>Cu >Ag.(4)若采用丙实验方案也可得出相同结论,则金属C是Cu.【解答】解:(1)实验前需将金属丝打磨,目的是除去金属表面的氧化膜.(2)甲实验中铜能置换出硝酸银中的银,同时生成硝酸铜,发生反应的化学方程式为:Cu+2AgNO3═2Ag+Cu(NO3)2;乙实验中铁能置换出铜,同时生成了硫酸亚铁,观察到的现象为:铁丝的表面有一层红色物质,溶液由蓝色逐渐变为浅绿色.(3)通过甲、乙实验探究,可得出三种金属活动性由强到弱的顺序为:Fe>Cu >Ag.(4)由丙实验方案可知,若采用一种金属与两种盐溶液反应来比较三种金属的活动性强弱,可以采用活动性居中的金属与两种盐溶液反应,也可得出相同结论,则金属C是Cu.故答为:(1)除去金属表面的氧化膜;(2)Cu+2AgNO3═2Ag+Cu(NO3)2;铁丝的表面有一层红色物质,溶液由蓝色逐渐变为浅绿色.(3)Fe>Cu>Ag.(4)Cu.。
九年级化学第8单元金属和金属材料实验活动4 金属的物理性质和某些化学性质

知识点 1 金属的物理性质
实验步骤
实验现象
实验结论
观察镁、铝、 铁、铜的颜色 和光泽
镁、铝、铁是银白 色,铜是紫红色
金属都有金属 光泽,大多数 是银白色
铜片和铝片、 铜片在铝片上留有 铜 的 硬 度 比 铝
铜片和黄铜片 痕迹,黄铜片在铜 大 , 黄 铜 片 比
互相刻画
片上留有痕迹
铜的硬度大
实验步骤
(3)反应②还需要的一种反应物是 __C_(_或__C_O__或__H__2)_ (填化学式)。
(4)写出反应③的方程式,并注明基本反应类型: _F_e_+__C__u_S_O_4_=_=_=_=_F_e_S_O__4_+__C_u_(_合__理__即__可__)____ ( 置换反应 )。
知识点 3 比较金属的活动性
用电池、导线、 金属片、小灯泡 组成串联电路
实验现象 小灯泡亮
实验结论 金属有导电性
【例1】【中考·揭阳】下列性质属于金属共性的是( B ) A.硬度很大、熔点很高 B.有良好的导电性、传热性 C.是银白色的固体 D.易与酸反应产生氢气
导引:金属的种类很多,具有很多共同的性质, 如物理性质中,大多数金属都是固体,具有金属 光泽,具有较好的导电性、导热性和延展性,较 高的熔点和沸点等,但有的金属具有一些特性, 如不是所有的金属都是银白色的固体
(2)图B中属于金属材料的有 _钨__丝__、__铜__丝__、__焊__锡__、__铝___,
其中___焊__锡___是合金,该合 金的熔点比组成它的纯金属 ___低_____(填“高”或“低”)。
(3)图C是现今流通的1元钢芯镀镍合 金硬币,请根据你的经验和所学 的知识推测,该硬币具有的性质 有__耐__磨__、__抗__腐__蚀__性__强____等。
金属的物理性质和某些化学性质 课件

镁
大量气泡,反应最 Mg+H2SO4=MgSO4+H2↑
快
锌
许多气泡,反应快 Zn+H2SO4=ZnSO4+H2↑
铁
少量气泡,反应较 Fe+H2SO4=FeSO4+H2↑
慢,溶液由无色变为
浅绿色
铜
无现象
无
金属活动性顺序:
.
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
(3)金属都具有导电性、延展性、导热性。
二、金属的化学性质
活动1.用坩埚钳夹取一块铜片, 放在酒精灯火焰上加热,观察铜 片表面的变化。
在4支试管里分别放入镁、 锌、铁、铜,再分别加入 稀盐酸(或稀硫酸),观 察现象,比较反应的剧烈 程度。如果有气体生成, 判断反应后生成了什么气 体? (用燃着的小木条放在试 管口检验)
化学方程式
大量气泡,反应最 快
许多气泡,反应快
少量气泡,反应较 慢,溶液由无色变为 浅绿色
无气泡
金属与稀H2SO4
镁 锌 铁
铜
现象
大量气泡,反应最 快 许多气泡,反应快
少量气泡,反应较 慢,溶液由无色变 为浅绿色 无气泡
化学方程式
谁强谁弱你看清楚了吗?
God Save me!!
为什 么受 伤的 总是 我!
活动与探究三:金属与金属化合物溶液的反应
实验
现象
化学方程式
取一支试管倒入一定
量的CuSO4溶液, 将一根用砂纸打磨过
的铁丝浸入溶液中,
浸入溶液中的铁丝
表面覆盖一层紫红 色的物质
Fe+ CuSO4 ==Cu+ FeSO4
观察现象。
取一支试管倒入一定
量的AgNO3溶液, 将一根用砂纸打磨过
实验活动4金属的物理性质和某些化学性质实验

学科:化学 年级:九年级(人教版) 课题:
实验活动4金属的物理性质和某些化学 性质实 验
第八单元之
1.巩固和加深对金属性质的认识。 2.培养实验设计能力。
实验器材: 试管7支、酒精灯、坩埚钳、火柴、
石棉网、镊子、小木条。 实验药品:
镁条、锌粒、铝片、铁钉、铜片、 稀盐酸、稀硫酸、硫酸铜溶液、硝酸 银溶液。
注意: 1.探究过程中实验操作的规范。 2.观察时注意各自反应的剧烈程度, 产生气泡的快慢,是否放热等在探 究中请按要求填好的实验报告。
(A组 金属与盐酸反应)
金属
现象
反应的化学方程式
铜
没有明显变化
产生少量气泡,放出热
+2
铁
量,形成浅绿色的溶液
Fe+2HCl== FeCl2+H2↑ 氯化亚铁
锌
产生较多的气泡,放出 热量,形成无色的溶液
结论:铁>铜>银
铜>银
课外延伸
请请同学们设计并进行实验 ,证明金属具有导电性(或导热 性、延展性)。
再见
亲爱的同学们,再见!
操作
现 象 化学方程式
用坩埚钳夹取一 块铜片,放在酒精
铜片表面变黑 2Cu+O2 =△ 2CuO
灯火焰上加热
发出耀眼白光,
用坩埚钳夹取一 放热,生成白
块镁条片,放在酒
色固体
点燃
2Mg+O2 = 2MgO
精灯火焰上点燃
(2)与酸的反应
(2)向4支试管中分别放入少量镁条、锌粒、铁钉 、铜片,然后分别加入5mL稀盐酸(或稀硫酸) ,观察现象。如果有气体生成,判断生成的气体 是什么。
金属的物理性质和某些化学性质的探究实验
导线
学生电源
说明:本表分实验填写,实验班级直接填写到课程表内,每个实验填写一张。
南平市第四中学化学实验通知单
九年级下学期实验名称金属的物理性质和某些化学性质的探究实验实验管理人员
2、实验节次与时间年月日——月日
星期
节次
星期一
星期二
星期三
星期四
星Hale Waihona Puke 五1234
5
6
7
1、实验仪器与药品
编号
名称
规格
数量
备注
64081
表面皿
60mm
64071
试管刷
64053
玻璃棒
φ3~φ4mm
61001
试管
φ12mm×70mm
61022
烧杯
100mL
64042
药匙
77003
硫酸
试剂
77011
盐酸
试剂
74012
镁条
教学用
70004
锌粒
试剂
70011
铜丝
教学用
77032
氢氧化钠
试剂
70086
无水硫酸铜
试剂
63041
滴瓶
30ml
70006
铁丝
教学用
64005
镊子
70047
三氯化铁
试剂
03008
试管架
砂纸
金属的化学性质

一、金属的物理性质常温下,金属一般为银白色固体(汞常温下为液体),具有良好的导电性、导热性、延展性,金属的熔沸点和硬度相差很大。
二、金属的化学性质多数金属的化学性质比较活泼,具有较强的还原性,在自然界多数以化合态形式存在。
容易与O2反应而生成氧化物,可以与酸溶液反应而生成H2,特别活泼的如Na等可以与H2O发生反应置换出H2,特殊金属如Al可以与碱溶液反应而得到H2。
1、金属和非金属的反应(1)钠的化学性质(2)金属与氧气的反应情况对比2、金属与酸和水的反应金属与酸、水、碱和盐的反应对比经典例题题1、(1)分别写出氧气在一定条件下生成下列物质的化学方程式(必须注明反应条件)。
①Na2O:__________________________________________。
②Na2O2:___________________________________________。
(2)指出氧元素在下列各物质中的化合价:O3______;Na2O2______;Na2O______。
(3)KO2能吸收CO2生成K2CO3和O2,故可用作特殊情况下的氧气源,试写出该反应的化学方程式________________________________________。
(4)人体内O2-离子对健康有害,使人过早衰老,但在催化剂SOD存在下可发生如下反应,请完成该反应的离子方程式:□O2+□H2O====□H2O2+□O2+□□□【分析】本题涉及的知识点较多,有碱金属的性质,氧及臭氧的知识,化合价的概念等。
其中大部分知识是考生已经学过的,但也渗入了一些新知识,不过在题目所给信息的引导下,考生应能将所学知识迁移过去解决新问题。
【答案】(1)①2Na+O2Na2O2②4Na+O22Na2O(2) 0;-1;-2(3)4KO2+2CO2====2K2CO3+3O2(4)2O2-+2H2O====H2O2+O2+2OH-题2、一块表面已被氧化为Na2O的钠块10.8 g,将其投入到100 g水中,产生H2 0.2 g。
金属的物理和化学性质

金属的物理和化学性质金属是一类广泛存在于地壳中的元素或化合物,具有独特的物理和化学性质。
本文将探讨金属的物理性质和化学性质,并深入了解它们的特点和应用。
一、金属的物理性质1. 密度高:金属的密度通常比较大,多数金属都比水的密度大很多。
这也是其在建筑、制造和工程领域中被广泛使用的原因之一。
2. 熔点和沸点高:相对于非金属物质,金属的熔点和沸点一般较高。
例如,铁的熔点为1538摄氏度,而氧气的熔点仅为-218摄氏度。
这些高熔点和沸点使得金属在高温环境下仍能保持稳定,从而被广泛应用于高温工况中。
3. 导电性好:金属是良好的导电体,能够自由地传导电子。
这是因为金属的晶体结构中存在可自由运动的电子,称为自由电子。
这种自由电子的存在使得金属能够传导电子,并具有良好的导电性能。
4. 导热性好:金属还具有良好的导热性,能够迅速传导热量。
这一特性使得金属常被用作热传导材料,例如铜制的散热器。
5. 良好的延展性和韧性:金属具有很强的延展性和韧性。
在外力的作用下,金属可以轻松改变形状而不破裂,这使得其成为制造工业中重要的材料之一。
二、金属的化学性质1. 金属与氧化反应:金属在氧气中发生氧化反应,产生金属氧化物。
例如,铁与氧气反应生成铁氧化物,常见的形式是铁锈。
这恰恰是铁生锈的原因。
2. 金属与非金属形成盐:金属与非金属元素(通常是非金属氧化物)反应时,会生成相应的金属盐。
例如,氯气与钠反应生成氯化钠,常见的食盐即为氯化钠。
3. 金属与酸反应:大多数金属在与酸反应时会产生产氢气的化学反应。
例如,锌与盐酸反应,生成氯化锌和氢气。
4. 金属与水反应:活泼金属(如钠、钾等)与水反应时,会放出氢气,并生成相应的碱性金属氢氧化物。
例如,钠与水反应生成氢气和氢氧化钠。
5. 金属的腐蚀:金属在一定的环境条件下会发生腐蚀现象,常见的是金属被氧化或腐蚀。
这是由于金属与周围环境中的水、氧气、酸碱等物质相互作用所致。
金属的物理和化学性质决定了它们在工业、建筑、电子等领域的广泛应用。
实验活动4---活动5知识练习题附答案 2022学年人教版九年级化学下册
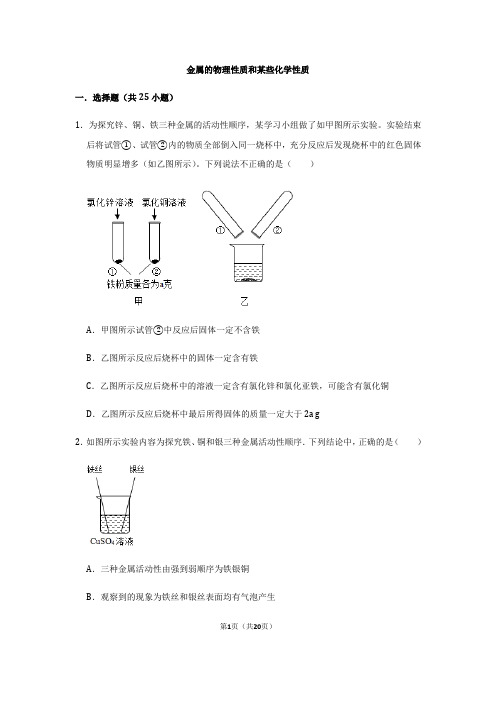
金属的物理性质和某些化学性质一.选择题(共25小题)1.为探究锌、铜、铁三种金属的活动性顺序,某学习小组做了如甲图所示实验。
实验结束后将试管①、试管②内的物质全部倒入同一烧杯中,充分反应后发现烧杯中的红色固体物质明显增多(如乙图所示)。
下列说法不正确的是()A.甲图所示试管②中反应后固体一定不含铁B.乙图所示反应后烧杯中的固体一定含有铁C.乙图所示反应后烧杯中的溶液一定含有氯化锌和氯化亚铁,可能含有氯化铜D.乙图所示反应后烧杯中最后所得固体的质量一定大于2a g2.如图所示实验内容为探究铁、铜和银三种金属活动性顺序.下列结论中,正确的是()A.三种金属活动性由强到弱顺序为铁银铜B.观察到的现象为铁丝和银丝表面均有气泡产生第1页(共20页)C.三种物质间能发生反应的化学方程式为Fe+CuSO4=FeSO4+CuD.观察到的现象为铁丝和银丝表面均附着一层紫红色固体,溶液颜色变浅3.有X、Y、Z三种金属,把Y投入X(NO3)2溶液中,Y表面有X析出,把X投入Z(NO3)溶液中,X表面有Z析出。
X、Y、Z三种金属的活动性由强到弱的顺序是()2A.Z>Y>X B.Y>X>Z C.X>Y>Z D.X>Z>Y4.小红用三根相同的铁钉进行铁制品锈蚀条件的探究(如图),一周后观察现象。
下列说法错误的是()A.该实验说明铁生锈需要与氧气和水同时接触B.对比甲和丙中出现的现象,可说明铁生锈需要氧气C.乙中的蒸馏水要事先煮沸,目的是除去水中溶解的氧气D.若把甲中蒸馏水换成食盐水,则铁钉更容易生锈5.氢气和一氧化碳还原氧化铜的实验装置如图,说法不正确的是()A.实验时都应该先通入气体一段时间后再加热,防止发生爆炸B.甲试管略向下倾斜,乙玻璃管保持水平,主要是因为两种气体的密度不同第2页(共20页)C.两者都可以通过观察黑色固体颜色的变化判断反应是否发生D.乙中需尾气处理装置,是因为一氧化碳有毒6.木炭与氧化铜、一氧化碳与氧化铜反应的实验装置如图所示,下列说法正确的是()A.两个实验都需要尾气处理B.两个实验的反应中,都只有碳元素的化合价发生了改变C.两个实验都可观察到红色固体变黑色D.两个实验的操作中都要防止石灰水倒吸7.氢气、一氧化碳、炭粉分别跟黑色氧化铜反应,下面叙述中错误的是()A.反应都需要加热B.都属于置换反应C.氧化铜都发生还原反应D.都有红色固体物质生成8.在反应:C+2CuO2Cu+CO2↑中,氧化剂是()A.C B.CuO C.Cu D.CO29.在隔绝空气下,用木炭还原氧化铜。
金属化学性质的归纳总结

金属化学性质的归纳总结金属是化学元素中的一类,具有独特的物理和化学性质。
金属化学性质的归纳总结可以帮助我们更好地理解金属的特点和用途。
本文将从金属的物理性质、化学性质、氧化还原性和反应性等方面进行归纳总结。
一、物理性质1. 密度和相对密度:金属的密度通常较高,有良好的重量感,相对密度大于1。
2. 导电性能:金属具有良好的导电性能,可以传导电流和热量,其中铜和银是最佳的导电体。
3. 热导性能:金属的热导率高,能够迅速传导热量,使其在制造热器具和散热设备中得到广泛应用。
4. 留有光泽:大部分金属具有光泽,即使暴露在空气中也能保持金属光泽。
5. 延展性和韧性:金属具有良好的延展性和韧性,可以制成各种形状,如铜丝和铝箔。
二、化学性质1. 金属的氧化反应:金属通常与氧气反应生成金属氧化物,称为氧化反应。
例如铁在空气中与氧气反应生成铁锈。
2. 金属的还原反应:金属具有良好的还原性,能够还原其他物质,参与氧化还原反应。
例如锌可以还原Cu2+离子生成Cu金属。
3. 金属的溶解性:一些金属如铝和锌可以与酸反应生成盐和氢气。
4. 金属的腐蚀性:金属在氧气和湿气的作用下容易发生腐蚀,产生金属氧化物,如铁生锈。
5. 金属的活泼性:金属的活泼性由金属元素的位置在元素周期表中决定,活泼性较高的金属更容易与酸和非金属元素反应。
三、氧化还原性1. 金属的氧化性:金属通常容易失去电子形成阳离子,表现出较强的氧化性。
2. 金属的还原性:金属由于具有较低的电负性,可以容易地将电子转移给其他物质,参与还原反应。
3. 金属的电化学活性:金属的电化学活性可以通过标准电极电位来预测,越容易被氧化的金属电极电位越低。
四、反应性1. 金属与非金属的反应:金属与非金属通常能够发生反应,形成离子化合物。
例如钠和氯气反应生成氯化钠。
2. 金属与水的反应:一些金属与水反应时会放出氢气,形成金属氢氧化物。
例如钠与水反应生成氢氧化钠和氢气。
3. 金属与酸的反应:一些金属可以与酸反应生成氢气和金属盐。
2020人教版化学九年级年级下册8单元重点考点专训-金属的物理性质和某些化学性质(附答案)

人教版化学九年级下册8章重点考点专训-金属的物理性质和某些化学性质1.下列是探究金属某些物理性质的实验,说法错误的是()A.镁片、铁片、铝片是银白色,铜为紫红色B.将打磨好的铁片、铜片分别接入串联电路中,灯泡发亮,说明金属具有导电性C.手拿铁丝的一端,在酒精灯火焰上加热另一端,手感到发热,说明铁能导热D.将纯铜片和黄铜片相互刻画,纯铜片上留下痕迹,说明铜的硬度比黄铜大2.【中考·揭阳】金属材料在人类活动中已得到越来越广泛的应用,下列性质属于金属共性的是()A.硬度很大,熔点很高B.是银白色的固体C.易与酸反应产生氢气D.能够导电,能够导热3.下列实验中,研究金属物理性质的是()①铜片和铝片相互刻画,观察何种金属表面有划痕②加热铜片,观察铜片表面是否变黑③加热铜片一端,观察另一端的蜡烛是否熔化,如图所示。
A.①②B.②③C.①③D.①②③4.整理物品,小小发现家中角落堆积的一些铁丝、银丝和铜丝。
(1)小小很容易辨别出铜丝,他依据的是___________________;三种金属都可拉成丝状,利用了金属的________性。
(2)三种金属都能用来制导线,这是利用了金属的________性;小小想验证铝丝具有导热性,可采用的实验方法是_________________________________________________。
5.【中考·黑龙江】人类每年要向自然界索取大量的金属矿物资源,金属的用途与它们的物理性质和化学性质都有着密切的关系,请回答下列问题:(1)如图1所示,将纯铜片和黄铜片互相刻画,纯铜片上留下明显划痕,这一实验现象说明什么?________________________________________。
(2)如图2所示,用坩埚钳夹取一根铜丝,放在酒精灯火焰上加热,铜丝表面会产生什么现象?_________________________________________。
2020人教版九年级化学下册课件:第八单元实验活动4金属的物理性质和某些化学性质(共32张PPT)

6.(2019广西梧州一模)要验证铁、铜、银的金属活动性顺序,除铁、铜、 银外还需要的一种试剂是 ( ) A.KNO3溶液 B.FeCl2溶液 C.稀盐酸 D.CuSO4溶液
答案 D 铁、铜、银均不能与KNO3溶液反应,不能验证铁、铜、银的金 属活动性顺序;铜、银均不能与FeCl2溶液反应,不能验证铜、银的金属活 动性顺序;铁能与稀盐酸反应生成氢气,铜、银均不能与稀盐酸反应,不能 验证铜、银的金属活动性顺序;铁能与硫酸铜反应生成硫酸亚铁和铜,银不 能与硫酸铜反应,说明金属活动性铁>铜>银,可以验证铁、铜、银的金属 活动性顺序。
4.(2019浙江金华中考)小丽为确认所回收易拉罐的主要成分是铝还是铁, 剪取金属片打磨后,设计了如图8-4-1所示的两种不同方法进行检验,这样 设计的依据是 ( )
图8-4-1 A.铁、铝有不同的物理性质 B.活泼金属易与氧气反应 C.排在氢前面的金属可以把酸中的氢置换出来 D.活动性较强的金属可把活动性较弱的金属从它的化合物溶液中置换出来
白铜片)相互刻画
(或白铜片)在铜片上留有痕迹 铜片)的硬度比铜大
用电池、导线、金属片、小灯 小灯泡亮 泡、单刀开关组成串联电路
金属有导电性
2.金属的化学性质 (1)金属与氧气的反应 【实验步骤】用坩埚钳夹取一块铜片,放在酒精灯火焰上加热。 【实验现象】铜片表面变黑。 【实验结论】铜能与氧气反应。 (2)金属与酸的反应 【实验步骤】向5支试管中分别放入少量镁条、铝片、锌粒、铁片、铜 片,然后分别加入5 mL稀盐酸(或稀硫酸),观察现象。 【实验现象】放镁条、铝片、锌粒、铁片的试管中有气体生成,生成的气 体能燃烧;放铜片的试管中没有气体生成。 【实验结论】金属镁、铝、锌、铁能与稀盐酸(或稀硫酸)反应生成氢气, 铜与稀盐酸(或稀硫酸)不反应。
金属的化学性质和物理性质

金属的化学性质和物理性质金属是我们常见的物质之一,在平常生活中我们不会很注意它们的特性,但在学化学就要知道金属的化学性质和物理性质。
今天小编在这给大家整理了金属的化学性质和物理性质简介,接下来随着小编一起来看看吧!金属的化学性质金属分为活性金属和钝性金属两种。
根据金属活动性顺序,氢前金属称为活性金属,氢后金属就是钝性金属。
钾钙钠镁铝锌铁锡铅 (氢) 铜汞银铂金K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au1、氢前面的金属能与弱氧化性强酸反应,置换出酸中的氢(浓硫酸、硝酸等强氧化性强酸与金属反应不生成氢气),如:Fe + 2HCl ═ FeCl2 + H2↑2、活动性强的金属能与活动性弱的金属盐溶液反应。
3、大多数金属能与氧气反应。
4、排在H前面的金属,理论上讲都能与水发生化学反应。
在常温下,钾,钙,钠等能与水发生剧烈反应,镁、铝等能与热水反应,铁等金属在高温下能与水蒸气反应。
5、金属均无氧化性,但金属离子有氧化性,活动性越弱的金属形成的离子氧化性越强。
6、金属都有还原性,活动性越弱的金属还原性越弱。
金属化学性能金属化学性能是指金属材料与周围介质扫触时抵抗发生化学或电化学反应的性能。
1、耐腐蚀性:指金属材料抵抗各种介质侵蚀的能力。
2、抗氧化性:指金属材料在高温下,抵抗产生氧化皮能力。
金属的物理性质1)金属物理性质的共性:常温下金属都是固体(汞除外),有金属光泽,大多数金属是电和热的良导体,有延展性,密度较大,熔点较高.2)金属物理性质的特性:大多数金属都是银白色,但铜呈紫红色,金呈黄色;在常温下大多数金属为固体,但汞是液体.密度:最大:锇最小:锂熔点:最大:钨最小:汞硬度:最大:铬最小:铯金属之最地壳中含量最高的金属元素:铝(含量为7.73%)人体中含量最高的金属元素:钙(含量为1.5%)目前世界年产量最高的金属:铁密度最小的金属:氢(2016年1月英国科学家在爱丁堡大学首次制成金属态氢,氢成为密度最小的金属)密度最大的金属:锇(22.48×10?㎏/m?)最硬的金属:铬(莫氏硬度约为9)最软的金属:铯(莫氏硬度约0.5)导电性最强的金属:银导热性最强的金属:银制造新型高速飞机最重要的金属:钛(被科学家称为“二十一世纪的金属”或“未来的钢铁”)海水中储量最大的放射性元素:铀(陆地铀矿的总储量约200万吨,海洋里含铀的总量高达40万万吨)含同位素最多的元素:锡(有10种稳定的同位素)含同位素最少的元素:钠(只有Na-23稳定)展性最强的金属:金(最薄的金厚度只有1/10000mm)延性最好的金属:铂(最细的铂丝直径只有1/5000mm)熔点最高的金属:钨(熔点:3410±20℃)熔点最低的金属:汞(熔点-38.8℃)熔沸点相差最大的元素是镓(熔点30℃,沸点2403℃)地壳中含量最少的金属是钫(即使是在含量最高的矿石中,每吨也只有37×10负13次方克;地壳中的含量约为1×10^-21 %) 光照下最易产生电流的金属元素:铯(当其表面受到光线照射时,电子便能获得能量从表面逸出,产生光电流)金属性最强的金属:铯世界上最贵的金属:锎(每克1千万美元,比金贵50多万倍)世界上最便宜的金属:铁最易应用的超导元素:铌(把它冷却到-263.9℃的超低温时,会变成一个几乎没有电阻的超导体)最能吸收气体的金属元素:钯(1体积胶状钯能吸收氢气1200体积)。
金属和非金属的物理和化学性质

金属和非金属的物理和化学性质金属和非金属是物质分类中的两大类别,它们在物理和化学性质上有着显著的差异。
本文将从物理性质和化学性质两个方面来讨论金属和非金属的特点。
一、物理性质1. 密度:金属的密度一般较高,如铁、铜等金属的密度都超过5克/立方厘米;而非金属的密度较低,如氧气、氮气等的密度远小于1克/立方厘米。
2. 熔点和沸点:金属一般具有较高的熔点和沸点,如铁的熔点约为1535摄氏度,铜的熔点约为1083摄氏度;而非金属的熔点和沸点较低,如氯的熔点约为-101摄氏度,碳的熔点约为3550摄氏度。
3. 电导性:金属具有良好的电导性,能够在外电场的作用下传导电流;而非金属的电导性较差,大多数非金属不能传导电流,如硫、氮等。
4. 导热性:金属具有优良的导热性,热能能够通过金属的形成中的自由电子传导;而非金属的导热性较差,热能不能够有效地通过非金属传导。
二、化学性质1. 电离能:金属一般具有低的电离能,容易失去外层电子形成阳离子;而非金属的电离能较高,不容易失去电子形成离子。
2. 与水反应:金属与水反应产生金属氢氧化物和氢气,如钠与水反应生成氢氧化钠和氢气;而非金属与水的反应因非金属类型的不同呈现出多种反应方式,如氢气与氧气反应生成水。
3. 活动性:金属的活动性较高,容易与其他物质发生化学反应;而非金属的活动性较低,不容易与其他物质发生化学反应。
4. 氧化性:金属具有较强的氧化性,容易与氧发生反应生成金属氧化物;而非金属的氧化性较弱,不容易与氧发生反应。
综上所述,金属和非金属在物理性质和化学性质上存在明显的差异。
金属具有较高的密度、熔点和沸点,以及优良的电导性和导热性;而非金属的特点是较低的密度、熔点和沸点,以及较差的电导性和导热性。
在化学性质方面,金属容易失去外层电子形成阳离子,与水发生反应生成金属氢氧化物和氢气,具有较强的氧化性和较高的活动性;而非金属的化学性质较为稳定,活动性较低。
以上是对金属和非金属的物理和化学性质的简单介绍,希望能够对读者对此有一定的了解和认识。
化学六年级金属的物理性质与化学性质实验

化学六年级金属的物理性质与化学性质实验一、金属的物理性质1. 密度金属的物理性质之一是密度。
密度是单位体积内所含质量的量度,通常以克/厘米³或克/毫升来表示。
金属一般具有较高的密度,比如铁、铜等金属的密度相对较大。
密度的大小与金属中原子的质量有关,质量越大,密度越大。
2. 熔点金属的熔点是指金属物质在加热过程中从固态转变为液态的温度。
不同金属的熔点范围各不相同。
例如,铁的熔点约为1535℃,而铜的熔点约为1083℃。
金属的熔点常常用作判定矿石中的金属成分的重要依据。
3. 导电性金属具有良好的导电性。
这是由于金属中的自由电子能够在金属内部自由运动以及在外部电场的作用下形成电流。
该性质使得金属常被用来制造电线、电器等导电材料。
另外,金属还具有较低的电阻率,使得电流能够在金属内部迅速传导。
4. 导热性金属材料具有良好的导热性。
金属内部的自由电子能够传导热量,使得金属成为非常适合制作热导体的材料。
例如,铝是一种常用的热导体,具有较高的热传导能力。
这种导热性质使得金属材料常被应用于散热器、锅具等领域。
二、金属的化学性质1. 氧化反应金属与氧气反应会形成金属氧化物,这被称为氧化反应。
不同金属与氧气进行氧化反应的速度各不相同。
例如,钠在与氧气反应时会迅速燃烧,产生白色固体氧化钠。
而金属铝则与氧气反应较为缓慢,生成氧化铝。
氧化反应是金属腐蚀的一种表现。
2. 酸和金属的反应金属与酸反应会生成盐和氢气。
这是一种常见的化学性质。
一些活泼金属,比如钠、镁等,在与酸反应时会迅速放出氢气。
例如,将镁与盐酸反应可以观察到产生气泡的现象,同时生成氯化镁和氢气。
然而,并非所有金属都会与酸产生反应,一些稳定性较高的金属如铜、银等通常不与酸发生反应。
3. 金属与水的反应某些金属与水反应也会产生氢气。
例如,将钠投入水中,会观察到剧烈的反应,并有大量氢气释放。
反应还会生成氢氧化钠。
一些金属如铝、锌等也会与水反应,但反应速率较慢。
金属的物理性质及化学性质实验

金属的物理性质及化学性质实验金属是一类具有特殊性质的物质,它们具有高强度、导电导热性和可塑性等特点。
本文将介绍金属的物理性质和化学性质实验,并探讨它们对金属在实际应用中的重要性。
一、物理性质实验1. 密度测定实验金属的密度是衡量物质质量分布程度的物理量,常用单位是克/立方厘米(g/cm³)。
密度测定实验可以通过测量金属的质量和体积来得到。
首先,准备一个天平和一个容器,精确称量出一定质量的金属样品,然后将其置于容器中,测量容器的初始质量。
再将容器充满液体,测量容器和液体的总质量。
最后,用总质量减去容器质量,即可得到金属的质量。
将测得的质量除以液体的体积,即可得到金属的密度。
2. 熔点测定实验金属的熔点是指金属从固态转变为液态时的温度。
熔点测定实验可以通过加热和观察金属样品的温度变化来进行。
取一定质量的金属样品,放置于坩埚中,并放置在加热设备中,逐渐加热。
当金属样品开始熔化时,可以通过温度计测量到金属的熔点。
3. 电导实验金属具有良好的导电性,因此电导实验可以用来判断金属样品是否具有导电性。
实验中,将金属样品连接到电路中的两端,通过电流表观察电流的流动情况。
若金属样品能够导电,则电流表显示有电流通过;若金属样品不能导电,则电流表显示无电流通过。
二、化学性质实验1. 金属与酸的反应实验金属与酸反应是一种常见的化学反应,产生气体和盐的生成。
实验中,取一定质量的金属样品,将其与一定浓度的酸进行反应。
观察反应过程中是否产生气体的释放以及反应后产物的性质变化。
根据产生的气体种类和颜色变化,可以判断出金属与酸之间的化学反应类型。
2. 金属与氧化剂的反应实验金属与氧化剂的反应是指金属与氧气或其他氧化剂发生化学反应。
实验中,取一定质量的金属样品,将其加热至高温并暴露于氧气中,观察其是否能够与氧气发生反应。
根据反应过程中是否产生火花、火焰以及产生的氧化物的性质变化,可以判断金属与氧化剂的反应性质。
3. 金属与碱的反应实验金属与碱之间的反应是指金属与碱溶液进行化学反应,并产生氢气和盐的生成。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
3.实验中用酸、酒精灯要注意安全。
1.设计的实验方案
2.可能想到的实验注意事项,(想不到,教师补充)设计对比实验需要注意控制变量:酸的种类、浓度和用量;金属的种类、形状、质量;反应温度等
3.铁、铜、银活动性强弱方案:铁、银和硫酸铜溶液;硝酸亚铁溶液、硝酸银溶液和铜;盐酸、铁、铜、银、硝酸银溶液;盐酸、铁、铜、银、硫酸铜溶液
金属化学性质:设计实验方案,并在方案设计过程中思考实验中应该注意哪些事项。
巡视指导学生进行金属化学性质实验方案设计,启发学生思考注意事项
小组针对金属化学性质讨论设计实验方案并总结方案设计的注意事项和实验应注意的事项
着重学习对比实验设计,并进一步巩固金属化学性质
交流各组设计的实验方案和实验注意事项
1.比较铁、铜、银金属活动性强弱实验方案的设计可总结其规律为:氢前金属用金属和酸;金属和盐溶液;氢后金属用金属和盐溶液。方案很多,若学生提不出,教师补充,但条件所限今天只能进行部分方案的验证,有兴趣以后到实验室进行。
交流各组设计的实验方案和实验注意事项
教师点拨
1.金属导电性可以分别用铁丝和铜丝进行,学生不但亲身感知金属能导电,还能亲历不同金属的导电性不同
2.实验中用酒精灯要注意安全。
学生展示:
1.设计的实验方案
2.可能想到的实验注意事项,(想不到,教师补充)用金属单质进行实验要注意将金属打磨光。
保证实验安全和实验现象清楚易于观察,使实验能很好验证理论,从而保证学生乐于进行实验探究
保证实验安全和实验现象清楚易于观察,使实验能很好验证理论,从而保证学生乐于进行实验探究
进行实验探究
巡视指导学生安全完成实验,并观察记录好实验现象,分析原因,得出结论。研究实验出现的异常现象。
动手实验,观察记录实验现象,分析原因得出结论。
通过实验验证自己设计的实验,培养学生实验探究能力。
实验小结
主要针对金属化学性质实验根据实际情况对实验中的问题进行点拨
教学环节与方法
教师活动
学生活动
设计宗旨与意图
导课
出示PPT展示实验目标
本单元,我们一起研究了金属的性质和用途,一定很想通过实验验证我们学到的理论知识,今天我们就上一节实验活动课——金属的物理性质和某些化学性质
观看、理解
交代本课学习目标和任务,有利于学生做到心中有数,顺利达成目标和完成任务。
实
验
探
究
复习:金属活动性顺序;金属的化学性质用化学方程式表示
完善学生实验中的不足,使学生对金属物理性质有更清晰的理解并为下一步进行化学性质研究做铺垫
突破建议:根据生活经验和已经学过的知识,学生对金属的物理性质有了一定的认识,生活中的金属制品很多,建议开放性教学,除了教师准备的几种金属材料外,可以让每个实验小组带几种金属制品。在老师的指导下,自行设计实验仪器、方案来完成对金属物理性质的探究。
将语言表达提升为书面表达,强化知识
课堂小结
表扬方案设计和实验过程中积极参与,有合作精神的学生
激励学生勇于参与,积极合作
课后作业
进一步整理完成导学案的实验报告和课后思考题
独立完成作业
巩固金属的物理性质和化学性质,进一步提升实验设计能力
教师根据学生得出结论,板书
汇报金属化学性质实验验证情况、实验现象、结论以及需要注意的实验注意事项。
学生也可以补充自己通过实验产生的新想法和发现的问题。
进一步理解金属化学性质,掌握对比实验的设计方法,为以后的实验活动课顺利进行提供参考。
课堂练习
见导学案呈现的实验报告
巡视指导答疑
整理并记录交流结果,学生独立整理记录
提问
思考、回答
为学生实验扫清知识障碍,使学生顺利进行实验设计和实验
金属物理性质:下发导学案,设计实验方案,并在方案设计过程中思考实验中应该注意哪些事项。
下发报告,巡视指导学生进行物理性质实验方案设计,启发学生思考注意事项
小组针对金属物理性质讨论设计实验方案并总结方案设计的注意事项和实验应注意的事项
培养实验设计能力,置换反应进行简单的判断,学习利用对比法设计实验。
教学资源与教学手段
仪器药品
8支试管、酒精灯、坩埚钳、电池、导线、小灯泡、干电池、火柴、镁条、锌粒、铝片、硬铝片、铁片、铁丝、铁粉、铜片、铜丝、黄铜片、稀盐酸、稀硫酸、硫酸铜溶液、硝酸银溶液
演示文稿
PPT
其他资源
导学案
教学内容
实验活动
寿光市建桥学校
教学目标
知识与技能
过程与方法
学习利用对比法设计实验,进一步提高实验设计能力和归纳总结能力。
情感态度价值观
在实验过程中体验探究和合作的快乐,增强探究的欲望,养成严谨求实、乐于实践和善于合作的品质,并不断强化实验安全意识。
重点
认识常见金属的主要化学性质,能用金属活动性顺序表对有关的置换反应进行简单的判断。学习利用对比法设计实验。
进行实验探究
巡视指导学生安全完成实验,并观察记录好实验现象,分析原因,得出结论。研究实验出现的异常现象。
动手实验,观察记录实验现象,分析原因得出结论。
通过实验验证自己设计的实验,培养学生实验探究能力。
实验小结
针对金属物理性质实验根据实际情况对实验中的问题进行点拨
教师根据学生得出结论,板书
汇报金属物理性质实验验证情况、实验现象、结论以及需要注意的实验注意事项学生也可以补充自己通过实验产生的新想法和发现的问题。
