共沸蒸馏生产无水酒精工艺流程图
工业酒精制无水乙醇的流程

工业酒精制无水乙醇的流程今天咱们来唠唠工业酒精制无水乙醇的那些事儿。
工业酒精里其实还含有不少的水呢,要把它变成无水乙醇可没那么简单。
这就像是从一群混杂着杂质的小伙伴里挑出最纯净的那几个一样。
那具体咋做呢?一、蒸馏法。
蒸馏是个挺常用的办法。
就像是把混合着水和酒精的溶液放在一个大锅里煮,不过这个锅可是特制的蒸馏设备哦。
因为酒精的沸点比水低,所以当加热的时候,酒精就会先变成蒸汽跑出来。
然后把这些蒸汽收集起来,再让它冷却变回液态,这就初步把酒精和水给分开了一点。
但是呢,这个方法不能完全把水去掉,因为酒精和水会形成共沸物,就像两个分不开的小冤家一样,总有一部分水会跟着酒精一起跑出来。
所以啊,单纯靠蒸馏得到的酒精还不是真正的无水乙醇。
二、加入干燥剂。
既然蒸馏不能完全搞定,那就得来点别的手段啦。
这时候就可以加入干燥剂。
干燥剂就像是一个个小海绵,专门吸收水分。
常见的干燥剂有氧化钙之类的。
把氧化钙加到经过蒸馏初步处理的工业酒精里,氧化钙就会和水发生反应,把水给吸收掉。
这个过程就像是干燥剂在说:“哼,水啊水,你可别想在这儿捣乱啦,我要把你消灭掉。
”然后等反应完了,再进行一次蒸馏,把酒精和干燥剂的残渣分开,这样得到的酒精就更接近无水乙醇啦。
三、离子交换树脂法。
还有一种挺神奇的方法呢,就是离子交换树脂法。
离子交换树脂就像是一个个小魔法师,它们能把水里的离子抓住。
把工业酒精通过装有离子交换树脂的柱子,树脂就会把水里的离子吸附住,这样就相当于把水给去掉了一部分。
不过这个方法也有它的局限性,有时候不能完全把水除尽。
但是它的好处就是比较环保,不会像有些干燥剂那样产生废渣啥的。
从工业酒精制无水乙醇的过程就像是一场奇妙的冒险,要不断地想办法克服各种小麻烦,才能得到咱们想要的无水乙醇。
这个过程中每一个步骤都像是一个小关卡,需要我们用智慧和一些化学小技巧去闯过。
而且啊,这个过程也体现了化学的魅力,就像变魔术一样,把含有水的工业酒精一步一步变成纯净的无水乙醇。
酒精工艺流程、设备图
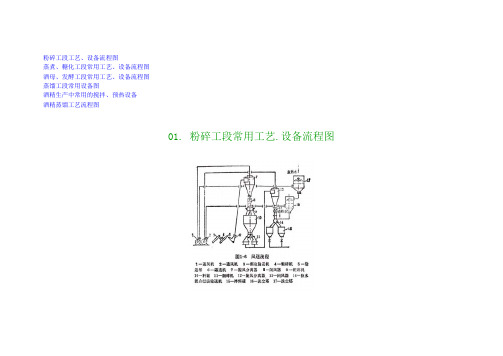
002.蒸煮、糖化工段常用工艺、设备流程004.蒸馏工段常用设备工艺流程图
005.酒精生产中常用的搅拌、预热设备
006.酒精蒸馏工艺流程图
1.回流装置 3.液相进塔的两塔流程 5.三塔蒸馏流程图 7.五塔蒸馏流程 9.上海酒精厂蒸馏流程 11.半直接式脱甲醇三塔蒸馏流程 13.五塔系醪液精馏机组 15.制取无水酒精的设备流程
粉碎工段工艺设备流程图蒸煮糖化工段常用工艺设备流程图酒母发酵工段常用工艺设备流程图蒸馏工段常用设备图酒精生产中常用的搅拌预热设备酒精蒸馏工艺流程图01
粉碎工段工艺、设备流程图 蒸煮、糖化工段常用工艺、设备流程图 酒母、发酵工段常用工艺、设备流程图 蒸馏工段常用设备图 酒精生产中常用的搅拌、预热设备 酒精蒸馏工艺流程图
2.精馏塔冷凝器装置 4.两塔气相过塔蒸馏流程图 6.半直接式三塔蒸馏流程图 8.哈尔滨五塔蒸馏流程 10.半直接式三塔蒸馏流程 12.四塔系酒精蒸馏机组工艺流程 14.五塔系醪液精馏设备 16.超阿罗斯帕斯式蒸馏机组工艺流程
共沸精馏提取无水乙醇工艺流程

共沸精馏提取无水乙醇工艺流程无水乙醇在很多地方都超级有用呢,像是医药啊、化工啊这些领域。
那怎么把它从一般的乙醇溶液里提取出来,弄成无水乙醇呢?共沸精馏就是个超棒的办法哦。
咱先来说说共沸精馏的原理吧。
乙醇和水这俩家伙,在一定比例的时候会形成共沸物。
就像是两个很要好的小伙伴,非要凑在一起。
这时候普通的精馏办法可就不好使啦。
但是共沸精馏呢,就会找一个特别的“第三者”加进去。
这个“第三者”能打破乙醇和水的这种“亲密关系”。
这个特别的物质啊,和乙醇或者水其中一个的关系更“铁”,这样就能把水或者乙醇给拉走,从而实现分离,最后得到无水乙醇。
那具体的工艺流程是啥样的呢?有个很重要的部分就是这个共沸剂的选择。
这个共沸剂得满足好多条件呢。
它得能和乙醇或者水形成新的共沸物,而且这个新的共沸物的沸点得和原来乙醇水共沸物的沸点有比较大的差别。
这样才好把它们分开呀。
就像找对象一样,得找个合适的才能好好过日子。
一般来说,像苯、环己烷这些物质就经常被当作共沸剂。
选好共沸剂之后,就开始正式的精馏过程啦。
把乙醇水溶液和共沸剂一起放到精馏塔里。
在精馏塔里面呢,就像一场热闹的聚会。
不同的物质在里面跑来跑去,寻找自己的“小伙伴”。
加热这个混合物的时候,因为有共沸剂的存在,共沸物就会先沸腾变成蒸汽跑到塔顶去。
这个蒸汽呢,再经过冷凝,就又变成液体啦。
这时候得到的液体呢,其实是共沸剂和水或者乙醇的混合物。
然后呢,再通过一些其他的设备,比如说分相器。
这个分相器就像是一个裁判,把共沸剂和水或者乙醇分开。
共沸剂呢,可以回收再利用,因为它可宝贵啦,不能浪费。
剩下的乙醇溶液经过多次这样的共沸精馏过程,乙醇的浓度就会越来越高,最后就得到了无水乙醇。
不过在这个过程中呢,还有好多小细节得注意。
比如说精馏塔的操作条件,像温度啊、压力啊这些,都得控制得刚刚好。
要是温度太高或者太低,就像做饭的时候火候没掌握好一样,出来的东西就不是咱们想要的啦。
还有这个共沸剂的加入量也很关键,加多了或者加少了都会影响最后的效果。
无水乙醇精馏
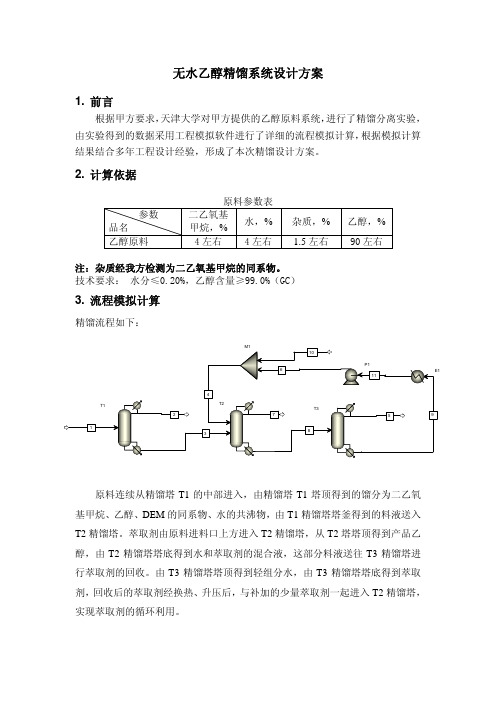
无水乙醇精馏系统设计方案1. 前言根据甲方要求,天津大学对甲方提供的乙醇原料系统,进行了精馏分离实验,由实验得到的数据采用工程模拟软件进行了详细的流程模拟计算,根据模拟计算结果结合多年工程设计经验,形成了本次精馏设计方案。
2. 计算依据注:杂质经我方检测为二乙氧基甲烷的同系物。
技术要求: 水分≤0.20%,乙醇含量≥99.0%(GC)3. 流程模拟计算精馏流程如下:原料连续从精馏塔T1的中部进入,由精馏塔T1塔顶得到的馏分为二乙氧基甲烷、乙醇、DEM的同系物、水的共沸物,由T1精馏塔塔釜得到的料液送入T2精馏塔。
萃取剂由原料进料口上方进入T2精馏塔,从T2塔塔顶得到产品乙醇,由T2精馏塔塔底得到水和萃取剂的混合液,这部分料液送往T3精馏塔进行萃取剂的回收。
由T3精馏塔塔顶得到轻组分水,由T3精馏塔塔底得到萃取剂,回收后的萃取剂经换热、升压后,与补加的少量萃取剂一起进入T2精馏塔,实现萃取剂的循环利用。
进料1 流股2 流股3 流股4 流股5 流股6 温度 C 30.0 76.9 78.6 30.1 69.1 60.1压力 bar 1.115 1.013 1.033 2.027 0.300 2.027质量流量 kg/hr 1100.000 470.000 630.000 1000.00026.002 999.998体积流量 cum/hr 1.416 0.647 0.880 0.903 0.027 0.903 质量分数二乙氧基甲烷 4.000 9.345 117PPM 0.000 0.000 0.000 乙醇 90.500 83.350 95.834 0.000 0.000 0.000水 4.000 3.800 4.150 2PPB 100.000511PPB DEM同系物 1.500 3.505 44PPM 0.000 0.000 0.000 萃取剂 0.000 0.000 0.000 100.000 0.000 99.999进料7 流股8 流股9 流股10 流股11 温度 C 78.3 165.7 162.1 30.0 30.0压力 bar 1.013 1.043 0.320 2.027 1.013质量流量 kg/hr 604.000 1026.000 99.998 0.002 999.998 体积流量 cum/hr 0.854 1.058 1.020 <0.001 0.903 质量分数二乙氧基甲烷 122PPM 0.000 0.000 0.000 0.000 乙醇 99.960 0.000 0.000 0.000 0.000 水 231PPM 2.534 511PPB 0.000 511PPB 杂质46PPM 0.000 0.000 0.000 0.000100.000 萃取剂 3PPM 97.466 99.999 100.0004.结构说明4.1T1精馏塔T1精馏塔采用常压操作,操作压力为1atm(a),设计塔径为φ900mm。
共沸精馏提取无水酒精工艺流程

共沸精馏提取无水酒精工艺流程
听说共沸精馏能提取无水酒精,这事儿听起来挺神奇的。
首先,你得把原料酒精送进脱水塔,跟洗衣服似的,给它甩甩水,把大部
分水分去掉。
然后啊,回收塔就得上场了。
这家伙就像个筛子,把脱水后的
酒精再过滤一遍,把里面的小杂质、小水分都筛出去。
这样一来,
酒精就变得更纯净了。
接下来是分离塔,这家伙可是个高手。
它能把酒精和水混在一
起的东西分开来。
通过调整温度和压力,就像玩魔术一样,让酒精
分子从混合物里跳出来。
再沸器呢,就像个大锅炉,不断给混合物加热,让酒精分子有
足够的能量逃出来。
这样一来,分离过程就能顺利进行了。
别忘了冷凝器,这家伙负责把酒精蒸气变成液体。
就像夏天喝
冰镇饮料一样,让酒精蒸气冷却下来,变成清爽的液体。
最后啊,成品冷凝器就是收尾工作了。
它把经过前面几道工序
处理过的无水酒精再做一次净化。
这样一来,最后得到的无水酒精就像新酿的美酒一样纯净。
总的来说啊,共沸精馏提取无水酒精这个过程就像一场魔术表演,每个步骤都像魔术师的手法一样巧妙。
不过别担心,只要掌握了这些技巧,你也能轻松变出纯净的无水酒精来!。
实验四 共沸精馏法制取无水乙醇 实验指导书
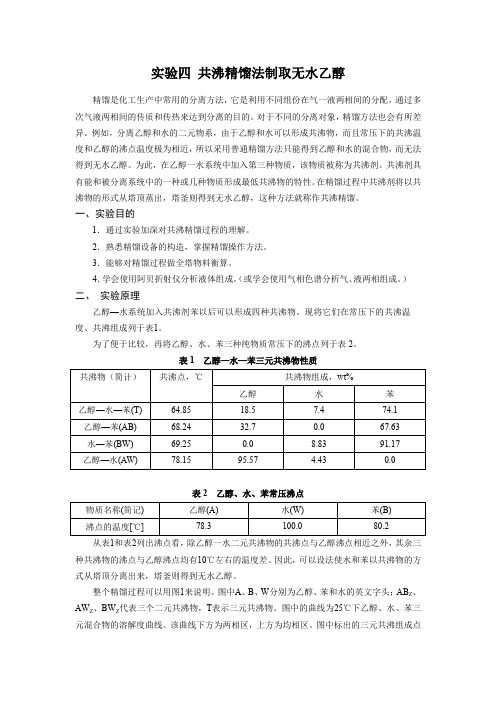
实验四共沸精馏法制取无水乙醇精馏是化工生产中常用的分离方法,它是利用不同组份在气一液两相间的分配,通过多次气液两相间的传质和传热来达到分离的目的。
对于不同的分离对象,精馏方法也会有所差异。
例如,分离乙醇和水的二元物系,由于乙醇和水可以形成共沸物,而且常压下的共沸温度和乙醇的沸点温度极为相近,所以采用普通精馏方法只能得到乙醇和水的混合物,而无法得到无水乙醇。
为此,在乙醇一水系统中加入第三种物质,该物质被称为共沸剂。
共沸剂具有能和被分离系统中的一种或几种物质形成最低共沸物的特性。
在精馏过程中共沸剂将以共沸物的形式从塔顶蒸出,塔釜则得到无水乙醇,这种方法就称作共沸精馏。
一、实验目的1.通过实验加深对共沸精馏过程的理解。
2.熟悉精馏设备的构造,掌握精馏操作方法。
3.能够对精馏过程做全塔物料衡算。
4.学会使用阿贝折射仪分析液体组成。
(或学会使用气相色谱分析气、液两相组成。
)二、实验原理乙醇—水系统加入共沸剂苯以后可以形成四种共沸物。
现将它们在常压下的共沸温度、共沸组成列于表1。
为了便于比较,再将乙醇、水、苯三种纯物质常压下的沸点列于表2。
表1 乙醇—水—苯三元共沸物性质表2 乙醇、水、苯常压沸点从表1和表2列出沸点看,除乙醇一水二元共沸物的共沸点与乙醇沸点相近之外,其余三种共沸物的沸点与乙醇沸点均有10℃左右的温度差。
因此,可以设法使水和苯以共沸物的方式从塔顶分离出来,塔釜则得到无水乙醇。
整个精馏过程可以用图1来说明。
图中A、B、W分别为乙醇、苯和水的英文字头;AB Z、AW Z、BW Z代表三个二元共沸物,T表示三元共沸物。
图中的曲线为25℃下乙醇、水、苯三元混合物的溶解度曲线。
该曲线下方为两相区,上方为均相区。
图中标出的三元共沸组成点T是处在两相区内。
以T为中心,连接三种纯物质A、B、W及三个二元共沸点组成点ABz、AWz、BWz,将该图分为六个小三角形。
如果原料液的组成点落在某个小三角形内,当塔顶采用混相回流时精馏的最终结果只能得到这个小三角形三个顶点所代表的物质。
无水乙醇的制备

有机化学实验报告实验名称:无水乙醇的制备学院:化学工程学院专业:化学工程与工艺班级:化工105班姓名:黄晓敏学号10402010515 指导教师:沈梁均方烨汶日期:2011年11月10日一、实验目的1、了解氧化钙法制备无水乙醇的原理和方法。
2、熟练掌握回流、蒸馏装置的安装和使用方法。
二、实验原理普通工业酒精是含乙醇95.6%和4.4%水的恒沸混合物,其沸点为78.15o C,用蒸馏的方法不能将乙醇中的水进一步除去。
要制得无水乙醇,在实验室中可加入生石灰后回流,使水分与生石灰结合后再进行蒸馏,得到无水乙醇。
CaO + H2O → Ca(OH)2三、主要试剂及物理性质试剂名称外形、性状熔点/℃沸点/℃乙醇(C2H6O)无色透明液体,有愉快的气味和灼烧味,易挥发-114.3 78.5生石灰(Ca O)外形为白色(或灰色、棕白),无定形,溶于酸水,不溶于醇2580 2850氢氧化钠(NaOH)常温下是一种白色晶体,具有强腐蚀性。
易溶于水,其水溶液呈强碱性,能使酚酞变红。
318 1390氯化钙(CaCl2)无色立方结晶体,无毒、无臭、味微苦,极易潮解772 大于1600无水硫酸铜(CuSO4)白色或灰白色粉末;溶液呈酸性,溶于水及稀的乙醇中而不溶于无水乙醇;在潮湿空气中易潮解,吸湿性很强——四、试剂用量及规格40ml 95%乙醇、10g 生石灰、少许苛性钠、少量氯化钙。
五、仪器装置回流装置 .蒸馏装置六、实验步骤及现象步骤现象回流:量取40ml95%的乙醇于100ml 圆底烧瓶中,再慢慢加入16g 颗粒状的生石灰和几颗NaOH ,接着回流1h 。
(14.15~15.15h )随着加热慢慢有蒸气溢出,之后回流管内也慢慢有液体流出蒸馏:回流毕,稍冷圆底烧瓶,改为蒸馏装置。
以圆底烧瓶做接收器,接引管支口上接盛有无水CaCl 2的干燥管。
冷凝管内壁慢慢出现小液滴,约78℃时有液体流入锥形瓶中检验:向蒸馏得出的乙醇中加入少许CuSO 4。
工业酒精制备无水乙醇的流程

工业酒精制备无水乙醇的流程今天咱们来唠唠工业酒精制备无水乙醇的那些事儿。
咱先得知道工业酒精是啥,工业酒精里含有乙醇,但是呢,它可不是纯的乙醇哦,里面还混着一些水和其他的小杂质呢。
那为啥要把工业酒精变成无水乙醇呢?这无水乙醇用处可大啦,在好多化学实验里,要求可严格了,有水的话可能就会搞砸实验,还有在一些医药生产啥的,也需要无水乙醇这种很纯的东西。
那怎么把工业酒精里的水去掉,让它变成无水乙醇呢?这就有一套有趣的流程啦。
有一种办法就是加干燥剂。
就像咱们家里潮湿了,会放干燥剂吸潮气一样。
在工业酒精里加干燥剂,干燥剂就会像小海绵吸水一样,把里面的水给吸走。
常见的干燥剂有氧化钙,也就是咱们常说的生石灰。
把氧化钙加到工业酒精里,氧化钙就开始和水发生反应啦。
这个反应可神奇了,氧化钙和水变成了氢氧化钙。
不过呢,这时候虽然水被反应掉了一部分,但是酒精里可能还有其他的小杂质,还得经过进一步的处理。
还有一种办法是用蒸馏的方法。
蒸馏就像是把不同的东西按照它们的沸点分开。
咱们知道水的沸点是100摄氏度,乙醇的沸点是78.4摄氏度。
把工业酒精加热,温度到了78.4摄氏度的时候,乙醇就会变成气体跑出来,然后通过专门的装置把这些乙醇气体收集起来,冷却之后又变成液体乙醇啦。
但是呢,这种蒸馏得到的乙醇可能还不是完全没有水的,可能还得再蒸馏几次才能得到比较纯的无水乙醇。
要是想得到更纯的无水乙醇,还可以用一些特殊的分馏柱进行分馏。
这种分馏柱就像是一个超级厉害的分离工具。
它可以让乙醇和水在里面反复地汽化、液化,经过这样的过程,就能把乙醇和水分离得更彻底。
另外,还有一种叫共沸蒸馏的方法。
这个方法有点复杂哦。
就是加入一种特殊的物质,这种物质和水会形成一种共沸物,这个共沸物的沸点和乙醇不一样。
加热的时候,这个共沸物就会先变成气体跑出去,这样就把水给带走了,剩下的就是比较纯的乙醇啦。
工业酒精制取无水乙醇的方法

工业酒精制取无水乙醇的方法工业酒精是直接用于工业领域的一种酒精产品,它的主要成分是含有高浓度的无水乙醇。
无水乙醇是一种非常重要的有机化工原料,在化工、制药、食品加工等领域有广泛的应用。
下面将详细介绍工业酒精制取无水乙醇的方法。
1.工业酒精的制备工业酒精的制备有两种常用的方法,一种是由粮食(如小麦、玉米等)发酵得到的,另一种是由石油等石油化工原料经过合成得到的。
无论是哪种方法,制备出来的酒精都不是无水乙醇,需要后续的精制过程来去除其中的水分。
2.精制工业酒精工业酒精中的水分含量通常很高,需要进行精制才能得到无水乙醇。
常用的精制方法有以下几种:-蒸馏法:通过蒸馏的方式,根据乙醇和水的沸点差异来将酒精中的水分蒸发掉。
一般采用多级蒸馏的方式,以提高蒸馏的效果。
-分子筛吸附法:利用分子筛吸附剂对酒精中的水分进行吸附,然后再用适当的方法去除吸附剂中的水分。
-膜分离法:利用特殊的膜片分离酒精和水,使水分通过膜片而流失,得到较为纯净的酒精。
3.无水乙醇的制备精制过的工业酒精中的水分含量在0.1%以下,但仍然不足以满足一些特殊需求的工业应用。
因此,还需要进一步处理才能得到无水乙醇。
-脱水法:使用一种或多种脱水剂(如正丁醇、石油醚等)与工业酒精混合,通过蒸馏的方式除去其中的水分。
脱水剂将水分与酒精形成共沸物,通过蒸馏可以得到无水乙醇。
-活性炭吸附法:利用活性炭对酒精中的水分进行吸附,然后再用适当的方法去除吸附剂中的水分。
-分子筛吸附法:与精制过程中的分子筛吸附法类似,但需要使用更强吸附剂来去除工业酒精中的水分。
无水乙醇的制备方法有很多种,以上仅仅是其中的一些常用方法。
选择适合的方法,需要根据具体的生产要求和设备条件来决定。
无论采用哪种方法,都需要仔细控制操作参数,以获得高质量的无水乙醇产品。
共沸精馏用苯作共沸剂制备无水乙醇
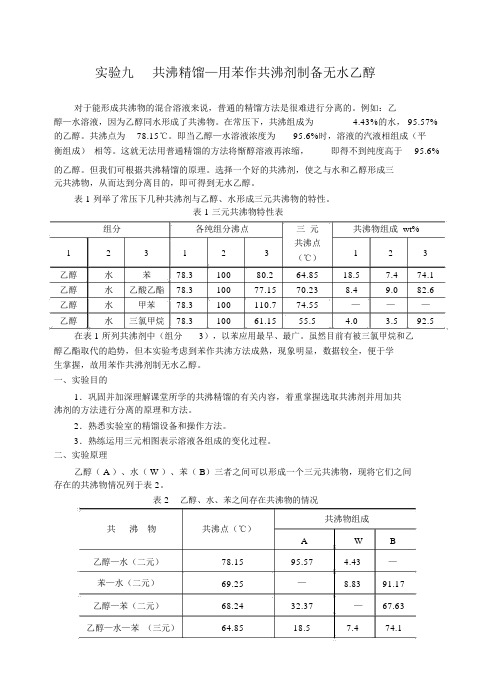
实验九共沸精馏—用苯作共沸剂制备无水乙醇对于能形成共沸物的混合溶液来说,普通的精馏方法是很难进行分离的。
例如:乙醇—水溶液,因为乙醇同水形成了共沸物。
在常压下,共沸组成为 4.43%的水, 95.57%的乙醇。
共沸点为78.15℃。
即当乙醇—水溶液浓度为95.6%时,溶液的汽液相组成(平衡组成)相等。
这就无法用普通精馏的方法将惭醇溶液再浓缩,即得不到纯度高于95.6%的乙醇。
但我们可根据共沸精馏的原理。
选择一个好的共沸剂,使之与水和乙醇形成三元共沸物,从而达到分离目的,即可得到无水乙醇。
表 1 列举了常压下几种共沸剂与乙醇、水形成三元共沸物的特性。
表 1 三元共沸物特性表组分各纯组分沸点三元共沸物组成 wt%123123共沸点123(℃)乙醇水苯78.310080.264.8518.57.474.1乙醇水乙酸乙酯78.310077.1570.238.49.082.6乙醇水甲苯78.3100110.774.55———乙醇水三氯甲烷78.310061.1555.5 4.0 3.592.5在表 1 所列共沸剂中(组分3),以苯应用最早、最广。
虽然目前有被三氯甲烷和乙醇乙酯取代的趋势,但本实验考虑到苯作共沸方法成熟,现象明显,数据较全,便于学生掌握,故用苯作共沸剂制无水乙醇。
一、实验目的1.巩固并加深理解课堂所学的共沸精馏的有关内容,着重掌握选取共沸剂并用加共沸剂的方法进行分离的原理和方法。
2.熟悉实验室的精馏设备和操作方法。
3.熟练运用三元相图表示溶液各组成的变化过程。
二、实验原理乙醇( A )、水( W )、苯( B)三者之间可以形成一个三元共沸物,现将它们之间存在的共沸物情况列于表 2。
表 2乙醇、水、苯之间存在共沸物的情况共沸物共沸点(℃)共沸物组成A W B乙醇—水(二元)78.1595.57 4.43—苯—水(二元)69.25—8.8391.17乙醇—苯(二元)68.2432.37—67.63乙醇—水—苯(三元)64.8518.57.474.1当添加适当数量的苯于工业乙醇中蒸馏时,则乙醇—水—苯三元共沸物首先馏出,其次为乙醇—苯二元共沸物,无水乙醇最后留于釜底,其蒸馏过程以图 1 说明。
实验四 共沸精馏法制取无水乙醇 实验指导书
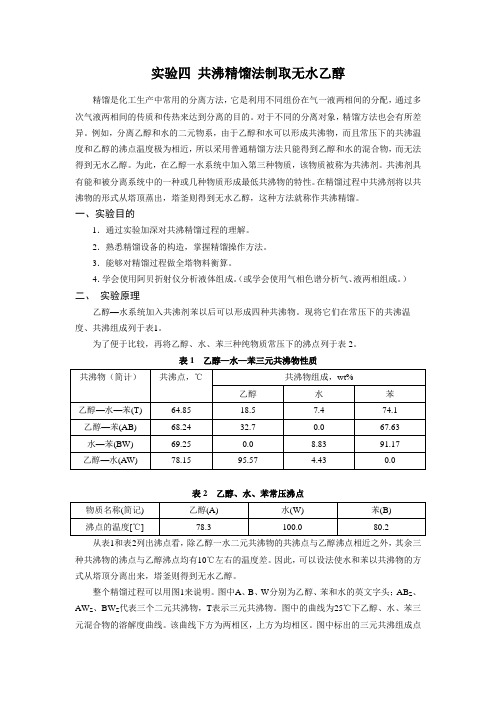
实验四共沸精馏法制取无水乙醇精馏是化工生产中常用的分离方法,它是利用不同组份在气一液两相间的分配,通过多次气液两相间的传质和传热来达到分离的目的。
对于不同的分离对象,精馏方法也会有所差异。
例如,分离乙醇和水的二元物系,由于乙醇和水可以形成共沸物,而且常压下的共沸温度和乙醇的沸点温度极为相近,所以采用普通精馏方法只能得到乙醇和水的混合物,而无法得到无水乙醇。
为此,在乙醇一水系统中加入第三种物质,该物质被称为共沸剂。
共沸剂具有能和被分离系统中的一种或几种物质形成最低共沸物的特性。
在精馏过程中共沸剂将以共沸物的形式从塔顶蒸出,塔釜则得到无水乙醇,这种方法就称作共沸精馏。
一、实验目的1.通过实验加深对共沸精馏过程的理解。
2.熟悉精馏设备的构造,掌握精馏操作方法。
3.能够对精馏过程做全塔物料衡算。
4.学会使用阿贝折射仪分析液体组成。
(或学会使用气相色谱分析气、液两相组成。
)二、实验原理乙醇—水系统加入共沸剂苯以后可以形成四种共沸物。
现将它们在常压下的共沸温度、共沸组成列于表1。
为了便于比较,再将乙醇、水、苯三种纯物质常压下的沸点列于表2。
表1 乙醇—水—苯三元共沸物性质表2 乙醇、水、苯常压沸点从表1和表2列出沸点看,除乙醇一水二元共沸物的共沸点与乙醇沸点相近之外,其余三种共沸物的沸点与乙醇沸点均有10℃左右的温度差。
因此,可以设法使水和苯以共沸物的方式从塔顶分离出来,塔釜则得到无水乙醇。
整个精馏过程可以用图1来说明。
图中A、B、W分别为乙醇、苯和水的英文字头;AB Z、AW Z、BW Z代表三个二元共沸物,T表示三元共沸物。
图中的曲线为25℃下乙醇、水、苯三元混合物的溶解度曲线。
该曲线下方为两相区,上方为均相区。
图中标出的三元共沸组成点T是处在两相区内。
以T为中心,连接三种纯物质A、B、W及三个二元共沸点组成点ABz、AWz、BWz,将该图分为六个小三角形。
如果原料液的组成点落在某个小三角形内,当塔顶采用混相回流时精馏的最终结果只能得到这个小三角形三个顶点所代表的物质。
用共沸精馏隔壁塔生产无水乙醇的研究_李军

的过量 , 塔釜的甲醇迅速增加 , 相当于引入了新的污 染物 , 增加了后续分离工艺 。 因此催化精馏工艺酸 醇比宜在 2 ~ 3 范围内 。
组分(反应段长度):1— 水(1.17 m);2 — 甲醇(1.17 m); 3 — 醋酸甲酯(1.17 m);4 —醋酸(1.17 m);5 — 水(0.72 m); 6 — 甲醇(0.72 m);7 — 醋酸甲酯(0.72 m);8 — 醋酸(0.72 m)
1 — 主塔 ;2— 侧线精馏塔
图 8 新工艺中隔壁塔内温度分布 由图 7 、8 可以看出 , 常规共沸精馏流程脱水塔 、 提浓塔与隔壁塔主塔 、侧线精馏段温度分布的趋势 基本相同 , 由于有共沸物的存在 , 在塔中都有一段温 度缓慢上升的曲线 , 但在隔壁塔侧线精馏段第 1 块 板 , 温度较高 , 这是由于在区域(1)底部提供了温度 较高的液相回流 。在隔壁塔中 , 只需要 1 个冷凝器 , 故其能耗较低 。 2.4 常规流程与隔壁塔内流量分布的比较
第 28 卷增刊(1) 2008 年 6 月
现代化工 Modern Chemical Industry
June 2008 · 93 ·
用共沸精馏隔壁塔生产无水乙醇的研究
李 军 , 孙兰义 , 胡有元 , 李青松 (中国石油大学化学化工学院 , 山东 青岛 266555)
摘要 :提出 1 种单塔共沸精馏生产无水乙醇的新工艺流程 , 即采用隔壁塔替代常规共沸精馏流程中的脱水塔及提浓 塔。 应
(School of Chemistry &Chemical Engineering , China University of Petroleum , Qiangdao 266555, China)
Abstract :A novel process of single-column azeotropic distillation process is proposed for the production of dehydration ethanol , where the dividing-wall column is used instead of the conventional dehydration column and concentrator .The new and the conventional process are simulated with Aspen Plus software .The results show that the energy consumption of the new process can be reduced by 28.2%, and the cost of equipment and operation can be decreased compared to the conventional process .
恒沸精馏法生产无水酒精

℃, 比乙醇的 78. 3 ℃或乙醇 —水溶液的恒沸点 78. 15 ℃都要低 得多 ,在精馏时从塔顶馏出 。三元恒沸物的组成(质量比 W %) 为 环己烷 76 % , 乙醇 17 % , 水 7 % , 其中水对乙醇的质量比为 0. 41 , 比乙醇 —水恒沸物的这一质量比 0. 046 要大得多 。故只要 有足量的环己烷作为夹带剂 ,在精馏时水将全部集中于三元恒沸 物中从塔顶馏出 ,塔底产品为无水酒精 。
(1) 脱水用的酒精浓度太低 ,大量的水坠入塔底 。(2) 开机过 程中提前进行脱水塔和回收塔之间的循环 ,由于此时回收塔内酒 精 、环己烷的贮量还较少 ,塔顶酒精浓度太低 ,致使回收塔内大量 的水被带入脱水塔中 。(3) 环己烷的加入量过少 ,塔釜温度过高或 过低 。
处理措施 : (1) 提高脱水用酒精浓度 ,至少应在 90 %以上 。(2) 开机过程中必须等回收塔内有足够量的酒精和环己烷时 ,才能开 始脱水塔和回收塔之间的循环 。(3) 适量补加脱水剂 。(4) 一旦发 现酒精浓度低 , 就应加大脱水塔向回收塔的送出量 , 减少回收塔 向脱水塔的送出量 , 尽快将脱水塔底部多余的水送入回收塔 , 然 后由回收塔底部排走 。(5) 在整个系统的运行过程中 ,要维持系统 的稳定 , 特别是进汽 、进料 、回流稳定 , 要控制好分离器的分层工 作 ,绝对避免重相中的水进入脱水塔中 。 6. 3 回收塔底部跑酒的原因 : 进汽量不足 , 进料不稳 , 塔板有漏 液 ,塔里液位忽高忽低 。
恒沸精馏制备无水乙醇的工艺流程

恒沸精馏制备无水乙醇的工艺流程In the process of preparing anhydrous ethanol through constant boiling distillation, it is essential to understand the key steps involved in this industry-standard technique. This method involves the separation of ethanol from water through the application of heat to create vapor, which is then condensed back into liquid form.在恒沸精馏制备无水乙醇的过程中,了解这一行业标准技术中涉及的关键步骤至关重要。
这种方法涉及通过加热将乙醇与水分离,从而产生蒸汽,然后将其冷凝为液体形式。
The first step in the process is to feed the ethanolic liquid mixture into a distillation column. This column is designed to allow for the separation of ethanol and water based on their differences in boiling points. As the mixture is heated, the ethanol will vaporize at a lower temperature than water, allowing for the separation.该过程的第一步是将乙醇液体混合物输送到一个蒸馏塔中。
该塔的设计旨在基于乙醇和水的沸点差异来实现它们的分离。
当混合物加热时,乙醇会在比水更低的温度下蒸发,从而实现分离。
无水乙醇制备(氧化钙法)

实验五:无水乙醇的制备(氧化钙法)一、实验目的:1、了解氧化钙法制备无水乙醇的原理或方法。
2、熟练掌握回流、蒸馏装置的安装或使用方法。
二、实验原理:普通的工业酒精是含乙醇95.6%和4.4%水的恒沸混合物,其沸点为78.15℃,用蒸馏的方法不能将乙醇中的水进一步除去。
要制的无水乙醇,在实验室中可加入生石灰后回流,是水与生石灰结合后再进行蒸馏,得到无水乙醇。
CaO + H2O → Ca(OH)2图1、蒸馏装置图2、回流装置三、仪器及药品:仪器:100ml的圆底烧瓶、直形冷凝管、球形冷凝管、干燥管等;药品:95%乙醇、氧化钙、氢氧化钠、氯化钙。
四、实验步骤:1、回流加热除水在100ml的圆底烧瓶中,加入40ml95%乙醇,慢慢放入16克小颗粒状的生石灰和几颗氢氧化钠,回流一小时。
2、蒸馏回流完毕,将回流装置改为蒸馏装置,以圆底烧瓶做接受器,接引管支口上接盛无水氯化钙的干燥管。
所蒸得的乙醇密封储存,并用无水硫酸铜检查。
五、数据处理:表一:无水乙醇制备数据六、结果及讨论1、工业酒精和氧化钙反应回流可以制的无水乙醇,蒸馏可以的到纯的无水乙醇。
2、本次实验采用的是氧化钙和工业酒精制取无水乙醇,采用无水硫酸铜检验水的存在与否,该次操作中用的氧化钙充足、回流时间长,保证了工业酒精中的水与氧化钙充分反应,注意蒸馏时蒸馏装置要干燥;蒸馏时首先没有无水氯化钙和干燥管导致后来的无水乙醇纯度不高。
还有冷凝水水速不宜过快,保证冷凝管温度适宜即可,这样可以节约水。
七、实验注意事项:1、仪器因该事先干燥。
2、接引管支口上因该接干燥管。
3、务必使用颗粒状的氧化钙,用粉末状的氧化钙,则爆沸严重。
4、在氧化钙中加入少许氢氧化钠。
5、实验完毕要及时清洗仪器。
有机化学实验报告实验名称:无水乙醇的制备(氧化钙法)学院:化学工程学院专业:化学工程与工艺班级:化工09-2班姓名:徐正林学号***********指导教师:肖勋文刘望才日期:2010年10月25日。
无水乙醇操作规程

无水乙醇操作规程年产30000吨无水乙醇操作规程一、生产原理本工艺采用苯作萃取剂,根据苯、酒精、水三元共沸的原理将95%(V/V)酒精中的水带走,获取99.9%以上的无水乙醇。
从下表可以看出:酒精、水和苯三元混合物的沸点比其中任何两种物质混合物及单体物质的沸点都低。
二、主要设备及其作用1.脱水塔脱水塔的作用是脱除普级酒精中的多余水分。
普级酒精和苯在塔内形成三个区域:顶部区域:苯、酒精和水三元混合物区(按一定比例组分);中部区域:苯和酒精的混合物区;底部区域:沸腾的高纯度无水乙醇区。
2.回收塔回收塔的作用是回收富水相中少量的苯和酒精,塔底排出废水。
3.压力表用来显示各设备的承受能力及运行情况。
三、工艺参数1.脱水塔塔釜压力:P1:0.01-0.04M Pa塔釜温度:T1:86-88℃第21板温度:T21:78-82℃第33板温度:T33:72.5-75℃塔顶温度:T2:65-66.5℃2.回收塔塔釜压力:P1:0.03-0.05 M Pa塔釜温度:T1:110±1℃塔顶温度:T2:102±1℃3.冷凝器组最后排放温度T:≤35℃四、操作规程㈠水、汽实验1.打开苯贮罐至苯分离器阀门,苯分离器至富苯泵阀门,富苯泵至脱水塔阀门。
给苯贮罐注水,启动富苯泵,完成脱水塔、苯分离器、富水泵、富苯泵的清洗、水试工作。
2.打开回流罐至回流泵阀门,回流泵至回收塔阀门,回收塔排空阀门。
给回流罐注水,启动回流泵,完成回流罐、回流泵、回收塔的清洗、水试工作。
3.开启相应的阀门和泵,完成其他设备、管道的清洗、水试工作。
4.回收塔及脱水塔注入干净水至玻璃液位计的中部,给回收塔通蒸汽,缓慢开启进气阀门并注意观察进压力及水的位置,水位下降后及时补充,使之保持在液位计中位置。
㈡、开机前的准备工作1.详细检查各设备、管道、和阀门开关到正确位置。
2.与维修、锅炉房联系,对仪器、仪表进行检验、校对。
3.按要求供汽。
㈢、投料开机1.给回收塔注水(干净水)至塔底液位计的1/2高度。
实验四无水乙醇的制备(氧化钙法)

实验四:无水乙醇的制备(氧化钙法)
[实验目的]
1.了解氧化钙法制备无水乙醇的原理和方法。
2.熟练掌握回流装置的安装和使用方法。
[实验原理]
普通的工业酒精是含乙醇95.6%和4.4%水的恒沸混合物,其沸点为78.150C,用蒸馏的方法不能将乙醇中的水进一步除去。
要制得无水乙醇,在实验室中可加入生石灰后回流,使水分与生石灰结合后再进行蒸馏,得到无水乙醇。
CaO
简单蒸馏的原理(略)
[仪器及药品]
仪器:100ml圆底烧瓶、直、球形冷凝管、干燥管等;
药品:95%乙醇、CaO、NaOH、CaCl2
[实验步骤]
1.回流加热除水
在100 ml的圆底烧瓶中,加入20 ml95%乙醇,慢慢放入8克小颗粒状的生石灰和几颗NaOH,回流1h。
2.蒸馏
回流毕,改为蒸馏装置,以圆底烧瓶做接受器,接引管支口上接盛有无水氯化钙的干燥管。
所蒸得的乙醇密封储存,并用无水CuSO4检验。
[实验注意事项]
1.仪器应事先干燥。
2.接引管支口上应接干燥管(为何?)。
3.务必使用颗粒状的氧化钙,切勿用粉末状的氧化钙,否则暴沸严重。
4.在CaO中还应该加入少许NaOH(为何?)。
