材料科学基础作业解答
材料科学基础习题与参考答案(doc14页)完美版

材料科学基础习题与参考答案(doc14页)完美版第⼀章材料的结构⼀、解释以下基本概念空间点阵、晶格、晶胞、配位数、致密度、共价键、离⼦键、⾦属键、组元、合⾦、相、固溶体、中间相、间隙固溶体、置换固溶体、固溶强化、第⼆相强化。
⼆、填空题1、材料的键合⽅式有四类,分别是(),(),(),()。
2、⾦属原⼦的特点是最外层电⼦数(),且与原⼦核引⼒(),因此这些电⼦极容易脱离原⼦核的束缚⽽变成()。
3、我们把原⼦在物质内部呈()排列的固体物质称为晶体,晶体物质具有以下三个特点,分别是(),(),()。
4、三种常见的⾦属晶格分别为(),()和()。
5、体⼼⽴⽅晶格中,晶胞原⼦数为(),原⼦半径与晶格常数的关系为(),配位数是(),致密度是(),密排晶向为(),密排晶⾯为(),晶胞中⼋⾯体间隙个数为(),四⾯体间隙个数为(),具有体⼼⽴⽅晶格的常见⾦属有()。
6、⾯⼼⽴⽅晶格中,晶胞原⼦数为(),原⼦半径与晶格常数的关系为(),配位数是(),致密度是(),密排晶向为(),密排晶⾯为(),晶胞中⼋⾯体间隙个数为(),四⾯体间隙个数为(),具有⾯⼼⽴⽅晶格的常见⾦属有()。
7、密排六⽅晶格中,晶胞原⼦数为(),原⼦半径与晶格常数的关系为(),配位数是(),致密度是(),密排晶向为(),密排晶⾯为(),具有密排六⽅晶格的常见⾦属有()。
8、合⾦的相结构分为两⼤类,分别是()和()。
9、固溶体按照溶质原⼦在晶格中所占的位置分为()和(),按照固溶度分为()和(),按照溶质原⼦与溶剂原⼦相对分布分为()和()。
10、影响固溶体结构形式和溶解度的因素主要有()、()、()、()。
11、⾦属化合物(中间相)分为以下四类,分别是(),(),(),()。
12、⾦属化合物(中间相)的性能特点是:熔点()、硬度()、脆性(),因此在合⾦中不作为()相,⽽是少量存在起到第⼆相()作⽤。
13、CuZn、Cu5Zn8、Cu3Sn的电⼦浓度分别为(),(),()。
材料科学基础章作业参考答案.
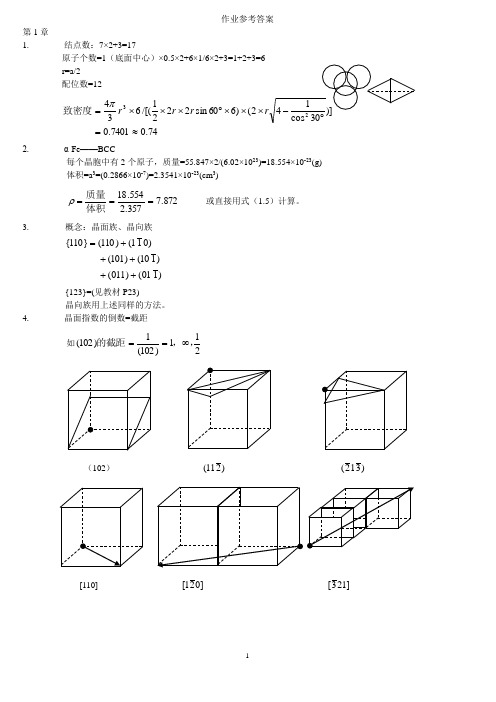
作业参考答案第1章1. 结点数:7×2+3=17原子个数=1(底面中心)×0.5×2+6×1/6×2+3=1+2+3=6r=a/2配位数=1274.07401.02()660sin2221/[(6343≈=⨯⨯⨯︒⨯⨯⨯=rrrπ致密度2. α-Fe——BCC每个晶胞中有2个原子,质量=55.847×2/(6.02×1023)=18.554×10-23(g)体积=a3=(0.2866×10-7)=2.3541×10-23(cm3)872.7357.2554.18===体积质量ρ或直接用式(1.5)计算。
3.概念:晶面族、晶向族)101()011()110()101()011()110(}110{+++++={123}=(见教材P23)晶向族用上述同样的方法。
4. 晶面指数的倒数=截距如211)102(1)102(,,的截距∞==(102))211()312( [110] ]021[]213[5.晶向指数:]101[和]011[6.7.8. 9. (略,不要求) 10.设晶格常数为a22100a =)面密度(785.048210022==⨯=ππr r )面致密度( 222110a=)面密度(555.02428211022==⨯=ππrr )面致密度(2234321111a r ==)面密度(906.03232111122==⨯=ππr r )面致密度( 11. (略,不要求)12. (略,不要求) 13. 6/2+12/4=614.立方晶系晶面间距计算公式:)011()110()112(]011[]2[]111[222lk h na d ++=① )nm (143.0286.02100121222100=⨯=++=ad)nm (202.0286.021011222110=⨯=++=a d)nm (0764.0286.0141321222123=⨯=++=a d②)nm (1825.0365.02100121222100=⨯=++=ad)nm (2107.0365.031111222111=⨯=++=a d)nm (09125.0365.042121121222112=⨯=++=ad③(略,不要求)15. (略,不要求) 16. (略,不要求)一、 单项选择题。
(完整版)材料科学基础第1-2章作业及解答彭

第一章作业——材料结构的基本知识1、简述一次键与二次键的差异及各键的特点。
2、简述三大类材料中的结合键类型及性能(物性、力性)特点。
3、为什么金属材料的密度比陶瓷材料及高分子材料密度高?4、用金属键的特征解释金属材料的性能-----①良好的导电;②良好的导热性;③正的电阻温度系数;④不透明性及具有金属光泽;⑤良好的塑性⑥金属之间的溶解性(固溶能力)。
5、简述晶体与非晶体的主要区别。
6、简述原子结构、原子结合键、原子的排列方式及显微组织对材料性能的影响。
第一章作业解答1、述一次键与二次键的差异及各键的特点。
解答:(1)一次键结合力较强,包括金属键、离子键、共价键;二次键结合力较弱,包括范德华键和氢键。
一次键主要依靠外壳层电子转移或共享以形成稳定的电子壳层;二次键是借原子之间的偶极吸引力结合而成。
(2)金属键电子共有化,没有方向性和饱和性;离子键没有方向性,但要满足正负电荷平衡要求;共价键有明显的方向性和饱和性;范德华键没有方向性、饱和性;氢键(X-H…Y)有饱和性、方向性。
2、简述三大类材料中的结合键类型及性能(物性、力性)特点。
解答:(1)三大类材料主要指金属材料、陶瓷材料和高分子材料。
(2)金属材料中的结合键主要是金属键,其次是共价键、离子键,使金属材料具有较高的熔点、密度,良好的导电、导热性能及较高的弹性模量、强度和塑性。
陶瓷材料中的结合键主要是离子键和共价键,使其熔点高、密度低,具有良好的绝缘性能和绝热性能,高的弹性模量和强度,但塑性差,脆性大。
高分子材料中分子链内部虽为共价键结合,但分子链之间为二次键结合,使其具有较低的熔点、密度,良好的绝缘性能、绝热性能及较低的弹性模量、强度和塑性。
3、为什么金属材料的密度比陶瓷材料及高分子材料密度高?金属材料的密度较高是因为①金属元素具有较高的相对原子质量,②金属材料主要以金属键结合,金属键没有方向性和饱和性,使金属原子总是趋于密集排列,达到密堆结构。
材料科学基础习题与参考答案(doc14页)(优质版)

材料科学基础习题与参考答案(doc14页)(优质版)第一章材料的结构一、解释以下基本概念空间点阵、晶格、晶胞、配位数、致密度、共价键、离子键、金属键、组元、合金、相、固溶体、中间相、间隙固溶体、置换固溶体、固溶强化、第二相强化。
二、填空题1、材料的键合方式有四类,分别是(),(),(),()。
2、金属原子的特点是最外层电子数(),且与原子核引力(),因此这些电子极容易脱离原子核的束缚而变成()。
3、我们把原子在物质内部呈()排列的固体物质称为晶体,晶体物质具有以下三个特点,分别是(),(),()。
4、三种常见的金属晶格分别为(),()和()。
5、体心立方晶格中,晶胞原子数为(),原子半径与晶格常数的关系为(),配位数是(),致密度是(),密排晶向为(),密排晶面为(),晶胞中八面体间隙个数为(),四面体间隙个数为(),具有体心立方晶格的常见金属有()。
6、面心立方晶格中,晶胞原子数为(),原子半径与晶格常数的关系为(),配位数是(),致密度是(),密排晶向为(),密排晶面为(),晶胞中八面体间隙个数为(),四面体间隙个数为(),具有面心立方晶格的常见金属有()。
7、密排六方晶格中,晶胞原子数为(),原子半径与晶格常数的关系为(),配位数是(),致密度是(),密排晶向为(),密排晶面为(),具有密排六方晶格的常见金属有()。
8、合金的相结构分为两大类,分别是()和()。
9、固溶体按照溶质原子在晶格中所占的位置分为()和(),按照固溶度分为()和(),按照溶质原子与溶剂原子相对分布分为()和()。
10、影响固溶体结构形式和溶解度的因素主要有()、()、()、()。
11、金属化合物(中间相)分为以下四类,分别是(),(),(),()。
12、金属化合物(中间相)的性能特点是:熔点()、硬度()、脆性(),因此在合金中不作为()相,而是少量存在起到第二相()作用。
13、CuZn、Cu5Zn8、Cu3Sn的电子浓度分别为(),(),()。
材料科学基础答案

材料科学基础答案1.为什么室温下金属晶粒越细强度,硬度越高,塑性韧性也越好答:金属晶粒越细,晶界面积越大,位错障碍越多,需要协调的具有不同位向的晶粒越多,金属塑性变形的抗力越高,从而导致金属强度和硬度越高。
金属的晶粒越细,单位体积内晶粒数目越多,同时参与变形的晶粒数目也越多,变形越均匀,推迟了裂纹的形成和扩展,使得在断裂前发生较大的塑性变形。
在强度和塑性同时增加的情况下,金属在断裂前消耗的功增大,因而其韧性也比较好。
因此,金属的晶粒越细,其塑性和韧性也越好。
2.冷塑性变形金属产生加工硬化的原因随变形量增加,空密度增加。
④由于晶粒由有利位向而发生几何硬化,因此使变形抗力增加。
随变形量增加,亚结构细化,亚晶界对位错运动有阻碍作用。
答:①晶体内部存在位错源,变形时发生了位错增值,随变形量增加,位错密度增加。
由于位错之间的交互作用,使变形抗力增加。
3.某厂用冷拉钢丝绳吊运出炉热处理工件去淬火,钢丝绳的承载能力远超过工件的质量,但在工件的运送过程中钢丝绳发生断裂,试分析其原因答:冷拉钢丝绳是利用热加工硬化效应提高其强度的,在这种状态下的钢丝中晶体缺陷密度增大,强度增加,处于加工硬化状态。
在淬火的温度下保温,钢丝将发生回复、再结晶和晶粒长大过程,组织和结构恢复软化状态。
在这一系列变化中,冷拉钢丝的加工硬化效果将消失,强度下降,在再次起吊时,钢丝将被拉长,发生塑性变形,横截面积减小,强度将比保温前低,所以发生断裂。
4细化晶粒方法1.在浇注过程中: 1)增大过冷度; 2)加入变质剂; 3)进行搅拌和振动等。
2. 在热轧或锻造过程中: 1)控制变形度; 2)控制热轧或锻造温度。
3. 在热处理过程中:控制加热和冷却工艺参数利用相变重结晶来细化晶粒。
4. 对冷变形后退火态使用的合金: 1)控制变形度; 2)控制再结晶退火温度和时间5、试说明滑移,攀移及交滑移的条件,过程和结果,并阐述如何确定位错滑移运动的方向。
解答:滑移:切应力作用、切应力大于临界分切应力;台阶攀移:纯刃位错、正应力、热激活原子扩散;多余半原子面的扩大与缩小交滑移:纯螺位错、相交位错线的多个滑移面;位错增殖位错滑移运动的方向,外力方向与b一致时从已滑移区→未滑移区。
材料科学基础课后作业答案

2
2
2
此反应满足几何条件但不满足能量条件,反应不能成立。
8. 在钢棒的表面,每20个铁的晶胞中有一个碳原子,在离表面
1mm处每30个铁的晶胞中有一个碳原子。温度为1000℃时扩散
系数是3×10-11m2/s,且结构为面心立方(a=0.365 nm)。问每
分钟因扩散通过单位晶胞的碳原子数是多少?
由已知可以计算出碳的浓度: C2=1/[30*(0.365×10-9m)3]=0.68×1027 /m3 C1=1/[20*(0.365×10-9m)3]=1.03×1027 /m3
a
b
• (c)[0 1 2]
(d)[1 3 3]
• (e)[1 1 1]
(f)[1 2 2]
• (g)[1 2 3]
(h)[1 0 3]
3. Determine the indices for the directions shown in the following cubic unit cell:222
此反应满足几何条件和 能量条件,反应能进行 。
解2: a[100] a [111] a [1 1 1]
2
2
(1)几何条件
反应前 a[100]
反应后
a [111] a [1 1 1]= a [200] a[100]
2
2
2
(2)能量条件
反应前
b2 a2
反应后
b2 ( a 12 12 12 )2 ( a 12 12 12 )2 3 a2 a2
9. 某固溶体的合金的相图如下图所示。合金成分为50 % B, 凝固到某温度时液相含有40 % B,固相含有80 % B,此时 液体和固体各占多少分数?
解:
材料科学基础作业参考答案
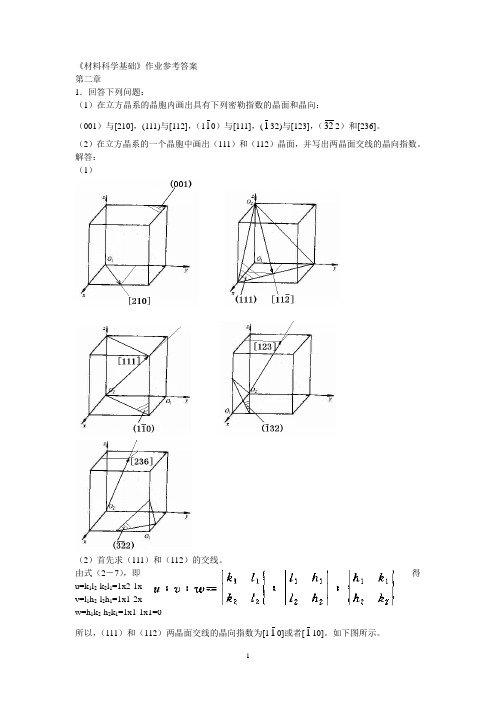
《材料科学基础》作业参考答案第二章1.回答下列问题:(1)在立方晶系的晶胞内画出具有下列密勒指数的晶面和晶向:(001)与[210],(111)与[112],(110)与[111],(132)与[123],(322)和[236]。
(2)在立方晶系的一个晶胞中画出(111)和(112)晶面,并写出两晶面交线的晶向指数。
解答:(1)(2)首先求(111)和(112)的交线。
由式(2-7),即得u=k1l2-k2l1=1x2-1x1=1v=l1h2-l2h1=1x1-2x1=-1w=h1k2-h2k1=1x1-1x1=0所以,(111)和(112)两晶面交线的晶向指数为[110]或者[110]。
如下图所示。
3 立方晶系的{111}、{110}、{123}晶面族各包括多少晶面?写出它们的密勒指数。
解答:++++++++=)213()231()321()132()312()321()231()123(}123{+++++++)312()132()213()123()132()312()231()132()123()213()321()231()213()123()312()321(++++++++注意:书中有重复的。
如(111)与(111)应为同一晶面,只是位于坐标原点的位置不同。
6.(略)7.(题略) (1)(2)用公式求。
(3) 用公式 求。
(1)d(100)=0.286nmd(110)=0.202nmd(123)=0.076nm显然,d(100)最大。
hkl d =(2) d(100)=0.365nmd(111)=0.211nmd(112)=0.149nm显然,d(100)最大。
(3) d(1120)=0.1605 nmd(1010)=0.278nmd(1012)=0.190nm显然,d(1010)最大。
由(1)、(2)、(3)得低指数的面间距较大,而高指数的晶面间距则较小8.回答下列问题:(1)通过计算判断(110)、(132)、(311)晶面是否属于同一晶带?(2)求(211)和(110)晶面的晶带轴,并列出五个属于该晶带的晶面的密勒指数。
材料科学基础经典习题及答案

第一章 材料科学基础1.作图表示立方晶体的()()()421,210,123晶面及[][][]346,112,021晶向。
2.在六方晶体中,绘出以下常见晶向[][][][][]0121,0211,0110,0112,0001等。
3.写出立方晶体中晶面族{100},{110},{111},{112}等所包括的等价晶面。
4.镁的原子堆积密度和所有hcp 金属一样,为0.74。
试求镁单位晶胞的体积。
已知Mg 的密度3Mg/m 74.1=mg ρ,相对原子质量为24.31,原子半径r=0.161nm 。
5.当CN=6时+Na 离子半径为0.097nm ,试问:1) 当CN=4时,其半径为多少?2) 当CN=8时,其半径为多少?6. 试问:在铜(fcc,a=0.361nm )的<100>方向及铁(bcc,a=0.286nm)的<100>方向,原子的线密度为多少?7.镍为面心立方结构,其原子半径为nm 1246.0=Ni r 。
试确定在镍的(100),(110)及(111)平面上12mm 中各有多少个原子。
8. 石英()2SiO 的密度为2.653Mg/m 。
试问: 1) 13m 中有多少个硅原子(与氧原子)?2) 当硅与氧的半径分别为0.038nm 与0.114nm 时,其堆积密度为多少(假设原子是球形的)?9.在800℃时1010个原子中有一个原子具有足够能量可在固体内移动,而在900℃时910个原子中则只有一个原子,试求其激活能(J/原子)。
10.若将一块铁加热至850℃,然后快速冷却到20℃。
试计算处理前后空位数应增加多少倍(设铁中形成一摩尔空位所需要的能量为104600J )。
11.设图1-18所示的立方晶体的滑移面ABCD 平行于晶体的上、下底面。
若该滑移面上有一正方形位错环,如果位错环的各段分别与滑移面各边平行,其柏氏矢量b ∥AB 。
1) 有人认为“此位错环运动移出晶体后,滑移面上产生的滑移台阶应为4个b ,试问这种看法是否正确?为什么?2)指出位错环上各段位错线的类型,并画出位错运动出晶体后,滑移方向及滑移量。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第一章1.简述一次键与二次键各包括哪些结合键这些结合键各自特点如何答:一次键——结合力较强,包括离子键、共价键和金属键。
二次键——结合力较弱,包括范德瓦耳斯键和氢键。
①离子键:由于正、负离子间的库仑(静电)引力而形成。
特点:1)正负离子相间排列,正负电荷数相等;2)键能最高,结合力很大;②共价键:是由于相邻原子共用其外部价电子,形成稳定的电子满壳层结构而形成。
特点:结合力很大,硬度高、强度大、熔点高,延展性和导电性都很差,具有很好的绝缘性能。
③金属键:贡献出价电子的原子成为正离子,与公有化的自由电子间产生静电作用而结合的方式。
特点:它没有饱和性和方向性;具有良好的塑性;良好的导电性、导热性、正的电阻温度系数。
④范德瓦耳斯键:一个分子的正电荷部位和另一个分子的负电荷部位间的微弱静电吸引力将两个分子结合在一起的方式。
也称为分子键。
特点:键合较弱,易断裂,可在很大程度上改变材料的性能;低熔点、高塑性。
2.比较金属材料、陶瓷材料、高分子材料在结合键上的差别。
答:①金属材料:简单金属(指元素周期表上主族元素)的结合键完全为金属键,过渡族金属的结合键为金属键和共价键的混合,但以金属键为主。
②陶瓷材料:陶瓷材料是一种或多种金属同一种非金属(通常为氧)相结合的化合物,其主要结合方式为离子键,也有一定成分的共价键。
③高分子材料:高分子材料中,大分子内的原子之间结合方式为共价键,而大分子与大分子之间的结合方式为分子键和氢键。
④复合材料:复合材料是由二种或者二种以上的材料组合而成的物质,因而其结合键非常复杂,不能一概而论。
3. 晶体与非晶体的区别稳态与亚稳态结构的区别晶体与非晶体区别:答:性质上,(1)晶体有整齐规则的几何外形;(2)晶体有固定的熔点,在熔化过程中,温度始终保持不变;(3)晶体有各向异性的特点。
结构上,晶体原子排列有序,非晶体排列长程无序。
稳态与亚稳态结构的区别同种材料在不同条件下可以得到不同的结构,其中能量最低的结构称为稳态结构。
而能量相对较高的结构称为亚稳态结构。
第二章1.布拉菲将晶体结构共分为哪几大晶系试画出面心立方、体心四方、简单六方与简单三斜这四种布拉菲点阵的晶胞,并写出其棱边长度与夹角关系答:分为七大晶系:立方晶系、四方晶系、菱方晶系、六方晶系、正交晶系、单斜晶系、三斜晶系。
面心立方:,a=b=c,α=β=γ= 90°体心四方:,a=b≠c,α=β=γ= 90°简单六方:,a=b≠c,α=β= 90°,γ=120 °简单三斜:,a≠b≠c,α≠β≠γ2. 画出立方晶系中下列晶面和晶向:(010),(011),(231),;[010],[111],。
3.针对体心立方(BCC)晶胞:(1)写出BCC晶体中的配位数(CN)、原子数(N)、原子半径r与点阵常数a的关系式;(2)在晶胞图上画出任一个四面体和八面体间隙的位置,并指出该四面体间隙和八面体间隙的中心位置。
(3)写出BCC晶胞中四面体间隙和八面体间隙的数量。
答:(1)配位数CN=8,致密度K=,原子数N=2,r=31/2a/4。
(2)图中八面体间隙位于六面体的面中心,四面体间隙位于面平分线1/4处。
(3)四面体间隙和八面体间隙的数量分别为12,6。
(3分)4. 针对FCC和BCC晶胞:(1)分别在晶胞图上画出任一个四面体和八面体间隙的位置。
(2)指出该四面体间隙和八面体间隙的中心位置。
(3)写出每种晶胞中四面体间隙和八面体间隙的数量。
答:①P49 图2-15,图2-16②FCC:图中八面体间隙位于晶胞中心,四面体间隙位于晶胞体对角线上靠结点1/4处BCC:图中八面体间隙位于六面体的面中心,四面体间隙位于面平分线1/4处③FCC:四面体间隙和八面体间隙的数量分别为8,4;BCC:四面体间隙和八面体间隙的数量分别为12,65. 画出下述物质的一个晶胞,并指出5种物质的晶体结构所属的布拉菲点阵类型。
NaCl 金刚石闪锌矿纤锌矿CsCl答:NaCl、CsCl、闪锌矿、纤锌矿:课本P59图2-23(a),(b),(c),(d)金刚石:图2-25NaCl、CsCl、闪锌矿、纤锌矿、金刚石点阵为:面心立方、简单立方、面心立方、简单六方、面心立方点阵6.简述离子晶体的结构规则。
答:鲍林第一、第二、第三规则(书本P57-58)第三章1. 根据链节中主链化学组成的不同,高分子链可以分为碳链高分子、杂链高分子和元素有机高分子。
2.二元共聚物单体的连接方式包括无规共聚、交替共聚、嵌段共聚和接枝共聚。
3.高分子链的结构形态包括线型、支化、梳形、星形、交联和体型。
4.高分子链的构象是由于C-C单键内旋转引起的原子在空间据不同位置所构成的分子链的各种形象。
5. 影响高分子链柔顺性的主要因素有主链结构和侧基性质。
6. 按照高分子几何排列的特点,固体聚合物的聚集态结构分为晶态结构和非晶态结构 两种。
7. 高分子材料的玻璃化温度T g 指的是:当一块玻璃冷却到熔点温度以下时,在某一温度范围内它仍是塑性的.却到某个温度时,发生玻璃硬化,该温度称之为玻璃化温度 。
8. 热固性塑料和热塑性塑料的区别:热塑件塑料由于具有线型结构,因而具有较好的弹性和组件、易于加工成型和可反复使用等特性;热固性塑料不能进行塑性加工和反复使用。
第四章1. 已知某晶体在500℃时,每1010个原子中可以形成有1个空位,请问该晶体的空位形成能是多少(已知该晶体的常数A=,玻尔兹曼常数k=×10-23J/K ) 答:3.位错具有较高的能量,因此它是不稳定的,可能会发生位错反应。
请判断下列位错反应能否进行:]111[2]111[6]112[3a a a →+ 答:几何条件:反应后]111[2]111[6]112[3a a a =+,与反应前一致,满足几何条件能量条件:反应前 43))1(116()2113(2222222222a a ab =-+++++=∑反应后 反应前==++=∑43)1112(222222a ab 此反应不满足能量条件,只满足几何条件,故不能进行。
4. 试比较肖脱基缺陷与弗兰克尔缺陷的异同答:相同:都是点缺陷,都会形成空位。
不同:弗兰克尔缺陷:原子离开平衡位置进入间隙,形成等量的空位和间隙原子。
肖脱基缺陷:由于热运动,晶体中阳离子及阴离子脱离平衡位置,跑到晶体表面或晶界位置上,只形成空位不形成间隙原子。
(构成新的晶面)。
5. 试比较刃位错和螺位错的滑移特征书本P1076. 画图并叙述变形过程中位错增殖的机制。
书本P341 F-R 源7. 试列举金属的四种典型强化机制这四种机制对材料韧性会产生什么影响 答:(1)细晶强化,固溶强化,加工硬化,第二相强化。
(2)细晶强化可以提高韧性;第二相强化有时能提高,有时降低;其他强化不能提高。
第五章1.下图所示为经简化了的铁碳合金相图:(1)请在图中空白区域标出各相区的相(写在圆括号内);(2)写出A、G、S、P、C、E点各自代表的意义;(3)写出GS线、ES线、PSK线代表的含义;(4)分析w c=%(虚线①)的铁—碳合金从液态平衡冷却至室温的结晶过程;分析w c=%(虚线②)的铁—碳合金从液态平衡冷却至室温的结晶过程。
(5)计算45钢(含碳量%)与T10钢(含碳量1%)的相组成物的相对量并根据计算结果说明它们机械性能的差别。
答:(1)(2)课本P178(3)课本P179(4)①w c=%②w c=%(5)45钢的相组成物为F和Fe3C,其相对量为:Q F =()/()ⅹ100% =%Q Fe3C = % = %T10钢的相组成物为F和Fe3C,其相对量为:Q F =()/()ⅹ100% =%Q Fe3C = % = %计算结果表明:由于45钢中的F含量比T10钢高,因此,45钢的塑性、韧性比T10钢高;由于T10钢中的Fe3C含量比45钢高,因此,T10钢的硬度比45钢高。
第六章1.画图并指出典型铸锭(如钢水在砂模中)的组织,并指出其形成原因要获得成分、性能、均匀的铸锭往往要扩大什么区答:铸锭的典型组织特点为表层为细晶区,中心为等轴晶区,这两个晶区之间为柱状晶区。
形成的原因为,表面散热最快,过冷度最大,所以晶粒细小;心部各个方向上热量散失速度基本相同,故为等轴晶粒;在这两个晶区之间,热量沿垂直于铸模壁的方向散失最快,所以晶粒为柱状晶粒(晶粒在热量散失最快的方向上长得最快)。
扩大心部等轴晶区。
2.根据凝固理论,试讨论在凝固过程中细化晶粒的基本途径有哪些答:根据凝固理论可知,在凝固过程中决定晶粒度的因素有形核率(N)和长大速度(G),且N/G越大,晶粒愈细小。
因此我们可以从以下几点着手:(1)增加过冷度:ΔT↑→N/G↑→晶粒愈细小,可以采用降低铸造温度的方法增加过冷度。
(2)提高冷却速度:冷却速度↑→ΔT↑→N/G↑→晶粒愈细小。
可以采用用金属型铸造代替砂型的方法提高冷却速度。
(3)变质处理:变质处理是在液态金属结晶前,加入一些细小高熔点的物质,促使非自发形核的方法。
如钢中加入Ti、V、Al,这种方法易实现、效果明显、最常用。
(4)振动,搅拌方法:破碎作用→提高形核率。
2.假设某纯金属液体按均匀形核方式结晶,晶胚呈半径为r的圆球形。
晶胚的单位面积表面能为σ,液固两相单位体积的吉布斯自由能差为ΔG V。
试问:①该形核过程的驱动力和阻力分别是什么②临界形核半径r*的表达式③临界形核功ΔG V*的表达式答:(1)驱动力:体积自由能差;阻力:新增表面能(2)△G=驱动力(体积自由能差)+ 阻力(新增表面能)=-△Gv +△G S=-V*△Gv +σ*A=-(4/3)πr3△Gv + 4πr2σ两端对r求导,有△G‘=-4πr2△Gv+8πrσ令△G‘=0有r*=-2σ/△Gv(3)带入r*,有ΔG k*=16πσ3/[3(△Gv)2]第七章1. 简述固态相变的一般特点。
答:(1)相变阻力大。
相变阻力多出了应变能一项且扩散困难。
(2)新相晶核与母相之间存在一定的晶体学位向关系。
沿应变能最小的方向和界面能最低的界面发展。
(3)惯习现象:新相沿特定的晶向在母相特定晶面上形成。
(4)母相晶体缺陷促进相变。
缺陷处晶格畸变、自由能高,促进形核及相变。
(5)易出现过渡相。
因为固态相变阻力大,直接转变困难→协调性中间产物(过渡相)。
2.常用的热处理工艺有哪些试列举出四种常用热处理工艺在机械制造中的目的或作用。
答:常见的热处理工艺有正火,退火,固溶,时效,淬火,回火,退火,渗碳,渗氮,调质,球化,钎焊等。
①正火:将钢材或钢件加热到临界点AC3或A CM以上的适当温度保持一定时间后在空气中冷却,得到珠光体类组织的热处理工艺。
②退火:将亚共析钢工件加热至AC3以上20―40度,保温一段时间后,随炉缓慢冷却(或埋在砂中或石灰中冷却)至500度以下在空气中冷却的热处理工艺。
