有机化学上册复习要点
高中化学高考复习有机化学必记知识点(共48条)

高中化学有机化学必记知识点1、常温常压下为气态的有机物:1~4个碳原子的烃,一氯甲烷、新戊烷、甲醛。
2、在水中的溶解度:碳原子较少的醛、醇、羧酸(如甘油、乙醇、乙醛、乙酸)易溶于水;液态烃(如苯、汽油)、卤代烃(溴苯)、硝基化合物(硝基苯)、醚、酯(乙酸乙酯)都难溶于水;苯酚在常温微溶与水,但高于65℃任意比互溶。
3、有机物的密度:所有烃、酯、一氯烷烃的密度都小于水;一溴烷烃、多卤代烃、硝基化合物的密度都大于水。
4、能使溴水反应褪色的有机物有:烯烃、炔烃、苯酚、醛、含不饱和碳碳键(碳碳双键、碳碳叁键)的有机物。
能使溴水萃取褪色的有:苯、苯的同系物(甲苯)、CCl4、氯仿、液态烷烃等。
5、能使酸性高锰酸钾溶液褪色的有机物:烯烃、炔烃、苯的同系物、醇类、醛类、含不饱和碳碳键的有机物、酚类(苯酚)。
6、碳原子个数相同时互为同分异构体的不同类物质:烯烃和环烷烃、炔烃和二烯烃、饱和一元醇和醚、饱和一元醛和酮、饱和一元羧酸和酯、芳香醇和酚、硝基化合物和氨基酸。
7、无同分异构体的有机物是:烷烃:CH4、C2H6、C3H8;烯烃:C2H4;炔烃:C2H2;氯代烃:CH3Cl、CH2Cl2、CHCl3、CCl4、C2H5Cl;醇:CH4O;醛:CH2O、C2H4O;酸:CH2O2。
8、属于取代反应范畴的有:卤代、硝化、磺化、酯化、水解、分子间脱水(如:乙醇分子间脱水)等。
9、能与氢气发生加成反应的物质:烯烃、炔烃、苯及其同系物、醛、酮、不饱和羧酸(CH2=CHCOOH)及其酯(CH3CH=CHCOOCH3)、油酸甘油酯等。
10、能发生水解的物质:金属碳化物(CaC2)、卤代烃(CH3CH2Br)、醇钠(CH3CH2ONa)、酚钠(C6H5ONa)、羧酸盐(CH3COONa)、酯类(CH3COOCH2CH3)、二糖(C12H22O11)(蔗糖、麦芽糖、纤维二糖、乳糖)、多糖(淀粉、纤维素)((C6H10O5)n)、蛋白质(酶)、油脂(硬脂酸甘油酯、油酸甘油酯)等。
有机化学复习重点

sp 2有机化学复习重点第一章 绪 论1.共价键理论现代共价键理论基本要点①当两个原子互相接近到一定距离时, 自旋方向相反的单电子相互配对, 使电子云密集于两核之间, 降低了两核间正电荷的排斥力, 增加了两核对电子云密集区域的吸引力,因此, 使体系能量降低, 形成稳定的共价键。
② 每个原子所形成共价键的数目取决于该原子中的单电子数目, 即一个原子含有几个单电子, 就能与几个自旋方向相反的单电子形成共价键, 这就是共价键的饱和性。
③ 当形成共价键时, 原子轨道重叠程度越大, 核间电子云越密集, 形成的共价键就越稳定。
因此, 共价键总是尽可能地沿着原子轨道最大重叠方向形成, 这就是共价键的方向性。
2.杂化轨道理论杂化轨道理论 (orbital hybridization theory):原子在形成分子时,由于原子间的相互影响,同一个原子内的不同类型、能量相近的原子轨道可以重新组合成能量、形状和空间方向与原来轨道完全不同的新的原子轨道。
这种重新组合过程称为杂化,所形成的新的原子轨道称为杂化轨道(hybridization orbitals )。
3.sp 3, sp 2, sp 杂化对应碳原子空间构型4.共价键的属性第二章 烷 烃1.系统命名法①对于支链烷烃,把它看作是直链烷烃的烷基取代衍生物。
spsp 3键长 :成键原子的核间距离 键角:两共价键之间的夹角键能:离解能或平均离解能键的极性: 成键原子间的电荷分布决定分子 空间构型→ 化学键强度 → 影响理化性质支链烷烃的命名法的步骤:选取主链(母体)。
选一个含碳原子数最多的碳链作为主链。
(写出相当于这个主链的直链烷烃的名称)含多取代基时,编号采用“最低次序”原则。
所谓“最低序列”指的是碳链以不同方向编号,得到两种或两种以上的不同编号序列,则顺次比较各系列的不同位次,最先遇到的位次最小者为“最低系列”。
②主链碳原子的位次编号:确定主链位次的原则是要使取代基的位次最小。
有机化学知识点复习归纳(同系物、同分异构体)

一、同系物: 结构相似,在分子组成上相差一个或若干个CH2 原子团的有机物。
同系物的判断要点: 1、通式相同,但通式相同不一定是同系物。 2、组成元素种类必须相同 3、结构相似指具有相似的原子连接方式,相同的官能团类别和
数目。结构相似不一定完全相同,如CH3CH2CH3和(CH3)4C, 前者无支链,后者有支链仍为同系物。 4、在分子组成上必须相差一个或几个CH2原子团,但通式相同组 成上相差一个或几个CH2原子团不一定是同系物,如 CH3CH2Br和CH3CH2CH2Cl都是卤代烃,且组成相差一个CH2 原子团,但不是同系物。 5、同分异构体之间不是同系物。
谢谢!
应的化学方程式:
练习5
化合物
有一种链状的同分异构体,
能发生银镜反应,核磁共振氢谱有2个峰,该
同分异构体的结构简式为:
同分异构体小结
各类有机物异构体情况: ⑴CCHn3H(C2nH+22:)3C只H能3、是C烷H烃3C,H而(C且H3只)C有H2碳C链H3异、构C(。CH如3)4
⑵ CnH2n:单烯烃、环烷烃。如CH2=CHCH2CH3、
团异构。 如:1—丁炔与1,3—丁二烯、丙烯与环丙烷、乙醇
与甲醚、丙醛与丙酮、乙酸与甲酸甲酯、葡萄糖与 果糖、蔗糖与麦芽糖等。画出结构简式。
练习2
写出C5H12O2能使NaHCO3溶液反应的同分 异 构体;
思路:碳链异构→官能团位置异构。
写出C5H12O2能与NaOH溶液反应的同分异 构体;
思路:官能团异构→碳链异构→官能团位置异构。
CH3CH=CHCH3、CH2=C(CH3)2、
、
⑶ CnH2n-2:炔烃、二烯烃。如:CH≡CCH2CH3、 CH3C≡CCH3、CH2=CHCH=CH2
大一有机化学复习

H2N-
CHO 对-醛基苯胺;对-氨基苯甲醛
HO-CH2CH2-NH2 2-氨基乙醇;2-羟基乙胺
三、有机物主要化学性质
熟悉各类有机物的主要化学性质,相互变化关系, 掌握各类化合物的鉴别方法.
四、用化学方法鉴别化合物 鉴别就是利用有机化合物化学性质之间的差异来
26、油脂的碘值大小说明; 油脂的碘值大说明油脂的C=C键多;碘值小说明油脂 的C=C键多少。
27、产生旋光性的原因: 分子有手性;或分子不对称性
28、旋光异构体数目:
分子有n个手性C原子,旋光异构体数目≤ 2n
29、消除反应
按扎依切夫规则进行,生成取代基多的烯。
例如: CH3CHOH-CH2CH3 -H2O
CH2=CH-OH
CH2=CH-C·H2
P~π共轭
22、共轭体系特点(共轭效应) 有大π键;体系稳定;外电场作用下交替极化;
23、蛋白质沉淀原理 破坏了蛋白质微粒的电荷及水化膜
24、蛋白质变性原理 破坏了蛋白质的空间结构(2~4级结构)
25、油脂的皂化值大小说明:
油脂的皂化值大说明油脂的平均分子量小;油脂 的皂化值小说明油脂的平均分子量大。
X RCOOH > RCOOH >Y RCOOH
有吸电子基
有斥电子基
例:F-CH2COOH > CH3COOH > CH3-CH2COOH;
CH3OH >CH3CH2OH >( CH3)2CHOH> (CH3)3OH ;
伯醇
仲醇
叔醇
=
6、碱性大小 NH
R4NOH 、 H2N-C-NH2(胍) > >( R2NH , RNH2 , R3N )> NH3 > Ar-NH2 > RCO-NH2(酰胺)
高中有机化学基础知识点归纳(全)

高中《有机化学基础》知识点一、重要的物理性质1.有机物的溶解性(1)难溶于水的有:各类烃、卤代烃、硝基化合物、酯、绝大多数高聚物、高级的(指分子中碳原子数目较多的,下同)醇、醛、羧酸等。
(2)易溶于水的有:低级的[一般指N(C)≤4]醇、(醚)、醛、(酮)、羧酸及盐、氨基酸及盐、单糖、二糖。
(它们都能与水形成氢键)。
二、重要的反应1.能使溴水(Br2/H2O)褪色的物质(1)有机物①通过加成反应使之褪色:含有、—C≡C—的不饱和化合物②通过取代反应使之褪色:酚类注意:苯酚溶液遇浓溴水时,除褪色现象之外还产生白色沉淀。
③通过氧化反应使之褪色:含有—CHO(醛基)的有机物(有水参加反应)注意:纯净的只含有—CHO(醛基)的有机物不能使溴的四氯化碳溶液褪色④通过萃取使之褪色:液态烷烃、环烷烃、苯及其同系物、饱和卤代烃、饱和酯(2)无机物①通过与碱发生歧化反应3Br2 + 6OH- == 5Br- + BrO3- + 3H2O或Br2 + 2OH- == Br- + BrO- + H2O②与还原性物质发生氧化还原反应,如H2S、S2-、SO2、SO32-、I-、Fe2+2.能使酸性高锰酸钾溶液KMnO4/H+褪色的物质1)有机物:含有、—C≡C—、—OH(较慢)、—CHO的物质苯环相连的侧链碳上有氢原子的苯的同系物(但苯不反应)2)无机物:与还原性物质发生氧化还原反应,如H2S、S2-、SO2、SO32-、Br-、I-、Fe2+3.与Na反应的有机物:含有—OH、—COOH的有机物与NaOH反应的有机物:常温下,易与—COOH的有机物反应加热时,能与卤代烃、酯反应(取代反应)与Na2CO3反应的有机物:含有—COOH的有机物反应生成羧酸钠,并放出CO2气体;与NaHCO3反应的有机物:含有—COOH的有机物反应生成羧酸钠并放出等物质的量的CO2气体。
4.既能与强酸,又能与强碱反应的物质(1)氨基酸,如甘氨酸等H2NCH2COOH + HCl → HOOCCH2NH3ClH2NCH2COOH + NaOH → H2NCH2COONa + H2O(2)蛋白质分子中的肽链的链端或支链上仍有呈酸性的—COOH和呈碱性的—NH2,故蛋白质仍能与碱和酸反应。
大学《有机化学》期末考试题与总结
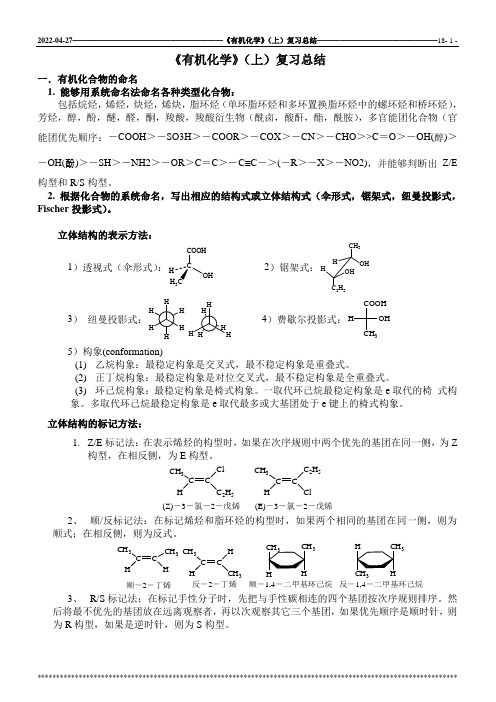
《有机化学》(上)复习总结一.有机化合物的命名1. 能够用系统命名法命名各种类型化合物:包括烷烃,烯烃,炔烃,烯炔,脂环烃(单环脂环烃和多环置换脂环烃中的螺环烃和桥环烃),芳烃,醇,酚,醚,醛,酮,羧酸,羧酸衍生物(酰卤,酸酐,酯,酰胺),多官能团化合物(官能团优先顺序:-COOH >-SO3H >-COOR >-COX >-CN >-CHO >>C =O >-OH(醇)>-OH(酚)>-SH >-NH2>-OR >C =C >-C≡C ->(-R >-X >-NO2),并能够判断出Z/E 构型和R/S 构型。
2. 根据化合物的系统命名,写出相应的结构式或立体结构式(伞形式,锯架式,纽曼投影式,Fischer 投影式)。
立体结构的表示方法:1)透视式(伞形式):CCOOHOH3 2)锯架式:CH 3OHHHOH C 2H 53)纽曼投影式:4)费歇尔投影式:COOHCH 3OH H5)构象(conformation)(1) 乙烷构象:最稳定构象是交叉式,最不稳定构象是重叠式。
(2) 正丁烷构象:最稳定构象是对位交叉式,最不稳定构象是全重叠式。
(3) 环己烷构象:最稳定构象是椅式构象。
一取代环己烷最稳定构象是e 取代的椅 式构象。
多取代环己烷最稳定构象是e 取代最多或大基团处于e 键上的椅式构象。
立体结构的标记方法:1. Z/E 标记法:在表示烯烃的构型时,如果在次序规则中两个优先的基团在同一侧,为Z 构型,在相反侧,为E 构型。
CH 3CC HC 2H 5CH 3CC H2H 5Cl(Z)-3-氯-2-戊烯(E)-3-氯-2-戊烯2、 顺/反标记法:在标记烯烃和脂环烃的构型时,如果两个相同的基团在同一侧,则为顺式;在相反侧,则为反式。
CH 3C CHCH 3HCH 3CH HCH 3顺-2-丁烯反-2-丁烯333顺-1,4-二甲基环己烷反-1,4-二甲基环己烷3、 R/S 标记法:在标记手性分子时,先把与手性碳相连的四个基团按次序规则排序。
有机化学知识要点

有机化学知识复习一.有机化合物的命名1.普通命名法:正、异、新的定义2.系统命名法:主链的选择:最长的、取代基最多的连续碳链。
编号:使官能团的位次尽可能小,取代基的位次总和尽可能小。
写名称:取代基按优先顺序从小到大写在前面,取代基的位次有阿拉伯数字标明,阿拉伯数字与汉字之间用短划分开,相同的取代基用汉字二、三、四标出。
命名优先顺序:SO3H > -COOH > -CHO > C=O > -OH > -NH2>C=C >R,C6H5,Cl,Br,NO2脂环化合物的命名:螺环和桥环化合物的命名。
芳香烃的命名:o- 、m-、p-;α、β、γ杂环化合物的命名:主要母体化合物的音译名称,嘧啶、嘌呤等衍生物的名称。
3.俗名:二.有机化合物的的结构1.有机化合物共价键的形成碳原子的杂化轨道:SP3、SP2、SP杂化。
轨道的成键能力:SP3>SP2>SP>P>S价键法,原子轨道的重叠,σ-键和π-键的形成。
σ-键π-键头碰头重叠肩并肩重叠重叠程度大,稳定重叠程度小,活泼键合原子间可以自由旋转键合原子间不能自由旋转有不同的构象有不同的构型2.有机化合物结构表示法结构式、透视式、费雪尔投影式和纽曼投影式3.同分异构现象构造异构:碳架异构,位置异构,官能团异构,互变异构构型异构:顺反异构:产生的条件,构型表示法,顺、反,Z、E命名规则。
旋光异构:产生的条件构型表示法,相对构型,D、L表示法,绝对构型和R、S表示法。
构象:交叉式,重叠式,优势构象;环己烷的构象,椅式、船式,a-键、e-键。
4.分子间的作用力:范德华力和氢键5.分子中的电子效应:诱导效应:产生的原因:分子中有极性键的存在诱导效应的特点:可从下列卤代酸的酸性看出:HCH2COOH ICH2COOH BrCH2COOH ClCH2COOH FCH2COOHpk a 4.75 3.12 2.87 2.86 2.66 HCH2COOH ClCH2COOH Cl2CHCOOH Cl3CCOOH pk a 4.75 2.86 1.26 0.64CH3CH2CH2COOH CH2CH2CH2COOH CH3CHCH2COOH CH3CH2CHCOOHCl Cl Cl pk a 4.82 4.52 4.06 2.84共轭效应:存在于共轭体系中,有π-π共轭、p-π共轭、和σ-π超共轭。
有机化学上册复习资料

有机化学上册复习资料有机化学在高中化学中是一个非常重要的分支,它讲的是碳原子和氢原子以及其他元素的化合物,这些化合物在我们的生活中无处不在。
学好有机化学需要理论方法和实践技能相结合,而复习有机化学也需要认真总结课堂知识,结合教材和题目进行深入思考,下面是一些有机化学上册复习资料的总结。
一、基础概念有机化学包括很多基础概念,比如有机化合物的命名法,它是理解和学习有机化学的基础。
常用的有机物分为醇、醛、酮、酸和酯等,名字的后缀规律和定位数的统一是进行命名的重要基础。
在命名的基础上,还需要理解分子式、电离、分子式与结构式的转化,构建化学式和化学结构式的技巧等等。
二、官能团有机化合物中的官能团包括碳氢键、氨基和羟基等,它们分别对应着不同的芳香性、酸性、碱度等属性。
这些官能团的性质在形成有机化合物的过程中都扮演着重要的角色,对于分子的反应机理和性质都有不可替代的影响。
学习官能团时需要注意它们的形成和性质,以及在有机化合物中的分别地位。
三、主要反应有机化学中的反应相对来说比较复杂,但很多反应都是相通的,学起来也是很有规律的。
例如氧化还原反应、加成及消脱反应、酸碱反应和取代反应等。
对于这些反应类型的学习,重点需要关注化学式、机理、特点等方面。
掌握这些反应类型的本质是解决有机反应机理和数学问题的关键,可以在复习过程中进行分类总结,形成概念体系。
四、实验技能理论知识和实验技能是相辅相成、相互促进的。
在有机化学学习中,实验重要性很大。
从实验中能学习到有机化合物的制备、特点和反应等方面的知识,更有助于深入理解有机化学的各个方面。
在进行实验时需要正确掌握物料的测量和混合,注意保护学生的安全,同时注意实验后归还物品和清理工作。
五、拓展应用有机化合物是在现实生活中普遍存在的,有着多种多样的拓展应用。
通过学习有机化学,可以深入了解到它的应用领域,例如生物化学、石油化学、食品化学等等。
此外,有机化学还可以应用于环保、新材料等众多领域,为我国的现代化建设做出巨大的贡献。
有机化学要点知识归纳

有机化学知识点归纳(一)一、同分异构体化合物具有相同的分子式,但具有不同结构的现象叫做同分异构现象。
具有同分异构现象的化合物互称同分异构体。
1、同分异构体的种类:⑴ 碳链异构:指碳原子之间连接成不同的链状或环状结构而造成的异构。
如C 5H 12有三种同分异构体,即正戊烷、异戊烷和新戊烷。
⑵ 位置异构:指官能团或取代基在在碳链上的位置不同而造成的异构。
如1—丁烯与2—丁烯、1—丙醇与2—丙醇、邻二甲苯与间二甲苯及对二甲苯。
⑶ 异类异构:指官能团不同而造成的异构,也叫官能团异构。
如1—丁炔与1,3—丁二烯、丙烯与环丙烷、乙醇与甲醚、丙醛与丙酮、乙酸与甲酸甲酯、葡萄糖与果糖、蔗糖与麦芽糖等。
⑷ 其他异构方式:如顺反异构、对映异构(也叫做镜像异构或手性异构)等,在中学阶段的信息题中屡有涉及。
各类有机物异构体情况:⑴ C n H 2n +2:只能是烷烃,而且只有碳链异构。
如CH 3(CH 2)3CH 3、CH 3CH(CH 3)CH 2CH 3、C(CH 3)4 ⑵ C n H 2n :单烯烃、环烷烃。
如CH 2=CHCH 2CH 3、CH 3CH=CHCH 3、CH 2=C(CH 3)2、 、 ⑶ C n H 2n -2:炔烃、二烯烃。
如:CH ≡CCH 2CH 3、CH 3C ≡CCH 3、CH 2=CHCH=CH 2⑷ C n H 2n -6:芳香烃(苯及其同系物)、 ⑸ C n H 2n +2O :饱和脂肪醇、醚。
如:CH 3CH 2CH 2OH 、CH 3CH(OH)CH 3、CH 3OCH 2CH 3⑹ C n H 2n O :醛、酮、环醚、环醇、烯基醇。
如:CH 3CH 2CHO 、CH 3COCH 3、CH 2=CHCH 2OH 、、 、 ⑺ C n H 2n O 2:羧酸、酯、羟醛、羟基酮。
如:CH 3CH 2COOH 、CH 3COOCH 3、HCOOCH 2CH 3、HOCH 2CH 2CHO 、CH 3CH(OH)CHO 、CH 3COCH 2OH⑻ C n H 2n +1NO 2:硝基烷、氨基酸。
有机化学知识点归纳全

有机化学知识点归纳全有机化学是研究有机化合物的结构、性质、合成和反应的学科,是化学的重要分支之一、下面将有机化学的知识点进行详细的归纳。
1.有机化合物的结构:有机化合物的结构主要包括官能团和骨架。
官能团是分子中带有特定化学性质的基团,如羟基、羧基、胺基等。
骨架是指有机分子中碳原子构成的主链或环。
2.结构顺序:有机分子的结构顺序是指官能团和骨架的排列顺序。
它对于有机分子的物理化学性质和反应性质有很大的影响。
3.构象和立体化学:有机化合物的构象是指分子在空间中不同的排列方式。
立体化学研究分子在空间中的空间取向和空间排布。
4.价键理论:有机化学的价键理论主要包括共价键理论、杂化理论和共振理论。
这些理论研究了有机化合物中化学键的形成和性质。
5.有机反应:有机化学反应是指有机分子中原子间氢、电子和其他原子核的重新分配。
有机反应是有机合成的基础,可以用以构建复杂的有机分子。
6.光化学:光化学是研究有机分子在光照下发生的化学反应。
光化学反应可用于合成新的有机化合物和研究生物分子的功能。
7.有机分析:有机分析是研究有机化合物的分析方法和技术。
有机分析可以用于确定有机化合物的结构和性质。
8.有机合成:有机合成是指有机化合物的合成方法和技术。
有机合成可以用于合成天然产物、药物和功能分子。
9.有机催化:有机催化是指利用有机催化剂催化有机反应。
有机催化可以提高反应速度、选择性和产率。
10.药物发现和设计:有机化学在药物发现和设计中起着重要的作用。
有机化合物可用于合成和优化药物分子。
11.酸碱理论:酸碱理论是有机化学的基础。
它用来描述有机化合物在溶液中的酸碱性质和反应。
12.物理有机化学:物理有机化学是研究有机分子中存在的物理现象和现象的研究。
物理有机化学是有机反应和分子结构的基础。
13.手性化学:手性化学是研究手性分子的性质和反应的学科。
手性分子是指它们的镜像不可重叠。
14.有机多步合成:有机多步合成是指通过一系列的有机反应制备复杂有机分子的方法。
有机化学基础知识点总复习

有机化学基础知识点总复习一、协议关键信息1、有机化学的基本概念有机化合物的定义与特点:____________________________官能团的概念与常见官能团:____________________________同系物、同分异构体的定义与判断:____________________________2、烃类化合物烷烃的结构、性质与命名:____________________________烯烃的结构、性质与加成反应:____________________________炔烃的结构、性质与化学性质:____________________________芳香烃的结构、性质与苯的同系物:____________________________3、烃的衍生物卤代烃的性质与卤代烃的取代反应:____________________________醇的结构、性质与醇的氧化反应:____________________________酚的结构、性质与酚的酸性:____________________________醛的结构、性质与醛的氧化还原反应:____________________________羧酸的结构、性质与羧酸的酯化反应:____________________________酯的结构、性质与酯的水解反应:____________________________4、有机化学反应类型取代反应的特点与常见实例:____________________________加成反应的特点与常见实例:____________________________消去反应的条件与常见实例:____________________________氧化反应与还原反应的判断与常见反应:____________________________聚合反应的分类与常见聚合反应:____________________________5、有机化合物的合成合成路线的设计原则:____________________________官能团的引入与转化方法:____________________________有机合成中的保护与去保护策略:____________________________6、有机化合物的结构鉴定红外光谱、核磁共振氢谱的原理与应用:____________________________有机化合物结构推断的方法与思路:____________________________二、协议内容11 有机化学的基本概念111 有机化合物是指含碳的化合物,但一些简单的含碳化合物如一氧化碳、二氧化碳、碳酸盐等通常被归类为无机化合物。
《有机化学》(第四版)复习提纲

有机化学复习提纲《有机化学》(第四版)第一章绪论1、有机化合物的定义。
2、碳原子的SP、SP2、SP3杂化轨道的杂化原理和共价键的构成方式。
3、诱导效应的概念。
4、酸碱的概念。
第二章饱和烃:烷烃和环烷烃1、烷烃的命名。
脂环烃、桥环烃、螺环烃的命名方法。
2、环烷烃的环结构与稳定性的关系。
3、取代环已烷的稳定构象。
4、烷烃的卤代反应历程(自由基型取代反应历程)。
5、烷烃的卤代反应取向与自由基的稳定性。
6、脂环烃的取代反应。
7、脂环烃的环的大小与开环加成活性关系。
8、取代环丙烷的开环加成规律。
9、环烯烃的π键加成与α-氢的卤代反应区别。
第三章不饱和烃:烯烃和炔烃1、碳-碳双键、碳-碳三键的组成。
2、π键的特性。
3、烯烃、炔烃的命名;烯烃的Z,E-命名法,烯炔的命名。
4、烯烃、炔烃的加氢催化原理及其烯烃、炔烃的加氢反应活性比较。
5、炔烃的部份加氢——注意区分顺位部分加氢和反位部分加氢的条件或试剂。
6、何谓亲电加成?(烯烃中被亲电试剂进攻的不饱和碳上电子密度越高,亲电加成活性越大)7、烯烃、炔烃可以与哪些试剂进行亲电加成,这些加成有哪些应用。
8、烯烃亲电加成反应机理。
9、亲电加成反应规律(MalKovniKov规律)。
10、烯烃、炔烃与HBr的过氧化物效应加成及其规律。
(惟一只有溴化氢才能与烯烃、炔烃存在过氧化物效应,其它卤化氢不存在过氧化物效应。
)11、烯烃亲电加成与炔烃亲电加成活性的比较。
12、不同结构的烯烃亲电加成活性的比较——不饱和碳上电子密度越高的烯烃或越容易生成稳定碳正离子的烯烃,亲电加成反应的活性越大。
13、碳正离子的结构和碳正离子的稳定性之间的关系——正电荷越分散,碳正离子就越稳定。
14、烯烃经硼氢化—氧化水解在合成醇上的应用;炔烃经硼氢化—氧化水解在合成醛或酮上的应用。
15、碳-碳双键的α-碳上有支链的烯烃与卤化氢加成时的重排反应。
(P88)16、烯烃与次卤酸加成及加成规律。
炔烃与水加成及重排产物。
有机化学知识点高三上册

有机化学知识点高三上册有机化学是高中化学学科的重要组成部分,旨在研究有机物的结构、性质以及有机反应。
而高三上册的有机化学知识点较为复杂,需要我们认真学习和理解。
以下是高三上册有机化学的主要知识点概述。
一、有机化学基础知识1.有机物的定义与分类:有机物是由碳、氢和其他一些元素(例如氧、氮、硫等)构成的化合物。
根据有机物所含有的碳原子数目不同,可以将其分为烷烃、烯烃、炔烃等不同类别。
2.有机化学键与杂化轨道:有机化学中,碳原子通常形成四个单键。
碳原子通过杂化轨道可以形成四个等价的sp3杂化轨道,用于形成σ键。
sp2和sp杂化轨道常见于烯烃和炔烃等多共轭体系中。
3.键能与键长:分子中碳-碳键能力最小,而碳-氧键和碳-氮键能力逐渐增强。
键长通常与键能成反比,键长越短,键能越大。
二、有机化学反应1.饱和烃的反应:烷烃具有较低的反应性,常见的烷烃反应有燃烧、臭氧化、卤代反应等。
2.烯烃的反应:烯烃的反应性较高,常见的烯烃反应有加成反应、氢化反应、卤代反应等。
3.芳香族化合物的反应:芳香族化合物的共有电子对云较强,不易发生加成反应。
常见的芳香族化合物反应有亲电取代反应、羟基化反应等。
4.醇的反应:醇具有亲电取代性质,醇的酸碱性较弱。
常见的醇的反应有醚化反应、脱水反应、氧化反应等。
三、重要有机化合物1.醛与酮:醛和酮是由碳氧双键连接的有机化合物。
常见的醛与酮有甲醛、乙酰甲酸乙酯等。
醛和酮具有亲电性,能够发生亲电取代反应和加成反应。
2.羧酸与酯:羧酸和酯是有机化合物中含有羧基的化合物,常见的有乙酸、醋酸乙酯等。
羧酸具有酸性,容易与醇发生酯化反应。
3.胺:胺是有机化合物中含有氨基的化合物,常见的有甲胺、乙酰胺等。
胺具有碱性,能够与酸发生盐类反应。
四、官能团与有机化学合成1.官能团的概念:官能团是指有机分子中影响化学性质的原子或原子团。
官能团的存在决定了有机分子的化学性质和反应类型。
2.有机化学合成:有机化学合成是通过一系列有机反应,将简单的有机物合成为复杂的有机分子。
有机化学复习重点

H C = O C 3 C = H OR C = O P C = O h C 3 C = H O
H
H
H
H
C 3 H
C 3 C = H OR C = OC 3 C = H OR C = OP C = h O
R
R
PhPh Ph
苯 甲 酸 酯 化 : A . 正 丙 醇 B . 乙 醇 C 甲 醇 D . . 仲 丁 醇
C=C
CH H OH
(2R,3Z)-3-戊烯-2-醇
5
4. 多官能团化合物的命名
当分子中含有两种或两种以上官能团时,其命名遵循官能团优 先次序、最低系列和次序规则。
官能团次序优先
2
2
二、有机化合物的基本性质
自己总结
6
三、完成反应式
(1) 确定反应类型;
(2) 确定反应部位;
(3) 考虑反应的区域选择性;
A . ( 3 ) 2 C C 2 B B H H . C 3 r C 2 B C H C . C H r 3 C 2 C H 2 B H D H . ( H 3 r ) 3 C C 2 B
BC A D
R相同时,卤代烃的反应活性顺序是: RI RB rRCl
◆ 亲核加成:
亲核加成反应主要包括醛、酮的亲核加成反应和羧酸亲核加成 -消除反应。
Cl 2 ° RX
1 ° RX
乙 烯 型 卤
AB C D
A . C 2 C B H .C l l C 2 C C H .C l 3 O H C 2 C D H .O l 2 N C 2 C
+
C2HCl
δC +2H
C3 O H
δC +2H O 2 N
有机化学复习知识点

有机化学总复习第一章绪论一、有机化合物及其特点1.1 历史简介1828年,魏勒偶然用无机物合成了有机物——尿素(NH4Cl + AgOCN→NH4OCN−→−∆NH2CONH2),魏勒——“有机化学之父”有机化合物有一个共同点,即都含有碳元素——碳的化合物、有机化学——碳化合物的化学1874年,德国化学家肖莱马提出,可以把碳氢化合物(烃)看作有机化合物的母体,把含有其他元素的有机化合物看作是烃的衍生物,因此他把有机化合物定义为“烃及其衍生物”。
也常把有机物称为“碳氢及其衍生物”1.2 有机化合物的特点可燃性;熔点和沸点较低;难溶于水,易溶于有机溶剂;反应速度慢、复杂,常常有副反应1. 分子结构复杂2. 有机物与无机物的性质差别有机物无机物可燃性一般可燃不易燃熔点低(一般<400℃)高溶解性多数难溶于水,易溶于水,不易易溶于有机溶剂溶于有机溶剂反应性速度慢产物复杂速度快,产物固定副反应多1.3 研究领域有机化学:研究有机化合物来源、制备、结构、性能、应用以及有关理论、变化规律和方法学的科学。
三项内容:分离、结构、反应和合成[分离] 从自然界或反应产物通过蒸馏、结晶、吸附、萃取、升华、色谱分离等操作分离出单一纯净的有机物。
(分离提纯的方法之一:柱层析俗称过柱子即梯度洗涤,分液漏斗中从上至下依此放海沙、硅胶、砂芯,然后将样品从上口倒下过滤洗涤)[结构] 对分离出的有机物进行化学和物理行为的了解,阐明其结构和特性。
[反应和合成] 从某一有机化合物(原料)经过一系列反应转化成一已知的或新的有机化合物(产物)。
二、有机化合物的结构概念1:化学结构(构造): 分子中原子相互结合的顺序和方式。
(大致分为:直链状、支链状、环状)概念2:同分异构现象和同分异构体同分异构现象:分子式相同而结构式不同的现象。
同分异构体:分子式相同而结构式不同的化合物。
(比如:乙醇与甲醚)三、共价键电子理论1. 化学键的两种基本类型,就是离子键与共价键,离子键是由原子间电子的转移形成的,共价键则是原子间共用电子形成的。
有机化学知识点总结

有机化学知识点总结1. 有机化学概述1.1 定义:研究含碳化合物的化学性质、结构、合成及其应用的科学。
1.2 特点:碳的四价性、碳链结构、官能团的存在。
2. 有机化合物的分类2.1 烃类:仅含碳氢元素的有机化合物。
2.1.1 饱和烃:碳原子之间全为单键,如烷烃。
2.1.2 不饱和烃:含有双键或三键,如烯烃、炔烃。
2.2 衍生物:由烃类通过取代或加成反应生成的化合物。
2.2.1 醇、酚:含羟基的化合物。
2.2.2 醛、酮:含羰基的化合物。
2.2.3 羧酸、酯:含羧基的化合物。
2.2.4 胺、酰胺:含氨基的化合物。
3. 有机化学反应类型3.1 取代反应:化合物中的一个原子或基团被另一个取代。
3.1.1 核式取代:如卤代反应。
3.1.2 亲核取代:如醇的生成。
3.2 加成反应:不饱和化合物与另一个分子结合形成饱和化合物。
3.2.1 电子对受体与亲电试剂的反应。
3.3 消除反应:化合物中的两个原子或基团脱离形成不饱和化合物。
3.4 重排反应:分子内部原子的重新分布。
3.5 聚合反应:单体分子通过重复的化学反应形成大分子链。
4. 有机分子的结构4.1 碳原子的杂化:sp、sp2、sp3杂化。
4.2 立体化学:手性、对映体、消旋体。
4.3 分子轨道理论:分子的电子结构。
5. 有机化学中的分析技术5.1 光谱分析:红外光谱、核磁共振光谱、紫外-可见光谱。
5.2 色谱分析:气相色谱、液相色谱、薄层色谱。
6. 有机合成策略6.1 逆合成分析:目标分子的合成路径设计。
6.2 保护基策略:对活性官能团的保护与去保护。
6.3 绿色化学:环保、可持续的合成方法。
7. 有机化学的应用7.1 药物合成:药物分子的设计、合成与改良。
7.2 材料科学:高分子材料、生物材料的开发。
7.3 能源化学:生物质能源、太阳能转换。
8. 有机化学的发展趋势8.1 新合成方法的开发。
8.2 新材料的设计与合成。
8.3 生物有机化学的交叉研究。
有机化学复习要点

有机化学复习要点有机化学是研究有机物(含碳的化合物)的合成、结构、性质和反应的科学。
下面是有机化学复习的重点要点:1.有机化合物的分类:根据碳的连接方式,有机化合物可分为链状、环状和支链状化合物。
根据它们的官能团,化合物可以被进一步分类为醇、酮、酯、醛、酸、胺等等。
2.有机化合物的命名:有机化合物的命名是有机化学的基础。
在命名时,需要确定主链、编号碳原子、标记官能团和提供适当的前缀和后缀。
3.有机化合物的构造:有机化合物的构造表示确定其分子的原子结构,包括原子的类型、化学键的类型(单键、双键、三键)和宇称等。
4.共价键的极性:共价键是由两个原子之间共享电子形成的,极性共价键指电子不均匀地共享。
这导致一侧带有部分正电荷,而另一侧带有部分负电荷,形成极性分子。
5.引入官能团:官能团是有机化合物中特定原子或原子组合的集合,确定化合物的性质和反应。
常见官能团有羟基(-OH)、醛基(-CHO)、酮基(-C=O)、羧基(-COOH)、胺基(-NH2)等等。
6.有机反应的基本原理:有机反应是有机化学的核心,包括加成反应、消除反应和取代反应。
加成反应是指在化合物中添加一个原子或基团;消除反应是指分子中的两个基团消除,形成一个双键或三键;取代反应是指一个基团被替换成另一个基团。
7.重要的有机反应:有机化学有许多重要的反应,其中一些包括酯化、醇酸化、加氢、亲电取代、亲核取代、还原和氧化等等。
了解这些反应及其机理对于理解有机化学非常重要。
8.常见的有机化学术语:在有机化学中,有许多常见的术语和概念,例如:轴手性、对映体、立体异构体、环状化合物等等。
了解这些术语可以帮助理解和解决有机化学问题。
9.溶剂的选择:在有机化学实验中,溶剂的选择非常重要。
常见的有机溶剂包括乙醇、丙酮、乙醚、二甲基甲酰胺等等,选择合适的溶剂可以促进反应的进行。
10.立体化学:立体化学涉及分子和化合物的空间构型和对称性。
手性和立体异构体是立体化学的重要概念,影响分子的性质和化学反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
39. 下列化合物最易与 HBr 加成的是
A. B. C. D.
40. 下列化合物与卢卡斯试剂反应最快的是 A、正丁醇 B、2-丁醇 C、2-甲基-2-丁醇 41. 下列化合物哪个最不稳定?
Br H Br H
H Br
D、正丙醇
H Br
A、
H Br
B、
H Br
Br
H Br
C、
H
D、
42. SN2 反应的特征是: (Ⅰ)生成正碳离子中间体;(Ⅱ) 立体化学发生构型翻转;(Ⅲ)反应速率受反应物浓度影响, 与亲核试剂浓度无关; (Ⅳ)在亲核试剂的亲核性强时容易发生。 A.Ⅰ和Ⅱ B. Ⅲ 和Ⅳ C. Ⅰ和Ⅲ D.Ⅱ和Ⅳ 43. 烯烃和溴化氢在过氧化物存在下的加成,生成反马氏规则加成产物,其反应
18. 下列化合物在水中的溶解度最小的是 A. 1-丁醇 B. 1-己醇 C. 乙二醇 D. 丙三醇 19. 下列构象中稳定的反-1-甲基-4-异丙基环己烷是:
CH3 CH3 CH3 CH3
(H3C)2HC
A
CH(CH3)2
B
(H3C)2HC
C
CH(CH3)2
D
20. 下面化合物中无芳香性的是:
+
A. B. C.
历程为: A、自由基历程 B、亲核加成反应 C、亲核取代反应 D、亲电取代反应 44. 乙醇的沸点比二甲醚的高,其原因是: A、乙醇分子间形成氢键 B、乙醇分子内形成氢键 C、二甲醚分子量小 D、二甲醚分子内形成氢键
45. 下列化合物中最易起SN1 反应的是: A、CH3Br B、CH3CH2Br C、(CH3)2CHBr
各位同学大家好! 为了方便同学复习迎接有机化学上册的期末考试, 特准备了以下问题请大家思考, 并独自完 成总结,选择题看书后完成,不必问老师答案是什么。 Part I. 本概念: 1. 有机化学的定义 2. 共价键及其键参数 3. 原子核外电子的排布规律是什么 4. 化学键的类型 5. 强酸性和强碱性的有机化合物结构特征是什么 6. 烷烃及同分异构体 7. 有机化合物 8. 次序规则 9. 立体化学,烷,烯及炔碳中心的杂化方式 10. 构象 11. 手性,手性分子 12. 烷烃,烯烃和炔烃的定义 13. 有机化学反应的基本类型 14. 亲核取代,消除反应 15. 诱导效应的定义和类型 16. Walden 翻转 17. Zaitsev 规则 18. 亲电加成,马氏规则 19. 醇的定义,结构特征 20. 芳香性,芳烃结构特征,休克尔规则,Birch 还原及其特点 Part II. 选择题 1. 下列化合物与KOH的乙醇溶液按SN2 反应进行,其反应速度最快的是:
64. 下列化合物酸性最弱的是 A. CH3SO3H B. CH3COOH C. ClCH2COOH D. CH4
65. 下列 C-H 键其键的解离能最小的是 A. (CH3)2CH-H B. (CH3)3C-H C. CH3CH2CH2CH2-H D. CH3-H )种
66. 二氯丙烷的同分异构体有四种, 从而可推知六氯丙烷的同分异构体有( A. 3 B4 C. 5 D 6
51. 下列化合物构型的确定,哪个不正确?
H CHO OH CH2OH CHO Cl H H CHO Cl CH2OH (S 型) COOH OH CH3
A、
(R 型)
B、
H
C、
CH2OH (S 型)
D、
(R 型)
52. 下列化合物哪些有旋光性:
53. 下列化合物和溴反应最快的是 A 乙烯; B 乙炔 C 环丁烷 D 苯 54. 下列不是共价键键参数的 A 键长; B 键角 C 键能 D 偶极矩 E 色散力 F 范德华力 G 氢键 H 燃烧热 55. 下列化合物名称正确的有: (a) 新己烷,(b) 新辛烷 (c) 辛庚烷 (d) 新丁烷 56 下列化合物不能够与金属钠反应释放氢气的有 a. 丙酮 b. 乙酰乙酸乙酯 c. 2,4-戊二酮 d. 苯酚 57 下列化合物中沸点最高的是
D.
21. 在苯乙烯分子中,存在的共轭效应为:
A. δ-p 超共轭
B. π-π 共轭
C. δ-π 超共轭
D. p-π 共轭
22. 下列取代基中属于第二类定位基的是 A、–CH=CH2 B 、–Ph C 、-Me D、-SO3H 杂化轨道与其它原子结合
23. 在碳正离子,带正电荷的碳原子是以
A、sp B 、sp2 C 、s D、-sp3 24. 环丙烷不如环己烷稳定,是因为环丙烷分子有 的缘故 A、不饱和性 B 、角张力 C 、色散力 D、范德华力 25. (Z)-2-丁烯分子中有 个对称面。 A、1 B 、2 C 、3 D、4 26. 乙醚久置后加热,蒸干后往往容易发生爆炸,这是因为有部分乙醚生成了 的缘故。
Cl NO2 OH
D、(CH3)3CBr
NH2
46. 下列四个取代苯,亲电取代反应发生在邻对位,且取代反应活性比苯小的是
A、
B、
C、
D、
47. 开链化合物也称为: A、脂肪族化合物 B、脂环族化合物 C、饱和脂肪烃 D、不饱和脂肪烃
48. 下列各组化合物中,哪些是对映体?
CHO CHBrCH2CH3 D. CH3CH2CBr2CH3
29. 比较下列化合物与环戊二烯反应的活性大小
a 环戊二烯 b 丙烯酸乙酯 A d>c>b>a C c>b>d>a
c.顺丁烯二酸酐 B a>b>c>d D b>c>d>a C、丙酸乙酯
d.四氰基乙烯
30. 如用酯与格氏试剂的反应制备 3-戊醇,你认为应选择的酯是:
CHO HO H COOH
与
COOH H Br CH3 CH3 H2N C6H5 与 H
与
COOH H Br C6 H5 H3C H NH2 CH3
CH3
A、
B、
COOH HO H CH2OH H2N
CH2OH H
C、
D、
49. 手性分子的正确定义的是: A、不具有任何对称因素的分子 C、与其镜像不能重叠的分子 50. 1-丁烯与 2-丁烯互为: A、位置异构 B、差向异构 B、含有手性碳原子的分子 D、含有手性因素的分子 C、构象异构 D、顺反异构
12. 下列化合物中,属于内消旋体的是:
CH3 H A. Br Br H CH3 H B. H C 3 Br CH3 Br H C. H H 3C OH CH3 Br H D. H HO COOH OH H COOH
13. 由CH3CH2CH2Br 合成 CH3CHBrCH3,应采取的方法是: A.①KOH,醇;②HBr,过氧化物 C. ①HOH,H+;②HBr,过氧化物 B. ①HOH,H+;②HBr D. ①KOH,醇;②HBr
A、乙酸乙酯
B、甲酸乙酯
D、丁酸乙酯
31. 下列化合物形成的聚合物中,称为涤纶的是:
A、丙烯腈 C、对苯二甲酸二甲酯和乙二醇
32.
B、苯酚和甲醛 D、2-甲基丙烯酸甲酯
A
B C D 33. 下述哪一个化合物可以和顺丁烯二酸酐发生双烯加成( ) A 苯 B 吡啶 C 环戊二烯 D 环己酮
34. 下列共价键极性最强的是: A、H-C B. C-O C. C-Br D. O-H
a. 正丙醇 b. 醋酸 c. 丙醛 d. 甲乙醚 58 下列化合物沸点最高的是 a. 正丁烷 b. 1-丁烯 c. 丁醛 d. 1-丁醇 59 下列卤代烃亲核取代反应活性最高的是 a. 氯苯 b. 溴苯 c. 烯丙基溴 d. 1-溴丙烷 60 下列化合物中不能与格氏试剂反应的是 a. 甲苯 b. 甲醇 c. 甲胺 d. 水 61. 下与溴发生反应的有 a. 环丙烷 b. 丙烷 c. 环丁烷 d. 丁烷 62 规则下列基团最优基团为 a. -H b. –CH2Br c. CH2F d. –CH2Cl 63. 某烃与Cl2反应只能生成一种一氯代物,该烃的分子式为 A. C3H8 B C4H10 C. C5H12 D C6H14
67. 下列化合物有偶极矩的是: A. I2 B. CCl4 C. CH3CH3 D. CH3OCH3
68. 下列各物质在碱性条件下最易发生SN2 反应的是
A Br OH B Br OH C Br OH D Br OH
Part III. 基元反应 需要总结如下反应 1) 氧化反应:自我总结—含饱和键和不饱和键类化合物的氧化 2) 还原反应:自我总结饱和键和不饱和键类化合物的还原 3) 亲电加成:自我总结 4) 亲核取代:自我总结 5) 消除:E1 消除和 E2 消除:自我总结 6) 卤代反应:自我总结 7) 自由基反应(取代和加成):自由基反应发生的条件,烷烃和环烷烃的自由基卤化反应, 烯烃的 alpha-H 卤代, 芳烃侧链 alpha-H 卤代, 烯烃和炔烃在过氧化物存在下与卤化氢的加 成, 卡宾的加成反应及特点。 8)开环反应: 有角张力的小环烷烃的开环(有 HX, X2 的加成),环醚的开环等 9) 亲核加成反应。
16. 下列亲核试剂在质子溶剂中与CH3CH2Br反应速度最快的是
A. CH3CH2CH2OB. CH3CH2CH2SC. CH3CH2CH2NHD. CH3CH2CH2CH2-
17. 为了除去苯中混入的少量乙醚,可用下述方法除去: A、用 NaOH 溶液洗 B、用石油醚洗 C、用浓硫酸洗 D、用分子筛吸附
14. 下列叙述中,有利于按SN2 历程反应的有:
A. 增加亲核试剂的浓度,反应速度无明显变化; B. 两步反应,第一步是决定反应速度的一步; C. 进攻试剂的亲核性越强,反应速度越快; D. 产物发生外消旋化。 15. 下列化合物在酸性条件下最容易脱水生成烯烃的是:
CH2CH2OH A. B. CH2CHCH3 OH C. CH2CH2OH D. CH2CHCH3 OH
