2-甲基-2-丁醇合成
叔丁醇钾反应机理

叔丁醇钾反应机理引言叔丁醇(又称2-甲基-2-丁醇)是一种重要的有机化合物,在有机合成和工业生产中广泛应用。
它可以通过苄基钠与乙酸乙酯反应得到,其中反应机理尚不清楚。
本文将探讨叔丁醇钾反应的机理,并详细介绍其反应的步骤和可能的中间产物。
叔丁醇钾反应的步骤叔丁醇钾反应的步骤可以分为四个阶段,具体如下:1.生成叔丁基盐首先,乙酸钾(CH3COOK)与叔丁醇(C4H10O)在甲醇(CH3OH)溶剂中反应生成叔丁基盐(C4H9K)和乙酸(CH3COOH)。
反应的化学方程式如下所示:CH3COOK + C4H10O -> C4H9K + CH3COOH2.脱醇反应在第二个步骤中,生成的叔丁基盐会继续与甲醇反应,发生脱醇反应。
这个反应会生成叔丁烯(C4H8)和甲醇钾(CH3OK)。
反应的化学方程式如下所示:C4H9K + CH3OH -> C4H8 + CH3OK3.分解反应第三个步骤是分解反应,叔丁烯会继续分解为丁烯(C4H6)和丙烯(C3H4)。
此反应需要高温和加热条件。
反应的化学方程式如下所示:C4H8 -> C4H6 + C3H44.热解反应在最后一个步骤中,丙烯会发生热解反应,产生苯乙烯(C8H8)。
这个反应需要高温和加热条件。
反应的化学方程式如下所示:C3H4 -> C8H8叔丁醇钾反应的中间产物在叔丁醇钾反应过程中,存在着一些可能的中间产物。
下面列出了可能的中间产物和相应的反应步骤:1.叔丁烯 (C4H8):在脱醇反应后生成的中间产物,它可以通过分解反应进一步转化为丁烯和丙烯。
2.丁烯 (C4H6):由叔丁烯分解得到的中间产物,它可以进一步热解为苯乙烯。
3.丙烯 (C3H4):由叔丁烯分解得到的中间产物,它经过热解反应生成苯乙烯。
叔丁醇钾反应的应用叔丁醇钾反应具有重要的应用价值,主要体现在以下几个方面:1.有机合成:叔丁醇钾反应是合成有机化合物的重要步骤。
通过控制反应条件和中间产物的选择,可以合成出多种有机化合物,如丁烯和苯乙烯等。
2-甲基-2-丁醇的制备

北京石油化工学院综合性有机化学实验报告题目名称:2-甲基-2-丁醇的制备学生姓名:XXX专业:化学工程与工艺学院:化学工程学院年级:20XX级指导教师:XXX20XX 年 12 月 1 日2-甲基-2-丁醇的制备XXX(北京石油化工学院化学工程学院,北京102600)摘要:2-甲基-2-丁醇是常用的有机溶剂与有机原料,可用于生产药物、香料、增塑剂、浮选剂等。
本实验首先利用溴乙烷与镁合成Grignard试剂[1],再用Grignard试剂与丙酮反应,经酸化得到2-甲基-2-丁醇,最后用Lucas试剂检验产物。
本实验是常量实验,实验共使用1.8g(0.073mol)镁、10mL(4.4g,0.13mol)溴乙烷、5mL(3.95g,0.068mol)丙酮,得到产物2.7g,产率45%,产率适中,适合实验室少量制备醇类化合物使用。
关键词:2-甲基-2丁醇;制备;Grignard试剂1 前言2-甲基-2-丁醇,俗称“叔戊醇”,结构式如右图。
常温下为无色液体,沸点102℃,相对密度20d为0.805,折4射率20n为1.4052,有类似樟脑气味。
微溶于水,与乙醇、D乙醚、苯、氯仿、甘油互溶。
易燃,易发生消除反应。
实验室中常用Grignard试剂合成。
工业上由丙酮与乙炔加成得乙炔基异丙醇后镍催化加氢制得,也可用2-甲基-2-丁烯在硫酸中水化制取。
用作溶剂和有机原料,生产药物、香料、增塑剂、浮选剂等。
2 实验部分[2]2.1实验仪器及药品仪器:电子天平PL601-S,梅特勒-托利多仪器(上海)有限公司;调温电热套DZH10,北京市光明医疗仪器厂;250mL圆底三口烧瓶,扬州市信谊玻璃仪器有限公司;100mL单口烧瓶,扬州市信谊玻璃仪器有限公司;恒压滴液漏斗,扬州市信谊玻璃仪器有限公司;球形冷凝管,扬州市信谊玻璃仪器有限公司;干燥管,扬州市信谊玻璃仪器有限公司;分液漏斗,扬州市信谊玻璃仪器有限公司;锥形瓶,扬州市信谊玻璃仪器有限公司;蒸馏头,扬州市信谊玻璃仪器有限公司;温度计(150℃),扬州市信谊玻璃仪器有限公司;直形冷凝管,扬州市信谊玻璃仪器有限公司;接受弯头,扬州市信谊玻璃仪器有限公司。
2-甲基-2-丁醇

2-甲基-2-丁醇(1)化学品及企业标识化学品中文名:2-甲基-2-丁醇,二甲基乙基甲醇,第三戊醇,二甲基乙基原醇化学品英文名:tert-Amylalcohol,tert-Pentylalcohol,Dimethylethylcarbinol,Ethyldimethylcarbinol,tert-Pentanol,Amylenhydrate分子式:C5H12O相对分子量:88.17(2)成分/组成信息成分:纯品CAS No:75-85-4(3)危险性概述危险性类别:第3.3类高闪点液体侵入途径:健康危害:中等毒性,刺激眼、鼻和呼吸器官。
吸入其蒸气可引起眩晕、头痛、咳嗽、恶心、耳鸣、谵语,严重者可致高铁血红蛋白病和糖尿病等。
大鼠经口LD50为1000mg/kg。
生产设备应密闭,防止泄漏。
操作人员应穿戴防护用具。
环境危害:燃爆危险:与空气混合可爆(4)急救措施皮肤接触:食入:吸入、食入或皮肤接触该物质可引起迟发反应,确保医务人员了解该物质相关的个体防护知识,注意自身防护(5)消防措施危险特性:遇明火、高温、氧化剂较易燃; 燃烧产生刺激烟雾有害燃烧产物:灭火方法:干粉、干砂、二氧化碳、泡沫、1211灭火剂灭火注意事项及措施:(6)泄漏应急处理应急行动:(7)操作处置与储存操作注意事项:储存注意事项:库房通风低温干燥; 与氧化剂分开存放(8)接触控制/个体防护监测方法:工程控制:呼吸系统防护:眼睛防护:身体防护:手防护:其他防护:(9)理化特性外观与性状:无色易燃液体PH值:无资料熔点(℃):-12 °C沸点(℃):102 °C(lit.)相对密度(水=1): 0.805 g/mL at 25 °C(lit.)相对蒸气密度(空气=1):3 (vs air)饱和蒸气压(kPa):燃烧热(kJ/mol):临界温度(℃):临界压力(MPa):辛醇/水分配系数:闪点(℃):20 °C引燃温度(℃):爆炸下限(%): 爆炸上限(%):溶解性:溶于水,可混溶于乙醇、丙酮、苯、氯仿、油类主要用途:用作合成香料、农药的原料,也是优良的溶剂;主要用于生产新型农药粉锈宁、频那酮、三唑酮、三唑醇、种子保护剂等;并可用于合成茚烷麝香,以及作彩色胶片的成色剂。
2-甲基-2-丁醇的制备

实验12-7 2-甲基-2-丁醇的制备
1.本实验为什么使用的药品仪器均需绝对干燥?为此应采取什么措施? Grignard 反应必须在无水和无氧条件下进行,所用仪器和试剂均需干燥,因为微量水分的存在不但阻碍卤代烃和镁之间的反应,而且会破坏形成的Grignard 试剂而影响产率。
本实验所用的合成反应的试剂在实验前必须进行无水处理,溴乙烷用无水氯化钙干燥,蒸馏纯化;丙酮用无水碳酸钾干燥,蒸馏纯化;无水乙醚若为市售,需用压钠机向瓶内压入钠丝,瓶口用带有无水氯化钙干燥管的橡皮塞塞紧,放置24 h (放在远离火源的阴凉黑暗处保存),直至无氢气泡放出。
2.如反应未开始前,加入大量溴乙烷有什么不好?
反应未开始前,加入大量溴乙烷会发生卤代烃的偶联反应,增加副产物。
3.乙醚在本实验各步骤中的作用是什么?使用乙醚应注意哪些安全问题? 进行反应时乙醚作溶剂,后处理是乙醚作萃取剂。
4.为什么碘能促使反应发生?卤代烷与格氏试剂反应的活性顺序如何? 加入一小粒碘起催化作用,反应开始后,碘的颜色立即褪去。
碘催化过程可用下列方程式表示:
Mg + I 2
MgI 2Mg 2Mg I ··Mg I ·+ RX
R + MgXI MgXI + Mg
·Mg X ·Mg I +R ··Mg X +RMgX
5.本实验有哪些可能的副反应,如何避免?
用活泼的卤代烃制备Grignard 试剂时,偶合反应是主要的副反应,可以采取搅拌、控制卤代烃的滴加速度和降低溶液浓度等措施减少副反应的发生。
6.为什么本实验得到的粗产物不用无水氯化钙干燥。
醇与氯化钙干燥可以反应生成醇合物。
2-甲基-2-丁醇结构式

2-甲基-2-丁醇结构式
甲基-2-丁醇,又称丁醇甲醚,是一种有机化合物,化学
式为CH3CH2CH2OH。
它属于烷醇类化合物,是一种有机烷
醇类化合物,具有一个烷基和一个醇基。
甲基-2-丁醇是烷醇
类化合物中最简单的化合物,是一种一元烷醇,也是一种甲醇醚。
甲基-2-丁醇是一种液体,具有无色至淡黄色的特性,有
一种特殊的果香气味。
它沸点为107.9℃,比重为0.805,溶于水,溶解度比乙醇低。
它的熔点为-117.2℃,易挥发,沸点低
而折射率高。
甲基-2-丁醇的制备方法有许多,最常用的方法是用丁醇
与甲苯反应,在高温下反应,将丁醇转化为甲基-2-丁醇。
该
反应也可以用乙醇和甲苯反应,但是需要使用催化剂。
甲基-2-丁醇主要用于制备染料、润滑油、催化剂、溶剂、香料、药物、柠檬酸等产品。
它还被广泛用于精细化学品、有机合成和医药行业。
甲基-2-丁醇不仅具有优良的物理性能和化学性能,而且
它的毒性较低,安全性较高,所以被广泛应用于各种工业场合。
它还具有优良的物理性能和化学性能,可以用于溶剂、润滑剂和消毒剂等。
由于其特殊的物理性能和化学性能,它也被用于制备其他有机化合物。
甲基-2-丁醇是一种重要的有机化合物,它不仅广泛应用于工业,而且在生物学和医学上也有很多应用,如在药物合成和药物研究中。
它是一种重要的化学原料,它的研究也为有机化学的发展做出了重要贡献。
有机化学课后习题及答案(第六章)

有机化学课后习题及答案(第六章)6章思考题6.1 试解释实验中所遇到的下列问题:(1)(1)⾦属钠可⽤于除去苯中所含的痕量H2O,但不宜⽤于除去⼄醇中所含的⽔。
(2)(2)为什么制备Grignard试剂时⽤作溶剂的⼄醚不但需要除去⽔分,并且也必须除净⼄醇(⼄醇是制取⼄醚的原料,常参杂于产物⼄醚中)。
(3)(3)在使⽤LiAlH4的反应中,为什么不能⽤⼄醇或甲醇作溶剂?6.2 叔丁基醚[(CH3)3C]2O既不能⽤Williamson法也不能⽤H2SO4脱⽔法制得,为什么?6.3 苯酚与甲苯相⽐有以下两点不同的物理性质:(a)苯酚沸点⽐甲苯⾼;(b)苯酚在⽔中的溶解度较甲苯⼤。
你能解释其原因吗?6.4 解释下列现象(1)(1)从2-戊醇所制得的2-溴戊烷中总含有3-溴戊烷。
(2)(2)⽤HBr处理新戊醇(CH3)2C-CH2OH时只得到(CH3)2CBrCH2CH3。
解答6.1 答(1)⼄醇的活泼氢能与Na发⽣反应,苯与Na⽆反应。
(2)RMgX不仅是⼀种强的亲核试剂,同时⼜是⼀种强碱,可与醇羟基中的H结合,即RMgX可被具活性氢的物质所分解,如(3)LiAlH4既是⼀种强还原剂,⼜是⼀种强碱,它所提供H-与醇发⽣反应,如6.2叔丁基醚⽤H2SO4脱⽔法合成时,主要产⽣烯烃。
6.3 答甲苯和苯酚的相对分⼦质量相近,但是甲苯的沸点110.6℃,⽽苯酚的沸点181.8℃,这是由于苯酚可以形成分⼦间氢键;甲苯不溶于⽔,⽽苯酚易溶于⽔,是由于苯酚与⽔分⼦之间会形成氢键:6.4习题6.1⽐较下列各组化合物与卢卡斯试剂反应的相对速度:(1) 正戊醇, 2-甲基-2-戊醇, ⼆⼄基甲醇(2) 苄醇, 对甲基苄醇, 对硝基苄醇(3)(3)苄醇, α-苯基⼄醇, β-苯基⼄醇6.26.2区别下列各组化合物:(1) CH2=CHCH2OH, CH3CH2CH2OH , CH3CH2CH2Br, (CH3)2CHI(2) CH3CH(OH)CH3, CH3CH2CH2OH , C6H5OH , (CH3)3COH , C6H5OCH3(3) α-苯基⼄醇, β-苯基⼄醇, 对⼄基苯酚, 对甲氧基甲苯6.36.3写出下列各反应主要产物:6.4合成题:(1)(1)甲醇, 2-丁醇→ 2-甲基丁醇(2)(2)正丙醇, 异丙醇→ 2-甲基-2-戊醇(3)(3)甲醇, ⼄醇→正丙醇, 异丙醇(4)(4)2-甲基丙醇, 异丙醇→ 2,4-⼆甲基-2-戊烯(5)(5)丙烯→⽢油→三硝酸⽢油酯(6)(6)苯, ⼄烯, 丙烯→ 3-甲基-1-苯基-2-丁烯(7)(7)⼄醇→ 2-丁醇(8)(8)叔丁醇→ 3, 3-⼆甲基-1-丁醇(9)(9)⼄烯→三⼄醇胺(10)(10)丙烯→异丙醚(11)(11)苯, 甲醇→ 2,4-⼆硝基苯甲醚(12)(12)⼄烯→正丁醚(13)(13)苯→间苯三酚(14)(14)苯→对亚硝基苯酚(15)(15)苯→ 2,6-⼆氯苯酚(16)(16)苯→对苯醌⼆肟6.5某醇C5H12O氧化后⽣成酮,脱⽔则⽣成⼀种不饱和烃, 将此烃氧化可⽣成酮和羧酸两种产物的混合物, 试推测该醇的结构.6.6有⼀化合物(A)的分⼦式为C5H11Br, 和NaOH⽔溶液共热后⽣成C5H12O(B). B具有旋光性.能和钠作⽤放出氢⽓, 和浓硫酸共热⽣成C5H10(C). C经臭氧化和在还原剂存在下⽔解, 则⽣成丙酮和⼄醛. 试推测A, B, C的结构, 并写出各步反应式.6.7新戊醇在浓硫酸存在下加热可⽣成不饱和烃. 将这不饱和烃经臭氧化后, 在锌粉存在下⽔解, 可得到⼀种醛和⼀种酮. 试写出反应历程及各步反应产物的构造式.6.8分离下列各组化合物:(1)(1)⼄醚中混有少量⼄醇(2)(2)戊烷, 1-戊炔和1-甲氧基-3-戊醇6.9 下列各醚和过量的浓氢碘酸反应, 可⽣成何种产物?(1)(1)甲丁醚(2)(2)2-甲氧基⼰烷(3)(3)2-甲基-1-甲氧基戊烷6.10有⼀化合物的分⼦式为C6H14O, 常温下不与⾦属钠反应, 和过量的浓氢碘酸共热时⽣成碘烷, 此碘烷与氢氧化银作⽤则⽣成丙醇. 试推测此化合物的结构, 并写出反应式.6.11 有⼀化合物的分⼦式为C7H16O, 并且:(1)(1)在常温下它不和⾦属钠反应;(2)(2)它和过量浓氢碘酸共热时⽣成C2H5I和C5H11I . 后者与氢氧化银反应⽣成的化合物的沸点为138℃.试推测原化合物的结构, 并写出各步反应式.6.12有⼀化合物的分⼦式为C20H21O4N, 与热的浓氢碘酸反应可⽣成碘甲烷. 当此化合物4.24 mg与氢碘酸反应, 所⽣成的碘甲烷通⼈硝酸银的醇溶液, 得到11.62mg碘化银. 问此化合物含有⼏个甲氧基?6.13 写出环氧⼄烷与下列试剂反应的⽅程式:(1)(1)有少量硫酸存在下的甲醇(2)(2)有少量甲醇钠存在下的甲醇6.14 推测下列反应的机理。
2-甲基-2-丁醇化学式

2-甲基-2-丁醇化学式2-甲基-2-丁醇,也被称为4-甲基-2-戊醇,是一种有机化合物。
其化学式为C6H14O,可以简写为Me2BuOH。
在化学结构中,2-甲基-2-丁醇包含一个甲基基团和一个丁醇基团。
该化合物具有许多独特的性质和应用。
本文将介绍2-甲基-2-丁醇的结构、性质和应用。
结构2-甲基-2-丁醇的分子式为C6H14O。
它的分子量是102.18克/摩尔。
该化合物的结构中包含一个甲基基团(CH3)和一个丁醇基团(C3H7OH)。
甲基基团位于丁醇分子的第二个碳原子上,因此被称为2-甲基-2-丁醇。
它是一种有机化合物,由碳、氢和氧元素组成。
性质2-甲基-2-丁醇是一种无色液体,具有特殊的气味。
它的沸点为117-120摄氏度,密度为0.81克/毫升。
2-甲基-2-丁醇具有较低的溶解度,在水中的溶解度仅为0.05克/毫升。
然而,它可以溶解在许多有机溶剂中,如乙醇、丙酮和乙醚。
它不易挥发,在室温下相对稳定。
应用2-甲基-2-丁醇在工业和实验室中具有许多应用。
以下是其中几个常见的应用:1. 溶剂:由于其良好的溶解性,2-甲基-2-丁醇常用作溶剂。
它可以溶解许多有机物,如树脂、油漆、染料等。
在工业生产和实验室实验中,它可以作为反应物或产物的溶剂。
2. 化学反应中的中间体:2-甲基-2-丁醇可以在许多化学反应中用作中间体。
例如,在有机合成中,它可以被用作酯化反应的底物。
通过与酸催化剂反应,可以得到2-甲基-2-丁醇的酯类衍生物,这些酯类化合物在医药和香料工业中具有重要的应用。
3. 助溶剂:2-甲基-2-丁醇具有良好的溶解性和挥发性,常被用作某些涂料和清洗剂中的助溶剂。
它可以帮助其他成分更好地溶解并提供可调节的挥发性。
4. 医药领域:2-甲基-2-丁醇在医药领域也有一些应用。
它常用于合成药物和化合物的研究和生产过程中。
此外,它还可以被用作一些药物的添加剂,以增强其溶解度和稳定性。
总结2-甲基-2-丁醇是一种有机化合物,其化学式为C6H14O。
有机化学题库(二)
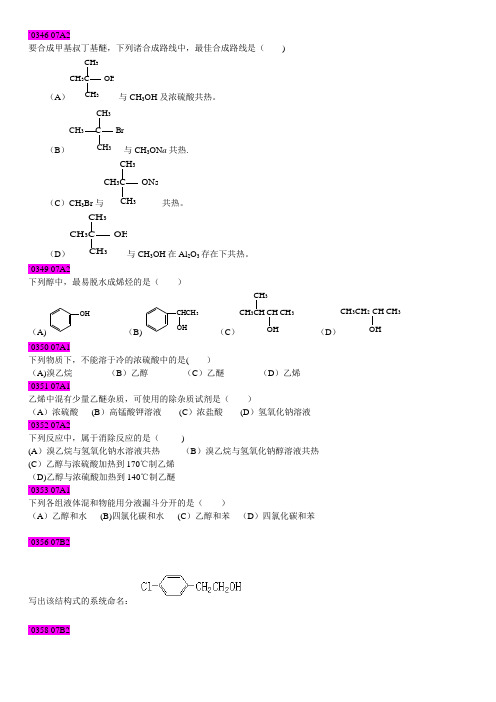
`0346 07A2要合成甲基叔丁基醚,下列诸合成路线中,最佳合成路线是( )(A )CH 3C OHCH 3CH 3与CH 3OH 及浓硫酸共热。
(B )CH 3 C BrCH 3CH 3与CH 3ON a 共热.(C )CH 3Br 与CH 3CH 3CH 3C ONa共热。
(D )CH 3C OHCH 3CH 3与CH 3OH 在Al 2O 3存在下共热。
`0349 07A2下列醇中,最易脱水成烯烃的是( )(A)OH(B)CHCH 3OH(C )CH 3CH CH CH 3CH 3OH(D )CH 3CH 2 CH CH 3OH`0350 07A1下列物质下,不能溶于冷的浓硫酸中的是( )(A)溴乙烷 (B )乙醇 (C )乙醚 (D )乙烯 `0351 07A1乙烯中混有少量乙醚杂质,可使用的除杂质试剂是( )(A )浓硫酸 (B )高锰酸钾溶液 (C )浓盐酸 (D )氢氧化钠溶液 `0352 07A2下列反应中,属于消除反应的是( )(A )溴乙烷与氢氧化钠水溶液共热 (B )溴乙烷与氢氧化钠醇溶液共热 (C )乙醇与浓硫酸加热到170℃制乙烯 (D)乙醇与浓硫酸加热到140℃制乙醚 `0353 07A1下列各组液体混和物能用分液漏斗分开的是( )(A )乙醇和水 (B)四氯化碳和水 (C )乙醇和苯 (D )四氯化碳和苯`0356 07B2写出该结构式的系统命名:`0358 07B2写出该结构式的系统命名:`0360 07B2写出该化合物的构造式:对硝基苄基苯甲醚`0362 07B2写出该化合物的构造式:2,3-二甲氧基丁烷`0364 07C1用简便且有明显现象的方法鉴别下列各组化合物CH2OH OHCH3`0365 07C2用简便且有明显现象的方法鉴别下列各组化合物CH3CH2OCH2CH3 , CH3CH2CH2CH2OH , CH3(CH2)4CH3 `0366 07C1`0370 07C1完成下列各反应:`0371 07C1用简单的化学方法区别以下各组化合物正丁醇,甲丙醚,环已烷.`0372 07C2用简单的化学方法区别以下各组化合物乙苯,苯乙醚,苯酚,1-苯基乙醇。
实验六 2甲基-2-己醇的合成

实验五 2-甲基-2-己醇的合成一、实验目的1.通过格氏反应制备产物。
2.熟悉格氏试剂的制备、应用和进行格氏反应的条件。
3.掌握无水反应装置、机械搅拌装置和滴液漏斗的使用。
4.正确安装无水反应、并且带有滴液漏斗和回流冷凝管的机械搅拌装置。
二、实验原理醇的制法很多,简单和常用的醇在工业上利用水煤气合成、淀粉发酵、烯烃水合及易得的卤代烃的水解等反应来制备。
实验室醇的制备,除了羰基还原(醛、酮、羧酸和羧酸酯)和烯烃的硼氢化—氧化等方法外,利用Grignard 反应是合成各种结构复杂的醇的主要方法。
卤代烷和溴代芳烃与金属镁在无水乙醚中反应生成烃基卤化镁,又称Grignard 试剂。
芳香和乙烯型氯化物,则需用四氢呋喃(沸点66℃)为溶剂,才能发生反应。
RX + Mg无水乙醚RMgXCrignard 试剂为烃基卤化镁与二烃基镁和卤化镁的平衡混合物:2Mg + MgX 2乙醚在Crignard 试剂的制备中有重要作用,醚分子中氧上的非键电子可以和试剂中带部分正电荷的镁作用,生成络合物:EtEt Et EtR-Mg-X乙醚的溶剂作用是使有机镁化合物更稳定,并能溶解于乙醚。
此外,乙醚价格低廉,沸点低,反应结束后容易除去。
卤代烷生成Grignard 试剂的活性次序为:RI >RBr >RC1。
实验室通常使用活性居中的溴化物,氯化物反应较难开始,碘化物价格较贵,且容易在金属表面发生偶合,产生副产物烃〔R —R )。
Grignard 试剂中,碳—金属键是极化的,带部分负电荷的碳具有显著的亲核性质,在增长碳链的方法中有重要用途,其最重要的性质是与醛、酮、羧酸衍生物、环氧化合物、二氧化碳及腈等发生反应,生成相应的醇、羧酸和酮等化合物。
RMgXR-C-OMgXRH+C=O R-C-OHR' C OCH 3O RMgX R' C OMgXR2H+R R' C OHR22H 2CCH 2RMgXRCH 2CH 2OMgXH +RCH 2CH 2OHH 2ORCO 2RMgXOR C OMgXH +O R C OHR' C NR' C NMgXH+R' C RO2H 2O反应所产生的卤化镁络合物,通常由冷的无机酸水解,就可使有机化合物游离出来。
2_甲基丁醇的合成与应用研究进展

3288 8 杜卫红等. 分子催化, 1996, 11 (2) : 73~ 76 9 J P 1993 214, 159 10 J P 1992 230 239 11 J P 1995 138 596 12 EP 368 592
2 丁烯来源广泛, 价格低, 故此方法生产所 需费用较低。 1. 2. 2 以 2 甲基 1 丁烯为原料[5]
用异戊烯 (2 甲基 1 丁烯) 为原料, 在有机
收稿日期: 1999 10 31; 修改稿收到日期: 2000 09 14。 作者简介: 崔文峰 36 岁, 硕士, 主要从事炼油化工生产和
HO
CH 3CH 2
CH 3
C CH 2 + CH 3 C CH 3
H 3C
OH
CH 3
1. 4 以醛为原料[7 ]
以 2 甲基丁醛为原料, 用 2 丙醇为溶剂, 在
Zr2O 3·XH 2O 催化剂催化下还原为醇。
CHO H 2
催化剂
OH
其收率达 80%。
2 2 甲基丁醇的应用
2 甲基丁醇由于它具的旋光性, 用它生产出
日本专利[11]报道了 2 甲基丁醇作为一种水 漂洗剂的应用; 欧洲专利[12] 报道了用 2 甲基丁 醇合成噻唑衍生物作为一种除草剂。
另外 2 甲基丁醇可作为合成酯类的原料, 用 作合成食用香料的组分。 3 开发建议
a. 2 甲基丁醇是一种高附加值的精细化工 产品, 由于具有旋光活性具有特殊用途, 具有明显 的开发价值。
叔丁醇结构式

叔丁醇结构式叔丁醇,也称为2-甲基-2-丁醇或异丁醇,是一种有机化合物,化学式为C4H10O。
它是一种无色液体,在常温常压下具有特殊的气味。
叔丁醇是最简单的醇之一,它的结构式是CH3CH(CH3)CH2OH。
在化学工业中,叔丁醇被广泛应用于溶剂、化学合成的中间体和表面活性剂等领域。
叔丁醇具有类似酒精的性质,可以与酸反应生成酯,与醛反应生成亚胺,与卤素反应生成叔碳富烷等。
它的空间结构使得叔丁醇在化学反应中表现出较高的活性和选择性。
叔丁醇可以发生酯化、酯交换、羰基化反应等。
例如,通过与醋酸反应,可以得到叔丁醋酸叔丁酯(又称叔丁酯)。
叔丁醇还可以被氧化为叔丁醛,在氧化反应中起催化剂的作用。
叔丁醇在化学工业中的主要应用之一是作为溶剂。
由于其低毒、低挥发性和较高的溶解力,叔丁醇被广泛用于油漆、油墨、清洁剂和香精等化学产品中。
叔丁醇还可以用作化学合成的中间体,参与酯化、羰基化、饱和烷基化等反应。
在药物合成中,叔丁醇常被用作合成抗生素、激素和维生素等化合物的重要原料。
除了在化学工业中的应用,叔丁醇还具有一定的生物学效应。
据研究发现,叔丁醇可以作为一种有效的保护剂,减轻肝脏和心肌缺血再灌注损伤,具有保护心血管系统的作用。
此外,叔丁醇还可以用作氨基酸的保护剂,在蛋白质合成和生物工程领域具有重要意义。
叔丁醇的制备方法有多种,常用的方法是通过异丁烯的氢化制备。
在实验室中,可以通过丁醛的还原或者乙酸的重酸化来制备叔丁醇。
此外,还可以通过烷烃的脱水饱和反应得到叔丁醇。
作为一种常见的有机化合物,叔丁醇在日常生活中也有一定的存在。
例如,在香水中,叔丁醇可以作为调香剂的一种成分,给香水带来独特的气味。
此外,在个人护理产品中,叔丁醇也常被用作防腐剂和杀菌剂,保护产品的稳定性和安全性。
综上所述,叔丁醇是一种重要的有机化合物,具有广泛的应用领域。
在化学工业中,叔丁醇作为溶剂、化学合成的中间体和表面活性剂等发挥着重要作用。
叔丁醇还具有一定的生物学效应,在保护心血管系统和生物工程领域具有应用潜力。
2-甲基-2-丁醇的合成

2-甲基-2-丁醇的合成摘要:本文研究了以溴乙烷与镁为原料,无水乙醚作溶剂,在无水无氧条件下反应,生成Grignard试剂。
利用Grignard和丙酮加成反应生成醇盐,经水解来制备2-甲基-2-丁醇的过程,探讨了反应原理。
反应中,要求反应体系干燥无水,采用在冷凝管上装氯化钙干燥管。
Grignard反应中,贮存过久的金属镁条容易氧化,形成一层氧化薄膜,反应前需去掉表层。
2-甲基-2-丁醇的能与水形成共沸物,因此粗产物必须很好的干燥,否则前馏分将大大的增加,降低产率。
试验表明,本法与其他方法相比,具有流程短,收率高,产品质量稳定的持点。
关键词: 2-甲基-2-丁醇、Grignard反应、合成、乙基溴化镁、叔戊醇2-甲基-2-丁醇又名叔戊醇,它作为一种基本有机化工原料有着相当广泛的用途,广泛应用于频呐酮、彩色胶片成色剂、佳乐麝香和粉檀麝香、叔戊基过氧化物、N一苯基氨基甲酸叔戊醇、酰氟基对氧萘酮的制备等行业,同时还可用于回收石油的溶液添加剂与氯化物清洗剂的稳定剂[1]。
七十年代中叶,日本研究以2-甲基-2-丁醇为原料合成中间体频那酮获得成功,使一批高附加值的延伸产品问世,将2-甲基-2-丁醇的深度加工推向一个新的高度。
2-甲基-2-丁醇的合成是有机合成实验中比较经典的传统实验。
2-甲基-2-丁醇合成方法有多种,包括以乙炔和丙酮为原料,固体氢氧化钾为催化剂,在液氨介质中,采用釜式反应器合成甲基丁炔醇,还对甲基丁炔醇选用釜式反应器进行液相加氢合成2-甲基-2-丁醇;异戊烯法采用直接水合法和硫酸水台法两种流程,原料是2-甲基-1-丁烯和2-甲基-2-丁烯。
但硫酸水合法,对设备腐蚀严重,废酸较难处理是其缺点,有被直接水合法取代的趋势。
直接水台法是用酸性阳离子交换树脂催化剂、在超临界条件下进行的水合反应。
反应温度和压力等操作条件与生产仲丁醇的方法相似[2];此外还有乙烯和丙烯共聚法、丙烯和异丁烯歧化法、异戊二烯选择性加氧法、3-甲基-1一丁烯异构化法等众多合成方法[3]。
有机化学综合练习四(合成)

有机化学综合练习五化合物的转化或合成(用反应式表示)1. 用乙烯和乙炔为原料合成1-丁炔。
2. 由乙炔转化为3-己炔。
3.由溴乙烷和异丙醇制备2-甲基-2-丁醇。
4.从甲苯转化为苄醇。
5.以硝基苯为原料,制备间二碘苯。
6.从苯转化为正丙苯。
7.从丙烯转化为丙酮。
8.以丙烯和丙醛为原料,制备2-甲基-3—戊醇9.从甲苯转化为1-苯基2-丙醇。
10.由转化为。
11.由1-溴丙烷转化为2-溴丙烷12. 由2-甲基-3-戊醇转化为2-溴-2-甲基戊烷。
13.由异丙醇转化为正丙醇。
14.由乙醛转化为2-丁烯醛。
15.由苯酚转化为苯甲醚。
解题提示或答案1.乙烯转化为卤代烷,乙炔转化为乙炔钠,再由卤代烷与乙炔钠反应。
H 2C=CH 2 + HBr CH 3CH 2BrHC CH HC CNa HC C-CH 2CH 32.乙炔转化为乙炔二钠,再与卤代乙烷反应。
3.异丙醇氧化成丙酮,溴乙烷转化为格氏试剂与丙酮加成后酸性水解。
4.甲苯在光照条件下 氯代后再水解。
5.硝基苯与发烟硝酸、硫酸在加热条件下制得间二硝基苯,用铁屑和盐酸在加热条件下还原成间二苯胺,将氨基转化为重氮盐后被碘取代。
6.苯与丙酰氯进行付氏酰基化反应,然后将羰基还原成亚甲基。
7.丙烯水合得到2-丙醇,再氧化为丙酮。
2 NaNH 2 CH 3CH 2Br CH 3 Cl 2 ,光照 CH 2Cl H 2O/OH - CH 2OH H 2SO 4 H 2O OSO 3H OOHK 2Cr 2O 7 H 2SO 4 CH 3CHCH 3 CH 3CHCH 3 CH 3CH=CH 2 CH 3C-CH 38.丙烯加氯化氢再制成格氏试剂与丙醛加成后酸性水解。
9.甲苯在光照条件下 氯代后制成格氏试剂与乙醛加成后酸性水解。
10、邻氯硝基苯用铁屑和盐酸在加热条件下还原成邻氯苯胺,将氨基转化为重氮盐后再被氯取代。
11.1-溴丙烷在氢氧化钾的乙醇溶液中加热发生消除生成丙烯,再与溴化氢加成。
2022-2023学年江西省南昌市第二中学高二下学期5月月考化学试题

2022-2023学年江西省南昌市第二中学高二下学期5月月考化学试题1.我国科技自立自强,近年来取得了重大进展。
下列有关科技成果的说法不正确的是A.“异域深海,宝藏无穷”——自主开采的可燃冰燃烧时,向环境释放热量B.“科技冬奥,温暖护航”——C 60与发热服饰材料中的石墨烯互为同位素C.“高产水稻,喜获丰收”——水稻中含有的淀粉和纤维素都是有机高分子D.“浩渺太空,无限征途”——月壤中磷酸盐矿物的晶体结构可用X射线衍射仪测定2.下列化学用语表达正确的是A.乙醛的结构简式:CH 3 COH B.碳化硅的分子式:SiCC.乙醇的分子式:C 2 H 5 OH D.羟基的电子式:3.利用超分子可分离C60和C70,将C60、C70混合物加入一种空腔大小适配C60的“杯酚”中进行分离的流程如图。
下列说法正确的是A.一个C 60分子中含有120个键B.“杯酚”与C 60形成氢键C.此分离过程只需杯酚就能完成C 60和C 70的分离D.该分离过程利用的是超分子的分子识别特征4.甘油酸是一种食品添加剂,可由甘油氧化制得。
下列说法不正确的是A.甘油与足量金属钠反应生成 (标准状况下)B.甘油酸中含有键的数目约为C.可用溶液区分甘油和甘油酸D.甘油和甘油酸均易溶于水5.有关单质碘升华过程的描述中,错误的是A.该过程吸热B.分子间距增大C.分子间作用力增大D.不会破坏共价键6.下列说法正确的是A.C 6 H 6分子结构中一定存在不饱和键B.有机物CH 3 CH=CH 2的分子在核磁共振氢谱中存在5组峰C.C 6 H 12表示的物质中可能存在顺反异构体,也可能存在手性碳原子D.戊二烯与环戊烷互为同分异构体7.类比推理是化学中常用的思维方法,下列推理正确的是A.CH 3 CH 2 OH在水中的溶解度很大,则1-戊醇在水中的溶解度也很大B.CCl 4的熔沸点小于SiCl 4,则NCl 3的熔沸点小于PCl 3C.N≡N由于键能大而结构稳定,则C≡C键能也大结构也很稳定D.AgNO 3溶液和过量NaOH反应先生成白色沉淀,然后转变为灰色,则AgNO 3溶液和过量NH 3 ·H 2 O反应现象也相同8.下列实验现象与实验结论都正确的是9.某种新型储氢材料的晶胞如图,八面体中心为金属离子铁,顶点均为配体;四面体中心为硼原子,顶点均为氢原子。
Grignard反应制备2-甲基-2-丁醇

Grignard反应制备2-甲基-2-丁醇一、 实验项目简介本实验在无水乙醚中将溴乙烷与金属镁反应,制备格氏试剂--乙基溴化镁。
将格氏试剂与丙酮反应,得到亲核加成产物,然后将其用稀硫酸分解,得到目标分子2-甲基-2-丁醇。
(详见教案)二、 实验项目的综合性本实验是在学生掌握有机实验的基本单元操作的基础上设立的一个综合性较大的项目,要求学生能够把各方面的知识综合联系起来,使其在实验技能与技巧方面能够得到更好的训练,以提高他们的实践能力与创新能力。
1) 实验操作的综合性a) 实验的前期处理内容较多:需要学生将仪器洗涤洁净并充分干燥;将所有反应物进行无水处理;镁条需打磨或酸洗以去除表面氧化物。
b) 因为各个单元反应均较为剧烈,要让学生掌握缓慢滴加反应物的技巧,培养学生认真观察反应现象的能力与耐心。
c) 反应中使用低沸点的溶剂和反应物,要求学生进一步熟悉回流操作,掌握缓和均匀回流的技巧。
d) 粗产物采用乙醚萃取,因其极低的沸点,要求学生进一步正确熟练掌握萃取的操作要点。
e) 目标分子与水形成恒沸物,要求学生掌握干燥剂“适量”的标准以及干燥的基本操作。
f) 进一步熟悉蒸馏操作。
g) 了解无水操作处理的基本要素,了解常见溶剂的无水处理的方法。
2)实验目的的综合性a) Grignard试剂是有机化学基本理论学习中的重点,本项目要求学生在实验之前回顾Grignard试剂的有关知识。
通过本次实验既要让学生实实在在的了解其制备过程的复杂性,又要让学生真实感受到其在有机合成中应用的广泛性。
b) 羰基是一类非常活泼的基团,自然界有大量的含羰基的化合物。
本项目也要求回顾各种羰基参与的反应以及羰基的制备方法。
通过本次实验要求学生进一步掌握亲核加成反应的机理及其应用。
三、 实验操作要点1) 安装好回流滴加装置。
2) 将15mL无水乙醚和20mL干燥的溴乙烷放入滴液漏斗中,然后缓慢滴加到盛有3.5克镁屑和20mL无水乙醚的干燥的250mL三口烧瓶中,保持反应物正常平稳的回流与沸腾。
2-甲基-2-丁醇的制备

实验七 2-甲基-2-丁醇的制备一、实验目的:通过2-甲基-2-丁醇的制备学习并掌握使用格利雅试剂和醛酮反应制备醇。
熟悉并基本掌握憎水和低沸点试剂的实验。
学会格利雅试剂的制备,格利雅试剂与醛酮的反应,如何进行憎水性实验。
二、试剂:1、无水乙醚25mL2、镁 1.8g(0.73mol)3、无水丙酮5mL(3.95g,0.68mol)4、溴乙烷10mL(14.4g,0.13mol)5、乙醚30mL6、碘少许7、10%硫酸8、10%碳酸钠水溶液15mL9、无水碳酸钾三、反应原理:产物数据:2-甲基-2-丁醇 2-methyl-2-butanolMF: C5H12O MW: 88.15 vapor pressure: 12mmHg(20℃) bp: 102℃ n20/D:1.405,mp:-12℃, d: 0.805g/ml(25℃)四、实验仪器及实验装置图:250mL圆底三口烧瓶、100mL圆底单口烧瓶球、球形冷凝管、干燥管、分液漏斗、锥形瓶、蒸馏头、温度计、直形冷凝管、接受弯头、调压器、加热套。
反应装置图蒸馏装置图五、操作步骤:在装有平衡加料漏斗和球形冷凝管(上端装干燥管)的250mL三口烧瓶(另一个口用塞子塞上)中加入10mL无水乙醚、1.8g镁、少许碘。
滴液漏斗中加入10mL无水乙醚和10mL溴乙烷,轻轻摇动平衡加料漏斗,使其混合均匀。
自滴液漏斗中先放出~三分之一溴乙烷乙醚溶液,立即用手加热烧瓶使反应开始,反应变缓后再滴加溴乙烷乙醚溶液,保持反应比较激烈的进行。
当反应变慢后轻轻摇动反应装置,使反应加速,再变慢时加入溴乙烷乙醚溶液,控制加入速度,即要反应比较激烈进行,又不要使反应过于激烈而造成反应过快,乙醚来不及冷凝而逸出。
全部加完后开始小心加热回流直至金属镁基本消失为止。
取下加热套,用冰水冷却烧瓶至室温。
关闭平衡加料漏斗,向其中加入5mL 丙酮和5mL无水乙醚,轻轻摇动反应装置,使丙酮与无水乙醚混合均匀。
2甲基2丁醇的反应原理

2甲基2丁醇的反应原理
2甲基2丁醇的反应原理是指2甲基2丁醇在一定条件下与其他化合物发生化学反应的原理。
以下是2甲基2丁醇的几种常见反应原理:
1. 氧化反应:2甲基2丁醇可以被氧化剂如氧气、过氧化氢等氧化为2-丁酮或2-丁醛。
反应条件下,氧化剂与2甲基2丁醇接触并提供足够的能量,使2甲基2丁醇中的碳氢键被氧化剂氧化断裂,生成相应的氧化产物。
2. 脱水反应:2甲基2丁醇在脱水条件下,如高温、浓硫酸等催化剂的存在下,丢失一个水分子,生成2-丁烯。
3. 酯化反应:2甲基2丁醇与酸反应时,酸中的羧基与2甲基2丁醇中的羟基反应,生成相应的酯。
此反应常用于有机合成中的酯类产物的制备。
4. 烷基化反应:2甲基2丁醇与碱金属如钾反应,钾金属催化下,醇中的羟基被去质子化,生成烷基金属中间体,再与其他化合物反应,生成相应的烷基化产物。
5. 脱氢反应:2甲基2丁醇在高温条件下,可发生脱氢反应,生成丁烯和乙醛。
这些反应原理可以根据具体的条件和反应物进行调节,以制备所需的化合物或开展有机合成反应。
2-甲基-2-丁醇的制备

四、实验步骤
1、Grignard试剂的制备 在三口瓶中加入1.8g镁粉、12.5mL无水乙醚及1小粒 碘;在恒压滴液漏斗中加入7mL溴乙烷、6mL无水乙醚。 加沸石,安装搅拌、回流装置,从恒压滴液漏斗中 向四口瓶中加入20滴(约1mL)溴乙烷、乙醚混合液。 待反应缓和后,开动搅拌器,从恒压滴液漏斗向四 口瓶中加入剩余的溴乙烷、乙醚混合液,控制滴速加热, 温度控制在50-60℃,继续搅拌,回流0.5h。停止搅拌, 冷却至室温。
4、产品的精制
将粗产物转移到圆底烧瓶中,加入沸石, 安装好常压蒸馏装置,先用温水浴蒸去乙醚, 再用电热套加热蒸馏,收集95~105℃的馏分。
计算产品的产量与产率。
五、注意事项
1、根据分配定律,用相同量的溶剂,分几次萃取要比 一次萃取效率高。因此,一般情况下,分2~4次萃取, 就可以把绝大部分被萃取物萃取出来。 2、在实验中,往往因为强烈摇振分液漏斗而发生乳化 现象。为了破坏乳化现象,通常可以采取以下措施: 一是盐析;二是遇碱性溶液乳化时可以加入少量稀硫 酸或乙醇;三是增加有机层的相对密度;四是将乳液 静置较长时间。
液-液萃取有机溶剂的选择: 1、与原溶剂不相溶;
2、与原溶剂密度差相对较大;
3、被萃取的有机物在该有机溶剂中溶剂度较大; 4、化学稳定性好; 5、具有挥发性,易于与被萃取物分离; 6、无毒性、不易燃。
(二)机械搅拌装置
机械搅拌 装置通常包括: 电动搅拌器、 搅拌棒、密封 装置、圆底烧 瓶等回流或蒸 馏装置。
二、实验原理
卤代烷在无水乙醚中与发生加成—水解反应,得 到叔醇。
C2H5Br + Mg
无水Et2O
C2H5MgBr
①(CH3)2CO,无水Et2O
②H2O,H
徐寿昌主编有机化学(第二版)_课后1_13章习题答案
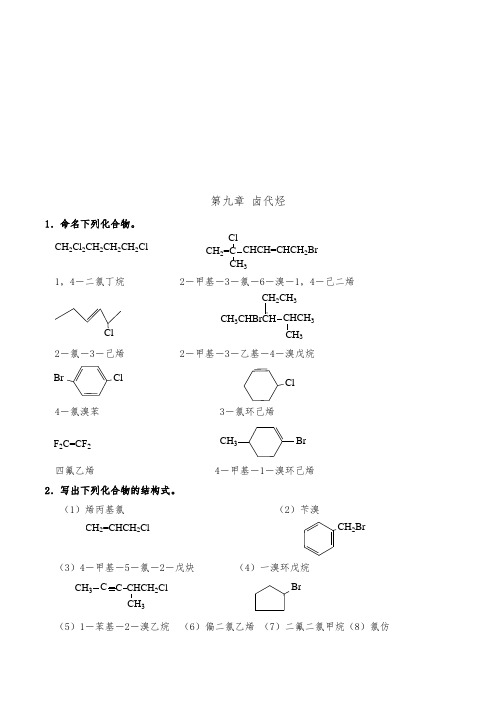
第九章卤代烃1.命名下列化合物。
CH2Cl2CH2CH2CH2Cl CH2=C CHCH=CHCH2BrCH3Cl1,4-二氯丁烷 2-甲基-3-氯-6-溴-1,4-己二烯CH3CH2CH3CHCH3CH32-氯-3-己烯 2-甲基-3-乙基-4-溴戊烷ClBr Cl4-氯溴苯 3-氯环己烯F2C=CF2CH3Br四氟乙烯 4-甲基-1-溴环己烯2.写出下列化合物的结构式。
(1)烯丙基氯(2)苄溴CH2=CHCH2Cl CH2Br(3)4-甲基-5-氯-2-戊炔(4)一溴环戊烷CH3C C CHCH2ClCH3Br(5)1-苯基-2-溴乙烷(6)偏二氯乙烯(7)二氟二氯甲烷(8)氯仿CH2CH2Br CL2C=CH2CCl2F2HCCl33.完成下列反应式:CH3CH=CH2+HBr CH3CHCH3CH3CHCH3CN(1)CH3CH=CH2+HBr CH3CH2CH2Br H2O(KOH)CH3CH2CH2OH(2)CH3CH=CH2+Cl 5000C ClCH2CH=CH2Cl+H O ClCH2CHCH2ClOH(3)+Cl2ClCl2KOH(4)KICH3COCH3I(5)CH3CH CHCHCH3OHPCl5CH3CH CHCH3CH3ClNH3CH3CHCH3NH2CH3(6)(CH3)3CBr+KCN25CH2=C(CH3)2(7)CH3CHCH3OHPBrCH3CHCH3AgNO3/C2H5OHCH3CHCH3ONO2(8)C2H5MgBr+CH3CH2CH2CH2C CH CH3CH3+CH3CH2CH2CH2C CMgBr(9)ClCH=CHCH2Cl+CH3COONa3ClCH=CHCH2OOCCH3+NaCl(10)CH CH+25ClC=CClHClCl2CHCHCl22Cl(11)CH2Cl+3CH2CH2CH2CH2CH2OC2H5CNNH2IOH(12)4.用方程式表示CH3CH2CH2CH2Br与下列化合物反应的主要产物。
2-甲基-2-丁醇的制备

2-甲基-2-丁醇的性质
分子式:C5H12O CAS:75-85-4 相对分子质量88.15 性状:无色澄清挥发液体。 能与乙醇、乙醚、苯、氯仿、甘油及油类混溶 相对密度(d20)0.8084。 熔点 -9℃。 沸点 102.5℃(101.98kPA)。 易燃。低毒,半数致死量(大鼠,经口)1000mG/kG。对粘膜 有刺激性。高浓度时有麻醉作用。 密封阴凉避光通风保存。 用途:有机合成。溶剂。高纯度的可用作气相色谱分析中定 性、定量的标准物质。
通常以通式RMgX表示。格氏试剂是一 种活泼的有机合成试剂,能进行多种反应, 主要包括:烷基化反应,羰基加成,共轭 加成,及卤代烃还原等。
格氏试剂一般有两种 1:氯苯类(氯化苄)在乙醚(四氢呋喃) 下和镁反应, 2:溴代环戊烷在乙醚(四氢呋喃)下和镁 (锌)反应。
实验原理
卤代烷在无水乙醚中与金属镁发生反应生成卤化 镁,生成的卤化镁与酮发生加成-水解反应,得到 叔醇。
2-甲基-2-丁醇的制备
实验目的
1.学习格氏试剂的制备和使用 2.初步掌握低沸点易燃液体的处理方式
溴乙烷的性质
化学式:C2H5Br 结构式:CH3-CH2Br 分子量 :108.9651 性状:无色油状液体。有类似乙醚的气味和 灼烧味。露置空气或见光逐渐变为黄色。易 挥发。能与乙醇、乙醚、氯仿和多数有机溶 剂混溶。相对密度1.4612。凝固点-119℃。 沸点38.2℃。蒸气有毒。浓度高时有麻醉作 用。能刺激呼吸道。溴乙烷在水溶液中或熔 化状态下均不电离,是非电解质。
2-甲基-2-丁醇的制备
7.乙基溴化镁溶液用冷水浴冷却,再搅拌下缓慢滴 加无水丙酮和无水乙醚的混合液 8.再继续滴加硫酸溶液 9.将混合液倒入分液漏斗中,分层。保留水层,醚 层用碳酸钠溶液洗涤,分出醚层保留,后碱层和水 层合并,萃取。 10.合并后的醚层加入无水碳酸钾干燥,加塞、振摇, 至澄清透明 11.干燥后用旋转蒸发仪蒸出溶液 12.残留液蒸出馏分,得到2-甲基-2-丁醇 13.计算产率
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
2-甲基-2-丁醇的合成
指导教师:邹平姓名:崔仁勇专业:化学生物学学号:20064072
摘要:本实验采用来制备醇,即采用醛、酮、羧酸等与Grignard加成生成醇盐,经水解形成醇。
通过丙酮18ml(14.5g)与Grignard试剂反应生成了10.0g2-甲基-2-丁醇,产率为68.96%。
关键词:2-甲基-2-丁醇Grignard反应Grignard试剂
醇在有机化学中应用及其广泛,不但可以用作有机溶剂,而且易于形成卤代物、烯、醚、醛、酮等有机物,因此是一类重要的化工原料。
实验室醇的制备方法较多,常用的就是采取Grignard反应来制备,即采用醛、酮、羧酸等与Grignard 加成生成醇盐,经水解形成醇。
根据这种方法通过采用不同的原理可以制备相应的伯、仲、叔醇。
Grignard试剂的制备时在无水乙醚存在下,卤代烷与金属镁作用后形成的烷基卤化镁RMgX。
R-X+Mg RMgX(X=Cl,I,Br) 对于芳香族卤化物和卤乙烯类型的化合物,一般以乙醚作溶剂的条件下,不生成Grignard实际。
如改用碱性较强,沸点较高的四氢呋喃作溶剂,则它们可以生产Grignard实际,且操作比较安全。
Grignard反应必须在无水、无氧条件下进行。
因为微量的水分存在,不但阻碍卤代烷和镁之间反应,同时也会破坏Grignard试剂而影响产率,Grignard试剂遇水会发生下列分解:
RMgX+H2O RH+Mg(OH)X 除此以外,还可以和具有活泼氢的化合物(醇、羧酸等)发生分解反应。
Grignard试剂遇氧后,发生如下反应:
RMgX+O2ROMgBr ROH+Mg(OH)X
因此,格式试剂的制备以及反映均需在无水、无醇以及无氧的条件下进行。
反应是体系最好采用氮气保护以隔绝空气。
一般采用乙醇作溶剂,利用乙醇的挥发性大,也可以赶走反应体系中的空气。
另外还要保证反应体系中绝对干燥。
此外,在Grignard反应过程中,有热量放出,所以滴加速度不宜过快。
必
要时反应瓶需用冷水冷却。
在制备Grignard试剂时必须先加入少量的卤代烷和镁作用,待发生后,再将其余的卤代烷逐滴加入。
调节滴加速度,使乙醇保持微沸。
对于活性较差的卤代烷或反应不易发生时,可采用加热或加少许碘粒来引发反应。
Grignard试剂与醛酮反应形成加成物时,在酸性条件下进行水解,如通常采用稀盐酸或稀硫酸以使产生的碱式卤化镁转变成易于水解的镁盐,便于乙醚溶液和水溶液分层。
由于水解时放热,故要在冷却下进行。
对于遇酸极易脱水的醇,最好采用氯化铵溶液水解。
1实验部分
1.1主要仪器与试剂
250ml 三颈瓶回流套装装置溴乙烷镁条无水乙醚丙酮20%硫酸5%碳酸钠无水碳酸钾
1.2实验步骤
在250ml三颈瓶上分别装置搅拌器、回流冷凝管及恒压漏斗,在冷凝管上端装置氯化钙干燥管。
瓶内放置7.0g(约0.29mol)镁条和50ml无水乙醚。
在恒压漏斗中加入28ml溴乙烷(40.0g,0.37mol)及25ml无水乙醚,混合均匀。
先往是三颈瓶中滴加3-4ml混合液,数分钟后即见溶液微微沸腾,乙醚自行回流(若不发生反应,可温热促进反应)。
反应开始时比较剧烈,待反应缓和后,开动搅拌,滴加其余的溴乙烷混合溶液。
控制地价速度维持乙醚溶液呈微沸状态。
加完后,再继续搅拌回流15min,至镁条几乎消失,然后在冰水浴冷却和搅拌下,慢慢滴加18ml丙酮(14.5g,0.25mol)及15ml无水乙醚的混合溶液。
滴加速度仍维持乙醚溶液呈微沸状态。
加完后,再继续搅拌回流15min。
瓶中有灰白色或黑色粘稠状固体析出。
将反应瓶在冰水浴冷却和搅拌下,自滴液漏斗中分批加入130ml20%硫酸溶液,分解产物。
待分解完全后,将溶液导入分液漏斗中,分出醚层。
水层每次用25ml乙醚萃取两次,合并醚层,用30ml5%碳酸钠溶液洗涤一次。
再用无水碳酸钾干燥。
将干燥的粗产物醚溶液滤入干燥的50ml蒸馏瓶中。
温热蒸去乙醚,然后再
加热蒸馏,收集95-105℃馏分,产量为10-15g,产率为46-55%。
Ⅱ结果与分析
本实验采用Grignard反应来制备醇,即采用醛、酮、羧酸等与Grignard加成生成醇盐,经水解形成醇。
试验中反映仪器及试剂必须充分干燥,镁条应用新炮制,为了使开始时溴乙烷局部浓度较大,易于发生,故搅拌应在开始后进行。
本实验因在无水条件下反应,因为微量的水分存在,不但阻碍卤代烷和镁之间反应,同时也会破坏Grignard试剂而影响产率。
该实验丙酮18ml(14.5g)与Grignard 试剂反应生成了10.0g2-甲基-2-丁醇,产率为68.96%。
参考文献
[1] 刘灿叫,刘志光对羟基苯乙酮制备工艺研究[J].精细化工中间体2007.32(6).35
[2]Ma Y, Luo W, Quinn P J, et al. J Med Chem [J], 2004, 47(25):6349-6362.
[3]张珍明,李树安,葛洪玉. 8-羟基喹啉制备技术进展. 广州化学. 2007年6月,第32卷第2期。
