中药饮片—— 洗、润生产记录
中药饮片批生产记录

产品生产台帐RED-P 01.01№****** 药业有限公司领 料 单 RED-P 01.02第一联 仓 库QA : 领料人: 发放人: 日期:领料 单 RED-P 01.02第二联 领料部门QA:领料人:发放人:日期:净选岗位生产记录RED-P 01.03******药业有限公司洗润岗位生产记录******药业有限公司切制岗位生产记录******药业有限公司干燥岗位生产记录******药业有限公炒制岗位生产记录******药业有限公司蒸制岗位生产记录******药业有限公司煅制岗位生产记录******药业有限公司粉碎岗位生产记录******药业有限公司筛选岗位生产记录******药业有限公司发芽岗位生产记录RED-P 01.12******药业有限公司包装岗位生产记录******药业有限公司炼蜜岗位生产记录RED-P 01.14******药业有限公司蜜炙麸皮岗位生产记录RED-P 01.15******药业有限公司批生产记录归档台帐RED-P 01.17..净选岗位生产记录RED-P 01.03苏州市博源药业有限公司洗 润 岗 位 生 产 记 录 RED-P 01.04苏州市药业有限公司切 制 岗 位 生 产 记 录 RED-P 01.05苏州市健生源药业有限公司干 燥 岗 位 生 产 记 录 RED-P 01.06蒸 煮 制 岗 位 生 产 记 录 RED-P 01.08苏州市博源药业有限公司筛 选 岗 位 生 产 记 录 RED-P 01.11******药业有限公司批生产档案RED-P 01.16产品名称生产批号生产日期批量㎏******药业有限公司。
中药饮片——包装批生产记
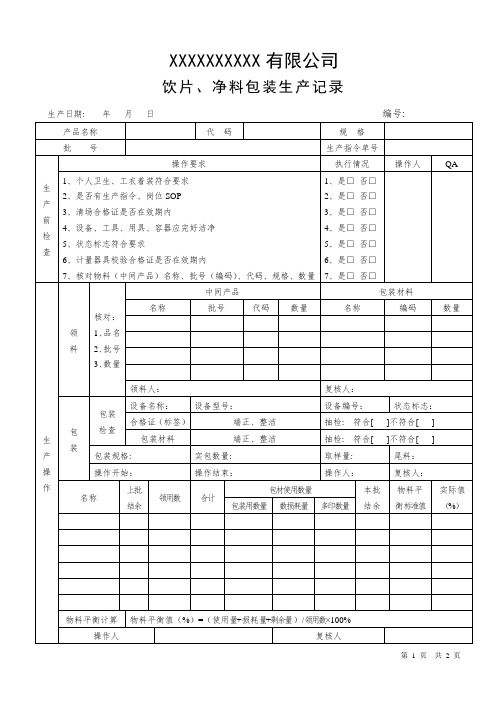
饮片、净料包装生产记录
生产日期:年月日编号:
产品名称
代码
规格
批号
生产指令单号
生
产
前
检
查
操作要求
执行情况
操作人
QA
1、个人卫生、工衣着装符合要求
2、是否有生产指令、岗位SOP
3、清场合格证是否在效期内
4、设备、工具、用具、容器应完好洁净
5、状态标志符合要求
6、计量器具校验合格证是否在效期内
操作人
复核人
XXXXXXXXXX有限公司
饮片、净料包装生产记录
生产日期:年月日编号:
产品(kg)
入库时间
入库人:
复核人:
入库数量(kg)
入库时间
入库人:
复核人:
入库数量(kg)
入库时间
入库人:
复核人:
合计
合计人:
复核人:
收率计算
物料平衡标准
标准值
实际值
结论
内包物料平衡公式
端正、整洁
抽检:符合[ ]不符合[ ]
包装材料
端正、整洁
抽检:符合[ ]不符合[ ]
包装规格:
实包数量:
取样量:
尾料:
操作开始:
操作结束:
操作人:
复核人:
名称
上批结余
领用数
合计
包材使用数量
本批结余
物料平衡标准值
实际值(%)
包装用数量
数损耗量
多印数量
物料平衡计算
物料平衡值(%)=(使用量+损耗量+剩余量)/领用数×100%
内包工序物料平衡(%)=(合格品数量+废弃数量+取样量)/投料量(半成品)×100%
中药饮片批生产记录(毒性药材)

中药饮片批生产记录 (毒性药材)
产品名称
产品代号产品规格
产品批号
成品数量
QA
车间主任
生产日期:
制定人/日期
审核人/日期
批准人/日期
有限公司
批生产汇总表(毒性药材)
填表人:
批生产指令单(毒性药材)产品名称:规格:产品代号:
产品名称:规格:产品代号:
中药饮片净制岗位生产记录(毒性药材)
中药饮片净制岗位生产记录(毒性药材)
中药饮片洗润岗位生产记录(毒性药材)
中药饮片洗润岗位生产记录(毒性药材)
中药饮片切制岗位生产记录(毒性药材)
中药饮片切制岗位生产记录(毒性药材)
中药饮片干燥岗位生产记录(毒性药材)
中药饮片干燥岗位生产记录(毒性药材)
中药饮片蒸煮岗位生产记录(毒性药材)
产记录(毒性药材)
中药饮片蒸煮岗位生
中药饮片炒制岗位生产记录(毒性药材)
中药饮片炒制岗位生产记录(毒性药材)
生产日期:页次:2/2
中药饮片内包装岗位生产记录(毒性药材)
中药饮片内包装岗位生产记录(毒性药材)
:
中药饮片外包装岗位生产记录(毒性药材)
批生产记录确认记录(毒性药材)
QA:生产部:车间主任:车间质量员:。
中药饮片批生产记录模板

云南楷林中药饮片有限责任公司REC-SC1005-00-03第1页共1页编制人:日期:年月日审核人:日期:年月日批准人:日期:年月日颁发部门质量管理部颁发日期:年月日生效日期:年月日分发部门质量管理部、生产管理部批生产记录品名:批号:生产日期:计划产量:生产负责人:审核人(QA):云南楷林中药饮片有限责任公司REC-SC1005-01-03第1页共1页生产指令单品名规格生产批号生产日期计划产量计划生产周期生产依据按生产工艺规程进行生产操作工艺代码 1.净选2.洗润3.切制4.炒制5.蒸制6.煮制7.干燥8.微生物控制9.粗碎10.粉碎11.混合原辅料计划领料量序号物料名称入库批号/编码计划领料量单位备注拟定人签名:日期:年月日审核人签名:日期:年月日接收人签名:生产部质量部仓库年月日年月日年月日注:1.本生产指令单一式三份,生产部、质量部、仓库各一份。
质量部接到生产指令后需对指令内容进行核对并安排检验、监管工作;仓库按生产指令发放物料、并核对相应信息;生产车间严格按生产指令内容安排生产,生产结束后生产车间指令单归集至批生产记录中统一收回。
2.物料入库批号或代码由仓库管理员填写。
3.指令接收人指定为生产车间主管、质量部QA或QA主管及仓库管理员。
云南楷林中药饮片有限责任公司REC-SC1005-02-03第1页共1页原辅料收料记录品名产品批号计划产量生产日期年月日序号物料名称物料编码批号数量/重量单位备注12345仓库发料人车间收料人复核人日期年月日日期年月日日期年月日净选工序记录品名产品批号计划产量生产日期年月日操作步骤与要点工艺控制范围操作记录1.工前准备1.1核对文件与记录1.2确认上批清场结果1.3确认设备完好、清洁状态1.4检查物料及标识状态1.1.生产文件、记录齐全且已受控1.2.清场合格并在有效期内1.3.设备完好已清洁合格1.4.物料品种、数量正确且检验合格,已有标识且与物料相一致1.□符合规定□不符合规定2.□符合规定□不符合规定3.□符合规定□不符合规定4.□符合规定□不符合规定2.净选方法执行该品种工艺规程□设备设备名称:设备编号:设备型号:□人工2.1除去非药用部位、杂质及霉变品、虫蛀品等。
中药饮片炮制及生产管理

2提提示示
① 批准的饮片标准 和依据;
编制工艺规程的技术基础
中药饮片必须按照国家药品标准炮制;国家药
品标准没有规定的;必须按照省 自治区 直辖市人 民
政府药品监督管理部门制定的炮制规范炮制;
中药饮片标准工艺规程岗位SOP批生 产记录应 一一对应;
3 7
2提提示示
② 规范的工艺流程图
物料 工序
2 6
3 标准
D级别洁净区微生物监测的动态标准如下:
洁净度 级别
D级
浮游菌 cfu/m3
200
沉降菌90mm cfu
表面微生物
/4小时2
接触55mm cfu
5指手套
/碟
cfu /手套
100
50
注:1表中各数值均为平均值; 2单个沉降碟的暴露时间可以少于4小时;同一位置可使用多个 沉降碟 连续进行监测并累积计数;
* 确保生产操作和过程监控有章可循; * 确保所有操作人员都经过培训;明确各自的 职责和任务; * 确保批生产记录的真实 可靠;能进行生产全 过程的有效追踪;
* 确保成品放行前审核文件的完整性和准确性;
3 5
二 生产文件管理
4 生产管理主要技术文件 1工艺规程 1规定内内容容 补充规定中明确中药饮片生产 工艺规程 内容包括:名称;规格;炮制工艺的操作要求和技 术参数;物料 中间产品 成品的质量标准及贮存 注意事项;物料平衡的计算方法;包装规格等要 求;
批生产记录 含义 内容 管理 审核
生产管理
生产流程管理
生产准备 文件 物料 现场 记 录
生产操作 配料复核 生产包装 过程监控
生产结束 清场 结料 流转 记录
生产过程管理
偏差管理 物料平衡 中间产品管理 不合格品管理 状态标志管理 批号管理 防污染混淆 工艺用水管理
中药饮片批生产记录

备 注
三、清场:按清场规程进行清场。清场结束报请QA进行现场检查,合格后签发清场合格证
清场项目
操作人
检查人
检查结果
作业室及设备的状态标志更换成“待清洁” □
对岗位记录等有关文件进行整理 □
按相应SOP对设备和容器具进行清洗 □
对操作台、作业室环境进行清洁 □
对清洁工具清洗并存放指定位置 □
异常情况及处理:
□
有“设备完好”标识,操作台、工器具清洁并有效保持
□
二、净选作业 方式:风选□ 筛选□ 挑选□ 刷净□ 刮除□ 剪切□。
1.来料确认
名称、规格、批号、产地、数量与生产指令一致□;称重㎏。
确认人
2.设备使用
设备名称
风选机□柔性支撑斜面筛选机□振动式筛选机□
操作者
Q A
3.手工过筛
操作时间
--
操作者
净选收量
□
操作间整洁,无上次生产遗留物,无与本次生产无关的物料
□
设备、操作台、工器具清洁并有效保持
□
二、水处理作业:洗药用流动水;用过的水不得用于洗涤其它药材;洗净的药材不得直接接触地面。
1.洗
净
清洗方式: 淋洗□ 抢水洗□ 淘洗□ 机洗□其他□
开始时间
结束时间
洗药用时间
时 分
时 分
时 分
时 分
时 分
操作者
Q A
三、清场:按清场规程进行清场。清场结束报请QA进行现场检查,合格后签发清场合格证
清场项目
操作人
检查人
检查结果
作业室及设备的状态标志更换成“待清洁” □
对岗位记录等有关文件进行整理 □
按相应SOP对设备和容器具进行清洗 □
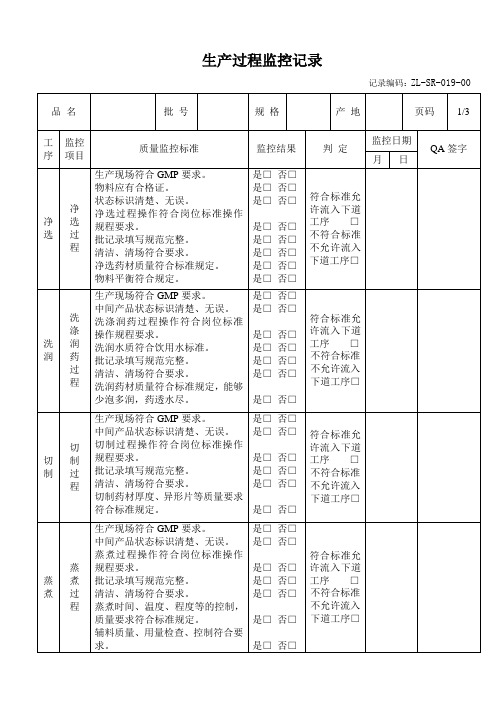
中药饮片生产过程监控记录
筛
选
筛
选
过
程
生产现场符合GMP要求。
中间产品状态标识清楚、无误。
筛选过程操作符合岗位标准操作规程要求。
批记录填写规范完整。
清洁、清场符合要求。
筛目、筛选净度的控制,质量要求符合标准规定。
物料平衡符合规定。
是□否□是□否□
是□否□
是□否□
是□否□
是□否□
是□否□
符合标准允许流入下道工序□
中间产品状态标识清楚、无误。
炒制过程操作符合岗位标准操作规程要求。
批记录填写规范完整。
清洁、清场符合要求。
炒制时间、温度、程度等的控制,质量要求符合标准规定。
辅料质量、用量检查、控制符合要求。
物料平衡符合规定。
是□否□
是□否□
是□否□
是□否□
是□否□
是□否□
是□否□
是□否□
符合标准允许流入下道工序□
洗润药材质量符合标准规定,能够少泡多润,药透水尽。
是□否□
是□否□
是□否□
是□否□
是□否□
是□否□
是□否□
符合标准允许流入下道工序□
不符合标准不允许流入下道工序□
切
制
切
制
过
程
生产现场符合GMP要求。
中间产品状态标识清楚、无误。
切制过程操作符合岗位标准操作规程要求。
批记录填写规范完整。
清洁、清场符合要求。
碰碎过程操作符合岗位标准操作规程要求。
批记录填写规范完整。
清洁、清场符合要求。
碰碎粒度等的控制,质量要求符合标准规定。是□否□是□□是□否□是□否□
是□否□
中药的饮片批生产记录簿

产品生产台帐RED-P 01.01№****** 药业有限公司领料单RED-P 01.02 产品名称:生产批号:№第一联仓库QA:领料人:发放人:日期:领料单RED-P 01.02第二联领料部门QA:领料人:发放人:日期:净选岗位生产记录 RED-P 01.03******药业有限公司******药业有限公司******药业有限公司干燥岗位生产记录******药业有限公炒制岗位生产记录******药业有限公司蒸制岗位生产记录******药业有限公司煅制岗位生产记录******药业有限公司粉碎岗位生产记录******药业有限公司筛选岗位生产记录******药业有限公司发芽岗位生产记录 RED-P 01.12******药业有限公司包装岗位生产记录******药业有限公司炼蜜岗位生产记录 RED-P 01.14******药业有限公司蜜炙麸皮岗位生产记录 RED-P 01.15******药业有限公司批生产记录归档台帐 RED-P 01.17净选岗位生产记录 RED-P 01.03苏州市博源药业有限公司洗 润 岗 位 生 产 记 录 RED-P 01.04苏州市药业有限公司切 制 岗 位 生 产 记 录 RED-P 01.05苏州市健生源药业有限公司干 燥 岗 位 生 产 记 录 RED-P 01.06蒸 煮 制 岗 位 生 产 记 录 RED-P 01.08苏州市博源药业有限公司筛 选 岗 位 生 产 记 录 RED-P 01.11******药业有限公司批生产档案RED-P 01.16产品名称生产批号生产日期批量㎏******药业有限公司。
SOR-01-中药饮片总批生产记录(DOC)备课讲稿

******药业有限公司
批生产记录
产品名称:
产品批号:
生产周期:月日—月日生产负责人:
质量受权人:
批生产指令单
签发人:签发日期:
工序批生产记录
洗润工序批生产记录
切药工序批生产记录
晾晒工序批生产记录
烘药工序批生产记录
炮制(制)工序批生产记录
干燥温度、时间控制曲线图
进箱时间:出箱时间:进箱时间:出箱时间:
100
90
80
70
60
50
40
30
20
10
进箱时间:出箱时间:进箱时间:出箱时间:
100
90
80
70
60
50
40
30
20
10
进箱时间:出箱时间:进箱时间:出箱时间:
附到批生产记录
附到批生产记录
产品进站清单
附到批生产记录
产品进站清单
产品出站清单
附到批生产记录
附到批生产记录
产品出站清单
产品出站清单
产品出站清单
产品出站清单
清场检查记录
年月日
偏差处理单
领料单年月日
领料单年月日
成品入库单年月日
成品入库单年月日
领料单年月日
领料单年月日
成品入库单年月日
成品入库单
年月日
破碎工序批生产记录。
中药饮片炮制工艺的规程通则

中药饮⽚炮制⼯艺的规程通则1.⽬的本通则规定了饮⽚⽣产全过程的⼯艺技术、质量、物耗、安全、⼯艺卫⽣、环境保护等内容。
2.适⽤范围本通则适⽤于饮⽚⽣产的全过程,是各部门共同遵循的技术准则。
3.引⽤标准《中国药典》2010年版《全国中药炮制规范》1988年版《⼴西中药饮⽚炮制规范》(2007年版)《中药饮⽚验收检查项⽬》2005年版《中药饮⽚质量标准通则(试⾏)》(国家中医药管理局颁布)《药品⽣产质量管理规范》1998年修订本4.职责编写:技术员汇审:总经办、质量保证部及其他相关部门负责⼈批准:总经理执⾏:各级⽣产质量管理⼈员及操作⼈员监督管理:质量部QA⼈员、⽣产管理⼈员5.产品概述项⽬要求如下,其内容按各品种项下规定。
5.1产品名称5.1.1品名5.1.2汉语拼⾳5.2来源5.3性状5.4性味归经5.5功能主治5.6⽤法与⽤量5.7贮藏5.8规格6.⼯艺流程图6.1清炒⼯艺流程图6.2加辅料炒⼯艺流程图6.3炙制⼯艺流程图6.4燀制⼯艺流程图6.5煮制⼯艺流程图6.6蒸制⼯艺流程图6.7烫制⼯艺流程图6.8煨制⼯艺流程图6.9⽔飞⼯艺流程图6.10煅制⼯艺流程图7. 操作过程及⼯艺条件7.1净制: 按照领料程序从库房领出原料,根据《中国药典》2005年版、《全国中药炮制规范》1988年版、《⼴西中药饮⽚炮制规范》2007年版及该品种《炮制⼯艺规程》进⾏净制⽣产。
7.1.1净选操作⼈员严格按照净制SOP进⾏操作。
7.1.1.1操作⼈员选⽤不锈钢筛⽹,筛除泥沙、杂质,⼿选去⾮药⽤部份及霉变药材。
7.1.1.2操作⼈员将净选后的药材在QA监控下转⼊洗药区。
7.1.2.1洗药前的检查,洗药间不得有上次⽣产剩余的物料,洗药池洁净度应符合⽣产要求。
7.1.2.2洗药操作:7.1.2.1检查为正常后⽅可将药材放⼊洗药池内,先打开排⽔阀,再打开进⽔阀将清洁⽔喷⼊洗药池内,使药材得到充分清洗(冲5分钟),清洗⼲净后起料,起料后放⼊洗药⽤料盘内滤去余⽔。
中药饮片工艺验证0009-大黄方案

中药饮片工艺验证0009-大黄方案文件名称大黄工艺验证方案版本号 00-2015文件类别技术标准起草人日期文件编码 M-VL-0009 审核人日期执行日期批准人日期分发部门质量管理部、生产设备部一、概述:1.生产情况概述:中药饮片在进行了关键岗位员工培训及各种设备安装确认、运行确认、计量器具校验后,开始中药饮片的生产。
现对大黄的生产工艺关键工序进行验证,以确定大黄生产过程的稳定性,保证在规定的条件下始终如一地生产出质量可靠的大黄饮片。
2.产品概述:2.1 品名:大黄2.2.规格:2-4mm厚片。
2.3.性状:本品呈类圆柱形、圆锥形、卵圆形或不规则块状,长3,17cm,直径3,lOcm。
除尽外皮者表面黄棕色至红棕色,有的可见类白色网状纹理及星点(异型维管束)散在,残留的外皮棕褐色,多具绳孔及粗皱纹。
质坚实,有的中心稍松软,断面淡红棕色或黄棕色,显颗粒性;根茎髓部宽广,有星点环列或散在;根木部发达,具放射状纹理,形成层环明显,无星点。
气清香,味苦而微涩,嚼之粘牙,有沙粒感。
二、范围:适用于大黄生产工艺的验证。
三、人员与职责:验证小组负责对此工艺的验证,生产人员协助操作,具体见下表:姓名职务所在部门及职务验证过程中的职责批准验证方案及验证报告梁文峰组长总经理落实验证文件起草者,安排验证过程按进度有序进行,审核验证方案、记石殿祥成员生产设备部经理录是否完整及最终验证结果评价。
负责验证方案的审核及验证报告评价。
李文平成员质量部经理负责起草验证方案,负责验证数据的收集、校对、复核确认工作。
负责整梁宗海成员生产设备部理文件记录的归档工作及最终验证报告。
负责验证确认过程中现场检测相关工作。
马富巧成员质量部QA负责取样、检验,出具检验报告,确认验证结果。
陈玉芳成员质量部QC 负责设备运转正常,辅助完成工艺验证王建中成员生产设备部四、验证依据:大黄生产工艺规程(Y/M-TS-0016)五、大黄生产工艺流程:大黄拣选洗润切厚片干燥酒炙蒸制炒炭筛选包装 M-VL-0009 1 /18六、本次验证内容:本验证将对大黄的清洗、润、切、干燥、筛选、包装等关键工序进行验证。
中药饮片管理制度(附各类记录表格)

中药饮片管理制度(附各类记录表格)某某某某医院中药饮片管理制度二〇一六年九月目录中药饮片质量管理办法3中药饮片采购管理制度3中药饮片入库验收管理制度4不合格药品及药品退货管理制度4中药饮片保管储存养护管理制度5温湿度记录管理制度6中药饮片调剂管理制度6中药饮片处方调剂操作规程7煎药室工作制度8煎药室操作规范8中药煎药室清洁与消毒操作规程9中药安全性监测管理制度10中药不良反应事件报告制度10中药供药企业药品评估管理细则11处方点评管理办法与中药饮片处方点评实施细则12附件:中药饮片管理各类记录、表格14表一:中药饮片供应商资质定期评审记录14表二:中药饮片购进、验收、入库记录16表三:中药饮片养护检查记录17表四:中药库中药饮片退货记录18表五:药房温湿度记录表19表六:中药房煎药室操作记录20表七:煎药室煎药设备器械容器日常清洁、消毒记录21表八:煎药室质量控制监测检查表22表九:煎药室工作质量满意度调查表23表十:钟祥同仁医院中药处方(病历)点评工作表24表十一:药品不良反应报告表25中药饮片质量管理办法为科学、规范地管理本院的中药饮片,保证用药安全、有效、经济、合理,保障人民身体健康,依据《中华人民共和国药品管理法》、《医疗机构药事管理规定》、《医院中药饮片管理规范》、《中药处方格式及书写规范》、《医疗机构中药煎药室管理规范》等法律法规,制定本办法。
一、本院药事管理与药物治疗学小组在院长的领导下,负责全院的中药饮片质量管理工作,院长为中药饮片管理的第一责任人,药剂科(药房)负责中药饮片质量管理的日常工作。
某某某某医院药事管理与药物治疗学小组组长:副组长:成员:二、建立健全中药饮片质量监督体系,各临床相关科室有专人负责中药饮片质量管理工作,药剂科定期检查中药饮片质量。
三、中药饮片质量管理人员、医院职工及患者,如果发现中药饮片质量问题,有权直接向医院领导或院药事管理与药物治疗学小组反映,任何科室和个人不得无故干涉和打击报复。
中药饮片批生产记录

中药饮片批生产记录一、基本信息1.产品名称:XXX中药饮片2.生产批号:XXX-2024XXX3.生产日期:2024年XX月XX日4.生产线号:XXX二、原料准备1.原料名称:XXXX(按照普通名称、拼音首字母排序,加入合适的说明)。
2.原料品牌:XXX(生产商名称),批号:XXX3.用量:按照处方和配方要求,准确称量。
4.检查:检查原料外观,气味、湿度、杂质等,并在记录中注明合格与否。
5.清洗:如有需要,对原料进行清洗处理,保证无杂质。
三、生产过程1.设备清洁:确认生产设备已经清洁干净,符合卫生要求。
2.操作员:XXX3.操作步骤:(1)根据工艺流程,准备生产所需的器具和设备。
(2)按照生产配方,将称好的原料依次放入料斗中。
(3)启动搅拌机,根据工艺要求进行搅拌,搅拌时间、速度和转速等需要记录。
(4)运送:将搅拌好的料移送至下一个工序。
4.温度、湿度记录:记录生产过程中的温度和湿度,确保符合工艺要求。
四、包装和贮存1.包装要求:根据产品要求选择包装材料并包装好。
2.包装记录:记录包装过程中的产品批号、包装材料、操作人员等信息。
3.贮存要求:按照产品要求的环境条件进行贮存。
五、清洁、消毒和废弃物处理1.清洁:生产设备的清洁,如搅拌机等。
2.消毒:根据产品特性和卫生要求,做好设备的消毒处理。
3.废弃物处理:按照相关规定妥善处理生产过程中产生的废弃物。
六、记录与复核1.生产记录:记录生产过程中的详细操作步骤、温度湿度、称量、检查结果等信息。
2.复核记录:复核记录的人员姓名、复核时间、复核结果等信息。
七、备注1.根据实际需要,添加合适的备注信息。
以上是一份中药饮片批生产记录的简要示例,生产记录的内容应根据具体情况进行调整和补充。
同时,为了确保生产质量,生产过程中还需要严格遵守相关的操作规范和卫生要求。
中药饮片各岗位标准操作规程

第八部分生产管理标准操作规程XXXXXX有限公司目录1.净选岗位操作规程 SOP-08-1012.洗润岗位操作规程 SOP-08-1023.蒸制岗位操作规程 SOP-08-1034.切制岗位操作规程 SOP-08-1045.干燥岗位操作规程 SOP-08-1056.炒制岗位操作规程 SOP-08-1067.炙制岗位操作规程 SOP-08-1078.筛选岗位操作规程SOP-08-1089.煅制岗位操作规程 SOP-08-10910.破碎岗位操作规程SOP-08-11011.内包装岗位操作规程 SOP-08-11112.外包装岗位操作规程 SOP-08-112标准操作规程题目:净选岗位操作规程编号:SOP-08-101制定人:制定日期:2017年月日版本: 1 页数: 1/2 审核人:审核日期:2017年月日颁发部门:质量部批准人:批准日期:2017年月日生效日期:2017年月日目的:建立净选岗位操作规程,确保产品质量。
范围:净选岗位责任:净选员工,班长及监控员。
标题正文1.1.11.21.3 1.3.1 1.3.2 1.3.3 1.3.4 1.41.52.2.1 2.2 2.3生产前准备净选工序班长到车间主任办公室领取批生产记录(含指令)和空白状态标识。
净选岗位操作工执行《生产区人员更衣更鞋规程》(SOP-08-312)提前10分钟进入生产区。
进入生产岗位检查是否有前次清场合格证副本。
检查净选间是否有已清洁状态标识,且在有效期内。
检查容器具、工器具是否有已清洁状态标识,且在有效期内。
检查是否有与本次生产无关的文件,确认无上次生产遗留物。
检查合格后,经QA检查确认,班长根据批生产指令的要求,取下现场状态标识牌,换上生产运行中状态标识,标明本岗位需要生产的药品品名、规格、生产批号、生产批量、生产岗位、生产日期、操作人、复核人。
领料,执行《车间领发料管理规程》(SMP-08-023)领取物料。
生产操作规程净选岗位操作工在物料缓冲间内,脱去中药材外包装,倒入洁净的周转箱内,再转至净选间后,用手或撮子取出一些倒于净选台上,按照大小规格进行净选,除去杂质或非药用部位。
中药饮片生产记录表净选、软化、切制、干燥

表12-1 XXX 饮片公司净选岗位生产指令单产品批号 原 料 生产数量 批号 数量 批号 数量 批号 数量 生产时间 年 月 日操作要求 按《净选岗位标准操作规程》操作质量要求备注:发指令人复核人净选岗位生产记录原料批号 产品批号 生产日期 风选机型号 原料数量 损耗数量 风选时间净货数量 损耗率%清理时间 清理时间 清理时间 清理时间 净货 杂质 净货 杂质 净货 杂质 净货 杂质操作人复核人质量员 ×××检查情况检查日期 年 月 日 时 分 ~ 时 分杂质含量非药用部分含量结论: □ 符合规定 检查人: 复核人: 备注:清场:按清场规程进行清场。
清场结束报请QA 进行现场检查,合格后签发清场合格证序号 清场项目 清洁标准 清场结果 清场时间清场人1原料和本批净选产品已清理和送中间站□ 已清理 □ 未清理 月 日时 分2净选生产状态标志生产状态标志已经撤清□ 已清理 □ 未清理3废弃包装材料和净选的杂质收集清出岗位 □ 已清理 □ 未清理 4净选工具及器具水清洗,擦干净 □ 已清理 □ 未清理 检查人5风选机水清洗,擦干净 □ 已清理 □ 未清理6生产环境按《生产岗位清场清洁规程》要求清理□ 已清理 □ 未清理7更换产品品种《按生产岗位清场清洁规程》(更换品种)要求清理□ 已清理 □ 未清理备注:表12-1 XXX饮片公司软化岗位生产指令单产品批号投料数量生产时间年月日生产数量操作要求按《软化岗位标准操作规程》操作质量要求备注:发指令人复核人软化岗位生产记录产品批号生产日期年月日设备型号清洗辅料品名生产数量润药数量投料数量软化过程清洗清洗次序清洗数量清洗时间操作人复核人第一次时分~时分第二次时分~时分第三次时分~时分第四次时分~时分第五次时分~时分润药润药次序润药数量辅料数量水量温度压力润药时间第一次时分~时分第二次时分~时分第三次时分~时分第四次时分~时分第五次时分~时分操作人复核人质量员软化检查情况检查日期年月日时分~时分软化指标结论操作人复核人质量员备注伤水量% □符合规定未润透量% □符合规定腐败、变质□符合规定清场:按清场规程进行清场。
中药饮片的生产管理

(三)要求
(2)设备管理 《1》明显的状态标志; 《2》与设备连接的固定管道标明管内物料的名称、流 向 《3》计量管理 计量仪表、衡器等的使用范围及精度要求; 计量检定计划,记录,定检校验,合格标志等。 《4》明确专人管理,并有使用、维修、保养等制度及 记录。
(四)区域划分
和内控标准; 确保生产操作和过程监控有章可循; 确保所有操作人员都经过培训,明确各自的职
责和任务; 确保批生产记录的真实、可靠、能进行生产全
过程的有效追踪; 确保成品放行前审核文件的完整性和准确性
(二)生产文件管理
4、生产管理主要技术文件 (1)工艺规程
《1》规定内容 “补充规定”中明确中药饮片“生产
相互妨碍; (4)厂房应有防止昆虫和其他动物进入的设施; (5)厂房内表面应平整,易清洁,不易产生脱落物,不易滋生霉
菌; (6)生产区的面积和空间与其生产规模相适应; (7)生产过程产生的废气、废水、粉尘应经处理后排放,并符合
国家环保要求; (8)净制、切制、炮炙等操作间应有相应的通风、除尘、除烟、
一、中药饮片生产特点
(二)工序管理: 1、中药饮片生产流程: 原料→生产(粗选→洗润→切制→干燥→
细选→炮炙→内包→外包)→入库→销 售。 2质量控制 全面质量管理,全过程的控制
原料药材
成分定性、 定量分析
基源鉴定、产地认证 (准确性、道地性
原料仓库
出库审核
饮片生产车间
饮
片
TLC定性、HPLC定量
质
经验鉴别
中药饮片
分析
量
气味 颜色、 味道、片形 饮片 规格等
管
理
水分、灰分、浸出物、 重金属农药残留、
润药工序操作规程

目的:建立洗药工序标准操作规程,统一规范洗药工序的操作,保证中药饮片生产的均一性。
范围:适用于本公司中药饮片车间洗药工序。
职责:润药岗位操作人员对执行本规程负责,上、下工序操作人员、车间主管及车间QA对执行本规程相关内容负责,车间QA负责监督本规程的执行。
内容:1.生产前准备:1.1. 复核清场清洁情况,确认无上次遗留物。
1.1.1. 确认生产场地无与本批生产相关的文件及杂物。
1.1.2. 检查润药室门上的状态标示牌是否为“清场清洁合格证”,证上是否有车间QA的签字,是否在有效期内。
1.1.3. 车间QA按《生产场地清场清洁操作规程》复核清场清洁情况。
1.2. 接受生产指令:1.2.1. 接受“批生产指令”、“润药生产记录”、“中间产品标签”等文件。
1.2.2. 仔细阅读“批生产指令”、“润药生产记录”,清楚了解生产的产品名称、产地、批号、批量、使用设备及操作规程,工艺参数及要求、注意事项等润药操作指令。
1.3. 物料准备:1.3.1. 根据指令到上一工序领取待润原药材。
1.3.2. 阅读中间产品标签上的内容,核对其品名、产地、批号是否与生产指令相符,数量是否与实物相符,是否有车间QA的签名及日期。
1.3.3. 检查待润原药材是否超过最长加工期限,是否霉变有异味。
1.3.4. 根据生产指令领取周转容器,清点的同时检查是否已清洁干净,有无破损。
1.3.5. 将待润原药材、周转容器分别运到润药室,置于指定位置。
1.3.6. 领取待润原药材的同时,把本批的“生产记录”文件夹带到润药室置于记录台上。
1.4. 检查润药池是否干净、光滑。
1.5. QA确认并发证:1.5.1. 操作人员认为准备工作就绪后,向车间QA申请检查。
1.5.2. 车间QA进行检查,确认场地、卫生及生产前准备工作符合要求,签发“准产证”。
2. 生产过程:。
2.1. 投料前,复核人对待润原药材进行复检,复核其品名、产地、批号。
2.2. 确认无误后,将待润原药材置于润药池内,根据药材的不同特性分别加入不等的生产用水,根据药材的不同质地,每隔一段时间翻动一次。
批生产记录

中药饮片批生产记录
产品名称
产品代号产品规格
产品批号
成品数量
QA
车间主任
|
生产日期:
制定人/日期
审核人/日期
批准人/日期
泰州仁济中药饮片有限公司
批生产汇总表
填表人:
批生产包装指令单
产品名称:规格:产品代号:批号:批量:
中药饮片净制岗位生产记录
中药饮片洗润岗位生产记录
中药饮片煅制岗位生产记录
中药饮片切制岗位生产记录
中药饮片干燥岗位生产记录
中药饮片粉碎、过筛岗位生产记录
1/2
中药饮片蒸煮岗位生产记录
中药饮片炒制岗位生产记录
中药饮片炒制岗位生产记录
内包装岗位生产记录
外包装岗位生产记录
批生产记录确认记录
QA:生产部:车间主任:车间工艺员:#。
SOR01中药饮片总批生产记录DOC

****** 药业有限企业批生产记录产品名称:产品批号:生产周期:月日—月日生产负责人:质量授权人:批生产指令单产品名称批号计划产量kg生产日期炮制工艺:生产部长(署名):领料数目物料名称领用数目原药材()包装资料()包装资料()签发人:签发日期:产品:批号:操作步骤操作要求操作记录操作人QA 检查岗位 SOP 有〔〕否〔〕切合〔〕检查文件设备 SOP 有〔〕否〔〕不切合〔〕洁净 SOP 有〔〕否〔〕相应记录检查设备状态完满清场合格证计量用具有效性现场检查状态标记清场合格证操作台的检查状态标记清场合格证查对:1、药材名领料2、批次3、数目有〔〕否〔〕是〔〕否〔〕有效:是〔〕否〔〕有效:是〔〕否〔〕校正:切合〔〕不切合〔〕已洁净〔〕待洁净〔〕有效:是〔〕否〔〕已洁净〔〕待洁净〔〕有效:是〔〕否〔〕药材名:批次:数目:kg件切合〔〕不切合〔〕切合〔〕不切合〔〕切合〔〕不切合〔〕切合〔〕不切合〔〕切合〔〕不切合〔〕4、状态标记状态标记:色个在操作台上是〔〕否〔〕药用与非药用拣后数目: kg 件部分分容器盛挑选放荒弃物量:kg生产时间:月日时结束时间:月日物料均衡计算:标准值: 99%--101% 评论:收率=(拣后数目 +荒弃物) / 领药材实质值:总量计算人:项目要求检查结果净选料置净料暂存间切合〔〕不切合〔〕清场荒弃物置荒弃物站切合〔〕不切合〔〕容器置容器清洗室切合〔〕不切合〔〕操作台洁净 SOP 切合〔〕不切合〔〕现场洁净 SOP 切合〔〕不切合〔〕结论:检查人:QA :切合〔〕不切合〔〕时清场人清场时间月日时工序批生产记录洗润工序批生产记录产品:批号:操作步骤操作要求操作记录操作人QA 检查岗位 SOP 有〔〕否〔〕切合〔〕设备 SOP 有〔〕否〔〕不切合〔〕检查文件洁净 SOP 有〔〕否〔〕相应记录有〔〕否〔〕检查设备状态完满清场合格证计量用具有效性现场检查状态标记清场合格证容器的检查状态标记清场合格证查对:4、药材名领料5、批次6、数目4、状态标记在洗药池或洗药机使用流动水冲洗洗后闷润润后量是〔〕否〔〕有效:是〔〕否〔〕有效:是〔〕否〔〕校正:切合〔〕不切合〔〕已洁净〔〕待洁净〔〕有效:是〔〕否〔〕已洁净〔〕待洁净〔〕有效:是〔〕否〔〕药材名:批次:数目:kg件状态标记:色个是〔〕否〔〕是〔〕否〔〕是〔〕否〔〕kg切合〔〕不切合〔〕切合〔〕不切合〔〕切合〔〕不切合〔〕切合〔〕不切合〔〕切合〔〕不切合〔〕切合〔〕不切合〔〕生产时间:月日时---日时闷润时间:时分项目要求润后料置暂存间清场置荒弃物站荒弃物容器置容器洁净室洗药机或洗药池洁净 SOP现场洁净 SOP 结论:检查人:检查结果切合〔〕不切合〔〕切合〔〕不切合〔〕切合〔〕不切合〔〕切合〔〕不切合〔〕切合〔〕不切合〔〕QA :清场人清场时间月日时切药工序批生产记录产品:批号:操作步骤操作要求操作记录操作人QA 检查岗位 SOP 有〔〕否〔〕切合〔〕设备 SOP 有〔〕否〔〕检查文件不切合〔〕洁净 SOP 有〔〕否〔〕相应记录有〔〕否〔〕检查设备状态完满是〔〕否〔〕有切合〔〕清场合格证效:是〔〕否〔〕不切合〔〕计量用具有效性有效:是〔〕否〔〕切合〔〕校正:切合〔〕不切合〔〕不切合〔〕现场检查状态标记 已洁净〔 〕待洁净〔 〕切合〔〕 清场合格证 有效:是〔 〕 否〔 〕 不切合〔 〕容器的检查状态标记 已洁净〔 〕待洁净〔 〕切合〔〕 清场合格证 有效:是〔 〕 否〔 〕不切合〔 〕产品: 查对: 药材名:7、药材名 批号:操作步骤操作记录批次:操作人QA 检查操作要求领料8、批次数目:kg 有件[ ]无[ ]切合〔〕岗位 SOP检查文件洁净 SOP状态标记: 有[ ]无[ ]符 合 [ ]4、状态标记色 个 ]无[ ]设备 SOP有[不切合 []斜直切式切药旋是〔〕否〔〕 ]无[ ]相应记录有[切合〔〕转式切药机是〔〕否〔〕室内温度 18~26℃符 合 []室内相对湿度45 ~室内实质温:℃检查温湿度饮片规格:%不切合〔〕65%室内实质相对湿度:不切合 []切制切后数目:kg 件]否[ ]有效性有效: 是[ 符 合 [] 计量用具 校正 余料量: kg ]月 日 时 校正:切合 [ ] 不切合 [ 时 不切合 [] 生产时间:结束时间: 月 日物料均衡计算: 洁净 标准值: 99%--101% ] 评论: 工用具 实质值:是[ 否[ ] 收率=(切后数目+异形片量)/ 领药 材总量 状态完满 计算人:是[ ] 否[ ] 检查晾 项目要求 有效: 检查结果 否[ ] 药架盘 清场合格证 是[ ] 饮片 置净料暂存间 切合〔 〕不切合〔 〕 清场 余料 置余料暂存间 切合〔 〕不切合〔 〕容器 置容器洁净室 切合〔 〕不切合〔 〕 切药机洁净 SOP切合〔 〕不切合〔 〕现场洁净 SOP 切合〔 〕不切合〔 〕切合[ ] 不切合[ ]切合[]清场人 不切合[ ]清场时间月 日 时结论:检查人:QA :晾晒工序批生产记录现场 状态标记 已洁净 [ ]待洁净[ ] 检查清场合格证有效: 是[ ] 否[ ]查对:品名品名: 领料 批次 批次:查对数目数目:kg桶将药装入干净晾药盘并搁置于晾切合 [ ] 不切合[ ]晾药晒间晾晒台(或架)晾药数目车kg盘晾置时间月日时分——月日时分QA 署名:项目清场要求清场结果晾合格的药连同布袋装桶置选药间 切合 [ ]不切合 [ ] 清场晾药架盘洁净 SOP 切合 [ ]不切合 [ ] 干燥剂 置干燥剂寄存室 切合 [ ]不切合 [ ] 现场岗位洁净 SOP 切合 [ ]不切合 [ ] 设备及现场状态标记改换切合 [ ]不切合 [ ]清场合格证有[] 无[ ]清场结论合格[ ]不合格[ ]检查人:QA 检查结论:QA 署名:烘药工序批生产记录产品:批号:操作步骤操作要求 操作记录操作人岗位 SOP有〔 〕否〔〕检查文件设备 SOP有〔 〕 否〔 〕 洁净 SOP 有〔 〕 否〔 〕相应记录有〔 〕否〔 〕检查设备状态完满 是〔 〕 否〔 〕有清场合格证 效:是〔 〕否〔 〕 计量用具有效性有效:是〔 〕否〔〕 校正:切合〔〕不切合〔〕现场检查状态标记 已洁净〔 〕待洁净〔 〕 清场合格证 有效:是〔 〕 否〔 〕容器的检查状态标记 已洁净〔 〕待洁净〔 〕 清场合格证有效:是〔 〕 否〔 〕领料查对:药材名:切合[]不切合[ ]切合[]不切合[ ]切合[]不切合[ ]操作人QA 检查切合〔〕不切合〔 〕切合〔〕不切合〔 〕 切合〔〕不切合〔 〕切合〔〕不切合〔 〕切合〔〕不切合〔 〕1、药材名批次:切合〔〕2、批次数目:kg 件3、数目不切合〔 〕状态标记:色 个4、状态标记干燥设备:干燥温度:℃干燥干燥后数目:kg 切合〔〕荒弃物量:kg不切合〔 〕生产时间: 月 日 时结束时间: 月 日 时晾药开始时间: 月 日 时结束时间:月 日 时项目要求检查结果清场人清场饮片置净料暂存间切合〔 〕不切合〔 〕荒弃物 置荒弃物站切合〔 〕不切合〔 〕热风循环烘箱洁净 SOP切合〔 〕不切合〔 〕容器 置容器洁净室切合〔 〕不切合〔 〕清场时间现场洁净 SOP 切合〔 〕不切合〔 〕月 日 时结论:检查人:QA :炮制(制)工序批生产记录品名:批号:操作步骤操作要求 操作记录 操作人QA 检查岗位 SOP有〔 〕否〔 〕设备 SOP有〔 〕否〔 〕符合检查文件〔 〕 洁净 SOP有〔 〕否〔 〕 不 符 合相应记录有〔 〕否〔 〕〔 〕状态完满 完 好 : 是 〔〕 否 符合 检查设备清场合格证 〔 〕有效: 是〔 〕〔〕否〔 〕 不符 合〔 〕有效:是〔〕 否 符合 计量用具有效性〔 〕〔 〕 校正:切合〔〕不切合不符 合〔 〕〔 〕状态标记 已洁净〔 〕待洁净〔 〕 符合 现场检查清场合格证 有效:是〔 〕 否〔 〕〔 〕 不符 合〔 〕 容器的检查状态标记 已洁净〔 〕待洁净〔 〕 符合 清场合格证 有效:是〔 〕 否〔 〕〔〕不符合〔〕查对:品名:4、品名批次:5、批次符合领料6、数目数目:kg 〔〕4、状态标记状态标记:□合格□不合不符合〔〕格使用设备及型炮炙方法:号:炮制(制)晾药清场结论:辅料名称:符合辅料量:kg〔〕不符合炮制后数目:kg 〔〕时间:时分 - 时分温度:开端:;过程:开始时间:月日时结束时间:月日时项目要求检查结果清场人饮片置净料暂存间符合〔〕不切合余料□置暂存间□荒弃符合〔〔〕〕不切合容器置容器洁净间符合〔〔〕〕不切合设备严格履行洁净 SOP符合〔〔〕清场时间〕不切合现场严格履行洁净 SOP符合〔〔〕〕不切合月日时〔〕检查人:QA:干燥温度、时间控制曲线图℃ 1 ℃ 2100 10090908070806050 7040603020 501040302010t 0 t 每格单位()分钟每格单位()分钟进箱时间:出箱时间:进箱时间:出箱时间:℃ 3 ℃ 41001009080 90708060705040 6030502010 40操作步骤操作要求操作记录操作人QA 检查0 t 0每格单位()分钟每格单位()分钟进箱时间:出箱时间:进箱时间:出箱时间:℃ 5 ℃ 1100 10090908070806050 7040603020 5010403020100 t 0每格单位()分钟每格单位()分钟进箱时间:出箱时间:进箱时间:出箱时间:t t检查文件检查设备计量用具工用具现场检查领料查对包装岗位 SOP设备 SOP洁净 SOP相应记录状态完满清场合格证有效性校正洁净状态标记清场合格证查对:品名批次数目包装规格/袋包材使用状况领药使用状况有[ ] 无[ ]有[ ] 无[ ]有[ ] 无[ ]有[ ] 无[ ]是[ ] 否 [ ]有效:是[ ] 否 [ ]有效:是[ ] 否 [ ]校正:切合 [ ] 不切合 [ ]是[ ] 否 [ ]已洁净[ ]待洁净[]有效:是[]否[]品名批次kg数目桶抽检 : 切合 [ ]不切合[ ]实领量套使用量套消耗量套结余量套使用量kg消耗量kg结余量kg切合[]不切合[]切合[]不切合[]切合[]不切合[]切合[]不切合[]切合[]不切合[]切合[]不切合[]切合[]不切合[]设备运行参数设备 SOP要求实质运转转/分钟产量 : 袋包装时间 :QA 署名: 月日~月日物料均衡 : A=包材实领量 +领药量B=包材使用量 +领药使用量C=包材消耗 +领药消耗 D=包材结余量 +领药结余B+C+D均衡收率 =×100%A项目清场要求工用具置工用具清洗间设备洁净 SOP清场现场岗位洁净 SOP 节余包材置暂存间包装产品置中转站状态标记设备及现场状态标记改换清场合格证清场结论合格[ ]不合格[] 清场时间年月日备注:控制:~%计算值 :评价: 切合[ ]不切合[ ] 说明:计算人 : 复核人 :清场结果操作人切合 [ ]不切合[ ]切合 [ ]不切合[ ]切合 [ ]不切合[ ]切合 [ ]不切合[ ]切合 [ ]不切合[ ]切合 [ ]不切合[ ]有[ ] 无 [ ]QA 署名:内包装工序批生产记录外包装工序批生产记录产品:批号:操作步骤操作要求操作记录操作人QA 检查检查文件岗位 SOP 有〔〕否〔〕设备 SOP 有〔〕否〔〕切合〔〕检查设备计量用具现场检查容器的检查领料包装物料均衡计算:洁净 SOP 有〔〕否〔〕相应记录有〔〕否〔〕状态完满是〔〕否〔〕有效:清场合格证是〔〕否〔〕有效性有效:是〔〕否〔〕校正:切合〔〕不切合〔〕状态标记已洁净〔〕待洁净〔〕清场合格证有效:是〔〕否〔〕状态标记已洁净〔〕待洁净〔〕清场合格证有效:是〔〕否〔〕查对:药材名:7、药材名批次:8、批次数目:kg 件9、数目状态标记:色个10、状态标志包材名称11、包材名包材数目称是〔〕否〔〕操作台封口机是〔〕否〔〕包装规格:kg/袋包装后数目:kg 件物料节余量:包材节余量:个包材残损量:个生产时间:月日时标准值: 99%--101%不切合〔〕切合〔〕不切合〔〕切合〔〕不切合〔〕切合〔〕不切合〔〕切合〔〕不切合〔〕切合〔〕不切合〔〕切合〔〕不切合〔〕kg结束时间:月日时评论:收率 =(包装后数目 +物料节余量) / 实质值:领药材总量计算人:包材均衡计算:计算人:评论:领用量=使用量+节余量+残损量项目要求检查结果清场人清场饮片置成品库切合〔〕不切合〔〕节余物料置净料暂存间切合〔〕不切合〔〕节余包材置包材库切合〔〕不切合〔〕现场洁净 SOP 切合〔〕不切合〔〕月日时结论:检查人:QA :产品进站清单品名:批次(号):总重量:kg 总件数:件进站日期:月日时分送料人:接收人:产品进站清单品名:批次(号):总重量:kg总件数:件进站日期:月日时分送料人:接收人:附到批生产记录产品进站清单品名:批次(号):总重量:kg总件数:件进站日期:月日时分送料人:接收人:附到批生产记录产品进站清单品名:批次(号):总重量:kg总件数:件进站日期:月日时分送料人:接收人:附到批生产记录产品出站清单品名:批次(号):总重量:kg总件数:件出站日期:月日时分领料人:发料人:附到批生产记录产品出站清单品名:批次(号):总重量:kg 总件数:件出站日期:月日时分领料人:发料人:附到批生产记录产品出站清单品名:批次(号):总重量:kg 总件数:件出站日期:月日时分附到批生产记录产品出站清单品名:批次(号):总重量:kg总件数:件出站日期:月日时分领料人:发料人:附到批生产记录产品出站清单品名:批次(号):总重量:kg总件数:件出站日期:月日时分领料人:发料人:附到批生产记录产品出站清单品名:批次(号):总重量:kg总件数:件出站日期:月日时分领料人:发料人:附到批生产记录原生产品名:批号:原生产品名:批号:清场合格证清场合格证(正本)(副本)清场班组:清场者署名:清场班组:清场者署名:清场日期:检查者署名:清场日期:检查者署名:有效期:有效期:原生产品名:批号:原生产品名:批号:清场合格证清场合格证(正本)(副本)清场班组:清场者署名:清场班组:清场者署名:清场日期:检查者署名:清场日期:检查者署名:有效期:有效期:清场检查记录年月日清产品名称生产批号场前生产时间班组清场内容记录清场者检查者QA 检查是残留物料及状态标记消除现场否地面、墙面无积水、无粉渣、无尘埃、是无异物否工具、容用具管道按该区洁净规程洁净是至无异物,无黏液,物见本色否设备按该设备标准操作规程中洁净规程是洁净至无浆块,无油垢,物见本色否是相关设备、环境干净整齐,物放有序否是其余:否尾料办理 ( 不合格品 ) 接续名种质检员签数目品名去处批号交接人数目误差办理单。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
复核人:
传递
交接时间
移交人
交接量
接收人
复核人
清
场
项目
要求
检查结果
清场人:
废弃物
置废弃物站
符合〔〕不符合〔〕
设备
清洁SOP
符合〔〕不符合〔〕
容器
置器具清洗间
符合〔〕不符合〔〕
清场时间:月日时
现场
清洁SOP
符合〔〕不符合〔〕
结论:
检查人:
QA:
备注:
清场合格证附背面
不符合□
月日时分---月日时分
符合□
不符合□
常温静置时间
操作人:
复核人:
3、机润
是〔〕否〔〕
压力
Pa
设定温度
℃
润药锅次
投料量kg/锅
开始时间
结束时间
法检查
检查结果
符合□
不符合□
符合□
不符合□
符合□
不符合□
符合□
不符合□
符合□
不符合□
符合□
不符合□
符合□
不符合□
符合□
不符合□
符合□
不符合□
符合□
不符合□
XXXXXXXXXX
洗、润工序生产记录
生产日期:年月日编号:
产品名称
代码
规格
批号
生产指令单号
生
产
前
检
查
操作要求
执行情况
操作人
QA
1、个人卫生、工衣着装符合要求
2、是否有生产指令、岗位SOP
3、清场合格证是否在效期内
4、设备、工具、用具、容器应完好洁净,状态标志符合要求
5、计量器具校验合格证是否在效期内
是〔〕否〔〕
2、用流动水
是〔〕否〔〕
洗药时间
法检查
检查结果
月日时分---月日时分
符合□
不符合□
月日时分---月日时分
符合□
不符合□
月日时分---月日时分
符合□
不符合□
月日时分---月日时分
符合□
不符合□
月日时分---月日时分
符合□
不符合□
月日时分---月日时分
符合□
不符合□
月日时分---月日时分
符合□
操作人:
复核人:
4、闷润
kg/次
不符合□
符合□
不符合□
符合□
不符合□
符合□
不符合□
符合□
不符合□
符合□
不符合□
符合□
不符合□
操作人:
复核人:
5、浸泡
kg/次
开始时间
结束时间
法检查
检查结果
符合□
不符合□
符合□
不符合□
符合□
不符合□
符合□
不符合□
符合□
不符合□
洗、润后数量:kg
6、核对物料名称、编码、规格、数量
7、生产用水符合要求
1、是□否□
2、是□否□
3、是□否□
4、是□否□
5、是□否□
6、是□否□
7、是□否□
生
产
操
作
领料
药材名
编码
数量(kg)
操作人
复核人
洗
润
洗、润方法
机洗〔〕淋润〔〕枪洗〔〕漂〔〕机润〔〕闷润〔〕浸泡〔〕抢水洗〔〕
主要设备
设备编号
主要设备
设备编号
1、在洗药机
