实验室常用溶剂的化学位移
常用氘代溶剂和杂质峰在1H谱中的化学位移

常用氘代溶剂和杂质峰在1H谱中的化学位移测试核磁的样品一般要求比较纯,并且能够溶解在氘代试剂中,这样才能测得高分辨率的图谱。
为不干扰谱图,所用溶剂分子中的氢都应被氘取代,但难免有氢的残余(1%左右),这样就会产生溶剂峰;除了残存的质子峰外,溶剂中有时会有微量的H2O而产生水峰,而且这个H2O峰的位置也会因溶剂的不同而不同;另外,在样品(或制备过程)中,也难免会残留一些杂质,在图谱上就会有杂质峰,应注意识别。
以下给出了一些常见溶剂峰和杂质峰的化学位移:常用氘代溶剂和杂质峰在1H谱中的化学位移单位:ppm溶剂—CDCl3 (CD3)2CO (CD3)2SO C6D6 CD3CN CD3OH D2O溶剂峰—7.26 2.05 2.49 7.16 1.94 3.31 4.80水峰— 1.56 2.84 3.33 0.40 2.13 4.87 —乙酸— 2.10 1.96 1.91 1.55 1.96 1.99 2.08丙酮— 2.17 2.09 2.09 1.55 2.08 2.15 2.22乙腈— 2.10 2.05 2.07 1.55 1.96 2.03 2.06苯—7.36 7.36 7.37 7.15 7.37 7.33 —叔丁醇CH3 1.28 1.18 1.11 1.05 1.16 1.40 1.24OH —— 4.19 1.55 2.18 ——叔丁基甲醚CCH3 1.19 1.13 1.11 1.07 1.14 1.15 1.21OCH3 3.22 3.13 3.08 3.04 3.13 3.20 3.22氯仿—7.26 8.02 8.32 6.15 7.58 7.90 —环己烷— 1.43 1.43 1.40 1.40 1.44 1.45 —1,2-二氯甲烷 3.73 3.87 3.90 2.90 3.81 3.78 —二氯甲烷— 5.30 5.63 5.76 4.27 5.44 5.49 —乙醚CH3(t) 1.21 1.11 1.09 1.11 1.12 1.18 1.17CH2(q) 3.48 3.41 3.38 3.26 3.42 3.49 3.56二甲基甲酰胺CH 8.02 7.96 7.95 7.63 7.92 7.79 7.92CH3 2.96 2.94 2.89 2.36 2.89 2.99 3.01CH3 2.88 2.78 2.73 1.86 2.77 2.86 2.85二甲基亚砜— 2.62 2.52 2.54 1.68 2.50 2.65 2.71二氧杂环— 3.71 3.59 3.57 3.35 3.60 3.66 3.75乙醇CH3(t) 1.25 1.12 1.06 0.96 1.12 1.19 1.17CH2(q) 3.72 3.57 3.44 3.34 3.54 3.60 3.65OH(s) 1.32 3.39 3.63 — 2.47 ——乙酸乙酯CH3CO 2.05 1.97 1.99 1.65 1.97 2.01 2.07OCH2(q) 4.12 4.05 4.03 3.89 4.06 4.09 4.14CH3(t) 1.26 1.20 1.17 0.92 1.20 1.24 1.24甲乙酮CH3CO 2.14 2.07 2.07 1.58 2.06 2.12 2.19CH2(q) 2.46 2.45 2.43 1.81 2.43 2.50 3.18CH3(t) 1.06 0.96 0.91 0.85 0.96 1.01 1.26乙二醇— 3.76 3.28 3.34 3.41 3.51 3.59 3.65润滑脂CH3(m) 0.86 0.87 —0.92 0.86 0.88 —CH2(br) 1.26 1.29 — 1.36 1.27 1.29 —正己烷CH3(t) 0.88 0.88 0.86 0.89 0.89 0.90 —CH2 (m) 1.26 1.28 1.25 1.24 1.28 1.29 —甲醇CH3 3.49 3.31 3.16 3.07 3.28 3.34 3.34 OH 1.09 3.12 4.01 2.16 ——正戊烷CH3(t) 0.88 0.88 0.86 0.87 0.89 0.90 —CH2(m) 1.27 1.27 1.27 1.23 1.29 1.29 —异丙醇CH3(d) 1.22 1.10 1.04 0.95 1.09 1.50 1.17 CH 4.04 3.90 3.78 3.67 3.87 3.92 4.02硅脂—0.07 0.13 —0.29 0.08 0.10 —四氢呋喃CH2 1.85 1.79 1.76 1.40 1.80 1.87 1.88 CH2O 3.76 3.63 3.60 3.57 3.64 3.71 3.74甲苯CH3 2.36 2.32 2.30 2.11 2.33 2.32 —CH(o/p)7.17 7.20 7.18 7.02 7.30 7.16 —CH(m)7.25 7.20 7.25 7.13 7.30 7.16 —三乙基胺CH3 1.03 0.96 0.93 0.96 0.96 1.05 0.99 CH2 2.53 2.45 2.43 2.40 2.45 2.58 2.57石油醚—0.5-1.5 0.6-1.9 —————。
溶剂峰化学位移表__解释说明以及概述

溶剂峰化学位移表解释说明以及概述1. 引言1.1 概述溶剂峰化学位移表是有机化学中一个重要的参考工具,用于研究和识别在核磁共振(NMR)光谱中出现的溶剂峰。
在有机合成和结构鉴定等领域,正确解读溶剂峰化学位移对准确确定分子结构起着至关重要的作用。
因此,我们需要深入了解并掌握溶剂峰化学位移表的使用方法。
1.2 文章结构本文将从以下几个方面对溶剂峰化学位移表进行解释说明和概述:- 第2部分将解释定义溶剂峰化学位移,以及影响其数值的因素,并介绍计算这一参数的方法。
- 第3部分将详细阐述如何使用溶剂峰化学位移表,并提供一些范例解析。
同时,还将介绍在有机合成中应用该数据的实际案例,以及常见溶剂的峰化学位移数据。
- 第4部分将讨论溶剂峰化学位移表存在的局限性和问题,并提出改进方法来提高其可靠性和应用价值。
- 最后,在第5部分中我们将对全文进行总结,并展望溶剂峰化学位移表的发展和应用前景。
1.3 目的本文的目的是帮助读者深入理解溶剂峰化学位移表,并掌握准确使用该表以解读NMR光谱中的溶剂峰。
同时,我们还将讨论溶剂峰化学位移表存在的局限性,并提出改进方法来提高其可靠性与应用价值。
期望本文能对有机化学研究者、有机合成领域从业人员以及相关科研工作者提供有益的参考信息。
2. 溶剂峰化学位移表的解释说明2.1 溶剂峰化学位移的定义溶剂峰化学位移是指在核磁共振(NMR)光谱中,由于不同溶剂对样品的影响而导致的化学位移变化。
每种溶剂都会产生一个特定的峰,其化学位移值可以作为溶剂信号进行测量和分析。
2.2 影响溶剂峰化学位移的因素溶剂峰化学位移受多种因素影响,包括物理性质、磁性等。
其中一些可能影响峰位置和强度以及NMR光谱形状的因素包括普透明度、离子强度、极性、粘度、重金属离子污染等。
2.3 计算溶剂峰化学位移的方法计算溶剂峰化学位移常使用参考标准物质与待测样品进行比较。
通过测量已知标准物质并确定其相对于参考峰位置的差距,可以计算待测样品中各个组分的相对位置。
溶剂峰化学位移

溶剂峰化学位移
溶剂峰化学位移(Solvent Peak Chemical Shift,简称SPCS)是指在核磁共振实验中发生的现象,它表明溶剂对核磁共振信号的影响可以产生有意义的化学位移。
由于溶剂对基团的极化作用的存在,基团原子的化学位置会发生变化,导致核磁共振信号随着溶剂改变而发生化学位移。
溶剂峰化学位移又称为线性化学位移(Linear Chemical Shift),按照物质形成的三维结构改变而改变的定义,可以将溶剂峰化学位移定义为有序变化化学位移。
因此,溶剂峰化学位移是一种有比较整齐的曲线,在某一原子化学位置上有一峰值,然后随着溶剂不同改变而发生有规律的化学位移。
溶剂峰化学位移的有效性及应用受到诸多因素的影响,包括基团原子的结构、形位和互变异构体配位以及尺寸变化换位的影响,对基团的位置极化的影响,和溶剂的离子手性的影响等。
特别是当基团量子效应出现时,溶剂峰化学位移就会发生较大的变化,包括轴向和同种溶剂上不同峰值等。
比较典型的溶剂峰化学位移情形有水平型、P-键、K抛物线型及曲线型等。
溶剂峰化学位移在聚合物相互作用研究、合成化学及活性立体化学等方面都有着广泛的应用。
当同一种原子组成不同**、优势体系或歪斜取向时,其随溶剂改变而发生的化学位移可以清楚的反映出来。
此外,溶剂峰化学位移可以用于判断多种结构的立体位置,或用来分析整个基团结构的改变。
因此,溶剂峰化学位移在核磁共振实验中是一种常用而有效的方法,为理解物质结构及相互作用提供了重要的技术保障。
常见核磁氢谱位移

常见核磁氢谱位移
核磁氢谱中的化学位移是衡量分子中氢原子特性的重要参数。
以下是常见的核磁氢谱位移:
1.烷基(烷烃):通常位于0-3 ppm范围内,如甲基(CH3)的化学位移约
为0.9 ppm。
2.烯烃:通常位于4.5-6.5 ppm范围内,如乙烯(CH2=CH2)的化学位移约
为5.5 ppm。
3.脂肪醇:通常位于0.5-5 ppm范围内,如乙醇(CH3CH2OH)的化学位移
约为1.3 ppm。
4.芳香族化合物:通常位于6.5-8.0 ppm范围内,如苯(C6H6)的化学位移
约为7.3 ppm。
5.活泼氢:通常位于10-14 ppm范围内,如羧酸中的羧基(-COOH)的化学
位移约为13 ppm。
需要注意的是,不同官能团的化学位移具有一定的特征性,但也会因分子结构和其他因素而有所变化。
因此,在实际应用中,需要根据具体分子结构和其他测试数据进行综合分析。
h谱常见试剂化学位移

h谱常见试剂化学位移化学位移是一种研究化学反应中原子或分子位置变化的重要手段。
在化学反应中,原子或分子之间的化学键发生改变,导致它们的位置发生移动。
化学位移可以帮助我们理解化学反应的机理,并用于解释反应速率、平衡常数等热力学和动力学性质。
本文将介绍化学位移的一些常见试剂。
一、氢代试剂(Hydrogenating reagents)氢代试剂被广泛应用于有机合成中,它们能够将双键加氢转化为单键。
常见的氢代试剂包括氢气(H2)、硼氢化钠(NaBH4)和氢化锂(LiAlH4)等。
1. 氢气(H2):氢气是最常用的氢代试剂之一,它可以和许多有机物反应,如加入含双键的烯烃或芳香族化合物,发生加氢反应生成饱和化合物。
例如,乙烯与氢气在催化剂的存在下反应,生成乙烷。
2. 硼氢化钠(NaBH4):硼氢化钠是一种选择性较弱的还原剂,常用于还原醛、酮、羰基酸酯等功能团,并形成相应的醇或胺化合物。
例如,对于醛,NaBH4会与醛中的羰基氧进行反应,生成相应的醇。
3. 氢化锂(LiAlH4):氢化锂是一种强还原剂,可用于还原醛、酮、酰氯等化合物,生成相应的醇、胺或醚。
与硼氢化钠相比,氢化锂的反应条件更为严苛。
例如,丙酮可以与LiAlH4反应生成丙醇。
二、溴代试剂(Brominating reagents)溴代试剂在有机合成中可用于引入溴原子。
它们通常以有机铯盐为催化剂,反应选择性高,速度较快。
常见的溴代试剂有氯化次丁基铯(CsCl)和硫脲基溴盐(NBS)等。
1. 氯化次丁基铯(CsCl):氯化次丁基铯广泛用于上氯酮的亲核取代反应。
它与溴或氯发生置换反应,引入溴原子。
例如,原醇与氯化次丁基铯反应,生成相应的氯代醇。
2. 硫脲基溴盐(NBS):硫脲基溴盐是一种常用的溴代试剂,它可以与氯代烃反应,生成相应的溴代烃。
NBS在反应中同时作为溴源和氧化剂。
例如,正丁基氯可以与NBS反应,生成溴代正丁烷。
三、氰基试剂(Cyanating reagents)氰基试剂可以将氰基引入有机化合物中,通过亲核取代反应进行。
常用氘代溶剂和杂质峰在1H谱中的化学位移

常用氘代溶剂和杂质峰在1H谱中的化学位移测试核磁的样品一般要求比较纯,并且能够溶解在氘代试剂中,这样才能测得高分辨率的图谱。
为不干扰谱图,所用溶剂分子中的氢都应被氘取代,但难免有氢的残余(1%左右),这样就会产生溶剂峰;除了残存的质子峰外,溶剂中有时会有微量的H2O而产生水峰,而且这个H2O峰的位置也会因溶剂的不同而不同;另外,在样品(或制备过程)中,也难免会残留一些杂质,在图谱上就会有杂质峰,应注意识别。
以下给出了一些常见溶剂峰和杂质峰的化学位移:常用氘代溶剂和杂质峰在1H谱中的化学位移单位:ppm溶剂—CDCl3 (CD3)2CO (CD3)2SO C6D6 CD3CN CD3OH D2O溶剂峰—7.26 2.05 2.49 7.16 1.94 3.31 4.80 水峰— 1.56 2.84 3.33 0.40 2.13 4.87 —乙酸— 2.10 1.96 1.91 1.55 1.96 1.99 2.08 丙酮— 2.17 2.09 2.09 1.55 2.08 2.15 2.22 乙腈— 2.10 2.05 2.07 1.55 1.96 2.03 2.06 苯—7.36 7.36 7.37 7.15 7.37 7.33 —叔丁醇CH3 1.28 1.18 1.11 1.05 1.16 1.40 1.24 OH —— 4.19 1.55 2.18 ——叔丁基甲醚CCH3 1.19 1.13 1.11 1.07 1.14 1.15 1.2 1OCH3 3.22 3.13 3.08 3.04 3.13 3.20 3.22 氯仿—7.26 8.02 8.32 6.15 7.58 7.90 —环己烷— 1.43 1.43 1.40 1.40 1.44 1.45 —1,2-二氯甲烷 3.73 3.87 3.90 2.90 3.81 3.78 —二氯甲烷— 5.30 5.63 5.76 4.27 5.44 5.49 —乙醚CH3(t) 1.21 1.11 1.09 1.11 1.12 1.18 1.17CH2(q) 3.48 3.41 3.38 3.26 3.42 3.49 3.56 二甲基甲酰胺CH 8.02 7.96 7.95 7.63 7.92 7.79 7.92 CH3 2.96 2.94 2.89 2.36 2.89 2.99 3.01CH3 2.88 2.78 2.73 1.86 2.77 2.86 2.85二甲基亚砜— 2.62 2.52 2.54 1.68 2.50 2.65 2.71 二氧杂环— 3.71 3.59 3.57 3.35 3.60 3.66 3.75 乙醇CH3(t) 1.25 1.12 1.06 0.96 1.12 1.19 1.17CH2(q) 3.72 3.57 3.44 3.34 3.54 3.60 3.65 OH(s) 1.32 3.39 3.63 — 2.47 ——乙酸乙酯CH3CO 2.05 1.97 1.99 1.65 1.97 2.01 2.07OCH2(q) 4.12 4.05 4.03 3.89 4.06 4.09 4.1 4CH3(t) 1.26 1.20 1.17 0.92 1.20 1.24 1.24 甲乙酮CH3CO 2.14 2.07 2.07 1.58 2.06 2.12 2.19CH2(q) 2.46 2.45 2.43 1.81 2.43 2.50 3.18 CH3(t) 1.06 0.96 0.91 0.85 0.96 1.01 1.26 乙二醇— 3.76 3.28 3.34 3.41 3.51 3.59 3.65 润滑脂CH3(m) 0.86 0.87 —0.92 0.86 0.88 —CH2(br) 1.26 1.29 — 1.36 1.27 1.29 —正己烷CH3(t) 0.88 0.88 0.86 0.89 0.89 0.90 —CH2 (m) 1.26 1.28 1.25 1.24 1.28 1.29 —甲醇CH3 3.49 3.31 3.16 3.07 3.28 3.34 3.34 OH 1.09 3.12 4.01 2.16 ——正戊烷CH3(t) 0.88 0.88 0.86 0.87 0.89 0.90 —CH2(m) 1.27 1.27 1.27 1.23 1.29 1.29 —异丙醇CH3(d) 1.22 1.10 1.04 0.95 1.09 1.50 1.17CH 4.04 3.90 3.78 3.67 3.87 3.92 4.02硅脂—0.07 0.13 —0.29 0.08 0.10 —四氢呋喃CH2 1.85 1.79 1.76 1.40 1.80 1.87 1.88 CH2O 3.76 3.63 3.60 3.57 3.64 3.71 3.74 甲苯CH3 2.36 2.32 2.30 2.11 2.33 2.32 —CH(o/p)7.17 7.20 7.18 7.02 7.30 7.16 —CH(m)7.25 7.20 7.25 7.13 7.30 7.16 —三乙基胺CH3 1.03 0.96 0.93 0.96 0.96 1.05 0.99 CH2 2.53 2.45 2.43 2.40 2.45 2.58 2.57 石油醚—0.5-1.5 0.6-1.9 ————常见溶剂的化学位移常见溶剂的1H在不同氘代溶剂中的化学位移值常见溶剂的化学位移常见溶剂的13C在不同氘代溶剂中的化学位移值。
常见物质化学位移

常见物质化学位移常见物质化学位移化学位移是指发生化学反应后,原子核在磁场中的共振吸收现象被感应出来的电磁波信号频率改变的数值,是核磁共振(NMR)技术中的一项重要指标。
在物质的研究中,化学位移常常作为检测手段使用,可以对物质的结构、状态以及反应进行有效的探测和表征。
在此,本文将对常见物质化学位移进行阐述。
1. 溶液中极性分子的化学位移当氢原子所处的物质环境有所改变时,其核磁共振信号出现的频率也会随之改变。
在溶液中,极性分子与溶剂之间的相互作用会影响分子内氢原子的化学位移,使其发生变化。
举例来说,对于分子量较小的甲酸,其氢原子的化学位移在不同溶剂中会产生不同的位移,主要是甲基基团与溶剂之间的相互作用的差异造成的。
2. 烷基取代的化学位移在烷烃分子中,烷基的取代会对周围其它分子产生影响,导致氢原子的化学位移发生变化。
通常,烷基取代的化学位移存在两种不同模式,即α-和β-模式。
α-模式的原理是基于烷基取代后其α-碳原子的影响。
在α-位取代的烷烃中,与α-碳原子相邻的氢原子的化学位移会发生变化。
在β-模式中,取代烷基的β-碳原子对氢原子的化学位移产生影响。
3. 分子啤酒取代的化学位移啤酒烷分子(cycloalkanes)是一类含有分子环的有机分子。
与烷基取代类似,分子环的取代也会造成氢原子的化学位移改变。
分子啤酒取代的化学位移在分子中分为内核和外围晶体两类。
内核的化学位移是由于分子环结构对氢原子化学位移的影响,而外围晶体则是由于邻域结构发生变化。
4. 芳香环的化学位移芳香环(aromatic rings)中的氢原子通常具有较高的化学位移,且与烷基取代有所不同。
这种现象是由于芳香环结构导致氢原子在芳香性环境中的存活时间长,进而导致化学位移的增加。
在芳香环中,邻位上的氢原子化学位移大于对位和间位。
综上所述,化学位移在物质的结构和状态表征中具有重要的作用,掌握物质化学位移的常见模式和机制对于物质的研究和开发具有非常重要的意义。
在不同溶剂中氢谱位移

在不同溶剂中氢谱位移
氢谱位移是指氢原子在分子中的化学位移,常用化学位移(δ)
表示。
不同的溶剂会影响化学位移的大小和位置,下面我们将从几种常见的溶剂出发,探讨氢谱位移的变化。
1. 水溶液中的氢谱位移
水是最常用的氢谱溶剂之一,它对氢谱位移的影响比较大。
水分子的氧原子含有两个孤对电子,因此它具有强烈的电负性。
当氢原子靠近水分子时,它们会受到水分子的电子云吸引,导致氢原子的化学位移变大。
此外,在水中还可能出现氢键作用,这种作用会使氢谱位移更加复杂。
2. 有机溶剂中的氢谱位移
有机溶剂是常用的氢谱溶剂之一,如甲醇、乙醇、二氯甲烷等。
它们的分子结构中有许多不同的官能团,这些官能团可以对氢原子的化学位移产生影响。
例如,当有机溶剂中含有羟基(-OH)官能团时,它们会使氢原子的化学位移变大。
而存在醇羟基(-C-OH)官能团时,会使得氢原子的化学位移变小。
3. 脂类溶剂中的氢谱位移
脂类溶剂是指一类具有较长的碳链的物质,如正己烷、氯仿等。
这些溶剂中的氢原子受到溶剂分子内部的共振效应的影响,其化学位移会出现位移,且具有一定的规律性。
因此,在脂类溶剂中进行氢谱分析时,需要考虑到这种共振效应的影响,以便准确地确定化学位移。
总之,不同的溶剂会对氢谱位移产生不同的影响,这些影响需要
在氢谱分析中得到合理的考虑和处理。
常见溶剂化学位移

C
69.15
68.13
66.88
68.19
68.74
69.4
70.36
CH3
3125
3072
3038
3047
3068
3091
3029
氯仿
CH
77.36
79.19
79.16
77.79
79.17
79.44
环己烷
CH2
26.94
27.51
26.33
27.23
27.63
27.96
1.2-二氯乙烷
CH2
Sh
3.49
3.31
3.16
3.07
3.28
3.34
3.34
OH
Sgh
1.09
3.12
4.01
2.16
吡啶
CH(2)
m
8.62
8.58
8.58
8.53
8.57
8.53
8.52
CH(3)
m
7.29
7.35
7.39
6.66
7.33
7.44
7.45
CH(4)
m
7.68
7.76
7.79
6.98
7.73
7.85
CO
171.36
170.96
170.31
170.44
171.68
172.89
175.26
CH2
60.49
60.56
59.74
60.21
60.98
61.5
62.32
CH3
1419
145
144
1419
常用氘代溶剂和杂质峰在1H谱中的化学位移
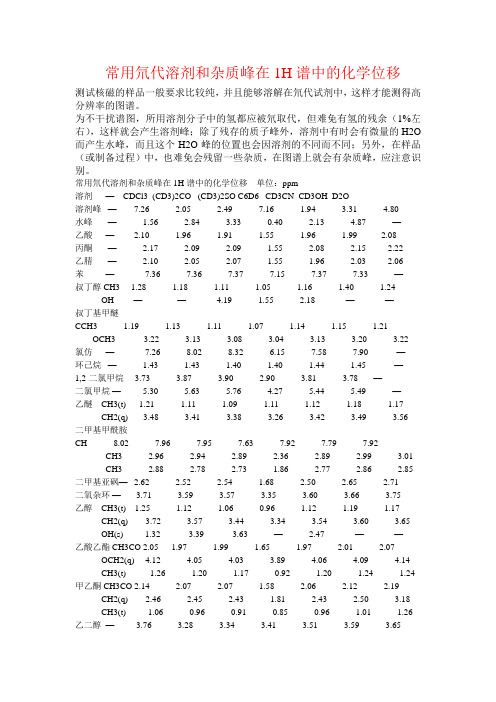
常用氘代溶剂和杂质峰在1H谱中的化学位移测试核磁的样品一般要求比较纯,并且能够溶解在氘代试剂中,这样才能测得高分辨率的图谱。
为不干扰谱图,所用溶剂分子中的氢都应被氘取代,但难免有氢的残余(1%左右),这样就会产生溶剂峰;除了残存的质子峰外,溶剂中有时会有微量的H2O 而产生水峰,而且这个H2O峰的位置也会因溶剂的不同而不同;另外,在样品(或制备过程)中,也难免会残留一些杂质,在图谱上就会有杂质峰,应注意识别。
常用氘代溶剂和杂质峰在1H谱中的化学位移单位:ppm溶剂—CDCl3 (CD3)2CO (CD3)2SO C6D6 CD3CN CD3OH D2O溶剂峰—7.26 2.05 2.49 7.16 1.94 3.31 4.80水峰— 1.56 2.84 3.33 0.40 2.13 4.87 —乙酸— 2.10 1.96 1.91 1.55 1.96 1.99 2.08丙酮— 2.17 2.09 2.09 1.55 2.08 2.15 2.22乙腈— 2.10 2.05 2.07 1.55 1.96 2.03 2.06 苯—7.36 7.36 7.37 7.15 7.37 7.33 —叔丁醇CH3 1.28 1.18 1.11 1.05 1.16 1.40 1.24 OH —— 4.19 1.55 2.18 ——叔丁基甲醚CCH3 1.19 1.13 1.11 1.07 1.14 1.15 1.21 OCH3 3.22 3.13 3.08 3.04 3.13 3.20 3.22氯仿—7.26 8.02 8.32 6.15 7.58 7.90 —环己烷— 1.43 1.43 1.40 1.40 1.44 1.45 —1,2-二氯甲烷 3.73 3.87 3.90 2.90 3.81 3.78 —二氯甲烷— 5.30 5.63 5.76 4.27 5.44 5.49 —乙醚 CH3(t) 1.21 1.11 1.09 1.11 1.12 1.18 1.17 CH2(q) 3.48 3.41 3.38 3.26 3.42 3.49 3.56二甲基甲酰胺CH 8.02 7.96 7.95 7.63 7.92 7.79 7.92 CH3 2.96 2.94 2.89 2.36 2.89 2.99 3.01CH3 2.88 2.78 2.73 1.86 2.77 2.86 2.85 二甲基亚砜— 2.62 2.52 2.54 1.68 2.50 2.65 2.71二氧杂环— 3.71 3.59 3.57 3.35 3.60 3.66 3.75乙醇 CH3(t) 1.25 1.12 1.06 0.96 1.12 1.19 1.17 CH2(q) 3.72 3.57 3.44 3.34 3.54 3.60 3.65OH(s) 1.32 3.39 3.63 — 2.47 ——乙酸乙酯CH3CO 2.05 1.97 1.99 1.65 1.97 2.01 2.07 OCH2(q) 4.12 4.05 4.03 3.89 4.06 4.09 4.14CH3(t) 1.26 1.20 1.17 0.92 1.20 1.24 1.24 甲乙酮CH3CO 2.14 2.07 2.07 1.58 2.06 2.12 2.19 CH2(q) 2.46 2.45 2.43 1.81 2.43 2.50 3.18CH3(t) 1.06 0.96 0.91 0.85 0.96 1.01 1.26 乙二醇— 3.76 3.28 3.34 3.41 3.51 3.59 3.65润滑脂 CH3(m) 0.86 0.87 —0.92 0.86 0.88 —CH2(br) 1.26 1.29 — 1.36 1.27 1.29 —正己烷CH3(t) 0.88 0.88 0.86 0.89 0.89 0.90 —CH2 (m) 1.26 1.28 1.25 1.24 1.28 1.29 —甲醇CH3 3.49 3.31 3.16 3.07 3.28 3.34 3.34 OH 1.09 3.12 4.01 2.16 ——正戊烷 CH3(t) 0.88 0.88 0.86 0.87 0.89 0.90 —CH2(m) 1.27 1.27 1.27 1.23 1.29 1.29 —异丙醇CH3(d) 1.22 1.10 1.04 0.95 1.09 1.50 1.17 CH 4.04 3.90 3.78 3.67 3.87 3.92 4.0 2硅脂—0.07 0.13 —0.29 0.08 0.10 —四氢呋喃 CH2 1.85 1.79 1.76 1.40 1.80 1.87 1.88 CH2O 3.76 3.63 3.60 3.57 3.64 3.71 3.74 甲苯 CH3 2.36 2.32 2.30 2.11 2.33 2.32 —CH(o/p)7.17 7.20 7.18 7.02 7.30 7.16 —CH(m) 7.25 7.20 7.25 7.13 7.30 7.16 —三乙基胺 CH3 1.03 0.96 0.93 0.96 0.96 1.05 0.99 CH2 2.53 2.45 2.43 2.40 2.45 2.58 2.57 石油醚—0.5-1.5 0.6-1.9 —————。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
NMR Chemical Shifts of Common Laboratory Solvents as Trace Impurities Hugo E.Gottlieb,*Vadim Kotlyar,andAbraham Nudelman*Department of Chemistry,Bar-Ilan University,Ramat-Gan52900,IsraelReceived June27,1997In the course of the routine use of NMR as an aid for organic chemistry,a day-to-day problem is the identifica-tion of signals deriving from common contaminants (water,solvents,stabilizers,oils)in less-than-analyti-cally-pure samples.This data may be available in the literature,but the time involved in searching for it may be considerable.Another issue is the concentration dependence of chemical shifts(especially1H);results obtained two or three decades ago usually refer to much more concentrated samples,and run at lower magnetic fields,than today’s practice.We therefore decided to collect1H and13C chemical shifts of what are,in our experience,the most popular “extra peaks”in a variety of commonly used NMR solvents,in the hope that this will be of assistance to the practicing chemist.Experimental SectionNMR spectra were taken in a Bruker DPX-300instrument (300.1and75.5MHz for1H and13C,respectively).Unless otherwise indicated,all were run at room temperature(24(1°C).For the experiments in the last section of this paper,probe temperatures were measured with a calibrated Eurotherm840/T digital thermometer,connected to a thermocouple which was introduced into an NMR tube filled with mineral oil to ap-proximately the same level as a typical sample.At each temperature,the D2O samples were left to equilibrate for at least 10min before the data were collected.In order to avoid having to obtain hundreds of spectra,we prepared seven stock solutions containing approximately equal amounts of several of our entries,chosen in such a way as to prevent intermolecular interactions and possible ambiguities in assignment.Solution1:acetone,tert-butyl methyl ether,di-methylformamide,ethanol,toluene.Solution2:benzene,di-methyl sulfoxide,ethyl acetate,methanol.Solution3:acetic acid,chloroform,diethyl ether,2-propanol,tetrahydrofuran. Solution4:acetonitrile,dichloromethane,dioxane,n-hexane, HMPA.Solution5:1,2-dichloroethane,ethyl methyl ketone, n-pentane,pyridine.Solution6:tert-butyl alcohol,BHT,cyclo-hexane,1,2-dimethoxyethane,nitromethane,silicone grease, triethylamine.Solution7:diglyme,dimethylacetamide,ethyl-ene glycol,“grease”(engine oil).For D2O.Solution1:acetone, tert-butyl methyl ether,dimethylformamide,ethanol,2-propanol. Solution2:dimethyl sulfoxide,ethyl acetate,ethylene glycol, methanol.Solution3:acetonitrile,diglyme,dioxane,HMPA, pyridine.Solution4:1,2-dimethoxyethane,dimethylacetamide, ethyl methyl ketone,triethylamine.Solution5:acetic acid,tert-butyl alcohol,diethyl ether,tetrahydrofuran.In D2O and CD3OD nitromethane was run separately,as the protons exchanged with deuterium in presence of triethylamine.ResultsProton Spectra(Table1).A sample of0.6mL of the solvent,containing1µL of TMS,1was first run on its own.From this spectrum we determined the chemical shifts of the solvent residual peak2and the water peak. It should be noted that the latter is quite temperature-dependent(vide infra).Also,any potential hydrogen-bond acceptor will tend to shift the water signal down-field;this is particularly true for nonpolar solvents.In contrast,in e.g.DMSO the water is already strongly hydrogen-bonded to the solvent,and solutes have only a negligible effect on its chemical shift.This is also true for D2O;the chemical shift of the residual HDO is very temperature-dependent(vide infra)but,maybe counter-intuitively,remarkably solute(and pH)independent. We then added3µL of one of our stock solutions to the NMR tube.The chemical shifts were read and are presented in Table 1.Except where indicated,the coupling constants,and therefore the peak shapes,are essentially solvent-independent and are presented only once.For D2O as a solvent,the accepted reference peak(δ)0)is the methyl signal of the sodium salt of3-(trimeth-ylsilyl)propanesulfonic acid;one crystal of this was added to each NMR tube.This material has several disadvan-tages,however:it is not volatile,so it cannot be readily eliminated if the sample has to be recovered.In addition, unless one purchases it in the relatively expensive deuterated form,it adds three more signals to the spectrum(methylenes1,2,and3appear at2.91,1.76, and0.63ppm,respectively).We suggest that the re-sidual HDO peak be used as a secondary reference;we find that if the effects of temperature are taken into account(vide infra),this is very reproducible.For D2O, we used a different set of stock solutions,since many of the less polar substrates are not significantly water-soluble(see Table1).We also ran sodium acetate and sodium formate(chemical shifts: 1.90and8.44ppm, respectively).Carbon Spectra(Table2).To each tube,50µL of the stock solution and3µL of TMS1were added.The solvent chemical shifts3were obtained from the spectra containing the solutes,and the ranges of chemical shifts(1)For recommendations on the publication of NMR data,see: IUPAC Commission on Molecular Structure and Spectroscopy.Pure Appl.Chem.1972,29,627;1976,45,217.(2)I.e.,the signal of the proton for the isotopomer with one less deuterium than the perdeuterated material,e.g.,C H Cl3in CDCl3or C6D5H in C6D6.Except for CHCl3,the splitting due to J HD is typically observed(to a good approximation,it is1/6.5of the value of the corresponding J HH).For CHD2groups(deuterated acetone,DMSO, acetonitrile),this signal is a1:2:3:2:1quintet with a splitting of ca.2 Hz.(3)In contrast to what was said in note2,in the13C spectra the solvent signal is due to the perdeuterated isotopomer,and the one-bond couplings to deuterium are always observable(ca.20-30Hz). Figure1.Chemical shift of H DO as a function of tempera-ture..Chem.1997,62,7512-7515S0022-3263(97)01176-6CCC:$14.00©1997American Chemical Societyshow their degree of variability.Occasionally,in order to distinguish between peaks whose assignment was ambiguous,a further1-2µL of a specific substrate were added and the spectra run again.Table1.1H NMR Dataproton mult CDCl3(CD3)2CO(CD3)2SO C6D6CD3CN CD3OD D2O solvent residual peak7.26 2.05 2.507.16 1.94 3.31 4.79 H2O s 1.56 2.84a 3.33a0.40 2.13 4.87acetic acid CH3s 2.10 1.96 1.91 1.55 1.96 1.99 2.08 acetone CH3s 2.17 2.09 2.09 1.55 2.08 2.15 2.22 acetonitrile CH3s 2.10 2.05 2.07 1.55 1.96 2.03 2.06 benzene CH s7.367.367.377.157.377.33tert-butyl alcohol CH3s 1.28 1.18 1.11 1.05 1.16 1.40 1.24 OH c s 4.19 1.55 2.18tert-butyl methyl ether CCH3s 1.19 1.13 1.11 1.07 1.14 1.15 1.21 OCH3s 3.22 3.13 3.08 3.04 3.13 3.20 3.22 BHT b ArH s 6.98 6.96 6.877.05 6.97 6.92OH c s 5.01 6.65 4.79 5.20ArCH3s 2.27 2.22 2.18 2.24 2.22 2.21ArC(CH3)3s 1.43 1.41 1.36 1.38 1.39 1.40chloroform CH s7.268.028.32 6.157.587.90 cyclohexane CH2s 1.43 1.43 1.40 1.40 1.44 1.451,2-dichloroethane CH2s 3.73 3.87 3.90 2.90 3.81 3.78 dichloromethane CH2s 5.30 5.63 5.76 4.27 5.44 5.49diethyl ether CH3t,7 1.21 1.11 1.09 1.11 1.12 1.18 1.17 CH2q,7 3.48 3.41 3.38 3.26 3.42 3.49 3.56 diglyme CH2m 3.65 3.56 3.51 3.46 3.53 3.61 3.67 CH2m 3.57 3.47 3.38 3.34 3.45 3.58 3.61OCH3s 3.39 3.28 3.24 3.11 3.29 3.35 3.37 1,2-dimethoxyethane CH3s 3.40 3.28 3.24 3.12 3.28 3.35 3.37 CH2s 3.55 3.46 3.43 3.33 3.45 3.52 3.60 dimethylacetamide CH3CO s 2.09 1.97 1.96 1.60 1.97 2.07 2.08 NCH3s 3.02 3.00 2.94 2.57 2.96 3.31 3.06NCH3s 2.94 2.83 2.78 2.05 2.83 2.92 2.90 dimethylformamide CH s8.027.967.957.637.927.977.92 CH3s 2.96 2.94 2.89 2.36 2.89 2.99 3.01CH3s 2.88 2.78 2.73 1.86 2.77 2.86 2.85 dimethyl sulfoxide CH3s 2.62 2.52 2.54 1.68 2.50 2.65 2.71 dioxane CH2s 3.71 3.59 3.57 3.35 3.60 3.66 3.75 ethanol CH3t,7 1.25 1.12 1.060.96 1.12 1.19 1.17 CH2q,7d 3.72 3.57 3.44 3.34 3.54 3.60 3.65OH s c,d 1.32 3.39 4.63 2.47ethyl acetate CH3CO s 2.05 1.97 1.99 1.65 1.97 2.01 2.07C H2CH3q,7 4.12 4.05 4.03 3.89 4.06 4.09 4.14CH2C H3t,7 1.26 1.20 1.170.92 1.20 1.24 1.24 ethyl methyl ketone CH3CO s 2.14 2.07 2.07 1.58 2.06 2.12 2.19C H2CH3q,7 2.46 2.45 2.43 1.81 2.43 2.50 3.18CH2C H3t,7 1.060.960.910.850.96 1.01 1.26 ethylene glycol CH s e 3.76 3.28 3.34 3.41 3.51 3.59 3.65“grease”f CH3m0.860.870.920.860.88CH2br s 1.26 1.29 1.36 1.27 1.29n-hexane CH3t0.880.880.860.890.890.90CH2m 1.26 1.28 1.25 1.24 1.28 1.29HMPA g CH3d,9.5 2.65 2.59 2.53 2.40 2.57 2.64 2.61 methanol CH3s h 3.49 3.31 3.16 3.07 3.28 3.34 3.34 OH s c,h 1.09 3.12 4.01 2.16nitromethane CH3s 4.33 4.43 4.42 2.94 4.31 4.34 4.40 n-pentane CH3t,70.880.880.860.870.890.90CH2m 1.27 1.27 1.27 1.23 1.29 1.292-propanol CH3d,6 1.22 1.10 1.040.95 1.09 1.50 1.17 CH sep,6 4.04 3.90 3.78 3.67 3.87 3.92 4.02 pyridine CH(2)m8.628.588.588.538.578.538.52 CH(3)m7.297.357.39 6.667.337.447.45CH(4)m7.687.767.79 6.987.737.857.87 silicone grease i CH3s0.070.130.290.080.10 tetrahydrofuran CH2m 1.85 1.79 1.76 1.40 1.80 1.87 1.88 CH2O m 3.76 3.63 3.60 3.57 3.64 3.71 3.74 toluene CH3s 2.36 2.32 2.30 2.11 2.33 2.32CH(o/p)m7.177.1-7.27.187.027.1-7.37.16CH(m)m7.257.1-7.27.257.137.1-7.37.16 triethylamine CH3t,7 1.030.960.930.960.96 1.050.99 CH2q,7 2.53 2.45 2.43 2.40 2.45 2.58 2.57a In these solvents the intermolecular rate of exchange is slow enough that a peak due to HDO is usually also observed;it appears at2.81and3.30ppm in acetone and DMSO,respectively.In the former solvent,it is often seen as a1:1:1triplet,with2J H,D)1Hz. b2,6-Dimethyl-4-tert-butylphenol.c The signals from exchangeable protons were not always identified.d In some cases(see note a),the coupling interaction between the CH2and the OH protons may be observed(J)5Hz).e In CD3CN,the OH proton was seen as a multiplet atδ2.69,and extra coupling was also apparent on the methylene peak.f Long-chain,linear aliphatic hydrocarbons.Their solubility in DMSO was too low to give visible peaks.g Hexamethylphosphoramide.h In some cases(see notes a,d),the coupling interaction between the CH3and the OH protons may be observed(J)5.5Hz).i Poly(dimethylsiloxane).Its solubility in DMSO was too low to give visible peaks.Notes .Chem.,Vol.62,No.21,19977513.Chem.,Vol.62,No.21,1997NotesTable2.13C NMR Data aCDCl3(CD3)2CO(CD3)2SO C6D6CD3CN CD3OD D2O solvent signals77.16(0.0629.84(0.0139.52(0.06128.06(0.02 1.32(0.0249.00(0.01206.26(0.13118.26(0.02acetic acid CO175.99172.31171.93175.82173.21175.11177.21 CH320.8120.5120.9520.3720.7320.5621.03 acetone CO207.07205.87206.31204.43207.43209.67215.94 CH330.9230.6030.5630.1430.9130.6730.89 acetonitrile CN116.43117.60117.91116.02118.26118.06119.68 CH3 1.89 1.12 1.030.20 1.790.85 1.47 benzene CH128.37129.15128.30128.62129.32129.34tert-butyl alcohol C69.1568.1366.8868.1968.7469.4070.36 CH331.2530.7230.3830.4730.6830.9130.29 tert-butyl methyl ether OCH349.4549.3548.7049.1949.5249.6649.37 C72.8772.8172.0472.4073.1774.3275.62C C H326.9927.2426.7927.0927.2827.2226.60 BHT C(1)151.55152.51151.47152.05152.42152.85C(2)135.87138.19139.12136.08138.13139.09CH(3)125.55129.05127.97128.52129.61129.49C(4)128.27126.03124.85125.83126.38126.11CH3Ar21.2021.3120.9721.4021.2321.38C H3C30.3331.6131.2531.3431.5031.15C34.2535.0034.3334.3535.0535.36chloroform CH77.3679.1979.1677.7979.1779.44cyclohexane CH226.9427.5126.3327.2327.6327.961,2-dichloroethane CH243.5045.2545.0243.5945.5445.11 dichloromethane CH253.5254.9554.8453.4655.3254.78diethyl ether CH315.2015.7815.1215.4615.6315.4614.77 CH265.9166.1262.0565.9466.3266.8866.42 diglyme CH359.0158.7757.9858.6658.9059.0658.67 CH270.5171.0369.5470.8770.9971.3370.05CH271.9072.6371.2572.3572.6372.9271.63 1,2-dimethoxyethane CH359.0858.4558.0158.6858.8959.0658.67 CH271.8472.4717.0772.2172.4772.7271.49 dimethylacetamide CH321.5321.5121.2921.1621.7621.3221.09 CO171.07170.61169.54169.95171.31173.32174.57NCH335.2834.8937.3834.6735.1735.5035.03NCH338.1337.9234.4237.0338.2638.4338.76 dimethylformamide CH162.62162.79162.29162.13163.31164.73165.53 CH336.5036.1535.7335.2536.5736.8937.54CH331.4531.0330.7330.7231.3231.6132.03 dimethyl sulfoxide CH340.7641.2340.4540.0341.3140.4539.39 dioxane CH267.1467.6066.3667.1667.7268.1167.19 ethanol CH318.4118.8918.5118.7218.8018.4017.47 CH258.2857.7256.0757.8657.9658.2658.05 ethyl acetate C H3CO21.0420.8320.6820.5621.1620.8821.15 CO171.36170.96170.31170.44171.68172.89175.26CH260.4960.5659.7460.2160.9861.5062.32CH314.1914.5014.4014.1914.5414.4913.92 ethyl methyl ketone C H3CO29.4929.3029.2628.5629.6029.3929.49 CO209.56208.30208.72206.55209.88212.16218.43C H2CH336.8936.7535.8336.3637.0937.3437.27CH2C H37.868.037.617.918.148.097.87 ethylene glycol CH263.7964.2662.7664.3464.2264.3063.17“grease”CH229.7630.7329.2030.2130.8631.29n-hexane CH314.1414.3413.8814.3214.4314.45CH2(2)22.7023.2822.0523.0423.4023.68CH2(3)31.6432.3030.9531.9632.3632.73HMPA b CH336.8737.0436.4236.8837.1037.0036.46 methanol CH350.4149.7748.5949.9749.9049.8649.50c nitromethane CH362.5063.2163.2861.1663.6663.0863.22 n-pentane CH314.0814.2913.2814.2514.3714.39CH2(2)22.3822.9821.7022.7223.0823.38CH2(3)34.1634.8333.4834.4534.8935.302-propanol CH325.1425.6725.4325.1825.5525.2724.38 CH64.5063.8564.9264.2364.3064.7164.88 pyridine CH(2)149.90150.67149.58150.27150.76150.07149.18 CH(3)123.75124.57123.84123.58127.76125.53125.12CH(4)135.96136.56136.05135.28136.89138.35138.27 silicone grease CH3 1.04 1.40 1.38 2.10 tetrahydrofuran CH225.6226.1525.1425.7226.2726.4825.67 CH2O67.9768.0767.0367.8068.3368.8368.68 toluene CH321.4621.4620.9921.1021.5021.50C(i)137.89138.48137.35137.91138.90138.85CH(o)129.07129.76128.88129.33129.94129.91CH(m)128.26129.03128.18128.56129.23129.20CH(p)125.33126.12125.29125.68126.28126.29triethylamine CH311.6112.4911.7412.3512.3811.099.07 CH246.2547.0745.7446.7747.1046.9647.19a See footnotes for Table1.b2J PC)3Hz.c Reference material;see text.For D2O solutions there is no accepted reference for carbon chemical shifts.We suggest the addition of a drop of methanol,and the position of its signal to be defined as49.50ppm;on this basis,the entries in Table2were recorded.The chemical shifts thus obtained are,on the whole,very similar to those for the other solvents. Alternatively,we suggest the use of dioxane when the methanol peak is expected to fall in a crowded area of the spectrum.We also report the chemical shifts of sodium formate(171.67ppm),sodium acetate(182.02and 23.97ppm),sodium carbonate(168.88ppm),sodium bicarbonate(161.08ppm),and sodium3-(trimethylsilyl)-propanesulfonate[54.90,19.66,15.56(methylenes1,2, and3,respectively),and-2.04ppm(methyls)],in D2O. Temperature Dependence of HDO Chemical Shifts.We recorded the1H spectrum of a sample of D2O, containing a crystal of sodium3-(trimethylsilyl)propane-sulfonate as reference,as a function of temperature.The data are shown in Figure1.The solid line connecting the experimental points corresponds to the equation which reproduces the measured values to better than1 ppb.For the0-50o C range,the simplergives values correct to10ppb.For both equations,T is the temperature in°C.Acknowledgment.Generous support for this work by the Minerva Foundation and the Otto Mayerhoff Center for the Study of Drug-Receptor Interactions at Bar-Ilan University is gratefully acknowledged.JO971176Vδ)5.060-0.0122T+(2.11×10-5)T2(1)δ)5.051-0.0111T(2)Notes .Chem.,Vol.62,No.21,19977515。
