高考化学 化学能与电能综合试题附答案解析
全国高考化学化学能与电能的综合高考真题汇总及详细答案

全国高考化学化学能与电能的综合高考真题汇总及详细答案一、化学能与电能1.研究小组进行图所示实验,试剂A为0.2 mol·L−1 CuSO4溶液,发现铝条表面无明显变化,于是改变实验条件,探究铝和CuSO4溶液、CuCl2溶液反应的影响因素。
用不同的试剂A进行实验1~实验4,并记录实验现象:实验序号试剂A实验现象10.2 mol·L−1 CuCl2溶液铝条表面有气泡产生,并有红色固体析出20.2 mol·L−1 CuSO4溶液,再加入一定质量的NaCl固体开始铝条表面无明显变化,加NaCl后,铝条表面有气泡产生,并有红色固体析出3 2 mol·L−1 CuSO4溶液铝条表面有少量气泡产生,并有少量红色固体4 2 mol·L−1 CuCl2溶液反应非常剧烈,有大量气泡产生,溶液变成棕褐色,有红色固体和白色固体生成(1)实验1中,铝条表面析出红色固体的反应的离子方程式为_________。
(2)实验2的目的是证明铜盐中的阴离子Cl−是导致实验1中反应迅速发生的原因,实验2中加入NaCl固体的质量为_________ g。
(3)实验3的目的是_________。
(4)经检验知,实验4中白色固体为CuCl。
甲同学认为产生白色固体的原因可能是发生了Cu + CuCl 22CuCl的反应,他设计了右图所示实验证明该反应能够发生。
① A极的电极材料是_________。
② 能证明该反应发生的实验现象是_________。
(5)为探究实验4中溶液呈现棕褐色的原因,分别取白色CuCl固体进行以下实验:实验序号实验操作实验现象i加入浓NaCl溶液沉淀溶解,形成无色溶液ii加入饱和AlCl3溶液沉淀溶解,形成褐色溶液iii向i所得溶液中加入2 mol·L-1 CuCl2溶液溶液由无色变为褐色查阅资料知:CuCl难溶于水,能溶解在Cl-浓度较大的溶液中,生成[CuCl2]-络离子,用水稀释含[CuCl2]-的溶液时会重新析出CuCl沉淀。
高考化学化学能与电能综合练习题及答案

高考化学化学能与电能综合练习题及答案1. 一根铁棒在氧气中燃烧,生成了Fe2O3。
如果该反应释放了热量,那么该反应是一个__________反应。
答案:放热反应。
2. 在标准状态下,1mol H2O的生成焓是__________kJ。
答案:-285.8kJ。
3. 在标准状态下,1mol CO2的生成焓是__________kJ。
答案:-393.5kJ。
4. 在标准状态下,1mol O2的生成焓是__________kJ。
答案:0kJ。
5. 在标准状态下,1mol H2的生成焓是__________kJ。
答案:-285.8kJ。
6. 在标准状态下,1mol Fe2O3的生成焓是__________kJ。
答案:-826.8kJ。
7. 在标准状态下,1mol CH4的生成焓是__________kJ。
答案:-74.8kJ。
8. 在标准状态下,1mol C2H5OH的生成焓是__________kJ。
答案:-277.6kJ。
9. 在标准状态下,1mol NH3的生成焓是__________kJ。
答案:-46.1kJ。
10. 在标准状态下,1mol HCl的生成焓是__________kJ。
答案:-92.3kJ。
11. 在标准状态下,1mol H2SO4的生成焓是__________kJ。
答案:-814.5kJ。
12. 在标准状态下,1mol NaOH的生成焓是__________kJ。
答案:-469.6kJ。
13. 在标准状态下,1mol CaO的生成焓是__________kJ。
答案:-635.1kJ。
14. 在标准状态下,1mol NH4Cl的生成焓是__________kJ。
答案:-314.4kJ。
15. 在标准状态下,1mol KCl的生成焓是__________kJ。
答案:-436.6kJ。
16. 在标准状态下,1mol NaCl的生成焓是__________kJ。
答案:-411.2kJ。
17. 在标准状态下,1mol MgO的生成焓是__________kJ。
2020-2021高考化学化学能与电能的综合题试题及答案解析

2020-2021高考化学化学能与电能的综合题试题及答案解析一、化学能与电能1.如图所示,E为浸有Na2SO4溶液的滤纸,并加入几滴酚酞。
A、B均为Pt片,压在滤纸两端,R、S为电源的电极。
M、N为惰性电极。
G为检流计,K为开关。
试管C、D和电解池中都充满KOH溶液。
若在滤纸E上滴一滴紫色的KMnO4溶液,断开K,接通电源一段时间后,C、D中有气体产生。
(1)R为电源的__,S为电源的__。
(2)A极附近的溶液变为红色,B极的电极反应式为__。
(3)滤纸上的紫色点移向__(填“A极”或“B极”)。
(4)当试管C、D中的气体产生到一定量时,切断外电源并接通开关K,经过一段时间,C、D中气体逐渐减少,主要是因为_,写出有关的电极反应式:__。
【答案】负极正极 2H2O-4e-=4H++O2↑ B极氢气和氧气在碱性环境下发生原电池反应,消耗了氢气和氧气 2H2+4OH--4e-=4H2O(负极),O2+2H2O+4e-=4OH-(正极)【解析】【分析】(1)根据电极产物判断电解池的阴阳极及电源的正负极;(2)根据电解池原理及实验现象书写电极反应式;(3)根据电解池原理分析电解质溶液中离子移动方向;(4)根据燃料电池原理分析解答。
【详解】(1)断开K,通直流电,电极C、D及氢氧化钾溶液构成电解池,根据离子的放电顺序,溶液中氢离子、氢氧根离子放电,分别生成氢气和氧气,氢气和氧气的体积比为2:1,通过图象知,C极上气体体积是D极上气体体积的2倍,所以C极上得氢气,D极上得到氧气,故R是负极,S是正极,故答案为:负极;正极;(2)A极是阴极,电解高锰酸钾时,在该极上放电的是氢离子,所以该极上碱性增强,酚酞显红色,B极是阳极,该极附近发生的电极反应式为:2H2O-4e-=4H++O2↑,故答案为:2H2O-4e-=4H++O2↑;(3)浸有高锰酸钾的滤纸和电极A、B与电源也构成了电解池,因为R是负极,S是正极,所以B极是阳极,A极是阴极,电解质溶液中的阴离子高锰酸根离子向阳极移动,紫色点移向B极,故答案为:B极;(4)当C、D里的气体产生到一定量时,切断外电源并接通开关K,构成氢氧燃料电池,氢气和氧气在碱性环境下发生原电池反应,消耗了氢气和氧气;在燃料电池中,燃料氢气为负极,在碱性环境下的电极反应式为:2H2+4OH--4e-=4H2O,C中的电极作负极,D中的电极作正极,电极反应式为O2+2H2O+4e-=4OH-,故答案为:氢气和氧气在碱性环境下发生原电池反应,消耗了氢气和氧气;2H2+4OH--4e-=4H2O(负极),O2+2H2O+4e-=4OH-(正极)。
2020-2021高考化学 化学能与电能综合试题含答案解析

2020-2021高考化学化学能与电能综合试题含答案解析一、化学能与电能1.方法与规律提炼:(1)某同学利用原电池装置证明了反应Ag++Fe2+=Ag+Fe3+能够发生,设计的装置如下图所示。
为达到目的,其中石墨为_________极,甲溶液是____________,证明反应Ag++Fe2+=Ag +Fe3+能够发生的实验操作及现象是_________________________(2)用零价铁(Fe)去除水体中的硝酸盐(NO)已成为环境修复研究的热点之一。
Fe还原水体中NO3-的反应原理如图所示。
上图中作负极的物质是___________。
正极的电极反应式是______________。
(3)在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案,主要包括电化学过程和化学过程,如下图所示:阴极区的电极反应式为_______________。
电路中转移1 mol电子,需消耗氧气_______L(标准状况)。
(4)KClO3也可采用“电解法”制备,装置如图所示。
写出电解时阴极的电极反应式___________________电解过程中通过阳离子交换膜的离子主要为_________,其迁移方向是_____________(填a→b或b→a)。
学法题:通过此题的解答,请归纳总结书写电极反应式的方法____【答案】负 FeSO4或FeCl2溶液分别取电池工作前与工作一段时间后左侧烧杯中溶液,同时滴加KSCN溶液,后者红色加深铁 NO3-+8e-+10H+=NH4++3H2O Fe3++e-= Fe2+ 5.6L 2H++2e-= H2 ↑ K+a→b原电池中先确定原电池的正负极,列出正负极上的反应物质,并标出相同数目电子的得失;注意负极反应生成的阳离子与电解质溶液中的阴离子是否共存。
电解池中电极反应式的书写看阳极材料,如果阳极是惰性电极(Pt、Au、石墨),则应是电解质溶液中的离子放电,应根据离子的放电顺序进行书写。
高考化学 化学能与电能 综合题含详细答案

高考化学化学能与电能综合题含详细答案一、化学能与电能1.研究小组进行图所示实验,试剂A为0.2 mol·L−1 CuSO4溶液,发现铝条表面无明显变化,于是改变实验条件,探究铝和CuSO4溶液、CuCl2溶液反应的影响因素。
用不同的试剂A进行实验1~实验4,并记录实验现象:实验序号试剂A实验现象10.2 mol·L−1 CuCl2溶液铝条表面有气泡产生,并有红色固体析出20.2 mol·L−1 CuSO4溶液,再加入一定质量的NaCl固体开始铝条表面无明显变化,加NaCl后,铝条表面有气泡产生,并有红色固体析出3 2 mol·L−1 CuSO4溶液铝条表面有少量气泡产生,并有少量红色固体4 2 mol·L−1 CuCl2溶液反应非常剧烈,有大量气泡产生,溶液变成棕褐色,有红色固体和白色固体生成(1)实验1中,铝条表面析出红色固体的反应的离子方程式为_________。
(2)实验2的目的是证明铜盐中的阴离子Cl−是导致实验1中反应迅速发生的原因,实验2中加入NaCl固体的质量为_________ g。
(3)实验3的目的是_________。
(4)经检验知,实验4中白色固体为CuCl。
甲同学认为产生白色固体的原因可能是发生了Cu + CuCl 22CuCl的反应,他设计了右图所示实验证明该反应能够发生。
① A极的电极材料是_________。
② 能证明该反应发生的实验现象是_________。
(5)为探究实验4中溶液呈现棕褐色的原因,分别取白色CuCl固体进行以下实验:实验序号实验操作实验现象i加入浓NaCl溶液沉淀溶解,形成无色溶液ii加入饱和AlCl3溶液沉淀溶解,形成褐色溶液iii向i所得溶液中加入2 mol·L-1 CuCl2溶液溶液由无色变为褐色查阅资料知:CuCl难溶于水,能溶解在Cl-浓度较大的溶液中,生成[CuCl2]-络离子,用水稀释含[CuCl2]-的溶液时会重新析出CuCl沉淀。
全国高考化学化学能与电能的综合高考真题汇总及答案解析

全国高考化学化学能与电能的综合高考真题汇总及答案解析一、化学能与电能1.为探究Ag+与Fe3+氧化性的相关问题,某小组同学进行如下实验:已知:相关物质的溶解度(20℃)AgCl:1.5×10-4g Ag2SO4:0.796g (1)甲同学的实验如下:序号操作现象实验Ⅰ将2mL1mol/L AgNO3溶液加入到1mL1mol/L FeSO4溶液中产生白色沉淀,随后有黑色固体产生取上层清液,滴加KSCN溶液溶液变红注:经检验黑色固体为Ag① 白色沉淀的化学式是_____________。
② 甲同学得出Ag+氧化了Fe2+的依据是_______________。
(2)乙同学为探究Ag+和Fe2+反应的程度,进行实验Ⅱ。
a.按右图连接装置并加入药品(盐桥中的物质不参与反应),发现电压表指针偏移。
偏移的方向表明:电子由石墨经导线流向银。
放置一段时间后,指针偏移减小。
b.随后向甲烧杯中逐渐加入浓Fe2(SO4)3溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
① a中甲烧杯里的电极反应式是___________。
② b中电压表指针逆向偏移后,银为_________极(填“正”或“负”)。
③ 由实验得出Ag+和Fe2+反应的离子方程式是___________。
(3)为进一步验证乙同学的结论,丙同学又进行了如下实验:序号操作现象实验Ⅲ将2mL2mol/L Fe(NO3)3溶液加入有银镜的试管中银镜消失实验Ⅳ将2mL1mol/L Fe2(SO4)3溶液加入有银镜的试管中银镜减少,未消失实验Ⅴ将2mL2mol/L FeCl3溶液加入有银镜的试管中银镜消失① 实验Ⅲ___________(填“能”或“不能”)证明Fe3+氧化了Ag,理由是_____________。
② 用化学反应原理解释实验Ⅳ与Ⅴ的现象有所不同的原因:_____________。
【答案】Ag2SO4有黑色固体(Ag)生成,加入KSCN溶液后变红 Fe2+-e-=Fe3+负Fe2++Ag+Fe3++Ag 不能因为Fe(NO3)3溶液呈酸性,酸性条件下NO3-也可能氧化Ag 溶液中存在平衡:Fe3++Ag Fe2++Ag+,且AgCl比Ag2SO4溶解度更小,Cl-比SO42-更有利于降低Ag+浓度,所以实验Ⅴ比实验Ⅳ正向进行的程度更大(或促使平衡正向移动,银镜溶解)。
高考化学化学能与电能综合题附答案解析

高考化学化学能与电能综合题附答案解析一、化学能与电能1.研究+6价铬盐不同条件下微粒存在形式及氧化性,某小组同学进行如下实验:已知:Cr2O72-(橙色)+H2O2CrO42-(黄色)+2H+△H=+13.8kJ/mol,+6价铬盐在一定条件下可被还原为Cr3+,Cr3+在水溶液中为绿色。
(1)试管c和b对比,推测试管c的现象是_____________________。
(2)试管a和b对比,a中溶液橙色加深。
甲认为温度也会影响平衡的移动,橙色加深不一定是c(H+)增大影响的结果;乙认为橙色加深一定是c(H+)增大对平衡的影响。
你认为是否需要再设计实验证明?__________(“是”或“否”),理由是____________________________________________________。
(3)对比试管a、b、c的实验现象,可知pH增大2-272-4c(Cr O)c(CrO)_____(选填“增大”,“减小”,“不变”);(4)分析如图试管c继续滴加KI溶液、过量稀H2SO4的实验现象,说明+6价铬盐氧化性强弱为Cr2O72-__________CrO42-(填“大于”,“小于”,“不确定”);写出此过程中氧化还原反应的离子方程式_________。
(5)小组同学用电解法处理含Cr2O72-废水,探究不同因素对含Cr2O72-废水处理的影响,结果如表所示(Cr2O72-的起始浓度,体积、电压、电解时间均相同)。
实验ⅰⅱⅲⅳ是否加入Fe2(SO4)3否否加入5g否是否加入H2SO4否加入1mL加入1mL加入1mL电极材料阴、阳极均为石墨阴、阳极均为石墨阴、阳极均为石墨阴极为石墨,阳极为铁Cr2O72-的去除率/%0.92212.720.857.3①实验ⅱ中Cr2O72-放电的电极反应式是________________。
②实验ⅲ中Fe3+去除Cr2O72-的机理如图所示,结合此机理,解释实验iv中Cr2O72-去除率提高较多的原因_______________。
高考化学压轴题专题化学能与电能的经典综合题附答案解析

高考化学压轴题专题化学能与电能的经典综合题附答案解析一、化学能与电能1.钛工厂TiCl4烟尘中含有大量的ScCl3、MgCl2及SiO2小颗粒等物质,某研究所利用上述烟尘回收Sc2O3,并制备钛白粉(TiO2),其工艺流程如下所示:(1)酸浸过程中,HCl的作用是_______________________。
(2)已知Sc3++3HTBP Sc(TBP)3+3H+,则上述洗脱剂最好选择___________(选填“酸性”、“碱性”或“中性”)溶液。
在实验室模拟完成上述操作Ⅰ和操作Ⅱ所涉及的玻璃仪器有______________。
(3)草酸“沉钪”得到草酸钪的化学反应类型为____________________________。
(4)在空气中灼烧草酸钪即可得到氧化钪(Sc2O3),其化学反应方程式为__________________________。
(5)“水相”的主要离子有TiOCl42-、H+、Cl- 及________,写出加入大量的水并加热发生的相关离子反应方程式__________________________。
(6)钛的冶炼新法是剑桥电解法(如右图)。
以含少量CaCl2的CaO熔融物作为介质,电解时。
在阴极生成的Ca进一步还原TiO2得钛。
写出阳极电极主要反应方程式:__________________________;利用中学所学知识可以预测CaCl2的作用包含增强导电性、___________;F=96500C/mol,当I=0.5A,通电80分钟,理论上获得Ti的质量为__________g(计算表达式)。
【答案】抑制TiOCl42-的进一步水解(多答Mg2+、Sc3+水解亦给分)酸性分液漏斗、烧杯复分解反应3O2+2Sc2(C2O4)32Sc2O3+12CO2Mg2+TiOCl42-+(1+x)H2O TiO2·xH2O+2H++4Cl-2O2--4e-=O2↑降低CaO的熔点【解析】(1)为了防止TiOCl42-、Mg2+、Se3+水解,酸浸过程中加入HCl可以,故答案为:抑制TiOCl42-的进一步水解;(2)根据Sc3++3HTBP Sc(TBP)3+3H+,则上述洗脱剂最好选择酸性溶液洗涤,可以抑制Sc3+与HTBP的反应;操作Ⅰ和操作Ⅱ为分液,所涉及的玻璃仪器有分液漏斗、烧杯,故答案为:酸性;分液漏斗、烧杯;(3)ScCl3与草酸发生复分解反应生成草酸钪,故答案为:复分解反应;(4)在空气中灼烧草酸钪即可得到氧化钪(Sc2O3),同时草酸根离子被氧化生成二氧化碳,反应的化学反应方程式为3O2+2Sc2(C2O4)32Sc2O3+12CO2,故答案为:3O2+2Sc2(C2O4)32Sc2O3+12CO2;(5)根据流程图,钛工厂TiCl4烟尘中含有大量的ScCl3、MgCl2及SiO2小颗粒等物质,酸浸后,过滤除去了二氧化硅,再用有机溶剂萃取,“水相”中主要离子有TiOCl42-、H+、Cl- 及Mg2+,在水相中加入大量的水并加热促进TiOCl42-水解生成TiO2·xH2O,反应的离子方程式为TiOCl42-+(1+x)H2O TiO2·xH2O+2H++4Cl-,故答案为:Mg2+;TiOCl42-+(1+x)H2O TiO2·xH2O+2H++4Cl-;(6)在阴极,氧化钙被还原生成Ca,被还原的Ca进一步还原TlO2获得钛,电极反应为Ca2++2e-=Ca、2Ca+TlO2=2CaO+Ti,阳极石墨上氧离子失去电子生成氧气,电极反应式为2O2--4e-=O2↑,电解质为混有氯化钙的熔融的氧化钙,加入氯化钙可以增强电解质的导电性,同时可以降低CaO的熔点,节约能量;电流强度为0.5A,电池工作80分钟,则电量为0.5A×80×60s=2400C,转移电子的物质的量=,生成Ti的质量=×48g/mol=×48g,故答案为:2O2--4e-=O2↑;降低CaO 的熔点;×48。
高考化学化学能与电能综合题汇编及详细答案

高考化学化学能与电能综合题汇编及详细答案一、化学能与电能1.(1)利用原电池装置可以验证Fe3+与Cu2+氧化性相对强弱,如下图所示。
该方案的实验原理是自发进行的氧化还原反应可以设计为原电池。
写出该氧化还原反应的离子方程式:__________。
该装置中的负极材料是______(填化学式),正极反应式是_______。
(2)某研究性学习小组为证明2Fe3++2I-⇌2Fe2++I2为可逆反应,设计如下两种方案。
方案一:取5mL0.1mol/LKI溶液,滴加2mL0.1mol/L的FeCl3溶液,再继续加入2mLCCl4,充分振荡、静置、分层,再取上层清液,滴加KSCN溶液。
①方案一中能证明该反应为可逆反应的现象是______。
②有同学认为方案一设计不够严密,即使该反应为不可逆反应也可能出现上述现象,其原因是(用离子方程式表示)_____。
方案二:设计如下图原电池...装置,接通灵敏电流计,指针向右偏转(注:灵敏电流计指针总是偏向电源正极),随着时间进行电流计读数逐渐变小,最后读数变为零。
当指针读数变零后,在右管中加入1mol/L FeCl2溶液。
③方案二中,“读数变为零”是因为____________.④“在右管中加入1mol/L FeCl2溶液”后,观察到灵敏电流计的指针______偏转(填“向左”、“向右”或“不”),可证明该反应为可逆反应。
【答案】Cu+2Fe3+=Cu2++2Fe2+ Cu Fe3+ + e- = Fe2+下层(CCl4层)溶液呈紫红色,且上层清液中滴加KSCN后溶液呈血红色 4Fe2++O2+4H+=2H2O+4Fe3+该可逆反应达到了化学平衡状态向左【解析】【分析】(1)验证Fe3+与Cu2+氧化性强弱时,应将反应Cu+2Fe3+=Cu2++2Fe2+设计成原电池,原电池中铜作负极发生氧化反应被损耗,选用金属性弱于铜的金属或非金属C作正极,电解质溶液为可溶性的铁盐;(2)方案一:如该反应为可逆反应,加入四氯化碳,四氯化碳层呈紫红色,上层清液中滴加KSCN后溶液呈血红色;但在振荡过程中,Fe2+离子易被空气中氧气生成Fe3+,不能证明Fe3+未完全反应;方案二:图中灵敏电流计的指针指向右,右侧烧杯为正极,当指针读数变零后,在右管中加入1mol/LFeCl2溶液,如为可逆反应,可发生2Fe2++I2⇌2Fe3++2I-,I2被还原,指针应偏向左。
高考化学化学能与电能综合题含答案解析

高考化学化学能与电能综合题含答案解析一、化学能与电能1.某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和碳粉置于锥形瓶底部,塞上瓶塞(如图1)。
从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化。
(1)请完成以下实验设计表(表中不要留空格):编号实验目的碳粉/g铁粉/g醋酸/%①为以下实验作参照0.5 2.090.0②醋酸浓度的影响0.5__36.0③__0.2 2.090.0(2)编号①实验测得容器中压强随时间变化如图2。
t2时,容器中压强明显小于起始压强,其原因是铁发生了_____________腐蚀,请在图3中用箭头标出发生该腐蚀时电子流动方向;此时,碳粉表面发生了__(“氧化”或“还原”)反应,其电极反应式是___________________________________。
(3)该小组对图2中0~t1时压强变大的原因提出了如下假设,请你完成假设二:假设一:发生析氢腐蚀产生了气体;假设二:______________________________;……(4)为验证假设一,某同学设计了检验收集的气体中是否含有H2的方案。
请你再设计一个实验方案验证假设一,写出实验步骤和结论。
实验步骤和结论(不要求写具体操作过程):__________【答案】2.0 碳粉含量的影响吸氧还原反应 2H2O+O2+4e-=4OH- (或4H++O2+4e-=2H2O)反应放热,温度升高,体积膨胀实验步骤和结论(不要求写具体操作过程)①药品用量和操作同编号①实验(多孔橡皮塞增加进、出导管)②通入氩气排净瓶内空气;③滴入醋酸溶液,同时测量瓶内压强变化(也可测温度变化,检验Fe2+等)。
如果瓶内压强增大,假设一成立。
否则假设一不成立。
(本题属于开放性试题,合理答案均给分)【解析】【详解】(1)探究影响化学反应速率,每次只能改变一个变量,故有②中铁的量不变,为2.0g;③中改变了碳粉的质量,故为探究碳粉的量对速率的影响。
高考化学 化学能与电能综合试题含答案解析

高考化学化学能与电能综合试题含答案解析一、化学能与电能1.某小组同学利用如图所示装置进行铁的电化学腐蚀原理的探究实验:装置分别进行的操作现象i.连好装置一段时间后,向烧杯中滴加酚酞ii.连好装置一段时间后,向烧杯中滴加K3[Fe(CN)6]溶液铁片表面产生蓝色沉淀(1)小组同学认为以上两种检验方法,均能证明铁发生了吸氧腐蚀。
①实验i中的现象是___。
②用电极反应式解释实验i中的现象:___。
(2)查阅资料:K3[Fe(CN)6]具有氧化性。
①据此有同学认为仅通过ii中现象不能证明铁发生了电化学腐蚀,理由是___。
②进行下列实验,在实验几分钟后的记录如下:实验滴管试管现象0.5mol·L-1K3[Fe(CN)6]溶液iii.蒸馏水无明显变化iv.1.0mol·L-1NaCl溶液铁片表面产生大量蓝色沉淀v.0.5mol·L-1Na2SO4溶液无明显变化以上实验表明:在有Cl-存在条件下,K3[Fe(CN)6]溶液可以与铁片发生反应。
为探究Cl-的存在对反应的影响,小组同学将铁片酸洗(用稀硫酸浸泡后洗净)后再进行实验iii,发现铁片表面产生蓝色沉淀。
此补充实验表明Cl-的作用是___。
(3)有同学认为上述实验仍不够严谨。
为进一步探究K3[Fe(CN)6]的氧化性对实验ii结果的影响,又利用(2)中装置继续实验。
其中能证实以上影响确实存在的是__(填字母序号)。
实验试剂现象A酸洗后的铁片、K3[Fe(CN)6]溶液(已除O2)产生蓝色沉淀(4)综合以上实验分析,利用实验ii中试剂能证实铁发生了电化学腐蚀的实验方案是:连好装置一段时间后,___(回答相关操作、现象),则说明负极附近溶液中产生了Fe2+,即发生了电化学腐蚀。
【答案】碳棒附近溶液变红 O2+4e-+2H2O=4OH- K3[Fe(CN)6]可能氧化Fe生成Fe2+,会干扰由于电化学腐蚀负极生成Fe2+的检验 Cl-破坏了铁片表面的氧化膜 AC 取铁片(负极)附近溶液于试管中,滴加K3[Fe(CN)6]溶液,若出现蓝色沉淀【解析】【分析】(1)①实验i中,发生吸氧腐蚀,在碳棒附近溶液中生成OH-,使酚酞变色。
全国高考化学化学能与电能的综合高考真题汇总含详细答案

全国高考化学化学能与电能的综合高考真题汇总含详细答案一、化学能与电能1.亚硝酰氯NOCl可用于合成清洁剂等。
它可用Cl2与NO在常温常压下合成:它的熔点为-64.5℃,沸点为-5.5℃,常温下是黄色的有毒气体,遇水易水解。
请按要求回答下列相关问题:(1)过量铁屑和稀硝酸充分反应制备NO的离子方程式为:______________________。
(2)制备NOCl的装置如下图所示,连接顺序为:a→_________________________(按气流自左向右方向,用小写字母表示)。
①装置A和B作用是①干燥NO和Cl2,②___________________________________________。
②装置D的作用是______________________________________。
③装置E中NOCl发生反应的化学方程式为________________。
(3)工业生产过程中NO尾气处理方法有多种,其中间接电化学法,其原理如图所示:该过程中阴极的电极反应式为:__________________________________________。
【答案】3Fe+8H++2NO3—=3Fe2++2NO↑+4H2O e→f→c→b→d或f→e→c→b→d观察气泡调节气体流速防止E中水蒸气进入F,引起NOCl的水解 NOCl+2NaOH=NaCl+NaNO2+H2O 2HSO3—+2e—+2H+= S2O42—+ 2H2O【解析】【分析】(1)过量铁屑和稀硝酸反应生成硝酸亚铁、一氧化氮和水;(2)将氯气和NO干燥后在装置F中发生反应,在冰盐中冷凝收集NOCl,氯气、NO以及NOCl均不能排放到空气中,用氢氧化钠溶液吸收,注意NOCl遇水易水解。
(3)由间接电化学法示意图可知,阴极上HSO3—放电生成S2O42—,S2O42—在吸收塔中将NO还原为N2。
【详解】(1)过量铁屑和稀硝酸反应生成硝酸亚铁、一氧化氮和水,反应的离子方程式为3Fe+8H++2NO3—=3Fe2++2NO↑+4H2O,故答案为3Fe+8H++2NO3—=3Fe2++2NO↑+4H2O;(2)将氯气和NO干燥后在装置F中发生反应,在冰盐中冷凝收集NOCl,氯气、NO以及NOCl均不能排放到空气中,用氢氧化钠溶液吸收,NOCl遇水易水解,故在收集装置和尾气处理装置之间需加一个干燥装置,故答案为e→f(或f→e)→c→b→d;①装置A和B作用是除干燥NO、Cl2外,另一个作用是通过观察气泡调节气体的流速控制反应的发生,故答案为观察气泡调节气体流速;②NOCl遇水易水解,装置D中氯化钙做干燥剂,吸收水蒸气,防止E中水蒸气进入反应器F中,引起NOCl的水解,故答案为防止E中水蒸气进入F,引起NOCl的水解;③装置E的目的吸收尾气,防止污染环境,NOCl与氢氧化钠溶液反应生成NaCl、NaNO2和H2O,反应的化学方程式为NOCl+2NaOH=NaCl+NaNO2+H2O,故答案为NOCl+2NaOH=NaCl+NaNO2+H2O;(3)由间接电化学法示意图可知,阴极上HSO3—放电生成S2O42—,S2O42—在吸收塔中将NO还原为N2,阴极的电极反应式为2HSO3—+2e—+2H+= S2O42—+ 2H2O,故答案为2HSO3—+2e—+2H+= S2O42—+ 2H2O。
全国高考化学化学能与电能的综合高考真题汇总含答案解析

4
2 mol·L−1 CuCl2 溶液
反应非常剧烈,有大量气泡产生,溶液变成棕褐 色,有红色固体和白色固体生成
(1)实验 1 中,铝条表面析出红色固体的反应的离子方程式为_________。 (2)实验 2 的目的是证明铜盐中的阴离子 Cl−是导致实验 1 中反应迅速发生的原因,实验 2 中加入 NaCl 固体的质量为_________ g。 (3)实验 3 的目的是_________。 (4)经检验知,实验 4 中白色固体为 CuCl。甲同学认为产生白色固体的原因可能是发生 了 Cu + CuCl2 2CuCl 的反应,他设计了右图所示实验证明该反应能够发生。
成,加入 KSCN 溶液后变红;
(2)①实验过程中电压表指针偏移,偏移的方向表明:电子由石墨经导线流向银,依据原
电池原理可知银做原电池正极,石墨做原电池负极,负极是甲池溶液中亚铁离子失电子发
实验 序号
试剂 A
实验现象
1
0.2 mol·L−1 CuCl2 溶液
铝条表面有气泡产生,并有红色固体析出
0.2 mol·L−1 CuSO4 溶液,再加入 开始铝条表面无明显变化,加 NaCl 后,铝条表
2
一定质量的 NaCl 固体
面有气泡产生,并有红色固体析出
3
2 mol·L−1 CuSO4 溶液
铝条表面有少量气泡产生,并有少量红色固体
3.为探究 Ag+与 Fe3+氧化性的相关问题,某小组同学进行如下实验: 已知:相关物质的溶解度(20℃)AgCl:1.5×10-4g Ag2SO4:0.796 g (1)甲同学的实验如下:
序号
操作
现象
实验Ⅰ
将 2 mL 1 mol/L AgNO3 溶液加 产生白色沉淀,随后有黑色固体产生 入到 1 mL 1 mol/L FeSO4 溶液中
全国高考化学化学能与电能的综合高考真题汇总附答案解析

全国高考化学化学能与电能的综合高考真题汇总附答案解析一、化学能与电能1.氯化亚砜又称亚硫酰氯,其分子式为 SOCl2,常温常压下为淡黄色液体,遇水易水解。
国内的氯化亚砜主要应用于医药、农药、染料等行业。
实验室用干燥纯净的 Cl2、SO2和SCl2制备 SOCl2的部分装置如图所示:已知:①SOCl2沸点为 78.8℃,SCl2 的沸点为 50℃,且两种液体可互溶。
②SOCl2遇水剧烈反应,液面上产生白雾,并有气体产生。
请回答:(1)实验室制取 SOCl2的反应方程式为____________(2)写出丙中发生的离子反应_____________(3)仪器 e 的名称是___________,实验仪器的连接顺序为a→_________(仪器可以重复使用)。
(4)仪器 f 的作用是 ____________(5)实验结束后,将三颈烧瓶中混合物分离的实验操作名称是______。
(6)工业上常用 ZnCl2·2H2O 与 SOCl2共热制取 ZnCl2。
写出用惰性电极电解ZnCl2和盐酸的混合溶液的总反应离子反应式为_______。
甲同学认为 SOCl2还可用作FeCl3·6H2O 制取无水FeCl3的脱水剂,但乙同学对此提出质疑,可能的原因是____【答案】SO2+Cl2+SCl22SOCl22MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O球形冷凝管c→d→c→d→b吸收SO2、Cl2,防止外界水蒸气进入装置分馏(或蒸馏)2H++2Cl—H2↑+Cl2↑SOCl2可能会与Fe3+发生氧化还原反应【解析】【分析】由实验装置图可知,丙装置中浓盐酸与高锰酸钾反应制备氯气,因氯气中混有氯化氢和水蒸气,所以先将气体通过盛有饱和食盐水的乙装置除去氯化氢,再通过盛有浓硫酸的乙装置除去水蒸气,干燥的氯气、二氧化硫和SCl2在三颈烧瓶中,在活性炭作催化剂作用下,反应制得SOCl2,二氯化硫(SCl2)的沸点低,甲装置中球形冷凝管的作用是起冷凝回流SCl2的作用,干燥管中碱石灰的作用是防止有毒的氯气与二氧化硫逸出污染环境,同时防止空气中的水蒸气进入烧瓶中使氯化亚砜水解。
2020-2021高考化学专题《化学能与电能》综合检测试卷含答案解析

2020-2021高考化学专题《化学能与电能》综合检测试卷含答案解析一、化学能与电能1.以NaCl为主要成分的融雪剂会腐蚀桥梁、铁轨等钢铁设备。
某研究小组探究NaCl溶液对钢铁腐蚀的影响。
(1)将滤纸用3.5%的NaCl溶液润湿,涂上铁粉、碳粉的混合物,贴在表面皿上。
在滤纸上加几滴检验试剂,再缓慢加入NaCl溶液至没过滤纸,操作如下所示:①实验ⅰ的现象说明,得电子的物质是_______________________________。
②碳粉的作用是___________________________________________________。
③为了说明NaCl的作用,需要补充的对照实验是_____________________。
(2)向如图示装置的烧杯a、b中各加入30mL 3.5%的NaCl溶液,闭合K,指针未发生偏转。
加热烧杯a,指针向右偏转。
①取a、b中溶液少量,滴加K3[Fe(CN)6]溶液,a中出现蓝色沉淀,b中无变化,b中铁片作________极。
②加热后,指针发生偏转的原因可能是_____________________。
(3)用(2)中图示装置探究不同浓度NaCl溶液对钢铁腐蚀的影响,向烧杯a、b中各加入30mL不同质量分数的NaCl溶液,实验记录如下表所示。
实验a b指针偏转方向I0.1%0.01%向右II0.1% 3.5%向左Ⅲ 3.5%饱和溶液向右①Ⅱ中,b中电极发生的电极反应式是_______________________________。
②Ⅲ中,铁在饱和NaCl溶液中不易被腐蚀。
查阅资料可知:在饱和NaCl溶液中O2浓度较低,钢铁不易被腐蚀。
设计实验证明:_______________________________。
(4)根据上述实验,对钢铁腐蚀有影响的因素是_______________________________。
【答案】O2与铁组成原电池,作原电池的正极用水代替NaCl溶液进行上述实验正温度升高,Fe还原性增强,反应速率加快 Fe-2e-=Fe2+另取两个烧杯,分别往其中加入铁片和一定量的饱和NaCl溶液,再分别滴加几滴K3Fe(CN)6溶液,然后往其中一个烧杯中通入O2,观察现象温度、NaCl溶液的浓度、O2的浓度【解析】【分析】(1)铁、碳以氯化钠溶液为电解质形成原电池,发生吸氧腐蚀生成氢氧根离子,溶液显碱性,遇到酚酞变红;(2)①K3[Fe(CN)6]溶液与二价铁离子反应生成蓝色沉淀;②温度升高,Fe还原性增强,反应速率加快;(3)①依据不同浓度下,检流计指针偏转方向判断电极,书写电极反应式;②要证明在饱和NaCl溶液中O2浓度较低,钢铁不易被腐蚀,可以设计对比试验,一个实验中通入氧气,另一个实验中不通入氧气,观察铁的腐蚀情况;(4)依据上述实验总结归纳解答。
全国高考化学化学能与电能的综合高考真题汇总含答案解析.docx

全国高考化学化学能与电能的综合高考真题汇总含答案解析一、化学能与电能-11.研究小组进行图所示实验,试剂 A 为 0.2 mol ·L CuSO4溶液,发现铝条表面无明显变化,于是改变实验条件,探究铝和CuSO4溶液、 CuCl2溶液反应的影响因素。
用不同的试剂A 进行实验1~实验 4,并记录实验现象:实验试剂 A实验现象序号1-12铝条表面有气泡产生,并有红色固体析出0.2 mol L· CuCl 溶液-14开始铝条表面无明显变化,加NaCl 后,铝条表20.2 mol L· CuSO 溶液,再加入一定质量的 NaCl 固体面有气泡产生,并有红色固体析出3-14铝条表面有少量气泡产生,并有少量红色固体2 mol L· CuSO 溶液4-1溶液反应非常剧烈,有大量气泡产生,溶液变成棕褐2 mol L· CuCl2色,有红色固体和白色固体生成(1)实验 1中,铝条表面析出红色固体的反应的离子方程式为_________。
(2)实验 2的目的是证明铜盐中的阴离子Cl-是导致实验 1 中反应迅速发生的原因,实验2 中加入 NaCl 固体的质量为 _________ g。
(3)实验 3 的目的是 _________。
(4)经检验知,实验 4 中白色固体为 CuCl。
甲同学认为产生白色固体的原因可能是发生了 Cu + CuCl22CuCl 的反应,他设计了右图所示实验证明该反应能够发生。
① A 极的电极材料是_________。
②能证明该反应发生的实验现象是_________。
(5)为探究实验 4 中溶液呈现棕褐色的原因,分别取白色CuCl固体进行以下实验:实验序号实验操作实验现象i加入浓 NaCl 溶液沉淀溶解,形成无色溶液ii加入饱和 AlCl 溶液沉淀溶解,形成褐色溶液3iii向 i 所得溶液中加入- 1CuCl2溶液溶液由无色变为褐色2 mol L·查阅资料知: CuCl 难溶于水,能溶解在Cl-浓度较大的溶液中,生成[CuCl2] -络离子,用水稀释含 [CuCl2]-的溶液时会重新析出CuCl 沉淀。
高考化学专题复习化学能与电能的综合题附答案解析

高考化学专题复习化学能与电能的综合题附答案解析一、化学能与电能1.甲同学向做过银镜反应的试管滴加0.1mol/L的Fe(NO3)3溶液(pH=2),发现银镜部分溶解,和大家一起分析原因:甲同学认为:Fe3+具有氧化性,能够溶解单质Ag。
乙同学认为:Fe(NO3)3溶液显酸性,该条件下NO3-也能氧化单质Ag。
丙同学认为:Fe3+和NO3-均能把Ag氧化而溶解。
(1)生成银镜反应过程中银氨溶液发生_____________(氧化、还原)反应。
(2)为得出正确结论,只需设计两个实验验证即可。
实验I:向溶解了银镜的Fe(NO3)3的溶液中加入____________(填序号,①KSCN溶液、②K3[Fe(CN)6]溶液、③稀HC1),现象为___________,证明甲的结论正确。
实验Ⅱ:向附有银镜的试管中加入______________溶液,观察银镜是否溶解。
两个实验结果证明了丙同学的结论。
(3)丙同学又把5mLFeSO4溶液分成两份:第一份滴加2滴KSCN溶液无变化;第二份加入1mL0.1mol/LAgNO3溶液,出现白色沉淀,随后有黑色固体产生(经验证黑色固体为Ag颗粒),再取上层溶液滴加KSCN溶液变红。
根据上述的实验情况,用离子方程式表示Fe3+、Fe2+、Ag+、Ag之间的反应关系_______________。
(4)丁同学改用如图实验装置做进一步探究:①K刚闭合时,指针向左偏转,此时石墨作_________,(填“正极”或“负极。
此过程氧化性:Fe3+_______Ag+(填>或<)。
②当指针归零后,向右烧杯中滴加几滴饱和AgNO3溶液,指针向右偏转。
此过程氧化性:Fe3+_______Ag+(填>或<)。
③由上述①②实验,得出的结论是:_______________________。
【答案】还原②产生蓝色沉淀 pH=2 0.3mol/L KNO3或NaNO3溶液 Ag + Fe3+ ⇌Ag+ + Fe2+或(Ag+ + Fe2+ ⇌Ag + Fe3+) 正极><其它条件不变时,物质的氧化性与浓度有关系,浓度的改变可导致平衡的移动【解析】【分析】(1)根据元素化合价的变化判断;(2)实验Ⅰ:甲同学认为:Fe3+具有氧化性,能够溶解单质Ag,则要证明甲的结论正确,可验证Fe3+的还原产物Fe2+的存在;实验Ⅱ:进行对照实验;(3)根据实验现象判断溶液中发生的反应;(4)根据指针偏转方向判断正负极,判断电极反应,并结合氧化还原反应中氧化剂的氧化性大于氧化产物分析解答。
高考化学专题题库∶化学能与电能的综合题及答案解析

高考化学专题题库∶化学能与电能的综合题及答案解析一、化学能与电能1.氯化亚砜又称亚硫酰氯,其分子式为 SOCl2,常温常压下为淡黄色液体,遇水易水解。
国内的氯化亚砜主要应用于医药、农药、染料等行业。
实验室用干燥纯净的 Cl2、SO2和SCl2制备 SOCl2的部分装置如图所示:已知:①SOCl2沸点为 78.8℃,SCl2 的沸点为 50℃,且两种液体可互溶。
②SOCl2遇水剧烈反应,液面上产生白雾,并有气体产生。
请回答:(1)实验室制取 SOCl2的反应方程式为____________(2)写出丙中发生的离子反应_____________(3)仪器 e 的名称是___________,实验仪器的连接顺序为a→_________(仪器可以重复使用)。
(4)仪器 f 的作用是 ____________(5)实验结束后,将三颈烧瓶中混合物分离的实验操作名称是______。
(6)工业上常用 ZnCl2·2H2O 与 SOCl2共热制取 ZnCl2。
写出用惰性电极电解ZnCl2和盐酸的混合溶液的总反应离子反应式为_______。
甲同学认为 SOCl2还可用作FeCl3·6H2O 制取无水FeCl3的脱水剂,但乙同学对此提出质疑,可能的原因是____【答案】SO2+Cl2+SCl22SOCl22MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O球形冷凝管c→d→c→d→b吸收SO2、Cl2,防止外界水蒸气进入装置分馏(或蒸馏)2H++2Cl—H2↑+Cl2↑SOCl2可能会与Fe3+发生氧化还原反应【解析】【分析】由实验装置图可知,丙装置中浓盐酸与高锰酸钾反应制备氯气,因氯气中混有氯化氢和水蒸气,所以先将气体通过盛有饱和食盐水的乙装置除去氯化氢,再通过盛有浓硫酸的乙装置除去水蒸气,干燥的氯气、二氧化硫和SCl2在三颈烧瓶中,在活性炭作催化剂作用下,反应制得SOCl2,二氯化硫(SCl2)的沸点低,甲装置中球形冷凝管的作用是起冷凝回流SCl2的作用,干燥管中碱石灰的作用是防止有毒的氯气与二氧化硫逸出污染环境,同时防止空气中的水蒸气进入烧瓶中使氯化亚砜水解。
高考化学化学能与电能综合经典题及答案解析
高考化学化学能与电能综合经典题及答案解析一、化学能与电能1.二氧化氯(ClO2)具有强氧化性,在工业上常用作水处理剂、漂白剂。
ClO2是一种易溶于水的黄绿色气体,其体积分数超过10%时易引起爆炸。
某研究小组欲用以下三种方案制备ClO2,回答下列问题:(1)以黄铁矿(FeS2)、氯酸钠和硫酸溶液混合反应制备ClO2,黄铁矿中的硫元素在酸性条件下被ClO3-氧化成SO42-,写出制备ClO2的离子方程式__。
(2)用过氧化氢作还原剂,在硫酸介质中还原NaClO3制备ClO2,并将制得的ClO2用于处理含CN-废水。
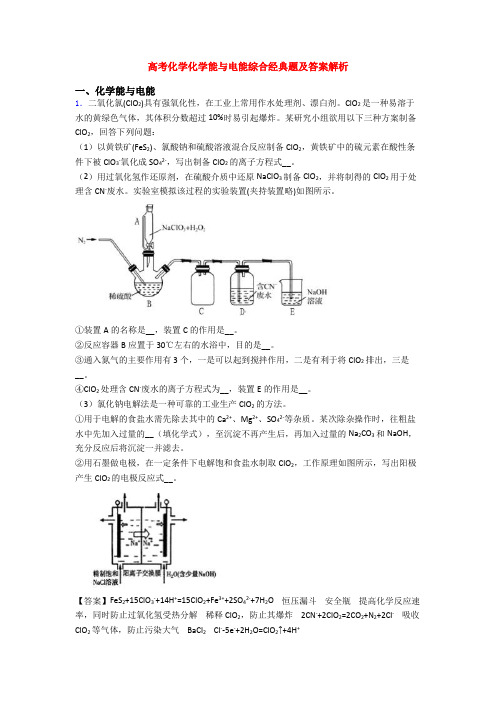
实验室模拟该过程的实验装置(夹持装置略)如图所示。
①装置A的名称是__,装置C的作用是__。
②反应容器B应置于30℃左右的水浴中,目的是__。
③通入氮气的主要作用有3个,一是可以起到搅拌作用,二是有利于将ClO2排出,三是__。
④ClO2处理含CN-废水的离子方程式为__,装置E的作用是__。
(3)氯化钠电解法是一种可靠的工业生产ClO2的方法。
①用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO42-等杂质。
某次除杂操作时,往粗盐水中先加入过量的__(填化学式),至沉淀不再产生后,再加入过量的Na2CO3和NaOH,充分反应后将沉淀一并滤去。
②用石墨做电极,在一定条件下电解饱和食盐水制取ClO2,工作原理如图所示,写出阳极产生ClO2的电极反应式__。
【答案】FeS2+15ClO3-+14H+=15ClO2+Fe3++2SO42-+7H2O 恒压漏斗安全瓶提高化学反应速率,同时防止过氧化氢受热分解稀释ClO2,防止其爆炸 2CN-+2ClO2=2CO2+N2+2Cl-吸收ClO2等气体,防止污染大气 BaCl2 Cl--5e-+2H2O=ClO2↑+4H+【分析】二氧化氯(ClO2)具有强氧化性,在工业上常用作水处理剂、漂白剂。
分别利用无机反应和电解原理制备二氧化氯,三种方法均利用了氧化还原反应。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高考化学化学能与电能综合试题附答案解析一、化学能与电能1.硝酸是氧化性酸,其本质是NO3-有氧化性,某课外实验小组进行了下列有关NO3-氧化性的探究(实验均在通风橱中完成)。
实验装置编号溶液X实验现象实验Ⅰ 6 mol·L-1稀硝酸电流计指针向右偏转,铜片表面产生无色气体,在液面上方变为红棕色。
实验Ⅱ15 mol·L-1浓硝酸电流计指针先向右偏转,很快又偏向左边,铝片和铜片表面产生红棕色气体,溶液变为绿色。
(1)实验Ⅰ中,铝片作____________(填“正”或“负”)极。
液面上方产生红棕色气体的化学方程式是____________。
(2)实验Ⅱ中电流计指针先偏向右边后偏向左边的原因是________________。
查阅资料:活泼金属与1 mol·L-1稀硝酸反应有H2和NH4+生成,NH4+生成的原理是产生H2的过程中NO3-被还原。
(3)用上图装置进行实验Ⅲ:溶液X为1 mol·L-1稀硝酸溶液,观察到电流计指针向右偏转。
① 反应后的溶液中含NH4+。
实验室检验NH4+的方法是________。
② 生成NH4+的电极反应式是________。
(4)进一步探究碱性条件下NO3-的氧化性,进行实验Ⅳ:① 观察到A中有NH3生成,B中无明显现象。
A、B产生不同现象的解释是________。
②A中生成NH3的离子方程式是________。
(5)将铝粉加入到NaNO3溶液中无明显现象,结合实验Ⅲ和Ⅳ说明理由________。
【答案】负 2NO+O2=2NO2 Al开始作电池的负极,Al在浓硝酸中迅速生成致密氧化膜后,Cu作负极取少量待检溶液于试管中,加入浓NaOH溶液,加热,若产生使湿润的红色石蕊试纸变蓝的气体,则溶液中含NH4+ NO3-+8e-+10 H+=NH4++3H2O Al与NaOH溶液反应产生H2的过程中可将NO3-还原为NH3,而Mg不能与NaOH溶液反应 8Al+3NO3-+5OH-+2H2O=3NH3↑+8AlO2-因为铝与中性的硝酸钠溶液无生成H2的过程,NO3-无法被还原【解析】【分析】【详解】(1)实验Ⅰ中,由于Al的金属活动性比Cu强,因此Al做负极。
铜片表面产生的无色气体是NO,在液体上方NO被空气中的氧气氧化成红棕色的NO2,方程式为2NO+O2=2NO2;(2)实验Ⅱ中, Al的金属活动性比Cu强,Al开始作电池的负极,电流计指针先偏向右边;由于Al在浓硝酸中迅速生成致密氧化膜,阻止了内层金属的进一步反应,因此,Cu 作负极,电流计指针偏向左边;(3)①实验室检验NH4+有两种常用方法:方法一,取少量待检溶液于试管中,加入浓NaOH溶液,加热,若产生使湿润的红色石蕊试纸变蓝的气体,则溶液中含NH4+;方法二,取少量待检溶液于试管中,加入浓NaOH溶液,加热,并在试管口放一蘸有浓盐酸的玻璃棒,若有白烟生成,证明溶液中含NH4+;②NH4+的生成是NO3-被还原的结果,其电极反应式为NO3-+8e-+10 H+=NH4++3H2O(4)①观察到A中有NH3生成,是由于Al与NaOH溶液反应产生H2,并且与此同时,H2可将NO3-还原为NH3;B中无现象是由于Mg与NaOH溶液不反应;②A中生成NH3的离子方程式为 8Al+3NO3-+5OH-+2H2O=3NH3↑+8AlO2-;(5)铝与中性的硝酸钠溶液不能生成H2, NO3-无法被还原,因此将铝粉加入到NaNO3溶液中无明显现象。
2.亚硝酰氯NOCl可用于合成清洁剂等。
它可用Cl2与NO在常温常压下合成:它的熔点为-64.5℃,沸点为-5.5℃,常温下是黄色的有毒气体,遇水易水解。
请按要求回答下列相关问题:(1)过量铁屑和稀硝酸充分反应制备NO的离子方程式为:______________________。
(2)制备NOCl的装置如下图所示,连接顺序为:a→_________________________(按气流自左向右方向,用小写字母表示)。
①装置A和B作用是①干燥NO和Cl2,②___________________________________________。
②装置D的作用是______________________________________。
③装置E中NOCl发生反应的化学方程式为________________。
(3)工业生产过程中NO尾气处理方法有多种,其中间接电化学法,其原理如图所示:该过程中阴极的电极反应式为:__________________________________________。
【答案】3Fe+8H++2NO3—=3Fe2++2NO↑+4H2O e→f→c→b→d或f→e→c→b→d观察气泡调节气体流速防止E中水蒸气进入F,引起NOCl的水解 NOCl+2NaOH=NaCl+NaNO2+H2O 2HSO3—+2e—+2H+= S2O42—+ 2H2O【解析】【分析】(1)过量铁屑和稀硝酸反应生成硝酸亚铁、一氧化氮和水;(2)将氯气和NO干燥后在装置F中发生反应,在冰盐中冷凝收集NOCl,氯气、NO以及NOCl均不能排放到空气中,用氢氧化钠溶液吸收,注意NOCl遇水易水解。
(3)由间接电化学法示意图可知,阴极上HSO3—放电生成S2O42—,S2O42—在吸收塔中将NO还原为N2。
【详解】(1)过量铁屑和稀硝酸反应生成硝酸亚铁、一氧化氮和水,反应的离子方程式为3Fe+8H++2NO3—=3Fe2++2NO↑+4H2O,故答案为3Fe+8H++2NO3—=3Fe2++2NO↑+4H2O;(2)将氯气和NO干燥后在装置F中发生反应,在冰盐中冷凝收集NOCl,氯气、NO以及NOCl均不能排放到空气中,用氢氧化钠溶液吸收,NOCl遇水易水解,故在收集装置和尾气处理装置之间需加一个干燥装置,故答案为e→f(或f→e)→c→b→d;①装置A和B作用是除干燥NO、Cl2外,另一个作用是通过观察气泡调节气体的流速控制反应的发生,故答案为观察气泡调节气体流速;②NOCl遇水易水解,装置D中氯化钙做干燥剂,吸收水蒸气,防止E中水蒸气进入反应器F中,引起NOCl的水解,故答案为防止E中水蒸气进入F,引起NOCl的水解;③装置E的目的吸收尾气,防止污染环境,NOCl与氢氧化钠溶液反应生成NaCl、NaNO2和H2O,反应的化学方程式为NOCl+2NaOH=NaCl+NaNO2+H2O,故答案为NOCl+2NaOH=NaCl+NaNO2+H2O;(3)由间接电化学法示意图可知,阴极上HSO3—放电生成S2O42—,S2O42—在吸收塔中将NO还原为N2,阴极的电极反应式为2HSO3—+2e—+2H+= S2O42—+ 2H2O,故答案为2HSO3—+2e—+2H+= S2O42—+ 2H2O。
【点睛】本题考查化学实验方案的设计与评价,侧重考查分析问题和解决问题的能力,注意化学方程式的书写和排列实验先后顺序的方法,掌握电极反应式的书写方法是解答关键,3.甲同学向做过银镜反应的试管滴加0.1mol/L的Fe(NO3)3溶液(pH=2),发现银镜部分溶解,和大家一起分析原因:甲同学认为:Fe3+具有氧化性,能够溶解单质Ag。
乙同学认为:Fe(NO3)3溶液显酸性,该条件下NO3-也能氧化单质Ag。
丙同学认为:Fe3+和NO3-均能把Ag氧化而溶解。
(1)生成银镜反应过程中银氨溶液发生_____________(氧化、还原)反应。
(2)为得出正确结论,只需设计两个实验验证即可。
实验I:向溶解了银镜的Fe(NO3)3的溶液中加入____________(填序号,①KSCN溶液、②K3[Fe(CN)6]溶液、③稀HC1),现象为___________,证明甲的结论正确。
实验Ⅱ:向附有银镜的试管中加入______________溶液,观察银镜是否溶解。
两个实验结果证明了丙同学的结论。
(3)丙同学又把5mLFeSO4溶液分成两份:第一份滴加2滴KSCN溶液无变化;第二份加入1mL0.1mol/LAgNO3溶液,出现白色沉淀,随后有黑色固体产生(经验证黑色固体为Ag颗粒),再取上层溶液滴加KSCN溶液变红。
根据上述的实验情况,用离子方程式表示Fe3+、Fe2+、Ag+、Ag之间的反应关系_______________。
(4)丁同学改用如图实验装置做进一步探究:①K刚闭合时,指针向左偏转,此时石墨作_________,(填“正极”或“负极。
此过程氧化性:Fe3+_______Ag+(填>或<)。
②当指针归零后,向右烧杯中滴加几滴饱和AgNO3溶液,指针向右偏转。
此过程氧化性:Fe3+_______Ag+(填>或<)。
③由上述①②实验,得出的结论是:_______________________。
【答案】还原②产生蓝色沉淀 pH=2 0.3mol/L KNO3或NaNO3溶液 Ag + Fe3+ ⇌Ag+ + Fe2+或(Ag+ + Fe2+ ⇌Ag + Fe3+) 正极><其它条件不变时,物质的氧化性与浓度有关系,浓度的改变可导致平衡的移动【解析】【分析】(1)根据元素化合价的变化判断;(2)实验Ⅰ:甲同学认为:Fe3+具有氧化性,能够溶解单质Ag,则要证明甲的结论正确,可验证Fe3+的还原产物Fe2+的存在;实验Ⅱ:进行对照实验;(3)根据实验现象判断溶液中发生的反应;(4)根据指针偏转方向判断正负极,判断电极反应,并结合氧化还原反应中氧化剂的氧化性大于氧化产物分析解答。
【详解】(1)往AgNO3溶液中逐滴加入氨水,银离子和氨水反应生成白色的氢氧化银沉淀和铵根离子,Ag++NH3•H2O═AgOH↓+NH4+;继续滴入氨水白色沉淀溶解,氢氧化银和氨水反应生成银氨溶液和水,AgOH+2NH3•H2O═Ag(NH3)2OH+2H2O,若用乙醛进行银镜反应,再加入乙醛溶液后,水浴加热,生成乙酸铵,氨气、银和水,化学反应方程式为:CH3CHO+2Ag(NH3)2OHΔ−−→CH3COONH4+2Ag↓+3NH3+H2O,银氨溶液中的银为+1价,被醛基还原生成0价的银单质,故答案为:还原;(2)实验Ⅰ:甲同学认为:Fe3+具有氧化性,能够溶解单质Ag,则要证明甲的结论正确,可验证Fe3+的还原产物Fe2+的存在即可,验证Fe2+的实验是取少量除尽Ag+后的溶液于试管中,加入K3[Fe(CN)6]溶液会和Fe2+反应生成蓝色沉淀,故答案为:②;产生蓝色沉淀;实验Ⅱ:丙同学认为:Fe3+和NO3-均能把Ag氧化而溶解,且两个实验结果证明了丙同学的结论,而实验I验证了Fe3+具有氧化性,能够溶解单质Ag,则实验II需要验证NO3-也能把Ag氧化而溶解,需进行对照实验,0.1mol/L的Fe(NO3)3溶液(pH=2),NO3-为0.3 mol/L,所以需向附有银镜的试管中加入pH=2的 0.3 mol/L KNO3或NaNO3溶液,故答案为:pH=2的 0.3 mol/L KNO3或NaNO3;(3)Fe3+遇KSCN溶液变红,第一份滴加2滴KSCN溶液无变化,说明FeSO4溶液中无Fe3+,第二份加入1ml 0.1mol/L AgNO3溶液,出现白色沉淀,随后有黑色固体Ag产生,再取上层溶液滴加KSCN溶液变红,说明有Fe3+产生,说明Fe2+被Ag+氧化生成Fe3+,Ag+被还原为Ag,又Fe3+具有氧化性,能够溶解单质Ag,则该反应为可逆反应,反应的离子方程式为:Fe3++Ag⇌Fe2++Ag+或Ag++Fe2+⇌Ag+Fe3+;(4)①K刚闭合时,指针向左偏转,则银为负极,石墨为正极,该电池的反应本质为Fe3++Ag⇌Fe2++Ag+,该反应中铁离子为氧化剂,银离子为氧化产物,则氧化性:Fe3+>Ag+,故答案为:正极;>;②当指针归零后,向右烧杯中滴加几滴饱和AgNO3溶液,指针向右偏转,则此时石墨为负极,银为正极,右侧烧杯中银离子浓度增大,反应Fe3++Ag⇌Fe2++Ag+的平衡左移,发生反应Ag++Fe2+⇌Ag+Fe3+,此时Ag+为氧化剂,Fe3+为氧化产物,则氧化性:Fe3+<Ag+;③由上述①②实验,得出的结论是:在其它条件不变时,物质的氧化性与浓度有关,浓度的改变可导致平衡移动。
