北大《定量化学分析简明教程》
(完整版)北京大学有机化学实验要点总结

(完整版)北京⼤学有机化学实验要点总结据当年出题助教给的要点进⾏的总结(见⽂末图⽚),可能由没写全或者⾃⼰⽐较熟悉就没总结的地⽅,每年考核重点也在变化,仅供参考,⼀般考试涉及知识点很全,没有考不到,只有想不到,思考题也要复习到,会有原题内容:重⾯不重点,包括绪论课,实验基础知识与基本操作。
⾊谱、合成实验等。
题型:填空题,图释题,纠错题,简答题,综合题绪论课知识点提要1. 产率的计算:理论产量:根据反应式原料全部转化成产物的数量。
实际产量:实验中获得的纯产物的数量。
产率:实际产量/理论产量*100%。
[1.71/(210*0.0100)]*100%=81.4% 注意有效数字2. 环保要求:节约;回收(所有产品和部分溶液需要回收)严禁使⽤有机溶剂清洗仪器(浪费、⼄醇等易燃的不能直接倒⼊⽔池中)2. 防⽕:不能⽤烧杯或敞⼝容器盛装易燃物⾦属着⽕只能⽤黄沙灭⽕有贵重仪器的实验室不能⽤⼲淀粉灭⽕器因为⼲粉灭⽕器中含有NaHCO3,受热分解产⽣H2O,导致⼲粉附着在仪器表⾯损坏仪器,精密仪器的灭⽕应该使⽤3. 防爆:常压蒸馏禁⽌在封闭体系内进⾏4. 部分危险品标志5. 个⼈安全:紧急洗眼器的位置:每个实验台上,⽔龙头旁边;淋浴花洒的位置:楼道⾥;灭⽕器的位置:6. 浓酸烧伤:⼤量⽔洗,3-5%碳酸氢钠溶液洗,涂烫伤油膏。
浓碱烧伤:⼤量⽔洗,1-2%硼酸溶液洗,涂烫伤油膏。
7. 取样注意事项:玻璃棒转移液体,镍勺、刮⼑转移固体取样:取出的试剂……⽴即盖好药瓶的瓶盖……回收试剂,切记不要与原试剂混淆……药品遗洒后必须⽴刻清理(尤其使⽤电⼦天平,上⾯不能残留任何药品)。
8. 升华法:⽔蒸⽓蒸馏法:9. 有机化学⽂献常见英⽂缩写:10. 临床药物合成阿司匹林的⽅法:(酸酐)(酰氯)11. 化学设计多步合成12. 药物⼿性差异导致疗效不同还会考各仪器名称,⼀些不常⽤的⼀定要记住,会考实验装置图第⼀次实验提要1. 位置:门;通风橱:实验室两头2. 常压蒸馏:在⼀个⽓压下进⾏,利⽤蒸馏操作分离两种混溶液体的操作【原理】蒸汽压:由于分⼦运动,液体分⼦有变为⽓体分⼦的倾向,⽤来衡量这种倾向⼤⼩的客观量度为蒸汽压。
《分析化学》电子教材

《分析化学》电子教材使用教材:《分析化学》(第五版)上册武汉大学主编教学参考书:1.《定量分析化学简明教程》彭崇慧等编2.《定量分析中的误差和数据评价》宋清编3.《分离及复杂物质的分析》邵令娴编4.Analytical Chemistry(中译本:李克安等译,分析化学,北京大学出版社,2001)5.Modern Analytical Chemistry, D.Harvey(McGraw Hill)教学课时安排:共15周每周4学时共60学时�第1章概论(4学时)�第2章分析试样的采集与制备(2学时)�第3章分析化学中的误差和数据处理(8学时)�第4章分析化学中的质量保证与质量控制(2学时)�第5章酸碱滴定法(10学时)�第6章络合滴定法(8学时)�第7章氧化还原滴定法(8学时)�第8章沉淀滴定法和滴定分析小结(2学时)�第9章重量分析法(6学时)�第10章吸光光度法(6学时)�第11章分析化学中常用的分离和富集方法(4学时)第1章概论教学目的:1.理解分析化学的学科定义、任务及分类;2.掌握分析方法的选择原则;3.掌握定量分析基本过程及分析结果的表示方法;4.掌握滴定分析法基本原理、相关概念及滴定分析结果的结算。
教学重点:正确理解以下概念:标准溶液、基准物质、滴定分析法、滴定、化学计量点、滴定终点、终点误差;分析化学的分类。
教学难点:根据滴定反应确定计量关系并进行相关的计算。
教学内容:1.1分析化学的定义、任务和作用定义:分析化学是研究测定物质组成的分析方法及其相关理论的科学。
其他定义:itinen:化学表征与测量的科学。
任务:鉴定物质的化学成分定性分析测定各组分的含量定量分析确定物质的结构结构分析作用:a.21世纪是生命和信息科学的世纪,科技和社会生产发展的需要要求分析化学尽可能快速、全面和准确地提供丰富地信息和有用的数据。
b.现代分析化学正在把化学与数学、物理学、计算机科学、生物学、精密仪器制造科学等学科结合起来。
北京大学招生简章-北大化学(化学基因组学)考研招生简章、专业目录、参考书、报录比、分数线

九、违纪处罚 若发现考生有申报虚假材料、考试作弊及其它违反考试纪律的行为,我校将通知其所在单位,并按教育部《国家 教育考试违规处理办法》进行严肃处理。
北大化学(化学基因组学)考研报录比
应试生(含全国统考、专业学位联考、单独考试及专项计划)
院系名称 学科专业名称
2011 年ቤተ መጻሕፍቲ ባይዱ
2012 年
2013 年
报考 录取 百分比 报考 录取 百分比 报考 录取 百分比
合计
667 163 24.44 1193 296 24.81 1309 391 29.87
西方经济学
(5)已获硕士、博士学位的人员。在校研究生报考须在报名前征得所在培养单位同意。 5、以同等学力身份报考我校的考生,须在国家核心期刊上发表一篇以上与所报考专业相关的学术论文(署名前 2
位)。除复试外还须加试两门本科专业基础课,部分专业还将加试实验等科目。 6、参加专业学位考试考生的报考条件,详见在我校研究生院招生网页(网址:
启道考研—专注北京名校考研|保研|考博辅导 /
7、复试成绩不及格者不予录取。复试成绩及格者能否录取,以考生的总成绩名次为准。总成绩包括两部分,即初 试成绩和复试成绩。复试成绩占总成绩的权重一般在 30%至 50%的范围内。
8、复试实行差额复试,择优录取。具体差额比例和初试、复试成绩所占权重由各院系根据本学科、专业特点及生 源状况在复试前确定。对于经过初试和复试仍不能确定是否录取的考生,我校将进一步组织复试。
1、各院系推免生遴选工作小组对申请材料初审后,通知通过初审的申请者来我校参加复试。 2、复试实行差额复试,择优录取。具体差额比例由各院系根据自身特点和生源状况自行确定。 3、选拔办法由各院系根据其学科特点制定,笔试或面试不及格者不予录取。选拔办法一经公布不得随意更改。 4、推免生的综合面试时间原则上不少于 20 分钟。北大化学(化学基因组学)考研 (三)、待录取与公示 1、院系通过教育部推免服务系统向拟接收的申请者发送待录取通知,请申请者在院系规定的时间内在网上确认是 否接受待录取。若在规定时间内未确认,则视为放弃。 2、我校不再另行向接收的推荐免试研究生(含硕士生和直博生)发送接收函。 3、2014 年 10 月 25 日前,院系在网上公示待录取名单。推免生可登录院系网站查询公示名单,或在研究生院硕士、 博士招生网页的“录取信息”查询。若有疑问,可于公示期内向院系提出,各院系予以及时答复。 (四)、复审与录取 在正式发出录取通知书之前,我校将对获得待录取资格的推免生,按照我校有关要求进行资格复审,未通过者将 被取消录取资格。北大化学(化学基因组学)考研 二、报名考试 (一)、报考条件 报名参加全国统一考试,须符合下列条件: 1、中华人民共和国公民。 2、拥护中国共产党的领导,品德良好,遵纪守法。 3、身体健康状况符合国家和我校规定的体检要求。 4、考生的学历必须符合下列条件之一:
(完整版)分析化学(高教第四版)习题及答案(第一章:定量分析化学概论)

分析化学习题及答案(第四版)第一章:定量分析化学概论5. 某试样中汉MgO约30%,用定量法测定时,Fe有1%进入沉淀。
若要求测定结果的相对误差小于0.1%,求试样中Fe2O3允许的最高质量分数为多少?解:设Fe2O3的质量分数为Fe2O3,试样质量记为m样测定的相对误差= =即 0.1% =Fe2O3 2Fe , nFe O = nFeFe O = ,nFe O = mFe=nFe MFe=2nFe2O3 MFe=2 MFe=代入0.1%=0.001=Fe O =0.043=4.3%6. 某含Cl-试样中含有0.10%Br-,用AgNO3进行滴定时,Br-与Cl-同时被滴定,若全部以Cl-计算,则结果为20.0%。
求称取的试样为下列质量时,Cl-分析结果的绝对误差及相对误差:a. 0.1000g, b. 0.5000g, c. 1.000g.解:设Cl- 真实含量x,称取试样质量ms(g)。
则0.2000=x+∴x=0.200-0.001 =0.200-4.4 10-4=0.1996E=x-T∴绝对误差:4.4 10-4(即0.044%)相对误差: 100%=0.22%7. 某试样中含有约5%的S,将S氧化为SO42-,然后沉淀为BaSO4。
若要求在一台灵敏度为0.1mg的天平上称量BaSO4的质量时可疑值不超过01.%,问必须称取试样多少克?解:设必须称取x克S -- SO42---BaSO432.066 233.39x 5% m BaSO天平上的绝对误差 0.1mg 2 (两次读取)相对误差= 0.1%=∴ x= = =0.6g8. 用标记为0.1000 HCl标准溶液标定NaOH溶液,求得浓度为0.1018 ,已知HCl溶液真实浓度为0.0999 ,标定过程中其他误差均小,可以不计,求NaOH溶液的真实浓度。
解:设真实浓度为x,则有OH-+H+=H2OHCL的相对误差应等于NaOH的相对误差所以 =∴x=0.10179. 称取纯金属锌0.3250g,溶于HCl后,稀释到250ml容量瓶中。
简明物理有机化学教程(8)

其中M表示迁移基团,﹡表示原子自身的带电性质(依次分别 表示为碳正离子、自由基、碳负离子)。
碳正离子的1,2-迁移反应 1922年,Meerwein和van Emster在研究萜类化合物重排反 应的机理时,提出反应经历了碳正离子1,2-烷基迁移的过程, 这被认为是碳正离子重排化学的起源。
邻二醇在酸作用下发生的频哪醇重排是由碳正离子经过 1,2-烷基(芳基)迁移重排为更加稳定的正离子。
除了基团从一个碳原子向缺电性的碳正离子迁移外, 也可以从碳原子向缺电性的其他原子(如N和O原子)上 迁移,伴随新的碳正离子的生成。
碳正离子的1,2-迁移反应经历“桥联键”(bridged bond)的过 渡态。迁移的 R 基团与两个碳原子形成三元环的结构,使 得正电荷得到分散,随后R基团发生迁移。
叶立德的形成是由于s,p的p-d轨道重叠,而氮原子却不可 能有这种效应,因为第二周期元素没有低能量的空d轨道可以 接受这种孤对电子。
8.6 中间体的1,2-迁移反应(1,2-shift)
1,2-迁移反应是有机化学反应中各类中间体所具有的共同 的反应类型。通过 1,2-迁移的过程,活泼反应中间体生成稳 定的中间体或产物。 活性中间体的 1,2-迁移反应是自由基、碳正离子、碳负 离子和卡宾等中间体的后续反应中所共有的一类重排反应。
有关碳正离子结构的实验 以下的实验可以间接说明碳正离子采取sp2杂化轨道。 实验一:下面三个三级溴化物在80% EtOH/H2O, 20 oC的 水解速率有非常大的差别。这里取代反应显然只能以SN1 机理进行。由于体系的刚性增大,形成平面结构的能量将 大为增加。水解反应速率的差别反映了中间体碳正离子的 稳定性,锥形的碳正离子是非常难形成的。
自由基的1,2-氢迁移被认为是十分困难的,因为在形成到足够的稳定。
物理书籍整理

科普:《定性与半定量物理学》赵凯华《边缘奇迹:相变和临界现象》于渌《QED: A Strange Theory about Light and Matter》Feynman《大宇之形》丘成桐《Gauge Fields, Knots and Gravity》Baez《趣味力学》别莱利曼《趣味刚体力学》刘延柱(小书,挺有意思)考研习题集用超星图书里的那本清华大学编写的普通物理学考研辅导教材(大约这个名字)数学分析:书目:《数学分析教程》常庚哲《数学分析新讲》张筑生《数学分析》卓里奇《数学分析八讲》辛钦《数学分析讲义》陈天权《数学分析习题课讲义》谢惠民等《数学分析习题集》北大版《特殊函数概论》王竹溪线性代数Linear Algebra内容:行列式、矩阵代数、线性方程组、线性空间、线性变换、欧几里得空间、n元实二次型等。
书目:《高等代数简明教程》蓝以中《Linear Algebra and Its Applications》Gilbert Strang《Linear Algebra and Its Applications》Peter D. Lax《Linear Algebra and Its Applications》David C. Lay力学Mechanics先修课程:高等数学内容:质点运动学、质点动力学、动量定理和动量守恒定律、功和能及碰撞问题、角动量、刚体力学、固体的弹性、振动、波动和声、流体力学、相对论简介。
书目:《力学》赵凯华《力学》舒幼生《经典力学》朗道《An Introduction To Mechanics》Daniel Kleppner、Robert Kolenkow狭义相对论:《狭义相对论》刘辽《The Principle of Relativity》Einstein广义相对论:《Einstein Gravity in a Nutshell》Zee《Spacetime and Geometry》Carroll热学Thermology先修课程:力学、高等数学内容:主要包括三部分,以实验为依据、以热力学第零定律、热力学第一定律、热力学第二定律为基本理论的宏观的热力学理论,研究物质宏观热现象和宏观状态变化规律;以气体分子统计物理学,研究大量分子热运动统计规律和热现象的微观实质;以Van der Waals方程和Clapeyron方程,研究气体状态变化及相变规律;以非平衡态理论的分子动理论,研究输运现象的宏观规律。
大学几乎所有学科课本答案

大学几乎所有学科课本答案来源:李殿武的日志经济金融[PDF格式]《会计学原理》同步练习题答案[Word格式]《成本会计》习题及答案(自学推荐,23页)[Word格式]《成本会计》配套习题集参考答案[Word格式]《实用成本会计》习题答案[Word格式]《会计电算化》教材习题答案(09年)[JPG格式]会计从业《基础会计》课后答案[Word格式]《现代西方经济学(微观经济学)》笔记与课后习题详解(第3版,宋承先)[Word格式]《宏观经济学》习题答案(第七版,多恩布什)[Word格式]《国际贸易》课后习题答案(海闻P.林德特王新奎)[PDF格式]《西方经济学》习题答案(第三版,高鸿业)可直接打印[Word格式]《金融工程》课后题答案(郑振龙版)[Word格式]《宏观经济学》课后答案(布兰查德版)[JPG格式]《投资学》课后习题答案(英文版,牛逼版)[PDF格式]《投资学》课后习题答案(博迪,第四版)[Word格式]《微观经济学》课后答案(高鸿业版)[Word格式]《公司理财》课后答案(英文版,第六版)[Word格式]《国际经济学》教师手册及课后习题答案(克鲁格曼,第六版)[Word格式]《金融市场学》课后习题答案(张亦春,郑振龙,第二版)[PDF格式]《金融市场学》电子书(张亦春,郑振龙,第二版)[Word格式]《微观经济学》课后答案(平狄克版)[Word格式]《中级财务会计》习题答案(第二版,刘永泽)[PDF格式]《国际经济学》习题答案(萨尔瓦多,英文版)[JPG格式]《宏观经济学》课后答案(曼昆,中文版)[PDF格式]《宏观经济学》答案(曼昆,第五版,英文版)pdf格式[Word格式]《技术经济学概论》(第二版)习题答案[Word格式]曼昆《经济学原理》课后习题解答[PDF格式]西方经济学(高鸿业版)教材详细答案[Word格式]完整的英文原版曼昆宏观、微观经济学答案[Word格式]《金融市场学》课后答案(郑振龙版)化学物理[Word格式]《固体物理》习题解答(方俊鑫版)[Word格式]《简明结构化学》课后习题答案(第三版,夏少武)[Word格式]《生物化学》复习资料大全(3套试卷及答案+各章习题集)[PDF格式]《光学教程》习题答案(第四版,姚启钧原著)[Word格式]《流体力学》实验分析答案(浙工大版)[Word格式]《高分子化学》课后习题答案(第四版,潘祖仁主编)[PDF格式]《化工热力学》习题与习题答案(含各种版本)[Word格式]《材料力学》习题答案[Word格式]《量子力学导论》习题答案(曾谨言版,北京大学)[PDF格式]《理论力学》习题答案(动力学和静力学)[Word格式]《大学物理》完整习题答案[PPT格式]流体输配管网习题详解(重点)[PDF格式]《结构化学基础》习题答案(周公度,北大版)[PDF格式]《物理化学》习题答案与课件集合(南大)[Word格式]《传热学》课后习题答案(第四版)[Word格式]《控制电机》习题答案[PDF格式]《化工原理答案》课后习题答案(高教出版社,王志魁主编,第三版)[PDF格式]《工程力学》课后习题答案(梅凤翔主编)[PDG格式]《工程电磁场导论》习题详解[PDF格式]《材料力学》习题答案(单辉祖,北京航空航天大学)[Word格式]《热工基础》习题答案(张学学主编,第二版,高等教育出版社)[Word格式]《大学物理实验》实验题目参考答案(第2版,中国林业出版社)[Word格式]《大学物理基础教程》课后习题答案(第二版,等教育出版社)[Word格式]《水力学》习题答案(李炜,徐孝平主编,武汉水利电力大学出版社)[PDF格式]《普通物理学教程电磁学》课后习题答案(梁灿斌,第2版)[Word格式]《激光原理与激光技术》习题答案完整版(北京工业大学出版社)[Word格式]《固体物理》习题解答(阎守胜版)[PPT格式]《仪器分析》课后答案(第三版,朱明华编)[Word格式]《高分子化学》习题答案(第四版)[PDF格式]《物理化学》习题答案(南大,第五版)[PPT格式]《高频电子线路》习题参考答案(第四版)[PDF格式]《原子物理学》习题答案(褚圣麟版)[PPT格式]《分析力学》习题答案[Word格式]《分析化学》习题答案(第三版,上册,高教版)[PPT格式]《普通物理》习题答案(磁学,电学,热学)[PDF格式]《材料力学》课后习题答案(单辉祖,第二版,高教出版社)[Word格式]《分析化学》课后习题答案(第五版,高教版)[Word格式]《分析化学》习题解答[Word格式]《理论力学》课后习题答案(赫桐生,高教版)[Word格式]《大学物理学》习题解答[PDF格式]《电动力学》习题答案(第三版,郭硕宏)[PDF格式]《大学物理》课后答案(陈信义)上下册的[PDF格式]《数学物理方法》(第三版)习题答案[JPG格式]《普通化学(第五版)》习题详解(配套浙大编的)[PDF格式]《光学》习题答案及辅导(赵凯华)[PDF格式]《工程光学》习题答案[PDF格式]《材料力学》详细习题答案及辅导(第四版,刘鸿文)[PDF格式]《电磁场与电磁波》(第4版)习题答案及自学辅导[PDF格式]《量子力学教程》习题解答(周世勋版)[Word格式]《流体力学》习题答案[PDF格式]《有机化学》课后习题答案(胡宏纹,第三版)[Word格式]《有机化学》习题答案(汪小兰主编)[Word格式]《化工热力学》习题及详细解答[PDF格式]《工程热力学》课后全解(第三版,沈维道编,高教版)[PDF格式]《理论力学》课后习题答案[Word格式]自动控制原理习题集(自学辅导推荐)[PDF格式]《自动控制原理》课后题答案(胡寿松,第四版)[PDF格式]大学物理习题及答案[PDF格式]《物理学》习题分析与解答(马文蔚主编,清华大学,第五版)[PDF格式]《电机与拖动基础》课后习题答案(第四版,机械工业出版社,顾绳谷主编)[Word格式]《土力学》习题解答/课后答案[PDF格式]《数学物理方法》习题解答案详细版(梁昆淼,第二版)[PDF格式]《传热学》课后答案(杨世铭,陶文铨主编,高教版)[PDF格式]《材料力学》详细辅导及课后答案(PDF格式,共642页)[Word格式]大学物理实验绪论课指导书及参考答案[Word格式]《大学基础物理学》课后答案(共16个单元)[PDF格式]流体力学课后答案(高教版,张也影,第二版)[PDF格式]程守洙、江之永主编《普通物理学》(第五版)详细解答及辅导电子信息[PDF格式]《数字通信》习题答案(第四版,Proakis)[PDF格式]《信号与系统》习题答案(第四版,吴大正)[Word格式]《基础电子技术》习题解答(哈工大,蔡惟铮)[Word格式]《微机原理及应用》习题答案[PPT格式]《通信电路》课后习题答案(沈伟慈,西安电子科技大学出版社)[JPG格式]《信号与系统》习题答案详解(郑君莉,清华大学,牛逼完整版)[PPT格式]《电路分析》习题答案(第2版,高等教育出版社,胡翔俊)[Word格式]《热工测量与自动控制》习题及答案[PDF格式]《信息论与编码》学习辅导及习题详解(傅祖芸版)[PDF格式]《电工学——电子技术》习题答案(下册)[PDF格式]《数字逻辑电路与系统设计》习题答案[Word格式]《数字电路与逻辑设计》课后习题答案,讲解详细[Word格式]《电工学》课后习题答案(第六版,上册,秦曾煌主编)[PDF格式]《数字信号处理》完整习题答案(程佩青,英文版)[Word格式]《微机原理》作业答案(李继灿版)[Word格式]《通信原理》课后习题答案及每章总结(樊昌信,国防工业出版社,第五版)[PDF格式]《信号与系统》课后习题答案[PDF格式]《数字电子技术基础》课后习题答案(完整答案版)[Word格式]《电子线路-非线性部分》课后答案(谢嘉奎高等教育出版社)[Word格式]《通信原理》习题答案[PDF格式]《电路分析》课后答案及学习指导(第二版,胡翔骏,高教版)[PDF格式]《数字信号处理——基于计算机的方法》习题答案(第二版)[PDF格式]《数字电子技术基础》详细习题答案(阎石第四版)[Word格式]《测控电路》习题答案(机械出版社)[Word格式]《电力电子技术》习题答案(第四版,王兆安,王俊主编)[Word格式]《单片机及接口技术》课后答案(梅丽凤,王艳秋,清华大学出版社)[PDF格式]《电路》习题答案上(邱关源,第五版)[PPT格式]《信息论与编码》辅导PPT及部分习题答案(曹雪虹,张宗橙,北京邮电大学出版社)[PDF格式]《电子电路分析与设计》课后题答案(英文版)[PDF格式]《电力电子技术》习题答案(第4版,西安交通大学)[Word格式]《自动控制原理》课后题答案(卢京潮主编,西北工业大学出版社)[Word格式]《控制工程基础》课后习题解答(清华版)[Word格式]《控制工程基础》习题答案(第二版,燕山大学)[PPT格式]《自动控制原理》习题答案[SWF格式]《微电子器件与IC设计》习题答案(科学出版社)[PDF格式]《电力拖动自动控制系统》习题答案[PDF格式]《电工学》习题答案(第六版,秦曾煌)[Word格式]《数字信号处理》习题答案[PDF格式]《信号与系统》习题及精解[PDF格式]《信号与系统》课后习题答案(于慧敏著)[PDF格式]《信号与系统》课后习题答案(西安电子科技大学)[Word格式]电子技术数字和模拟部分答案(第四版,康华光)[Word格式]《信息论与编码》习题答案(高等教育出版社)仇佩亮编[PDF格式]《现代控制系统》答案(英文版)730页[PDF格式]《数字电子技术》课后习题答案详解(阎石,第四版)[PDF格式]《数字电子技术基础》习题答案(阎石,第五版)[PDF格式]《信号与系统》习题详解(奥本海姆版)[PDF格式]《信号与线性系统分析》习题答案及辅导参考(吴大正版)[Word格式]《信号与系统》习题解析(燕庆明,第3版)非常详细[Word格式]《IBM-PC汇编语言》课后习题答案[PDF格式]《数字信号处理教程》习题解答(第二版)[PDF格式]《数字信号处理》课后答案及详细辅导(丁美玉,第二版)[Word格式]《现代通信原理》习题答案(曹志刚版)[Word格式]《模拟电子技术基础》详细习题答案(童诗白,华成英版,高教版)[Word格式]《模拟电子技术基础简明教程》课后习题答案(杨素行第三版)[Word格式]《单片机原理及应用》课后习题答案(张毅刚主编,高教版)[Word格式]《数字逻辑》(第二版)习题答案(欧阳明星主编)[PPT格式]《模拟电子技术基础》课后习题答案(共10章)[PDF格式]《数字逻辑》第四版习题答案法学政治[PDF格式]《公共关系学》习题及参考答案(复习必备)[Word格式]《公司法》课后练习及参考答案[Word格式]《国际经济法》课后参考答案[Word格式]思想道德修养与法律基础课后习题答案[Word格式]《毛泽东思想和中国特色社会主义理论体系概论》习题答案(2008年修订版的)[Word格式]《马克思主义基本原理概论》新版完整答案文学历史[PDF格式]《语言学概论》习题答案(自考,新版教材)[PDF格式]《语言学概论练习题》答案[PDF格式]《语言学教程》课后答案[Word格式]选修课《中国现当代文学》资料包[Word格式]《传播学教程》课后答案(郭庆光主编,完整版)[Word格式]现代汉语题库(语法部分)及答案[Word格式]《中国近代史纲要》课后习题答案[Word格式]《中国近现代史》选择题全集(共含250道题目和答案)[Word格式]《中国近代史纲要》完整课后答案(高教版)数学应用[Word格式]高等数学习题答案及提示[PDF格式]《线性代数》习题答案(魏福义,黄燕苹,中国农业出版社)[Word格式]《概率论与数理统计》8套习题及习题答案(自学推荐)[Word格式]《线性代数》9套习题+9套相应答案(自学,复习推荐)[PDF格式]《概率论与数理统计》习题册答案(四川大学版)[PDF格式]《近世代数基础》习题解答(张瑞禾版,高教版)[Word格式]《数值分析)大作业(详细,英文版)[PDF格式]《算法导论》课后习题答案(英文版)[Word格式]《概率论》完整习题答案(李贤平,复旦版)[Word格式]《概率论与数理统计》课后习题解答(东南大学出版社)[PDF格式]《数学分析》完整习题答案(第二版,陈传璋编,复旦大学高等教育出版社)[PDF格式]《概率论与数理统计》优秀学习资料[Word格式]《概率论与数理统计及其应用》课后答案(浙江大学盛骤谢式千编著)[Word格式]《常微分方程》习题解答(王高雄版)[PDF格式]《泛函分析》习题解答(张恭庆版)[Word格式]《线性代数》课后习题答案(陈维新,科学出版社)[PDF格式]《高等代数与解析几何》习题答案(同济大学)[PDF格式]《运筹学(第三版)》讲解和习题答案(清华大学出版社)[PDF格式]《复变函数》习题答案(第四版)[PDF格式]《理工类复习全书》课后答案详解(陈文灯)[PDF格式]《积分变换》习题答案(配套东南大学张元林编的)[Word格式]《离散数学》习题答案(高等教育出版社)[Word格式]《线性代数》习题解答(王中良)[Word格式]工程数学《概率统计简明教程》习题全解(高教版)[Word格式]《概率论与数理统计》习题答案(复旦大学出版社)[PDF格式]《概率论与数理统计》习题详解(浙大二、三版通用)[PDF格式]《复变函数与积分变换》习题答案[PPT格式]高等数学上下《习题PPT》[PPT格式]《概率论与数理统计》习题答案[Word格式]离散数学习题解答(第四版)清华大学出版社[Word格式]《统计学》课后答案(第二版,贾俊平版)[Word格式]《教育统计学》课后练习参考答案(共有12章)[PDF格式]高等数学(同济第五版)课后答案(PDF格式,共495页)[PDF格式]《线性代数》(同济第四版)课后习题答案(完整版)[PDF格式]统计学原理作业及参考答案[PDF格式]大学数学基础教程课后答案(微积分)医药农学[PDF格式]《遗传学》课后习题答案(朱军主编,完整版)[PDF格式]《普通动物学》完整课后答案(刘凌云,郑光美版)[Word格式]《动物学》习题集与答案(资料相当丰富)[PDF格式]《畜禽解剖学与组织胚胎学》习题答案参考[PDF格式]《微生物学》课后习题答案(周德庆版)[Word格式]药用植物的两份习题(自己感觉比较有用)英语外文[PDF格式]《大学英语自学教程》课后习题答案(上册)[PDF格式]《大学英语自学教程》课后习题答案(下册)[Word格式]新时代交互英语视听说2.3.4级答案[Word格式]多维教程-探索(研究生英语)课后习题答案答案[Word格式]《计算机英语(第2版)》参考译文[Word格式]《新编大学英语》课后答案(第三册)[Word格式]《全新版大学英语综合教程》(第四册)练习答案及课文译文[Word格式]《全新版大学英语综合教程》(第三册)练习答案及课文译文[Word格式]《全新版大学英语综合教程》(第二册)练习答案及课文译文[Word格式]《全新版大学英语综合教程》(第一册)练习答案及课文译文[PDF格式]《简明法语教程》配套习题答案[Word格式]新编大学英语4(外研版)课后练习答案[Word格式]《新视野大学英语读写教程(第二版)第三册》课后答案[Word格式]《新视野大学英语读写教程(第二版)第二册》课后答案[Word格式]新视野大学英语读写教程(第二版)第一册》课后答案[PDF格式]大学英语精读第3册答案(外教社)[PDF格式]21世纪大学英语读写教程(第四册)课后答案[PDF格式]21世纪大学英语读写教程(第三册)课文翻译[PDF格式]21世纪大学英语读写教程(第三册)参考答案[PDF格式]21世纪大学实用英语综合教程(第一册)课后答案及课文翻译计算机类[Word格式]《计算机原理》8套习题及答案(自学推荐)[PDF格式]《(C#)大学实用教程》习题答案(电子工业出版社,郭洪涛,刘丹妮,陈明华)[Word格式]《编译原理》习题答案(第二版)[PDF格式]《计算机操作系统》习题答案(汤子瀛版,完整版)[Word格式]《全国计算机等级考试二级教程——C语言程序设计》课后习题详解[Word格式]《汇编语言程序设计》习题答案(第二版,沈美明,温冬婵,清华大学出版社)[PDF格式]《计算机网络——自顶向下方法与Internet特色》习题答案(第三版,英文版)[Word格式]《C语言大学实用教程》全部参考答案(苏小红版)[Word格式]《全国计算机等级考试——三级C语言》上机100题+源程序[Word格式]《数据库系统概论》课后习题(第四版)[Word格式]《C语言程序设计》课后习题答案(地质出版社)[PDF格式]《操作系统概念》习题答案(第七版,英文版,影印版)[Word格式]《数据结构与算法分析》习题与解答[Word格式]《算机操作系统教程》习题详解(第二版)[PDF格式]《计算机组成与结构》习题讲解[HTM格式]数据结构1800例题与详细答案[Word格式]《计算机组成原理》课后习题答案(白中英主编第三版科学出版社)[CHM格式]《数据结构习题集》答案(C版,清华大学,严蔚敏)[Word格式]《VB程序设计》课后习题答案(第四版,邵洁主编的)[Word格式]C语言资料大全(有课后答案,自学资料,C程序等)[Word格式]《C语言》习题解答[Word格式]《C++程序设计》课后习题答案(第2版,吴乃陵,高教版)[Word格式]《数据库系统原理与设计》课后答案(第四版,王珊,萨师煊)[Word格式]《计算机网络》(第4版)习题答案(英文版)[Word格式]《计算机网络》习题答案(第三版,英文版)[Word格式]《计算机网络》课后习题答案(第5版和第4版)[PDF格式]《C语言设计》(谭浩强,第三版)227页[PDF格式]《数据与计算机通信》习题答案(第七版,英文版)[Word格式]《VB程序设计》习题答案(蒋加伏)[PDF格式]《数据库系统概论》习题答案(第四版)[PDF格式]《数字图象处理》习题答案(冈萨雷斯,第二版)[PDF格式]《c语言程序与设计》习题答案(谭浩强,第三版)[PDF格式]《编译原理》答案(陈火旺版,第三版)[Word格式]《编译原理》课后答案(清华版)[Word格式]《社会统计分析与SAS应用》习题及答案及程序数据[PDF格式]谢希仁《计算机网络教程》(第五版)习题参考答案(共48页)[PDF格式]网页设计与制作各章习题及答案[PDF格式]《社会统计分析与SAS 应用》习题及答案及程序数据机械制造[Word格式]《极限配合与测量技术基础》课程详解+习题+答案(自学必备)[Word格式]机械设计——《螺旋传动设计说明书》仅供参考[Word格式]《机电传动》课后习题答案(邓星钟版)[PDF格式]《机械原理》习题答案和超多例题(西北工业大学,第六版)[Word格式]液压试题库及参考答案(32页word,复习推荐)[Word格式]《汽车理论》1-4章编程(含源码,MATLAB编的程序)[Word格式]机械设计课程设计——带式运输机的传动装置的设计[PDF格式]《机械制造技术》习题集与答案解析[PPT格式]《画法几何》资料包(含习题答案,自学辅导课件)[PPT格式]《机械设计基础》大作业(轴承部件设计——直齿圆柱齿轮减速器的输出轴)[Word格式]安全人机工程海量习题及答案[Word格式]《汽车构造》习题集与详细答案[Word格式]《汽车构造》(底盘)习题集含答案[Word格式]《机械测试技术基础》习题答案[PDF格式]《机械原理》复习精要与习题精解(第7版,西北大学)[PPT格式]《机械制图》习题册答案(近机类、非机类,清华大学出版社)[Word格式]《化工设备机械基础》习题解答[Word格式]《钢结构设计原理》习题答案[Word格式]《汽车构造》习题集及答案,还有很很相关资料[Word格式]《机械优化设计》习题参考答案(第3版,孙靖民,哈工大)[Word格式]《汽车理论》课后答案详细解答(余志生,机械工业出版社)[PDF格式]《机械设计》课后习题答案(高教版,第八版,西北工业大学)[Word格式]《混凝土结构习题集》(适合自学辅导)[PDF格式]机械原理课程设计——压片机(附详细说明书)[Word格式]机械设计课程设计——二级斜齿圆柱齿轮减速器(WORD+原图)[Word格式]《机械工程测试技术基础》(第三版,熊诗波等主编)课后答案[Word格式]机械设计基础(第五版)习题答案[杨可桢等主编][Word格式]《液压传动》第2版思考题和习题解答(共36页)管理学类[PDF格式]《管理学》课后答案(周三多)[Word格式]《管理学——原理与方法》课后习题答案[Word格式]《管理学》课后习题答案(罗宾斯,人大版,第7版)[PDF格式]《管理信息系统简明教程》课后习题答案[Word格式]《组织行为学》习题集答案(参考下,还是蛮好的)[PDF格式]《财务管理学》章后练习参考答案(人大出版,第四版)[JPG格式]《管理理论与实务》课后题答案(手写版,中央财经大学,赵丽芬)[Word格式]《管理学》经典笔记(周三多,第二版)[Word格式]《汽车运输企业管理》配套习题集及答案[PDF格式]《管理运筹学》第二版习题答案(韩伯棠教授)教育体育[Word格式]《教育心理学》课后习题答案(皮连生版)[Word格式]教育统计与测量管理心理学(自考必备资料,牛逼打印版)[Word格式]《教育技术》课后习题答案参考(北师大)。
高中化学教辅书推荐

高中化学教辅书推荐篇一:高中化学参考书推荐※基础:1. 《高考学业水平考试课课通高一化学同步精讲与精炼(朱观华编,上海社会学院出版社)无论知识点还是题目都特基础,因此推荐大家在自己预习时候配套使用。
2. 《华东师大版一课一练》这个很基础,基本学校里的配套练习都用这个,我就不说了,大家都懂的。
※中等:1.《走进新课程课课练化学》(文汇出版社)这个是分年级的,和教材同步。
题目的设置上是层层递进的。
平时可以同步做。
2. 《新教材全解金牌教练》(吉林教育出版社)上海教材同步,内容递进,全面。
3. 《新标准精编教辅丛书最新版绿面书化学能力训练与提高》(上海教育出版社)中等难度,配有范例精讲,有题目多种解法,每个范例还有评注提出解题关键和注意点,并且配有训练题、单元测试,和上海教材配套。
关键还有个最大的好处,就是薄,刷起来比较有成就感。
还有解析非常详细。
4. 《高中知识清单》(首都师范大学,教育科学出版社)全国教材配套,概念配例题,比较详细,讲解清晰。
5. 《公式定理大全高中化学及时查》(机械工业出版社,冯建设主编)概念,基础,全国教材配套,上海可选用。
6. 《图解基础知识手册高中化学》(刘来刚主编吉林大学出版社)全国教材配套,知识点全面,总结归纳教好,疑点难点规律总结较好(基本为易错点、易考点),例题均有详细解析。
就是有些图总结的很怪:比如俯视仰视刻度线对于读数的影响,四大基本反应和氧化还原反应之间的关系,哈哈,可能是和我的习惯画法不同吧。
特点:除了正常目录(按知识体系分)之外,还有概念和知识点索引,是按拼音首字母排列的,方便查找。
以上4-6都属于真个高中知识点详析的书,建议从一开始学习的时候就可以同步的翻翻,做做题,高考复习的时候也可以用。
7. 《课标本教材完全解读王后雄学案》配苏教版(人教版等)高中化学分册分为必修1,必修2等篇二:高中化学竞赛用书推荐高中化学竞赛用书推荐常规/高考类:化学岛用户名:****************密码:woaihuaxuedao以下是另一个公邮密码:huaxuedaogongyou提供公共邮箱的目的还是方便大家交流,如果遇到超出流量限制的问题,可以直接把邮件转发出去。
《定量分析简明教程》习题二参考答案

一、 选择题1、用同一NaOH 滴定相同浓度和体积的两种弱一元酸,则a K Θ较大的弱一元酸(B ) A 消耗NaOH 多;B 突跃范围大;C 计量点pH 较低;D 指示剂变色不敏锐。
2、滴定分析要求相对误差±0.1%,万分之一的分析天平绝对误差为±0.0001g ,则一般至少称取试样质量为(B )A0.1g ;B0.2g ;C0.3g ;D0.4g.3、以HCl 溶液滴定某碱样,滴定管的初读数为0.25±0.01ml ,终读数为32.25±0.01ml ,则用去HCl 溶液的准确体积为(D )A32.0ml ;B32.00ml ;C32.00±0.01ml ;D32.00±0.02ml 。
4、指示剂的变色范围越窄,则(A )A 滴定越准确;B 选择指示剂越多;C 变色敏锐;D 滴定越不准确。
5、溶液pH 降低,EDTA 的配位能力会(B )A 升高;B 降低;C 不变;D 无法确定。
6、用KMnO 4法测定Ca 2+离子,所采用的滴定方式是(B )法A 直接滴定法;B 间接滴定法;C 返滴定法;D 置换滴定法。
7、不同波长的电磁波,具有不同的能量,其波长与能量的关系为(B )A 波长愈长,能量愈大;B 波长愈长,能量愈小;C 波长无能量无关。
8、在酸性条件下,莫尔法测Cl -,其测定结果(B )A 偏低;B 偏高;C 正好;D 无法确定。
9、下列有关配体酸效应叙述正确的是(B )A 酸效应系数越大,配合物稳定性越大;B 酸效应系数越小,配合物稳定性越大;CpH 越高,酸效应系数越大。
10、酸性介质中,用草酸钠标定高锰酸钾溶液,滴入高锰酸钾的速度为(B )A 同酸碱滴定一样,快速进行;B 开始几滴要慢,以后逐渐加快;C 始终缓慢;D 开始快,然后逐渐加快,最后稍慢。
11、酸碱滴定中,选择指示剂可不考虑的因素是(D )ApH 突跃范围;B 要求的误差范围;C 指示剂的变色范围;D 指示剂的结构。
无机及分析化学课后习题答案

第1章1. 下列各测量值含有的有效数字是几位?(定量化学分析简明教程(北大编第3版)P38-2.8)解:0.0030;26.023 ⨯ 1023;464.120;54.80 ⨯ 10-10;30.998;3(也可认为是四位)1000;不明确1.1⨯ 103;2pH=5.23。
22. 按有效数字计算下列结果:(定量化学分析简明教程(北大编第3版)P38-2.9,有修改)解:(1)213.64+4.4+0.3244;=213.6+4.4+0.3=218.3(2)10004182.1)1003206.16239.1400.20(0982.0⨯⨯⨯-⨯(注:3、100、1000为自然数)=0.0982×(20.00-7.780)/(1.4182×1000)=0.0982×12.22/(1.4182×1000)=0.0982×12.2/(1.42×1000)=8.44×10-4(3)pH=12.00 溶液的[H+]1.0×10-12mol/L3.甲乙二人同时分析一矿物试样中含硫量,每次称取试样4.7克,分析结果报告为:甲:0.062% ,0.061% ;乙:0.06099% ,0.06201%;问哪一份报告是合理的,为什么?(定量化学分析简明教程(北大编第3版)P37—思考题5,有修改)解:有效数字第9章1.定量分析过程中出现下面的情况,试回答它造成什么性质的误差,如何改进?(1) 过滤时错用了定性滤纸,最后灰份加大;(2) 过滤时沉淀发生穿滤;(3) 试剂中含有少量被测组分;(4) 滴定管读数时,最后一位估计不准;(5) 天平砝码锈蚀;(6) 天平零点稍有偏移;(7) 双臂天平臂长不等;(8) 容量仪器未经校正;(9) 指示剂的变色点于化学计量点不一致;(10) 溶液溅失。
解:(1) 过失重做(2) 过失重做(3) 系统更换试剂(4) 随机培训(5) 系统更换砝码(6) 系统校准(7) 系统校准(8) 系统校准(9) 系统(10) 过失重做2.某人对某铁矿石标准样品中铁的含量分别进行了两次测定,数据如下:①57.21%,58.35%,59.18%。
定量化学分析简明教程第3版答案

⎛1 ⎞ n⎜ KHC 2 O 4 ⋅ H 2 C 2 O 4 ⎟ = n( NaOH) ⎝3 ⎠
氧化还原反应中:
V (KMnO 4 ) =
第 2 章 习题参考答案
2.2 测定试样中 CaO 的质量分数时,得到如下结果:35.65%、35.69%、35.72%、35.60%。问: (1)统计处理后的分析结果应如何表示? (2)比较 95%和 90%置信度下总体平均值的置信区间。 答案: (1) 结果表示为:n=4, x = 35.66% ,s=0.052% (2) 1 − α = 0.95 ,则 α = 0.05 , t 0.05 (3) = 3.18
4
答
案
2.1 测定某样品中氮的质量分数时,六次平行测定的结果是 20.48%、20.55%、20.58%、20.60%、 20.53%、20.50%。 (1) 计算这组数据的平均值、 中位数、 平均偏差、 标准差、 变异系数和平均值的标准差; (20.54%, 20.54%, 0.12%, 0.037%, 0.046%, 0.22%, 0.019%) (2)若此样品是标准样品,其中氮的质量分数为 20.45%,计算以上测定结果的绝对误差和相对 误差。(+0.09%, 0.44%)
∴σ1 与σ2 无显著差异。 (2)用 t 检验法检验μ1 是否等于μ2 假设μ1=μ2
课 后
(1)用 F 检验法检验σ1=σ2 是否成立(α =0.10) 假设σ1=σ2
F计算
2 s大 0.9 2 = 2 = = 2.2 < F表 = F0.05 (4,3) = 9.12 s小 0.6 2
度(c)的 Na2C2O4 溶液?要配制 100mL 溶液,应称取 Na2C2O4 多少克?
中国科学技术大学2024年招收攻读硕士学位研究生参考书目

《无机化学例题、要点、习题》张祖德等编中国科技高校出版社第三版
?
441分析化学
误差与数据处理;酸碱滴定,配位滴定,氧化-还原滴定,重量分析;沉淀滴定,常用的分别方法与困难物质分析
《分析化学》武汉高校主编高等教化出版社
《定量化学分析》李龙泉等编著中国科学技术高校出版社
442有机化学
《有机化学》伍越环编著的全部内容
《有机化学》伍越环编中国科学技术高校出版社
《有机化学试验》兰州高校、复旦高校编高等教化出版社
443结构化学
量子力学基础、原子分子电子结构、分子光谱、晶体结构
《物质结构》潘道皑人民教化出版社
444高分子化学
聚合反应基本原理及高分子化学反应
《高分子化学》潘才元中国科大出版社
《近代物理学》徐克尊高等教化出版社;
《原子物理学》杨福家第三版,高等教化出版社;
《原子物理学》褚圣麟高等教化出版社
《量子力学导论》曾谨言高等教化出版社
436电动力学A
电磁现象的普遍规律;静电场和静磁场;电磁波的传播,电磁波的辐射(包括低速和高速运动带电粒子的辐射);狭义相对论
《电动力学》郭硕鸿其次版高等教化出版社
《数学分析教程》常庚哲中国科大出版社
322分析和代数
数学分析:一元和多元微积分,无穷级数,广义积分。线性代数:行列式,矩阵,线性方程组和线性变换,欧氏空间,矩阵标准形
《数学分析》(一、二、三册)何琛高等教化出版社
《线性代数》李炯生中国科大出版社
323科技考古学
现代科学技术在考古学各领域的应用。
科技考古论丛(其次辑),中国科学技术高校出版社,2024年版,王昌燧主编,左健副主编;
分析化学教案设计

教案2013~2014学年课程名称分析化学院(系)化学与环境科学学院教研室(实验室) 化学系授课班级主讲教师职称副教授使用教材华中师大等编《分析化学(上册)》兰州城市学院化学与环境科学学院制教案(首页)注:课程类别:公共基础课、专业基础课、专业必修课、专业选修课、集中实践环节、实验课、公共选修课教学内容:第一章绪论一、分析化学的任务和作用1.分析化学的任务分析化学是研究关于物质的化学结构、化学组成及测定方法的一门学科。
它是化学科学的一个重要分支。
定性分析的任务:就是鉴定物质的化学结构和化学组成。
定量分析的任务:就是测定物质中各组分的相对含量。
2.分析化学的作用分析化学作为一门学科,对于化学本身的发展起过重大作用。
化学上的基本定律都是依靠大量的分析实验数据才得以创立和发展起来的,而其它各门学科的发展又进一步推动了分析化学的发展。
分析化学对工业、农业、国防和科学技术的发展都有重要的作用。
分析化学在高等学校理、工、农、医、师范各有关专业中,是一门重要的化学基础课。
三、定量分析的方法1.按对象分2.按操作方法分类3.按试样用量分类4.根据被测组分含量分类5.其它专有名词四、分析化学的发展趋势(一)分析化学的发展简史(二)当前的发展趋势第二章定性分析教学内容:§2-1 概述一、定性分析的任务和方法1.任务:鉴定物质中所含有的组分。
2.方法⑴干法:指分析反应在固体之间进行。
⑵湿法:指分析反应在溶液之间进行。
(主要学习湿法分析)二、定性分析反应进行的条件共5点三、鉴定方法的灵敏度和选择性1.鉴定方法的灵敏度鉴定反应的灵敏度常用“最低浓度”和“检出限量”来表示。
⑴最低浓度⑵检出限量⑶检出限量和最低浓度之间的关系2.鉴定反应的选择性四、空白试验和对照试验空白试验:用配制试液用的蒸馏水代替试液,用同样的方法和条件重做试验进行鉴定,就叫做空白试验。
对照试验:用已知溶液代替试液,用同样方法进行鉴定,就叫做对照试验。
数学教材推荐

似乎是不错的选择,应用数学专业好像都是用这本。
12《数值分析基础》李庆扬,王能超,易大义
13《数值逼近》蒋尔雄,赵风光
14《微分方程数值解法》余德浩,汤华中
15《微分方程数值解法》李立康,於崇华,朱政华
看一个学校的计算数学是真的计算数学还是所谓的信息与计算,只要看一下上不上微分方程数值解就行了。
1《近世代数引论》冯克勤
2《近世代数》熊全淹
3《代数学》莫宗坚
4《代数学引论》聂灵沼
5《近世代数》盛德成
常微分方程
1《常微分方程教程》丁同仁、李承治,高等教育出版社
公认的国内写的最好的教材。
2《常微分方程》王高雄等
使用相当广泛的教材。初学建议从1,2中选
3《常微分方程》V.I.Arnold
解析几何
解析几何有被代数吃掉的趋势,不过就数学系的学生而言,还是应该好好学一下,我大一没有好好学,后来学别的课时总感觉哪里有些不太对劲,后来才发现是自己的数学功底尤其是几何得功底没有打好。
1吴光磊《解析几何简明教程》高等教育出版社
写的简单明了,我基础没有打好,快速翻了一下这本书收获还是不少的。不过打基础的时候还是从下面三本选一本看,把这本当参考书。
11《高等代数习题集》杨子胥著
相对8,9很容易买到,很多人用来做考研的参考书,而且符合所谓的教学或考研大纲。
12《线性代数》蒋尔雄,高锟敏,吴景琨著
名为线性代数,实际上是一本高等代数教材。是一本非常老的为当时计算数学专业编写的书。市面上根本找不到,但各大学的藏书中肯定会有。
近世代数
不光是数学系最重要的几门课,而且在计算机方面有很多应用,通常的离散数学第二部分就是近世代数内容,也叫抽象代数。
定量分析简明教程赵士铎答案(第三版)

第一章 定量分析的误差和数据处理 1-2下列情况,将造成哪类误差?如何改进?(1) 天平两臂不等长,属于系统误差。
可对天平进行校正或者更换天平。
(2)测定天然水硬度时,所用蒸馏水中含Ca 2+。
属于系统误差。
可更换蒸馏水,或作空白试验,扣除蒸馏水中Ca 2+对测定的影响。
1-3 填空(1) 若只作两次平行测定,则精密度应用相对相差表示。
(2)对照试验的目的是检验测定中有无系统误差,空白试验的目的是判断测定中的系统误差是否因试剂、蒸馏水不纯等所致。
(3)F 检验的目的是检验两组测定结果的精密度有无显著性差异。
(4)为检验测定结果与标准值间是否存在显著性差异,应用t 检验。
(5)对一样品做六次平行测定,已知d 1~d 6分别为0、+0.0003、-0.0002、-0.0001、+0.0002,则d 6为-0.0002。
(提示:一组平行测定,各单次测定结果偏差的代数和为0) 1-4解:%3.0mL50.6mL02.01r ±=±=E%08.0mL65.25mL02.02r ±=±=E上述计算说明为减小滴定管的体积误差,应适当增大取液的体积。
1- 5解: 纯FeSO 4·7H 2O 试剂中w (Fe)的理论值是:%09.20mol g 0.278mol 55.85g O)H 7FeSO (Fe)(Fe)(1--124=⋅⋅=⋅=M M w%06.20%405.2004.2003.2010.20=+++=xd i 分别为:0.04%,-0.03%,-0.02%,-0.01% %03.0%401.002.003.004.0=+++==d 平均偏差%2.0%06.20%03.0===x d d r %03.0%09.20%06.20-=-=-=T x Ea%2.0%06.20%03.0-=-==x Ea E r %03.01401.002.003.004.02222=-+++=S%2.0%06.20%03.0===x S 变异系数 6解:1- 7解:①用Q 值检验法:∴12.47应保留。
分析化学的任务和作用

0.01-0.1 g < 0.1 mg
4.按方法原理分:
化学分析法 重量分析法 滴定分析法(酸碱、络合、沉淀、氧化还原)
光学分析法 仪器分析法 电化学分析法
色谱分析法
特殊命名的方法:
仲裁分析,例行分析,微区分析,表面分 析,在线分析……
三.本课程特点及要求
通过这门课及分析化学实验课的学习,掌 握分析化学的基本原理和测定方法,树立准确 量的概念,培养严谨的科学态度,掌握基本实 验技能,提高分析问题和解决问题的能力。
21世纪是生命和信息科学的世纪,科技的 发展和社会生产发展的需要要求分析化学尽可 能快速、全面和准确地提供丰富的信息和有用 的数据。
现代分析化学正在把化学与数学、物理 学、计算机科学、生物学、精密仪器制造科学 等学科结合起来,发展成为一门多学科性的综 合性科学。
在工农业生产、科学技术、国防建设等社 会主义建设中起着重要作用。
第一章 定量分析概论
§1-1 定量分析的过程
我们所遇到的样品千千万万,组成不同,即使分析同样的
组分所用方法也不相同,具体步骤自然不同,但是定量分析大 体需要进行这样几个步骤:
一、取样
制备分析试样关键是取样有代表性,固体试样经粉碎、
过筛、缩分,得到少量分析试样,烘干去掉湿存水,保存于干
燥器待称量。
二、分解
在各学科的科学研究中的作用——科学技 术的眼睛。
社会
其他科学 技术领域
社会 需要
研究与 发展
分析 问题
分析化学
二.分析方法的分类
1.按任务分:按研究对象分:无机分析、有机分析
3.按试样用量和操作方法分:
常量分析 > 0.1 g 半微量分析 微量分析 0.1-10 mg 超微量分析
河北大学参考书目
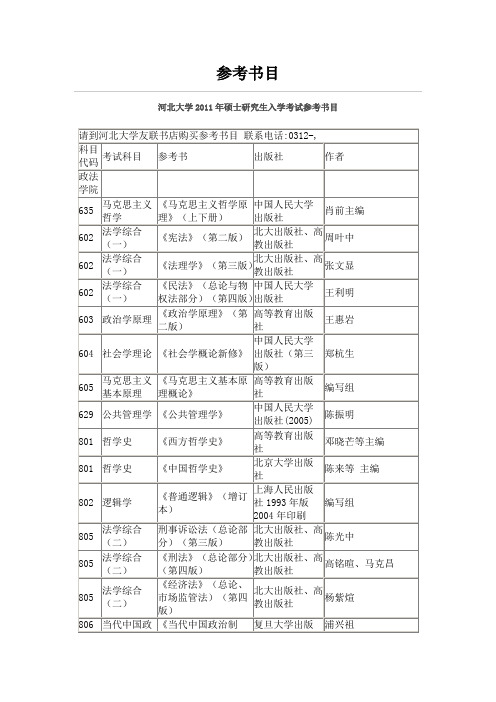
陈光中
805
法学综合(二)
《刑法》(总论部分)(第四版)
北大出版社、高教出版社
高铭暄、马克昌
805
法学综合(二)
《经济法》(总论、市场监管法)(第四版)
北大出版社、高教出版社
杨紫煊
806
当代中国政治与政府,政治社会学
《当代中国政治制度》
复旦大学出版社
浦兴祖
806
当代中国政治与政府,政治社会学
无参考书目
822
视听语言
《视听语言》
方圆电子音像出版社
郄建业、耿小博、陈晓红
336
艺术基础
艺术学概论
北京大学出版社
彭吉象
336
艺术基础
美术鉴赏
高等教育出版社
张道一
数计学院
科目代码
考试科目
参考书
出版社
作者
619
数学分析
《数学分析》(上、下册)
高等教育出版社
陈传璋
823
高等代数与解析几何
《高等代数》
高等教育出版社
808
人口学理论
《人口学》
浙江人民出版社(2004.4)
田雪原
431
金融学综合
《货币银行学》
高等教育出版社(2007.8)
康书生,鲍静海
432
统计学
《经济应用统计学教程》
经济日报出版社,2005.8
李林杰、董正信主编
434
国际商务专业基础
《国际商务》
中国人民大学出版社,2010.4
王亚星、王文谭编著
中华书局
王力
870
古代汉语与文献
《古代汉语》(1、2册)
络合滴定法——精选推荐

第六章 络合滴定法络合滴定法是以络合反应为基础的滴定分析方法。
从路易斯酸碱理论来说,络合反应也是路斯酸碱反应,所以络合滴定与酸碱滴定法有许多相似之处,学习时可对照比较,但络合滴定中也有自身的特点,内容更复杂。
络合反应在分析化学中应用广泛,有关理论和实践知识是分析化学重要的内容之一。
6.1 络合滴定分析中常用的络合剂和络合平衡 6.1.1 常用的络合剂络合反应中常用的络合剂很多,如测定金属离子的络合滴定剂、掩蔽剂、指示剂和金属缓冲溶液等等。
络合剂的分类方式也很多,按络合剂中的键合原子分类,可分为:(1)氧配位螯合剂:如磺基水扬酸、酒石酸、柠檬酸、乙酰丙酮等;2.氮配位络合剂:如氨、乙二胺、联吡啶、邻二氮菲等;(3)氧、氮配位络合剂:8-羟基喹啉、氨三乙酸及EDTA 氨羧络合剂等;(4)硫配位螯合剂:如铜试剂、2-巯基苯并噻唑等。
1. 氨羧络合剂络合滴定中重要的滴定剂是具有-N(CH 2COOH)2基团氨羧络合剂,常见的氨羧络合剂见下表。
2. 乙二胺四乙酸的性质:(1) 乙二胺四乙酸结构:(ethylenediaminetetreacetic acid )简称EDTA ,具有结构如图所示。
一个分子中含有二个-N(CH 2CO OH)2基团,与金属离子结合时有六个配位原子,可形成五个五元螯合环,具有很强的络合性能,是常用的络合滴定剂和掩蔽剂。
(2) EDTA 性质:EDTA 在水中的溶解度不大,EDTA 的二钠盐溶解度较大,EDTA 是六元酸,可用H 6Y 2+表示,有六级离解常数。
各级解离常数与对应的质子化常数如后。
,,,++++=Y H H Y H 5269.0a H69.02Y 6H Y 5H H a 101,10)()()(11====-+++K K c c c K Y H H Y H 45+=++6.1a H56.1Y 5H Y 4H H a 101,10)()()(22====-++K K c c c K -++=Y H H Y H 340.2H40.2Y 4(H )Y 3(H )(H a 10 ,10)3===--+K c c cK,,,各组分的分布分数如上图所示。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
北大《定量化学分析简明教程》
第一章
定量分析概论
1. 为什么用作滴定分析的化学反应必须有确定的计量关系?什么是“化学计量点”?什么是“终点”?为什么滴定分析对化学反应进行的完全程度的要求比重量分析高?
解答:
滴定分析所依据的化学反应只有具有了确定的计量关系,才能进行准确
的计算。
化学计量点是指当加入的滴定剂的量(摩尔)与被测物的量(摩尔)之间,正好符合化学反应式所表示的化学计量关系。
终点:指示剂为指示剂的变色点.
2. 若将H 2C 2O 4.·2H 2O 基准物长期保存于保干器中,用以标定NaOH 溶液的浓度时,结果是偏高还是偏低?分析纯的NaCl 试剂若不作任何处理用以标定 AgNO 3溶液的浓度,结果会偏高,试解释之。
解答:
H 2C 2O 4.·2H 2O 基准物质长期保存于保干器中易脱水,变成H 2C 2O 4·H 2O 或H 2C 2O 4,若在计算时仍以H 2C 2O 4.·2H 2O 计算,表观的NaOH 浓度为: ='
N a O H C N a O H
O
2H O C H V .22422n N a O H O 2H O C H V M 100022422⨯⨯=
∙标W 而实际的NaOH 浓度为:
N a O H O C H N a O H V M W C ⨯⨯=42210002标
或 N a O H O H O C H N a O H V M W C ⨯⨯=∙2
42210002标
M H2CO4·H2O < M H2CO4·2H2O
M H2CO4 < M H2CO+2H2O
∴ C’NaOH < C NaOH
即标定结果偏高。
同时可对NaCl 标定AgNO 3的情况进行分析。
NaCl 若不作处理含有较多的水分
表观的AgNO 3浓度为:
C’AgNO3=3
31000AgNO NaCl AgNO NaCl V M W V n ⨯⨯=标 而实际的AgNO 3浓度为:
3
231000AgNO O nH NaCl AgNO V M W C ⨯⨯=∙标
M NaCl ·nH2O >M NaCl ∴ C ’AgNO3 >C AgNO3
即表观浓度偏高。
3. 30.0ml 0.150MHCl 溶液和20.0ml 0.150MBa(OH)2溶液相混合,所得溶液是酸性、中性、还是碱性?计算过量反应物得摩尔浓度。
解:反应至化学计量点时,应有:
n HCl =2nBa(OH)2
n HCl =30.0×0.150 = 4.50 (mmol)
nBa(OH)2=20.0×0.150 = 3.00 (mmol)
c n HCl =4.50 < 2nBa(OH)2 =6.00
∴ 溶液呈碱性。
过量反应物的摩尔浓度为:
总V n n C HCl OH Ba OH Ba 2122)()(-=
.5025.200.3-= =0.0150 (mol / L)
答:过量反应物的摩尔浓度为 0.015mol / L 。
4. 称取纯金属锌 0.3250 g ,溶于 HCl 后,稀释到250ml 容量瓶中,计算Z n 2+溶液的摩尔浓度。
解:
)/(01988.0250
.038.653250.02L mol M W C V Zn Zn Zn =⨯==∙+ 答:Zn 2+的摩尔浓度为0.01988 mol / L 。
5. 欲配制Na 2C 2O 4溶液用于标定0.02MKMnO 4溶液(在酸性介质中),若要使标定时两种溶液消耗的体积相近,问应配制多大浓度(M )的Na 2C 2O 4溶液?要配制100ml 溶液,应称取c 多少克?
解:标定反应为:
O H CO Mn H O C MnO 22234248521652++==++++-
-
n Na 2C 2O 4=2.5n KMnO 4 C Na 2C 2O 4V Na 2C 2O 4=2.5C KMnO 4V KMnO 4
V Na 2C 2O 4=V KMnO 4
∴ n Na 2C 2O 4
=2.5n KMnO 4=2.5×0.02=0.05(mol / L) G Na 2C 2O 4 = C Na 2C 2O 4V Na 2C 2O 4×M Na 2C 2O 4
=0.05×0.100×134.0
= 0.67 (g)
答:应称取Na 2C 2O 40.67克。
6. 用KMnO 4法间接滴定石灰石中CaO 的含量,若试样中CaO 的含量均为40%,为使滴定时消耗0.020M KMnO 4约为30ml ,问应称取试样多少克?
解:间接测定的反应式为:
Ca 2++C 2O 42- == CaC 2O 4↓
CaC 2O 4+2HCl == Ca 2++2Cl -+2H 2C 2O 4
5C 2O 42-+2MnO 4-+16H + ==5CO 2+2Mn 2++8H 2O
化学计量关系为:
n CaO =n CaC2O4=2.5n KMnO4 )(21.0400
5630020.025*********%40G 4g M n M n CaO KMnO CaO CaO =⨯⨯⨯==⨯=样
答:应称取试样0.21克。
7. 某铁厂化验室经常要分析铁矿中铁的含量。
若使用的K 2Cr 2O 7溶液浓度为0.02000M 。
为避免计算,直接从所消耗的K 2Cr 2O 7溶液的毫升数表示出Fe%,问应当称取铁矿多少克?
解:滴定反应为:
6Fe 2++Cr 2O 72-+14H +==6Fe 2++2Cr 3++7H 2O
化学计量关系为:
n Fe =6n Cr2O72-
1000
M 6n 1000Fe%Fe O Cr -272⨯=⨯=样样G G M n Fe Fe 00.106722722⨯⨯⨯=样G M V C Fe
O Cr K O Cr K
Fe%=V K2Cr2O7
G 样=6C K2Cr2O72×M Fe ×0.1000=6×0.02000×55.85×0.1000=0.6702 (g) 答:应当称取铁矿0.6702 克。
8. 称取c 试剂0.8835g ,以甲基橙为指示剂,用0.1012MHCL 滴定至H2PO4-,共消耗HCl 溶液27.30ml 。
计算Na 2HPO 4·12H 2O 的百分含量。
并解释所得结果
(HCl 浓度、终点得确定以及仪器均无问题)。
解:
Na 2HPO 4·12H 2O%=1001000G M O
12H HPO Na O 2H HPO Na 242242⨯⨯⨯∙∙样n
1024212⨯=
∙样G M n O H HPO Na HCl %0.11210
8835.01.35830.271012.0=⨯⨯⨯= 答:Na 2HPO 4·12H 2O 的百分含量为112.0%。
滴定至化学计量点时,主成型体是Na 2H2PO 4,pH=4.7
而以甲基橙为指示剂,变色范围为3.1---4.4 ,变色点为3.4。
显然,变色点与化学计量点具有较大的差别。
故终点误差较大。
由于终点较化学计量点偏高,故引起正误差。
9. 分析不纯CaCO 3(其中不含分析干扰物)时,称取试样0.3000克,加入0.2500M HCl 标准溶液25.00ml 。
煮沸除去CO 2,用0.2012MNaOH 溶液返滴过量酸,消耗了5.84ml 。
计算试样中CaCO 3的百分含量。
解:有关化学计量关系为:
n CaCO3=0.5n HCl
100M n C a C O 3%33C a C O C a C O ⨯⨯=样
G 10
213⨯⨯=样G M n CaCO HCl %67.8410
3000.01.100)84.52012.000.252500.0(21=⨯⨯⨯-⨯= 答:计算出试样中CaCO 3的百分含量为84.67%。
