2药事管理组织机构
医院药事管理委员会组成及其职能

医院药事管理委员会组成及其职能为进一步健全医院药事管理委员会的组织机构,强化药事管理委员会的职能,保障人体用药安全,根据《中华人民共和国药品管理法》和质量管理年的相关要求,经研究决定,我院药事管理委员会组成人员如下,并重申药事管理委员会的职能。
1.药事管理委员会组成主任:副主任:秘书:委员(按姓氏笔划排序):专家库成员(按姓氏笔划排序):2.药事管理委员会职能2.1 药事会每年召开不少于两次,每次参会人数不少于药事会成员的3/4。
2.2 如果当次药事会讨论新药,除药事会成员外,必要时将从专家库成员中随机抽取若干名专家参加会议。
2.2 新进或淘汰药品,由相关专业科室提出申请,药事会讨论,≥2/3 票数通过。
2.3 监督检查本院贯彻执行药品管理法的情况。
2.4 监督检查本院合理用药情况,对不合理用药的科室和个人提出改进措施和处理意见。
2.5 检查并落实《抗菌药物合理应用指导原则》的执行情况,并定期进行通报。
2.6 解决药疗事故、严重用药差错和医疗用药的重大问题。
2.7 指导新药临床试验工作的规范化开展。
2.8 每次邀请纪委一位同志列席药事会会议。
3.新药申请规定新药申请具体规定24 条,详见附件。
本通知自下发之日起实行,望各科室认真执行,积极配合院药事管理委员会的工作。
附件:附件1:药事管理委员会委员及专家库成员资质附件2:新药申请表附件3:关于药品使用和新药申请的若干规定抄送:上海市申康医学发展中心办公室、上海交大医学院医管处附件1药事管理委员会委员及专家库成员资质附件2新药申请表编号:申请日期年月日生产企业商标注册书;6.国药准字号批件;7.药检报告;8.药品国家标准;9.上海市物价表;10.销售委托书和销售人员身份证复印件;11.使用说明书;12.药品应用临床资料总结;13.药理毒理试验总结报告(证明材料均需加盖公章,统一使用塑料封面左侧固定成册)申请科室:申请人:申请科室主任签名:日期:附件3关于新药申请和药品使用的若干规定根据国家和上海市有关药品使用规定,结合我院实际情况,就拟进入我院医保报销药品、自费药品的申请和药品使用做出如下相关规定:1. 医保报销品种(招标采购品种)进院的条件在充分保证患者安全、合理、经济用药的基础上,我院将依据药品质量、零售价、供货渠道、售后服务等标准,对拟进入我院的医保报销品种逐个进行遴选。
药事管理组织机构图
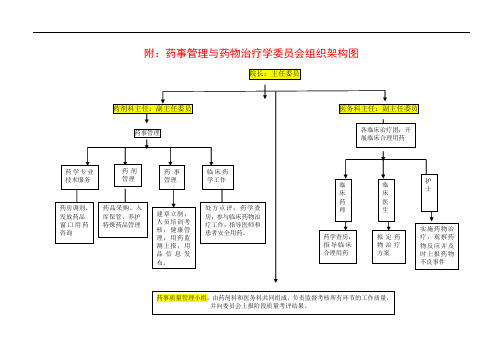
附:药事管理与药物治疗学委员会组织架构图
院长:主任委员
药剂科主任:副主任委员
药事管理
药学专业 技术服务
药剂 管理
药事 管理
临床药 学工作
药房调剂、 发放药品 窗口用药 咨询
药品采购、入 库保管、养护 特殊药品管理
建章立制; 人员培训考 核;健康管 理;用药监 测上报;用 品信息发 布。
处方点评;药学查 房;参与临床药物治 疗工作;指导医师和 患者安全委员
各临床治疗团:开 展临床合理用药
临 床 药 师
药学查房; 指导临床 合理用药
临 床 医 生
拟定药 物治疗 方案
护 士
实施药物治 疗,观察药 物反应并及 时上报药物 不良事件
药事质量管理小组:由药剂科和医务科共同组成,负责监督考核所有环节的工作质量, 并向委员会上报阶段质量考评结果。
医疗机构药事管理组织

治疗效果评估及持续改进
治疗效果评估
医疗机构应定期对患者的治疗效 果进行评估,分析药物治疗的有 效性和安全性。
持续改进措施
根据治疗效果评估结果,医疗机 构应采取相应的改进措施,包括 优化药物治疗方案、加强患者用 药教育等。
经验总结与分享
医疗机构应鼓励医师和药师进行 经验总结和分享,提高药物治疗 水平和患者满意度。
质量管理部
负责药品质量监控、风险评估、质量 控制等工作,确保药品质量符合相关 标准和规范。
科研与教学部
负责药学科研、教学培训、学术交流 等工作,提升药事管理组织的学术水 平和创新能力。
培训与考核机制
培ቤተ መጻሕፍቲ ባይዱ机制
制定完善的培训计划,包括岗前培训、 在职培训、专题培训等,提高药事管理 组织人员的专业素养和综合能力。
药品使用监管与评估
处方审核制度执行情况
处方审核流程
医疗机构应建立完善的处方审核流程,确保处方药物使用合理、 安全、有效。
处方审核人员资质
处方审核人员应具备相应的药学专业知识和临床经验,能够准确 判断处方用药的适宜性。
处方审核结果处理
对于审核不合格的处方,应及时与医师沟通并进行修改,确保患 者用药安全。
04
数据安全与隐私保护
加强数据安全管理和隐私保护, 确保数据的安全性和保密性。
智能化辅助决策支持系统
决策支持系统构建
构建智能化辅助决策支持系统,为医疗机构药事管理提供智能化支持 。
数据仓库与商业智能分析
建立数据仓库,运用商业智能分析技术,对数据进行整合、转换和挖 掘,为决策提供有力支持。
人工智能技术应用
药品不良反应监测与报告
药品不良反应监测
医疗机构应建立药品不良反应监 测制度,对患者用药过程中出现 的不良反应进行及时记录和分析
2药事管理第二章

国家药品监督管理局 药品评价中心
类型
中国食品药品 检定研究院
国家药典委员会
国家药品监督管理局 食品药品认证管理中心
国家药品监督管理局 药品审评中心
第二节 药品监督管理组织
三、药品监督管理技术机构及职责
(一)中国食品药品检定研究院
1.承担依法实施药品审批和质量监督检查所衔的检验和复验工作。 2.负责标定和管理国家药品标准、对照品。 3.负责组织药品、医疗器械的质量抽查检验工作并提供质量公告的技术数据,综合上报药品质量信 息和技术分析报告。 4.受国家药品监督管理局委托,对省、自治区、直辖市药品检验所及口岸药品检验所进行实验室技 术考核及业务指导,对药品生产企业、药品经营企业和医疗机构中的药品检验机构或人员进行业务 指导。 5.受国家药品监督管理局委托,承担生物制品批签发的具体业务工作。 6.对有关直接接触药品的包装材料和容器、药用辅料的药用要求与标准进行实验室复核并提出复核 意见。 7.承担司法机构委托的对涉嫌“足以危害人体健康”的假药进行药品含量和杂质成分等的技术鉴定。
第二节 药品监督管理组织
三、药品监督管理技术机构及职责
(四)国家药品监督管理局 (原国家食品药品监督管理总局) 药品审核查验中心
1.参与制定、修订《药物非临床研究质量管理规范》(GLP)、《药物临床试验质量管理规范》(GCP)、《药 品生产质量管理规范》(GMP)、《中药材生产质量管理规范(试行)》(GAP)、《药品经营质量管理规范》 (GSP)和《医疗器械生产质量管理规范》(医疗器械GMP)及其相应的实施办法。 2.对依法向国家药品监督管理局申请GMP认证的药品、医疗器械生产企业、GAP认证的企业(单位)和GCP认定 的医疗机构实施现场检查等相关工作。受国家药品监督管理局委托,对药品研究机构组织实施GLP现场检查等 相关工作。 3. 受国家药品监督管理局委托,对有关取得认证证书的单位实施跟踪检查和监督抽查;负责对省级 药品监督管 理局药品认证机构的技术指导;协助国家药品监督管理局依法开展医疗器械GMP的监督抽查等相关工作。 4.负责药品GMP认证检查员库及其检查员的日常管理工作,承担对药品、医疗器械认证检查员的培训、考核和 聘任的具体工作,组织有关企业(单位)的技术及管理人员开展GLP、GCP、GMP、GAP、GSP等规范的培训 工作。 5. 承担进口药品GMP认证及国际药品认证互认的具体工作,开展药品认证的国内、国际学术交流活动。 6.承办国家药品监督管理局交办的其它事项等。
医疗机构药事管理规定2

医疗机构药事管理规定医疗机构药事管理办法第一章总则第一条为科学、规范医疗机构药事管理工作,保证用药安全、有效、经济,保障人民身体健康,依据《中华人民共和国药品管理法》(以下简称《药品管理法》)、《医疗机构管理条例》和《卫生技术人员职务试行条例》,制定本办法。
第二条本办法所称医疗机构药事管理是指医疗机构内以医院药学为基础,以临床药学为核心,促进临床科学、合理用药的药学技术服务和相关的药品管理工作。
第三条卫生部、国家中医药管理局负责全国医疗机构药事管理工作。
县级以上地方卫生行政部门(含中医药行政管理部门)负责本行政区域内的医疗机构药事管理工作。
第四条医疗机构药事工作是医疗工作的重要组成部分。
医疗机构根据实际工作需要,应设立药事管理组织和药学部门。
第五条按国家有关规定依法经过资格认定的药学专业技术人员,方可从事药学专业技术工作。
非药学专业技术人员不得从事药学专业技术工作。
第二章药事管理组织第六条二级以上的医院应成立药事管理委员会,其他医疗机构(诊所、中医诊所、民族医诊所、卫生所、医务室、卫生保健所、卫生站除外)可成立药事管理组。
药事管理委员会(组)监督、指导本机构科学管理药品和合理用药。
三级医院药事管理委员会委员由具有高级技术职务任职资格的药学、临床医学、医院感染管理和医疗行政管理等方面的专家组成。
二级医院的药事管理委员会,可以根据情况由具有中级以上技术职务任职资格的上述人员组成。
其他医疗机构的药事管理组,可以根据情况由具有初级以上技术职务任职资格的上述人员组成。
医疗机构药事管理委员会(组)应建立健全相应的工作制度。
第七条药事管理委员会(组)由5~7人组成。
其中设主任委员1名,副主任委员1名。
机构主管负责人任主任委员,药学部门负责人任副主任委员。
药事管理委员会(组)的日常工作由药学部门负责。
第八条药事管理委员会(组)的职责是:(一)认真贯彻执行《药品管理法》,按照《药品管理法》等有关法律、法规制定本机构有关药事管理工作的规章制度;(二)确定本机构用药目录和处方手册;(三)审核本机构拟购入药品或配制新制剂及新药上市后临床观察的申请;(四)制定本机构新药引进规则,建立新药引进评审专家库,随机抽取组成评委,负责对新药引进的评审工作;(五)定期分析本机构药物使用情况,组织评价本机构所用药物的临床疗效与安全性,提出淘汰药品品种意见;(六)组织检查毒、麻、精神及放射性等药品的使用和管理情况,发现问题及时纠正;(七)组织药学教育、培训和监督、指导本机构临床各科室合理用药。
药事管理 第二章 药事管理组织体系与职能

• (五)组织实施国家药品管理的法律、法规;参与起草地方性 药品管理的法规和省政府规章草案;组织实施中药、民族 药质量标准,依法实施中药品种保护制度。
•
(六)组织实施国家医疗器械管理的法律、法规;负责医
疗器械产品的初审和监督管理;贯彻执行有关国家标准,组
织实施国家医疗器械产品行业标准、生产质量管理规范;
教育工作;负责执业药师施教机构资质管理工作。
•
(十三)开展与食品药品监督管理有关的交流
与合作。
•
(十四)承办省政府交办的其他事项
药品管理工作相关 部门(补充)
(一)卫生计生部门
国家卫生和计划生育委员会 职责范围内负责起草中医药事业发展的法律法规 草案,拟定政策规划,制定部门规章、标准和技 术规范。指导制定中医药中长期发展规划,并纳 入卫生和计划生育事业发展总体规划和战略目标。 负责组织推进公立医院改革,建立公益性为导向 的绩效考核和评价运行机制,建设和谐的医患关 系,提出医疗服务和药品价格政策的建议。
海关负责药品进出口口岸的设置;药品进 口与出口的监管、统计与分析。
(九)新闻宣传部门
新闻宣传部门负责加强药品安全新闻宣传 和舆论引导工作。
(十)公安部门
公安部门负责组织指导食品药品犯罪案件 侦查工作,与国家食品药品监督管理总局 建立行政执法和刑事司法工作衔接机制。
(十一)监察部门
监察部门负责调查处理药品监督管理人员 违反行政纪律的行为;依法如强监督,对 拒不执行国家法律法规、违法违规审批, 以及制售假劣药品和医疗器械问题严重的 地区和部门,严肃追究有关领导和人员的 责任。
第二节 药品监督管理
一、药品监督管理 概述
(一)药品监督管理的性质
1.药品监督管理是国家行政管理 2.药品监督管理具有法律性 3.药品监督管理主体受法律实施办 法并监督实施。建立食品安全隐患排查 治理机制,制定全国食品安全检查年度 计划、重大整顿治理方案并组织落实。 负责建立食品安全信息统一公布制度, 公布重大食品安全信息。参与制定食品 安全风险监测计划、食品安全标准,根 据食品安全风险监测计划开展食品安全 风险监测工作。
药事管理委员会及工作制度

药事管理委员会及工作制度
药事管理委员会是负责药事管理工作的组织机构,主要负责制定和监督医院内药事管理的政策、规章制度,协调各个相关部门的工作,确保药事管理的顺利进行。
药事管理委员会的职责包括:
1. 药品采购:负责药品的采购工作,确保药品的质量和供应的稳定性。
2. 药品配送:负责药品的配送工作,确保医院内各个科室的药品需求得到满足。
3. 药品储存和保管:负责药品的储存和保管工作,确保药品的安全和有效性。
4. 药物治疗监测:负责药物治疗监测工作,对患者用药情况进行跟踪和评估,及时发现和解决用药问题。
5. 药品信息管理:负责药品信息的管理工作,包括药品的分类、编码、价格管理等。
药事管理委员会的工作制度包括:
1. 会议制度:定期召开药事管理委员会会议,讨论和决定重大事项,及时协调解决药事管理中的问题。
2. 工作规范制度:制定和完善药事管理的工作规范,明确各个部门和人员的职责和权限,规范药事管理工作流程。
3. 信息管理制度:建立药品信息管理系统,对药品的采购、配送、储存等环节进行信息化管理,提高管理效率和准确性。
4. 药物治疗监测制度:建立患者药物治疗监测档案,定期对患者用药情况进行评估和跟踪,及时发现并解决用药问题。
5. 考核评估制度:建立药事管理工作的考核评估制度,对委员会成员和各个部门的工作进行考核评估,确保药事管理工作的质量和效果。
综上所述,药事管理委员会及其工作制度的建立和执行,对医院的药事管理工作具有重要的指导和监督作用,能够提高药事管理的效率和质量,确保患者用药的安全和有效性。
220-其他资源-《药事管理组织机构》自测题解答

模块一:药事管理基础教学单元2: 药事管理组织机构一、最佳选择题1. 国家食品药品监督管理局组建于( )年A、1978年B、1998年C、2001年D、2003年E、2008年参考答案:D解析:本题考查国家食品药品监督管理局组建的时间。
国家食品药品监督管理局组建于2003年。
2.目前我国主管全国药品监督管理工作的机关是( )A、国家医药管理局B、国家药品管理局C、国家药品监督管理局D、国家食品药品监督管理局E、国家中医药管理局参考答案:D解析:本题考查目前我国主管全国药品监督管理工作的机关。
目前我国主管全国药品监督管理工作的机关国家食品药品监督管理局。
3. 我国目前药品监督管理组织体系的框架为( )A.全国集中统一,实行垂直管理B.全国集中统一,省以下实行不垂直管理C.全国集中统一,省市统筹管理D.全国集中统一,中央、省、市三级管理参考答案:B解析:本题考查我国目前药品监督管理组织体系框架的内容。
我国目前药品监督管理组织体系的框架为全国集中统一,省以下实行不垂直管理。
4. 我国药品监督管理部门的主要药事管理职能涉及( )A、药品管理B、药事组织管理C、医疗保险用药管理D、药品价格管理E、药品、药事组织、执业药师管理参考答案:E解析:本题考查我国药品监督管理部门的主要药事管理职能的内容。
我国药品监督管理部门的主要药事管理职能涉及药品、药事组织、执业药师管理。
5. 下列不属于药品监督管理行政机构管辖的是( )A、药品使用管理B、药品广告管理C、药品注册管理D、药品储备管理E、药品流通管理参考答案:D解析:本题考查药品监督管理行政机构管辖的范围。
药品监督管理行政机构管辖药品使用管理、药品广告管理、药品注册管理和药品流通管理。
6. 国家药品监督管理局的职责之一是A、负责药品的储备管理B、制订医药行业的发展规划C、拟定、修订和颁布药品法定标准D、负责医药行业各专业统计工作E、组织实施中药、生化制药的行业管理参考答案:C解析:本题考查国家药品监督管理局职责的内容。
药事管理委员会章程

药事管理委员会章程引言概述:药事管理委员会章程是指药事管理委员会的组织结构、职责权限、工作程序和决策机制等方面的规定。
药事管理委员会是医疗机构内负责管理和监督药事工作的机构,其章程的制定和执行对于医疗机构的药事管理工作至关重要。
一、组织结构1.1 药事管理委员会的成员组成:药事管理委员会由医疗机构的领导、药学专家、临床医师、护士等相关人员组成,其中医疗机构的负责人通常担任委员会主任。
1.2 药事管理委员会的职责分工:根据各成员的专业背景和工作职责,药事管理委员会将工作任务进行合理分工,确保各项工作有序开展。
1.3 药事管理委员会的会议制度:药事管理委员会定期召开会议,讨论药事管理工作中的重要问题,制定相关政策和措施,监督和评估工作发展。
二、职责权限2.1 药事管理委员会的监督职责:药事管理委员会负责监督医疗机构药品采购、配送、使用等环节,确保药事工作符合法律法规和规范要求。
2.2 药事管理委员会的决策权限:药事管理委员会有权决定医疗机构药品管理政策、药品采购计划、药品使用指导等重要事项。
2.3 药事管理委员会的协调职责:药事管理委员会协调医疗机构内各部门之间的药事管理工作,促进信息共享和合作。
三、工作程序3.1 药事管理委员会的工作计划:药事管理委员会制定年度工作计划,明确工作重点和目标,确保药事管理工作有序推进。
3.2 药事管理委员会的会议程序:药事管理委员会会议按照规定程序召开,记录会议讨论内容和决议结果,确保会议决策的合法性和有效性。
3.3 药事管理委员会的工作报告:药事管理委员会定期向医疗机构领导和相关部门提交工作报告,汇报工作发展和存在的问题,提出改进建议。
四、决策机制4.1 药事管理委员会的决策原则:药事管理委员会的决策应当遵循科学、民主、公正、透明的原则,确保决策合理和公正。
4.2 药事管理委员会的决策程序:药事管理委员会在决策过程中应当听取各方意见,充分讨论,形成共识,做出科学决策。
2药事管理组织机构

•
• (1)制定药品、医疗器械、化妆品和消费环节食品安全监督管理的
政策、规划并监督实施,参与起草相关法律法规和部门规章草案。
• (2)负责消费环节食品卫生许可和食品安全监督管理。
• (3)制定消费环节食品安全管理规范并监督实施,开展消费环节食 品安全状况调查和监测工作,发布与消费环节食品安全监管有关的信 息。
2.1.5国家中药品种保护审评委员会
• 根据国务院《中药品种保护条例》的规定,1993年 10月10日,成立了国家中药品种保护审评委员会(简称 中药保护委员会),中药保护委员会是国家审批中药保护 品种的专业技术审查和咨询机构。 • 中药保护委员会由从事中医药医疗、科研、检验、药 品经营及管理等方面的专家组成。委员会设主任委员1人, 副主任委员、委员、特邀委员、顾问若干人,每届委员任 期4年。1 • 999年1月26日举行了国家中药品种保护审评委员会 第二届换届大会,国家药品监督管理局局长郑筱萸担任主 任委员。目前,国家中药品种保护审评委员会有审评委员 126人。
2.1.2药品检验机构P11
1、中国药品生物制品检验 所 中国药品生物制品检验所是全国药品检验的最高技术仲
welcome to use these PowerPoint templates, New
裁机构,是全国药品检验所业务技术的指导中心。
Content design, 10 years experience
2.3.3药学社会团体
• • (一)中国药学会 中国药学会成立于1907年,是我国成立较早的学术性社会团体之一。 1992年恢复加入了国际药学联合会(FIP),是亚洲药物化学联合会 (AFMC)的发起成员之一。 中国药学会是依法成立的由全国药学科学技术工作者组成的具有学术性、 公益性、非营利性的社会团体,是民政部批准登记的法人社会团体,是中国 科学技术协会的组成部分,是党和政府联系药学科学技术工作者的桥梁和纽 带,是推动中国药学科学技术事业发展的重要社会力量。 截止2002年,中国药学会己拥有10.5万名会员,1779名高级会员和43个 团体会员单位。 中国药学会根据药学发展的需要设立专业委员会,选举产生正副主任 委员,现有13个专业委员会。即中药和天然药物、药剂、抗生素、药物分析、 药物化学、生化药物、制药工程,医院药学、老年药学、海洋药物、药事管 理、药学史、军事药学专业委员会。学会根据工作需要设立工作委员会协助 理事会工作。现有组织工作、学术工作、科技开发工作、财务与基金管理工 作、国际学术交流工作、编辑出版工作、教育与科普工作7个委员会。
医疗机构药事管理规定

医疗机构药事管理规定第一章总则第一条为加强医疗机构药事管理,促进药物合理应用,保障公众身体健康,根据《中华人民共和国药品管理法》、《医疗机构管理条例》和《麻醉药品和精神药品管理条例》等有关法律、法规,制定本规定。
第二条本规定所称医疗机构药事管理,是指医疗机构以病人为中心,以临床药学为基础,对临床用药全过程进行有效的组织实施与管理,促进临床科学、合理用药的药学技术服务和相关的药品管理工作。
第三条卫生部、国家中医药管理局负责全国医疗机构药事管理工作的监督管理。
县级以上地方卫生行政部门、中医药行政部门负责本行政区域内医疗机构药事管理工作的监督管理。
军队卫生行政部门负责军队医疗机构药事管理工作的监督管理。
第四条医疗机构药事管理和药学工作是医疗工作的重要组成部分。
医疗机构应当根据本规定设置药事管理组织和药学部门。
第五条依法取得相应资格的药学专业技术人员方可从事药学专业技术工作。
第六条医疗机构不得将药品购销、使用情况作为医务人员或者部门、科室经济分配的依据。
医疗机构及医务人员不得在药品购销、使用中牟取不正当经济利益。
第二章组织机构第七条二级以上医院应当设立药事管理与药物治疗学委员会;其他医疗机构应当成立药事管理与药物治疗学组。
二级以上医院药事管理与药物治疗学委员会委员由具有高级技术职务任职资格的药学、临床医学、护理和医院感染管理、医疗行政管理等人员组成。
成立医疗机构药事管理与药物治疗学组的医疗机构由药学、医务、护理、医院感染、临床科室等部门负责人和具有药师、医师以上专业技术职务任职资格人员组成。
医疗机构负责人任药事管理与药物治疗学委员会(组)主任委员,药学和医务部门负责人任药事管理与药物治疗学委员会(组)副主任委员。
第八条药事管理与药物治疗学委员会(组)应当建立健全相应工作制度,日常工作由药学部门负责。
第九条药事管理与药物治疗学委员会(组)的职责:(一)贯彻执行医疗卫生及药事管理等有关法律、法规、规章。
审核制定本机构药事管理和药学工作规章制度,并监督实施;(二)制定本机构药品处方集和基本用药供应目录;(三)推动药物治疗相关临床诊疗指南和药物临床应用指导原则的制定与实施,监测、评估本机构药物使用情况,提出干预和改进措施,指导临床合理用药;(四)分析、评估用药风险和药品不良反应、药品损害事件,并提供咨询与指导;(五)建立药品遴选制度,审核本机构临床科室申请的新购入药品、调整药品品种或者供应企业和申报医院制剂等事宜;(六)监督、指导麻醉药品、精神药品、医疗用毒性药品及放射性药品的临床使用与规范化管理;(七)对医务人员进行有关药事管理法律法规、规章制度和合理用药知识教育培训;向公众宣传安全用药知识。
药事管理委员会章程

药事管理委员会章程引言概述:药事管理委员会是一个重要的组织机构,负责监督和管理医疗机构的药事工作。
药事管理委员会章程是规范该委员会运作的指导性文件,旨在确保药事工作的安全和有效性。
本文将详细介绍药事管理委员会章程的五个部分。
一、委员会组成1.1 委员会成员的组成:药事管理委员会由医疗机构的相关部门和专业人员组成,包括药学专家、医疗质量管理人员、临床医生等。
1.2 委员会成员的职责:每位委员会成员都有明确的职责和权限,如负责药物采购、药物配送、药物使用评估等。
1.3 委员会成员的任期和选举:委员会成员的任期一般为两年,可以连任一次。
选举过程应公开、公正,确保委员会成员的专业素质和能力。
二、委员会职责2.1 药物采购管理:药事管理委员会负责制定和实施药物采购管理制度,确保药物的质量、安全和合理使用。
2.2 药物配送管理:委员会负责制定和监督药物配送管理规范,确保药物的准确配送和储存。
2.3 药物使用评估:委员会负责对医疗机构内的药物使用情况进行评估和监督,及时发现和解决药物使用中存在的问题。
三、委员会运作机制3.1 会议制度:委员会定期召开会议,讨论和解决与药事管理相关的问题。
会议应有明确的议程和记录,确保决策的透明性和可追溯性。
3.2 决策程序:委员会成员在决策中享有平等的权利,决策应经过充分的讨论和协商。
重大决策需要经过多数委员的同意方可实施。
3.3 文件管理:委员会应建立健全的文件管理制度,确保文件的保存和归档,方便查阅和审查。
四、委员会监督与评估4.1 监督机制:委员会应建立监督机制,对医疗机构的药事工作进行定期检查和评估。
监督结果应及时反馈给医疗机构,并提出改进建议。
4.2 评估标准:委员会应制定评估标准,评估医疗机构的药事工作是否符合相关法规和规范要求。
4.3 效果评估:委员会应定期对自身的工作进行评估,评估委员会的运作是否有效,是否需要进行改进。
五、委员会的法律责任和权益5.1 法律责任:委员会成员在履行职责过程中应遵守相关法律法规,如保护患者隐私权、防止药物滥用等。
药事管理与法规-杨世民-第2版-第七章-

二、调剂业务管理
(二)门(急)诊调剂业务管理
西药调剂室
调剂区域
中药 调剂室
急诊 调剂室
二、调剂业务管理
门XX诊X调XX剂XX方XX法XX
独立配方法
协作配方法
结合法
二、调剂业务管理
(三)住院部调剂业务管理 XX供XX药X方XX式XXXX
凭处方发药
病区小药柜制
中心摆药制
二、调剂业务管理
(四)静脉用药集中配置管理
1 概述 2 医疗机构药学部门组织机构及人员管理 3 医疗机构药事管理与药物治疗学委员会 4 调剂与处方管理 5 医疗机构制剂的管理 6 医疗机构药品采购、储存管理 7 药品临床应用管理
第一节 概 述
一、医疗机构的概念及任务
(一)医疗机构的概念
医疗机构是指以救死扶伤,防病治病, 保护人们健康为宗旨,符合法定条件经批 准登记取得《医疗机构执业许可证》而从 事疾病诊断、治疗活动的社会组织。
(一)调剂的概念
• 调剂系指 配药,即配方、发药,又称为调配处方。调剂是专业 性、技术性、管理性、法律性、事务性及经济性综合一体的活动 过程。
• 调剂工作大体可分为:门诊调剂(包括急诊调剂),住院部调剂 ,中药配方 3个部分。
一、调剂工作概述
(二)调剂的流程和步骤
医生 (处方)
药师
病人
处接检 方受查 设处处 计方方
贯彻执行医疗卫生及药事管理等有关法律、法规、规章。审核制定本机构药 事管理和药学工作规章制度,并监督实施;
制定本机构药品处方集和基本用药供应目录; 推动药物治疗相关临床诊疗指南和药物临床应用指导原则的制定与实施,监 测、评估本机构药物使用情况,提出干预和改进措施,指导临床合理用药;
药事管理委员会章程 (2)

药事管理委员会章程一、总则药事管理委员会(以下简称“委员会”)是为了加强药事管理工作,提高药品质量和安全性,保障公众用药安全而设立的专门机构。
本章程旨在规范委员会的组织结构、职责权限、工作程序等方面的内容。
二、组织结构1. 委员会由主任委员、副主任委员和委员组成,主任委员由药事管理部门指定,副主任委员和委员由相关专业人士担任。
2. 主任委员负责组织和协调委员会工作,副主任委员协助主任委员履行职责,委员根据所属专业领域提供专业意见和建议。
3. 委员会设立秘书处,由秘书长负责具体的日常工作,包括会议组织、文件管理、信息采集和统计等。
三、职责权限1. 制定药事管理的政策和规范,提出药品质量和安全管理的意见和建议。
2. 审核和批准药品注册申请,制定药品注册的技术要求和程序。
3. 监督和检查药品生产、流通、使用环节的质量和安全情况,发现问题及时采取措施进行处理。
4. 组织开展药品质量和安全的监测和评估工作,定期发布药品质量和安全情况的报告。
5. 协调相关部门和单位,开展药品质量和安全的宣传教育工作,提高公众的药品安全意识和素质。
6. 对药品不良反应和药品安全事件进行调查和处理,建立药品不良反应和药品安全事件的报告和处理机制。
四、工作程序1. 委员会每年至少召开两次全体味议,主任委员或者副主任委员主持会议并提出议题。
2. 委员会会议的议题由主任委员和秘书长事先确定,委员可提出议题建议。
3. 委员会会议通过表决方式作出决策,决议需经过三分之二以上委员的允许方可生效。
4. 委员会会议的决议和意见书由秘书长起草,经主任委员审定后正式发布。
5. 委员会根据需要设立专门的工作组,负责具体的工作任务,工作组成员由委员会成员自愿报名并经主任委员批准。
五、附则1. 本章程的修改和解释权归药事管理委员会所有,修改和解释需经过三分之二以上委员的允许方可生效。
2. 本章程自发布之日起生效,委员会成立时即开始执行。
以上是药事管理委员会章程的详细内容,旨在规范委员会的组织结构、职责权限和工作程序。
医院相关药事管理制度范本

医院相关药事管理制度范本以下是一个医院药事管理制度的范本:1. 药事管理目标:- 确保患者获得安全有效的药物治疗;- 保证药物的采购、配送和使用过程的合规性;- 提高医院药物管理工作的效率和质量。
2. 药事管理组织架构:- 药事管理部门负责整个药物管理工作的组织和协调;- 药事管理委员会负责决策和监督相关事务;- 药师团队提供药物信息、指导和监督。
3. 药物采购与供应管理:- 严格按照国家相关法规和医院规定的采购程序进行采购;- 药物供应商必须符合医院规定的合格供应商要求;- 药物配送和存储必须符合相关规定,确保药物的安全和质量;- 采取有效措施防止药物盗窃、滥用和过期。
4. 药物处方和使用管理:- 医师必须符合相关规定,合理开具处方;- 药师必须认真审核处方的合理性和准确性;- 药师必须根据处方提供患者所需的正确药物信息和指导;- 避免患者重复用药和药物相互作用的风险。
5. 药物监测与抗菌药物管理:- 建立药物监测系统,及时收集和分析药物不良反应和药品质量问题;- 严格执行抗菌药物管理规定,防止抗菌药物滥用和耐药菌的产生。
6. 药物信息管理与教育培训:- 建立药物信息管理系统,确保药物信息的准确性和及时性;- 定期开展药学知识培训,提高医务人员的药物治疗水平;- 提供患者用药指导和药物信息咨询服务。
7. 药物管理规章制度:- 制定药品管理规章制度,明确各级别管理人员的职责和权限;- 提供药物管理相关的培训和指导材料,确保各级别管理人员理解和遵守规章制度;- 定期进行药品管理的评估和监督,发现问题及时纠正和改进。
请注意,上述范本仅供参考,实际的药事管理制度应根据医院的具体情况进行调整。
建议咨询专业药师或相关法律法规以确保制度的合规性。
药品零差价医院管理制度范文

药品零差价医院管理制度范文药品零差价是指药品在医院零售时的价格与采购价格之间的差额。
为了实现药品零差价、降低患者负担、推进医改,医院需要制定相应的管理制度,下面是药品零差价医院管理制度范文。
一、总则为规范医院药品零差价管理,促进医院合理用药和医改工作的顺利进行,制定本制度。
二、药品零差价管理组织机构1. 医务部门负责组织制定药品零差价管理细则、药品目录、药品采购和配送工作等。
2. 药事管理部门负责日常药品的管理工作,包括药品的采购、配送、库存控制、质量管理和核算等。
3. 审计部门负责对药品零差价管理进行监督和内部审核工作,确保管理制度的执行和效果。
三、药品零差价管理的基本原则1. 公开透明药品零差价管理应公开透明,确保患者和医务人员了解药品价格的合理性和合法性。
2. 严格控制药品采购成本医院要加强对药品采购的管理,严格控制药品采购成本,确保药品的质量和价格合理。
3. 合理利润分配医院药品零差价的利润应按照法律法规和相关政策规定进行合理的分配,确保医院的正常运营和发展。
四、药品零差价管理细则1. 药品目录制定医院应根据临床需要和患者用药情况,制定药品目录,将合适的药品纳入零差价管理范围,并在医院公示。
2. 药品采购和配送(1)采购渠道选择:医院应选择有资质的供应商进行药品采购,确保药品的质量和合理价格。
(2)采购方式:医院应采取公开招标、协议供货和集中采购等方式进行药品采购,确保采购过程公平公正。
(3)药品配送:医院应建立合理的药品配送机制,确保药品按时到达,减少库存积压。
3. 药品价格核算和调整(1)药品价格核算:医院应建立科学的药品价格核算制度,确保药品零售价格与采购价格之间的差额合理。
(2)药品价格调整:医院应根据国家政策和市场情况,及时调整药品价格,确保药品零售价格的合理性。
4. 药品信息共享和技术支持(1)药品信息共享:医院应充分利用信息化手段,加强药品信息共享的工作,提高药品采购的透明度。
2、药事管理学(第3章)

«美国药典» (U.S. Pharmacopeia ,USP) «国家处方集» (National Formulary, NF)
美国药典-国家处方集 (USP-NF) 是由美国药典委员会编辑出版 的关于药典标准的公开出版物。它包含关于药物、剂型、原料药、 辅料、医疗器械和食物补充剂的标准。
美国药典-国家处方集每年出版一次,最新版本:USP37 - NF 32, 于2014年5月1日生效。
二、欧洲药品管理局 European Medicines Agency,EMA
EMA原名为欧洲药品审评管理局(European Agency for the Evaluation of Medicinal Products,EMEA),成立于1995年,2004年改名 为欧洲药品管理局,总部设在伦敦。主要负责欧盟市场药品的审查、批准 上市,评估药品科学研究,监管药品在欧盟的安全性、有效性;同时还负 责协调、检查、监督欧盟各成员国的GAP、GMP、GLP、GCP等工作。
医学专业委员会 化学药品第一专业委员会 化学药品第二专业委员会 化学药品第三专业委员会 抗生素专业委员会 生化药品专业委员会 放射性药品专业委员会 生物技术专业委员会 病毒制品专业委员会 细菌制品专业委员会 血液制品专业委员会
国家药典委员会职责
(一)全体委员大会职责 1、修改和通过《药典委员会章程》; 2、审议和通过《中华人民共和国药典》编制大纲; 3、审议大会工作报告; 4、审议药品标准重大工作事项。 (二)执行委员会职责 1、监督检查全体委员大会有关决议的执行情况; 2、审议和通过《中华人民共和国药典》(草案)及其增补本; 3、审议和通过专业委员会年度工作报告和工作计划; 4、审议和决定药品标准发展战略问题;
中国食品药品检定研究院机构设置和职能
第2章药事管理组织机构

2、省食品药品监督管理局 主要职责: 主要职责: ⑴辖区内执行行政法规、规章。 辖区内执行行政法规、规章。 执行行政法规 发许可证,组织GMP GSP认证 GMP、 认证, ⑵发许可证,组织GMP、GSP认证,审查新药 申报资料 ⑶辖区内药品生产、经营、使用监督及抽验 辖区内药品生产、经营、 ⑷审查广告,发广告批准文号 审查广告, ⑸决定行政处罚 ⑹实施执业药师资格制度 ⑺领导省以下药品监督管理机构
§1 药品监督管理组织
一、药品监督管理组织体系 卫生部 --药政 药政、 --药政、药检 ↘ 国家药品监督管理局 (SDA) 1998
↓ 原国家医药管理局1978 原国家医药管理局1978 → 国家食品药品监督 管理局(SFDA) 管理局(SFDA) 2003 --药品生产 药品生产、 --药品生产、流通监管 直属国务院) (直属国务院) 1988↗ 国家中医药管理局 1988↗ 中药生产、 --中药生产 --中药生产、流通监管 ↓ 重属卫生部 2008
补充:SFDA内设机构 补充:SFDA内设机构 下设12个司室,包括: 下设12个司室,包括: 12个司室 规划财务司) 办公室 (规划财务司)、 食品安全协调司、 食品安全协调司、 药品注册司、 药品注册司、 药品安全监管司、 药品安全监管司、 人事教育司、 人事教育司、 机关党委、 机关党委、
药品监督管理的技术机构 三、药品监督管理的技术机构 1、中国药品生物制品检定所 主要职责: 主要职责: ①全国药品最高质量检定、仲裁 全国药品最高质量检定、 ②药品标准审批 ③提供标准物质 2、省药品检验所 3、市属机构 国家药典委员会: 1、国家药典委员会:制定和修订药品标准 药品审评中心: 2、药品审评中心:药品注册 3、药品认证管理中心 4、国家中药品种保护审评委员会办公室 兼管保健品) (兼管保健品) 药品评价中心: 5、药品评价中心:不良反应监测中心 6、执业药师资格认证中心 自学:每个机构的职能是什么? 自学:每个机构的职能是什么?
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
• (4)负责化妆品卫生许可、卫生监督管理和有关化妆品的审批工作。
• (5)负责药品、医疗器械行政监督和技术监督,负责制定药品和医 疗器械研制、生产、流通、使用方面的质量管理规范并监督实施。
• ( 6)负责药品、医疗器械注册和监督管理,拟订国家药品、医疗器 械标准并监督实施,组织开展药品不良反应和医疗器械不良事件监测, 负责药品、医疗器械再评价和淘汰,参与制定国家基本药物目录,配 合有关部门实施国家基本药物制度,组织实施处方药和非处方药分类 管理制度。
•
•
•
•
国家药典委员会的职责是组织制定和修订《中华人民共和国药典 》和药品标准;是法定的国家药品标准工作专业管理机构。常设办事 机构实行秘书长负责制。国家药典委员会由主任委员、副主任委员、 执行委员和委员组成,每五年换届一次。 现任的药典委员会是2002年10月组成的第八届委员会。下设24个 专业委员会,共有来自153个单位的311名委员组成。委员来自高校、 科研机构、医疗机构、药品检验部门、药品生产企业和管理部门。 为了提高药典委员会的学术地位、专业水平和社会影响力,第八 届国家药典委员会聘请了20名中国科学院和中国工程院院士为委员。
• •
3. 承办药品认证检查员的培训、考核和聘任,以及省 级药品监督管理部门的药品认证管理人员培训的具体工作; 组织与6个规章相关单位、企业的管理人员和技术人员的 培训。 • 4. 受国家食品药品监督管理局委托,负责《药品认证 公告》发布的具体工作。 • 5. 根据国家食品药品监督管理局的安排,开展药品认 证的国内、国际学术交流活动;承办国际间药品认证互认 的具体工作。 • 6. 承办国家食品药品监督管理局交办的其他事项.案 例 实施飞行检查制度。
•
省、自治区、直辖市药品检验所的业务技术科室一般设有:化学 药品室、中药室、抗生素室、药理室、生化室、药品标准室、药品监 督室、仪器分析室和实验动物饲养房等
2.1.3国家药典委员会
• 中华人民共和国药典委员会,简称国家药典委员会,为国家食品 药品监督管理局直属事业单位。 第一届中国药典编纂委员会,成立于1950年,负责制定中国药典。 是我国最早成立的标准化机构,是负责组织制定和修订国家药品标准 的技术委员会,是国家药品标准化管理的法定机构。 1998年,国家政府部门机构改革,国务院将卫生部的药政药检职 能调整移交给国家药品监督管理局,原隶属于卫生部的药典委员会从 1998年9月划归国家药品监督管理局,更名为国家药典委员会。 2003年,国家药典委员会归属国家食品药品监督管理局领导
•
•
2.1.4国家食品药品监督管理局药品审评中心P12
• 国家食品药品监督管理局药品审评中心为国家食品药 品监督管理局直属事业单位,是国家药品监督管理局药品 注册管理的技术审评机构。
•
ቤተ መጻሕፍቲ ባይዱ
其主要职责是为药品注册管理的科学化、规范化提供 技术支持,负责按照国家药品监督管理局颁布的《药品注 册管理办法》等规章,对有关药品注册申请进行技术审评。
1. 负责国家基本药物目录制定、调整的技术业务组织工作及其相 关工作。 2. 负责非处方药目录制定、调整的技术业务组织工作及其相 关工作。 3. 负责药品试生产期及上市后的再评价和药品淘汰筛选的技
术业务组织工作及其相关工作。
4. 负责全国药品、医疗器械产品不良反应监测的技术业务
组织工作及其相关工作。 5. 承办国家食品药品监督管理局交办的其他事项。
• 2.3.1药学教育组织
• 我国现代药学教育经历了近百年的发展历程,已形成由高等药学 教育、中等药学教育、药学继续教育构成的多层次、多类型、多种办 学形式的药学教育体系。据1999年底统计,我国有96所高等学校设 置有药学类专业(药学、中药学、药物制剂、制药工程等4种专业), 是世界上设置药学类专业的高校最多的国家。
2.1.6国家食品药品监督管理局药品评价中心
• 食品药品监督管理局药品评价中心设5个职 能处(室):办公室,国家基本药物处,非处方 药物处,药品临床评价处,药品不良反应监测处。
•
国家药品监督管理局药品评价中心事业编制 为40名。“国家药品不良反应监测中心”设在国 家食品药品监督管理局药品评价中心。主要职责
2 药事管理组织机构
案例导入:“肝素钠”事件有关调查情况
思考?
1、我国药品监督管理机构的主要职责是什么?
2、我国药品监督管理机构在保证药品安全方面做 了哪些工作?
2.1药品监督管理组织P9
welcome to use these PowerPoint templates, New Content design, 10 years experience
•
• •
• (二)药学协会P14
• 我国的药学协会主要有中国医药企业管理协会、中国大众药物协 会、中国化学制药工业协会、中国医药商业协会、中国医药教育协会 和中国执业药师协会。 • 1. 中国医药企业管理协会 成立于1985年,是我国医药工商企业 界的社会团体,该协会采取团体会员制的组织形式,只吸收团体会员。 协会主要从事人员培训、企业咨询、理论研究、信息服务等项工作, 编辑出版了《医药企业管理简讯》、《医药企业》杂志。中国医药企 业管理协会在业务上受中国企业管理协会的指导。 • 2. 中国非处方药物协会 其前身为中国大众药物协会(CPMA), 成立于1988年,并加入了世界大众药物协会。该协会也采取团体会 员制的组织形式。北京药厂、杭州中药二厂、中国医药工业公司等20 多个单位为其会员单位。1996年4月,在协会举行的第二届一次会员 代表大会上,更名为中国非处方药物协会。 • 3. 中国化学制药工业协会 成立于1988年,它是化学制药工业全 行业的社会经济团体,是政府与企业之间的桥梁和纽带,承担政府部 门委托的行业管理任务。该协会的宗旨是为企业服务,维护会员单位 的合法权益,依靠技术进步,提供信息服务,提高全行业经济效益。 截止1996年,共有会员单位316家。
2.2药品生产经营行业管理机构P13
• 药品生产经营组织为一种经济组织,主要包括药品生 产企业、药品经营批发企业、药品经营零售企业等。我国 药品生产经营组织及行业管理,为适应社会主义市场经济 发展的要求,正加速建立现代企业制度。 • 2.2.1我国医药行业管理机构的建立 • 1998年根据国务院机构调整方案,国家对药品行业的 职能进行调整,在国家经贸委下设医药管理处,履行对医 药行业管理职能。 • 2003年3月10号,十届全国人大一次会议通过了通过 了国务院机构改革方案,设立商贸部,主管国内外贸易和 国际经济合作。
2.3.3药学社会团体
• • (一)中国药学会 中国药学会成立于1907年,是我国成立较早的学术性社会团体之一。 1992年恢复加入了国际药学联合会(FIP),是亚洲药物化学联合会 (AFMC)的发起成员之一。 中国药学会是依法成立的由全国药学科学技术工作者组成的具有学术性、 公益性、非营利性的社会团体,是民政部批准登记的法人社会团体,是中国 科学技术协会的组成部分,是党和政府联系药学科学技术工作者的桥梁和纽 带,是推动中国药学科学技术事业发展的重要社会力量。 截止2002年,中国药学会己拥有10.5万名会员,1779名高级会员和43个 团体会员单位。 中国药学会根据药学发展的需要设立专业委员会,选举产生正副主任 委员,现有13个专业委员会。即中药和天然药物、药剂、抗生素、药物分析、 药物化学、生化药物、制药工程,医院药学、老年药学、海洋药物、药事管 理、药学史、军事药学专业委员会。学会根据工作需要设立工作委员会协助 理事会工作。现有组织工作、学术工作、科技开发工作、财务与基金管理工 作、国际学术交流工作、编辑出版工作、教育与科普工作7个委员会。
药品的特殊性,决定了对药品管理必须依法管理。我
国现行的药品监督管理组织,包括药品监督管理行政机构、
药品检验机构、国家食品药品监督管理局直属技术机构。 具体食品药品监督管理组织体系如图2-1-1所示。
Thank you!
2.1.1药品监督管理行政机构
•
2001年修订的《中华人民共和国药品管理法》中明确规定,国务院药品 监督管理部门主管全国药品监督管理工作。省、自治区、直辖市人民政府药 品监督管理部门负责所辖行政区域内的药品监督管理工作。 国家食品药品监督管理局是国务院部委管理的国家局,由卫生部管理,负 责对药品的研究、生产、流通、使用进行行政监督与技术监督;负责消费环 节食品卫生许可和食品安全监督管理,负责保健食品、化妆品的卫生许可和 卫生监督管理。其主要职责如下。
•
• (1)制定药品、医疗器械、化妆品和消费环节食品安全监督管理的
政策、规划并监督实施,参与起草相关法律法规和部门规章草案。
• (2)负责消费环节食品卫生许可和食品安全监督管理。
• (3)制定消费环节食品安全管理规范并监督实施,开展消费环节食 品安全状况调查和监测工作,发布与消费环节食品安全监管有关的信 息。
中国药品生物制品检定所的业务技术科室分为两大类,
即药品检验部分和生物制品检定部分。药品检验部分下设: 化学药物室、中药室、抗生素室、生化药品室、放射性同位 素室、计划生育药品室、药理毒理室、仪器分析室和情报资 料室等。生物制品检定部分下设:菌种室、菌苗室、肠道细 菌室、血清室、呼吸道病毒室、肠道病毒室、虫媒病毒室、
• 2.3.2药学科研组织 • 我国的药学科研组织有独立的药物研究院所以及附设在高等药学 院校、大型制药企业、大型医院中的药物研究所、室两种类型。全国 有独立的药物研究院所共130个,其行政管理隶属关系为中国科学院、 中国医学科学院、中医研究院、军事医学科学院等国家和地方科学院 系统以及中央和地方政府卫生行政主管部门、医药生产经营主管部门。 • 除大型制药企业设立的药物科研机构外,其他均为国家投资兴办的事 业单位。著名的药物研究单位有中国科学院上海药物研究所、中国医 学科学院药物研究所、中国中医研究院中药研究所、军事医学科学院 药物毒理研究所、上海医药工业研究院、天津药物研究院等。
