基础化学复习题
(整理)《基础化学》有机化学复习题.

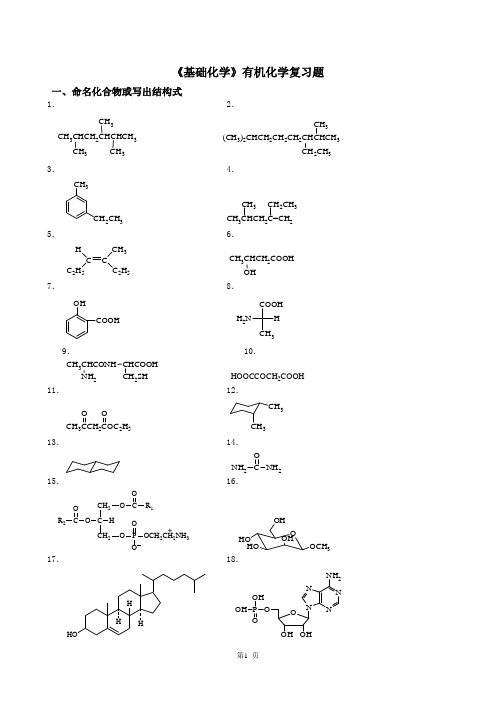
《基础化学》有机化学复习题一、命名化合物或写出结构式1. 2.CH 3CHCH 2CHCHCH 3CH 3CH 3CH 3(CH 3)2CHCH 2CH 2CH 2CHCHCH 3CH 2CH 3CH 33. 4.CH 3CH 2CH 3 CH 3CHCH 2C=CH 2CH 3CH 2CH 35. 6.C C H C 2H 5CH 3C 2H 5CH 3CHCH 2COOH7. 8.OHCOOHCOOHH 2NH CH 39. 10. CH 3CHCONH 2CHCOOH2SH HOOCCOCH 2COOH 11. 12.CH 322H 5O O3CH 313. 14. NH 2NH 2O15. 16.CH 2C CH 2O O OR 1HO C P OCH 2CH 2NH 3O OO R 2+O HOHOOHOCH 3OH17. 18.HHH HONNNN NH 2OOHOH P OH OH19.乙醚 20.顺-2-丁烯 21.异丙醇 22.乙酰苯胺 23.柠檬酸24.乙酸乙酯 25.阿司匹林 26.油酸 27.卵磷脂 28.葡萄糖29.半胱氨酸 30.赖氨酸 31.缩二脲 32.ATP二、是非题(正确的打 ,错误的打×)1.具有C n H2n通式的烃一定是烯烃。
()2.烷烃中的碳原子都是sp3杂化,烯烃中的碳原子都是sp2杂化。
()3.环己烯分子中的碳原子都是sp2杂化的。
()4.凡是双键碳原子都是sp2杂化。
()5.乙烷有两种构象,一种是重叠式构象,一种是交叉式构象。
()6.碳原子的类型分为伯、仲、叔、季碳,氢原子的类型也分为伯、仲、叔、季氢。
()7.具有旋光性的物质一定存在对映异构现象。
()8.一对对映体的混合物能用蒸馏的办法分开。
()9.左旋2-丁醇和右旋2-丁醇的混合液可用蒸馏方法分开。
()10.只有一个手性碳原子的分子一定具有旋光性。
()11.一个分子结构中含有3个手性碳原子,则这个分子一定是手性分子。
基础化学复习题

一、选择题1.下列关于电子云的说法不正确的是( )A. 电子云是描述核外某空间电子出现的几率密度的概念;B. 电子云是│ψ│2的数学图形;C. 电子云有多种图形,黑点图只是其中一种;D. 电子就象云雾一样在原子核周围运动,故称为电子云.2.下列说法不正确的是( )A. 氢原子中,电子的能量只取决于主量子数n;B. 多电子原子中,电子的能量不仅与n有关,还与l有关;C. 波函数由四个量子数确定;D. m s=±½表示电子的自旋有两种方式.3.n=4时m的最大取值为( )A. 4B. ±4C. 3D. 04.2p轨道的磁量子数可能有( )A. 1.2B. 0.1.2C. 1.2.3D. 0.+1.-15.原子中电子的描述不可能的量子数组合是( )A. 1.0.0.+½B. 3.1.1.-½C. 2.2.0.-½D. 4.3.-3.-½6.下列电负性大小顺序错误的是( )A. H>LiB. P<NC. Si>CD. Cl>Br7.下列说法错误的是( )A、电子的钻穿效应越强,电子能量越低;B、电子所受屏蔽效应越强,电子能量越低;C、n值相同,l越小,则钻穿效应越强;D、屏蔽效应和钻穿效应的结果引起能级交错.8.关于影响屏蔽常数σ大小的因素,正确的说法是( )A. 被屏蔽电子的l值越小,σ值越大;B. 屏蔽电子的n值越小,σ值越大;C. 被屏蔽电子离核越远,σ值越大;D. 屏蔽电子的数目越少,σ值越大;9.基态原子的核外电子在原子轨道上的能量大小关系不正确的是()A. 3s>2sB. 3p>3sC. 4s>3dD. 3d>3s10.下列关于原子半径的周期性变化描述不严谨的是()A.元素的原子半径随元素原子序数的递增呈周期性变化B.同周期元素随着原子序数的递增,元素的原子半径自左到右逐渐减小C.同主族元素随着原子序数的递增,元素的原子半径自上而下逐渐增大D.电子层数相同时,有效核电荷数越大,对外层电子的吸引作用越强11.下列各离子的电子排列式错误的是()A. Na+1s22s22p6B. F¯1s22s22p6C N3+ 1s22s22p6 D. O2¯1s22s22p612.下列有关认识正确的是()A.各电子亚层的原子轨道数量按s、p、d、f的顺序分别为1、3、5、7 B.各电子层的电子亚层能级都是从s能级开始至f能级结束C.各电子层含有的电子亚层数为n-1D.各电子层含有的电子数量为2n213.Ca原子的电子排布式写成1s22s22p63s23p63d2,其违背了()A.能量最低原理B.能量守恒原理C.泡利不相容原理D.洪特规则14.共价键最可能存在于()。
化学基础复习题(附答案)

化学基础复习题(附答案)一、单选题(共100题,每题1分,共100分)1、下列化合物中,不能发生酯化反应的是A、HCOOHB、CH3COOHC、CH3CH2OHD、CH3CHO正确答案:D2、能与浓溴水反应生成白色沉淀的是()A、乙烯B、苯酚C、乙醇D、苯正确答案:B3、乙醇沸点(78.3℃)与分子量相等的甲醚沸点(-23.4℃)相比高得多是由于 ( )A、乙醇能形成分子间氢键,甲醚不能B、甲醚能与水形成氢键C、甲醚能形成分子间氢键,乙醇不能D、乙醇能与水形成氢键,甲醚不能正确答案:A4、分子中含有碳碳双键的是( )A、苯B、丙烯C、乙炔D、聚乙烯正确答案:B5、下列使蛋白质变性的物理方法是( )A、紫外线照射B、加重金属盐C、加酸D、加有机溶剂正确答案:A6、一定温度下,加水稀释弱酸,数值将减小的是( )B、αC、pHD、[H+]正确答案:D7、与溶液渗透压大小有关的因素是A、溶质颗粒的大小B、溶质的颗粒总数C、溶质的性质D、溶剂的性质正确答案:B8、欲配制PH=4.50的缓冲溶液,若用HAc及NaAc配制,则c(HAc)及c(NaAc)的浓度之比为(HAc的pKa=4.76)( )A、4.76/1B、1/4.76C、1.78/1D、1/1.78正确答案:C9、下列哪项不属于羧酸衍生物()A、乳酸B、甲酸乙酯C、乙酰胺D、乙酸酐正确答案:A10、苯酚俗称()A、石炭酸B、溴苯C、苄醇D、甘油正确答案:A11、在常温下,pH=6的溶液与pOH=6的溶液相比,其氢离子浓度A、高10倍B、高2倍C、高100倍正确答案:C12、单糖与浓酸和α-萘酚反应能显紫色,这一鉴定糖的反应叫( )A、糖脎反应B、Seliwanoff反应C、成苷反应D、Molish反应正确答案:D13、下列不能做为配位体的物质是( )A、C6H5NH2B、CH3NH2C、NH4+D、NH3正确答案:C14、为了保证某工作液的PH值为4--5,应选用( )缓冲对配制缓冲溶液。
《基础化学》有机化学复习题
《基础化学》有机化学复习题一、命名化合物或写出结构式1. 2.H 3CHCH 2CHCHCH 3CH 3CH 3CH 3CH 3)2CHCH 2CH 2CH 2CHCHCHCH 2CH 3CH 33. 4.H 3CH 2CH 3H 3CHCH 2C=CH 2CH 3CH 2CH 35. 6.CH C 2H 5CH 3C 2H 5H 3CHCH 2COOH OH7. 8.HCOOHOOHH 2NH CH 39. 10. H 3CHCONH NH 2CHCOOH CH 2SHOOCCOCH 2COOH11. 12.H 3CCH 2COC 2H 5O OH 3CH 313. 14.NH 2NH 2O15. 16.C H 2CC H 2O OC OR 1HOCP O C H 2C H 2N H 3O OO R 2+17. 18.HHH H O19.乙醚 20.顺-2-丁烯 21.异丙醇 22.乙酰苯胺 23.柠檬酸 24.乙酸乙酯 25.阿司匹林 26.油酸 27.卵磷脂 28.葡萄糖 29.半胱氨酸 30.赖氨酸 31.缩二脲 32.ATP二、是非题(正确的打 ,错误的打×)1.具有C n H 2n 通式的烃一定是烯烃。
( ) 2.烷烃中的碳原子都是sp 3杂化,烯烃中的碳原子都是sp 2杂化。
( ) 3.环己烯分子中的碳原子都是sp 2杂化的。
( ) 4.凡是双键碳原子都是sp 2杂化。
( ) 5.乙烷有两种构象,一种是重叠式构象,一种是交叉式构象。
( ) 6.碳原子的类型分为伯、仲、叔、季碳,氢原子的类型也分为伯、仲、叔、季氢。
( ) 7.具有旋光性的物质一定存在对映异构现象。
( ) 8.一对对映体的混合物能用蒸馏的办法分开。
( ) 9.左旋2-丁醇和右旋2-丁醇的混合液可用蒸馏方法分开。
( ) 10.只有一个手性碳原子的分子一定具有旋光性。
( ) 11.一个分子结构中含有3个手性碳原子,则这个分子一定是手性分子。
基础化学复习题

基础化学复习题单项选择题1. 理想气体绝热自由膨胀时,则 BA . 0U ∆>,0S ∆=B .0U ∆=,0S ∆>C . 0U ∆>,0S ∆>D .0U ∆=,0S ∆= 2.下面关于标准摩尔生成焓的描述中,不正确的是 CA.生成反应中的单质必须是稳定的相态单质B.稳态单质的标准摩尔生成焓被定为零C.生成反应的温度必须是D.生成反应中各物质所达到的压力必须是100KPa 3. 理想气体在可逆的绝热膨胀过程中是 BA . 内能增加B . 熵不变C . 熵增大D . 温度不变 4. 封闭系统中吉布斯函数G 与热力学U 的关系是 DA. G > UB. G < UC. G = UD. 无固定关系A. 零级反应 B . 一级反应 C . 二级反应 D . 三级反应 5.工作在100℃和25℃的两个大热源间的卡诺机其效率是 AA . 20%B . 25%C . 75%D . 100% 6.若将人作为一个体系,则该体系是 CA .孤立体系 B.封闭体系 C.敞开体系 D.半封闭系统7.在100℃, kPa 下,1 mol 水全部向真空气化为100℃, kPa 的水蒸气,则该过程为 B A . ΔG < 0,不可逆 B . ΔG = 0,不可逆 C . ΔG > 0,不可逆 D . ΔG < 0,可逆 8. 液态水在100℃及 kPa 下汽化,则该过程的 DA . ΔH = 0B . ΔS = 0C . ΔA = 0D . ΔG = 0 9.对于封闭体系的热力学 , 下列各组状态函数之间的关系正确的是 B A . A > U B . A < U C . G < U D . H< A 10. 下列各式表示偏摩尔量的是 A A . )(..(B A n P T B A n U≠⎪⎭⎫ ⎝⎛∂∂ B . )(..S (B A n P B A n H ≠⎪⎭⎫ ⎝⎛∂∂C . )(..(B A n V T B A n A≠⎪⎭⎫ ⎝⎛∂∂ D . )(..B (B A n P T B A n ≠⎪⎭⎫ ⎝⎛∂∂μ 11.刚性绝热箱内发生一化学反应,则反应体系是 AA.孤立体系B.敞开体系C.封闭体系D.绝热体系 12. 已知反应Cs+O 2g →CO 2 g 的ΔH,下列说法中不正确的是 C A . ΔH 为CO 2g 的生成热 B . ΔH 为CS 的燃烧热 C . ΔH 与反应的ΔU 数值不等 D . ΔH 与反应的ΔU 数值相等 13.封闭系统中吉布斯函数A 与热力学U 的关系为 BA . A > UB . A < UC . A = UD . 无固定关系 14. 热力学第三定律可以表示是 BA . 在0K 时,任何晶体的熵等于零B . 在0K 时,纯物质完美晶体的熵等于零 C. 在0℃时,任何晶体的熵等于零 D . 在0℃时,完美晶体的熵等于零 15. 一级反应完成%所需时间是完成50%所需时间是 CA . 2倍B . 5倍C . 10倍D . 20倍 16. 选出下列性质参数中属于容量性质的量是 CA . 温度TB . 浓度cC . 体积VD . 压力p17. 在恒温,恒压下,已知反应A →2B 和2A →C 的反应热分别为ΔH 1和ΔH 2,则反应C →4B 的反应热ΔH 3是 DΔH 1+ΔH 2 B . ΔH 2-2ΔH 1 C . ΔH 1+ΔH 2 D . 2ΔH 1-ΔH 2 18. 不挥发的溶质溶于溶剂中形成溶液之后将会引起C A . 熔点升高 B . 沸点降低 C . 蒸汽压降低 D . 总是放出热量 19.下列是化学势的是 C A . )(..(B A n P T B A n U≠⎪⎭⎫ ⎝⎛∂∂ B . )(..(B A n P T B A n H ≠⎪⎭⎫ ⎝⎛∂∂ C . )(..(B A n V T B A n A≠⎪⎭⎫ ⎝⎛∂∂ D . )(..(B A n V T B A n G ≠⎪⎭⎫ ⎝⎛∂∂ 20. 在 - 10 °C, 下,水的化学式势μ水与冰的化学势μ冰的大小关系应为 CA . μ水=μ冰B . μ水 >μ冰C . μ水 <μ冰D . 无法确定21. 理想气体从状态p 1V 1T 自由膨胀至p 2V 2T ;此过程的ΔA 与ΔG 的关系是 C A . ΔA>ΔG B . ΔA<ΔG C . ΔA=ΔG D . 不能确定22. 某反应的反应物消耗一半的时间正好是反应物消耗1/4的时间的2倍,则该反应的级数是BA . 0.5级反应B . 0级反应 级反应 级反应23. 在25℃下反应COg+2H 2g =CH 3OHg 的16.90-⋅-=∆mol KJ H m r θ ,为提高反应的平衡产率,应采取的措施是 DA .升高温度和压力B . 降低温度和压力C .升高温度,降低压力D . 降低温度,升高压力24. 某二级反应,反应物消耗 1/3 需时间 10 min ,若再消耗 1/3 还需时间为 C A . 10 min B . 20 min C . 30 min D . 40 min 25. 对于某反应,若反应物反应掉其43所需时间恰是它反应掉21所需时间的2倍,则该反应的级数是 B填空题1.按标准摩尔生成焓与标准摩尔燃烧焓的定义,在C 石墨、COg 和CO 2g 之间, CO 2g 的标准摩尔生成焓正好等于 C 石墨 的标准摩尔燃烧焓;2. 亨利常数随温度的升高而 增大 增大、减小或不变;3. 反应2A → B ,则-dc A /dt 和dc B /dt 之间的关系是 -dc A /dt=2dc B /dt ;4. 在绝热、体积恒定的容器中发生一化学反应,使容器中温度、压力都增加,则该过程的∆U = 0;5. 设理想气体反应)(3)()(g C g B g A =+达化学平衡,在等温下维持系统总压不变,向系统中加入惰性气体,平衡__向右__移动;6. 反应A → 2B ,则-dc A /dt 和dc B /dt 之间的关系是 -2dc A /dt=dc B / ;7. A 、B 两理想液态混合物在T-x 图上出现最高点,则该混合物对拉乌尔定律产生 负偏差 偏差;8. 在恒温恒压下,一切相变化必然朝着化学势 降低 的方向自动的进行; 9. 化学反应热会随反应温度改变而改变的原因是 .r 0p m C ∆≠ ; 10. 实际气体绝热自由膨胀,则该过程的∆S _>__ 0;11. 糖可以顺利溶解在水中,说明固体糖的化学势较糖水中的糖的化学势__高__;12. 卡诺热机在T 1=600K 的高温热源和T 2=300K 的热源间工作,其热机效率η= 50% ; 13. 按标准摩尔生成焓与标准摩尔燃烧焓的定义,在C 石墨、COg 和CO 2g 之间, C 石墨的标准摩尔燃烧焓正好等于 CO 2g 的标准摩尔生成焓;14.在总压不变时,加入惰性气体的结果与___降低_____压强的结果是相同的; 15. 在绝热、体积恒定的容器中发生一化学反应,使容器中温度、压力都增加,则该过程的ΔU_____=_____0;名词解释 1. 偏摩尔量均相系统中,系统的广度性质Z 在恒温恒压除B 组分其它组分保持不变的条件下,Z 函数随B 组分的变化量为B 组分的偏摩尔量:..(,)Z Z m B T p n c c B n ≠⎛⎫∂= ⎪∂⎝⎭ 2. 分解压化合物的分解压是指该化合物纯液体或纯固体分解出气体的分解反应在指定温度下达到平衡时,生成物气体的总压力; 3. 化学势均相系统中,系统广度性质吉布斯函数在恒温恒压除B 组分其它组分保持不变的条件下,吉布斯函数随B 组分的变化量为B 组分的化学势即偏摩尔吉布斯函数:B ..(,)G m B T p n c c B G n μ≠⎛⎫∂== ⎪∂⎝⎭ 4. 卡诺循环热机以理想气体为工作介质,工作过程由两个等温可逆过程和两个绝热可逆过程组成,它的循环工作过程成为卡诺循环; 5. 吉布斯自由能吉布斯自由能G 是系统状态函数的组合即G=H -TS,也是系统的状态函数;封闭系统在恒温恒压非体积功为零的条件下,吉布斯自由能的变化量可以作为判据,判断过程的方向; 6. 化学反应速率化学反应速率的定义:设化学反应0B BB ν=∑ ,反应速率1BB dn d dt dtξν= 定容反应时反应速率1BB dc v dtν=7. 卡诺定理在两个不同温度热源之间工作的所有热机,以可逆热机效率最大;热机效率η只与两个热源的温度有关:121T T T η-=T 1是高温热源的温度,T 2是低温热源的温度 8. 亥姆霍兹自由能亥姆霍兹自由能A 是系统状态函数的组合即A=U —TS,也是系统的状态函数;封闭系统在恒温恒容非体积功为零的条件下,亥姆霍兹自由能的变化量可以作为判据,判断过程的方向;9. 稀溶液依数性稀溶液溶质是非挥发性的的某些性质只依赖溶液中溶质分子的数量,而与溶质分子本性无关的性质;如溶剂蒸汽压降低,凝固点降低,沸点升高和渗透压; 10. 标准平衡常数标准平衡常数K Θ的定义式:exp[/()]m K rG RT θθ=-∆标准平衡常数在理想气体化学反应中是一定温度下平衡时的压力商, 即()/BeqB BK p p νθθ=∏ 计算题1、4mol N 2 在27℃,等压升温至127℃,求此过程的W 、Q 、△U 和△H ; 该气体可视为理想气体,其 = ; 解:.21Q ()11.20p m H nC T T kJ =∆=-= .21U ()()7.874p m n C R T T kJ ∆=--=3.326W U Q kJ =∆-=-计算该反应CO 2g+4H 2g →CH 4g+2H 2Og 在时的G m r θ∆和K θ; 解:反应CO 2g+4H 2g →CH 4g+2H 2Og 的θm rH ∆=θνm f BB H ∆∑B,=θm f H ∆ CH 4,g +2θm f H ∆ H 2O,g- θm f H ∆ CO 2,g -4θm f H ∆ H 2,g =mol()∑=∆Bm B m K S K rS )15.298(15.298θθν=θm S CH 4,g +2θm S H 2O,g- θm S CO 2,g -4θm S H 2,g =所以1113.45.r m m m G rH T rS kJ mol θθθ-∆=∆-∆=-ln 45.77mrG K RTθθ∆=-= K Θ=3、已知水在100℃,下的摩尔蒸发焓140.668Vap m H kJ mol -∆=⋅,试计算1kg 水在100℃,条件下,蒸发为水蒸气的Q 、W 、△U 及△H;水蒸气可按理想气体处理2311810H O M kg mol --=⨯⋅解:. 100040.668/2259.318p Q H mol kJ mol kJ =∆=⨯= 310008.314373.1510172.3518W nRT kJ kJ -=-=-⨯⨯⨯=2087.05U W Q kJ ∆=+=4. 化学反应)(2)(2)()(224g H g CO g CO g CH +=+,已知25℃时热力学数据1利用θB m f H .∆θB m S .,求上述反应在25℃时θm rS ∆,θm rG ∆2利用θB m f G .∆,求上述反应在25℃时θm rG ∆及K θ; 解:1反应)(2)(2)()(224g H g CO g CO g CH +=+1242.269.247)()()(2)(2-=∆-∆-∆+∆=∆mol kJ CO H CH H H H CO H rH m f m f m f m f m θθθθθ242112()2()()()256.712..m m m m m rS S CO S H S CH S CO J K molθθθθθ--∆=+--=1.73.170-=∆-∆=∆mol kJ S T H G m r m r m r θθθ224212()2()()()170.74.m f m f m f m f m rG G CO G H G CH G CO kJ molθθθθθ-∆=∆+∆-∆-∆=ln 68.88mrG K RTθθ∆=-=- K 1Θ=5. 25℃下,密闭恒容的容器中有10g 固体萘)(810s H C 在过量的()g O 2中完全燃烧成()g CO 2和()l O H 2;过程放热;已知 1810.128)(-=mol g H C M ,求1()()()108222()12104C H s O g CO g H O l +=+的反应进度; 2)(810s H C 的θm c U ∆; 3)(810s H C 的θm c H ∆; 解:1mol M m 078125.012810===ξ 2 1.1.5142078125.0727.401--=-==∆mol kJ molkJQ U Vm c ξθ311131.06.5147.)96.41.5142(.1015.298314.82.1.5142------=--=⨯⨯⨯--=∆+∆=∆mol kJ mol kJ mol kJ molkJ nRTU H m c m c θθ6、 已知下列数据 物质COg H 2g CH 3OHg 11../--K mol J S m θ1./-∆mol kJ H m f θ求时,下列反应COg + 2H 2g == CH 3OHg 的θm rG ∆和θK ; 解:反应COg + 2H 2g == CH 3OHg 的 ∑--=∆-=∆1,.18.90molkJ H rH B m f Bm θθν11,..53.219--∑-==∆K mol J S rS B m B m θθν所以1.72.24--=∆-∆=∆mol kJ rS T rH G m m m r θθθ975.9ln =∆-=RTrG K mθθK Θ=7. 2mol 双原子理想气体从始态300K 、50dm 3,先恒容加热至400K,再恒压加热至体积增大到100 dm 3,求整个过程的Q,W.ΔU,及ΔH;已知R c m v 25.= 解:过程为⎪⎩⎪⎨⎧==−→−⎪⎩⎪⎨⎧==−→−⎪⎪⎩⎪⎪⎨⎧===23333)2(2122)1(1311100400503002pp dm V T p V V K T p dm V KT mol2为定压过程 所以K T V V T 8002233=⨯=J J J K R mol K R T T nC T T nC Q Q Q m p m v 2.274362.232794157)400800(272)300400(252mol )()(23.12.21=+=-⨯+-⨯=-+-=+= JK R T T nR V V p W W W W 2.6651)400800(2mol )()(23232221-=-⨯-=--=--==+=J K K R T T nC U m v 20785)300800(252mol )(13.=-⨯=-=∆ JK K R T T nC H m p 29099)300800(272mol )(13.=-⨯=-=∆ 8、 已知25℃时的下列数据: 物质Ag 2Os CO 2g Ag 2CO 3s11/.m S J mol K θ--⋅1/f m H kJ mol θ-∆⋅求25℃时Ag 2CO 3s 的分解反应Ag 2CO 3s →Ag 2Os + CO 2g 的m rG θ∆和K θ; 解:25℃时反应Ag 2CO 3s → Ag 2Os + CO 2g ∑-=∆-=∆1,.241.81mol kJ H rH B m f Bm θθν11,..64.167--∑==∆K mol J S rS B m B m θθν所以1.26.31-=∆-∆=∆mol kJ rS T rH G m m m r θθθ617.12ln -=∆-=RTrG K mθθK 1Θ=9. 1mol 理想气体于27℃,状态下等容升温至97℃,则压力升到;求整个过程的Q,W, ΔU 及ΔH;已知该气体的C v,m 恒定为mol; 解:已知: 1mol 理想气体 = J/Q =ΔU = T 2 – T 1 = kJ ΔH = T 2 – T 1 = kJ W = 010、已知在有如下数据 物质CO 2g NH 3g H 2Og CONH 22s 11/.m S J mol K θ--⋅1/f m H kJ mol θ-∆⋅求时,反应CO 2g+ 2NH 3g → H 2Og + CONH 22s 的m rG θ∆及标准平衡常数K Ө ; 解:,11m B f m BrH H θθν--∆=∆=⨯⋅=⋅∑(-241.83-333.19+393.51+246.19)kJ mol -89.13kJ mol ,1111188.82+104.60213.762192.61 305.56m B m BrS S J mol K J mol K θθν----∆==--⨯⋅⋅=-⋅⋅∑() 31189.13298.15305.56101.97.r m m mG rH T rS kJ mol kJ mol θθθ---∆=∆-∆=-+⨯⨯⋅=() ln 0.795mrG K RTθθ∆=-=- K Θ=。
基础化学复习题
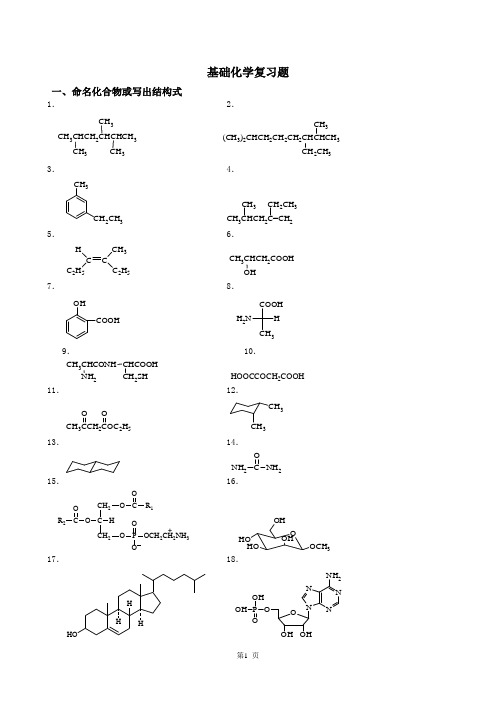
基础化学复习题一、命名化合物或写出结构式1. 2.CH 3CHCH 2CHCHCH 3CH 3CH 3CH 3(CH 3)2CHCH 2CH 2CH 2CHCHCH 3CH 2CH 3CH 33. 4.CH 3CH 2CH 3 CH 3CHCH 2C=CH 2CH 3CH 2CH 35. 6.C C H C 2H 53C 2H 5CH 3CHCH 2COOHOH7. 8.OHCOOHCOOHH 2NH CH 39. 10.CH 3CHCONH NH 2CHCOOHCH 2SH HOOCCOCH 2COOH11. 12.CH 3CCH 2COC 2H 5O OCH 3CH 313. 14. C NH 2NH 2O15. 16.CH 2C CH 2O O COR 1HO C P OCH 2CH 2NH 3O OO R 2+O HOHOOHOCH 3OH17. 18.HHH HONNNN NH 2OOHOH OOP OH OH19.苯酚 20.顺-2-丁烯 21.丙酮 22.乙酰苯胺 23.柠檬酸24.乙酸乙酯 25.阿司匹林 26.油酸 27.卵磷脂 28.葡萄糖29.半胱氨酸 30.赖氨酸二、是非题(正确的打✓,错误的打×)1.烷烃分子都是非极性分子。
()2.环己烷有两种构象,一种是椅式构象,一种是船式构象。
()3.在过氧化物存在下,烯烃与氯化氢的加成遵循马氏规则。
()4.凡是双键碳原子都是sp2杂化。
()5.乙烷有两种构象,一种是重叠式构象,一种是交叉式构象。
()6.碳原子的类型分为伯、仲、叔、季碳,氢原子的类型也分为伯、仲、叔、季氢。
()7.具有旋光性的物质一定存在对映异构现象。
()8.一对对映体的混合物能用蒸馏的办法分开。
()9.左旋2-丁醇和右旋2-丁醇的混合液可用蒸馏方法分开。
()10.只有一个手性碳原子的分子一定具有旋光性。
()11.一个分子结构中含有3个手性碳原子,则这个分子一定是手性分子。
《基础化学》复习题

《基础化学》复习题填空题1 .[Ag(NH3)2]+习惯名称______________。
2. 五羰基铁、银氨配离子的化学式分别为 ____________。
3.四氨合铜(Ⅱ)配离子的化学式是________________4. 2Cu+ Cu+Cu2+中,既为氧化剂又为还原剂是______,Cu与Cu2+氧化性强的是____________。
5.指出化学反应方程式 2KMnO4+5H2O2+6HNO3=2Mn(NO3)2+ 2KNO3+8H2O+5O2↑中氧化剂是__________,还原剂为_____________。
6.写出电对I2/I-的半反应: ________________________。
7. Fe3+,Fe2+,Fe三种氧化值不同的物种,氧化性最强的是Fe3+,还原性最强的Fe。
8.Hg2Cl2中Hg元素的氧化值为___________。
9. 赤铁矿的主要成分为________。
10.电子层,电子亚层,电子云的伸展方向,电子的自旋方向可以分别用_________,_________,________,____符号表示。
11.. Fe 原子在基态时有4个未配对的电子。
12.下列反应处于平衡状态, X(g)+Y(g) 4Z(g) △H=-45kJ·mol-1当同时升高温度加入正催化剂时,正反应速度将__________,化学平衡将________。
13.已知: A+B=C为简单反应,则此反应速度常数的单位是______________。
14.影响化学反应速率的外界条件主要有_____________、______________、_____________。
15.正反应的活化能大于逆反应的活化能,则______________为吸热反应。
16. 标准平衡常数的计算中,规定标准压力为_________,标准浓度为___________。
17. 可逆反应指的是__________________________。
化学基础习题库及答案

化学基础习题库及答案一、单选题(共100题,每题1分,共100分)1、下列化合物能与托伦试剂反应生成银镜的是()A、丙酸B、丙酮C、甲醇D、甲酸正确答案:D2、下列化合物中酸性最强的是()A、α-羟基丙酸B、β-羟基丙酸C、丙酸D、α,β-二羟基丙酸正确答案:D3、在氨溶液中加入少量盐酸,使:( )。
A、溶液OH-浓度变小B、NH3的Kb变大C、NH3的α增大D、pH值保持不变正确答案:C4、下列说法正确的是:()A、增大反应物的浓度,平衡向生成物浓度增大的方向移动。
B、有气体存在的可逆反应,该变压强,都会使化学平衡移动。
C、加热能使吸热反应速率加快,放热反应速率减慢,平衡向吸热反应方向移动。
D、凡能影响反应速率的因素,都能使化学平衡移动正确答案:A5、下列可用来区分葡萄糖和果糖的是( )A、斐林试剂B、苯肼C、托伦试剂D、赛利凡诺夫试剂正确答案:D6、 CH3CH2CH2CH3与CH3CH(CH3)2是什么异构体?( )A、碳架异构B、位置异构C、官能团异构D、互变异构正确答案:A7、既能发生水解反应,又能发生银镜反应的物质是()A、麦芽糖B、蔗糖C、丙酸甲酯D、葡萄糖甲苷正确答案:A8、欲使蛋白质沉淀而不变性,应选用( )A、浓硫酸B、重金属盐C、甲醛D、硫酸铵正确答案:B9、人体血浆中最重要的缓冲对是A、H2PO4 — HPO42-B、HCO3 — CO32-C、H2CO3 — HCO3-D、HPO42 — PO43-正确答案:C10、下列试剂中,常用于糖尿病患者尿液中葡萄糖含量检查的是( )A、FeCl3B、溴水C、班氏试剂D、茚三酮溶液正确答案:C11、医用生理盐水的质量浓度是多少?A、8g/LB、10g/LC、9g/LD、7g/L正确答案:C12、有关简单的饱和链烃的叙述:①都是易燃物;②特征反应都是取代反应;③相邻两个烷烃在分子上组成相差一个甲基。
正确的是( )A、②和③B、①和②C、①D、①和③正确答案:B13、可以用来判断油脂不饱和程度的是( )A、酸值B、皂化值C、碘值D、密度正确答案:C14、某缓冲溶液的共轭碱的Kb=1.0×10-6,从理论上推算该缓冲溶液的缓冲范围是( )A、5~7B、6~8C、7~9D、5~6正确答案:C15、 HPO42-的共轭酸是( )A、H2PO4-B、OH-C、H3PO4D、PO43-正确答案:A16、下列哪种物质具有致癌性( )A、蒽B、菲C、萘D、苯并芘正确答案:D17、下列有机物分子中不含有羧基的是()A、苯甲酸B、过氧乙酸C、乳酸D、苯酚正确答案:D18、人的肠胃不能消化的多糖是. ( )A、纤维素B、糖原C、右旋糖酐D、淀粉正确答案:A19、将淀粉碘化钾混合溶液装在半透膜中,浸泡在盛有蒸馏水的烧杯中,过一段时间后取出杯中液体进行试验,不能证明半透膜有破损的是:( )A、加入碘水变蓝B、加入碘化钠不变蓝C、加入FeCl3 溶液变蓝D、加入溴水变蓝正确答案:B20、下列化合物中无顺反异构现象的是()A、2-氯-2-丁烯B、2-甲基-2-丁烯C、3-甲基-2-戊烯D、2-丁烯正确答案:B21、下列不属于有机物的是 ( )A、HCOOHB、C2H4C、CH3OHD、HCN正确答案:D22、不能配制 pH = 7 左右的缓冲溶液的共轭酸碱混合物是( ) (已知HClO :K = 3.4 × 10-8 H2CO3 :K1 = 4.2 × 10-7 ,K2 = 5.6 × 10-11 H3PO4 :K1 = 7.6 × 10-3 ,K2 = 6.3 × 10-8 ,K3 = 4.4 × 10-13)A、NaHCO3-Na2CO3B、NaH2PO4-Na2HPO4C、HClO-NaClOD、H2CO3-NaHCO3正确答案:A23、构成蛋白质的基本单位是( )A、多肽B、β-氨基酸C、α-氨基酸D、肽链正确答案:C24、β-醇酸加热脱水生成( )。
基础化学II复习题

第七章烃第一节烷烃一、填空题1.具有同一,相似,且在组成上相差及其整数倍的一系列化合物称为。
2.有机物分子中,连接在伯、仲、叔碳原子上的氢原子分别称为、和。
3.烷烃分子中的的被其他原子或取代的反应,称为取代反应,被卤原子取代的反应称为。
4.在有机化学中,通常把在有机化合物分子中或的反应,称为氧化反应,5.烷烃的通式为. 。
烷烃的化学性质比较稳定,通常不与、和作用。
6.甲烷分子的立体构型为,4个氢原子占据的4个顶点,碳原子处在。
7.大多数有机化合物组成上含有、、、等元素。
8.烃是指由和两种元素组成的化合物。
答案:1.分子式,结构,CH2,同系物2.伯氢、仲氢、叔氢3.氢原子,原子团,卤代反应4.加氧,失氢5.C n H2n+2,强酸,强碱,强氧化剂6.正四面体结构,正四面体,正四面体的中心7.碳,氢,氧,氮8.碳,氢二、选择题1.有机物分子中的重要化学键是()A.离子键 B.共价键 C. 配位键 D.氢键2.下列物质中属于烷烃的是()A C2H2B C5H12C C2H4D C6H63.有机化合物的性质主要决定于()A.组成分子间的聚集状态B.所含官能团的种类、数目和分子量C.构成分子的各原子间的组成比例D.构成分子的各原子的空间排列4.己烷的异构体中哪一个沸点最高()A.己烷B.2-甲基戊烷C.2,3-二甲基丁烷D.2,2-二甲基丁烷5.烷烃卤化反应机理是通过生成何种中间体进行的()A.碳正离子B.游离基C.碳负离子D.协同反应无中间体6.下列物质属于有机物的是()A.COB.CH4C.H2CO3D.NaCO37.烷烃分子的结构特点是()A.含双键B. 含三键C.含苯环D. 只有碳氢单键8.某烃的分子式为C5H12,其构造异构体有A.2种B.3种C.4种D.5种9.脂肪族化合物是指A.开链化合物B.直链化合物C.碳环化合物D.含苯环的化合物10.下列物质中,在光照条件下,能与丙烷发生取代反应的是A.H 2B.H 2OC.HBrD.Cl 2答案:B 、B 、B 、A 、B 、B 、D 、B 、A 、D三、用系统命名法命名下列化合物,并指出1和3中各碳原子的级数1.2.(CH 3)3CCH 2CH 33.4. CH 3C (CH 3)35.(CH 3)2CHCH 2C(CH 3)36.7.8.答案:1. 3,3-二甲基己烷2. 2,2-二甲基丁烷3. 3-甲基己烷4. 2,2-二甲基丙烷(新戊烷)5. 2,2,4-三甲基戊烷6. 2,7,8-三甲基癸烷7. 3-甲基-4-乙基己烷8. 2,2,4,5-四甲基庚烷CH 3|CH 3CH 2CH 2-C -C 2H 5|CH 3CH 3|CH 3CH 2CH 2-CH -C 2H 5CH 3CH (CH 2)4-CH -CH -C 2H 5| | |CH 3 CH 3 CH 3四、写出下列化合物的结构式1. 2,3-二甲基己烷2. 2,4-二甲基-3-乙基戊烷3. 2,3,4-三甲基-3-乙基戊烷4. 2,2,5-三甲基-4-乙基己烷五、写出己烷(C6H14)构造异构体的结构简式,并用系统命名法命名。
《基础化学》有机化学复习题.doc

15.oIIO CH2-O-C-R!IIR2_C—O—C—H ©I II +CH2—O-P-OCH2CH2NH3o~17.《基础化学》有机化学复习题一、命名化合物或写出结构式1.CH3CHCH2CHCHCH3乩CH33.C 2H5 C2H57.OHCCXDH9.CH3CHCONH - CHCOOHNH2 CH2SH11.o o II II CH3CCH2COC2H513.HO2.CH3(CH O)2CHCH9CH0CH9CHCHCH OCH2CH34.CH3 CH2CH3CH.CHCH7C=CH9 。
,匕6.CH R CHCH'COOH•J■OH8.COOHH^N—J—HCH310.HOOCCOCH2COOH14.oIINH广C-NH,16.OH OH19.乙醍20.顺-2■丁烯21.异丙醇22.乙酰苯胺23.柠檬酸24.乙酸乙酯25.阿司匹林26.油酸27.卵磷脂28.葡萄糖29.半胱氨酸30.赖氨酸31.缩二脉32. ATP二、是非题(正确的打/,错误的打X)1.具有CJK通式的炷一定是烯炷。
()2.烷炷中的碳原子都是sp'杂化,烯炷中的碳原子都是s"杂化。
()3.环己烯分子中的碳原子都是s"杂化的。
()4.凡是双键碳原子都是sj杂化。
()5.乙烷有两种构象,一种是重叠式构象,一种是交叉式构象。
()6.碳原子的类型分为伯、仲、叔、季碳,氢原子的类型也分为伯、仲、叔、季氢。
()7.具有旋光性的物质一-定存在对映异构现象。
()8.一-对对映体的混合物能用蒸儒的办法分开。
()9.左旋2-丁醇和右旋2-丁醇的混合液可用蒸儒方法分开。
()10.只有一个手性碳原子的分子一定具有旋光性。
()11.一个分子结构中含有3个手性碳原子,则这个分子一•定是手性分子。
()12.手性分子具有旋光性,旋光度不等于妄,非手性分子无旋光性,旋光度为零。
内消旋酒石酸的旋光度为零,虽然内消旋酒石酸的分子有2个手性碳原子,但它一定是非手性分子。
有机化学基础复习题及答案

2022学年第二学期期末考试复习题一、单选题1、淀粉遇到碘显()色。
(1.3)A、红B、黄C、蓝D、绿正确答案:C2、乙醛与斐林试剂反应生成的沉淀是()。
(1.3)A、CuB、Cu 2OC、AgD、Fe正确答案:B3、能发生塞利凡诺夫反应的是()。
(1.3)A、核糖B、乳糖C、蔗糖D、麦芽糖正确答案:C4、皮肤遇到蛋白质变黄是因为发生了()反应。
(1.3)A、茚三酮反应B、莫力许反应C、二缩脲反应D、黄蛋白反应正确答案:D5、下列分子式表示的物质,具有同分异构体的是()。
(1.3)A、CH 2ClFB、C 3H 8C、CH 2Cl 2D、C 2H 4O 2正确答案:D6、天然气的主要成分是()。
A. 甲烷B. 乙烷C. 一氧化碳D. 乙烯正确答案:A7、2-甲基戊烷是饱和化合物,说明分子中所有的键都是()。
(1.3)A、单键B、双键C、三键D、以上三种键都有正确答案:A8、下列反应无论怎样调整反应物的用量都只能生成一种物质的是()。
(1.3)A、甲烷和氯气混合后光照发生反应B、乙烯与氯化氢的加成反应C、甲苯与等物质的量的Br 2发生反应D、乙炔和氯气的加成反应正确答案:B9、关于苯分子结构的叙述正确的是() 。
A. 含有三个碳碳双键和三个碳碳单键B. 分子中6个碳碳键完全相同C. 所有碳原子都在同一平面上,氢原子不处于同一平面上D. 每两个键之间的夹角都为60°正确答案:B10、下列溶液分别和溴水混合并振荡,静置后分为两层,水层和油层均为无色的是()。
(1.3)A、己烷B、CCl 4C、NaOH溶液D、己烯正确答案:D11、下列不是乙烯用途的是()。
(1.3)A、制塑料B、做灭火剂C、制有机溶剂D、做果实催熟剂正确答案:B12、碳氢化合物简称()。
(1.3)A、烃B、羟C、羰D、烷正确答案:A13、分子式相同而结构不同的化合物互称为()。
(1.3)A、结构式B、同分异构体C、同系物D、丙醛正确答案:B14、区别苯酚和苯甲醛时,可用的试剂是()。
大一基础化学复习题

基础化学复习题第一章溶液和胶体一、选择题1、将98%的市售浓硫酸500ml缓慢加入200g水中,所得到的硫酸溶液的质量百分浓度为(C)A 49%B 24.5%C 80.5%D 70%2、糖水的凝固点为(C)A 0℃B 高于0℃C 低于0℃D 难以判断3、下列0.1mol/L溶液的凝固点最高的是( B)A KClB CH3COOHC HClD K2SO44、在温度为375K时,沸水的压力应为(C )A 1000KPaB 10KPaC 高于100KPaD 低于100KPa5、在200g水中含有9g某非电解质溶液,其凝固点为-0.465℃,则溶液的摩尔质量为(D )A 135B 172.4C 90D 1806、某温度时,具有相同体积相同渗透压的甲醛和葡萄糖溶液中,甲醛和葡萄糖的质量比为(B )A 6:1B 1:6C 1:3D 3:17、胶体溶液中决定溶胶电性的物质时(B )A胶团B电位离子C反离子D胶粒8现有蔗糖,氯化钠,氯化钙三种溶液,它们的浓度均为0.1mol/L,则渗透压由高到低的顺序是(B )A CaCl2 < NaCl<C12H22O11B C12H22O11< NaCl < CaCl2C NaCl< C12H22O11<CaCl2D C12H22O11<CaCl2< NaCl9质量分数为5.8%NaCl溶液产生的渗透压接近:( C )(M(葡萄糖)=180g/mol,M(蔗糖)=342g/mol,M(NaCl)=58.5g/mol)A 5.8% 蔗糖溶液B 5.8% 葡萄糖C 2.0mol/L蔗糖溶液D 1.0mol/L葡萄糖溶液10在下列溶液组成标度的表示方法中,与温度有关的是( A )A 物质的量浓度B 质量分数C 物质的量分数D 质量摩尔浓度11非电解质稀溶液的蒸汽压下降,沸点升高和凝固点下降的数值取决于(B )A溶质的本性 B 溶液的质量摩尔浓度 C 溶液的体积 D 溶液的温度12 在等量的水中,分别加入质量相同的葡萄糖(M=180),蔗糖(M=342),KCl(M=74.5),CaCl2(M=111),其蒸汽压下降最少的是(A )A蔗糖溶液 B KCl溶液 C CaCl2 溶液D葡萄糖溶液13.某温度下,1mol/L糖水的饱和蒸汽压为P1,1mol/L的盐水的饱和蒸汽压为P2,则( B)A P2>P1B P2<P1C P2=P1D 无法判断二判断题1.由于溶液中溶质和溶剂的量是一定的,所以温度变化不影响溶液的浓度(×)2.难挥发非电解质稀溶液的依数性,不仅与溶液的浓度成正比,而且与溶质的种类有关(×)3.难挥发非电解质稀溶液在凝固时实际上是溶剂分子凝固(√)4.植物在较高温度下耐干旱是因为细胞液的蒸汽压下降所致(√)5. 渗透压力比较高的溶液,其渗透浓度也一定比较大(√)三填空题1 溶液的沸点升高是由于其蒸汽压 降低 的结果。
基础化学实验复习题

基础化学实验复习题1. 测水硬度时,采用的是()滴定法。
A. 酸碱B. 配位C. 沉淀D. 氧化还原2. pH=10时,以铬黑T作指示剂,用EDTA滴定水样从酒红色变为蓝色,消耗EDTA的是( )。
A. 钙离子B. 镁离子C. 钙离子和镁离子3. pH=12时,往水样中加少许钙指示剂,用EDTA滴定水样从酒红色变为蓝色,消耗EDTA的是( )。
A. 钙离子B. 镁离子C. 钙离子和镁离子4. 测水硬度时,若水样中含有微量Fe3+、Al3+,可用()进行掩蔽消除干扰?A. EDTAB. 三乙醇胺C. NaOHD. 草酸5. 根据()滴定方法测定亚铁盐中铁的含量?A. 酸碱B. 配位C. 沉淀D. 氧化还原6. 用滴管向试管中滴加液体时,可能的错误操作有哪些?A. 分不清是哪只滴瓶上的滴管,没有用专用滴管。
B. 滴管加液时伸入试管中。
C. 滴管加液时靠在试管壁。
D. 将装液的滴管斜放或倒放。
7. 旋光度值的大小与下列哪些因素有关?A. 物质本性B. 溶液浓度C. 温度D. 光源波长E. 旋光管长度8. 玻璃仪器洗涤时是否可用手沾洗涤剂洗涤,或用手指搓洗仪器?9. 可在酸性介质中使用氰化物吗?10. 测水硬度时,所用的滴定剂(标准溶液)是什么?11. 磷的工作曲线和标准曲线是一回事吗?12. 比色皿和比色管是一回事吗?13. 比色皿毛玻璃面要在光路上,对吗?14. 比色皿在装待测液之前只需用蒸馏水润洗,对吗?15. 分光光度法测磷实验中,先调T=100%后再调波长,对吗?16. 在测定物质折光率的过程中,阿贝折射仪能不能发生震动和撞击?17. 测旋光度时,其它条件相同时,旋光管越长,所测旋光度值越()。
18. 测旋光度时,其它条件相同时,所测溶液的浓度越大,旋光度值越()。
19. 比旋光度值与旋光管长度及溶液浓度是怎样的关系?20. 蒸馏完成后,能否直接拆除仪器?21. 蒸馏水与去离子水比较,哪个纯度高?22. 去离子水中含有什么杂质?23.绿色化学的核心是什么?24. 胶头滴管滴出的液体一般约多少滴为1mL?25. 酒精灯应怎样熄灭?26. 用蒸馏水洗玻璃仪器时应遵循的原则是什么?27. 常用吸量管读数应读至多少mL?28. 要精确配制0.100mol/L的NaCl溶液,称0.2g左右,天平要求精度至少是多少?29. 为什么盐酸的准确浓度要靠标定得到?30. 氯化亚铁溶液中要加入什么以免氧化?31. 氯化亚铁溶液中要加入盐酸的目的?32. 定容操作时,将溶液倒入容量瓶中要如何操作?33.有些带刻度的计量仪器快速干燥可使用什么方法?34.有些带刻度的计量仪器为什么不能直接加热干燥?35. 抽滤(减压过滤)与普通玻璃漏斗过滤相比,有什么优点?36. 润洗的目的是什么?37. 移液管上的“吹”字表示什么意思?38.粗食盐中的不溶性杂质如何去除?39.粗食盐中Mg2+、Ca2+如何去除?40.粗食盐中SO42-如何去除?41. 粗食盐提纯过程中加入的过量的氯化钡如何去除?42. 粗食盐提纯过程中加入的过量的碳酸钠如何去除?43. 酸碱标准溶液的浓度一般为多少?44. 用何物质标定HCl溶液的浓度?45. 用何物质标定NaOH 溶液的浓度?46. 测定水的总硬度时,溶液呈蓝色为终点,此蓝色化合物是什么?47. 测定水硬度中Ca2+含量时,水样调节pH值为10,加入铬黑T溶液呈紫红色,则该紫红色化合物是什么?48. 水硬度的大小是以水中()离子和()离子的总量来表示的。
《基础化学》复习题

《基础化学Ⅱ》复习题一、选择题1、下列有机基团叫做异丁基的是( )CH 3CH 2CH 2CH 2(CH 3)2CHCH 2CH 3CHCH 2CH 3(CH 3)3CA B C D2、将下列化合物按沸点降低的顺序排列正确的是( )①丁烷 ②己烷 ③3-甲基戊烷 ④2-甲基丁烷 ⑤2,3-二甲基丁烷 A ②>③>⑤>④>① B ③>②>⑤>④>① C ①>③>⑤>④>② D ②>③>④>⑤>① 3、下列碳正离子中,最稳定的是( )A CH 2=CH —CH 2+B CH 3—CH 2—CH 2+C CH 3—CH +—CH 3 D CH 2=CH —CH +—CH 34、结构CH 3CH==C (CH 3)2的烃中,下列哪种碳类型是不存在的( ) A 伯碳原子 B 仲碳原子 C 叔碳原子 D 季碳原子5、下列各组物质中,用Br 2/CCl 4试剂不能加以区别的是( )A 环丙烷和丙烷B 环已烯和环已烷C 1—丁炔和1—丁烯D 苯和苯乙烯6、分子式为C 4H 8化合物结构中,其中属于烯烃(包括顺反异构体)有( ) A 3种 B 4种 C 5种 D 6种7、按照“次序规则”基团大小的比较方法,下列四种基团中,其中最大的是( ) A —OH B —CH 2CH 3 C —COOH D —NO 2 8、正丁烷最稳定的构象是( )9、下列有机物结构中不存在顺反异构体的物质是( )CH 3CH=CH-CH 3CHBr=CH-CH 3CH 3H 3C (CH 3)2C=CHCH 3A B C D10、(反)1,2—二甲基环己烷最稳定的构象是( )11、在室温下往下列化合物中加AgNO 3醇溶液,即可生成沉淀的是( ) A 氯苯 B1-氯乙烷 C 苄氯 D1-氯丙烯 12、下列化合物在AgNO 3/C 2H 5OH 体系中最不易生成沉淀的是( )A CH 3ClB H 2C=CH-ClC CH 3CH 2ClD CH 2=CHCH 2-X13、下列关于卤代烃亲核取代反应历程特点描述,属于S N 2反应的特点是( ) A 反应速率与碱的的浓度无关 B 反应分两步进行 C 反应过程中生成活性中间体碳正离子 D 产物的构型完全转化 14、下列有机物发生硝化反应时,活性由强到弱顺序正确的是( ) NO 2ClOHCH 3④②③①A ①>②>③>④B ④>③>②>①C ③>④>②>①D ①>②>④>③ 15、下列物质名称叫做(R )-2-溴丁烷的是( )16、根据休克尔规则,下列化合物具有芳香性的的是( )17、将下列化合物的沸点最高的是 ( )A CH 3CH 2COOHB CH 3CH 2CH 2OHC CH 3CH 2CHOD CH 2CH 2CH 3 18、下列化合物碱性最强的是( )NH 2NH 2NH 2NH 2ABCDCH 3NO 219、下面化合物中,不能发生卤仿反应的是( )A CH 3CH(OH)CH 2CH 2CH 3B CH 3CH 2CH 2OHC CH 3COCH 2CH 2COCH 3D C 6H 5COCH 3 20、下列二元羧酸受热不放出CO 2的是 ( )A.COOH B. CH 2COOH C.CH 2COOH 2COOHD.(CH 2)5COOH COOH21、将RCH==CHCOOH 还原成RCH==CHCH 2OH 的还原剂是( )A LiAlH 4B Zn —Hg/HClC Zn+HClD Na+C 2H 5OH 22、可用来鉴别CH 3CHO 和CH 3COCH 3的试剂是( )A 2,4-二硝基苯肼B 托伦试剂C NaHSO 3D I 2+NaOH 23、氯化重氮苯与下列化合物发生偶联反应时,最难反应的是( )NH 2NH 2NHCH 3NH 2ABCDCH 3NO 224、下列化合物属于单糖的是 ( )A 蔗糖B 乳糖C 糖原D 核糖 25、亲电取代反应活性最大的是 ( )A 吡咯B 苯C 噻吩 D.呋喃 26、与NaHSO 3反应速率最小的是 ( )A Ph 2COB CH 3CHOC HCHOD PhCHO27、下列化合物酸性最弱的是( )COOH COOHCOOHCOOHO-CH 3CH 3NO 2ABCD28、下列物质中碱性最强的是A 对甲苯胺B 苄胺C 2,4-二硝基苯胺D 对硝基苯胺 29、下列化合物易发生水解反应的是 ( )CH 3ClClNO 2NO 2ClO 2Cl.. D.C.B A30、下列物质中水解反应速度最快的是( )A CH 3COClB CH 3CONHCH 3C (CH 3CO)2OD CH 3COOC 2H 531、反-1-甲基-3-叔丁基环己烷的优势构象为( )CH 3C(CH 3)3C(CH 3)3C(CH 3)3C(CH 3)3CH 3CH 3CH 3A B C D32、下列描述不.属于S N 1反应特征的是( ) A 中间体是正碳离子 B 叔卤代烷比仲卤代烷反应快 C 产物的绝对构型完全转化 D 有重排产物生成 33、下列几种还原剂,不能把酯还原成醇的是 ( )A Na +C 2H 5OHB NaBH 4C LiAlH 4 DH 2/Pt 34、下列化合物与HCN 发生亲核加成反应活性最小的是( )C-CH 2CH 3CH 3CH 2-C-CH 3CH 3CH 2CHOCH 3CHOOOAB C D35、下列碳负离子稳定性最高的是( )(CH 3)3C-CH 3CH 2CH 2-(CH 3)2CH--CH 3A B C D36、下列化合物没有旋光性的是( )A:B:C:D:COOHCOOHOH OH H HCOOH CH 2OHOH HOH H COOHCH 2OHOH H OH HCOOH COOHOH HOH H37、下列化合物碱性最弱的是( ).A CH 3CH 2NH 2B NH 3C CH 3CONH 2D PhNH 2 38、下列化合物酸性最强的是( )A CH 3COOHB CH 3CHClCOOHC Cl 3CCOOHD ClCH 2CH 2COOH 39、下列酸与醇在酸催化下成酯,反应速率最快的是( ) A (CH 3)3CCOOH 与 HOC 2H 5 B CH 3CH 2COOH 与HOC 2H 5 C (CH 3)2CHCOOH 与HOC 2H 5 D CH 3CH 2COOH 与HOCH 2CH 2CH 3 40、下列化合物中不具有芳香性的是( )A 吡咯B 噻吩C 吡啶D 四氢呋喃 41、下列化合物发生氨解反应时活性最小的是( )CH 3COOC 2H 5C 6H 5COCl(CH 3CO)2OCH 3CONHCH 3A CB D42、下列化合物中,沸点最低的是( )A 3,3-二甲基戊烷B 正庚烷C 2-甲基庚烷D 2-甲基己烷 43、下列化合物中,酸性最强的是( )A CH 3CH 2OHBC 6H 5OH C H 2CO 3D CH 3COOH 44、下列化合物中 ,碱性最弱的是( )A 甲胺B 三甲胺C 苯胺D 氨 45、下列化合物,发生硝化反应时活性最大的是( )SO 3HNH 2CH 3Cl ACBD46、下列化合物是手性分子的是( )A CB D HH COOH CH 3HCH 3Cl 3C 2H 5H COOC 2H 52CH 3HCH 2CH 3Cl CH 347、鉴别环丙烷、丙烯与丙炔三种物质,需要的试剂和顺序是( ) A Br 2的CCl 4溶液,KMnO 4溶液 B AgNO 3的氨溶液,KMnO 4溶液 C HgSO 4/H 2SO 4,KMnO 4溶液 D Br 2的CCl 4溶液,AgNO 3的氨溶液 48、下列化合物在浓碱作用下,不能发生Cannizzaro (歧化)反应的是 ( )OCHO CHO(CH 3)3CHO(CH 3)2CHCHOA BC D49、下列化合物与FeCl 3溶液不显色的是( )A 对苯醌B 对甲苯酚C 乙酰乙酸乙酯D 2,4-戊二酮 50、下列化合物在水中溶解度最大的是( )A 乙二醇B 环已酮C 正丁醇D 苯 51、下列烯烃中,存在顺反异构的是( ) CH 3CH 3CH 3CH=C(CH 3)2ClCH=CHCH 3A CB DCH 3CH 2=CHCH 2CH 352、下列化合物中,酸性最强的是( )A CH 2 BrCH 2CH 2COOHB CH 3CHBrCH 2COOHC CH 3CH 2CHBrCOOHD CH 3CH 2CH 2COOH 53、下列羧酸衍生物与甲醇反应时,活性最强的是( )A 乙酐B 乙酰氯C 乙酰胺D 乙酸乙酯 54、下列化合物发生亲核加成反应时,活性最强的是( )A 甲醛B 乙醛C 丙酮D 苯甲醛 55、可用来鉴别苯甲醛和丙醛的试剂是( )A I 2+NaOHB 托伦试剂C 2,4-二硝基苯肼D 斐林试剂 56、下列四种化合物,其中α-H 活性最差的是( )A 丙酮B 乙酸C 乙醛D 丙醛 57、下列物质,受热生成环戊酮的是 ( )A 丁二酸B 戊二酸C 己二酸D 庚二酸 58、下列四种氯代烃,S N 1和S N 2反应活性均最低的是( )A CH 3CH 2CH 2ClB CH 3CH=CHClC CH 2=CHCH 2ClD (CH 3)2CHCl59、下列化合物芳香性最强的是 ( )A 噻吩B 吡啶C 吡咯D 苯 60、下列化合物中,沸点高低顺序排列正确的是( )①乙醇 ②乙醛 ③乙酸 ④乙烷 A ①②③④ B ①③②④ C ③①②④ D ③②①④ 61、下列化合物中 ,碱性最强的是( )NH 2O 2NNHCH 3ClNH 2CH 2NH 2A C BD62、下列化合物中能发生碘仿反应的是( )A 乙醇B 正戊醛C 3-戊酮D 环戊酮 63、下列芳香酸,酸性最强的是( )ACBDCOOH CH 3COOHCOOHBrCOOHNO 264、将RCOCH 2COOH 还原成RCH 2CH 2COOH 的还原剂是( )A Zn+HClB Zn —Hg/HClC LiAlH 4D Na+C 2H 5OH 65、下列羰基化合物与羟氨(NH 2-OH )发生反应时,速度最快的是( )66、(R )—2—溴丁烷与(S )—2—溴丁烷相比较,哪种性质不同( ) A 密度 B 旋光度 C 化学性质 D 折光率 67、下列四个反应按历程分类,属于亲核取代历程的是( )A CH 3ONa + CH 3Cl CH 3-O-CH 3 + NaClB CH 3CH 2OH CH 2=CH 2 + H 2OC CH 2=CH 2 + Br 2 CH 2Br-CH 2BrD CH 3CH 3 + Cl 2 CH 3CH 2Cl + HCl68、实现下列转化,最好的线路是( )ClSO 3HNO 2O 2NA 先硝化,再磺化,最后卤代B 先磺化,再硝化,最后卤代C 先卤代,再磺化,最后硝化D 先卤代,再硝化,最后磺化 69、下列化合物能溶于稀NaOH 溶液的是( )A 苯甲醚B 氯乙烯C 对硝基苯酚D 溴苯70、分子式为C 9H 12的芳香烃,氧化是生成三元羧酸,硝化时只有一种一元硝基化合物,则该化合物的结构为( )CH 3H 3CCH 3CH 3CH 3CH 3CH 3C 2H 5CH 3CH 3CH 3A CBD71、下列化合物与NaHSO 3发生亲核加成反应时,活性最大的是( ) A CH 3CHO B CH 3COCH 3 C ClCH 2CHO D CH 3COCH 2CH 372、下列物质中能进行重氮化反应的是 ( )A 苯胺 BN-甲基苯胺 C N ,N-二甲基苯胺 D 三乙胺73、下列化合物酯化反应速度由大到小的顺序,排列正确的是 ( ) a. CH 3COCl b. CH 3COOC 2H 5 c. CH 3CONH 2 d.(CH 3CO )2OA a >b >c >dB a >d >b >cC a >b >d >cD b >c >d >a 74、下列费歇尔投影式中属于S 构型的是( )HCl CH 3C 2H 5ClH CH 3C 2H 5H 3CCl HC 2H 5H 3CC 2H 5Cl H A C B D75、下列化合物中最容易与浓硫酸发生磺化反应的是 ( ) A 溴苯 B 硝基苯 C 甲苯 D 邻二甲苯 76、下列化合物的构象中最稳定的是( )3233(H 3C)23(H 3C)2323AB C D77、下列物质中酸性最强的是 ( )A 对叔丁基苯酚B 对氯苯酚C 对甲基苯酚D 对硝基苯酚 78、下列糖中不与吐伦试剂反应的是 ( )A 葡萄糖B 果糖C 蔗糖D 麦芽糖79、下列酯类化合物在碱性条件下水解反应(亲核取代)速度最大的是( )NO 2O-CH 3Cl COOCH 3COOCH 3COOCH 3COOCH 3ACBD80、下列化合物亲电取代反应活性最强的是( )A 喃呋B 噻吩C 吡咯D 苯 81、下列化合物与卢卡斯试剂反应最快的是( )A 正丁醇B 正丙醇 C2-丁醇 D2-甲基-2-丁醇82、不对称烯烃和HBr 在过氧化物存在下发生加成反应,生成反马氏规则加成产物,其反应机理是( ) A 自由基加成历程 B 亲核加成历程 C 亲电加成历程 D 自由基取代历程 83、下列化合物亲电取代反应发生在邻、对位,且反应活性比苯小的是( ) A苯胺 B硝基苯 C苯酚 D氯苯 84、下列各组化合物中,哪个是对映异构体( )H OH CHO CH 3HO CH 3CHO HH Br COOH CH 3H CH 3COOHHO H COOH CH 2OH HO CH 2OHCOOHH H 2N C 6H 5CH 3H 3CNH 2C 6H 5A C B D 和和和和85、下列化合物中碱性最弱的是( ) A B CDN NH 2NH 3CH 3NH 286、下列物质中,属于还原性二糖的是( )A 葡萄糖B 麦芽糖C 蔗糖D 果糖 87、下列化合物既能发生碘仿反应,又能和NaHSO 3加成的是:( )A CH 3COCH 2CH 3B CH 3CHOHCH 2CH 3C CH 3COC 6H 5D CH 3CH 2CH 2CHO二、命名下列化合物(CH 3)2CHC(CH 3)23)2CHCH 3CH=C(CH 3)CCH 2CH 3H 3CCH 2CH=CH 2BrCH 312345CH 3CH 2-C-N(C 2H 5)2OCH=CH-CHO(CH 3CH 2CO)2O OCHO OHCOOHH 3CN 2+Cl -CH 3CH 2CHCH 2CH-CHCH 3CH 3CH 3CH 2CH 2CH 3OHCH 3SO 3H OOCOOHH-C-N-CH 3O3C CO OO (CH 3)2CH-C-ClCH 3COCH 2COOC 2H 5NC COOCOOH O-CH 3SO 3HOHH 3CH 3C H CH 22CH 3CH 3CH 2-C-NH-CH 3(CH 3)2CH-C-CH 3CH 3-C-CH 2CH 2COOH(CH 3CH 2CH 2CO)2OCONH 2N 2+Br -CH 3OOCH 3CH=CHCOOHC O C O O6789101112131415161718192021222324252627282930C-NHCH 3OO 2N3C 2H C-BrH 3C-O O O OO NCH 2COOH(CH 3)2CH-O-CH 2CH=CH 2313233343536C C(H 3C)2HCBr2CH 2CH 3CH 3OH NO 2O 2NNO 2CH 3CH 2COOCH 2CH=CH 2N N(CH 3)4N +OH-CH 3CH 2COOHO 2N N-CH 3CH 3N=NHOHO 3S373839404142434445三、写出下列化合物的结构式1、(R )-2-氯丁烷的Fischer 投影式2、(Z )-3-甲基-2-戊烯3、乙烷稳定构象(用纽曼投影式表示)4、甲基环己烷的优势构象5、苄基6、 顺-1-甲基-4-叔丁基环己烷的稳定构象7、5-甲基-2-溴-3-己酮8、β-萘胺9、 β—D —吡喃葡萄糖(哈沃斯式) 10、偶氮苯 11、正丁烷的稳定构象(纽曼投影式) 12、(R )2—羟基丙酸 13、邻苯二甲酸甲乙酯 14、 N ,N —二甲基苯胺 15、对—甲基苯磺酰氯 16、 (Z)-3,4-二甲基-3-己烯 17、氢氧化四甲铵 18、甲酸异丙酯 19、β-羟基丁酸 20、N-乙基苯胺 21、4-硝基-1-萘酚 22、对,对-二羟基偶氮苯 23、(S )-2-甲基-1,2-二氯丁烷 24、 对-甲基苯磺酰氯 25、(反)-2-丁烯 26、苯丙烯酸(肉桂酸) 27、四氢呋喃28、对甲基氯化重氮苯 29、对-硝基-对羟基偶氮苯 30、3-(间甲氧苯基)丁醛 31、(R )-2-羟基丁二酸的费歇尔投影式 32、乙酰乙酸 33、1,4-萘二胺 34、顺丁烯二酸酐 35、α-(D )-吡喃葡萄糖的哈沃斯式 36、对甲基苯磺酰胺 37、水杨酸四、用简便的化学方法鉴别下列各组化合物1、1—丁炔、1—丁烯、甲基环丙烷、丁烷2、叔丁基氯、氯苯、氯代环己烷3、丙醛、丙酮、丙醇、异丙醇4、苯胺、苄胺、N-甲基苄胺5、吡啶、3—甲基吡啶、苯胺6、苯酚、苯甲醛、苯甲酸、苯7、戊酸、戊醛、2—戊酮、环己酮8、苯酚、苯甲醚、苯甲醇、苄氯9、丙醛、丙酮、苄醇和乙醇 10、邻甲苯胺 、N-甲基苯胺 、苯甲酸和水杨酸 11、甲醛、乙醛、2-戊酮、3-戊酮 12、2,4-戊二酮、邻羟基苯甲酸、2-羟基丙酸、苯酚13、苯胺、N-乙基苯胺、N ,N-二乙基苯胺 14、苯甲醛、戊醛、2-戊酮、环己酮、环己醇 15、丙胺、丙醛、丙酸和丙酮 16、苯乙酮、苯甲醇、2-氯苯酚、苄氯 17、苯甲醛、苯乙酮、苯甲酸、苯甲醇、苯酚 18、3-戊酮、正戊醛、2-戊酮、3-戊醇、2-戊醇五、完成下列反应的机理1、请用合理的机理解释(1)HCN 加成反应的活性是: 甲醛>乙醛>丙酮(2)不同醇与氢卤酸反应的活性次序为:叔醇>仲醇>伯醇 2、为下列反应事实提出合理的机理CH 3HOH3H +C CCH 3CH 3CH 3CH 3H 3CH 3C CH 3CH 3CH 2=C-CH-CH 3++80%20%0.4%CH 3-C C-CH 3CH 3-C-CH=CH 2CH 2=CH 2 + Br 2NaCl+H 2OCH 2-CH 2OHCH 2-CH 2CH 2-CH 2++CH 32OH CH 3+ HBr CH 3-CH-CH 2Br CH 3+CH 3-C-CH 3CH 3H OH CH 3C 2H 5HBrH Br CH 32H 5Br H CH 3C 2H 5+(S)(S)(R)+ HBrCH 2CH 3BrCH 3-C-CH 2OHCH 3CH 3H+CH 2=C-CH 2CH 3CH 3CH 3+CH 3-C=CH-CH 3(1)(2)(3)(4)(5)(6)六、按指定性由大小或由难易排列(1)与HCN 发生亲核加成反应活性大小H-C-HCH 3-C-HCH 3-C-CH 3O OO C-HO COC O CH 3a b cdef(2)按酸性增强的顺序排列a CH 3CH 2CHBrCOOHb CH 3CHBrCH 2COOHc CH 3CH 2CH 2COOHd C 6H 5OHe CH 3CH 2CH 2CH 2OHf H 2CO 3g Br 3CCOOHh H 2O (3)按次序规则,基团优先次序A CH 3CH 2-B CH 2=CH-C CH ≡C-D (CH 3)3C-E HO-F CH 3O- (4)碳正离子稳定性大小CH 3-CH-CH 3CH 3CH 2CH 2CH 2=CH-CH 2++++A B C D CH 2=CH-CH-CH 3CH 3+E(6)酸性强弱次序COOH COOHCOOHCOOH3NO 2ABCDCOOHNO 22E(7)自由基稳定性稳定大小AB C D C CH 33CCH 3H 3C CH 3CH 33CH 3(8)硝化反应活性大小NO 2CH 3OCH 3ClABCDE(9)S N 1反应活性CH 2BrCH 3CH 3BrBr CHBrCH 3BrAB CDE(10)烯烃稳定性A CH 3-CH=CH 2B CH 3CH=CHCH 3C (CH 3)2C=CH-CH 3D (CH 3)2C=C(CH 3)2(11)与HBr 反应的活性大小CH 3CH 2CH 2OHCH 3CHCH 3(CH 3)3C-OH CH 3OHA B C D OH(12)沸点高低次序A CH 3CH 2OHB CH 3COOHC CH 3OCH 3D CH 3CHOE CH 3CH 2CH 3 (13)S N 2反应活性大小CH 2BrCH 3CH 3BrBr CHBrCH 3BrAB CDE(14)消去反应活性大小CH 2CH 2CH 2OHCH 2CHCH 3CHCH 2CH 3C-CH 3CH-CH 2OH OHOHCH 3OHCH 3AB CD E七、推导结构题1、化合物A ,C 16H 16,能吸收1mol 氢,使Br 2/CCl 4溶液褪色,与KMnO 4酸性溶液作用生成苯二甲酸,该酸只有一种单溴代产物,给出A 的结构。
基础化学复习题

基础化学复习题—、填空题1对于一个确定的化学反应,化学反应速率常数只与有关。
2在BaSO4饱和溶液中加入NaC1则BaSO4的溶解度会增大,这种现象称为3共价键具有_ 性和方向性。
4命名[Cu(NH2)]SO4 和[Ni(CO)4]5.稀溶液的依数性适用于__ 、非电解质的稀溶液。
6用于配置标准溶液的基准物质应具备_ 、、物质组成与化学式完全符合和摩尔质量大等四个条件。
7.根据催化剂的性质可分为多相催化、均相催化、_ 、和酶催化等五种。
8、配置标准溶液的基准物质应具备、、和物质组成与化学式完全符合等四个条件。
9配合物[Fe(en)3]Cl3,其配位体是__ ,中心高子的配位数是,命名: _10、对于一个确定的化学反应,化学反应速率常数只与___ _有关。
11、分子间作用力主要有H键和范德华力,其中,范德华力有三类_ 、、12、写出下列各基态原子或离子的电子排布:N ,Fe ,Cr13、按照电子云重叠方式分,共价键分为__ _键和_ _键。
14维持人体血液PH=7.40+0.5的缓冲溶液主要成分有 _、等.15、高分子材料是由一种或几种简单的低分子化合物(称为_ )经_ 或而成。
16,在化学反应中凡(一步)直接完成的反应称为反应。
17.在BaSO4饱和溶液中加入NaC1则BaSO4的溶解度会 .这种现象称为盐效应。
18共价键具有饱和性和 _性。
19.命名K4[Fe(CN)]和[PtC12(NH3)2] _20.稀溶液的依数性适用于难挥发的、的稀溶液。
21滴定分析法的主要方式有直接、返滴、 __和 _四种。
22、CC14分子中心原子发生杂化,空间构型是分子。
23、在化学反应中凡(一步)直按完成的反应称为 _反应。
24、K4[Fe(CN)]其配位体是 _,中心高子是 _,中心高子的配位数是_25、被称为现代三大合成材料的是、、26、写出下列各基态原子或高子的电子排布: :K ,Fe2+,Cl-27、标准氢电极的电极电势是28、难挥发非电解质稀溶液具有通性,即: 、、和渗透压。
基础化学复习题(xin)

一、判断题11. 100.142-⋅=L mol c SO H ,则12150.042-⋅=L mol c SO H 。
×2.难挥发非电解质稀溶液的依数性不仅与溶质种类有关,而且与溶液的浓度成正比。
×3.难挥发非电解质稀溶液的蒸气压实际上是溶液中溶剂的蒸气压。
√一、判断题:2√3.一个反应体系达到平衡时的特征是正逆反应速率相等。
√4.催化剂只能缩短反应达到平衡的时间而不能改变平衡状态。
×5.酸性水溶液中不含OH -,碱性水溶液中不含H +。
√6.在一定温度下,改变溶液的pH ,水的离子积不变。
√9.电离度和电离常数都能表示电离程度的强弱。
一、 判断题3×1.AgCl 在水中溶解度很小,所以它的离子浓度也很小,说明AgCl 是弱电解质。
√2.溶度积的大小决定于物质的本性和温度,与浓度无关。
×4.控制一定的条件,沉淀反应可以达到绝对完全。
√6.难溶电解质的溶度积和溶解度都是表示其溶解能力的大小。
一、判断题4×2.NH 4+中,氮原子的氧化数为-3;ClO -中,氯原子的氧化数为+7。
√4.在设计原电池时,E Ө值大的电对应是正极,而E Ө值小的电对应为负极。
√5.原电池中盐桥的作用是盐桥中的电解质中和两个半电池中过剩的电荷。
√6.标准电极电势表中的E Ө值是以标准氢电极作参比电极而测得的标准电极电势值。
√7.电极电势大的氧化态物质氧化能力强,其还原态物质还原能力弱。
一、 判断题52.中心离子的配位数等于配合物中配位体的数目。
(⨯)4.配合物转化为沉淀时,难溶电解质的溶解度愈小,则愈易转化。
(√)5.配离子在任何情况下都能转化为另一种配离子。
(⨯)6.酸度对配合物稳定性无影响。
(⨯)一、 判断题 6√1.可以通过增加平行试验的次数减小测定过程中的偶然误差。
×2.NaOH 标准溶液可用直接配制法配制。
×3.偶然误差是由一些偶然因素的变动引起的,无法减小。
基础化学复习题

基础化学复习题一、填空题:1.理想气体的微观模型是 、 。
2.稀溶液的依数性包括_________、_________、_________、_________。
3.2mol 理想气体,在300K 、400kPa 下的体积V = 。
4.在300K 、400kPa 下,摩尔分数y B =0.40的5molA 、B 理想气体混合物。
其中A 气体的分压力p A = kPa 。
5. 在101.325kPa 的大气压力下,将蔗糖溶于纯水中所形成的稀溶液缓慢地降温时,先析出纯冰。
相对于纯水而言将会出现:蒸气压 、沸点 、凝固点 。
6.应用热力学基本原理研究化学变化及其与之有关的物理变化中能量转化规律的科学,称为 。
7.热力学系统性质就是它一系列宏观性质的总和,而这些描述系统状态的性质又称为 ;在n 、V 、T 、x B 中,属于广延性质的是 ,属于强度性质的是 。
9.基元反应 2NO + Cl 2 → 2NOCl 是_______分子反应,是_______级反应,其速率方程为________________________。
10.在密闭容器中进行2NO + 2H 2 = N 2 +2H 2O 的反应,其速率方程V=K .c 2(NO) .c (H 2),则压力增大到原来的2倍,反应速率增大 _____ 倍。
11.可逆反应 2A(g) + B(g) 2C(g) ;Δr H m θ< 0 。
反应达到平衡时,容器体积不变,增加B 的分压,则C 的分压 __________,A 的分压 ___________ ;减小容器的体积,B 的分压 ___________, K θ___________。
12.可逆反应: I2+H 22HI 在713K 时K θ=51,若将上式改写为 :21I 2 +21H 2 HI 则其K θ为 ______。
13.质子理论认为,凡能 质子的物质是酸,凡能 质子的物质是碱。
14.已知吡啶的θb K =1.7×10—9,则其共轭酸的θa K = ,已知氨水的θb K =1.8×10—5,则其共轭酸的θa K = 。
化学基础知识习题

一、选择题:1. 对分子的叙述,正确的是A、分子是构成物质的惟一粒子B、由分子构成的物质,保持物质性质的是分子C、同种物质的每一个分子的化学性质都相同D、分子的大小会随着物质体积的增大而变大2 下列变化中,构成物质的分子本身发生变化的是A、糖溶于水B、衣箱中樟脑丸不久不见了C、工业上蒸发液态空气制氧气D、红磷燃烧3、分子和原子的主要区别是A. 分子是构成物质的微粒,原子不是构成物质的微粒B. 分子质量都大于原子质量C. 分子永恒运动,原子在分子中是不运动的D. 分子在化学反应中可分,原子在化学反应中不能再分4. 保持水的化学性质的粒子是A. 氢原子B. 氧分子C. 氢分子D. 水分子5. 下列物质中,肯定是由一种分子(或原子)构成的物质是A、水B、纯净物C、混合物D、糖水6. 2008年9月27日,我国航天员翟志刚进行了首次太空行走。
在此次活动中需要“人造空气”来供航天员呼吸,这种“人造空气”中含有体积分数为70%的氮气、20%以上的氧气、还有二氧化碳。
下列关于“人造空气”的说法中,不正确的是A. “人造空气”比空气中的氮气含量低B. “人造空气”中供给航天员呼吸的是氧气C. “人造空气”中的氧气和空气中的氧气化学性质相同D. 氮气对航天员呼吸没有任何作用,因此“人造空气”可以不需要氮气7.分子和原子的主要区别是()。
A.分子大、原子小B.分子的质量大,原子的质量小C.分子可直接构成物质,原子则要先构成分子后再构成物质D.在化学变化中分子可再分,原子则不能再分8.下列变化能证明分子在化学反应中可分的是()。
A.铁矿石磨成粉末B.碘受热升华C.加热水有水蒸气生成D.加热氧气汞生成汞和氧气9.下列说法中,正确的是()。
A.化学反应中,分子的种类改变,但分子的数目不变B.电解水产生氢气和氧气,所以水中含有氢气和氧气C.分子能构成物质,有些原子也能直接构成物质D.氧气是由两个氧原子构成的10.由分子参加的化学反应,反应前后一定发生变化的是()。
有机化学(基础化学)习题及参考答案

有机化学(基础化学)习题及参考答案一、单选题(共40题,每题1分,共40分)1、下列化合物命名正确的是A、顺—1,2—二氯乙烯B、反—1,2—二氯乙烯C、二氯乙烯D、1,2—二氯乙烯正确答案:B2、乙硫醇具有极难闻的气味,常作为无气味燃料气漏气的警报。
下列化合物中属于乙硫醇结构的是A、CH3CH2SHB、CH3CH2OHC、HOCH2CH2OHD、HSCH2CH2OH正确答案:A3、下列基团属于醛基的是A、-COOHB、#REF!C、-CHOD、-OH正确答案:C4、禁用工业酒精配制饮用酒,是因为工业酒精中含有A、乙醇B、甲醇C、丙三醇D、丙醇正确答案:B5、二氧化碳和氨气各1mol,在标准状况下相同的是A、质量B、体积C、所含原子数D、摩尔质量正确答案:B6、下列化合物能与FeCl3溶液发生颜色反应的是A、苄醇B、苯酚C、β-苯基乙醇D、苯乙烯正确答案:B7、下列醇的沸点有小到大的顺序为A、甲醇<乙醇<正丙醇<正丁醇B、甲醇<乙醇<正丁醇<正丙醇C、正丙醇< 甲醇< 乙醇< 正丁醇D、正丁醇 < 正丙醇< 乙醇< 甲醇正确答案:A8、下列试剂中不属于易制毒化学品的是A、浓盐酸B、高锰酸钾C、无水乙醇D、浓硫酸正确答案:C9、下列化合物中,哪一个能与三氯化铁溶液显色A、苯甲醇B、对-甲苯酚C、丙醇D、环己醇正确答案:B10、关于反应速率方程,下列说法正确的是A、纯固态或纯液态需写入反应速率方程B、反应速率方程适用于元反应C、温度不影响反应速率D、反应速率与各反应物浓度的乘积成正比正确答案:B11、化学烧伤中,酸的蚀伤,应用大量的水冲洗,然后用()冲洗,再用水冲洗A、0.3mol/LHAc溶液B、2%NaHCO3溶液C、0.3mol/LHCl溶液D、2%NaOH溶液正确答案:B12、醇的官能团是A、醛基B、羰基C、氨基D、羟基正确答案:D13、HOOC-COOH命名为A、乙酸B、醋酸C、二乙酸D、乙二酸正确答案:D14、制备格氏试剂所用的溶剂为A、无水乙醇B、无水乙醚C、无水乙醛D、丙酮正确答案:B15、羧酸与醇反应生成的物质称为A、酸酐B、醚C、酯D、酮正确答案:C16、关于pH的表述,下列说法不正确的是A、pH值大于7溶液显碱性B、pH值越小,溶液的酸度越低C、pH值小于7溶液显酸性D、pH=7溶液显中性正确答案:B17、有关实验室制乙烯的说法中,不正确的是A、温度计的水银球要插入到反应物的液面以下B、反应过程中溶液的颜色会逐渐变黑C、生成的乙烯中混有刺激性气味的气体D、加热时要注意使温度缓慢上升至170℃正确答案:D18、甲醛俗称为A、伯醛B、蚁醛C、酒精D、福尔马林正确答案:B19、下列反应中,不属于取代反应的是A、乙醇在一定条件下生成乙烯B、甲烷跟氯气反应生成一氯甲烷C、乙酸乙酯的水解D、苯的硝化反应正确答案:A20、正常人的血浆中每100ml含Na+ 0.326g,M(Na+)=23.0g/mol,试计算其物质的量浓度A、0.00142 mol﹒L-1B、1.42 mol﹒L-1C、0.0142 mol﹒L-1D、0.142 mol﹒L-1正确答案:D21、下列化合物相对分子量相近,其中沸点最高的是A、正丁醇B、正丁醛C、丁酮D、正戊烷正确答案:A22、关于反应速率的有效碰撞理论要点,下列说法不正确的是A、为了发生化学反应,反应物分子必须碰撞B、只有沿着特定方向碰撞才能发生反应C、只有具有足够高的能量的哪些分子的碰撞才能发生反应D、对活化分子不需要具备一定的能量正确答案:D23、关于标准平衡常数Kθ,下列说法不正确的是A、Kθ值越小反应物的平衡浓度或分压越大B、Kθ值越大产物的平衡浓度或分压越大C、Kθ与反应物的浓度或分压有关D、Kθ与温度有关正确答案:C24、戊炔的同分异构体有A、5种B、4种C、2种D、3种正确答案:D25、下列环烷烃中,最稳定的是A、环戊烷B、环丙烷C、环己烷D、环丁烷正确答案:C26、下列羧酸分子中,沸点最高的是A、正己酸B、正庚酸C、正辛酸D、正戊酸正确答案:C27、在常温下,水的pH为6.5,则其pOH值应为A、7.5B、6.5C、大于7.5D、小于6.5正确答案:A28、可用来鉴别1-丁炔和2-丁炔的溶液是A、溴水B、三氯化铁C、银氨溶液D、氢氧化钠正确答案:C29、有关芳香族化合物的特性叙述不正确的是A、苯环易发生取代反应B、含有苯环结构的烃称为芳香烃C、芳香族化合物的特性是指具有芳香味D、芳香性是指苯环不易发生加成反应和氧化反应正确答案:C30、能与AgNO3的氨水溶液生成白色沉淀的是A、丁烷B、2-丁炔C、1-丁烯D、1-丁炔正确答案:D31、下列哪类化合物在空气中极易被氧化A、戊烷B、苯胺C、氯苯D、苯甲酸正确答案:B32、下列化合物,遇FeCl3显紫色的是A、甘油B、苯酚C、苄醇D、对苯二酚正确答案:B33、下列哪种作用力不属于分子间作用力A、取向力B、色散力C、氢键力D、诱导力正确答案:C34、下列中毒急救方法错误的是A、呼吸系统急性中毒性,应使中毒者离开现场,使其呼吸新鲜空气或做抗休处理B、H2S中毒立即进行洗胃,使之呕吐C、误食了重金属盐溶液立即洗胃,使之呕吐D、皮肤、眼、鼻受毒物侵害时立即用大量自来水冲洗正确答案:B35、关于溶液的渗透方向,下列说法正确的是A、总是浓溶液一方往稀溶液一方渗透B、总是从纯溶剂一方往溶液一方,或者从稀溶液一方往浓溶液一方渗透C、总是从纯溶剂一方往溶液一方渗透D、总是稀溶液一方往浓溶液一方渗透正确答案:B36、在实验室中下列哪种物质最易引起火灾A、乙醇B、乙醚C、四氯化碳D、煤油正确答案:B37、对于可逆反应CO(g)+H2O(g)=CO2(g)+H2(g),如果要提高CO的转化率,可以采取的方法是A、增加CO的量B、增加H2O(g)的量C、同时增加CO和H2O(g)的量D、降低H2O(g)的量正确答案:B38、关于化学平衡,下列说法正确的是A、化学平衡是动态的平衡B、化学平衡时,正向反应的速率大于逆向反应的速率C、化学平衡是静态的平衡D、化学平衡时,逆向反应的速率大于正向反应的速率正确答案:A39、下列关于物质内部范德华力的说法中错误的是A、非极性分子间没有取向力B、极性分子间没有色散力C、极性越强的分子之间取向力越大D、氮气分子间只存在色散力正确答案:B40、关于影响化学平衡的因素,下列说法不正确的是A、压力对有气体参加的化学反应可能有影响B、温度对化学平衡有影响C、浓度对化学平衡有影响D、催化剂对化学平衡有影响正确答案:D二、多选题(共20题,每题1分,共20分)1、在实验中,遇到事故采取正确的措施是A、在实验中,衣服着火时,应就地躺下、奔跑或用湿衣服在身上抽打灭火B、若不慎吸入溴氯等有毒气体或刺激的气体,可吸入少量的酒精和乙醚的混合蒸汽来解毒C、割伤应立即用清水冲洗D、不小心把药品溅到皮肤或眼内,应立即用大量清水冲洗正确答案:BD2、根据两个碳碳双键的相对位置不同,二烯烃可分为A、累积二烯烃B、隔离二烯烃C、多烯烃D、共轭二烯烃正确答案:ABD3、下列叙述正确的是A、糯米中的淀粉一经发生水解反应,就酿造成酒B、棉花和人造丝的主要成分都是纤维素C、福尔马林是一种良好的杀菌剂,但不可用来消毒饮用水D、室内装饰材料中缓慢释放出的甲醛、甲苯等有机物会污染空气正确答案:BCD4、有机物分子中碳原子的类型有A、季碳B、叔碳C、仲碳D、伯碳正确答案:ABCD5、苯及其同系物容易发生取代反应,包括有A、硝化反应B、卤化反应C、烷基化与酰基化反应D、磺化反应正确答案:ABCD6、在实验室中,皮肤溅上浓碱液时,在用大量水冲洗后继而应A、用1:5000KMnO4溶液处理B、用5%硼酸处理C、用2%醋酸处理D、用5%小苏打溶液处理正确答案:BC7、下列属于真溶液的有A、食盐溶液B、蛋清C、豆浆D、蔗糖溶液正确答案:AD8、在采毒性气体时应注意的是A、分析完毕球胆随意放置。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
基础化学复习题单项选择题1. 理想气体绝热自由膨胀时,则 BA . 0U ∆>,0S ∆=B .0U ∆=,0S ∆>C . 0U ∆>,0S ∆>D .0U ∆=,0S ∆= 2.下面关于标准摩尔生成焓的描述中,不正确的是 CA.生成反应中的单质必须是稳定的相态单质B.稳态单质的标准摩尔生成焓被定为零C.生成反应的温度必须是298.15KD.生成反应中各物质所达到的压力必须是100KPa 3. 理想气体在可逆的绝热膨胀过程中是 BA . 内能增加B . 熵不变C . 熵增大D . 温度不变 4. 封闭系统中吉布斯函数G 与热力学U 的关系是 DA. G > UB. G < UC. G = UD. 无固定关系A. 零级反应 B . 一级反应 C . 二级反应 D . 三级反应 5.工作在100℃和25℃的两个大热源间的卡诺机其效率是 AA . 20%B . 25%C . 75%D . 100% 6.若将人作为一个体系,则该体系是 CA .孤立体系 B.封闭体系 C.敞开体系 D.半封闭系统7.在100℃,101.325 kPa 下,1 mol 水全部向真空气化为100℃,101.325 kPa 的水蒸气,则该过程为 BA . ΔG < 0,不可逆B . ΔG = 0,不可逆C . ΔG > 0,不可逆D . ΔG < 0,可逆 8. 液态水在100℃及101.325 kPa 下汽化,则该过程的 DA . ΔH = 0B . ΔS = 0C . ΔA = 0D . ΔG = 0 9.对于封闭体系的热力学 , 下列各组状态函数之间的关系正确的是 B A . A > U B . A < U C . G < U D . H< A 10. 下列各式表示偏摩尔量的是 A A . )(..(B A n P T B A n U≠⎪⎭⎫ ⎝⎛∂∂ B . )(..S (B A n P B A n H ≠⎪⎭⎫ ⎝⎛∂∂C . )(..(B A n V T B A n A≠⎪⎭⎫ ⎝⎛∂∂ D . )(..B (B A n P T B A n ≠⎪⎭⎫ ⎝⎛∂∂μ 11.刚性绝热箱内发生一化学反应,则反应体系是 AA.孤立体系B.敞开体系C.封闭体系D.绝热体系 12. 已知反应C (s )+O 2(g) →CO 2 (g)的ΔH ,下列说法中不正确的是 C A . ΔH 为CO 2(g)的生成热 B . ΔH 为C (S )的燃烧热 C . ΔH 与反应的ΔU 数值不等 D . ΔH 与反应的ΔU 数值相等 13.封闭系统中吉布斯函数A 与热力学U 的关系为 BA . A > UB . A < UC . A = UD . 无固定关系 14. 热力学第三定律可以表示是 BA . 在0K 时,任何晶体的熵等于零B . 在0K 时,纯物质完美晶体的熵等于零 C. 在0℃时,任何晶体的熵等于零 D . 在0℃时,完美晶体的熵等于零 15. 一级反应完成99.9%所需时间是完成50%所需时间是 CA . 2倍B . 5倍C . 10倍D . 20倍 16. 选出下列性质参数中属于容量性质的量是 CA . 温度TB . 浓度cC . 体积VD . 压力p17. 在恒温,恒压下,已知反应A →2B 和2A →C 的反应热分别为ΔH 1和ΔH 2,则反应C →4B 的反应热ΔH 3是 DA .2ΔH 1+ΔH 2B . ΔH 2-2ΔH 1C . ΔH 1+ΔH 2D . 2ΔH 1-ΔH 2 18. 不挥发的溶质溶于溶剂中形成溶液之后将会引起C A . 熔点升高 B . 沸点降低 C . 蒸汽压降低 D . 总是放出热量 19.下列是化学势的是 C A . )(..(B A n P T B A n U≠⎪⎭⎫ ⎝⎛∂∂ B . )(..(B A n P T B A n H ≠⎪⎭⎫ ⎝⎛∂∂ C . )(..(B A n V T B A n A≠⎪⎭⎫ ⎝⎛∂∂ D . )(..(B A n V T B A n G ≠⎪⎭⎫ ⎝⎛∂∂ 20. 在 - 10 °C, 101.325kPa 下,水的化学式势μ(水)与冰的化学势μ(冰)的大小关系应为 CA . μ(水)=μ(冰)B . μ(水) >μ(冰)C . μ(水) <μ(冰)D . 无法确定21. 理想气体从状态p 1V 1T 自由膨胀至p 2V 2T 。
此过程的ΔA 与ΔG 的关系是 C A . ΔA>ΔG B . ΔA<ΔG C . ΔA=ΔG D . 不能确定22. 某反应的反应物消耗一半的时间正好是反应物消耗1/4的时间的2倍,则该反应的级数是BA . 0.5级反应B . 0级反应C .1级反应D .2级反应23. 在25℃下反应CO(g)+2H 2(g)=CH 3OH(g)的16.90-⋅-=∆mol KJ H m r θ ,为提高反应的平衡产率,应采取的措施是 DA .升高温度和压力B . 降低温度和压力C .升高温度,降低压力D . 降低温度,升高压力24. 某二级反应,反应物消耗 1/3 需时间 10 min ,若再消耗 1/3 还需时间为 C A . 10 min B . 20 min C . 30 min D . 40 min 25. 对于某反应,若反应物反应掉其43所需时间恰是它反应掉21所需时间的2倍,则该反应的级数是 B填空题1.按标准摩尔生成焓与标准摩尔燃烧焓的定义,在C (石墨)、CO (g )和CO 2(g)之间, CO 2(g)的标准摩尔生成焓正好等于 C(石墨) 的标准摩尔燃烧焓。
2. 亨利常数随温度的升高而 增大 (增大、减小或不变)。
3. 反应2A → B ,则-dc A /dt 和dc B /dt 之间的关系是 -dc A /dt=2dc B /dt 。
4. 在绝热、体积恒定的容器中发生一化学反应,使容器中温度、压力都增加,则该过程的∆U = 0。
5. 设理想气体反应)(3)()(g C g B g A =+达化学平衡,在等温下维持系统总压不变,向系统中加入惰性气体,平衡__向右__移动。
6. 反应A → 2B ,则-dc A /dt 和dc B /dt 之间的关系是 -2dc A /dt=dc B / 。
7. A 、B 两理想液态混合物在T-x 图上出现最高点,则该混合物对拉乌尔定律产生 负偏差 偏差。
8. 在恒温恒压下,一切相变化必然朝着化学势 降低 的方向自动的进行。
9. 化学反应热会随反应温度改变而改变的原因是 .r 0p m C ∆≠ 。
10. 实际气体绝热自由膨胀,则该过程的∆S _>__ 0。
11. 糖可以顺利溶解在水中,说明固体糖的化学势较糖水中的糖的化学势__高__。
12. 卡诺热机在T 1=600K 的高温热源和T 2=300K 的热源间工作,其热机效率η= 50% 。
13. 按标准摩尔生成焓与标准摩尔燃烧焓的定义,在C (石墨)、CO (g )和CO 2(g)之间, C (石墨)的标准摩尔燃烧焓正好等于 CO 2(g) 的标准摩尔生成焓。
14.在总压不变时,加入惰性气体的结果与___降低_____压强的结果是相同的。
15. 在绝热、体积恒定的容器中发生一化学反应,使容器中温度、压力都增加,则该过程的ΔU_____=_____0。
名词解释 1. 偏摩尔量均相系统中,系统的广度性质Z 在恒温恒压除B 组分其它组分保持不变的条件下,Z 函数随B 组分的变化量为B 组分的偏摩尔量:..(,)Z Z m B T p n c c B n ≠⎛⎫∂= ⎪∂⎝⎭ 2. 分解压化合物的分解压是指该化合物(纯液体或纯固体)分解出气体的分解反应在指定温度下达到平衡时,生成物气体的总压力。
3. 化学势均相系统中,系统广度性质吉布斯函数在恒温恒压除B 组分其它组分保持不变的条件下,吉布斯函数随B 组分的变化量为B 组分的化学势(即偏摩尔吉布斯函数):B ..(,)G m B T p n c c B G n μ≠⎛⎫∂==⎪∂⎝⎭ 4. 卡诺循环热机以理想气体为工作介质,工作过程由两个等温可逆过程和两个绝热可逆过程组成,它的循环工作过程成为卡诺循环。
5. 吉布斯自由能吉布斯自由能G 是系统状态函数的组合(即G=H -TS ),也是系统的状态函数。
封闭系统在恒温恒压非体积功为零的条件下,吉布斯自由能的变化量可以作为判据,判断过程的方向。
6. 化学反应速率化学反应速率的定义:设化学反应0B BB ν=∑ ,反应速率1BB dn d dt dtξν= 定容反应时反应速率1BB dc v dtν=7. 卡诺定理在两个不同温度热源之间工作的所有热机,以可逆热机效率最大。
热机效率η只与两个热源的温度有关:121T T T η-=(T 1是高温热源的温度,T 2是低温热源的温度) 8. 亥姆霍兹自由能亥姆霍兹自由能A 是系统状态函数的组合(即A=U —TS ),也是系统的状态函数。
封闭系统在恒温恒容非体积功为零的条件下,亥姆霍兹自由能的变化量可以作为判据,判断过程的方向。
9. 稀溶液依数性稀溶液(溶质是非挥发性的)的某些性质只依赖溶液中溶质分子的数量,而与溶质分子本性无关的性质。
如溶剂蒸汽压降低,凝固点降低,沸点升高和渗透压。
10. 标准平衡常数标准平衡常数K Θ的定义式:exp[/()]m K rG RT θθ=-∆标准平衡常数在理想气体化学反应中是一定温度下平衡时的压力商, 即()/Beq BBK pp νθθ=∏计算题1、4mol N 2 在27℃,1.0MPa 等压升温至127℃,求此过程的W 、Q 、△U 和△H 。
该气体可视为理想气体,其 C p.m =28.00 J.mol -1.K -1。
解:.21Q ()11.20p m H nC T T kJ =∆=-= .21U ()()7.874p m n C R T T kJ ∆=--=3.326W U Q kJ =∆-=-计算该反应CO 2(g)+4H 2(g)→CH 4(g)+2H 2O(g)在298.15K 时的G m r θ∆和K θ。
解:反应CO 2(g)+4H 2(g)→CH 4(g)+2H 2O(g)的θm rH ∆(298.15K )=θνm f BB H ∆∑(B,298.15K)=θm f H ∆( CH 4,g) +2θm f H ∆( H 2O,g)- θm f H ∆( CO 2,g) -4θm f H ∆( H 2,g)=-164.88kJ/mol()∑=∆Bm B m K S K rS )15.298(15.298θθν=θm S ( CH 4,g) +2θm S ( H 2O,g)- θm S ( CO 2,g) -4θm S ( H 2,g) =-172.51J/mol.K所以1113.45.r m m m G rH T rS kJ mol θθθ-∆=∆-∆=-ln 45.77mrG K RTθθ∆=-= K Θ=7.53x 10193、已知水在100℃,101.325kPa 下的摩尔蒸发焓140.668Vap m H kJ mol -∆=⋅,试计算1kg 水在100℃,101.325kPa 条件下,蒸发为水蒸气的Q 、W 、△U 及△H 。
