氯化锌标准溶液配制记录
化学溶液配置

细骨料有机物含量:
标准溶液:取2g鞣酸溶解于98ml浓度为10%乙醇溶液中(无水乙醇10ml加蒸馏水90ml)即得所需的鞣酸溶液。
然后取该溶液25ml注入975ml浓度为3%的氢氧化钠溶液中(3g氢氧化钠溶于97ml蒸馏水中),加塞后剧烈摇动,静置24h即得标准溶液。
细骨料轻物质含量:
重液:向1000ml的量杯中加水至600ml刻度处,再加入1500g 氯化锌;用玻璃棒搅拌使氯化锌充分溶解;待冷却至室温后,将部分溶液倒250ml量筒中测其相对密度;若相对密度小于2000kg/m3,则倒回1000ml量杯中,再加入氯化锌,待全部溶解并冷却至室温后测其密度,直至溶液密度达到2000kg/m3为止。
粉煤灰游离氧化钙:
1、氢氧化钠无水乙醇溶液:将0.2g氢氧化钠溶解于50ml无水乙醇中,切勿长时间高温加热,可用平头玻璃棒边加热边压碎。
2、乙二醇-乙醇溶液:将1000ml乙二醇与500ml无水乙醇混合,再加入0.06g酚酞,摇匀,用氢氧化钠溶解于中和呈微红色,储存于干燥器的玻璃瓶中备用。
3、苯甲酸无水乙醇标准溶液:称12.2g苯甲酸溶于少量无水乙醇中,然后转移到1000ml容量瓶中,用无水乙醇冲至刻度,摇匀备用。
2020版《中国药典》氯化锌滴定液配制与标定操作规程

一、目的:的配制、标定操作内容、方法与要求。
二、范围:适用于氯化锌滴定液(0.1mol/L)的配制和标定操作。
三、职责:化验室对实施本规程负责。
四、内容:1、仪器与用具:电子天平(万分之一)、烧杯(1000ml )、量筒、锥形瓶(250m1)、滴定管(50.0m1、A 级)、刻度吸管(10ml 、A 级)、恒湿器。
2、试药与试液:2.1氯化锌(AR )。
2.2盐酸(1+2000):精密量取盐酸(AR )1ml 加2000ml 水,混匀即得。
2.3硝酸镁饱和溶液:取新沸的冷水100ml 加一定量的硝酸镁(AR ),至硝酸镁不再溶解即得。
2.4乙二胺四乙酸二钠(基准试剂)。
2.5氨-氯化铵缓冲溶液:(ph ≈10)(见EK/SOP-QC8002缓冲液配制操作规程)。
2.6铬黑T 指示液(5g/l ):称取0.5g 铬黑T 和2g 盐酸羟胺,溶于乙醇(95%),用乙醇(95%)稀释至100ml 。
临用前制备。
3、配制:称取14g 氯化锌,溶于1000ml 盐酸溶液(1+2000)中,摇匀。
4、标定与复标:4.1操作方法:称取1.4g 经硝酸镁饱和溶液恒湿器中放置7d 后的工作基准试剂乙二胺四乙酸二钠,溶于100ml 热水中,加10ml 氨-氯化铵缓冲溶液(ph ≈10),用配制好的氯化锌溶液滴定,近终点时加5滴铬黑T 指示液(5g/l ),继续滴定至溶液由蓝色变为紫红色。
同时做空白试验。
4.2计算:氯化锌标准滴定溶液的浓度[C(ZnCl 2)],按下式计算:MV V m ZnCl C ⨯-⨯=)(1000)(212 式中: m 为乙二胺四乙酸二钠的质量,g ;V 1 为氯化锌溶液的体积,ml ;V 2为空白试验消耗氯化锌溶液的体积,ml ;M 为乙二胺四乙酸二钠的摩尔质量,g/mol ,[M(EDTA)=372.24]。
5、贮藏:本液置中性小口玻璃塞瓶中密闭贮存。
五、参考文献:GB/T 601—2016六、相关文件:EK/SOP-QC8002缓冲液配制操作规程EK/SOP-QC8003指示剂与指示液配制操作规程七、相关记录:N/A八、变更记录及原因:。
标准溶液配制记录

标准溶液配制记录一、前言。
标准溶液是化学分析中常用的一种溶液,它的浓度和成分都是经过严格计算和实验确定的。
正确、精确地配制标准溶液对化学分析结果的准确性和可靠性至关重要。
本文档旨在记录标准溶液的配制过程,以供参考和借鉴。
二、配制目的。
本次配制的标准溶液是XXX试剂,其主要用途是作为XXX分析的定量标准品。
通过配制标准溶液,可以确保在化学分析中得到准确的定量结果。
三、实验步骤。
1. 确定溶液浓度。
首先,根据实验需要和已知的化学反应式,计算出所需的标准溶液的浓度。
在确定浓度的过程中,需要考虑到实验的精确度和所需的最终结果。
2. 准备试剂和仪器。
在配制标准溶液之前,需要准备好所需的试剂和仪器。
试剂的纯度和仪器的准确度对标准溶液的配制至关重要。
3. 溶解试剂。
按照计算得出的配方,将所需的试剂溶解在适量的溶剂中。
在溶解过程中,需要充分搅拌并保持恒温,以确保试剂充分溶解。
4. 调整溶液体积。
根据需要,将溶解好的试剂溶液调整至所需的体积。
在调整体积时,需要使用准确的容量瓶或移液器,并注意避免气泡的产生。
5. 校正浓度。
配制好标准溶液后,需要进行浓度的校正。
校正的方法可以是比色法、滴定法或仪器分析法,根据实际情况选择合适的方法进行校正。
6. 记录实验数据。
在配制标准溶液的整个过程中,需要准确记录每一步的操作和实验数据。
这些数据将作为实验结果的依据,并在实验后的数据分析中起到重要的作用。
四、实验结果。
经过以上步骤,我们成功配制出了XXX浓度为XXX的标准溶液。
经过校正后,其浓度符合实验要求,可以用于后续的化学分析实验。
五、结论。
本次标准溶液配制实验成功完成,得到了符合要求的标准溶液。
在实验过程中,我们严格按照操作规程进行操作,严格控制试剂的纯度和仪器的准确度,最终取得了满意的实验结果。
六、致谢。
在实验过程中,得到了实验室老师和同事们的帮助和支持,在此表示衷心的感谢。
七、参考文献。
[1] XXX. 化学分析实验指导. 化学出版社, 20XX.[2] XXX. 分析化学. 化学工业出版社, 20XX.以上就是本次标准溶液配制的记录,希望对您有所帮助。
重液化学药品配制记录.

重液____化学药品配制记录
1. 选用的化学药品原料名称及数量:
氯化锌:
2. 配制主要过程:
在 1000ml 的量筒中加水至 600ml 刻度处,再加入 1500g 氯 化锌,用玻璃棒使氯化锌全部溶解,待冷却至室温后,将部 分溶液倒入 250ml 量筒测其相对密度 量杯中,再加入氯化锌 ,则倒回 1000ml
,待全部溶解并冷却至室温后测
3
其密度,直至溶液密度达到 2000kg/m 。
3. 配制结果与配制得到的数量:
配制结果合格,制得重液ml
配制人:
配制日期:存放期限: Nhomakorabea
氯化锌废液中锌含量的测定(EDTA容量法)

氯化锌废液中锌含量的测定(EDTA容量法)本法基于在PH5.5-6醋酸-醋酸钠缓冲液中,以二甲酚橙作指示剂,用EDTA标准溶液滴定锌。
1.试剂配制1.1醋酸-醋酸钠缓冲液(PH5.5-6)称取醋酸钠200g,用水溶解加冰醋酸10ml,用水稀释至1升1.2二甲酚橙指示剂0.5%称取0.5g试剂用少量水湿润,加氨水4-5滴,用水稀释至100ml 1.3EDTA标准溶液(约0.015M)称取乙二胺四乙酸二钠5.5g与烧杯中,加水加热溶解,冷却后移入1L容量瓶中,用水稀释至刻度,摇匀1.4锌标液称取金属锌(99.9%)1.0000g与烧杯中,加盐酸(2+1)20ml,加热溶解后,加入1L容量瓶中,用水稀释至刻度标定:吸取锌标准溶液20ml于250ml锥形瓶中,加甲基橙指示剂1滴,用氨水(1+1)中和,使溶液由橙色到刚显黄色,以少量水冲洗瓶壁,加醋酸-醋酸钠缓冲液20ml,加二甲酚橙指示剂1滴,用EDTA 标准溶液滴定,由酒红色至亮黄色为终点,同时做空白。
T=W/(V-V0)式中:T-EDTA对锌的滴定度(g/mL)W-吸取新标准溶液含锌量(g)V-滴定所耗EDTA标准溶液体积V0-空白所耗EDTA标准溶液体积分析步骤称取试2.5000-3.0000g于300ml烧杯中,加水20ml,低温加热5-6分钟,稍冷却后加氯酸钾1-2g,继续加热蒸发至溶液体积5-6ml,取下加水使溶液体积保持在100ml左右,加入30%硫酸铵溶液10ml,加热煮沸,用氨水中和并过量15ml,加入20%氟化钾溶液10ml,加热煮沸1分钟,取下稍冷,加氨水5ml,乙醇10ml,冷却后加入250ml 容量瓶中,用水稀释至刻度,摇匀。
干过滤,弃出最初流下的15-20ml滤液,吸取100或50ml溶液于250ml锥形瓶中,加热煮沸以除去大部分氨(但勿使氢氧化锌白色沉淀出现),冷却,加0.1%甲基橙指示剂1滴,用盐酸(1+1)中和至甲基橙变红色,然后加氨水(1+1)1滴,使其变黄,加入醋酸-醋酸钠缓冲液10ml,加10%硫代硫酸钠溶液2-3ml,摇匀,加0.5%二甲酚橙指示剂2-3滴,用EDTA标准溶液滴定至溶液由酒红色变亮黄色为终点。
标准溶液配制记录

标准溶液配制记录一、实验目的。
本实验旨在掌握标准溶液的配制方法,提高实验操作技能,确保实验结果的准确性和可靠性。
二、实验原理。
标准溶液是已知浓度的溶液,用于测定未知物质的浓度或进行定量分析。
标准溶液的配制需要根据溶质的摩尔质量、所需溶液的体积和浓度来计算所需的溶质量或溶液体积。
三、实验步骤。
1. 根据实验要求和所需标准溶液的浓度,计算所需溶质的质量或所需溶液的体积;2. 取适量溶剂加入容器中,如水或其他溶剂;3. 将溶质逐渐加入溶剂中,并充分搅拌,直至溶解完全;4. 用稀释瓶加入适量溶剂,将溶液稀释至最终体积;5. 用PH试纸或PH计检测溶液的PH值,确保溶液的酸碱度符合实验要求;6. 用天平称取少量标准溶液,装入干燥洁净的烧杯中,放入干燥器中干燥至恒定质量;7. 记录标准溶液的配制过程和实验数据,如溶质的质量、溶剂的体积、稀释倍数等。
四、实验注意事项。
1. 实验操作过程中要注意安全,避免溶液溅出或溶剂挥发造成伤害;2. 溶质的加入要逐渐,充分搅拌,确保溶解完全;3. 稀释时要准确控制溶剂的加入量,避免误差;4. 配制标准溶液的容器和工具要干燥洁净,避免杂质污染;5. 实验数据要准确记录,确保实验结果的可靠性。
五、实验结果分析。
根据实验数据计算标准溶液的浓度,与理论值进行比较,分析实验误差的原因,提出改进意见,确保实验结果的准确性和可靠性。
六、实验总结。
通过本次实验,掌握了标准溶液的配制方法,提高了实验操作技能,加深了对标准溶液配制原理的理解,为今后的实验工作打下了良好的基础。
七、参考文献。
[1] 《化学实验指导书》。
[2] 《标准溶液的配制与使用》。
以上是本次标准溶液配制记录,如有不当之处,欢迎批评指正。
氯化锌标准溶液配制记录
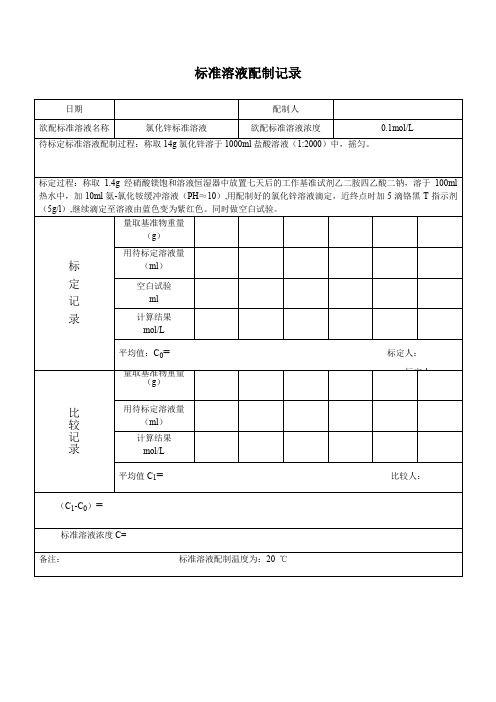
配制人
欲配标准溶液名称
氯化锌标准溶液
欲配标准溶液浓度
0.1mol/L
待标定标准溶液配制过程:称取14g氯化锌溶于1ห้องสมุดไป่ตู้00ml盐酸溶液(1:2000)中,摇匀。
标定过程:称取1.4g经硝酸镁饱和溶液恒湿器中放置七天后的工作基准试剂乙二胺四乙酸二钠,溶于100ml热水中,加10ml氨-氯化铵缓冲溶液(PH≈10),用配制好的氯化锌溶液滴定,近终点时加5滴铬黑T指示剂(5g/l),继续滴定至溶液由蓝色变为紫红色。同时做空白试验。
标定记录
量取基准物重量(g)
用待标定溶液量(ml)
空白试验
ml
计算结果
mol/L
平均值:C0=标定人:
标定人:
比较记录
量取基准物重量
(g)
用待标定溶液量(ml)
计算结果
mol/L
平均值C1=比较人:
(C1-C0)=
标准溶液浓度C=
备注:标准溶液配制温度为:20℃
标准溶液配制记录
氯化锌废液中锌含量的测定(EDTA容量

1.试剂配制1.1醋酸-醋酸钠缓冲液(PH5.5-6)称取醋酸钠200g,用水溶解加冰醋酸10ml,用水稀释至1升1.2二甲酚橙指示剂0.5%称取0.5g试剂用少量水湿润,加氨水4-5滴,用水稀释至100ml1.3EDTA标准溶液(约0.015M)称取乙二胺四乙酸二钠5.5g与烧杯中,加水加热溶解,冷却后移入1L容量瓶中,用水稀释至刻度,摇匀1.4锌标液称取金属锌(99.9%)1.0000g与烧杯中,加盐酸(2+1)20ml,加热溶解后,加入1L容量瓶中,用水稀释至刻度标定:吸取锌标准溶液20ml于250ml锥形瓶中,加甲基橙指示剂1滴,用氨水(1+1)中和,使溶液由橙色到刚显黄色,以少量水冲洗瓶壁,加醋酸-醋酸钠缓冲液20ml,加二甲酚橙指示剂1滴,用EDTA标准溶液滴定,由酒红色至亮黄色为终点,同时做空白。
T=W/(V-V0)式中:T-EDTA对锌的滴定度(g/mL)W-吸取新标准溶液含锌量(g)V-滴定所耗EDTA标准溶液体积V0-空白所耗EDTA标准溶液体积分析步骤称取试2.5000-3.0000g于300ml烧杯中,加水20ml,低温加热5-6分钟,稍冷却后加氯酸钾1-2g,继续加热蒸发至溶液体积5-6ml,取下加水使溶液体积保持在100ml左右,加入30%硫酸铵溶液10ml,加热煮沸,用氨水中和并过量15ml,加入20%氟化钾溶液10ml,加热煮沸1分钟,取下稍冷,加氨水5ml,乙醇10ml,冷却后加入250ml容量瓶中,用水稀释至刻度,摇匀。
干过滤,弃出最初流下的15-20ml滤液,吸取100或50ml溶液于250ml锥形瓶中,加热煮沸以除去大部分氨(但勿使氢氧化锌白色沉淀出现),冷却,加0.1%甲基橙指示剂1滴,用盐酸(1+1)中和至甲基橙变红色,然后加氨水(1+1)1滴,使其变黄,加入醋酸-醋酸钠缓冲液10ml,加10%硫代硫酸钠溶液2-3ml,摇匀,加0.5%二甲酚橙指示剂2-3滴,用EDTA标准溶液滴定至溶液由酒红色变亮黄色为终点。
标准溶液配制记录

标准溶液配制记录一、实验目的。
本实验旨在记录标准溶液的配制过程,以及相关实验数据,为后续实验提供准确可靠的参考依据。
二、实验原理。
标准溶液是已知浓度的溶液,通常用于分析化学中的定量分析。
在配制标准溶液时,需要根据溶质的化学性质和实验要求,选择适当的溶剂和溶质的质量,按照一定的比例配制而成。
三、实验步骤。
1. 准备实验所需的试剂和仪器设备,包括天平、容量瓶、移液管等。
2. 根据实验要求,选择合适的溶剂和溶质,并按照所需的浓度比例进行称量。
3. 将称量好的溶质溶解于适量的溶剂中,摇匀使其充分溶解。
4. 用容量瓶将溶液定容至刻度线,摇匀混合。
5. 将配制好的标准溶液转移至干净的密封瓶中,标注好溶液的名称、浓度、配制日期等信息。
四、实验数据记录。
| 溶质 | 质量/g | 溶剂 | 体积/mL | 浓度/mol/L | 配制日期 |。
|------|--------|------|---------|------------|----------|。
| NaCl | 5.85 | 水 | 1000 | 0.1 |2022/03/15|。
| KCl | 7.20 | 水 | 1000 | 0.2 |2022/03/16|。
五、实验结果分析。
通过本次实验的记录数据,我们成功配制出了两种浓度不同的标准溶液,分别为0.1mol/L的NaCl溶液和0.2mol/L的KCl溶液。
在实验过程中,我们严格按照配制步骤进行操作,确保了实验结果的准确性和可靠性。
六、实验总结。
本次实验记录了标准溶液的配制过程和相关数据,为后续实验提供了重要的参考依据。
在实验中,我们需要严格按照配制步骤进行操作,确保实验结果的准确性和可靠性。
同时,对于配制好的标准溶液,我们也需要做好标注和保存工作,以便后续实验的使用。
七、实验注意事项。
1. 在配制标准溶液时,需要准确称量溶质和溶剂,严格按照比例进行配制。
2. 配制好的标准溶液需要标注清楚名称、浓度、配制日期等信息,并保存在干净的密封瓶中。
化验室标准溶液配制标定原始记录

复 标 误 差(±%)
标准样
验证
记录
项目
LOSS
SiO2
Al2O3
Fe2O3
CaO
MgO
SO3
测试值
标准值
误差
结论:
验证日期: 验证人:
溶
液
使
用
浓
度
通
知
通知日期:通知人:
溶液名称配制浓度目标值moll配制体积使用期限配制时室内温度配制日期配制人基准试剂名称及配制成的浓度与总体积ml项目序号基准试剂数消耗标准溶液体积ml溶液浓度moll平均溶液浓度moll标定人及日期项目losssiocaomgoso测试值标准值误差结论
化验室标准溶液配制标定原始记录(总1页)
化验室标准溶液配制标定原始记录
配制
记录
溶液名称
配制浓度目
标值(mol/L)
配制体积
(L)
溶质数()
使用期限
配制时室内
温度(℃)
配制日期
配制人
标
定
记
录
基准试剂名称及
配制成的浓度与
总体积(ml)
项目
序号
基准试剂数
()
消耗标准溶
液体积(ml)
溶液浓度
(mol/L)
平均溶液
浓度(mol/L)标定人来自及日期其它
浓
度
形
式
换
算
1
2
3
复
标
记
录
1
2
EDTA标准溶液的配制和标定(氧化锌标液)[资料]
![EDTA标准溶液的配制和标定(氧化锌标液)[资料]](https://img.taocdn.com/s3/m/97d869fce109581b6bd97f19227916888486b9e4.png)
EDTA标准溶液的配制和标定(氧化锌标液)一、目的:1、学习EDTA标准溶液的配制和标定方法。
2、学习配位滴定法的原理,了解该滴定法的特点。
二、原理:标定EDTA的基准物质有Zn、CaCO3、Bi、Cu、MgSO4·7H2O等。
(M EDTA=372.2g/mol)指示剂:EBT 1%(称取1克EBT加入三乙醇胺75ml、无水乙醇25ml)。
在PH=10.0的缓冲溶液中:Zn2++In3- ZnIn-(酒红色)ZnIn-+HY3-←→ ZnY2-+HIn2-(蓝色)三、用ZnO作为基准物质时所需试剂:EDTA ZnO(烘干) NH3—NH4Cl缓冲液(PH=10.0) 1+1氨水 EB T 1% 6mol·L-1的HCl (M ZnO=81.37)四、实验步骤:1、配制0.02mol·L-1EDTA500mL在台称上称取EDTA二钠盐3.5—3.8g溶入150—200mL温水中,稀释至500mL,装入试剂瓶中、待标定。
2、配制ZnO标准溶液250mL在分析天平上准确称取ZnO 0.3—0.4g于小烧杯中。
滴加6mol·L-1的HCl至全部溶解(约5~10mL),转移至250mL的容量瓶中。
3、准确取三份各25.00mL+25mL蒸馏水入三角锥瓶中。
慢慢滴加NH3水,至刚好出现白色浑浊,加入10mL缓冲液,滴加3—4滴铬黑T。
4、0.02mol·L-1EDTA滴定,由酒红色→蓝色为终点。
五、数据及计算:公式:C EDTA=(m ZnO /M ZnO×25/250)/ (V EDTA/1000)样品号 1 2 3 ZnO的质量(g)ZnO基准溶液用量(mL)EDTA终读数(mL)EDTA初读数(mL)V EDTA (mL)C EDTA(mol·L-1)C EDTA 平均值(mol·L-1)绝对偏差相对平均偏差(%)二、思考题:1、配位滴定中为什么需要采用缓冲溶液?2、为什么在ZnO中加入HCl?3、通过计算说明为什么称取0.32—0.4g ZnO?怎么标定0.05mol/L的EDTA标准溶液基准物是氧化锌指示剂是铬黑T固体?准确称取1.0g已于900℃温度下灼烧至恒重的基准氧化锌,溶于盛有10mL 1+1盐酸中,溶解较慢时可适当加热使其溶解,冷却后转移至250mL容量瓶中并稀释至刻度,摇匀。
氯化锌标准溶液配制记录

量取基准物重量(g)
用待标定溶液量(ml)
空白试验
ml
计算结果
mol/L
平均值:C0=标定人:
标定人:
比较记(ml)
计算结果
mol/L
平均值C1=比较人:
(C1-C0)=
标准溶液浓度C=
备注: 标准溶液配制温度为:20 ℃
标准溶液配制记录
氯化锌标准溶液配制记录
日期
配制人
欲配标准溶液名称
氯化锌标准溶液
欲配标准溶液浓度
L
待标定标准溶液配制过程:称取14g氯化锌溶于1000ml盐酸溶液(1:2000)中,摇匀。
标定过程:称取1.4g经硝酸镁饱和溶液恒湿器中放置七天后的工作基准试剂乙二胺四乙酸二钠,溶于100ml热水中,加10ml氨-氯化铵缓冲溶液(PH≈10),用配制好的氯化锌溶液滴定,近终点时加5滴铬黑T指示剂(5g/l),继续滴定至溶液由蓝色变为紫红色。同时做空白试验。
氯化锌标准溶液配制记录
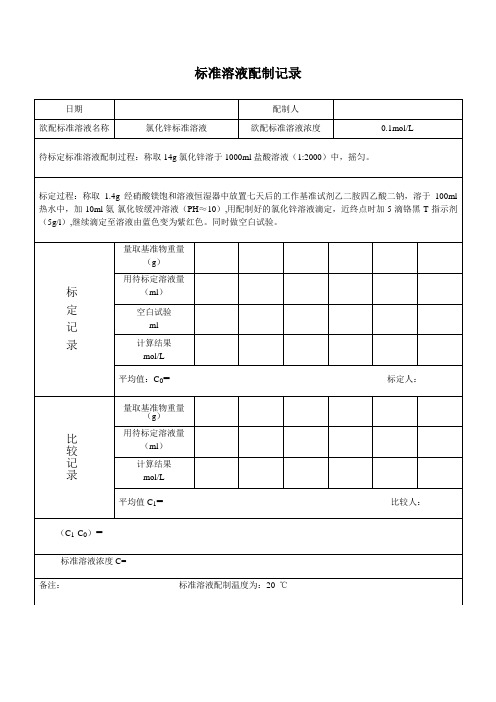
配制人
欲配标准溶液名称
氯化锌标准溶液
欲配标准溶液浓度
0.1mol/L
待标定标准溶液配制过程:称取14g氯化锌溶于1000ml盐酸溶液(1:2000)中,摇匀。
标定过程:称取1.4g经硝酸镁饱和溶液恒湿器中放置七天后的工作基准试剂乙二胺四乙酸二钠,溶于100ml热水中,加10ml氨-氯化铵缓冲溶液(PH≈10),用配制好的氯化锌溶液滴定,近终点时加5滴铬黑T指示剂(5g/l),继续滴定至溶液由蓝色变为紫红色。同时做空白试验。
标定记录
量取基准物重量(g)
用待标定溶液量(ml)
空白试验
ml
计算结果
mol/L
平均值:C0=标定人:
标定人:
比较记录
量取基准物重量
(g)
用待标定溶液量(ml)
计算结果
mol/L
平均值C1=比较人:
(C1-C0)=
标准溶液浓度Biblioteka =备注:标准溶液配制温度为:20℃
标准溶液配制记录
标准溶液‘配制’教(学)案‘标定’原始记录文本
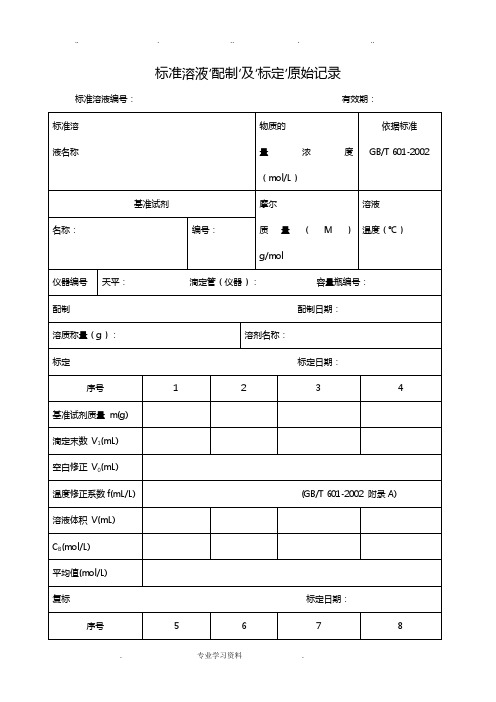
标准溶液‘配制’及‘标定’原始记录标准溶液编号:有效期:标准溶液名称物质的量浓度(mol/L)依据标准GB/T 601-2002基准试剂摩尔质量(M)g/mol溶液温度(℃)名称:编号:仪器编号天平:滴定管(仪器):容量瓶编号:配制配制日期:溶质称量(g):溶剂名称:标定标定日期:序号 1 2 3 4 基准试剂质量m(g)滴定末数V1(mL)空白修正V0(mL)温度修正系数f(mL/L) (GB/T 601-2002 附录A) 溶液体积V(mL)C B(mol/L)平均值(mol/L)复标标定日期:序号 5 6 7 8基准试剂质量m(g)滴定末数V1(mL)空白修正V0(mL)温度修正系数f(mL/L) (GB/T 601-2002 附录A) 溶液体积V(mL)C B(mol/L)平均值(mol/L)计算式:V=(V1-V0)×(1+f/1000)C B=1000m/(M×V)说明:每次滴定必须从“0”开始备注:配制人:标定:复标:审核:标准物质配制(标定)记录编号:CHEC/QBG-075名称:、配制方法:使用天平型号编号室温℃、湿度%RH 配制:取定溶mL 标定:取份:⑴⑵⑶⑷用溶液滴定,滴定消耗量(mL)V1= 、V2= 、V3= 、V4= 、V0= 。
标准溶液浓度计算公式:C=计算结果():C1= C2= C3= C4= C = 相对偏差(%):S1= S2= S3= S4=备注:。
配制人:复核人:配制日期:年月日有效期年月日标准溶液配制记录编号:CHEC/QBG-147标准溶液名称:规格:配制方法:仪器名称:溯源标准:温度:℃、湿度:%RH标准溶液拟配浓度:配制或稀释过程:配制日期:年月日有效期:年月日配制人:复核人:0.1mol/L盐酸标准滴定溶液的标定编号:JL/LJ-001-01一、标定方法:GB/T5009.1-2003二、使用仪器:AEL-200电子天平(仪器编号:JYB001)马弗炉(仪器编号:JYC009)三、操作1、量取9ml盐酸,加适量水并稀释至1000ml。
最新试液配制记录

试液(试药)配制记录3 试液(试药)配制记录6 试液(试药)配制记录10 试液(试药)配制记录11121314 试液(试药)配制记录15所用试药、溶剂硫酸、水1617 试液(试药)配制记录181920 试液(试药)配制记录212223 试液(试药)配制记录242526 试液(试药)配制记录272829 试液(试药)配制记录30试液(试药)配制记录3334 35 试液(试药)配制记录36323738 试液(试药)配制记录39试液(试药)配制记录4243 44 试液(试药)配制记录4540414647 试液(试药)配制记录4950 试液(试药)配制记录515253 试液(试药)配制记录5556试液(试药)配制记录575859 试液(试药)配制记录606162 试液(试药)配制记录636465 试液(试药)配制记录666768 试液(试药)配制记录697071 试液(试药)配制记录7276试液(试药)配制记录73 74 75备 注 77787980 试液(试药)配制记录818283 试液(试药)配制记录848586 试液(试药)配制记录8889 试液(试药)配制记录9192 试液(试药)配制记录939495 试液(试药)配制记录969798 试液(试药)配制记录99100101试液(试药)配制记录102_____________________________________________103104 试液(试药)配制记录105106107 试液(试药)配制记录109 110 111 试液(试药)配制记录112113114试液(试药)配制记录115 _____________________________________________116117 试液(试药)配制记录118119120121122 试液(试药)配制记录所用试药、溶剂硫酸铜结晶、水、酒石酸钾钠结晶、氢氧化钠124125 126 试液(试药)配制记录127128 试液(试药)配制记录129130 试液(试药)配制记录132133 试液(试药)配制记录134135136试液(试药)配制记录137 _____________________________________________139140141142试液(试药)配制记录143 ____________________________________________144145试液(试药)配制记录146_____________________________________________147148 试液(试药)配制记录149备注153154 试液(试药)配制记录155所用试药、溶剂氢氧化®I、水156157 试液(试药)配制记录158159160试液(试药)配制记录161 _____________________________________________试液(试药)配制记录165 166 试液(试药)配制记录167163168169 试液(试药)配制记录174 试液(试药)配制记录171 172 173备 注175177178 试液(试药)配制记录180181 试液(试药)配制记录182183184 试液(试药)配制记录185试液(试药)配制记录所用试药、溶剂 钥酸铉、水186 187188189190191 试液(试药)配制记录193194 试液(试药)配制记录195196 197 198 试液(试药)配制记录199。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
日期
配制人
欲配标准溶液名称
氯化锌标准溶液
欲配标准溶液浓度
L
待标定标准溶液配制过程:称取14g氯化锌溶于1000ml盐酸溶液(1:2000)中,摇匀。
标定过程:称取1.4g经硝酸镁饱和溶液恒湿器中放置七天后的工作基准试剂乙二胺四乙酸二钠,溶于100ml热水中,加10ml氨-氯化铵缓冲溶液(PH≈10),用配制好的氯化锌溶液滴定,近终点时加5滴铬黑T指示剂(5g/l),继续滴定至溶液由蓝色变为紫红色。同时做空白试验。
标定记录
量取基准物重量(g)
用待标定溶液量(ml)
空白试验
ml
计算结果moຫໍສະໝຸດ /L平均值:C0=标定人:
标定人:
比较记录
量取基准物重量
(g)
用待标定溶液量(ml)
计算结果
mol/L
平均值C1=比较人:
(C1-C0)=
标准溶液浓度C=
备注:标准溶液配制温度为:20℃
标准溶液配制记录
