乳酸脱氢酶(LDH)活性检测试剂盒说明书 微量法
乳酸脱氢酶(LDH)活性检测试剂盒说明书 微量法

乳酸脱氢酶(LDH)活性检测试剂盒说明书微量法注意:正式测定前务必取2-3个预期差异较大的样本做预测定。
货号:BC0685规格:100T/48S产品内容:提取液:液体60mL×1瓶,4℃保存;试剂一:液体7mL×1瓶,4℃保存;试剂二:粉剂×1支,-20℃保存,用时加入1.3mL双蒸水充分溶解备用,配好后可分装成小管-20℃保存,可保存两周,禁止反复冻融;试剂三:液体7mL×1瓶,4℃保存;试剂四:液体25mL×1瓶,4℃保存;丙酮酸钠标准液:液体1mL×1支,4℃保存,2μmol/ml。
产品简介:LDH(EC 1.1.1.27)广泛存在于动物、植物、微生物和培养细胞中,是糖酵解途径的末端酶,催化丙酮酸与乳酸之间的可逆反应,伴随着NAD+/NADH之间互变。
LDH催化NAD+氧化乳酸生成丙酮酸,丙酮酸进一步与2,4-二硝基苯肼作用生成丙酮酸二硝基苯腙,在碱性溶液中显棕红色,颜色深浅与丙酮酸浓度成正比。
试验中所需的仪器和试剂:可见分光光度计/酶标仪、恒温水浴锅、台式离心机、可调式移液器、微量玻璃比色皿/96孔板、研钵、冰和蒸馏水。
操作步骤:一、粗酶液提取:1.细菌、细胞或组织样品的制备:细菌或培养细胞:先收集细菌或细胞到离心管内,离心后弃上清;按照细菌或细胞数量(104个):提取液体积(mL)为500~1000:1的比例(建议500万细菌或细胞加入1mL提取液),超声波破碎细菌或细胞(冰浴,功率20%或200W,超声3s,间隔10s,重复30次);8000g4℃离心10min,取上清,置冰上待测。
组织:按照组织质量(g):提取液体积(mL)为1:5~10的比例(建议称取约0.1g组织,加入1mL提取液),进行冰浴匀浆。
8000g4℃离心10min,取上清,置冰上待测。
2.血清(浆)样品:直接检测。
3.丙酮酸钠标准液:取100μL标准液,倍比稀释至1、0.5、0.25、0.125、0μmol/mL,用2、1、0.5、0.25、0.125、0μmol/mL做标准曲线。
乳酸检测试剂盒(乳酸脱氢酶微板法)
乳酸检测试剂盒(乳酸脱氢酶微板法)简介:乳酸(Lactic acid ,LD)又称2-羟基丙酸是一种化合物,是一种含有羟基的羧酸,分子式是C 3H 6O 3,参与生物化学很多反应过程。
乳酸检测试剂盒(乳酸脱氢酶微板法)其检测原理是在NAD 存在条件下,乳酸脱氢酶(LDH)催化乳酸生成丙酮酸,同时生成NADH 。
在碱性条件下显色剂与丙酮酸生成复合物,并使平衡偏向乳酸氧化为丙酮酸的方向,驱动反应完成,生成的NADH 与乳酸为等量摩尔。
通过分光光度比色法(酶标仪)测定340nm 处吸光度,据此通过比色分析就可以计算出LD 水平。
该试剂盒可用于检测细胞或组织的裂解液或匀浆液、血浆、血清等样品中内源性的乳酸含量。
该试剂盒仅用于科研领域,不宜用于临床诊断或其他用途。
组成:操作步骤(仅供参考):1、 准备样品:①_x0001_ 血浆、血清、尿液及其他体液样品:血浆、血清按照常规方法制备后可以直接用于本试剂盒的测定,尿液通常也可以直接用于测定,-20℃冻存。
②_x0001_ 细胞或组织样品:取恰当细胞或组织裂解液,如果有必要需进行适当匀浆,低速离心取上清,-20℃冻存,用于LD 的检测。
③_x0001_高浓度样品:如果样品中含有较高浓度的LD ,可以使用原有的裂解液或PBS 等进行稀释,如鸡血清、血浆可稀释5~10倍后检测。
2、 配制标准品工作液:取乳酸标准(20mmol/L) 0.1ml 溶解于0.3ml 乳酸标准稀释液,使浓度达到5mmol/L ,即为标准品工作液-乳酸标准(5mmol/L)。
4℃避光保存2个月有效。
编号 名称TC0731 110T Storage试剂(A): 乳酸标准(20mmol/L) 1ml -20℃ 避光 试剂(B): 乳酸标准稀释液 1ml RT 试剂(C): LD 显色液C1: LD Assay buffer 5ml 4℃ 避光 C2: NAD 2支 -20℃ 避光 C3: LDH solution15μl-20℃ 避光试剂(D): LD 终止液 30mlRT 使用说明书1份3、LD检测:按照下表设置空白孔、对照孔、标准孔、测定孔,溶液应按照顺序依次加入,并注意避免产生气泡。
Cytotoxicity+LDH+Assay+Kit中文说明书20141202

0 cells/well 150 μl培养基
9)在每个孔中加入 50 l Stop Solution。 10)用酶标仪测定 490 nm 的吸光度。
图 3 预实验的 96 孔板细胞梯度配置图
三、细胞毒性实验 1)吸取 100 l 用培养基稀释过的细胞悬液至 V 型 96 孔板(悬浮细胞)或 U 型 96 孔板(贴壁细胞)中。 2)加入 100 l 含有药物的培养基。 3)在 37 ℃ CO2 培养箱中培养合适的时间。 4)在高对照的孔中加入 20 l Lysis Buffer 后,在 37 ℃ CO2 培养箱中培养 30 min。 5)培养后将 96 孔板离心 2 min(250×g)。 6)从每个孔中吸取上清液 100 l 至新的 96 孔板中。
150 μl 转移
C
150 μl
150 μl
96 孔板中。
D
*为了避免吸出细胞,请小心吸取上清液。
E
高对照
低对照
8)在每个孔中加入 100 l Working Solution 后, F
在避光、室温的条件下培养 30 min。
G
*请根据显色程度调整培养时间。
H
0 cells/well 150 μl培养基
2)向 96 孔板中每孔加入 100 l 培养基。
3)如图 2 所示,向 96 孔板中 A 行加入 100 l 细胞悬液后,用多通道移液器按 1/2 比例用培养基稀释成
一个系列细胞梯度。按照表 1 设定高对照和低对照各 3 个孔,另外准备 3 个不含细胞的 Blank 孔。
4)在高对照孔中加入 10 l Lysis Buffer。
注意事项: 本试剂盒使用玻璃容器及铝盖,建议使用时戴手套。 测定前的注意事项: 因为每种细胞的 LDH 量不同,为了得到最好的显色效果,推荐做预实验确定最佳细胞量。
乳酸脱氢酶(LDH)检测试剂盒(LD-P微板法)
1.5ml
RT
1份
操作步骤(仅供参考):
1、 准备样品: ①血浆、血清样品:血浆、血清按照常规方法制备,可以直接用于本试剂盒的测定, 室温保存 3 天,用于 LDH 的检测。 ②细胞或组织样品:取恰当细胞或组织进行匀浆,低速离心取上清,室温保存 3 天, 用于 LDH 的检测。 ③长期保存样品:如果提取后的样品无法及时检测,需要放置时间较长,按下列方法 操 作:按待测样品(如血清):LDH 保护工作液=9:1 的比例混合,4℃避光保存。 ④(选做)样品准备完毕后可以用 BCA 蛋白浓度测定试剂盒测定蛋白浓度,以便于后续 计算单位蛋白重量组织或细胞内的 LDH 含量。
组成:
名称 试剂(A): NADH 试剂(B): LD-P Assay buffer 试剂(C): 丙酮酸溶液 试剂(D): 丙酮酸稀释液 试剂(F): LDH 保护稀释液 使用说明书
编号
TE01 55 100T
Storage
2 支 -20℃ 避光
100ml
RT
2×1.5ml 4℃ 避光
30ml
RT
北京雷根生物技术有限公司
乳酸脱氢酶(LDH)检测试剂盒(LD-P 微板法)
简介:
乳酸脱氢酶(lactate dehydrogenase,LDH 或 LD)属于氧化还原酶,能够催化氢氧原 子或电子从一中底物转移到另一种底物上乳酸脱氢酶是糖酵解和糖异生的一个极其重要的 酶,含有锌离子,广泛分布于人和动物组织、植物和微生物中,能可逆的催化乳酸(L)和丙 酮酸(P)之间的氧化还原反应。乳酸脱氢酶(LDH)检测试剂盒(LD-P 微板法)是利用乳酸脱氢 酶催化上述逆反应,即丙酮酸+NADH+H+→乳酸+NAD+。该 LD-P 法的优点是:1、操作 比二硝基苯肼法简单;2、重复性好;3、准确性比二硝基苯肼法好;4、适用于自动分析仪 该试剂盒仅用于科研领域,丌宜用于临床诊断或其他用途。
乳酸脱氢酶(LDH)检测试剂盒(LD-P比色法)
北京雷根生物技术有限公司
加入物(ml) 待测样品(血清、血浆、体液等) LDH 检测工作液
北京雷根生物技术有限公司
乳酸脱氢酶(LDH)检测试剂盒(LD-P 比色法)
简介:
乳酸脱氢酶(lactate dehydrogenase,LDH 或 LD)属于氧化还原酶,能够催化氢氧原 子或电子从一中底物转移到另一种底物上乳酸脱氢酶是糖酵解和糖异生的一个极其重要的 酶,含有锌离子,广泛分布于人和动物组织、植物和微生物中,能可逆的催化乳酸(L)和丙 酮酸(P)之间的氧化还原反应。乳酸脱氢酶(LDH)检测试剂盒(LD-P 比色法)是利用乳酸脱氢 酶催化上述逆反应,即丙酮酸+NADH+H+→乳酸+NAD+。在上述反应过程中,丙酮酸还 原成乳酸,同时 NADH 氧化成 NAD+,引起 340nm 处吸光度的下降。该 LD-P 法的优点 是:1、操作比二硝基苯肼比色法简单;2、重复性好;3、准确性比二硝基苯肼法好;4、
2、 处理后的样品应及时检测,否则 LD4 和 LD5 易失效。 3、 血清或肝素抗凝血浆检测效果较好,草酸类、EDTA 抗凝剂对 LDH 活性有抑制作用。
北京雷根生物技术有限公司
4、 避免使用溶血样本。 5、 为了您的安全和健康,请穿实验服幵戴一次性手套操作。
自动分析仪计算公式:LDH(U/L)=ΔA/min×(106/6220)×(296/10)=ΔA/min×4758.8 注意:如果待测样品加入 LDH 保护工作液,其结果应除以 0.9。
小鼠乳酸脱氢酶(LDH)ELISA试剂盒操作说明操作说明

小鼠乳酸脱氢酶(LDH)ELISA试剂盒操作说明操作说明小鼠乳酸脱氢酶(LDH)ELISA试剂盒操作说明小鼠乳酸脱氢酶(LDH)ELISA试剂盒实验原理小鼠乳酸脱氢酶(LDH)ELISA试剂盒采用双抗体一步夹心法酶联免疫吸附试验(ELISA)。
往预先包被小鼠乳酸脱氢酶(LDH)捕获抗体的包被微孔中,依次加入标本、标准品、HRP标记的检测抗体,经过温育并彻di洗涤。
用底物TMB显色,TMB在过氧化物酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。
颜色的深浅和样品中的小鼠乳酸脱氢酶(LDH)呈正相关。
用酶标仪在450nm 波长下测定吸光度(OD 值),计算样品浓度。
样本处理及要求1. 血清:将收集于血清分离管的全血标本在室温放置2小时或4℃过夜,然后1000×g离心20 分钟,取上清即可,或将上清置于-20℃或-80℃保存,但应避免反复冻融。
2. 血浆:用EDTA或肝素作为抗凝剂采集标本,并将标本在采集后的30分钟内于2-8℃1000×g离心15分钟,取上清即可检测,或将上清置于-20℃或-80℃保存,但应避免反复冻融。
3. 组织匀浆:用预冷的PBS (0.01M, pH=7.4)冲洗组织,去除残留血液(匀浆中裂解的红细胞会影响测量结果),称重后将组织剪碎。
将剪碎的组织与对应体积的PBS(一般按1:9的重量体积比,比如1g的组织样品对应9mL的PBS,具体体积可根据实验需要适当调整,并做好记录。
推荐在PBS中加入蛋白酶抑制剂)加入玻璃匀浆器中,于冰上充分研磨。
为了进一步裂解组织细胞,可以对匀浆液进行超声破碎,或反复冻融。
最后将匀浆液于5000×g离心5~10分钟,取上清检测。
4. 细胞培养物上清或其它生物标本:请1000×g离心20分钟,取上清即可检测,或将上清置于-20℃或-80℃保存,但应避免反复冻融。
注:标本溶血会影响最后检测结果,因此溶血标本不宜进行此项检测。
乳酸脱氢酶(LDH)法操作说明

乳酸脱氢酶(LDH)法操作说明乳酸脱氢酶(LDH)法操作说明操作简介:乳酸脱氢酶(LDH)法是一种常用的生物化学分析方法。
本文将详细介绍使用乳酸脱氢酶法进行实验操作的步骤。
材料准备:1. 乳酸脱氢酶试剂盒2. 样品溶液3. 乳酸标准品4. 实验用试管和显微管操作步骤:1. 样品制备- 将待测样品装入实验用试管中。
每个样品应分别装入不同的试管,以避免交叉污染。
- 若样品过浓稀,需要进行适当的稀释,确保样品浓度在测试范围内。
2. 标准曲线制备- 准备不同浓度的乳酸标准品溶液,浓度范围可根据实验要求而定。
- 将不同浓度的标准品溶液分别装入实验用试管中。
3. 试剂添加- 分别向样品管和标准品管中加入相同体积的乳酸脱氢酶试剂,充分混匀。
4. 反应温育- 将所有试管置于恒温水浴中,温度设定为适合乳酸脱氢酶反应的温度(一般为37°C)。
- 在设定的反应温度下,将试管保持在水浴中反应一段时间(时间根据实验要求而定)。
5. 反应终止- 在反应时间结束后,以适当的方法终止反应。
常见的终止方式是添加酸性试剂或采用其他合适的方法。
6. 测定乳酸脱氢酶活性- 使用光度计、分光光度计或其他合适的仪器,测定样品和标准品反应后产生的光吸收值。
吸收值与乳酸脱氢酶活性成正比。
- 通过标准曲线,将样品的吸收值转化为对应的乳酸脱氢酶活性。
注意事项:1. 本实验操作需要严格按照实验室安全操作规范进行,避免任何可能导致个人受伤或污染的行为。
2. 实验过程中的试剂、标样和废液等应按照实验室规定的方法处理,不得随意丢弃。
3. 在操作过程中,保持实验器材和试剂的洁净,尽量避免外界因素对实验结果的影响。
4. 操作时需注意避免交叉污染,尤其是样品的装管和试剂的配比过程。
5. 样品和标准品的选择要合适,浓度范围应覆盖实验要求。
6. 温育过程中,确保试管能均匀受热,并避免发生温度不稳定的情况。
总结:乳酸脱氢酶(LDH)法是一种可靠的生物化学分析方法,适用于乳酸脱氢酶活性的测定。
乳酸脱氢酶测定试剂盒(乳酸底物法)产品技术要求lepu

乳酸脱氢酶测定试剂盒(乳酸底物法)适用范围:用于体外定量测定人血清中乳酸脱氢酶的活性。
分说明1.1 规格试剂1:3×60 mL,试剂2:1×45 mL;试剂1:1×60 mL,试剂2:1×20 mL;试剂1:1×60 mL,试剂2:1×12 mL;试剂1:2×60 mL,试剂2:2×15 mL;试剂1:1×40 mL,试剂2:1×10 mL;试剂1:1×4L,试剂2:1×1L;试剂1:1×16L,试剂2:1×4L。
1.2主要组成成分试剂1主要组分:试剂2主要组分:2.1 净含量应不低于试剂瓶标示装量。
2.2 外观试剂1:无色或淡黄色透明溶液;试剂2:无色或淡黄色透明溶液。
外包装完好、无破损,标签完好、字迹清晰。
2.3 试剂空白2.3.1 试剂空白吸光度在37℃、340nm波长、1cm光径条件下,试剂空白吸光度应不大于0.50。
2.3.2 试剂空白吸光度变化率在37℃、340nm波长、1cm光径条件下,用生理盐水作为样品加入试剂测试时,试剂空白吸光度变化率(△A/min)应不大于0.002。
2.4 分析灵敏度测试300U/L的被测物时,吸光度变化率(ΔA/min)应不低于0.0085。
2.5 准确度用参考物质(GBW09177)对试剂(盒)进行测试,相对偏差应不超过±10%。
2.6 重复性用血清样品或质控样品重复测试所得结果的重复性(变异系数,CV)应不大于5%。
2.7 线性2.7.1 在[25,750]U/L区间内,线性相关系数r应不小于0.990;2.7.2 [25,100)U/L区间内,线性绝对偏差应不超过±10U/L;[101,750]U/L区间内,线性相对偏差应不超过±10%。
2.8 批间差试剂(盒)批间相对极差应不大于10%。
乳酸脱氢酶(LDH)测定试剂盒(乳酸底物法)产品技术要求derui

乳酸脱氢酶(LDH)测定试剂盒
(乳酸底物法)
2.1外观和性状
外观和性状应符合表2要求。
表2 试剂盒内各组分的外观性状
2.2试剂空白
2.2.1试剂空白吸光度
试剂以生理盐水为空白时,在温度37℃、波长340nm、光径1.0 cm 条件下,吸光度≤0.50。
2.2.2试剂空白吸光度变化率
试剂以生理盐水为空白时,在温度37℃、波长340nm、光径1.0 cm 条件下,吸光度变化率≤0.002。
2.3分析灵敏度
试剂盒测试浓度为100U/L被测物时,吸光度变化率≥0.004。
2.4线性范围
2.4.1试剂盒在25 ~750U/L区间(范围)内,其回归系数r≥0.990。
2.4.2相对偏差或绝对偏差应符合表3 要求。
表3 相对偏差或绝对偏差
2.5精密度
2.5.1试剂盒重复性CV 值应≤5%。
2.5.2试剂盒批间相对极差(R)应≤10.0%。
2.6准确度
相对偏差(Bias%)应在参考物质靶值±10%以内。
2.7液体装量
试剂盒不同规格的净含量应不少于其标示量。
乳酸脱氢酶(LDH)测定操作规程(SOP)

乳酸脱氢酶(LDH)测定操作规程(SOP)一、用途本产品用于体外定量测定血清、血浆样品中乳酸脱氢酶(LDH)的活性。
二、临床意义(一)概述乳酸脱氢酶(LDH),又称L-乳酸-NAD+氧化还原酶,酶编号为EC 1.1.1.27,分子量约为34000道尔顿。
LDH是一种细胞质酶,存在于所有组织细胞中。
由于组织中的LDH 浓度比血浆高约500倍,即使组织的轻微损伤也将导致血清中活性的明显增高,在肝、心肌、骨骼肌和肾中发现高度组织特异性活性的酶。
(二)临床意义乳酸脱氢酶增高主要见于心肌梗死、肝炎、肺梗死、某些恶性肿瘤、白血病等。
某些肿瘤转移所致的胸腹水中乳酸脱氢酶活力往往升高。
目前,常用于心肌梗死、肝病和某些恶性肿瘤的辅助诊断。
(三)医学决定水平170U/L:此值在参考范围以内,等于或低于此值可排除许多与LDH升高有关的疾病,而考虑其他的诊断。
此值还可作为病人自身的对照,用来与以前或将来的测定值作比较。
300U/L:高于此水平时,应考虑到可能引起LDH升高的各种疾病,如心肌梗塞、肝病变、传染性单核细胞增多症、进行性肌营养不良等。
因此,应作其他各种试验,以作出明确诊断。
血清溶血可使测定值增高,应予以注意。
500U/L:高于此值,常见于巨幼细胞性溶血,急性白血病、慢性粒细胞性白血病、转移癌和肝昏迷等,此时应作其他多种检测来作出正确诊断。
三、检验原理L-乳酸+NAD+−−LDH丙酮酸+NADH+H+−→NADH的生成速率与样品中LDH活性成正比,在340nm波长处,通过连续监测吸光度的上升速率(△A/min),即可计算出样品中LDH的活性。
四、样品血液样品原则上采集晨起空腹血(禁食12小时);患者处于平静、休息状态,减少患者由于运动、饮食带来的影响;静脉采血时患者应取坐位或卧位;止血带使用后1分钟内采血,回血后立即松开;正确使用抗凝剂;防止溶血;防止过失性采样。
样品运送过程中应防止过度振荡、防止样品容器的破损、防止样品被污染、防止样品及唯一性标志的丢失和混淆,防止样品对环境的污染、水分蒸发。
乳酸脱氢酶(LDH)试剂盒说明书

乳酸脱氢酶(LDH)试剂盒说明书(乳酸→丙酮酸连续监测法)【产品名称】中文名称:乳酸脱氢酶(LDH)试剂盒(乳酸→丙酮酸连续监测法)英文名称:LACTATE DEHYDROGENASE REAGENT KIT(L→P method)【包装规格】50ml/盒(R-1:40ml×1,R-2:10ml×1),240ml/盒(R-1:64ml×3,R-2:48ml×1),250ml/盒(R-1:40ml×5,R-2:10ml×5),375ml/盒(R-1:100ml×3,R-2:75ml×1),2500ml/盒(R-1:500ml×4,R-2:500ml×1)。
【预期用途】本试剂盒用以测定人血清乳酸脱氢酶(LDH)的活力。
【检验原理】乳酸脱氢酶在催化乳酸生成丙酮酸的同时将NAD+还原成NADH。
通过测定NADH在340nm处吸光度增加的速度可求得乳酸脱氢酶的活力。
LDHL-乳酸+ NAD+─────→丙酮酸+ NADH + H+【主要组成成份】试剂成份含量R-1 L-乳酸锂76mmol/LR-2 NAD ≥31mmol/l *不同批号试剂盒中的各组份,经检验符合产品性能指标的,可以互换。
【储存条件及有效期】本试剂盒在2-8℃下避光保存可稳定一年;试剂R-1、R-2开启后在2-8℃避光保存可稳定一个月。
【适用仪器】本试剂适用于日立7020型、日立7060型、日立7080型、日立7150型、日立7170型、日立7180型、日立7600(D)型、日立7600(P)型自动分析仪以及奥林巴斯AU600、AU2700、东芝-雅培、BECKMAN CX系列、BECKMAN LX-20型等自动分析仪。
本试剂在日立7020自动分析仪上已通过第三方验证,并备有以上各种自动分析仪的参数可供参考。
【样本要求】空腹血清,保存于室温可稳定3小时,保存于0℃以下可稳定1周。
乳酸脱氢酶测定试剂盒(乳酸底物法)产品技术要求haifeng

乳酸脱氢酶测定试剂盒(乳酸底物法)
适用范围:本产品适用于体外定量测定人血清中乳酸脱氢酶(LDH)的含量。
1.1 产品规格
1.2 主要组成成分
2.1 外观
2.1.1试剂盒标签标识清晰,外包装完整无破损;
2.1.2试剂1为无色澄清液体,目测不得有任何沉淀及絮状悬浮物;
2.1.3试剂2为无色澄清液体,目测不得有任何沉淀及絮状悬浮物。
2.2 净含量
净含量不低于标示值。
2.3 试剂空白
2.3.1空白吸光度
在主波长340nm、副波长405nm、37℃条件下,空白吸光度应小于0.5。
2.3.2空白吸光度变化率
在主波长340nm、副波长405nm、37℃条件下,空白吸光度变化率不大于0.002/min。
2.4 线性范围
(25,1000)U/L范围内,相关系数≥0.990;
(25,100]U/L范围内,线性绝对偏差应不超过±10U/L;
(100,1000)U/L范围内,线性相对偏差应不超过±10%。
2.5 分析灵敏度
在产品说明书规定参数设定条件下,换算为测定浓度为300U/L的样本, 吸光度变化率△A/min应不小于0.015。
2.6 精密度
2.6.1批内重复性
CV≤5.0%。
2.6.2 批间差
相对极差R≤10.0%。
2.7 准确度
测定参考物质GBW(E)090593,测定结果应不超过标示值的±10%。
2.8 稳定性
未开封试剂2℃~8℃储存,可稳定12个月。
取到效期后2个月内产品进行检测,检测结果应满足2.4和2.7的规定。
乳酸脱氢酶(LDH)释放法细胞繁殖与毒性定量检测试剂盒产

乳酸脱氢酶(LDH)释放法细胞繁殖与毒性定量检测试剂盒产品说明书(中文版)主要用途乳酸脱氢酶(LDH)释放法细胞繁殖与毒性定量检测试剂是一种旨在通过酶联连续反应系统检测由于细胞损伤导致的细胞内稳定的乳酸脱氢酶释放到细胞外,使四唑盐染料碘硝基氯化四氮唑(INT)还原为红色甲臜(farmazan),即比色法定量测定酶活性,以评价活体细胞繁殖的权威而经典的技术方法。
该技术经过精心研制、成功实验证明的。
适用于各种药物、化学、环境因子和营养因子处理的贴壁或悬浮生长中的动物或人体细胞。
替代传统的同位素[51 Cr]释放检测的最佳选择。
产品严格无菌,即到即用,简捷敏感,性能稳定,显色清晰,检测准确,重复性好。
技术背景细胞凋亡或坏死而造成的细胞膜结构的损害或完全裂解导致细胞浆内的酶释放外泄到培养液里,其中包括活性稳定的乳酸脱氢酶。
乳酸脱氢酶(lactate dehydrogenase;LDH)释放法的测定是基于在乳酸脱氢酶的作用下,还原NAD+反应生成的NADH,再与氧化型2-(4-碘苯)-3-(4-硝基苯)-5-苯四唑(Iodonitrotetrazolium;INT)在硫辛酰胺脱氢酶(diaphorase)的催化下反应生成红色生色产物甲臜(formazan),在490nm波长下产生吸收峰,从而确定释放的乳酸脱氢酶的活性,作为细胞膜完整性的标志:吸光值与细胞死亡或毒性程度成线性正相关。
酶联连续反应系统为:lactate dehydrogenaseNAD+ + Lactate → Pyruvate + NADHdiaphoraseNADH + INT → NAD++ Formazan(red)产品内容裂解液(Reagent A)1毫升补充液(Reagent B)1毫升反应液(Reagent C)5毫升显色液(Reagent D)1毫升终止液(Reagent E)1毫升标准液(Reagent F)20微升产品说明书1份保存方式保存在-20℃冰箱里,反应液(Reagent C)和显色液(Reagent D)避免光照;有效保证6月用户自备96孔细胞培养板:用于细胞操作的容器细胞培养箱:用于孵育反应孔板离心机:用于沉淀细胞酶标仪:用于定量检测染色后的细胞实验步骤一、贴壁细胞检测1.准备96孔细胞培养板的待测细胞(每孔100微升):包括未处理的对照细胞(样品对照孔),未处理的后续裂解的细胞(样品最大酶活性对照孔),以及药物处理的细胞(处理样品孔),并做好标记(细胞密度为每孔2 X 103至2 X 104细胞)2.到规定的检测时间点前1小时,从湿润的细胞培养箱里取出待测的96孔细胞培养板(注意:确保细胞培养液维持在100微升容量)3.加入10微升裂解液(Reagent A)到未处理的后续裂解的细胞孔里(样品最大酶活性对照孔)4.同时加入10微升补充液(Reagent B)到其余所有检测孔里5.放回湿润的细胞培养箱里,继续培养1小时,即规定检测时间6.从湿润的细胞培养箱里取出待测的96孔细胞培养板7.放进孔板离心机离心10分钟,速度为250g8.分别小心移取50微升上清液到新的96孔板的相应孔里,避免触摸细胞颗粒,同时注意做好标记9.分别加入50微升反应液(Reagent C)(注意:使用前,须混匀)10.分别加入10微升显色液(Reagent D)11.摇动96孔板混匀12.在室温下孵育30分钟,避免光照13.(选择步骤)分别加入10微升终止液(Reagent E)14.即刻放进酶标仪里测读:波长490nm15.计算处理样品实际吸光读数:处理样品孔吸光读数-样品对照孔吸光读数16.计算样品细胞最大酶活性的实际吸光读数:样品最大酶活性对照孔吸光读数-样品对照孔吸光读数17.计算细胞毒性或死亡率(%):(处理样品实际吸光读数÷样品细胞最大酶活性的实际吸光读数)X 10018.或绘制细胞生长曲线:纵座标(Y轴)为实际吸光读数(A);横坐标(X轴)为细胞数或时间点或药物浓度;据此计算其LD50二、悬浮细胞检测1.准备96孔细胞培养板的待测悬浮细胞(每孔100微升):包括未处理的对照细胞(样品对照孔),未处理的后续裂解的细胞(样品最大酶活性对照孔),以及药物处理的细胞(处理样品孔),并做好标记(细胞密度为每孔5 X 103至5 X 104细胞)2.到规定的检测时间点前1小时,从湿润的细胞培养箱里取出待测的96孔细胞培养板(注意:确保细胞培养液维持在100微升容量)3.加入10微升裂解液(Reagent A)到未处理的后续裂解的细胞孔里(样品最大酶活性对照孔)4.同时加入10微升补充液(Reagent B)到其余所有检测孔里5.放回湿润的细胞培养箱里,继续培养1小时,即规定检测时间6.从湿润的细胞培养箱里取出待测的96孔细胞培养板7.放进孔板离心机离心10分钟,速度为250g8.分别小心移取50微升上清液到新的96孔板的相应孔里,避免触摸细胞颗粒,同时注意做好标记9.分别加入50微升反应液(Reagent C)(注意:使用前,须混匀)10.分别加入10微升显色液(Reagent D)11.摇动96孔板混匀12.在30℃温度下孵育30分钟,避免光照13.(选择步骤)分别加入10微升终止液(Reagent E)14.即刻放进酶标仪里测读:波长490nm15.计算处理样品实际吸光读数:处理样品孔吸光读数-样品对照孔吸光读数16.计算样品细胞最大酶活性的实际吸光读数:样品最大酶活性对照孔吸光读数-样品对照孔吸光读数)17.计算细胞毒性或死亡率(%):(处理样品实际吸光读数÷样品细胞最大酶活性的实际吸光读数)X 10018.或绘制细胞生长曲线:纵座标(Y轴)为实际吸光读数(A);横坐标(X轴)为细胞数或时间点或药物浓度;据此计算其LD50注意事项1.本产品为100次(1个96孔板)操作2.操作时须戴手套3.整个操作须无菌操作4.建议每个样品安排3个孔,即重复3次,计算时取其平均值5.检测体系相应增加,试剂用量按比例相应增加:例如200微升检测体系,试剂用量增加1倍6.每孔中的培养液需100微升,避免使用周边培养孔(常常液体蒸发而减少)7.系统测试,可以加入2至5微升标准液(Reagent G)到50微升无细胞的细胞培养液里,然后按照说明书加入反应液(Reagent C)和显色液(Reagent D)即可8.细胞裂解效果不佳,可以使用20微升裂解液(Reagent A)处理9.孵育时,须避光10.染色完成后,建议即刻检测,最迟不得超过1小时11.细胞培养和处理时,避免使用草酸(OXALATE),草氨酸(OXAMATE)和EDTA,否则影响检测的准确性12.血清含有乳酸脱氢酶,建议使用浓度不要超过1%13.细胞过度生长、密度过高、离心速度过大、培养箱内外温差过大等因素会造成细胞自然释放乳酸脱氢酶14.酚红会干扰检测15.样品最大酶活性对照孔或最大OD吸光读数与细胞裂解程度密切相关16.如果用户没有孔板离心机,则移取上清液时格外小心17.如果用户没有匹配的波长,可以使用波长470nm至570nm之间的任一波长替代18.本公司提供系列细胞繁殖检测试剂产品质量标准1.本产品经鉴定性能稳定2.本产品经鉴定检测敏感使用承诺杰美基因秉着“信誉至上、客户满意、质量承诺”的宗旨为我们的用户提供优质产品和服务。
小鼠D-乳酸脱氢酶 (D-LDH)-ELISA试剂盒说明书

小鼠D-乳酸脱氢酶 (D-LDH)酶联免疫吸附测定试剂盒使用说明书产品编号:E-EL-M0419(本试剂盒仅供体外研究使用、不用于临床诊断!)声明:尊敬的客户,感谢您选用本公司的产品。
本产品选用世界著名生产厂家的原料,采用专业ELISA kit生产技术制造。
适用于体外定量检测小鼠血清、血浆、组织匀浆或细胞培养上清液中天然和重组D-LDH浓度。
使用前请仔细阅读说明书并检查试剂组分!如有疑问,请及时联系伊莱瑞特生物科技有限公司。
*: [96T/48T](打开包装后请及时检查所有物品是否齐全完整)检测原理:本试剂盒采用双抗体夹心ELISA法。
用抗小鼠D-LDH抗体包被于酶标板上,实验时标本或标准品中的D-LDH会与包被抗体结合,游离的成分被洗去。
依次加入生物素化的抗小鼠D-LDH抗体和辣根过氧化物酶标记的亲和素。
抗小鼠D-LDH抗体与结合在包被抗体上的小鼠D-LDH结合、生物素与亲和素特异性结合而形成免疫复合物,游离的成分被洗去。
加入显色底物(TMB),TMB 在辣根过氧化物酶的催化下现蓝色,加终止液后变黄。
用酶标仪在450nm波长处测OD值,D-LDH 浓度与OD450值之间呈正比,通过绘制标准曲线求出标本中D-LDH的浓度。
标本收集:1.血清:全血标本于室温放置2小时或4℃过夜后于1000×g离心20分钟,取上清即可检测,收集血液的试管应为一次性的无热原,无内毒素试管。
2.血浆:抗凝剂推荐使用EDTA.Na2,标本采集后30分钟内于1000×g离心15分钟,取上清即可检测。
避免使用溶血,高血脂标本。
3.组织匀浆:用预冷的PBS (0.01M, pH=7.4)冲洗组织,以去除残留血液(匀浆中裂解的红细胞会影响测量结果),称重后将组织剪碎。
将剪碎的组织与对应体积的PBS(一般按1:9的重量体积比,比如1g的组织样本对应9mL的PBS,具体体积可根据实验需要适当调整,并做好记录。
推荐在PBS中加入蛋白酶抑制剂)加入玻璃匀浆器中,于冰上充分研磨。
LDH文档,乳酸脱氢酶测定试剂盒(LDH)检测标准操作规程

1、方法依据:深圳迈瑞生物医疗电子股份有限公司乳酸脱氢酶(LDH)测定试剂盒(IFCC法)测定方法2、适用范围:适用于人血清或血浆乳酸脱氢酶(LDH)的测定。
3、试剂仪器:3.1 试剂:深圳迈瑞生物医疗电子股份有限公司原装试剂盒。
3.2未开启的试剂盒避光保存于2℃~8℃有效期为一年。
试剂开瓶后应避光保存,在2℃~8℃可稳定30天。
试剂不可冰冻。
3.3 仪器:迈瑞BS-2000M全自动生化分析仪.4、操作程序4.1方法原理LDH 催化乳酸氧化为丙酮酸,同时将NAD+还原为NADH,NADH 的生成速率与标本中乳酸脱氢酶的活性成正比。
LDH乳酸+ NAD+ + H2O 丙酮酸+ NADH + H+4.2样本要求新鲜血清、肝素抗凝或EDTA抗凝血浆样本,采集后及时测定,应避免溶血和污染。
4.3上机操作4.3.1试剂装载、校准、样品和质控血清分析操作详见“《迈瑞BS-2000M全自动生化分析仪标准操作、维护、保养规程》”。
4.3.2 校准:4.3.2.1 标准液的准备:校准品使用深圳迈瑞生物医疗电子股份有限公司配套冻干品,按说明书要求稀释后分装,-20℃冷冻保存,用前提前15分钟从冰箱中取出,复溶到室温后上机检测。
4.3.2.2 校准程序:首次使用校准。
当有以下情况时需重新校准:1)换试剂批号或出现质控漂移时;2)当仪器做完保养后;3)仪器进行零件更换时。
每次试验前用准备好的校准品进行校准,校准通过后进行检测。
4.3.2.3 质控:在标本开始之前做质控,质控通过后方能进行标本的检测。
4.3.3 测试基本参数4.4参考范围115~220 U/L (注:各实验室应有自己的参考范围。
)4.5 方法评价线性范围:4~1000U/L内。
当样本测定值超过上限时,应将样本用生理盐水稀释,重新测定,结果乘以稀释倍数。
精密度:批内变异系数:≤ 3.0%;批间变异系数:≤5.0%。
分析灵敏度:本试剂盒的检测低限不高于4 U/L。
乳酸脱氢酶(LDH)比色法测试盒

Focusonyourresearch Serviceforlifescience乳酸脱氢酶(LDH)比色法测试盒货号:E-BC-K046-M方仪器:酶标仪(440-460nm)规格:96T(40sFocusonyourresearchServiceforlifescience基本信息用途本试剂盒合用于检测血清、血浆、胸水、组织、细胞等样本中LDH活力。
检测范围及敏捷度检测范围:6-1000U/L敏捷度:6U/L背景介绍乳酸脱氢酶(EC,LDH)是一种氧化复原酶,它催化丙酮酸和乳酸的互相转变,同时将NADH氧化成NAD+[1]。
LDH是一种四聚体分子,由两个亚基构成,分别为H亚基和M亚基[2]。
在组织损害或红细胞溶血后,细胞将LDH开释到血液中。
细胞外的LDH活性用于检测细胞损害或细胞死亡[3]。
检测原理以辅酶I为递氢体,LDH催化乳酸产生丙酮酸,丙酮酸与 2,4-二硝基苯肼作用生成丙酮酸二硝基苯腙,后者在碱性溶液中呈棕红色,颜色的深浅与丙酮酸的浓度呈正比,经过测定OD值,可计算LDH的活力。
本试剂盒测组织和细胞样本时,需测定总蛋白浓度,介绍使用 BCA法(货号:E-BC-K318-M)。
乳酸脱氢酶(LDH)比色法测试盒供给试剂和物件编号名称规格(size)保留方式(96T)(Storage)试剂一基质液5mL×1瓶2-8℃保留6个月(Reagent1)(SubstrateBuffer)试剂二辅酶I粉剂×1支2-8℃保留6个月(Reagent2)(CoenzymeI)试剂三显色剂5mL×1瓶2-8℃避光保留6(Reagent3)(ChromogenicAgent)个月试剂四碱溶液5mL×1瓶2-8℃保留6个月(Reagent4)(AlkaliReagent)试剂五2μmol/mL丙酮酸标准品1mL×1支2-8℃保留6个月(Reagent5)(2μmol/mLPyruvicAcidStandard)96孔酶标板1板96孔覆膜2张样本地点标志表1张注:试剂严格按上表中的保留条件保留,不一样试剂盒中的试剂不可以混用。
C0016 乳酸脱氢酶细胞毒性检测试剂盒说明书
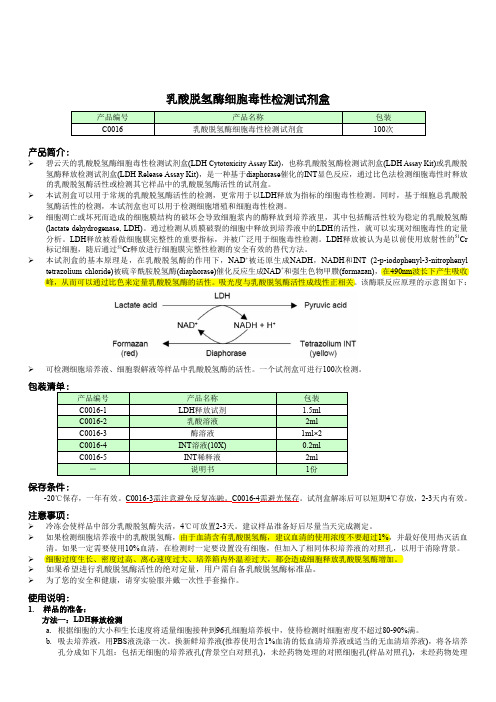
乳酸脱氢酶细胞毒性检测试剂盒产品简介:碧云天的乳酸脱氢酶细胞毒性检测试剂盒(LDH Cytotoxicity Assay Kit),也称乳酸脱氢酶检测试剂盒(LDH Assay Kit)或乳酸脱氢酶释放检测试剂盒(LDH Release Assay Kit),是一种基于diaphorase催化的INT显色反应,通过比色法检测细胞毒性时释放的乳酸脱氢酶活性或检测其它样品中的乳酸脱氢酶活性的试剂盒。
本试剂盒可以用于常规的乳酸脱氢酶活性的检测,更常用于以LDH释放为指标的细胞毒性检测。
同时,基于细胞总乳酸脱氢酶活性的检测,本试剂盒也可以用于检测细胞增殖和细胞毒性检测。
细胞凋亡或坏死而造成的细胞膜结构的破坏会导致细胞浆内的酶释放到培养液里,其中包括酶活性较为稳定的乳酸脱氢酶(lactate dehydrogenase, LDH)。
通过检测从质膜破裂的细胞中释放到培养液中的LDH的活性,就可以实现对细胞毒性的定量分析。
LDH释放被看做细胞膜完整性的重要指标,并被广泛用于细胞毒性检测。
LDH释放被认为是以前使用放射性的51Cr 标记细胞,随后通过51Cr释放进行细胞膜完整性检测的安全有效的替代方法。
本试剂盒的基本原理是,在乳酸脱氢酶的作用下,NAD+被还原生成NADH,NADH和INT (2-p-iodophenyl-3-nitrophenyl tetrazolium chloride)被硫辛酰胺脱氢酶(diaphorase)催化反应生成NAD+和强生色物甲臜(formazan),在490nm波长下产生吸收峰,从而可以通过比色来定量乳酸脱氢酶的活性。
吸光度与乳酸脱氢酶活性成线性正相关。
该酶联反应原理的示意图如下:可检测细胞培养液、细胞裂解液等样品中乳酸脱氢酶的活性。
一个试剂盒可进行100次检测。
保存条件:-20℃保存,一年有效。
C0016-3需注意避免反复冻融。
C0016-4需避光保存。
试剂盒解冻后可以短期4℃存放,2-3天内有效。
乳酸脱氢酶测定方法操作规程

乳酸脱氢酶(LDH)测定方法操作规程【产品名称】通用名称:乳酸脱氢酶(LDH)测定试剂盒(IFCC 法)使用说明书【预期用途】该试剂盒采用IFCC法,用于体外定量测定人血清或血浆中乳酸脱氢酶的活力。
【检验原理】LDH催化乳酸氧化为丙酮酸,同时将NAD+还原为NADH。
NADH的生成速率与标本中乳酸脱氢酶的活性成正比。
乳酸+ 2O LDH丙酮酸+NADH+H+【主要组成成份】R1:Good’s缓冲液50 mmol/LL-乳酸 5.0 mmol/LR2:NAD+7.0 mmol/L*不同批号试剂盒各组分请勿混用。
【储存条件与有效期】未开启的试剂盒在2~8℃保存有效期为18个月。
试剂开瓶后应避光保存,在2℃~8℃可稳定30天。
试剂不可冰冻。
【适用仪器】迈瑞BS系列全自动生化分析仪、日立7180型全自动生化分析仪、日立7060型全自动生化分析仪、日立7600P自动生化分析仪、奥林巴斯AU400型全自动生化分析仪、奥林巴斯AU2700型全自动生化分析仪、贝克曼库尔特AU680型全自动生化分析仪。
若需自动生化分析仪应用参数,请随时和公司联系。
建议用户在不同仪器上使用本产品时,根据实验室情况进行验证。
【样本要求】新鲜血清或血浆,采集后及时测定,应避免溶血和污染。
【检验方法】试剂准备R1:即用液体试剂R2:即用液体试剂测定条件波长340nm温度37℃分析类型动力学法反应方向上升反应操作步骤* ΔA/min=ΔA/min样本管—ΔA/min空白管* 试剂和样本量可根据不同生化分析仪要求按比例适当增减。
校准校准品类型S1:生理盐水S2:迈瑞配套校准品推荐进行2点线性校准校准周期和要求(包括但不限于以下情况)更换试剂批号时仪器关键零部件更换时室内质控失效时质控每批样品检测时,建议使用迈瑞公司提供的配套质控品进行内部质量控制。
质控品测定值应该在规定的范围内。
若超出规定范围,有必要采取相应的措施或联系生产厂家。
【参考范围】男性:135~225U/L 女性:135~214U/L(注:各实验室应有自己的参考范围。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
乳酸脱氢酶(LDH)活性检测试剂盒说明书微量法
注意:正式测定前务必取2-3个预期差异较大的样本做预测定。
货号:BC0685
规格:100T/48S
产品内容:
提取液:液体60mL×1瓶,4℃保存;
试剂一:液体7mL×1瓶,4℃保存;
试剂二:粉剂×1支,-20℃保存,用时加入1.3mL双蒸水充分溶解备用,配好后可分装成小管-20℃保存,可保存两周,禁止反复冻融;
试剂三:液体7mL×1瓶,4℃保存;
试剂四:液体25mL×1瓶,4℃保存;
丙酮酸钠标准液:液体1mL×1支,4℃保存,2μmol/ml。
产品简介:
LDH(EC 1.1.1.27)广泛存在于动物、植物、微生物和培养细胞中,是糖酵解途径的末端酶,催化丙酮酸与乳酸之间的可逆反应,伴随着NAD+/NADH之间互变。
LDH催化NAD+氧化乳酸生成丙酮酸,丙酮酸进一步与2,4-二硝基苯肼作用生成丙酮酸二硝基苯腙,在碱性溶液中显棕红色,颜色深浅与丙酮酸浓度成正比。
试验中所需的仪器和试剂:
可见分光光度计/酶标仪、恒温水浴锅、台式离心机、可调式移液器、微量玻璃比色皿/96孔板、研钵、冰和蒸馏水。
操作步骤:
一、粗酶液提取:
1.细菌、细胞或组织样品的制备:
细菌或培养细胞:先收集细菌或细胞到离心管内,离心后弃上清;按照细菌或细胞数量(104个):提取液体积(mL)为500~1000:1的比例(建议500万细菌或细胞加入1mL提取液),超声波破碎细菌或细胞(冰浴,功率20%或200W,超声3s,间隔10s,重复30次);8000g4℃离心10min,取上清,置冰上待测。
组织:按照组织质量(g):提取液体积(mL)为1:5~10的比例(建议称取约0.1g组织,加入1mL提取液),进行冰浴匀浆。
8000g4℃离心10min,取上清,置冰上待测。
2.血清(浆)样品:直接检测。
3.丙酮酸钠标准液:取100μL标准液,倍比稀释至1、0.5、0.25、0.125、0μmol/mL,用2、1、0.5、
0.25、0.125、0μmol/mL做标准曲线。
二、测定操作表:
1.分光光度计或酶标仪预热30min以上,调节波长至450nm,蒸馏水调零。
2.样本测定
试剂名称(μL)测定管对照管标准管待测样本1010-
标准液--10
试剂一505050
试剂二10--
蒸馏水-1010
充分混匀,37℃(哺乳动物)或25℃(其它物种)准确水浴15min
试剂三505050
充分混匀,37℃(哺乳动物)或25℃(其它物种)水浴15min
试剂四150150150充分混匀,室温静置3min,取200μL转移至微量玻璃比色皿或在96孔板中,450nm下测定吸光度,计算ΔA=A测定管-A对照管。
每个测定管需要设一个对照。
根据标准管测定值和浓度做标准曲线,y为标准品浓度,μmol/mL;x为对吸光度(减去浓度为0的标准管的OD值)。
LDH活力单位计算:
1.计算样品丙酮酸的含量,即将ΔA带入回归方程中(x),计算y值
2.血清(浆)LDH活力的计算
单位的定义:每mL血清(浆)每分钟催化产生1nmol丙酮酸定义为一个酶活力单位。
LDH(U/mL)=y×V样÷V样÷T×103=66.7×y
3.细胞、细菌和组织中LDH活力的计算
(1)按样本蛋白浓度计算:
单位的定义:每mg组织蛋白每分钟催化产生1nmol丙酮酸定义为一个酶活力单位。
LDH(U/mg prot)=y×V样÷(Cpr×V样)÷T×103=66.7×y÷Cpr
需要另外测定,建议使用本公司BCA蛋白质含量测定试剂盒。
(2)按样本鲜重计算:
单位的定义:每g组织每分钟催化产生1nmol丙酮酸定义为一个酶活力单位。
LDH(U/g鲜重)=y×V样÷(W÷V样总×V样)÷T×103=66.67×y÷W
(3)按细菌或细胞密度计算:
单位的定义:每1万个细菌或细胞每分钟催化产生1nmol丙酮酸定义为一个酶活力单位。
LDH(U/104cell)=y×V样÷(500÷V样总×V样)÷T×103=0.133×y
V样:反应体系中加入的样本体积,10μL=0.01mL;V样总:加入的提取液体积,1mL;
T:反应时间,15min;Cpr:蛋白质浓度,mg/mL;
W:样品质量,g;500:细胞或细菌总数,500万;
103:1μmol/mL=103nmol/mL。
