冰晶体
列举生活中常见的晶体和非晶体

列举生活中常见的晶体和非晶体晶体和非晶体是我们日常生活中常见的物质形态,它们在物理、化学、材料等领域都有着广泛的应用。
本文将按照物质的性质和用途,列举一些生活中常见的晶体和非晶体。
一、晶体1. 糖晶体:糖是我们日常生活中常见的食品,而糖晶体则是糖的一种晶体形态。
糖晶体呈现出六角形的晶体结构,具有透明、脆硬、易溶于水等特点。
2. 盐晶体:盐是我们日常生活中必不可少的调味品,而盐晶体则是盐的一种晶体形态。
盐晶体呈现出立方体的晶体结构,具有透明、脆硬、易溶于水等特点。
3. 钻石晶体:钻石是一种贵重的宝石,也是一种晶体形态。
钻石晶体呈现出六角形的晶体结构,具有高硬度、高折射率、高热导率等特点。
4. 冰晶体:冰是我们日常生活中常见的物质,而冰晶体则是冰的一种晶体形态。
冰晶体呈现出六角形的晶体结构,具有透明、脆硬、易溶于水等特点。
5. 石英晶体:石英是一种常见的矿物,也是一种晶体形态。
石英晶体呈现出六角形的晶体结构,具有高硬度、高折射率、高热稳定性等特点。
二、非晶体1. 玻璃:玻璃是一种非晶体材料,具有透明、硬度高、化学稳定性好等特点。
玻璃在建筑、家居、电子等领域都有着广泛的应用。
2. 塑料:塑料是一种非晶体材料,具有轻质、耐腐蚀、易加工等特点。
塑料在包装、建筑、汽车等领域都有着广泛的应用。
3. 橡胶:橡胶是一种非晶体材料,具有弹性好、耐磨损、耐寒性好等特点。
橡胶在轮胎、密封件、管道等领域都有着广泛的应用。
4. 聚酯纤维:聚酯纤维是一种非晶体材料,具有柔软、耐磨损、易洗涤等特点。
聚酯纤维在服装、家居、汽车等领域都有着广泛的应用。
5. 陶瓷:陶瓷是一种非晶体材料,具有耐高温、耐腐蚀、硬度高等特点。
陶瓷在建筑、家居、电子等领域都有着广泛的应用。
总之,晶体和非晶体在我们的日常生活中无处不在,它们的应用范围非常广泛。
通过了解它们的性质和用途,我们可以更好地利用它们,为我们的生活带来更多的便利和美好。
冰晶体的形成机理和过程.

为0.0099℃。
水只有被冷却到低于冻结点的某一温度时才开始
冻结,这种现象被称为过冷。
低于冻结点的这一温度被称为过冷点。
冻结点和过冷点之间的温度差称为过冷度。
水分冻结成冰包括晶核的形成和晶体的成长两个过程。
当水的温度降到冰点以下,水分子的热运动减慢,并开
始形成称为生长点的分子集团,生长点很小,长大后就
一、冰晶体的形成机理和过程
水是所有生命细胞的基本组成,它是生化反应、 溶质传递和细胞内pH调节的介质,也是许要作用。
图中AO线为液汽线,BO
线为固汽线,CO线为固 液线,O点为水的三相点 。由图可以看出,压力对 水的冻结点有影响,真空
(610Pa)下水的冻结点
形成新相的先驱,称之为晶核。 晶核的形成是一些水分子以一定规律结合成颗粒型的微 粒,晶核提供晶体成长的基础,冰晶的成长是水分子发 生位移并有秩序地结合到晶核上面,使晶体不断增大形 成冰晶体。
四种晶体的熔沸点

四种晶体的熔沸点
晶体是一种具有有序排列的分子、原子或离子结构的固体。
它们具有一定的熔沸点,也就是在一定的温度下能够融化或沸腾。
以下是四种常见晶体的熔沸点。
1. 钠氯化物晶体:钠氯化物晶体是一种由钠离子和氯离子组成的离子化合物。
它的熔点约为801℃,沸点约为1413℃。
2. 碳晶体:碳晶体是由碳原子组成的晶体,包括金刚石和石墨。
金刚石的熔点非常高,约为3927℃,而石墨的熔点相对较低,约为3730℃。
3. 冰晶体:冰晶体是由水分子组成的晶体。
它的熔点在标准大气压下约为0℃,沸点约为100℃。
4. 硫晶体:硫晶体是由硫原子组成的晶体。
它的熔点约为115℃,沸点约为444℃。
这些晶体的熔沸点与它们的化学结构、分子大小、相互作用力等有关。
熔沸点的知识在材料科学、化学工程等领域中有着广泛的应用。
- 1 -。
冰的科普知识

冰的科普知识
冰是在0摄氏度或32华氏度以下的温度下,水在固态状态下形成的物质。
以下是关于冰的一些科普知识:
1.冰的形成:当水温降到0摄氏度(32华氏度)以下时,水分
子开始减缓运动,逐渐形成固态结构,形成冰晶体。
2.分子结构:冰的分子结构是六方密堆积,每个水分子与周围六
个水分子通过氢键相连。
这种结构使得冰在固态时呈现规则的
晶体形状。
3.密度:冰的密度比液态水低,这是相当罕见的情况。
当水冷却
到0摄氏度以下时,其分子排列成晶体结构,导致冰的体积扩
大。
4.吸热性质:冰在从固态转变为液态水时吸收热量,这被称为熔
化潜热。
这种性质在自然界中的一些重要现象中起着关键作用,如冰融化时吸收的热量有助于维持水体的稳定温度。
5.晶体多态:冰有不同的晶体形态,如冰I、冰II等。
这些形态
取决于温度和压力的变化。
例如,冰I是最常见的冰晶体形态。
6.冰的颜色:纯冰通常呈透明或淡蓝色,因为它对可见光的透明
度很高。
然而,在某些情况下,冰的颜色也可能受到杂质的影
响而呈现其他色彩。
7.冰的应用:冰在日常生活中有广泛的应用,不仅用于制冷和冷
藏,还用于制作雪糕、冰淇淋等。
在科学研究中,冰也被用于
实验室中的冷冻保存和实验。
8.冰的存在于太阳系中:冰不仅存在于地球上,太阳系中的一些
天体,如行星、卫星和小行星,也包含大量的冰。
例如,木卫二的表面主要由水冰组成。
这些都是关于冰的基本科普知识,冰的性质和应用在自然界和科学研究中都起到了重要的作用。
冰晶的化学原理

冰晶的化学原理
冰晶是由水分子组成的晶体,其化学原理是由于水分子之间的氢键作用而形成的有序结构。
水分子(H2O)由一个氧原子和两个氢原子组成。
氧原子与两个氢原子之间通过共用电子对形成了两个氢键。
氢键是一种相对较弱的相互作用力,其强度大约为共价键的10%。
氢键使得水分子呈现出了特殊的物理和化学性质。
在冰晶中,大量的水分子通过氢键有序地排列成三维结构。
冰晶的晶格是由平面上排列成六角形的水分子所组成,每个水分子通过氢键与其周围的四个水分子相连。
这种排列使得冰晶具有有序的结构,形成了晶胞。
在低温下,水分子的热运动相对较小,氢键能够有效地保持水分子的有序排列。
水分子之间的氢键使得冰晶具有较高的结晶度,形成了比较稳定的晶体结构。
冰晶的晶格结构对其物理性质和化学性质有重要影响。
由于氢键的存在,水分子在冰晶中的排列相对密集,使得冰的密度较大。
正因为如此,冰在水中浮在水面上,而不会沉入水中。
当温度升高时,水分子的热运动增加,氢键逐渐断裂,使冰晶逐渐熔化成液态水。
液态水中水分子的热运动更加剧烈,使得氢键断裂更加频繁,水分子的排列变得无序。
因此,液态水没有明显的结晶特征。
总之,冰晶的化学原理是由于水分子之间的氢键作用而形成的有序结构。
氢键使得水分子在低温下有序排列形成晶格结构,从而形成冰晶晶体。
随着温度升高,氢键断裂,冰晶逐渐熔化成液态水,水分子排列无序。
以上就是冰晶的化学原理。
冰的晶体结构
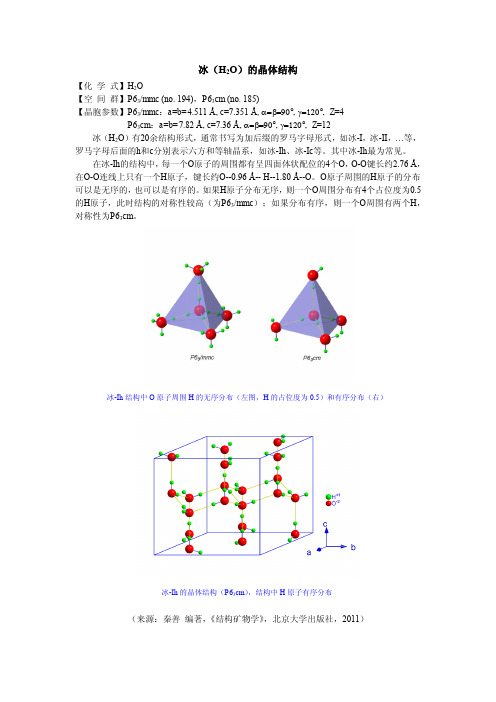
冰-Ih 的晶体结构(P63cm) ,结构中 H 原子有序分布
(来源:秦善 编著, 《结构矿物学》 ,北京大学出版社,2011)
冰(H2O)的晶体结构
【化 学 式】H2O 【空 间 群】P63/mmc (no. 194),P63cm (no. 185) 【晶胞参数】P63/mmc:a=b=4.511 Å, c=7.351 Å, ° ° Z=4 P63cm:a=b=7.82 Å, c=7.36 Å, ° ° Z=12 冰(H2O)有20余结构形式,通常书写为加后缀的罗马字母形式,如冰-I,冰-II,…等, 罗马字母后面的h和c分别表示六方和等轴晶系,如冰-Ih、冰-Ic等。其中冰-Ih最为常见。 在冰-Ih的结构中, 每一个O原子的周围都有呈四面体状配位的4个O, O-O键长约2.76 Å, 在O-O连线上只有一个H原子,键长约O--0.96 Å-- H--1.80 Å--O。O原子周围的H原子的分布 可以是无序的, 也可以是有序的。 如果H原子分布无序, 则一个O周围分布有4个占位度为0.5 的H原子,此时结构的对称性较高(为P63/mmc);如果分布有序,则一个O周围有两个H, 对称性为P63cm。
冰的18种晶体结构

冰的18种晶体结构冰是一种常见的物质,它存在于我们生活的各个角落中。
然而,你是否知道冰实际上存在着不同的晶体结构?下面我们将一一介绍冰的18种晶体结构。
1. 冰Ih:冰Ih是最常见的冰的结构,也是我们平常所说的冰块。
它具有六方晶体结构,每个水分子都与其他四个水分子相邻,形成一个六边形的结构。
2. 冰II:冰II是在高压下形成的一种冰的结构。
它具有四方晶体结构,水分子排列更加紧密,形成一个立方体的结构。
3. 冰III:冰III是在更高的压力下形成的一种冰的结构。
它具有同样的六方晶体结构,但水分子的排列更加紧密,相邻的水分子之间的距离更近。
4. 冰IV:冰IV是在更高压力下形成的一种冰的结构。
它具有六方晶体结构,水分子排列更加紧密,相邻的水分子之间的距离更近。
5. 冰V:冰V是在更高压力下形成的一种冰的结构。
它具有六方晶体结构,水分子排列更加紧密,相邻的水分子之间的距离更近。
6. 冰VI:冰VI是在更高压力下形成的一种冰的结构。
它具有六方晶体结构,水分子排列更加紧密,相邻的水分子之间的距离更近。
7. 冰VII:冰VII是在更高压力下形成的一种冰的结构。
它具有六方晶体结构,水分子排列更加紧密,相邻的水分子之间的距离更近。
8. 冰VIII:冰VIII是在更高压力下形成的一种冰的结构。
它具有六方晶体结构,水分子排列更加紧密,相邻的水分子之间的距离更近。
9. 冰IX:冰IX是在更高压力下形成的一种冰的结构。
它具有六方晶体结构,水分子排列更加紧密,相邻的水分子之间的距离更近。
10. 冰X:冰X是在更高压力下形成的一种冰的结构。
它具有六方晶体结构,水分子排列更加紧密,相邻的水分子之间的距离更近。
11. 冰XI:冰XI是在更高压力下形成的一种冰的结构。
它具有六方晶体结构,水分子排列更加紧密,相邻的水分子之间的距离更近。
12. 冰XII:冰XII是在更高压力下形成的一种冰的结构。
它具有六方晶体结构,水分子排列更加紧密,相邻的水分子之间的距离更近。
为什么冰是冷的?

为什么冰是冷的?
为什么冰是冷的?
冰是冷的主要是因为它的分子结构和物理性质决定了它能够吸收和储存热量的能力较低。
首先,让我们了解冰是如何形成的。
当水的温度降低到0摄氏度以下时,水分子开始减慢运动并逐渐聚集在一起形成冰晶体。
冰晶体的结构是由水分子以规律的方式排列而成,形成了一个稳定的晶格结构。
这种晶格结构导致冰的密度比液态水低,因此冰能够浮在水面上。
同时,冰晶体的结构也决定了它的热传导性较差。
冰晶体中的水分子之间通过氢键相互连接,这种连接方式使得冰的分子之间有一定的间隙,隔离了热量的传递。
当我们将热量加到冰上时,由于冰的热传导性较差,热量不能够快速传递到冰晶体的内部。
相反,冰晶体表面的水分子会吸收热量并逐渐转化为液态水。
这个过程需要消耗能量,因此我们感觉到冰是冷的。
此外,冰的熔点是0摄氏度,当环境温度高于0摄氏度时,冰会吸收来自环境的热量,并逐渐转化为液态水。
这也是为什么在温暖的天气中,冰会迅速融化的原因。
总结起来,冰是冷的主要是因为它的分子结构和物理性质使得它具有较低的热传导性,无法快速吸收和储存热量。
当我们接触冰时,它会吸收我们身体的热量,使我们感觉到冷。
冰的晶体结构

冰的晶体结构冰是一种有规则结构的物质,其内部结构分为晶体结构和熔融态体结构。
晶体结构是冰中最基本的结构,冰的熔融态体结构也可以由多条晶体结构组成,它们之间存在着相互关联。
在本文中,我们将讨论冰的晶体结构。
冰的晶体结构是由水分子组成的六方晶体结构,晶体结构的形状有方形、六边形和八角形等。
水分子的结构如下:水分子由两个原子组成,一个氧原子和两个氢原子,它们以一定比例排列组成水分子。
水分子之间的排列和其相应的键的强度决定了冰的六方晶体结构,从而构成了冰的晶体结构。
水分子之间的相互作用是由电子对构成的,电子对是由水分子中氢原子和氧原子内部共享电子构成的化学键。
这些电子对之间的相互作用使冰的晶体结构具有足够的稳定性,从而使冰能够在各种环境中保持稳定。
此外,电子对之间的相互作用也使水分子之间形成有序结构,使冰能够以规则的结构形成固态。
冰晶体结构的构成有很多种,以其结构构成的冰可以分为三种:冰Ih、冰Ⅰ和冰Ⅲ。
冰Ih是均匀的六边形晶体,它的晶胞是等边六边形,晶体的半径为280pm。
冰Ih的空间群结构是P3Ⅰm,晶体具有立方晶胞结构,晶胞的边长为450 pm。
冰Ⅰ的晶胞结构类似于冰Ih,唯一的区别在于它的空间群结构为P4Ⅰm,晶胞的边长为500 pm。
最后,冰Ⅲ的空间群结构为P6Ⅰm,晶胞的边长为600 pm。
冰中的晶胞结构与它的能量有关,晶胞结构与它的热力学特性有关。
在冰中,由于水分子之间的作用,氢键的总体强度使冰的晶体结构具有一定的稳定性,从而使冰的内部能量达到最低,从而形成固态冰。
冰的晶体结构不仅决定了冰的形状,还会影响它的其他特性,例如在冰中传播的光线、电磁波等。
综上所述,冰的晶体结构由水分子形成,水分子之间的电子对构成了强大的氢键,使冰的晶体结构具有一定的稳定性,形成固态冰,并会影响冰的其他特性。
希望本文可以为读者提供有关冰的晶体结构的知识,加深理解。
冰雪知识科普

冰雪知识科普
1. 冰雪的形成:冰是由水分子在低温下结晶形成的固态形式。
当水温降至0摄氏度以下时,水分子开始缓慢地聚集并形成冰晶体。
冰晶体的形状和大小取决于环境条件和冷却速率。
2. 冰的种类:常见的冰种类包括晶状冰、霜、雪和冰柱。
晶状冰是最常见的形态,它具有六角形的晶体结构。
霜是指空气中的水蒸气直接冷凝成固态的冰晶体,通常在低温表面出现。
雪是由大量冰晶体聚集形成的降水,其形状和结构取决于温度和湿度条件。
冰柱是在悬挂物体上形成的长形冰晶体,通常出现在冷冻水管或悬崖边缘。
3. 雪花的形状:每个雪花都有其独特的形状,这是因为雪花在形成过程中受到微小的温度和湿度变化的影响。
雪花通常具有六角形的对称性,但它们的分支和细节各不相同,形成了美丽而多样化的图案。
4. 冰川:冰川是由积累在高山或极地地区的大量积雪逐渐转变而来的。
它们是巨大的冰体,在一定的压力下会流动。
冰川通过融化和冻结来响应气候变化,它们在长时间尺度上对全球水循环和海平面起到重要的影响。
5. 冰雪活动:冰雪给人类带来了许多娱乐和运动活动的机会。
滑雪、滑冰、冰球和雪橇等活动都与冰雪密切相关。
这些活动不仅能够锻炼身体,还可以提供欣赏冰雪景观的机会。
这只是冰雪知识的一小部分,希望能够为您提供一些科普信息。
1。
冰晶体的堆积方式

冰晶体的堆积方式
1 冰晶的分类
冰晶是一类自然界中存在的晶体,属于单系胞大小的晶体,一般由小于米级的一般是水分子组成。
冰晶可分为尖晶石形冰晶、条纹冰晶、柱状冰晶、花状冰晶以及混合型冰晶等几种。
2 冰晶体的堆积方式
1.尖晶石形冰晶:它以四棱状的尖晶石结构为主要特征,并以六角形的结构堆积在16个面之上,形成规则的立方体形状,被称为“尖晶石形冰晶”。
2.柱状冰晶:柱状冰晶指的是细长的立方体晶体状的冰晶,它的堆积方式如同一堆细小的条状晶体堆叠在一起,它们呈现出多种不同类型的柱状结构,如椭圆柱、四方柱以及钰形柱等。
3.花状冰晶:这种冰晶具有条状晶和尖晶石形冰晶的混合特征,可以看作具备前述兩种的完美结合版本,它的堆积方式是由多个轴尖石结构汇集在一起形成多层的花状,中心多为五方柱,半径上一层粒子是六方柱而下一层则为八方柱,形成一个多面体朝向。
4.人造冰晶:这类冰晶指的是人工制造的冰晶,它们的制备工艺比自然形成的冰晶复杂许多,以冰晶图案贴窗最为常见。
它以水与碳烟碳混合在一起,在低温下分解成多种晶体,再用体积均匀及堆积密度更高的方式堆积而成冰晶。
3 总结
冰晶可分为尖晶石形冰晶、条纹冰晶、柱状冰晶、花状冰晶等几种,它们的堆积方式也各有不同,从四棱状、六角形、多层花状结构到人造冰晶等等。
每种冰晶的形状和堆积方式都很特别,为大家展示了大自然的多彩,我们更应该尊重大自然的奇妙之处,保护好自然环境,共同创造一个美好的家园!。
最大冰晶体形成带的概念

最大冰晶体形成带的概念
最大冰晶体形成带是指在某些条件下,冰晶体在冻结过程中沿特定方向形成的一系列冰晶体。
这些冰晶体形成带通常以类似条带的形式出现,并且具有相对较大的尺寸。
冰晶体形成带的形成与冰晶生长的过程和环境条件息息相关。
一般来说,当冰晶在特定条件下形成时,例如在云中形成,或者在冰冻的湖面上形成时,冰晶体往往会沿着特定的方向生长。
这可能是由于局部的温度和湿度差异,或者由于气流等外部因素的影响。
冰晶体形成带通常在冰表面上可见,形成带的宽度和间距可以根据环境条件和冰晶生长的速度而有所不同。
在某些情况下,冰晶体形成带可以形成美丽的图案,如冰上的条纹或图案。
研究冰晶体形成带对于了解冰的形成和冰晶生长过程具有重要意义。
可以通过观察和分析冰晶体形成带的特征,来研究冰的生长速度、结晶方式、环境条件等因素。
这对于气象学、地形学和环境科学等领域具有一定的应用价值。
冰晶体

冰晶体苏春霞120150089 食品科学摘要冰是由水分子有序排列形成的结晶,水分子之间靠氢键连接在一起形成非常稀疏(低密度)的刚性结构,这一点已通过X射线、中子衍射、电子衍射、红外和拉曼光谱分析研究得到阐明。
水分子通过四面体之间的作用力结晶。
在冰中,O-O核间距0.276nm,O-O -O键角约109°。
每一个水分子能同其它4个水分子缔合(配位数4)。
关键词冰晶体氢键核间距一、冰晶体的结构形式冰中除了普通HOH外,纯冰还含有HOH的同位素变种。
在研究水和冰结构时,主要考虑HOH、H+(H3+O)和OH-。
由于H3+O和OH-的运动以及HOH的振动,冰结晶总是有缺陷的,存在于冰结晶空隙中的HOH分子能缓慢地扩散通过晶格。
冰远非是静止或均一的,其特征还取决于温度,当温度接近-180℃或更低时,所有的氢键才是完整的。
冰(H2O)有20余结构形式,通常书写为加后缀的罗马字母形式,如冰-I,冰-II,…等,罗马字母后面的h和c分别表示六方和等轴晶系,如冰-Ih、冰-Ic 等。
其中冰-Ih最为常见。
[1]1、-Ih结构在冰-Ih的结构中,每一个O原子的周围都有呈四面体状配位的4个O,O-O键长约2.76 Å,在O-O连线上只有一个H原子,键长约O--0.96 Å-- H--1.80 Å--O。
O原子周围的H原子的分布可以是无序的,也可以是有序的。
如果H原子分布无序,则一个O周围分布有4个占位度为0.5的H原子,此时结构的对称性较高(为P63/mmc);如果分布有序,则一个O周围有两个H,对称性为P63cm。
[1]冰-I h的晶体结构(P63cm),结构中H原子有序分布二、溶质对冰晶结构的影响冰中溶质的种类和数量影响冰结晶的结构。
避免极端快速冻结、溶质的性质和浓度不显著妨碍水分子运动的条件下,食品中的冰总是以最有序的六方形冰结晶形存在。
三、影响与应用1、对食品结构的影响速冻能使食品中的水分成为微小的冰晶体,对食品的结构无所损害,如果是慢慢地冷冻,水分变成大的冰晶体,对食品结构有影响。
冰晶体堆积方式

冰晶体堆积方式冰晶体堆积,也称为冰晶体结构,是一种采用面内水冻结法在水面上形成物质结构的方法。
它将水分子从单个冰晶中拆分成一个个分子,然后将它们组合在一起,形成一个物质结构。
它可以用于生产冰原材料,以及用于反应冷冻,冷藏和低温滤过技术等各种技术。
冰晶体堆积方式是采用冰晶中的晶格结构组建的,其晶格的结构非常紧密,因此可以均匀地紧凑、凝固水分子并把它们固定在面上,形成一个井然有序的结构。
组成冰晶的水分子平衡的分布在晶格的三维空间中,使得冰晶的体积更为致密,强度和耐久性也更强。
采用冰晶体堆积方式生产冰原材料,需要先用射线照射冷凝水,使其形成水晶。
接着将水晶作为基础,通过凝胶结构将其他水晶一一组合,以形成一个冰晶结构。
然后将它放入冰冻池中凝固,并将其堆积起来。
最后,冰晶体结构就被完整地固定在冰柱结构中了。
采用冰晶体堆积方式生产冰原材料时,必须保持冷凝水的凝固温度稳定,这样才能确保处于最佳状态下的冰晶堆积。
因此,采用冰晶体堆积方式生产冰原材料,一般都需要设备高档,这样才能保证水池中水分子温度在指定范围内稳定变化,这样才能保证最佳冰晶堆积效果结果。
冰晶体堆积方式还可以应用在反应冷冻、冷藏和低温滤过技术中。
冰晶体堆积的原理是,冷冻物质时,会通过晶格将其固定在水面上,并形成固态的晶体结构,以在一定的冷冻温度范围内提供最佳的冷却效果。
反应冷冻时,由于冰晶的形状可以有效地控制混合物的冷却速度,因此可以更快地完成反应。
冷藏时,冰晶体不仅可以延长食物的保质期,而且还可以有效保护食品和其他物质的组织结构,以及维持其物理和化学特性,使其不易发生腐败和氧化变质。
除此之外,冰晶体堆积方式还可以用于低温滤过,可以帮助滤过液体更快地完成滤过,并且可以有效稳定滤过过程,以达到清澈的滤过效果。
冰晶体的结构模型

冰晶体的结构模型冰晶体是一种常见的晶体形态,其结构模型为冰晶体结构。
冰晶体结构由水分子构成,每个水分子由两个氢原子和一个氧原子组成,呈V字型排列。
冰晶体结构的形成与水分子的特殊性质密切相关。
在冰晶体中,水分子以氢键相互连接。
氢键是一种弱的电荷相互作用力,在冰晶体中起到了关键的作用。
氢键使得水分子呈现出特定的排列方式,形成规则的结晶结构。
冰晶体的结构可以用三维网格来描述。
每个网格节点上有一个水分子,这些水分子按照特定规则排列。
冰晶体结构中的水分子呈现出类似六角形的排列方式,构成了冰晶体中的晶格。
冰晶体结构的稳定性与氢键的形成有关。
氢键是由水分子中的氢原子与其周围的氧原子形成的。
在冰晶体中,氢原子与相邻氧原子形成氢键,氢键的形成使得冰晶体具有较高的稳定性。
冰晶体结构的稳定性也与水分子的排列方式有关。
在冰晶体中,水分子呈现出规则的六角形排列方式。
这种排列方式使得冰晶体具有较高的密度和较强的结晶性。
冰晶体结构的形成还与温度有关。
在较低的温度下,冰晶体结构比较稳定,水分子呈现出紧密的排列方式。
随着温度的升高,冰晶体结构逐渐解离,水分子呈现出更加松散的排列方式。
冰晶体结构的形成与冰晶体的性质密切相关。
冰晶体具有较高的熔点和热容,这与其结构的稳定性有关。
冰晶体结构中的氢键对热的传导起到了重要的作用,使得冰晶体具有较好的绝热性能。
冰晶体的结构模型在科学研究和工程应用中具有重要的意义。
科学家们通过研究冰晶体结构的特点,揭示了水分子的特殊性质和氢键的形成机制。
工程师们利用冰晶体结构的特点,设计出了一系列具有特殊性能的材料和器件。
冰晶体的结构模型为冰晶体结构,由水分子构成。
冰晶体结构的形成与水分子的特殊性质和氢键的形成密切相关。
冰晶体结构具有较高的稳定性和结晶性,与冰晶体的性质和应用密切相关。
冰晶体的结构模型在科学研究和工程应用中具有重要的意义。
ice晶体结构

Ice晶体结构介绍Ice是水的固态形式,也是地球上最常见的冰。
冰的晶体结构对水分子的排列方式和相互作用进行了描述。
了解冰的晶体结构有助于我们理解水分子在冰冻、融化和相变过程中的行为。
一级标题1. 传统的冰晶体结构Ice的晶体结构依赖于压力和温度的影响。
最常见的冰晶体结构是冰Ih,它是通常意义上的冰。
冰Ih是六角晶系的,由水分子组成。
水分子中的氧原子围绕着共享的氢键形成了一个均匀排列的晶格。
2. 冰的晶格结构冰的晶格结构是由水分子的排列方式决定的。
晶格结构的不同会影响到冰的物理性质。
冰的晶格通常由一个三维的网络结构构成,其中水分子在晶体中依次排列。
3. 冰的空洞结构在冰中,由于水分子之间的氢键的形成,会形成一些空洞。
这些空洞可以用来存储其他物质,如气体和溶液。
冰的空洞结构对于某些化学反应和物质传递具有重要意义。
二级标题1. 冰的相变冰的晶体结构可以在不同的温度和压力条件下发生相变。
例如,当温度超过0摄氏度时,冰Ih会融化成液态水。
冰的相变行为在自然界和科学研究中都具有重要的意义。
2. 冰的相变与气候变化随着全球气候变暖,冰川和极地冰层的融化现象日益严重。
冰的相变过程对于气候变化的研究具有重要意义。
冰的结构变化和融化速度的研究有助于预测未来的气候变化趋势。
3. 冰的相变应用冰的相变可以应用在各个领域。
例如,在食品领域中,冰的融化可以用来调节食物的温度。
在航天工程中,冰的相变可以用来推动火箭。
4. 冰的相变研究方法研究冰的相变过程需要使用各种实验方法和数学模型。
常见的实验方法包括差示扫描量热法、X射线衍射和中子衍射。
研究冰的相变过程还需要考虑到温度和压力的变化。
三级标题1. 冰的晶体结构图示以下是冰的晶体结构的示意图:1.冰晶体由六角晶系的结构组成。
2.水分子以二维或三维的晶格排列。
2. 冰的相变温度冰的相变温度取决于压力的大小。
常见的冰Ih在常温下的相变温度是0摄氏度。
但是,在高压条件下,冰的相变温度可以更低。
冰的晶体结构是什么样的?

冰的晶体结构是什么样的?一、晶体结构的基本概念晶体是指由具有一定周期性排列的原子或分子构成的物质。
晶体结构是指晶体中原子或分子的排列方式和空间组织结构。
对于冰来说,它的晶体结构对于其性质和物理特性具有重要影响。
二、冰的晶体结构概述冰的晶体结构可以追溯到水分子的特殊构型和特性。
冰是由水分子通过氢键相互结合而形成,形成的晶体结构呈现出六边形的网格状排列。
冰的晶胞结构由氧原子和氢原子组成,形成的晶格有序而规则。
三、冰的晶体结构的详细解析1. 六边形晶系:冰的晶体结构属于六边形晶系,晶胞中有一个正六角形的平面,并且在二维空间中无限延伸。
这种排列方式赋予了冰独特的形状和结构特征。
2. 氢键:冰的晶体结构中的氢原子与氧原子之间的氢键起着关键作用。
氢键是通过氢原子与其他电负性较大的原子之间的相互作用形成的。
它使得冰的分子间距离较大,因此冰的密度比水更大。
3. 排列方式:冰的晶体结构中的水分子呈现出有序的排列方式。
每个水分子都与四个相邻的水分子形成氢键。
这种有序的排列方式导致冰具有比水更稳定的固态结构。
四、冰的晶体结构的物理特性1. 密度和体积:由于冰的晶体结构中的氢键使得分子间的距离增大,冰的密度比水更大,并且占据的体积也更大。
2. 熔点和冰的相变:冰的晶体结构使得冰具有较高的熔点。
当温度升高时,冰的晶体结构会被破坏,分子之间的氢键断裂,导致冰转化为水。
3. 透明度:由于冰的晶体结构中的排列有序并具有规则性,冰在纯净情况下具有较高的透明度。
总结:冰的晶体结构是由水分子通过氢键相互结合而形成的,呈现出六边形晶系的有序排列。
这种特殊的结构赋予冰独特的性质和物理特性。
了解冰的晶体结构对于深入理解冰的性质和应用具有重要意义。
h2o的晶体类型

h2o的晶体类型
H2O的晶体类型
H2O是水的化学式,它是地球上最常见的化合物之一。
当水以固态存在时,它可以形成不同的晶体类型。
本文将介绍H2O的三种主要晶体类型:冰Ⅰ型、冰Ⅱ型和冰Ⅲ型。
1. 冰Ⅰ型
冰Ⅰ型是最为常见的冰晶体类型,也是我们日常生活中所熟知的冰。
它是由水分子按照规则的晶格结构排列而成。
冰Ⅰ型晶体呈现出六方密堆积的结构,每个氧原子都被四个氢原子包围。
冰Ⅰ型晶体在0°C以下形成,它的晶体结构稳定,存在于大部分地球表面的冰块中。
2. 冰Ⅱ型
与冰Ⅰ型不同,冰Ⅱ型晶体在极低温下形成。
它具有更紧密的结构,每个氧原子被六个氢原子包围。
这种结构使得冰Ⅱ型晶体比冰Ⅰ型更加密集。
冰Ⅱ型晶体在-80°C以下形成,它存在于极寒地区的冰川和冰帽中。
3. 冰Ⅲ型
冰Ⅲ型是一种高压冰晶体,形成于极高压力下。
它的晶体结构与冰Ⅰ型和冰Ⅱ型有所不同,氧原子被九个氢原子包围。
冰Ⅲ型晶体在-22℃以下的极低温和极高压力下形成,可以在深海底部的冰层中找
到。
总结:
H2O的晶体类型主要有冰Ⅰ型、冰Ⅱ型和冰Ⅲ型。
冰Ⅰ型是最常见的冰晶体,存在于大部分地球表面的冰块中;冰Ⅱ型在极低温下形成,存在于极寒地区的冰川和冰帽中;冰Ⅲ型是高压冰晶体,形成于极低温和极高压力的环境中,可以在深海底部的冰层中找到。
这些不同的晶体类型都展示了水分子在不同条件下的不同排列方式,使得水在自然界中呈现出多样的形态。
最大冰晶生成带

最大冰晶生成带
最大冰晶生成带指-1至-5℃的温度范围,大部分食品在此温度范围内约80%的水分形成冰晶的温度范围。
它对冻品质量来说是一个重要的温度区间。
多数冰晶体都是在-1至-5℃间形成,最大冰晶体生成带是保证
冻结食品质量的最重要的温度区间,最大冰晶体生成带内冰晶的生成方式对食品的品质起着较大的影响,冻结时通过最大冰晶体生成带的时间短,品质好,最大冰晶体生成带内淀粉的老化速度仍较快,耐低温的微生物在最大冰晶体生成带温度范围内仍可生长繁殖,有不少食品的冰点低于-1℃,最大冰晶生成带不同。
食品是由无数细胞构成,细胞内的液体含有盐类等物质,而细胞和细胞之间,存在液体的含盐量比细胞内液体低,但温度降低时冰晶首先在这里形成随着温度逐渐降低到细胞内溶液冰点时,在细胞内才会有冰晶。
冻结速度快,细胞内、外几乎同时达到形成冰晶的温度条件,此时在细胞内、外同时产生冰晶。
这种冰晶的颗粒小,细胞内外压力一样,细胞膜稳定。
如果冻结速度慢,在细胞和细胞之间首先出现冰晶,细胞内尚未冻结的液体,由于浓度增大和饱和蒸汽压的不同,就透过细胞膜扩散到细胞间隙中去,使大部分水分冻结于细胞间隙内,形成较大的冰晶。
我们知道,水变成冰体积要增大9%,体积的增大
对外壁产生一种张力。
由于食品的细胞组织在0℃以下逐渐硬化,这种不均衡的胀力破坏了原生质膜和细胞膜,当食品解冻时,大量汁液流出,品质明显降低。
而冻结速度快,形成冰晶小,而且分布均匀,
细胞膜破损小,解冻时细胞汁液流失少,食品的品质就高。
冰中含有的氢键数

冰中含有的氢键数
在化学的研究中,氢键是一个非常重要的概念。
它是一种分子间的相互作用力,并且
在很多生物化学反应中扮演着关键的角色。
在冰中,也存在着大量的氢键。
本文将重点介
绍冰中含有的氢键数以及这些氢键的性质。
首先,我们需要了解一下冰的结构。
冰是由水分子组成的,每个水分子包括两个氢原
子和一个氧原子。
当水分子凝结时,它们会形成一种特殊的晶体结构,这种结构被称为冰
晶体。
冰晶体是由细长的六角柱组成,其中每个六角柱都是由六个水分子组成的。
在冰晶体中,每个水分子都和它附近的四个水分子形成氢键。
这些氢键将水分子连接
在一起,并且稳定了冰的结构。
通过计算可以发现,在冰晶体中,每个水分子有两个氢键
与它相连。
这是由于每个水分子有两个氢原子,它们可以与相邻的两个氧原子形成氢键。
在冰晶体中,氢键的性质也非常重要。
氢键是一种比化学键弱的相互作用力,但是在
冰晶体中,它们的作用非常显著。
由于氢键的存在,水分子在冰中会形成比较稳定的结构。
这些结构可以确保冰的结构比较稳定,并且冰的融化需要大量的热量。
此外,冰中的氢键还具有一些其他的性质。
例如,它们可以影响冰的基本物理和化学
性质,如热容和折射率。
它们还可以影响冰的表面和边界,并且决定了水和其他物质之间
的相互作用。
总之,在冰中,每个水分子都包括两个氢键,并且这些氢键对于冰的结构和性质具有
重要的影响。
通过对冰中氢键的研究,我们可以更好地理解冰的性质以及从中派生出的许
多有趣的应用。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
冰晶体
苏春霞120150089 食品科学
摘要冰是由水分子有序排列形成的结晶,水分子之间靠氢键连接在一起形成非常稀疏(低密度)的刚性结构,这一点已通过X射线、中子衍射、电子衍射、红外和拉曼光谱分析研究得到阐明。
水分子通过四面体之间的作用力结晶。
在冰中,O-O核间距0.276nm,O-O -O键角约109°。
每一个水分子能同其它4个水分子缔合(配位数4)。
关键词冰晶体氢键核间距
一、冰晶体的结构形式
冰中除了普通HOH外,纯冰还含有HOH的同位素变种。
在研究水和冰结构时,主要考虑HOH、H+(H3+O)和OH-。
由于H3+O和OH-的运动以及HOH的振动,冰结晶总是有缺陷的,存在于冰结晶空隙中的HOH分子能缓慢地扩散通过晶格。
冰远非是静止或均一的,其特征还取决于温度,当温度接近-180℃或更低时,所有的氢键才是完整的。
冰(H2O)有20余结构形式,通常书写为加后缀的罗马字母形式,如冰-I,冰-II,…等,罗马字母后面的h和c分别表示六方和等轴晶系,如冰-Ih、冰-Ic 等。
其中冰-Ih最为常见。
[1]
1、-Ih结构
在冰-Ih的结构中,每一个O原子的周围都有呈四面体状配位的4个O,O-O键长约2.76 Å,在O-O连线上只有一个H原子,键长约O--0.96 Å-- H--1.80 Å--O。
O原子周围的H原子的分布可以是无序的,也可以是有序的。
如果H原子分布
无序,则一个O周围分布有4个占位度为0.5的H原子,此时结构的对称性较高(为P63/mmc);如果分布有序,则一个O周围有两个H,对称性为P63cm。
[1]
冰-I h的晶体结构(P63cm),结构中H原子有序分布
二、溶质对冰晶结构的影响
冰中溶质的种类和数量影响冰结晶的结构。
避免极端快速冻结、溶质的性质和浓度不显著妨碍水分子运动的条件下,食品中的冰总是以最有序的六方形冰结晶形存在。
三、影响与应用
1、对食品结构的影响
速冻能使食品中的水分成为微小的冰晶体,对食品的结构无所损害,如果是慢慢地冷冻,水分变成大的冰晶体,对食品结构有影响。
鱼肉在低温下冷冻时,肌肉
纤维的水发生内冻结,冰晶体小,可以较好地保持其组织结构的完整。
[2].冰晶体形成缓慢冻结时果实中形成的冰晶体大而少,迅速冻结则果实中形成的冰晶体小而多.冰晶体大,会损坏果实的细胞组织,果实解冻时汁液会流失。
[3] 空气冷冻结冰所需时间最长(154 min),形成较大且不规则的冰晶,对虾肉组织造成不可逆破坏;液体浸没冷冻速率相对较快(5.9 min),形成的冰晶比空气冷冻的小;200 MPa的卸压超冷速冻形成的冰晶颗粒最小最均匀,冰晶形成时间最短(2.1 min),能最大限度地保持虾的品质[4]。
2、应用
目前以冰晶体为模板制备了很多材料,有很广的应用前景。
以冰晶体为模板制备钠基蒙脱石质(Na-MMT)介孔材料。
[5]以冰晶体为模板使温敏性微凝胶自组装形成纤维,分别采用冰箱冷冻和液氮冷冻的方法对1wt%浓度的PNIPAM微凝胶水分散液进行冷冻,结果发现只有在液氮冷冻形成的冰晶体模板中PNIPAM微凝胶自组装形成了纤维。
[6]
四、结论
通过对冰晶体的了解,能够更好的控制产品生产过程中条件,开发更好的产品。
使产品结构更稳定。
五、参考文献
1、秦善编著,《结构矿物学》,北京大学出版社,2011)
2、张廷序;海洋水产研究,Marine Fisheries Research , 编辑部邮箱,1981年01期
3、高经成;上海农业科技,Shanghai Agricultural Science and Technology , 编辑部邮箱,1990年01期
4、苏光明;HosahalliS.Ramaswamy;朱松明;和劲松;于勇;周民生农业工程学报,Transactions of the Chinese Society of Agricultural Engineering , 编辑部邮箱,2013年22期
5、杨魁;杨长辉;李贞;无机材料学报,Journal of Inorganic Materials , 编辑部邮箱,2011年11期
6、蒋子珺;刘晓云;张福全;查刘生;电子显微学报,Journal of Chinese Electron Microscopy Society , 编辑部邮箱,2009年03期。
