丙氨酸氨基转移酶检测方法
血清丙氨酸氨基转移酶IFCC推荐方法测定

血清丙氨酸氨基转移酶IFCC推荐方法测定1.实验原理国际临床化学学会(IFCC)推荐的紫外连续监测法。
ALTL-丙氨酸+ -酮戊二酸丙酮酸+ L-谷氨酸LDH(乳酸脱氢酶)丙酮酸+ NADH + H+L-乳酸+ NAD+ + H2O加入磷酸吡哆醛(P-5-P)是为了稳定ALT活性,避免样品中因内源性磷酸吡哆醛不足造成测定结果假性偏低。
(如心肌梗死、肝病和特别监护病人的结果)[1]2. 标本:2.1 病人准备:12小时禁食。
2.2 类型:血清,肝素或EDTA血浆。
3. 标本存放:3天内的活性损失:2~8℃保存:<10%;15~25℃保存:<17%;标本稳定性:-20℃保存至少可稳定4周。
4. 标本运输:常温条件下保存运输。
5. 标本拒收标准:标本溶血、细菌污染的标本。
6. 实验材料6.1 试剂申能ALT测定试剂盒(货号:141 27017170 1 试剂 1 6×64ml 试剂2 6×16ml)6.1.1 试剂组成试剂1(R1):Tris缓冲液pH 7.5 100mmol/LL-丙氨酸500mmol/LLDH(乳酸脱氢酶)≥1200U/L试剂2(R2):a-酮戊二酸15mmol/LNADH 0.18mmol/L磷酸吡哆醛试剂:Good’s 缓冲液pH9.6 0.7mmol/L磷酸吡哆醛0.09mmol/L6.1.2 试剂准备:试剂为即用式。
6.1.3 试剂稳定性与贮存:试剂保存于2~8℃,若无污染,可稳定至失效期。
试剂不可冰冻。
6.1.4 变质指示:当试剂有看得见的微生物生长,有浊度,或者未开盖的液体有沉淀时,表明试剂已变质,不能继续使用。
6.1.5 注意事项:试剂中含叠氮钠(0.95g/L)为防腐剂。
不可入口!避免接触皮肤及粘膜。
应采取必要的预防措施使用试剂。
6.2 校准品:使用DiaSys公司提供的TruCal U校准品对自动分析仪进行校准,具体参见生化检验校准品和质控品.SOP文件。
ALTAST测定方法

ALTAST测定方法ALT和AST是两种常用的肝功能指标,用于评估肝脏疾病和损伤程度。
本文将介绍ALT和AST的测定方法。
一、ALT(丙氨酸氨基转移酶)的测定方法:ALT是一种肝细胞特异性酶,主要存在于肝细胞的胞浆中。
当肝细胞受损或破坏时,ALT会释放入血液中,因此血液中ALT水平的升高通常与肝脏疾病相关。
ALT的测定方法一般采用酶动力学法或颜色反应法。
1.酶动力学法:这种方法是通过衡量ALT催化丙酮酸和谷氨酸互相转化的速率来测定ALT的活性。
这种方法的原理是ALT催化丙酮酸和谷氨酸生成谷草转氨酶和谷氧化酶,同时反应中NADH的消耗会导致光学密度的变化。
通过测量这种变化可以确定ALT的活性水平。
2.颜色反应法:颜色反应法是用于测定ALT浓度的常用方法,它基于谷氨酸和丙酮酸在特定条件下与ALT催化生成谷草转氨酶和谷氧化酶的反应。
这种方法通常使用的试剂盒包含了特定的底物和酶,当ALT存在时,底物与其催化生成产物,产物的浓度可以通过光度计测量。
二、AST(天冬氨酸氨基转移酶)的测定方法:AST也是一种肝脏酶,但它不仅存在于肝细胞中,还存在于心肌、肌肉、肾脏和红细胞等组织中。
因此AST的升高并不一定代表肝脏疾病,也可能与其他组织的损伤有关。
AST的测定方法与ALT类似,也有酶动力学法和颜色反应法两种常见方法。
1.酶动力学法:该方法是通过测量AST催化天冬氨酸和α-酮戊二酸互相转化的速率来测定AST的活性。
反应中,NADH或NADPH的消耗导致光学密度的变化,可以用于测量AST的活性水平。
2.颜色反应法:AST的颜色反应法原理与ALT的相似,使用特定的底物和酶,当AST存在时,底物与其催化生成产物,产物的浓度可以通过光度计测量。
这些方法虽然有一定的差异,但一般都基于底物与酶的反应原理,通过测量底物与产物的光学密度变化或者测量酶活性来确定血液中ALT和AST的水平。
综上所述,ALT和AST的测定方法主要有酶动力学法和颜色反应法两种。
丙氨酸氨基转移酶检测操作程序
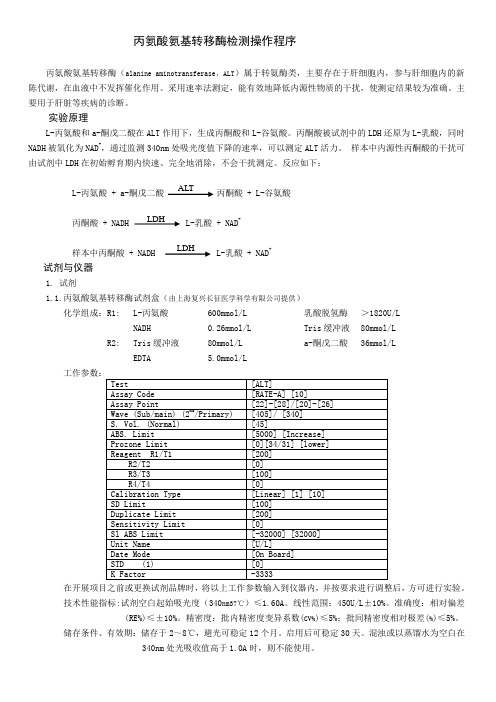
丙氨酸氨基转移酶检测操作程序丙氨酸氨基转移酶(alanine aminotransferase ,ALT )属于转氨酶类,主要存在于肝细胞内,参与肝细胞内的新陈代谢,在血液中不发挥催化作用。
采用速率法测定,能有效地降低内源性物质的干扰,使测定结果较为准确。
主要用于肝脏等疾病的诊断。
实验原理L-丙氨酸和a-酮戊二酸在ALT 作用下,生成丙酮酸和L-谷氨酸。
丙酮酸被试剂中的LDH 还原为L-乳酸,同时NADH 被氧化为NAD +,通过监测340nm 处吸光度值下降的速率,可以测定ALT 活力。
样本中内源性丙酮酸的干扰可由试剂中LDH 在初始孵育期内快速、完全地消除,不会干扰测定。
反应如下:L-丙氨酸 + a-酮戊二酸丙酮酸 + L-谷氨酸丙酮酸 + NADH L-乳酸 + NAD+样本中丙酮酸 + NADH L-乳酸 + NAD+试剂与仪器1. 试剂1.1.丙氨酸氨基转移酶试剂盒(由上海复兴长征医学科学有限公司提供)化学组成:R1: L-丙氨酸600mmol/L 乳酸脱氢酶 >1820U/L NADH 0.26mmol/L Tris 缓冲液 80mmol/L R2: Tris 缓冲液 80mmol/L a-酮戊二酸 36mmol/LEDTA5.0mmol/L在开展项目之前或更换试剂品牌时,将以上工作参数输入到仪器内,并按要求进行调整后,方可进行实验。
技术性能指标:试剂空白起始吸光度(340nm37℃)≤1.60A 。
线性范围:450U/L ±10%。
准确度:相对偏差(RE%)≤±10%。
精密度:批内精密度变异系数(CV%)≤5%;批间精密度相对极差(%)≤5%。
储存条件、有效期:储存于2~8℃,避光可稳定12个月。
启用后可稳定30天。
混浊或以蒸馏水为空白在340nm 处光吸收值高于1.0A 时,则不能使用。
ALTLDH LDH计算公式: ALT(U/L )= K= ——————————式中 TV=总反应体积(mL )SV=样本体积(mL )6.3=NADH 在340nm 处的毫摩尔吸光系数P=比色杯光径(cm )K 为工作参数表中的【K Factor 】以上是依据化学实验计算测试结果的公式,全自动分析时将工作参数(K 值)输入仪器即可。
丙氨酸氨基转移酶测定标准操作规程

丙氨酸氨基转移酶测定标准操作规程.检验原理:(酶偶联速率法)L-丙氨酸和α-酮戊二酸在丙氨酸氨基转移酶的作用下生成丙酮酸和L-谷氨酸。
丙酮酸在乳酸脱氢酶(LDH)作用下生成L-乳酸,同时还原型辅酶I(NADH)被氧化为氧化型辅酶I(NAD、在340nm处测得吸光度呈下降趋势与ALT活性成正比。
根据NADH吸光度下降程度计算丙氨酸氨基转移酶的活力单位。
试剂内不含磷酸弼哆醛。
1.-丙氨酸+Q-酮戊二酸一生→丙酮酸+L-谷氨酸丙酮酸+NADH+H,侬->L一乳酸+MUT3.2225828°C48-20°C保存7天,样本不可反复冻融!4.检验方法;仪器法(详见DF-603/DI-600标准操作规程)5.参考范围:6 .检验结果的解释:6.1 样本含量超出线性范围时,建议用0.9%(W∕V)的氯化钠溶液稀释样本。
6 .2.单位换算:ukat∕L=U∕L×16.67×10^37 .检验方法的局限性7.1 结果的准确性依赖于仪器的校正和测定温度、时间的控制。
7. 2若试剂浑浊,或以水空白在34Onnl处吸光度小于LOOO时不能使用。
8.试剂性能指标8.1 试剂外观:无色或淡黄色透明液体,无悬浮物及沉淀。
8. 2装量:不低于标识值。
8. 3试剂空白吸光度:在34Onnl处,光径ICnI时,空白吸光度A21.0008 .4试剂空白吸光度变化率:在34Onm处,光径ICm时,Z∖A∕minW0.0049 .5线性区间:试剂的线性区间为[10-500]U∕L,在此线性区间内:a)线性相关系数r应不小于0.9900;b)[10-50]U/L区间内,线性绝对偏差不超过±5U/L;(50-500)U/L 区间内,线性相对偏差不超过±10%。
8. 6准确度:相对偏差应不大于±15机8. 7分析灵敏度:在34Onrn处,光径ICnl时,测量已知浓度的样品后换算成W/L的丙氨酸氨基转移酶时,吸光度变化AAU∕L∕min22XIO-48. 8批内精密度:CV≤5%8. 9批间精密度:R≤10%8. 10稳定性:(2-8)C下,原包装存放的试剂有效期为12个月.取到期后一个月的试剂进行测试,应满足1-8的要求。
丙氨酸氨基转移酶测定方法操作规程

丙氨酸氨基转移酶(ALT)测定方法操作规程【产品名称】通用名称:丙氨酸氨基转移酶(ALT)测定试剂盒(IFCC法)【预期用途】该试剂盒采用IFCC法,用于体外定量测定人血清或肝素血浆中丙氨酸氨基转移酶的活力。
【检验原理】在ALT催化下,从丙氨酸转移到2个氨基到α-酮戊二酸上,生成产物谷氨酸和丙酮酸。
后者通过乳酸脱氢酶催化下转变成乳酸,在340nm波长条件下检测到NADH吸光度下降速率,与ALT的活力成比例。
L-ALT丙酮酸+ L-谷氨酸+LDH L-乳酸+NAD++H2O【主要组成成份】R1:Tris缓冲液150mmol/LL-丙氨酸750 mmol/L乳酸脱氢酶(LDH) 1200U/LNADH 0.4mmol/LR2:α-酮戊二酸90mmol/LNADH 0.9mmol/L*不同批号试剂盒各组分请勿混用。
【储存条件与有效期】未开启的试剂盒在2℃~8℃保存有效期为一年。
试剂开瓶后应避光保存,在2℃~8℃可稳定28天。
试剂不可冰冻。
【适用仪器】迈瑞BS系列全自动生化分析仪、日立7180型全自动生化分析仪、日立7060型全自动生化分析仪、日立7600P自动生化分析仪、奥林巴斯AU400型全自动生化分析仪、奥林巴斯AU2700型全自动生化分析仪、贝克曼库尔特AU680型全自动生化分析仪。
若需自动生化分析仪应用参数,请随时和公司联系。
建议用户在不同仪器上使用本产品时,根据实验室情况进行验证。
【样本要求】新鲜血清或肝素血浆样本,采集后及时测定,应避免污染。
【检验方法】试剂准备R1:即用液体试剂R2:即用液体试剂测定条件波长340nm温度37℃分析类型动力学法反应方向下降反应操作步骤* ΔA/min=ΔA/min样本管—ΔA/min空白管* 试剂和样本量可根据不同生化分析仪要求按比例适当增减。
校准校准品类型S1:生理盐水S2:迈瑞配套校准品推荐进行2点线性校准校准周期和要求(包括但不限于以下情况)更换试剂批号时仪器关键零部件更换时室内质控失效时质控每批样品检测时,建议使用迈瑞公司提供的配套质控品进行内部质量控制。
丙氨酸氨基转移酶检测

丙氨酸氨基转移酶检测1 检验目的规范丙氨酸氨基转移酶(ALT)检测试验,确保检测结果准确性和重复性。
2 测定方法酶动力学法3 检测原理在ALT的催化下,丙氨酸的氨基转移到a-酮戊二酸,生成丙酮酸及谷氨酸。
丙酮酸与NADH在LDH的催化下反应生成乳酸和NAD+。
NADH在波长340nm有特异吸收峰,其氧化的速率与样品中ALT的活力成正比,在340nm处测定NADH 下降的速率,即可计算出ALT活性。
ALTL-丙氨酸+α-酮戊二酸丙酮酸+ L-谷氨酸LDH丙酮酸+NADH+H+ L- L-乳酸 + NAD+4 样本血清、肝素或EDTA抗凝血浆,处理方法见生化标本采集程序。
稳定性:20~25℃稳定1天4~8℃稳定7天-20℃稳定1周5 仪器和试剂5.1 仪器:美国贝克曼-库尔特DXC800、AU5811全自动生化仪、迈瑞BS800M生化分析仪。
5.2 试剂:由武汉元景商贸公司提供原装贝克曼-库尔特试剂及迈瑞公司提供的生化试剂(详见试剂说明书),超过失效期的试剂不能使用。
5.3 校准物:Rodan混合校准品,符合WHO标准,贮存、准备严格遵照其说明书。
5.4 质控物:Rodan正常值及病理值质控品,符合WHO 标准,贮存、准备严格遵照说明书。
6 校准6.1 仪器校准:每年由该仪器维修工程师参照厂方的技术规范对仪器进行一次校准。
6.2 项目校准:试剂盒在仪器上放置稳定期后;试剂批号更换后;由质控结果随时决定。
7 操作步骤上机操作,操作程序、质量控制程序见相应生化仪操作程序。
8 参考范围≤41U/L9 患者结果可报告区间4~800U/L。
10 警告/危急值未规定。
11 性能指标11.1 线形上限:△A/min为0.40,800U/L。
11.2 精密度:批内、批间CV分别为7.3%、9.2%.11.3 准确度:不准确度≤15%.11.4 总胆红素达到180umol/L时不会有明显干扰;中、重度脂血明显干扰。
12 干扰因素及变异的潜在来源12.1 血清中含有酮酸能消耗NADH,使结果偏高;血清中谷氨酸脱氢酶增高时,在有氨存在的条件下,亦消耗NADH,使结果偏高。
丙氨酸氨基转移酶测定

丙氨酸氨基转移酶测定1.原理:ALTL-丙氨酸+a-酮戊二酸丙酮酸+L-谷氨酸LOH丙酮酸+NADH+H+ L-乳酸+NAD+2.标本采集与处理:2.1受检者准备:病人必须空腹12小时,不饮酒24小时后采集血样。
2.2静脉采血:除非是卧床的病人,一般采血取坐位,从肘静脉取血,使用止血带的时间不超过1分钟,穿刺成功后立即松开止血带;2.3标本处理:2.3.1血清要迅速与血细胞分离,因红细胞中AL T比血清中AL T的浓度高。
2.3.2血清中的AL T能在室温(20—25℃)下保存24小时或者在4℃下保存1周。
2.4采血管要求:采血时要求使用一次性无菌注射器,一人一管,用后毁形,用500mg/L有效氯浸泡消毒30分钟,回收、焚烧、做好登记。
2. 5标本拒收;接收标本应检查是否符合要求(有无溶血)试管是否填写完整,对不合格标本应重新采集。
3.试剂:3.1试剂盒组成:(柏定生物工程(北京)有限公司)a-酮戊二酸15mmol/LNADH 0.18 mmol/L乳酸脱氢酶(LDH)>5000U/LTris缓冲液100 mmol/L可接受的范围内,并且结果必须在1/4pT范围内。
3.2.1质控品批号及范围:批号022431,范围*±2st和*±3s。
3.2.2保存环境:在2—8℃保存,有效期内稳定。
3.3试剂贮存及稳定性:试剂在2—8℃保存可稳定至瓶签所示失效日期;工作液2—8℃可稳定30天。
4.仪器:上海迅达公司的半自动生化分析仪XD811。
5.操作程序:5.1试剂准备:在室温中按瓶签标定的体积,定量加入新鲜去离子水,轻轻混匀至试剂完全溶解。
5.2分析参数:方法:速率法;波长340nm温度:37℃比色杯光径: 1cm 延迟时间60秒5.3操作步骤:5.4计算方法:样品中AL T活动;AL T(U/L)=A/分*FV1F= *1000=1746Vs*消光系数V1=反应总体积Vs=样品体积NADH在340㎜的毫克分子消光系数=6.36.操作性能:线性范围:0—1000U/L(37℃)如果血清中ALT活力超出范围,则用生理盐水稀释血清重做,结果乘以稀释倍数。
检验科生化丙氨酸氨基转移酶ALT测定的标准操作规程

丙氨酸氨基转移酶测定的标准操作规程【目的】体外检测血清中丙氨酸氨基转移酶(ALT )的含量。
【职责】1.实验室工作人员均应熟知并严格遵守本SOP,室负责人监督落实。
2.本SOP的改动,可由任一使用本SOP的工作人员提出,并报经下述人员批准签字:室负责人、科主任。
【标本类型及实验前准备】1.受检者的准备病人空腹12h,不饮酒24h后采集血样。
体检对象抽血前应有两周的的正常状况记录。
注意有无应用影响测试项目的药物。
此外,对于体检者,采血的季节都应做相关记录,因为样本中各项目的含量有季节性变动,为了前后比较应在每年同一季节检验。
应嘱体检对象在抽血前24小时内不做剧烈运动。
2.静脉采血除非是卧床的病人,一般在采血时取坐位。
体位影响水分在血管内外的分布,会影响测试项目的浓度。
在采血前至少应静坐5分钟,一般从肘静脉取血,使用止血带的时间不超过1分钟,穿刺成功后立即松开止血带。
【仪器设备】东芝TBA-FX8全自动生化分析仪,低速离心机一、原理谷丙转氨酶催化L-丙氨酸的氨基转移,生成丙酮酸。
丙酮酸与NADH在LDH的催化下反应生成乳酸和NAD+。
NADH在340nm处有特异吸收峰,其被氧化的速率与血清中ALT的活性成正比,在340nm处测定NADH下降速率,即可测出ALT活性。
ALTL-丙氨酸+ a-酮戊二酸丙酮酸+ L-谷氨酸LDHNADH + 丙酮酸+ H+L-乳酸+ NAD+一、试剂1.试剂本科使用上海科华生物工程股份有限公司ALT试剂盒,为液体双试剂,各组分如下:2.校准血清使用上海科华生物工程股份有限公司提供的多项校准血清或采用因数法。
按照说明书提供的样本和试剂比例计算理论因数。
校准频次:空白定标:每日需做试剂空白定标。
全点定标:试剂换批号使用时或质控结果超过规定的2SD范围,需要全点定标。
三、操作样品为血清或肝素/EDTA抗凝血浆。
本法为IFCC法。
参数见后附,附录A。
试剂参数设置、定标操作以及样本检测常规操作,见仪器操作规程。
丙氨酸氨基转移酶的测定

丙氨酸氨基转移酶的测定
丙氨酸氨基转移酶(ALT)的测定主要通过肝功能检查进行,其参考值范围为0~40U/L。
在测定前,患者需要空腹12小时,不过不同年龄及人群参考范围没有明显差异。
当丙氨酸氨基转移酶数值偏高时,通常提示肝脏受到损害。
这可能是由多种原因导致的,如不良饮食习惯、过度劳累、药物因素等。
如果同时伴随肝区不适、全身乏力、食欲下降等情况,可能存在病毒性肝炎、脂肪肝、肝硬化等疾病。
丙氨酸氨基转移酶(ALT)的测定原理是催化丙氨酸与α-酮戊二酸之间的氨基转移反应。
具体来说,ALT催化丙氨酸的氨基转移到α-酮戊二酸上,生成丙酮酸和NADH,然后NADH在LDH的催化下生成NAD+。
在上述偶联反应中,NADPH的氧化速率与样本中酶活性呈正比,因此可以通过检测NADPH的氧化速率来确定ALT的活性。
总的来说,丙氨酸氨基转移酶的测定对于评估肝脏功能具有重要意义。
如果检测到肝脏功能受损,建议前往医院就诊,由专业医生进行评估和治疗。
丙氨酸氨基转移酶测定方法

丙氨酸氨基转移酶测定方法1. 简介嘿,朋友们!今天我们来聊聊一个很重要但又有点复杂的东西——丙氨酸氨基转移酶,简称ALT。
听起来很高大上对吧?其实它就是我们身体里的一个小助手,帮忙处理氨基酸和能量。
它主要在肝脏里工作,所以如果它的水平不正常,可能就意味着我们的肝脏在“发脾气”。
你知道的,肝脏可是个“好汉”,平时默默无闻,但一出问题可就不得了了!那我们到底要怎么测定ALT呢?别急,接下来我就来为大家一一解答。
2. 测定方法概述2.1 准备工作首先,进行ALT测定之前,我们得准备好一切工具。
你可别小看这点,仪器、试剂都得准备齐全。
一般来说,你需要一个生化分析仪、血清样本、以及一些化学试剂。
这些东西可不便宜,所以我们得好好珍惜它们,别搞得一团糟哦!然后,还要记得提前告知病人一些注意事项,比如要空腹来抽血,毕竟谁也不想一边吃着早饭,一边来检测身体状况吧?2.2 样本采集说到采集样本,这可是一门艺术!我们通常从病人的手臂静脉抽取血液,像是在给他们献上“能量”似的。
抽血的时候,护士小姐姐要是笑容满面,病人肯定会感觉轻松不少。
样本采集完毕后,要及时放入试管,别让它在外面“冻”着,毕竟,ALT可不喜欢低温。
接下来,就可以送去实验室啦!3. 测定过程3.1 反应原理在实验室里,我们要用到一种化学反应来测定ALT。
这种反应可谓是“连环反应”,ALT会把氨基酸和草酰乙酸结合起来,生成丙酮酸和谷氨酸。
听起来是不是有点复杂?其实就像做菜一样,把不同的材料混合,最后得到美味的成果。
这个反应的速度,直接和ALT的浓度成正比,简单说就是——ALT越多,反应越快,结果就越明显。
3.2 数据分析反应结束后,生化分析仪会自动读取结果,别小看这个过程,可是“高科技”的体现呢!结果会以单位每升(U/L)来表示,数值越高,表示肝脏的“工作压力”越大。
这时候,医生就会根据这些数据,给出专业的建议。
比如,如果ALT高得离谱,可能就要查查肝脏有没有“生病”。
血清丙氨酸氨基转移酶测定

赖氏法(30min) 金氏法(60min) 改良穆氏法(30min) 三种方法的原理、试剂、操作步骤和酶作用温度 都相似,单位定义和标准曲线绘制方法有差异。
1. 2.
3.
国内较多采用赖氏法,其优点为: 标准曲线中两种酮酸的量客观地反映了酶作 用的实际情况; 标准曲线上单位的数字准确地反映出酶活力 的大小; 测定结果可以直接与分光光度法相比较。
赖氏法原理: 丙酮酸和α-酮戊二酸在血清ALT的作用下生成丙 酮酸和谷氨酸,在酶反应到达规定时间内,加入溶于 酸的2,4-二硝基苯肼终止酶反应,并分别与产物丙酮 酸和剩余底物α-酮戊二酸生成相应的二硝基苯腙,在 碱性条件下均呈红棕色,二者吸收光谱在505nm处差 异最大,丙酮酸苯腙的呈色强度约为α-酮戊二酸苯腙 的3倍,据此可算出丙酮酸的生成量,:
血清中也含有酮酸及LDH,可以消耗 NADH而使测定结果偏高。 对策:采用过量的NADH(终浓度 0.14~0.2mmol/L),将血清同不含α-酮戊二酸 的所有试剂一起预温,使其他副反应充分进行, 再加入α-酮戊二酸以启动酶反应,监测光吸收 的变化,可完全排除这种干扰。
定时比色法
1、严重脂血症或黄疸血清可使测定管吸光度明 显增加,检测此类标本时,应作血清对照管。 2、加入2,4-二硝基苯肼溶液后应充分混匀,使 反应完全,否则影响重复性。 3、呈色物质配制必须准确。 4、应使用外观洁白、干燥的高纯度丙酮酸钠。 5、标本测定值超过150酶活力单位时,应用生理 盐水稀释后再测。
临床意义
ALT常作为判断肝细胞损伤的灵敏指标。 1、急性病毒性肝炎,可观察病情发展,作预后 判断。 2、慢性病毒性肝炎或脂肪肝,正常或轻度增高。 3、肝硬化、肝癌时,ALT轻度或中度增高,提 示可能并发肝细胞坏死。 4、其它原因引起的肝脏损害、骨骼肌损伤、多 发性肌炎等亦可引起ALT增高。
生化检验实验赖氏法测定血清丙氨酸氨基转移酶

步骤:一.组长取5个试剂瓶贴标签注明将要装的实际名称,然后倒取试剂。
血清由老师分装后,由组长领取。
二.测定血清ALT1.取2支试管,贴标签注明组别、学号、对照管(B)和测定管(U),用微量移液器分别加0.1ml血清。
2.用移液管向U管中加入0.5ml基质缓冲液。
B管不加。
混匀后同时在水浴温箱中37℃保温30min。
作用:U管中有酶促反应,B管无。
3.用移液管向B、U管各加0.5ml 2,4-二硝基苯肼溶液。
作用:终止反应,生成显色物质。
4.用移液管向B管加入0.5ml基质缓冲液,U管不加。
混匀后在水浴温箱中37℃保温20min。
作用:保证检测条件的一致性。
5.用移液管向B、U管各加2,4-二硝基苯肼溶液作用:碱性条件,显色。
6.B、U管室温放置5min,在波长505nm以蒸馏水调零,读取吸光度。
注意:基质缓冲液和2,4-二硝基苯肼溶液的加入顺序不能颠倒A。
表13-7三.ALT标准曲线绘制1.取5支试管,贴标签标明组别、学号、序号(0、1、2、3、4)。
用移液管取0.1 mol/l磷酸盐缓冲液,各加0.1ml。
2.用移液管取2.0 mol/l丙酮酸标准液加入各试管,0管不加,1、2、3、4管各加0.05、0.10、0.15、0.20ml。
作用:代替酶促反应产物。
3.用移液管取基质缓冲液加入各试管,0、1、2、3、4管分别加0.50、0.45、0.40、0.35、0.30ml。
4.用移液管取2,4-二硝基苯肼溶液加入各试管,各加0.5ml。
5.混匀,各试管同时在水浴温箱中37℃保温20min。
6.用移液管向各试管加2,4-二硝基苯肼溶液。
7.混匀,室温放置5min,在波长505nm以蒸馏水调零,读取吸光度A。
各管吸光度减去0管吸光度为该标准管的吸光度值。
8.以吸光度值为纵坐标,对应的卡门单位为横坐标,各标准管代表的活性单位与吸光度值作图,即成标准曲线。
表13-6。
丙氨酸氨基转移酶(ALT)检测(赖氏法)规程

丙氨酸氨基转移酶(ALT)检测(赖氏法)规程原理本法系依据丙氨酸氨基转移酶(Alaurine Transaminase 缩写为ALT)与由丙氨酸及α-酮戊二酸组成的底物缓冲液产生丙酮酸及谷氨酸。
丙酮酸与2,4-二硝基苯肼作用,生成丙酮酸2,4-二硝基苯腙,在碱性溶液中显红棕色。
通过比色测定可以了解血浆中丙氨酸氨基转移酶的活力。
试剂(1)0.1mol/L磷酸盐缓冲液(pH7.4)准确称取磷酸氢二钠二水合物15.04g、磷酸二氢钾1.09g溶于实验用水中,补加实验用水至500ml。
然后用1mol/L HCl溶液或1mol/L NaOH溶液调整pH至7.4,密封保存。
(2)底物缓冲液(200mmol/L DL-丙氨酸;2mmol/Lα-酮戊二酸)精确称取DL-丙氨酸1.79g 和α-酮戊二酸29.2mg,用0.1mol/L磷酸盐缓冲液溶解并稀释至100ml,用1mol/L氢氧化钠(约0.5ml)调节pH值至7.4,密封保存。
(3)1mmol/L2,4-二硝基苯肼溶液称取2,4-二硝基苯肼19.8mg,用1mol/L浓度的盐酸溶液溶解,并稀释至100ml。
(4)0.4mol/L氢氧化钠溶液称取氢氧化钠16.0g,用实验用水溶解至1000ml。
(5)2mol/L氢氧化钠溶液称取氢氧化钠80g,用实验用水溶解至1000ml。
(6)2mmol/L丙酮酸标准液精确称取丙酮酸钠22.0mg,置于100ml称量瓶中,加0.05mol/L 的硫酸溶液溶解,然后移入100ml容量瓶中,再用0.05mol/L的硫酸溶液洗涤称量瓶三次,将洗涤液并入容量瓶中,补加0.05mol/L的硫酸溶液至容量瓶刻度,摇匀。
(7)1mmol/L丙酮酸标准液取2mmol/L丙酮酸标准液用0.05mol/L的硫酸溶液作1:1稀释测定法(1)试管法(单点定量)样品酶活力按下式计算样品酶活力(单位)=样品管吸光度值÷标准管吸光度值×标准的单位(2)试管法(标准曲线)试验前将除氢氧化钠外检测试剂预热至37℃后使用。
丙氨酸氨基转移酶测定

丙氨酸氨基转移酶测定标准操作程序(SOP )文件单位:故城县计划生育技术服务站编写者:宿金涛日期:2012年5月28日一、方法学原理丙氨酸+2-氧代戌二酸 丙酮酸+L-谷氨酸丙酮酸+NADH+H + L-乳酸+NAD ++H 2O NADH 氧化成NAD +引起340nm 处吸光度的下降,其下降速率与样品中ALT 活性成正比。
二、试剂深圳迈瑞 规格:R1:6*40mL ,R2:2*32mL ,试剂文号:粤食药监械(准)字2009第2400553号主要组成成分:试剂1(R1):Tris 缓冲液 150mmol/LL-丙氨酸 750mmol/L乳酸脱氢酶 LDH ≥1200U/L试剂2(R2):α-酮戌二酸 90mmol/LNADH 0.9 mmol/L三、仪器迈瑞BS-390生化分析仪四、样本要求不溶血血清或肝素抗凝血浆。
样品中丙氨酸氨基转移酶在2-8℃可稳定7天。
五、检验方法:测定条件:主波长 340nm温度 37℃分析类型 连续监测法检测 扣队空白杯六、操作步骤:*ΔA/min-ΔA/min 样本营-ΔA/min 空白管计算:建议使用校准品校准仪器,以吸光度变化率(ΔA/min )为Y 轴,浓度为X 轴,在生化分析仪上建立校准曲线,根据样本的ΔA/min 在校准曲线上得到相应的浓度。
七、参考范围男性 女性37℃ <40U/L <28U/L30℃ <29U/L <20U/L仅供参考,建议各实验室对此予以确认或建立所服务人群的参考值。
空白/校准/样本 20uL试剂1 200uL混匀,37℃孵育1min试剂2 50uL混匀,37℃孵育1min 后,连续测定3min 内的吸光度,计算吸光度变化率(ΔA/min)。
LDH八、用途本试剂用于人血清或血浆中丙氨酸氨基转移酶的活性测定。
丙氨酸氨基转移酶在肝脏有较高的含量,而在心、肾、骨骼肌、胰、脾、肺中则含量较少。
丙氨酸氨基转移酶活性升高可由某些与肝脏有关的疾病,如:肝硬化、肝癌、病毒性或中毒性肝炎、阻塞性黄疸等引起。
丙氨酸氨基转移酶检测原理

丙氨酸氨基转移酶检测原理
丙氨酸氨基转移酶(AST)是一种参与氨基酸代谢的酶,主要存在于肝脏、心肌、肌肉和肾脏等组织中。
检测AST活性在临床上有重要意义,可用于诊断肝病、心肌梗死等疾病,以下是AST检测的原理。
AST检测通常采用血清测定方法。
检测过程中,将患者的静脉血样本
放置于离心管中,使用离心机进行离心分离,分离出清晰的血清液。
然后将血清液样本与特定的底物反应,该底物为天然丙酮酸盐,当AST存在时,则可加速底物反应,导致丙酮酸的分解产生谷氨酸和草
酰乙酸,同时放出一定量的NADH。
在此阶段,AST活性的测定需要NADH检测,以便测量它的光学密度。
使用分光光度计测量NADH在340nm的吸收值,该值可以反映出AST的活性水平。
AST的测定结果用单位每升(U/L)来表示,其活
性值与样本血浆中AST的浓度成正比。
AST检测的正常值通常为10-40U/L,超出该范围可能表明肝细胞损伤、心肌损伤或肌肉疾病等其他健康问题。
然而,仅凭单一的AST值很难
作出诊断,因为许多其他因素也可以影响AST的水平,如摄入药物或
饮酒等。
综上所述,AST检测的原理是通过测量血清中AST的活性水平来诊断临床问题。
虽然AST值不一定反映单一的疾病,但它仍然是评估肝肾和心脏等健康状况的常用指标之一。
临床生化检验:丙氨酸氨基转移酶测定 (速率法 )

丙氨酸氨基转移酶
丙氨酸氨基转移酶(ALT)又称为谷丙转氨酶(GPT )。是转移酶类的一种,能催化双底物分子之间基团 的转移,将供体分子基团或辅酶转移给受体分子。 主要存在于各种组织细胞中,以肝细胞中含量最多。 正常时只有极少量释放入血液中,故血清ALT活性很 低。各种肝炎的急性期,药物中毒性肝细胞性坏死等 疾病时,肝细胞酶大量释放入血中,使血清ALT活性 显著增高,因此它是诊断病毒性肝炎,中毒性肝炎等 肝病的重要指标。
反应式
试剂与器材
R1试剂: Tris缓冲液 100mmol/L L-丙氨酸 500mmol/L 乳酸脱氢酶(LDH) ≥ 2000U/L NADH
R2试剂: α-酮戊二酸 15mmol/L 还原型烟酰胺腺嘌呤二核苷酸(NADH) 0.18mmol/L
标准液:79U/L 病人血清 紫外分光光度计
样品要求
丙酮酸 NADH H LDH L 乳酸 NAD
上述偶联反应中, NADH被氧化为NAD+ , NADH 的氧化速率与标本中酶活性呈正比,在340nm波长处, NADH呈现特征性吸收峰,而NAD则没有。因此,可在 340nm处连续监测到NADH的消耗量(即吸光度的下降 速率-△A/min ),从而计算出ALT活性浓度。
性能指标
1、线性范围:0-400U/L范围内,剂量-反应曲线线 性相关系数应不低于0.9900
2、准确度:误差≤±10% 3、精密度:批内变异系数<6%,批间相对极差<
8% 4、空白吸光度:以蒸馏水为空白对照(340nm;
1cm;37℃)应不小于0.9
注意事项
1.操作中必须准确加入标准液及标本量,并严格控制反应 时间,准确读数。
2.血清不宜反复冰冻保存,以免影响酶活性。血清置 4℃冰箱1周,酶活性无显著变化,不推荐冰冻保存ALT测 定标本,而宜用新鲜血清标本。草酸盐、肝素、枸橼酸盐 虽不抑制酶活性,但可引起反应液轻度混浊。血液混浊时 可影响测定结果或无法测定(如血脂过高、血清蛋白变质 等)。红细胞内ALT含量为血清中3~5倍,应避免使用溶 血标本。
ALT检测操作规程

ALT检测操作规程ALT(丙氨酸氨基转移酶)是一种存在于细胞质中的酶,广泛分布于人体包括肝脏、心脏、肾脏等组织中。
ALT是肝脏功能的重要指标之一,通过测量血液中ALT的活性,可以评估肝脏功能的健康程度。
本文将介绍ALT(丙氨酸氨基转移酶)检测操作规程(速率法)。
一、实验器材和试剂准备1.乙醚:用于准备昏迷鼠模型;2.丙酮:用于制备丙酮胺溶液;3.氯化二乙酸:用于制备氯化二乙酰胺试剂;4.丙酮胺:用于制备丙酮胺溶液;5.磷酸氢二钾溶液:用于制备缓冲液;6.氧化丙酮胺:用于制备氧化丙酮胺试剂;7.pH7.0缓冲液:用于制备反应体系;8.4-氨基硫代洪美酸:用于停止反应;9.甲醛:用于制备甲醛溶液;10.维生素C溶液:用于制备维生素C溶液;11.肝组织磷酸化酰胺:用于制备肝组织提取液;12.酶提取液:用于提取ALT酶。
二、实验步骤1.制备ALT酶提取物:(1)取新鲜动物(小鼠)肝脏组织15g,加入磷酸缓冲液5倍的体积;(2)放入冷冻机中,-20℃下保存12h;(3)取出,加入万能匀浆器中,对肝脏组织进行研磨;(4)将研磨后的肝脏组织加入毛细管离心管中,进行离心,1800r/min 离心10 min;(5)将提取液转入新的毛细管离心管中,再次离心,3000r/min 离心10 min;(6)将上清液收集至离心管中,取出备用。
2.制备标准曲线:(1)取6个试管,分别标记为A、B、C、D、E、F,一个空白试管用作对照;(2)分别加入0.1ml、0.2ml、0.3ml、0.4ml、0.5ml、0.6ml的ALT 酶提取液;(3)加入pH 7.0缓冲液,使总体积为2.0ml;(4)每个试管中加入0.2ml的氧化丙酮胺试剂;(5)按顺序加入2ml、0.2ml、2ml的维生素C溶液、氧化丙酮胺试剂和ALT提取液;(6)加入4-氨基硫代洪美酸停止反应,并立即搅拌均匀;(7)用甲醛溶液处理样品;(8)分别在0.1、0.2、0.3、0.4及0.5的浓度范围内,测定样品的吸光度。
丙氨酸氨基转移酶测定的操作规程

丙氨酸氨基转移酶测定的操作规程1、用途:测定人血清中丙氨酸氨基转移酶的活性。
2、原理:丙氨酸氨基转移酶催化L-丙氨酸的氨基转移至α-酮戊二酸,生成丙酮酸和L-谷丙酸。
乳酸脱氢酶催化丙酮酸还原的同时,将NADH氧化成NAD+。
在340nm处测定NADH吸光度的下降速率,即可计算出ALT的活力。
3、适用仪器:奥林巴斯AU480型全自动生化分析仪.4、样本要求:4.1、样本种类:新鲜无溶血血清。
4.2、样本采集:常规静脉采血约2ml,不抗凝。
置普通管中,或采用含有分离胶的真空采血管。
4.3、样本干扰:对反映吸光度有干扰的样本,包括溶血和浑浊的样本都可能影响检测结果遇上述情况建议重新采集标本。
4.4、样本保存:血清样本2℃—8℃可稳定3天,-20℃可保存1个月,忌反复冻融。
5、检测方法:5.1、试剂的准备:试剂开瓶即可使用。
5.2、检测步骤:1cm)载→测定→结果审核→报告。
5.3、校准:用K因素进行试剂空白校准,也可使用Roche公司校准品进行校准操作,当试剂更换批号、出现质控漂移、仪器做完保养后及重要零件更换时,须重新校准。
5.4、结果计算:全自动生化分析仪会自动给出检测结果。
6、参考范围:(医院应根据本地区实际情况建立自己的参考范围。
)7、注意事项:7.1、试剂具有一定的酸碱性,避免直接接触皮肤和眼睛,切勿吞咽。
7.2、使用后的器具应按照规定处理,扔入指定的垃圾箱内,不可随处乱扔,防止环境污染和二次使用。
7.3、由于运输过程产生渗液或漏夜的产品,或在运输贮存中没有按照说明书要求进行维护的试剂,不可使用。
7.4、试剂只用于体外诊断。
8、参考文献:王惠萱、李雪梅、王冈,临床检验操作手册,云南科技出版社,2008.中华人民共和国卫生部医政司,全国临床检验操作规程(第三版),东南大学出版社,2006。
陆永绥、李清华、张伟民主编,临床检验自动化仪器分析标准操作规程,浙江大学出版社,2006.。
丙氨酸氨基转移酶标准

丙氨酸氨基转移酶标准丙氨酸氨基转移酶(alanine aminotransferase,简称ALT)是一种存在于肝脏、肾脏和心脏等组织中的酶类蛋白,其在氨基酸代谢过程中发挥着重要作用。
丙氨酸氨基转移酶标准是临床检验中常用的一项指标,用于评估肝脏功能和诊断肝脏疾病。
本文将详细介绍丙氨酸氨基转移酶标准的相关知识,以帮助读者更好地理解和应用这一指标。
丙氨酸氨基转移酶标准的测定方法主要包括酶测定法和免疫学测定法两种。
酶测定法是通过测定血清中ALT的活性来评估肝脏损伤程度,常用的试剂盒包括动态酶动力学法和直接测定法。
免疫学测定法则是通过测定血清中ALT的含量来进行评估,常用的试剂盒包括酶联免疫吸附法和化学发光法。
这两种方法各有优缺点,临床上可根据具体情况选择合适的方法进行检测。
在临床实践中,丙氨酸氨基转移酶标准的正常参考范围是性别和年龄相关的。
一般来说,成年男性的正常参考范围为10-40 U/L,成年女性的正常参考范围为7-35 U/L。
对于儿童和青少年,其正常参考范围则会有所不同。
需要特别注意的是,不同实验室所用的测定方法和试剂盒可能会导致参考范围略有差异,因此在临床应用中应当结合具体情况进行判断。
丙氨酸氨基转移酶标准的升高往往与肝脏疾病相关。
肝细胞损伤会导致ALT释放入血液中,因此血清ALT活性或含量的升高往往提示肝脏损伤。
常见的引起ALT升高的疾病包括肝炎、脂肪肝、肝硬化等。
此外,一些药物、酒精、肌肉损伤等因素也可能导致ALT 升高。
因此,在临床实践中,当发现患者ALT升高时,需要结合临床症状、其他肝功能指标以及影像学检查等综合分析,以明确病因并制定相应的治疗方案。
总之,丙氨酸氨基转移酶标准是评估肝脏功能和诊断肝脏疾病的重要指标之一。
通过本文的介绍,相信读者对丙氨酸氨基转移酶标准有了更深入的了解。
在临床实践中,我们需要结合具体情况,合理选择测定方法,正确解读检测结果,并且在临床诊疗中全面考虑患者的病情,以期达到更好的诊断和治疗效果。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
丙氨酸氨基转移酶检测方法
丙氨酸氨基转移酶(ALT)是一种重要的肝脏酶,也是一种常见的生
化指标。
检测方法通常用于判断肝脏功能的健康程度和疾病的演变趋势。
下面,我们将对丙氨酸氨基转移酶检测方法进行详细的阐述。
一、常规检测方法
常规检测方法是指采用血清学方法检测ALT水平。
具体步骤如下:
1.患者空腹4~8小时。
2.采集3~5ml静脉血标本,禁止吸烟和饮酒。
3.将血样放于离心管中,进行离心处理,得到血清样本。
4.通过检测仪器检测血清ALT酶的含量。
二、生物传感器检测方法
生物传感器检测方法可以检测非常低的ALT水平,可以提供更加精确
的测试结果。
具体步骤如下:
1.准备含有具有高选择性的生物传感器的电极。
2.采集患者的静脉血标本。
3.将血样与生物传感器电极接触并依据特定的工艺条件进行分析。
4.通过仪器获得ALT的浓度明确的结果。
三、免疫学方法
免疫学方法采用免疫学技术分析ALT特定抗体的含量。
具体步骤如下:
1.准备特定的抗ALT抗体试剂。
2.采集患者的静脉血标本。
3.加入抗ALT抗体图谱,进行特异性反应,每个抗原对应一个抗体。
4.使用适当的试剂盒,对空白对照样品和样品进行ELISA测定。
5.通过光学振荡仪读取ALT特定抗体的含量并获得浓度明确的结果。
综上所述,以上列出的三种方法都是常用的丙氨酸氨基转移酶检
测方法。
针对不同的病情和检测需求选择不同的检测方法非常重要。
总之,如果您的ALT测试结果不正常,医生会建议您进一步进行了解。
您可以向医生咨询,了解其他可能涉及的测试方法和预防方法。
