高效液相色谱法原理
高效液相色谱仪的原理及应用

高效液相色谱仪的原理及应用
高效液相色谱仪(High-Performance Liquid Chromatography,HPLC)是一种常用的分析仪器,根据物质在固定相和流动相
间的相互作用差异来实现物质分离和测定的方法。
高效液相色谱的主要原理如下:
1. 样品进样:样品通过进样器注入到流动相中。
2. 流动相泵:流动相泵将流动相以一定的压力送入进样阀。
3. 进样阀:进样阀控制样品的进入量,并通过连接固定相柱。
4. 固定相柱:固定相在柱中,对流动相和待分离的样品进行分离。
5. 检测器:根据样品的特性和分离程度选择合适的检测器进行检测。
6. 数据处理器:将检测的信号转化为柱温度、流量和检测器信号等数据。
高效液相色谱仪的主要应用包括:
1. 分析化学:用于定性和定量分析化学样品中的成分。
2. 生物化学:用于分析蛋白质、核酸、多肽等生物大分子。
3. 药学:用于分析药物中的活性成分、控制药品的质量。
4. 环境分析:用于监测环境中的有机污染物和无机物质。
5. 食品分析:用于检测食品中的添加剂、残留农药和毒性物质。
高效液相色谱仪的优点包括分离效率高、分析速度快、样品容量小、样品制备简单等。
然而,高效液相色谱仪的操作要求严格,仪器费用较高,且需要使用高纯度的溶剂和试剂。
高效液相色谱法的分离原理

高效液相色谱法的分离原理(原创版)目录一、高效液相色谱法的基本概念二、高效液相色谱法的分离原理1.流动相与固定相的相互作用2.溶质在两相间的分配3.平衡时的计算公式三、高效液相色谱法的应用领域四、高效液相色谱法的常见故障及其排除方法正文高效液相色谱法(High Performance Liquid Chromatography,HPLC)是一种以液体为流动相的色谱分析方法,广泛应用于医药卫生、食品安全、环境化学等各个领域。
其分离原理主要基于溶质在固定相和流动相之间的分配,达到平衡时,服从于高效液相色谱计算公式。
在高效液相色谱法中,流动相与固定相之间应互不相溶,且具有明显的分界面。
当试样进入色谱柱后,溶质会在两相间进行分配。
在达到平衡时,溶质在固定相和流动相中的浓度会达到一定的比例关系。
通过计算公式,我们可以得到溶质在固定相和流动相中的浓度。
高效液相色谱法的应用领域十分广泛,包括但不限于医药卫生、食品安全、环境化学等各个领域。
在医药卫生领域,高效液相色谱法可以用于药物分析、药物研发和药品质量控制等;在食品安全领域,可以用于食品成分分析、添加剂检测和农药残留检测等;在环境化学领域,可以用于水质分析、土壤污染检测和空气污染监测等。
在使用高效液相色谱法过程中,可能会遇到一些常见故障,如流动相泄漏、检测器信号不稳定、色谱柱分离效果差等。
对于这些故障,我们可以采取相应的排除和解决方法。
例如,对于流动相泄漏,可以检查流动相输送管路是否破损、接头是否松动等;对于检测器信号不稳定,可以检查检测器是否受到外界干扰、信号线是否接触良好等;对于色谱柱分离效果差,可以检查色谱柱是否损坏、固定相是否流失等。
综上所述,高效液相色谱法是一种分离效果高、速度快、应用广泛的色谱分析方法。
第1页共1页。
hplc高效液相色谱法

HPLC高效液相色谱法简介高效液相色谱法(HPLC)是一种利用液体作为流动相,通过高压输液系统,将样品中的各组分在固定相和流动相之间进行分配或吸附等作用而实现分离和检测的色谱技术。
HPLC具有分离效率高、灵敏度高、选择性强、分析速度快、样品适用范围广等优点,已成为化学、生物、医药、环境等领域中最重要的分析方法之一。
本文将简要介绍HPLC的基本原理、仪器组成、常用的色谱模式和应用领域,以期对HPLC感兴趣的读者有所帮助。
一、HPLC的基本原理HPLC的基本原理是利用样品中的各组分在固定相和流动相之间的不同亲和力,使其在色谱柱内以不同的速度移动,从而达到分离的目的。
固定相是填充在色谱柱内的颗粒状物质,可以是固体或涂于固体载体上的液体。
流动相是通过高压泵送入色谱柱的溶剂或溶剂混合物,可以是极性或非极性的。
样品是通过进样器注入流动相中,并随流动相进入色谱柱。
当样品中的各组分经过固定相时,会发生吸附、分配、离子交换、排阻等作用,导致它们在固定相中停留不同的时间。
这个时间称为保留时间(retention time),通常用tR表示。
保留时间是反映样品组分在色谱柱内分离程度的重要参数,不同的组分有不同的保留时间。
当样品组分从色谱柱出口流出时,会被检测器检测到,并产生一个信号。
这个信号随时间变化而变化,形成一个色谱峰(chromatographic peak)。
色谱峰的位置反映了样品组分的保留时间,色谱峰的面积或高度反映了样品组分的含量或浓度。
将检测器信号随时间变化而绘制出来,就得到了一条色谱图(chromatogram)。
色谱图上可以看到不同的色谱峰,每个峰对应一个样品组分。
通过比较保留时间和色谱峰面积或高度,就可以对样品进行定性和定量分析。
二、HPLC仪器组成HPLC仪器主要由以下几个部分组成:溶剂供给系统(solvent delivery system):负责提供恒定压力和流速的流动相,并将溶剂混合成所需比例。
高效液相色谱法的原理

高效液相色谱法的原理高效液相色谱法(HPLC)是一种常用的分离和分析技术,它是在液相色谱法的基础上发展起来的,具有高效、灵敏、准确、快速等特点。
其原理是利用液相在固定填料上的分配作用,通过样品在流动相中的分配系数不同,实现对混合物中各成分的分离和检测。
HPLC的原理主要包括样品的进样、流动相的选择、填料的选择和柱温控制等几个方面。
首先是样品的进样。
样品通过进样装置进入流动相中,然后被输送到填料柱中进行分离。
在进样过程中,要求样品能够均匀、快速地进入流动相中,以保证分析结果的准确性。
其次是流动相的选择。
流动相是HPLC分离的关键,它可以是有机溶剂、水、缓冲液等。
不同的流动相对于不同的样品具有不同的适用性,因此在选择流动相时需要考虑样品的性质和分离的要求。
填料的选择也是HPLC分离的重要因素。
填料是HPLC柱中的固定相,它的种类和粒径大小直接影响到分离的效果。
常用的填料有C18、C8、SiO2等,它们具有不同的分离机理和适用范围,需要根据具体的分析要求进行选择。
此外,柱温的控制也对HPLC分离有着重要的影响。
柱温的升高可以提高分离效率和分辨率,减少分离时间,但也会增加柱的压力和流动相的挥发,因此在实际应用中需要综合考虑。
总的来说,HPLC的原理是通过样品在流动相和固定相之间的分配作用,实现对混合物中各成分的分离和检测。
在实际应用中,需要根据具体的分析要求选择合适的进样方式、流动相、填料和柱温控制,以达到最佳的分离效果。
通过对HPLC原理的深入了解,可以更好地应用HPLC技术进行分离和分析,为科研和生产提供准确、可靠的数据支持。
同时,不断探索和创新HPLC技术,将有助于提高其分离效率和应用范围,推动科学研究和工程技术的发展。
高效液相色谱法的原理及影响因素

高效液相色谱法的原理及影响因素高效液相色谱(High Performance Liquid Chromatography,简称HPLC)是一种在液相中进行分离和分析的高效分析技术。
它具有高分辨率、高灵敏度、良好的线性范围和广泛的适用性。
以下是关于HPLC的原理和影响因素的详细介绍。
一、高效液相色谱的原理:高效液相色谱的原理基于物质在液态流动相中的分配和吸附特性,通过调节流动相的组成和性质,控制样品成分在固定相中的分离。
高效液相色谱的基本组成包括进样器、流动相系统、柱和检测器。
1.进样器:样品通过进样器引入色谱柱中。
进样器可以分为自动进样器和手动进样器两种类型。
2.流动相系统:流动相系统由溶剂混合器、溶剂泵和压力传递系统组成。
溶剂混合器用于混合不同溶剂的比例,以制备合适的流动相。
溶剂泵用于将流动相以一定的流速送入色谱柱中,常用的泵有恒压泵和梯度泵等。
3.柱:色谱柱是高效液相色谱的核心部件。
分离是通过样品成分在柱中的相互作用和分配系数的差异实现的。
色谱柱常见的填充物包括C18、C8和氨基硅胶等,不同填充物对于不同的样品具有不同的分离效果。
4.检测器:搭配不同的检测器可以对样品成分进行定性和定量分析。
常见的检测器包括紫外可见光谱检测器(UV)、荧光检测器(FLD)、电化学检测器和质谱检测器等。
五、高效液相色谱的影响因素:高效液相色谱的分离和分析结果受多种因素的影响,包括以下几个方面:1.流动相组成:流动相的组成直接影响样品成分在固定相上的分配系数,进而影响分离效果。
流动相的成分要根据样品的性质和需要进行选择。
常用的流动相包括纯溶剂、溶剂混合物和缓冲液等。
2.流动相性质:流动相的性质包括溶液的pH值、离子强度、流速和温度等。
其中,溶液的pH值和离子强度的变化可以影响分析物的离子态,进而影响分离效果。
流速的选择要根据分析物的种类和浓度进行调整。
温度的增加可以提高分子的扩散速度,加快分离过程。
3.色谱柱:色谱柱的类型、填充物和尺寸等也对分离效果有重要影响。
高效液相色谱原理
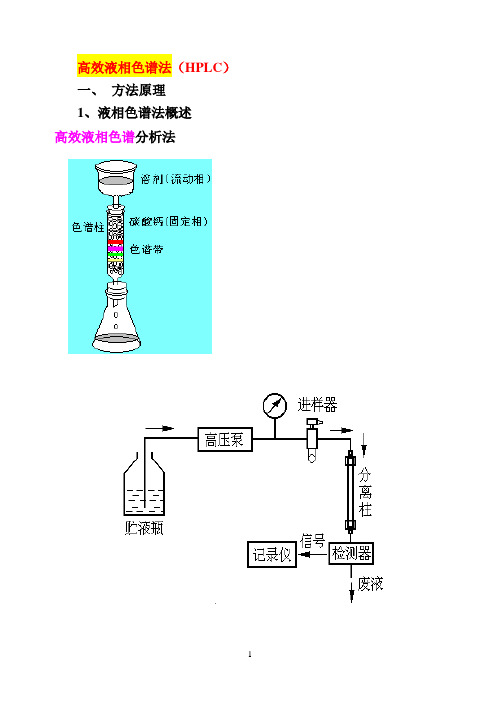
高效液相色谱法(HPLC)一、方法原理1、液相色谱法概述高效液相色谱分析法其工作流程为:高压输液泵将贮液器中的流动相以稳定的流速(或压力)输送至分析体系,在色谱柱之前通过进样器将样品导人,流动相将样品依次带入预柱、色谱柱,在色谱柱中各组分被分离,并依次随流动相流至检测器,检测到的信号送至数据处理系统记录、处理和保存。
HPLC仪器的基本结构2、高效液相色谱法的特点(HPLC)与经典柱色谱原理相同,是由液体流动相将被分离混合物带入色谱柱中,根据各组分在固定相及流动相中吸附能力、分配系数、离子交换作用或分子尺寸大小的差异来进行分离。
由于高压输液泵、高灵敏度检测器和高效固定相的使用,提高了柱效率,降低了检出限,缩短了分析时间。
特点是选择性高、分离效能高、分析速度快的特点。
高沸点有机物的分析、离子型化合物、高分子化合物、热稳定性差的化合物以及具有生物活性的物质,弥补了气相色谱法的不足。
高效液相色谱法与气相色谱法相比,各有所长,互相补充。
如果能用气相色谱法分析的样品,一般不用液相色谱法,因为气相色谱法分析速度更快、更方便、成本更低。
3、高效液相色谱法的固定相和流动相(1)固定相表面多孔型和全多孔型两大类。
(2)流动相(淋洗液)流动相的选择对改善分离效果产生重要的辅助效应。
从实用,选用的流动相具有廉价、易购的特点外,还应满足下列要求:①与固定相互不相溶,并能保持色谱柱的稳定性。
②高纯度,以防所含微量杂质在柱中积累,引起柱性能的改变。
③与所用的检测器相匹配。
④应对样品有足够的溶解能力,以提高测定的灵敏度。
⑤具有低的黏度(可减少溶质的传质阻力,提高柱效)和适当低的沸点。
⑥应避免使用具有显著毒性的溶剂,以保证工作人员的安全。
液相色谱法中常用的流动相有正己烷、正庚烷、甲醇、乙腈等。
4、高效液相色谱法的主要类型(1)液—固吸附色谱法①分离原理:基于各组分吸附能力的差异来进行混合物分离的。
②固定相:极性和非极性两种。
极性固定相:硅胶、氧化镁。
高效液相色谱仪工作原理

高效液相色谱仪工作原理高效液相色谱仪原理:在条件(流动相、固定相、温度和压力等)一定,样品浓度很低时(Cs、Cm很小)时,K只取决于组分的性质,而与浓度无关。
这只是理想状态下的色谱条件,在这种条件下,得到的色谱峰为正常峰;在许多情况下,随着浓度的增大,K减小,这时色谱峰为拖尾峰;而有时随着溶质浓度增大,K也增大,这时色谱峰为前延峰。
因此,只有尽可能减少进样量,使组分在柱内浓度降低,K恒定时,才能获得正常峰。
分配系数与组分、流动相和固定相的热力学性质有关,也与温度、压力有关。
在不同的色谱分离机制中,K有不同的概念:吸附色谱法为吸附系数,离子交换色谱法为选择性系数(或称交换系数),凝胶色谱法为渗透参数。
但一般情况可用分配系数来表示。
仪器使用:高效液相色谱法只要求样品能制成溶液,不受样品挥发性的限制,流动相可选择的范围宽,固定相的种类繁多,因而可以分离热不稳定和非挥发性的、离解的和非离解的以及各种分子量范围的物质。
与试样预处理技术相配合,HPLC所达到的高分辨率和高灵敏度,使分离和同时测定性质上十分相近的物质成为可能,能够分离复杂相体中的微量成分。
随着固定相的发展,有可能在充分保持生化物质活性的条件下完成其分离。
HPLC成为解决生化分析问题Z有前途的方法。
由于HPLC具有高分辨率、高灵敏度、速度快、色谱柱可反复利用,流出组分易收集等优点,因而被广泛应用到生物化学、食品分析、医药研究、环境分析、无机分析等各种领域。
高效液相色谱仪与结构仪器的联用是一个重要的发展方向。
液相色谱-质谱联用技术受到普遍重视,如分析氨基甲酸酯农药和多核芳烃等;液相色谱-红外光谱联用也发展很快,如在环境污染分析测定水中的烃类,海水中的不挥发烃类,使环境污染分析得到新的发展。
该仪器应用非常广泛,几乎遍及定量定性分析的各个领域。
1、分离混合物:高效液相色谱法只要求样品能制成溶液,不受样品挥发性的限制,流动相可选择的范围宽,固定相的种类繁多,因而可以分离热不稳定和非挥发性的、离解的和非离解的以及各种分子量范围的物质。
高效液相色谱HPLC基本原理

色谱柱的温度控制:优化色谱柱的 温度提高分离效率
添加标题
添加标题
添加标题
添加标题
色谱柱的维护:定期清洗和维护色 谱柱保证其性能稳定
色谱柱的填充:优化色谱柱的填充 方式提高分离效果
流动相的组成:有机溶剂和水
流动相的选择原则:根据样品性质和检测器类型选择
流动相的优化方法:通过改变有机溶剂和水的比例、改变有机溶剂的种类、改变有机 溶剂的浓度等方法进行优化
流动相的优化效果:提高分离效果、提高检测灵敏度、降低检测时间等
固定相的选择: 根据样品性质 和分离要求选 择合适的固定
相
固定相的粒径: 粒径越小分离 效果越好但会 增加压力和延
长分析时间
固定相的表面 处理:表面处 理可以提高固 定相的稳定性
和选择性
固定相的填充: 填充方式会影 响柱效和分离 效果常用的填 充方式有轴向 填充、径向填 充和螺旋填充
汇报人:
智能化:I技术在HPLC中的应用提 高分析效率和准确性
高通量:高通量HPLC技术的发展提 高分析速度和通量
添加标题
添加标题
添加标题
添加标题
微型绿色环保:环保型HPLC技术的发展 降低对环境的影响和污染
气相色谱-质 谱联用:提高 检测灵敏度和
准确性
样品采集:选择合适的样品采 集方法如抽样、取样等
样品预处理:对样品进行预处 理如过滤、离心、稀释等
样品保存:选择合适的样品保 存方法如冷藏、冷冻等
样品分析:对样品进行分析如 定性、定量等
进样器选择:根据样品性质 和实验要求选择合适的进样 器
样品准备:选择合适的样品 进行适当的处理和稀释
进样操作:将样品注入进样 器确保样品完全进入色谱柱
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
其他类型色谱法
其他类型色谱法 按分离机制分类: 液固吸附色谱法 离子色谱法 凝胶色谱法(分子排阻色谱法) (空间排阻色谱法)
液固吸附色谱实例
氯化噻吩嗪四种异构体的分离 异构体具有不同的空间排列方式,因此 吸附剂对它们的吸附能力有所不同,从 而得到了分离。
氯化噻吩嗪 四种异构体的分离色谱图
液固吸附色谱
液液分配色谱
液液分配色谱法 固定相 将特定的液态物质涂于担体表面 化学键合于担体表面而形成的有机键合层 如C18(十八烷基硅烷)、 C8(辛烷基)、氨基键合硅胶 ) 固定相类型 极性固定相:正相色谱 以极性有机基团如胺基(-NH2)、腈基(-CN)、醚基(-O-) 等键合在硅胶表面制成的 非极性固定相:反相色谱 反相色谱法最常用的固定相是C18、C8和苯基键合相的填料,在 分离极性很大的化合物时,也可以采用氨基、氰基等极性基团键 合固定相。
离子交换色谱法
离子交换色谱法 固定相:离子交换树脂,常用苯乙烯与二乙烯交联形成的聚合物骨架, 在表面未端芳环上接上羧基、磺酸基 在表面未端芳环上接上季胺基 阳离子交换树脂 阴离子交换树脂
流动相:电解质溶液、有机弱酸或有机弱酸盐溶液
+ HCO3- + SO42- + + HCO3- + CO 2- 3 + + HCO3- Cl- + HCO3- + HCO3- + + CO32-
键合相色谱—流动相
反相色谱 常见流动相 流动相洗脱强度顺序:水<甲醇<乙腈<乙醇<四氢呋喃<丙醇<二氯甲烷(与 水不混溶) 若采用含一定比例的甲醇或乙腈的水溶液作流动相,可用于分离极性化合物 若采用水和无机盐的缓冲液为流动相,则可分离一些易离解的样品,如有 机酸、有机碱、酚类等 常见固定相 反相色谱法最常用的固定相是C18、C8和苯基键合相的填料,在分离极性 很大的化合物时,也可以采用氨基、氰基等极性基团键合固定相。
分离机理实例
例:反相键合色谱中,键合相碳链越长,分离效果越好。
固定相: 固定相:C1 固定相: 固定相:C8 固定相: 固定相:C18
时间, 时间,min
1-尿嘧啶;2-苯酚;3-乙酰苯;4-硝基苯;5-苯甲酸甲酯;6-甲苯 尿嘧啶; 苯酚 苯酚; 乙酰苯 乙酰苯; 硝基苯 硝基苯; 苯甲酸甲酯 苯甲酸甲酯; 甲苯 尿嘧啶
液固吸附色谱法 固定相:吸附剂为硅胶或氧化铝,粒度5-10μm 流动相:有机溶剂 适用于分离分子量200-1000的组分,大多数用于 非离子型化合物的分离,常用于分离同分异构体。 各组分的出峰顺序 极性较小组分,吸附力较弱,容易解吸,先流出。 极性较大组分滞留作用大,后流出。 饱和烃 < 烯 < 芳烃 < 醚 < 醛酮 < 酸
键合相色谱—固定相
使用条件 为控制样品在分析过程的解离,常用缓冲液控制流动相的pH值, 但需要注意的是,C18和C8使用的pH值通常为2.5~7.5(2~8)。 太高的pH值会使硅胶溶解,太低的pH值会使键合的烷基脱落。 特点 使用过程中不流失 均一性和化学稳定性好 重现性好分离效率高 适于梯度洗脱 传质阻抗小
课程Байду номын сангаас入
液相色谱是如何完成混合物的分离? 混合物中各组分在固定相和流动 相之间会发生吸附、溶解或其他 亲和作用,这种作用存在差异, 从而使各组分在色谱柱中的迁移 速度不同得到分离
玻璃柱 色素 碳酸钙颗粒 石油醚
液液分配色谱
液液分配色谱法 实例:归一化法测定分析纯甲苯试剂的纯度 色谱柱: 4.6mm×150mm 固定相: 十八烷基硅烷键合相(ODS) 流动相: 水:甲醇=15:85
色谱类型选择
正确地选择色谱类型 尽可能多的了解样品性质 化学结构 极性和稳定程度 水中和有机溶剂中溶解度 相对分子质量的大小 熟悉各种色谱类型主要特点应用范围
色谱类型选择
液相色谱法实例
按固定相与流动相相对极性的不同,液液分配色谱可分 为哪两类方法?现在有A、B两物质,极性A>B,问在两种 液液分配色谱上的出峰顺序如何? 分离下述化合物,宜选用何种色谱方法? (A)聚苯乙烯相对分子量分布 (B)多环芳烃 (C)氨基酸 (D)Ca2+,Ba2+,Mg2+
CO32- CO32- HCO3-
Cl-
+ HCO3- + CO32- SO4 - + + HCO3- + CO32- + + HCO3- + HCO3- + HCO3- + + CO32-
CO32-
SO42- HCO3-
HCO3-
离子交换色谱法分离机理
离子交换色谱法 分离原理 树脂上可电离离子与流动相中具有相同电荷的离子及被测组分的 离子进行可逆交换而分离。 应用 离子交换色谱法主要用于分析阴,阳离子,凡是在溶剂中能够电离 的物质通常都可以用离子交换色谱法来进行分离。 分析物质 有机酸、氨基酸、多肽及核酸。
反相键合相色谱法的分离机理2 反相键合相色谱法的分离机理2
影响溶质保留的三个主要因素: 溶质分子中非极性部分的总表面积 溶质和固定相接触的总表面积愈大,保留值愈大,所以溶质的极性愈弱, 疏水性越强,保留值越大。 键合相上的烷基总面积 烷基键合固定相的作用在于提供非极性的作用表面。随着碳链的加长, 烷基的疏水特性增强,溶质的保留值也随烷基碳链长度的增加而增大。 流动相的表面张力 流动相的表面张力愈大,介电常数愈大,极性亦愈强;溶质和烷基键合 相的缔合作用愈强,流动相的洗脱强度弱,导致溶质的保留值大。
液相色谱分析法模块之
任务5 任务5 高效液相色谱法 分离原理
能力目标
理解已知分析方法中采用的色谱类型 能够正确解释色谱分离过程 能够根据组分性质选择合适的色谱类型
课程引入
归一化法测定分析纯甲苯试剂的纯度 色谱柱: 4.6mm×150mm 固定相: 十八烷基硅烷键合相(ODS) 流动相: 水:甲醇=15:85 外标法测定叶酸片中叶酸的含量 色谱柱: 4.6mm×250mm 固定相: 十八烷基硅烷键合相(ODS) 流动相: 磷酸二氢钠缓冲液:甲醇=80:20
凝胶色谱法实例
凝胶色谱(分子排阻色谱法) 油田用驱油剂聚丙烯酰胺损失量的测定? 色谱柱:150mm×46mm 固定相:二醇基键合相,孔径200A,粒径5um 流动相:甲醇/0.05mol/LNaH2PO4 1-聚丙烯酰胺 2-原油+石油磺酸盐+氯化钠
凝胶色谱分离机理
凝胶色谱:(分子排阻色谱法) 分离机理 • 以凝胶 (gel) 为固定相。它类似于 分子筛,但凝胶的孔径比分子筛要 大得多。 • 小分子量的化合物可以进入孔中, 滞留时间长;大分子量的化合物不 能进入孔中,直接随流动相流出。 • 常用于分离高分子化合物,如组织 凝胶色谱分离示意图 提取物、多肽、蛋白质、核酸等。
液固吸附色谱分离机理
液固吸附色谱法分离机理 吸附 脱附 再吸附 再脱附 … 分离过程是一个吸附 -脱附的平衡过程。
离子色谱法实例
离子交换色谱法 油田水质中的阴离子分析 固定相:薄壳型阴离子交换树脂 (3×250mm) 流动相:0.003mol·L-1 NaHCO3 / 0.0024 mol·L-1 Na2CO3
反相色谱法的分离机理1 反相色谱法的分离机理1
疏溶剂理论: 当溶质分子进入极性流动相后,即占 据流动相中相应的空间,而排挤一部分 溶剂分子; 当溶质分子被流动相推动和固定相接 触时,溶质分子的非极性部分或非极性 分子)会将非极性固定相上附着的溶剂 膜排挤开,直接和非极性固定相上的烷 基官能团相结合(吸附)形成缔合物, 构成单分子吸附层; 当流动相极性减小时,这种疏溶剂斥 力下降,会发生解缔,并把溶质分子释 放而被洗脱下来
液液分配色谱
正相色谱法 1.极性固定相 聚乙二醇、氨基与腈基键合相 2.相对非极性流动相 正已烷、环已烷 3.极性调节剂 乙醇、四氢呋喃、三氯甲烷 4.分离中等极性和极性较强化合物. 酚类、胺类、羰基类及氨基酸类 5.组分流出顺序 极性小先洗出 反相色谱法 1.非极性固定相 C18(简称ODS) 、C8 2.极性流动相 水或缓冲液 3.极性调节剂 甲醇、乙腈、四氢呋喃 4.分离非极性和极性较弱化合物 占整个HPLC应用的80%左右 5.组分流出顺序 极性大先洗出
