BC120全自动血培养系统sop
自动血培养仪的使用流程

自动血培养仪的使用流程简介自动血培养仪是一种高效、精准的实验设备,用于培养和检测微生物。
本文档将介绍自动血培养仪的使用流程,包括设备准备、样本处理、仪器设置、数据分析等方面的内容。
设备准备在使用自动血培养仪前,需要准备以下设备和材料:1.自动血培养仪:确保仪器处于正常工作状态,并且已经连接电源和网络。
2.培养皿:选择适合自动血培养仪的培养皿,并确保其完整无损。
3.样本:准备待测的血液样本,并按照标准操作进行样本采集和处理。
样本处理对于自动血培养仪的使用,合理的样本处理非常重要。
按照以下步骤进行样本处理:1.消毒:在进行任何样本处理之前,务必进行正确的消毒操作,确保无菌环境。
2.样本收集:使用合适的采样工具(如针头、血管)采集血液样本。
注意采样的时机和方法,遵循标准操作规程。
3.样本传输:将采样的血液样本转移至培养皿中。
注意避免空气进入培养皿,以免影响培养结果。
4.样本标记:为了方便追踪和识别,对培养皿上的样本进行适当的标记。
可以使用标签纸、透明胶带等方式进行标记。
仪器设置在对样本进行处理后,需要进行自动血培养仪的设置,以确保正确的操作和可靠的结果。
1.打开仪器:按照仪器的操作手册,正确地打开自动血培养仪的电源开关。
等待系统自检完成后,进入仪器的主界面。
2.选择程序:根据实验需求,在仪器的主界面上选择合适的培养程序。
可以根据样本来源、培养时间、培养条件等因素进行选择。
3.设置参数:根据实验要求,设置合适的培养参数,包括培养时间、培养温度、培养培养基等。
保证参数的准确性和合理性。
4.样本装载:将处理好的培养皿放置在自动血培养仪的样本舱中。
注意避免培养皿的碰撞和移位。
5.启动培养:在完成仪器设置后,启动自动血培养仪的培养程序。
仪器将根据设置的参数,自动进行培养和检测。
数据分析自动血培养仪在培养过程中会自动收集和分析数据,以便用户进行后续的结果分析。
以下是一些常见的数据分析方法:1.结果查看:在培养完成后,自动血培养仪会生成相关的样本报告。
血培养标准操作规

血培养标准操作规(SOP)一、采血指征:患者出现以下一种或同时具备几种临床表现时可作为血培养的重要指征:①发热(≥38 ℃)或低温(≤36 ℃),以间歇驰张型多见,革兰阴性杆菌,如大肠埃希菌引起的感染可见双峰热;②寒战;③白细胞增多(>10.0×109/ L,特别是有“核左移”时);④粒细胞减少(<1.0 ×109/ L);⑤血小板减少;⑥皮肤、黏膜出血,常见于溶血性链球菌感染的菌血症,伤寒病人第4~10天可出现玫瑰疹,斑疹伤寒第4~6天可出现暗红色斑丘血疹;⑦昏迷;⑧多器官衰竭;⑨血压降低;⑩呼吸加快(呼吸率>20/分或CO2分压<32mmHg);以及肝脾肿大;关节疼痛;C反应蛋白、内毒素、降钙素原升高等。
对新生儿可疑菌血症,还应同时做尿液和脑脊液培养。
老年菌血症患者可能不发热或体温不低,如伴有身体不适、肌痛或卒中,可能是感染性心内膜炎的重要指征。
二、标本采集时机:只要怀疑患者有血流感染的可能,在考虑使用抗菌药物之前,都应立即采集血培养标本。
若患者已行抗菌药物治疗,则应选择含有抗菌药物吸附物的培养瓶,并在下一次抗菌药物应用前采血培养。
细菌通常在寒战和发烧前1小时入血,此时为采集血培养标本进行病原菌培养的最佳时机。
三、采血的标准流程1、标本采集部位要求:从两侧上肢静脉采血,“双瓶双侧”采血培养。
必要时从下肢静脉采血做第三套血培养。
说明:不建议采集动脉血,其诊断价值不高,且增加了抽血污染的机会。
尽量避免从静脉留置导管采血培养,因其常伴有高污染率[10,11,12]。
如果必须从留置导管内采血,也应同时从外周静脉采集另外一个血培养标本以帮助阳性结果的判读(参见3.4 导管相关血流感染)。
1.1.3 血培养的次数:要求:对怀疑菌血症、真菌血症的成人患者,推荐同时或短时间间隔(10分钟内)从不同部位(如双臂)采集2~3套血培养标本,做到“双瓶双侧”。
如有必要,可同时或短时间间隔内从下肢静脉采血接种第三套培养瓶。
全自动血型及配血分析系统(AUTOVUEInnova)操作与维护管理规程

全自动血型及配血分析系统(AUTOVUEInnova)操作与维护管理规程全自动血型及配血分析系统(AUTOVUE Innova)操作与维护管理规程一、操作规程1、开机(1)打开仪器电源(2)打开电脑,启动AutoVue Innova软件,登录到常规模式,仪器初始化。
(3)初始化完成后,点击“维护”→“冲洗”→“执行”→“冲洗设置”→“蒸馏水”→“确定”,冲洗完成后,再根据上述步骤选择“生理盐水”冲洗5遍。
(4)冲洗完成后,点击“维护”→“吸头消除污染”→“执行”→“NAOH 小瓶位置”→“确定”→“执行”,完成后显示完成提示。
2、装载试剂(1)点击软件界面上的“主舱门”,等待提示打开主舱门,装载试剂和稀释板。
装载试剂时从设备中取出试剂架,将试剂小瓶轻轻翻转几次,使试剂红细胞完全混合,将试剂小瓶条码标签朝外小心放入试剂架正确位置,将瓶盖取下放在相应小瓶旁边。
稀释板平稳放在稀释台上,使左上角对齐。
(2)点击软件界面上的“抽屉”,等待提示打开抽屉,装载试剂卡。
装载时注意每张卡都要整齐排放,将贴有有效期一面朝左放置。
3、样本注册和装载(1)条形码自动扫描注册①点击软件界面的“样品”,点击“注册/装载”→“注册”→“样品”,用扫描仪依次扫描患者样品标识号信息,每个标本按照提示扫描2遍,所有标本扫描完毕,点击“发送到工作列表”。
然后点击“退出”。
②打开样品舱门,使用软件或设备上的旋转按钮将样本架旋转至适当装载位置,依次放入样本,关闭舱门,系统初始化样本转子以检查所有样本。
(2)指定位置注册①打开样品舱门,点击软件界面“样品”,点击“注册/装载”→“注册”→“样品”,选择优先级中“正常”或“急诊”,手工输入患者样品标识号信息2次,点击“发送到工作列表”。
然后点击“退出”。
②打开样品舱门,使用软件或设备上的旋转按钮将样本架旋转至适当装载位置,依次放入样本,关闭舱门,系统初始化样本转子以检查所有样本。
(3)手工装载①注册:在“样品架”界面,点击“样品”→“注册/装载”在注册模式下点击“样品”选择“优先级”(“正常”或“紧急检测”)在“实验组”中选“ABO/Rh Reverse”在“样品类型”中选择“CENTBLOOD”,在“样品”空格中输入样品号,验证2次,点击“发送到工作列表”。
医院检验中心BACTALert120全自动血培养仪操作规程及注意事项

医院检验中心BACTALert120全自动血培养仪操作规程及
注意事项
一.开机显示屏→打印机→主机→电脑自动进入监视屏幕
二、输入操作者密码
三、每日做仪器质控
四、每周做一次数据备份
五、出现断电现象,及时按关机步骤关闭计算机,来电后打开
六、每日做培养箱内温度计录
七、培养并放在室温阴凉处保存,严禁放入冰箱保存
八、每天保持仪器外表面清洁
九、每月用清洁刷清洁培养孔一次
十、每半年用酒精沙布清洁培养孔一次
十一、关机退出ESC→输入密码→F5→OFF→CD待显示屏显示根目录,关电脑主机→显示屏→打印机。
××省××市××××××医院检验科法国HORIBAABXPENTRA

××省××市×××××× 医院检验科法国HORIBA ABX PENTRA 120 RETIC全自动血细胞分析仪 标准操作程序为了促进实验室的规范管理,本检验科特制定此标准操作程序(SOP)文件。
实验室工作人员必须严格按照本SOP进行操作。
本SOP的改动,可由任一使用本仪器的工作人员提出,并报经本实验室负责人、科主任签字批准方可通过。
批准人:×××生效日:××××年××月××日仪器名称 全自动血细胞分析仪设备英文名称 AUTOMATED HEMATOLOGY ANALZER型号 PENTRA 120 RETIC技术规格 仪器体积 75.0×117.0×55.0cm仪器重量 110Kg测试原理网织红细胞:荧光染色法;白细胞:聚焦流阻抗法+化学染色法(双鞘流技术);红细胞和血小板:电阻抗法;血红蛋白:比色法测试速度 120 测试/小时光 源 高能卤素钨灯、氩离子激光系统温控 有仪器序列号 ××××××××国 别 法国制造商 HORIBA ABX出厂日期 ××××年××月设备到货日期 ××××年××月××日 设备到货状态 新设备使 用条件 环境要求 温度范围:18℃~32℃;相对湿度: <95% 电源要求 115/230V(±10%)、AC 50/60 Hz设备验收情况 合格设备启用日期 ××××年××月××日受培训人员 全体检验科工作人员代理商 ××××××××代理商维修工程师 ××××××××维修工程师联系电话/手机 ×××××××代理商联系地址 ×××××××××××××××设备安放位置 ××××××××设备当前状态 良好仪器说明书状态及存放处 良好/血液室主要负责人 ××××××××使用人 ××××××××第1节 PENTRA 120 Retic全自动血细胞分析仪的性能指标1、精密度参数CV% 范围WBC < 2.0% 4 - 10x103/μLRBC < 2.0% 3.6 - 6.2x106/μLHGB < 1.0% 12 - 18 g/dlHCT < 2.0% 36 - 54%PLT < 5.0% 150 - 500x103/μL2、线性范围参数线性范围-150WBC(x103/mm3) 0RBC(x106/mm3) 0-8.1HGB(g/dl) 0-25 HCT(%) 0-80 PLT(x103/mm3) 0-2000PLT(x103/mm3)浓缩模式下 0-45003、携带污染率项目名称WBC RBC HGB HCT PLT携带污染率< 2.0% < 0.5% < 0.5% < 2.0% < 2.0%第2节可报参数、临床意义和参考范围可报参数 参考范围 临床意义男 性 女 性红细胞计数(RBC) 106/mm34.50-6.50 4.50-6.50红细胞计数作为单一参数,诊断价值较小。
全自动血培养仪的使用流程

全自动血培养仪的使用流程1. 准备工作在使用全自动血培养仪之前,需要进行以下准备工作:•确定工作区域干净整洁,有足够的操作空间。
•检查仪器是否正常工作,包括电源是否接通、仪器是否处于待机状态等。
•准备好所需的培养基和标本。
2. 操作步骤2.1 打开仪器•按照仪器的启动流程,按下电源开关将仪器打开。
•等待仪器启动,进入待机状态。
2.2 导入样本•打开样本槽,将待测样本放入样本槽中。
•确保样本标识正确,避免样本混淆。
2.3 设置实验参数•进入仪器的设置界面,根据实验要求,设置相应的参数,如培养时间、温度等。
2.4 开始实验•点击开始按钮,仪器开始进行血培养实验。
•仪器将根据设置的参数,自动控制培养过程,包括温度控制、培养基投放等。
2.5 监测实验过程•仪器会自动记录实验过程,包括培养基的变化、细菌的生长等。
•可以通过仪器的监测界面,实时查看实验的进展情况。
2.6 实验结果分析•实验完成后,仪器会生成实验结果报告。
•可以通过仪器的结果界面,查看实验结果,并进行相应的分析和判断。
2.7 清洁和维护•实验完成后,及时清洁仪器,避免污染和交叉感染。
•定期对仪器进行维护,保持其正常工作状态。
3. 注意事项•在操作仪器时,应按照仪器的使用手册和操作指引进行操作。
•注意个人防护,包括戴手套、口罩等,避免操作时的交叉感染。
•注意仪器的维护保养,定期进行清洁和维护,保证其正常工作。
•注意样本的处理和处置,避免交叉感染和污染。
•注意实验结果的解读,结合临床情况进行综合分析。
以上是全自动血培养仪的使用流程,希望对您有帮助!。
血培养标本采集和运送SOP

• 6.血液接种到培养瓶后轻轻颠倒混匀, 以防血液凝固; • 7.填写化验单时,一定要记录每瓶的采 血时间和部位。
四、运送
• 接种后的血培养瓶应立即送往微生物实 验室(工作时间8:00~21:00)。如不能 立即送检,应放置室温下暂存,但时间 不宜超过2小时。血标本接种到血培养瓶 前或后,均不得放入冰箱冷藏或冷冻。
• 4.我院目前使用BD公司血培养系统,血培养瓶外 观和种类对照如下: • 蓝色瓶盖――需氧培养瓶 • 黄色瓶Байду номын сангаас――厌氧培养瓶 • 红色瓶盖――真菌和分支杆菌培养瓶 • 5.建议每套血培养同时接种至需氧瓶和厌氧瓶,有 利于微需氧菌和厌氧菌的检出。当厌氧菌感染不能 除外的病人,如腹部手术合并感染的病人,必须同 时做厌氧菌血培养。但如果不能满足推荐的采血量 时,应首先满足需氧瓶;
• 2. 决定拔除深静脉导管者 从独立的2个外周静脉部位,无菌采集2套血 培养,同时无菌下取出导管并剪下5cm导管 末梢送实验室(实验室采用Maki 半定量平板 滚动培养)
• 2.未留置深静脉导管或怀疑的BSI并非导管相关 • (1 )怀疑血流感染时,独立的外周静脉无菌采集2 套血培养 • (2 )当怀疑骨髓炎、脑膜炎、肺炎和肾盂肾炎合 并菌血症时,在抗菌药物使用前从不同部位抽取2套 血培养,两个来源的采血时间必须接近(建议≤5分 钟),各自做好标记; • (3) 对不明原因的发热、亚急性心内膜炎,抽取3 套血培养;心内膜炎患者起始采集的3套血培养24 小时内报告阴性,则继续采集2套血培养;
二.血培养标本采集次数
• 1.留置深静脉导管且怀疑导管相关血流感染 (CR-BSI): • 1.希望保留深静脉导管者 至少2套(1套血培养定义:从一个部位如静 脉穿刺或静脉导管所获血液的培养,不论被 接种在1个还是多个血培养瓶内)血培养,其 中至少一套来自外周静脉,另一套从导管采 集,两个来源的采血时间必须接近(建议≤5 分钟),并各自做好标记;
医院检验科完整SOP程序文件

C2、PreS1标准操作规程
C3、HBSAg标准操作规程
C4、HBSAb标准操作规程
C5、HBEAg标准操作规程
C6、HBcAb标准操作规程
C7、HBcAbIgM标准操作规程
C8、HCVIgG标准操作规程
C9、HCVIgM标准操作规程
C10、HDVAg标准操作规程
C11、HDVIgG标准操作规程
附件七临床输血申请单
附件八输血记录单
附件九输血不良反应回报单
一、科室设置
1、科室各实验室设置及负责人
2、科室人员结构
姓名
性别
出生
年月
学历
毕业院校
参加工作时间
现任职称
手机
3、科室平面图
4、检验中心工作流程图
住院病人就诊检验流程
门诊病人就诊检验流程
二、检验中心工作职责
(一)检验中心各级人员工作职责
1、检验中心主任、副主任工作职责
D26、TdT(MRD白血病残留病灶)测定标准操作规程
D27、血小板糖蛋白测定标准操作规程
D28、CD23(Ige低亲和力受体)测定标准操作规程
D29、CD95 / Fas测定标准操作规程
D30、FCM试剂配制标准操作规程
D31、Bcl-2测定标准操作规程
D32、ANNEXIN V测定标准操作规程
D33、P53测定标准操作规程
D10、铁染色标准操作规程
D11、酸性磷酸酶(ACP)染色标准操作规程
D12、红细胞渗透脆性试验标准操作规程
D13、自体溶血试验标准操作规程
D14、血清酸化溶血试验(Ham试验)标准操作规程
D15、热溶血试验(定性)标准操作规程
全自动血培养仪产品技术要求bosheng

全自动血培养仪适用范围:全自动血培养仪与伯泰细菌培养瓶配合使用,适用于临床实验室对体液样本进行体外培养,并检测其中微生物的存在。
1.1 产品型号/规格及其划分说明BST/MDSBST:微生物检测系统英文单词字头MDS:伯盛泰汉语拼音字头词字头1.2 结构组成机械结构组成:承载支架、驱动电机、传动部件、培养瓶支架、加热棒、加热风机、外观箱体;电气硬件组成:主板(工控PC)、主控制板、瓶架控制板、温度控板、温度显示和状态显示板;软件部分组成:下位机控制软件、上位机控制应用软件。
2.1 正常工作正常工作条件应满足下列要求:a) 环境温度:15℃~28℃;b) 相对湿度:30~75%;c) 电源电压:220V 50 Hz;d) 大气压力:860~1060hPa。
2.2 功能a)具有连续孵育功能。
b)自动监测和判断培养结果(培养阳性和培养阴性)。
c)培养阳性报警方式:仪器主体红灯指示和显示器培养基瓶位绿色指示灯变橙色。
d)温度失控报警:红色报警灯。
2.3 阳性培养试验全自动血培养仪对装有标准菌株的细菌培养瓶检测结果均应报告阳性。
2.4 阴性培养试验全自动血培养仪对没有装菌株的细菌培养瓶检测结果均应报告阴性。
2.5 温度准确度及波动2.5.1 全自动血培养仪温度准确度偏差应不超过± 1.5℃;2.5.2 温度波动应不超过±3.0℃。
2.6 外观全自动血培养仪外观应符合下列要求:a) 应整洁,无划痕,文字和标识清晰;b) 紧固件连接应牢固可靠,不得有松动;c) 仪器门开关自如,没有卡涩现象。
2.7 环境试验应符合GB /T 14710—2009 中气候环境组别I和机械环境组别I的要求。
2.8 电气安全应符合GB 4793.1—2007、GB 4793.9—2013、YY0648—2008中本产品适用的条款要求。
瞬态过压类别为Ⅱ类,额定污染等级为2级。
2.9 电磁兼容应符合GB/T 18268.1-2010和GB/T 18268.26-2010中本产品适用的条款要求。
SOP文件之血液培养操作标准规程

SOP文件之血液培养操作标准规程1 检验目的做疾病的病原学诊断,查找于疾病有关的病原菌以及了解与疾病的关系,指导临床治疗及预后和流行病学的调查。
2 原理使用BACT-IST黑马微生物鉴定系统,原理见鉴定系统操作规程。
3 标本要求(1)标本类型:(2)标本采集:给患者用抗生素前抽取。
见标本采集手册(3)标本储存和运输:室温放置,室温运输并立即送检。
(4)标本拒收状态:非无菌方式采集的标本。
4 容器和添加剂类型使用灭菌器皿或鉴定仪配备的血培养瓶盛放标本,不加任何防腐剂,抗凝剂。
5 试剂(1)试剂名称:革兰氏染液、氧化酶试剂、3%触酶、血平板、麦康凯平板、相关试剂等(2)试剂生产厂家:珠海贝索生物技术有限公司(3)包装规格:4X250Ml(4)试剂盒组成:试剂1:龙胆紫液试剂2:碘溶液试剂3:脱色液试剂4:沙黄溶液6设备:(1)接种针、接种环、酒精灯、(2)BACT-IST黑马微生物鉴定系统(3)、GNP-P270隔水式恒温培养箱、SW-CJ-IF超净工作台、MCO-15A三洋牌二氧化碳培养箱、0414-1台式、FA1004电子天平7 校准程序(送XX市计量质量检测研究所校准)8操作步骤(1)的分离培养:血培养瓶经12-18小时35℃孵育后,肉眼若见生长则转种血平板及麦康凯琼脂培养基,35℃培养过夜,观察结果。
菌落生长者挑取优势菌菌落做纯培养。
(若初次分离菌落单一且生长较多时可直接做鉴定)(2)涂片:取菌落涂片做革兰氏染色,确认时G+或G-以及是球菌还是杆菌(球杆菌)。
(3)细菌鉴定及药敏实验:革兰氏阴性杆菌做氧化酶试验(必要时做动力试验),氧化酶试验阳性或氧化酶试验阴性但不利用葡萄糖不产酸者使用非发酵鉴定测试板;氧化酶试验阴性者则使用肠杆菌科细菌测试板;革兰氏阳性球菌(主要是成簇或四联排列),触酶试验阳性者接种葡萄球菌、微球菌鉴定/药敏测试板;触酶试验阴性者则接种链球菌鉴定/药敏测试板。
(4)鉴定:按照鉴定仪要求调配菌液浓度,见BACT-IST 黑马微生物鉴定系统、PHOENX100全自动细菌鉴定药敏分析系统操作规程。
2120,120检验仪器SOP

SIEMENS ADVIA 2120/120 全自动血液分析仪标准操作规程(SOP )第 2 版 第 0 次修订文件类型:标准操作规程 SOP颁布日期:2013年1月1日编制:审核:审批:1仪器简介ADVIA 2120/120是原Bayer 公司在TECHNICON H 系列基础上发展起来的新型血细胞分析仪。
它采用细胞化学染色、激光二维技术和流式细胞学原理,去除了阻抗法计数血细胞的历史。
白细胞采用双通道计数;红细胞和血小板采用球形化技术,可直接测定细胞内容物的含量,可与换算结果进行比较查;二维血小板计数可基本排除小红细胞、红细胞碎片及红细胞残骸的影响;全自动网织红细胞计数,无需预处理;系统提供多达200余项参数供用户选择使用和研究。
该仪器采用集成流路板技术,取代了传统众多的夹阀和喉管。
试剂和样品采用微量化,多数试剂置于仪器内部,显得美观豪华。
2 工作原理ADVIA 2120/120血细胞分析仪有五个通道:过氧化物酶通道、红细胞/血小板通道、血红蛋白通道、嗜碱性粒细胞通道和网织红细胞通道。
2.1 过氧化物酶通道在过氧化物酶通道中,血样和过氧化物酶试剂混合后,溶解红细胞,不同的白细胞由于其胞浆中过氧化物酶活性不同,与过氧化物酶试剂反应后,染色的深浅不同。
嗜酸性粒细胞有很强的过氧化物酶活性,中性粒细胞有较强的酶活性,单核细胞次之,而淋巴细胞和嗜碱性粒细胞无此酶活性。
根据胞浆中过氧化物酶染色深浅和激光法测量的细胞大小不同,将白细胞分成嗜酸性粒细胞、单核细胞、中性粒细胞、大而未染色细胞、淋巴和嗜碱细胞,淋巴和嗜碱性粒细胞由于大小相似而不能分开。
2.2 嗜碱性粒细胞/分叶核通道在嗜碱通道中,血样和嗜碱反应试剂混合后,由于试剂中苯二甲酸和表面活性剂的作用,红细胞和血小板溶解,除嗜碱性粒细胞外,其他白细胞膜破裂而失去胞浆,根据细胞核的形状和复杂性,将白细胞分成单个核和多形核细胞,并可对中性粒细胞分叶程度进行分析。
血培养SOP

迪尔全自动血培养标准操作程序全自动血培养系统供临床实验室通过体外培养,检测人体血液或其它无菌体液中的微生物的自动化培养、检测系统。
包括“装瓶、卸瓶、结果、培养周期、历史曲线”五大功能。
仪器操作流程1、启动:按下血培养背面的“启动开关”,稍后进入血培养界面:●常见屏幕元素按钮图例可用按钮(蓝色)不可用按钮(灰色)●常见系统按钮:确定按钮-接受更改、储存数据或所输入的信息。
取消按钮-取消特定屏幕上的更改或输入的信息,保留原来的数值。
返回前一屏幕按钮-返回到前一屏幕下一屏幕按钮-转到下一有效屏幕2、主屏:显示总体统计信息,如加载的培养瓶总数、阳性培养瓶数、阴性培养瓶数、阳性匿名培养瓶数、阴性匿名培养瓶数;总体统计信息相应下面按钮,用于装瓶、卸瓶。
总体统计信息是动态的,当装瓶、卸瓶、状态改变时,相应数字会改变。
3、装瓶按下“装瓶”,含有可用单元的孵育箱抽屉的绿色指示灯会变亮;装载前检查每一个培养瓶及其底部的颜色,若有裂缝则不能使用。
当条形码输入栏光标闪烁时,通过扫描或手动键盘输入培养瓶条形码,将培养瓶瓶底插入亮灯提示的可用孵育单元。
单元指示灯缓慢闪烁确认培养瓶已被加载。
默认培养周期是七天。
装瓶状态时,必须输入条形码,瓶号出现时,单击“确认”,完成装瓶动作。
在非装瓶状态时,可以装入匿名瓶。
如果不扫描条形码而装瓶,将提示为匿名瓶;如果不按操作装瓶,当系统探测到有培养瓶装入,也提示为匿名瓶。
匿名瓶应该在移除时补充资料或用其他方法补充培养瓶资料。
否则可能丢失该瓶的信息。
装瓶扫描条形码时,如果该条形码已曾装瓶,系统将提示已装瓶,不允许再次装入。
注意培养瓶必须装入到可用单元,否则可能当废瓶处理,系统不记录数据,也没有任何提示。
加载完所有培养瓶后,关闭孵育抽屉,然后点击“确认”按钮。
4、卸瓶卸瓶模式有四种,分别为卸阳性瓶、卸阴性瓶、卸阳性匿名瓶、卸阴性匿名瓶,可卸载培养瓶所在的单元绿色指示灯会变亮,卸下指示灯指示的培养瓶,单元指示灯缓慢闪烁表明培养瓶已经卸下。
全自动血型配血系统作业指导书

全自动血型配血系统作业指导书ORTHO Auto Vue Innova全自动血型配血系统标准操作规程(一)检验项目1.ABO及RhD血型鉴定试验。
2.不规则抗体筛查试验。
3.交叉配血试验。
(二)主要试剂1.ORTHOBioVue ABO/RhD血型卡、ORTHO BioVue Coombs卡、3系3%抗体筛查细胞,3%反定细胞、蒸馏水(或去离子水)、生理盐水、BLISS液。
2.BLISS液细胞类试剂2~8℃保存,血型卡、Coombs 卡、生理盐水室温保存。
3.所有应放室温保存的试剂,注意防尘、防紫外线、防潮。
4.变质、超过效期的试剂不能使用。
(三)标本处理原始样品采集、制备、处理、检验和存放参见《输血相容性检测标本采集手册》《ABO及RhD血型鉴定试验标准操作规程》《不规则抗体筛查试验标准操作规程》《交叉配血试验标准操作规程》。
(四)仪器设备性能参数ORTHOAutoVue lnnova全自动血型配血系统性能指标见仪器使用说明书。
(五)仪器设备环境要求与使用安全措施1.仪器设备环境要求(1)空间安装要求:①将ORTHO Au-To Vue Innova全自动血型配血分析系统安放在通风良好、灰尘少的地方。
避免在过热或过冷以及日光直射的环境中。
②对于仪器的安装场所应该能够满足设备以下的参数要求:设备尺寸:75cm(深)×92cm(高)×140cm(宽);设备重量:230kg,应确保拟安装Ortho AutoVue lnnova全自动血型配血分析系统的工作台能够安全地支撑设备的总重量。
(2)运行条件:为保证仪器的正常运行,仪器必须在满足下列各条件并维持相应环境的情况下使用:①操作/环境温度:18~30℃;②操作相对湿度:20%~95%;③必须配备不间断电源(UPS),确保系统在断电的情况下能够完成试验;④电压:(100~120)/(200~240)V AC;⑤频率:50/60Hz;⑥功率:520V A;⑦保险丝:2×5.0 AT/250V(延时)。
BC120血培养仪简易操作规程

BC120血培养仪简易操作规程1.信息核对:核对申请单信息与血培养瓶上病人信息是否一致,将培养瓶的“ID号标签”帖在申请单上。
2.放瓶步骤:在主界面下,点击“放入键”,光标一般自动跳在ID号窗体内,扫描输入该培养瓶上的ID号(必输项目),屏幕上显示该瓶信息,选标本类型为血液,打开抽屉(严禁同时打开A、B两个抽屉),将培养瓶放入到抽屉中有指示灯亮起的任何空位内(插到底),会听到提示音,指示灯会闪烁,放瓶界面重新回到空白界面,同时在申请单上写上位置号:“注意是放的A箱还是B箱,例如放在A箱11号位置,则写为“A#11”,可继续放瓶,放完之后点击结束键,关闭抽屉,完成此操作。
3.取瓶步骤:当有阳性瓶或阴性瓶时,依据位置号找到检验申请单,主界面下点击“取阳瓶”/“取阴瓶”健,屏幕会显示每个箱体内阳性瓶/阴性瓶的数量。
打开抽屉,相应阳性/阴性瓶位指示灯的绿灯会亮起,依次取出,然后关闭抽屉,完成此操作。
4.常见问题及处理:(1)问题瓶的处理:放好瓶后,主界面上显示瓶子上标记问号“?”,可能是原因:“未扫描瓶子ID号直接放入,扫描信息不当,放入后又改变位置,仪器原因”。
单击该“问题瓶”的图标,点击右下角,查看/修改信息:①如该瓶放入放入时间不久(<0.2天),则将该瓶的结果由“在检测”改为“阴性”,保存修改并退出,按“取阴瓶”操作取出该瓶,核对申请单,重新执行放瓶操作并记录位置号;②如重新放瓶时提示“ID号重复”,则在单击“查询”,在出现的界面上直接点“查询”,或者在对话框中输入该瓶的ID号,找到该瓶的记录信息,仔细核对无误后删除该瓶信息,返回主界面,重新放瓶。
③如该瓶放入时间过长,则不用处理等待该瓶报告阴性后取出。
(2)不小心退出系统:全自动血培养控制系统V1.0,用户名和密码均为“admin”进入软件主界面,测量孔颜色信息:灰色<空置>,蓝色<在培养>,黄色<阳性>,绿色<阴性>。
微生物实验室SOP文件

微生物实验室SOP文件目录01 试剂贮存和配制区工作制度02 标本处理区工作制度03 细菌自动分析区工作制度04 试剂贮存和配制区标准操作程序05 标本处理区标准操作程序06 细菌自动分析区标准操作程序07 紫外消毒标准操作程序08 消毒液配制使用标准操作程序09 普通冰箱使用标准操作程序10 超低温冰箱标准操作规程11 洁净工作台使用操作规程12 VITEK32型自动分析系统标准操作程序13 移液器使用标准操作程序14 高速离心机操作标准操作程序15 冰箱维护和保养标准操作程序16 电热恒温水浴箱操作程序17 洁净工作台维护和保养程序18 可移动紫外消毒车使用操作程序19 加样器校准标准操作程序20 离心机维护保养操作程序21 温度计校准程序22 试剂的质检操作程序23_微生物实验室岗位职责(暂行)24 临床标本的保存程序25 普通培养阴性操作程序26 真菌培养阴性操作程序27 苛养菌培养阴性操作程序28 抗酸杆菌培养阴性操作程序29 支原体培养检验操作程序30 临床检验及收费程序31 微生物检验收收费价格01、标本处理区工作制度进入本区需穿工作服、工作鞋。
本区只能进行:临床标本的保存,标本接种、培养、及其菌株检验前处理、菌悬液制备、染色标本检查、非上机鉴定与药敏试验操作等危险操作,其它操作不得在此区进行。
在整个本区的实验操作过程中,操作者必须戴手套、口罩和帽子,严格按照操作规程进行。
工作结束后必须立即对工作区进行清洁或消毒。
非本实验室工作人员未经允许不得进入。
02、试剂配制和无菌区工作制度进入该区需穿专用工作服和工作鞋.本区只能进行贮存试剂的制备、试剂的分装和平板的制备.在整个本区的实验操作过程中,操作者必须戴手套和帽子,严格按照操作规程进行。
工作结束后必须立即对工作区进行清洁和消毒.非本实验室工作人员未经允许不得进入。
无菌室公能用于分装培养管或倒制平板培养基操作。
使用前以紫外灯消毒至少30分钟,定期用乳酸熏蒸,彻底消毒。
血液透析-----SOP的解读
• 执行SOP的最终目标是:提高工作质量
第二页,共39页。
为何需要SOP?
有助于指挥和领导
工作难度大为降低; 错误减少
执行者顺利完成任务
SOP 优点
有助于沟通; 节省工作时间
有助于经验传承
为工作引入稳定性
第三页,共39页。
2、SOP的基本特征
SOP是一种程序 SOP是一种操作程序
SOP是一种标准的操作程序
第二十六页,共39页。
导管全身感染的处理
留取血培养
根据检验结果
如果发热寒战 不能控制
做细菌学检查。
给予相应的抗菌素治疗
应拔掉深静脉导管
第二十七页,共39页。
1
导管感染的预防
✓ 最好的预防:避免不必要的留置导管,增加AVF
第二十八页,共39页。
导管感染的预防
2
✓ 人员定期学习和评估相关导管感染的知识和指 南
第四页,共39页。
SOP的特征
SOP是一种程序 是对一个过程的描述,不是对一个结果的描 述。是流程下面某个程序中控制点如何来规 范和实现的程序
第五页,共39页。
SOP的特征
SOP是一种操作程序 SOP首先是一种操作层面上的东西,是实实在 在的,具体可操作的,不是理念层次上的东西
第六页,共39页。
1.每天自我检查内瘘,触摸 有无震颤感觉。 2.避免压迫。 3.瘘管上方关节勿过度弯曲
勿穿过紧的衣物或过紧护腕 勿再建立瘘管的手臂戴手表
4.提重物时(>5Kg),勿压 迫在瘘管局部。 5.控制体重和血压。 6.避免在瘘管处量血压,打 针及抽血。 7.避免抽烟。 8.注意肢体保暖。
第十九页,共39页。
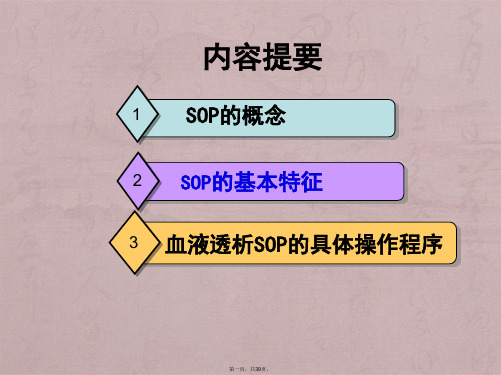
内容提要
1 SOP的概念 2 SOP的基本特征 3 血液透析SOP的具体操作程序
血常规SOP文件

全自动血细胞分析SOP一,检验目的及原理1,目的:用BC-3000 Plus全自动血细胞分析仪,在临床和实验室定量分析血液细胞,对人体的血液中三种有形成分(红细胞,白细胞,血小板)的19项参数和3个直方图进行对患者和健康人群来讲,观察有无各种原因引起的贫血,出血和失血,目前机体有无细菌及病毒感染,可筛查出各种血液病,如白血病,血小板减少性紫癜等。
2,原理:电阻法测量的血样先用稀释液进行指定比例的稀释,用以测量WBC、RBC、PLT 和HGB等参数。
WBC、RBC 计数池的稀释标本在负压作用下,分别通过各自的计数微孔,流入管道,通过两个光电传感器,在这两个光电传感器之间的液量就是仪器分析计数的标本量。
用阻抗法测量WBC、RBC 和PLT 的体积分布和数目。
电极插在液体中计数微孔的两边,在计数微孔的两边周围建立了一个电场环境,根据血细胞非传导性的性质,当有细胞通过计数微孔时,将引起阻抗的变化,阻抗变化的大小与细胞体积成正比。
WBC根据体积的大小,它有多种形态,由于稀释液、溶血剂和溶血时间的不同,WBC的体积大小会发生变化。
在一定的程序控制下,显示出WBC 的三分类——淋巴细胞、中间细胞(嗜酸+嗜碱+单核)和中性粒细胞。
被稀释的血样加入溶血剂后,红细胞溶解,释放出血红蛋白,血红蛋白与溶血剂结合形成复合物,用波长525nm 的单色光在WBC计数池内测定此化合物的透过光强,用这个透过光强与空白状态的透过光强相比较,得到血红蛋白浓度(空白状态是指WBC计数池中只有稀释液的状态)。
二,标本1,标本种类:末梢血为200-300微升,静脉血2毫升。
2,采集标本容器及添加剂:容器:末梢血为一次性朔料试管,静脉血为真空采血管。
添加剂:不同实验使用不同的抗凝剂,不能互相代替。
血常规用EDTA-k2抗凝。
3,采集方法:毛细血管采集或静脉穿刺采集。
采集时间:患者随到随时采集。
4,标本运送:标本采集后,应及时送检。
5,标本接受:标本的编号与化验单上的编号要一致,清楚,正确及完整。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
BC120全自动血培养系统
(一)检测原理
安图BC120系统中所使用的每一血培养瓶內底部都含有颜色感应器,其中有半滲透性硅胶膜隔离了培养基及颜色感应器,只有CO2可透过硅胶膜。
当血液培养瓶內有微生物生长时,释出的CO2滲透至感应器经水饱和后,产生氢离子(H)改变感应器酸碱度值,使感应器颜色产生变化,从灰色变为黄色,由颜色变化计算有无微生物生长。
反应如下:CO2+H2O→H2CO3→H+HCO3–。
孵育箱內, 每一测试槽底部都有一组激光器及反射光感应器,反射光感应器随瓶底颜色感应器颜色改变,产生不同的反射值。
光度信息经扩大、传送至电脑后,系统会自动连续分析及记录,然后判断阳性或阴性;系统随之以图象及声音报警。
电脑有下列三种阳性生长计算图表:如下图所示:
1、加速度法;培养瓶放入孵育箱时细菌还未生长;
2、速率法;培养瓶放入孵育箱时细菌正在生长期;
3、阈值法;培养瓶放入孵育箱前已经阳性;4.手工修改
(二)操作步骤
1.开机步骤:插上电源,打开仪器的UPS电源,待UPS亮灯稳定后,再打开仪器的电源开关(仪器开关在仪器的背面),程序会正常启动,登陆安图全自动血培养控制系统V1.0,进入软件主界面(用户名和密码均为“admin”)。
2.放瓶步骤:在主界面下,点击“放入键”,将光标放置在ID号窗体内,输入该培养瓶上的ID号(可手工和扫描输入,为必输项目),和对应的病人信息(可选项目)。
打开抽屉,将培养瓶放入到抽屉中有指示灯亮起的任何空置空位内,会听到提示音,指示灯会闪烁,放瓶界面重新回到空白界面,可继续放瓶,放完之后点击结束键,关闭抽屉,完成此操作。
3.取瓶步骤:在培养过程中:当有阳性瓶或阴性瓶时,可按下述步骤操作:主界面下点击“取阳瓶”/“取阴瓶”健,屏幕会显示每个箱体内阳性瓶/阴性瓶的数量。
打开血培养主机抽屉,相应阳性/阴性瓶位指示灯的绿灯会亮起,可依次取出,然后关闭抽屉,完成此操作。
4.信息查询和统计:
4.1培养瓶信息查询:主界面下单击某个有血培养瓶的图标,可查看该处血培养瓶的ID、病人信息、位置。
培养天数、报阳时间、报阳类别(1.加速度法,2。
速率法,3.阈值法,4,人工修改);主界面下双击某个有血培养瓶的图标,可查看该瓶的生长曲线。
4.2数据信查询和统计:主界面下点击“查询”健可按照条件查询本仪器所完成的所有实验;查询一定时期内的结果可进行统计分析其:阴阳性比率、培养基占用比、报阳时间率,并以图形反应。
5.仪器设置:在主界面下点击“设置”健可对数据库进行备份和还原、数据字典(输入医院病人类型、病区、科室、医生等)为放瓶时信息选择。
6.校准:主界面下单击“校准”健,屏幕上需要校准的仪器测量空位会出现一个“◇”标志,单击需要校准的空位,单击由灰色变黑色的“开始校准”健,将安图公司提供的校准棒的“4”端插入到对应的孔位中,插到底部,点击界面的标识“4”等待2秒钟,听到“滴”声后取出,依照上述步骤完成3到1的校准,校准完成后校准的孔位将原“◇”标志消失,可恢复使用。
(三)血培养标本的采集:
1采集指征:出现下述中一种或几种应视为血培养的指征:发热(间歇弛张热)、寒战、白细胞增多(>10,特别是有核作移时)、粒细胞减少(<1.0)、血小板减少、皮肤、黏膜出血、昏迷、多器官衰竭、血压下降、呼吸加快、肝脾肿大、关节疼痛、CRP(内毒素、降钙素原)升高等等;
2采集时间:抗菌药物使用前(或用抗菌药物吸附培养瓶),寒战和发热前1小时;
3 血液采集量:在一定条件下,病原菌检出率和采血量成正比,成人推荐采血量为20-30ml,每套不少于10ml,每瓶不少于5ml;婴幼儿采血量不少于其总血量的1%,每瓶不少于2ml;
4 血培养瓶采集说明
怀疑为菌血症、真菌血症的成年患者,应同时或短时间(10min)内,从不
同部位(如双臂)采集2-3套血培养标本,做到“双瓶双侧”,有必要时可在
下肢静脉采集第三套;婴幼儿同时采集两次不同的血培养标本。
相比单套或单瓶,双套和三套可显著提高病原菌的检出率。
(四)血培养的污染问题及其鉴别
1. 污染鉴别:
(1)48小时内仅有这一瓶血培养,则实验室人员需调取患者资料并与临床医生讨论可能的临床价值:病原菌/污染菌/不能确定。
除非临床要求,不做药敏。
(2)48小时内还有另一套或另一瓶血培养,但结果为阴性,则作为污染菌通知临床,除非临床要求,不做药敏试验。
(3)48小时内还有另一套或另一瓶血培养,结果为阳性,如果鉴定结果均为草绿色链球菌,则认为是病原菌,做药敏试验并将结果报告临床;如果鉴定结果均为同一种其他潜在污染菌,则其临床意义不能确定,需与临床医生讨论其可能的临床价值:病原菌/污染菌/不能确定。
除非临床要求,不做药敏试验。
8.2污染的鉴别依据:微生物鉴定、阳性检出时间、重复培养结果以及临床特征等。
(五)注意事项
1.应在病人发热初期或发热高峰使用抗生素之前抽血,对已经使用过抗生素的患者应在下一次用药前抽取血标本。
2、一旦血液注入血培养瓶后,严禁放入冰箱。
3、心包液、胸腔液、腹腔液、骨髓、脑脊液以及浆膜腔积液均可用血液培养瓶增菌。
4.医院应做好血培养采集技术培训减少污染的发生,选择合适的血培养瓶套数,提高检出率,建立客观准确的评估血培养阳性菌株是病原菌还是污染菌
的标准化程序。
5.血培养常见故障及处理详情见《BC120自动血培养系统操作手册》P27-29。
