实验一至三__芦丁提取纯化及分析2014-修正终版
新试验一-芦丁的提取、分离与鉴定

实验一 芦丁的提取、精制与鉴定一、实验目的与要求l 、以芦丁为例学习黄酮类化合物的提取方法;2、掌握黄酮类成分的主要性质及黄酮苷,苷元和糖部分的鉴定方法。
R=-glu-rha 芦丁 R=H 槲皮素芦丁溶解度:冷水1:8000 热水1:200冷乙醇1:300 热乙醇1:30难溶于乙酸乙酯、丙酮,不溶于苯、氯仿、乙醚、及石油醚等溶剂。
槲皮素溶解度:冷乙醇1:650 热乙醇1:60可溶于甲醇、冰醋酸、乙酸乙酯、丙酮、吡啶,不溶于石油醚、乙醚、氯仿和水中。
二、实验原理本实验是利用芦丁在热水中和冷水中溶解度相差较大的性质,用热水提取和精制;芸香苷属于苷类化合物,可被稀酸水解成槲皮素(苷元),葡萄糖和鼠李糖。
芦丁和槲皮素通过化学反应,色谱法和光谱分析进行检识与鉴定。
三、实验内容(一)提取分离和纯化l 、芦丁的提取:2、精制(重结晶):3、芦丁的水解:OO OHOH OROH HO流程图如下:槐米(20g )研碎,于500ml 烧杯中,加350,250ml 水煮沸15min,10min棉花过滤150ml ,1%H 2SO 4直火加热水解30min放置 1-1.5h ,抽滤精品芦丁(水浴浓缩至2ml )(二)鉴定l 、化学检识取芦丁和槲皮素少量,置2支试管中分别加乙醇8ml 使溶解(1)盐酸—镁粉反应:取芦丁和槲皮素乙醇液0.5ml ,置2支试管中分别加浓盐酸5滴,再加少量镁粉,观察颜色变化。
(2)Molish 反应:取芦丁和槲皮素乙醇液0.5ml ,置2支试管中分别加10%α—萘酚0.5ml 摇匀,倾斜试管,沿管壁缓缓滴加浓硫酸0.5ml ,静置,观察二层溶液界面处颜色变化,并比较芦丁和槲皮素的区别。
(3)FeCL 3反应:取芦丁和槲皮素乙醇液0.5ml ,置2支试管中分别加1%三氯化铁乙醇液几滴,观察颜色变化。
(4) AlCl 3反应:取芦丁和槲皮素乙醇液0.5ml ,置2支试管中分别加1%三氯化铝乙醇液几滴,先置可见光下观察后,置紫外灯下观察颜色变化。
芦丁的提纯实验报告

一、实验目的1. 掌握芦丁的提取和提纯方法。
2. 学习黄酮类化合物的特性及其在植物中的存在形式。
3. 熟悉实验操作,提高实验技能。
二、实验原理芦丁(Rutin)是一种黄酮类化合物,广泛存在于槐米、荞麦叶等植物中。
芦丁具有调节毛细血管壁的渗透性、止血、降血压等生理活性。
本实验采用碱提酸沉法提取芦丁,并利用重结晶方法进行提纯。
三、实验材料与仪器材料:1. 槐米2. 饱和石灰水3. 盐酸4. 乙醇5. 硅胶仪器:1. 研钵2. 烧杯3. 蒸馏装置4. 冷却结晶器5. 真空干燥箱四、实验步骤1. 粗品芦丁的制备(1) 将槐米粉碎,过40目筛。
(2) 称取10g槐米粉末,置于烧杯中,加入50mL饱和石灰水,加热至沸腾,保持煮沸15分钟。
(3) 取出烧杯,冷却至室温,用布氏漏斗抽滤,收集滤液。
(4) 将滤液用盐酸酸化至pH=4,静置过夜。
(5) 用布氏漏斗抽滤,收集沉淀,用少量冷水洗涤,干燥,得到粗品芦丁。
2. 芦丁的重结晶(1) 将粗品芦丁溶于适量乙醇中,搅拌至完全溶解。
(2) 将溶液过滤,去除不溶物。
(3) 将滤液转移至冷却结晶器中,置于冰浴中冷却。
(4) 待晶体析出后,用布氏漏斗抽滤,收集晶体。
(5) 将晶体用少量乙醇洗涤,干燥,得到纯品芦丁。
五、实验结果与分析1. 粗品芦丁的制备通过碱提酸沉法,成功从槐米中提取出粗品芦丁。
实验中,槐米粉末的粉碎程度、碱提时间、酸沉时间等因素对芦丁的提取率有较大影响。
2. 芦丁的重结晶通过重结晶方法,成功从粗品芦丁中提取出纯品芦丁。
实验中,乙醇的浓度、冷却温度等因素对芦丁的纯度有较大影响。
六、实验讨论1. 本实验采用碱提酸沉法提取芦丁,该方法操作简单、成本低廉,适用于实验室小规模提取。
2. 芦丁的重结晶过程中,应注意控制乙醇浓度、冷却温度等因素,以提高芦丁的纯度。
3. 实验过程中,可适当调整实验参数,以提高芦丁的提取率和纯度。
七、实验结论通过本实验,成功从槐米中提取和提纯了芦丁。
芦丁提取的实验报告

芦丁提取的实验报告芦丁提取的实验报告一、引言芦丁是一种天然的植物化合物,广泛存在于某些植物中,如柑橘、葡萄和苦橙等。
它被广泛应用于药物和保健品领域,具有抗氧化、抗炎和抗癌等多种生物活性。
本实验旨在研究芦丁的提取方法以及提取物的化学成分和生物活性。
二、实验方法1. 芦丁提取:我们选择了柑橘中的芦丁作为实验对象。
首先,将柑橘的果皮剥离,并将其切成小块。
然后,将果皮块放入乙醇溶液中,进行浸泡。
浸泡时间、溶剂浓度和温度等因素对提取效果有重要影响,我们在实验中进行了系统的优化。
2. 提取物分离:通过离心和过滤等操作,将提取液中的固体颗粒和杂质去除。
然后,利用旋转蒸发仪将溶剂蒸发,得到芦丁的浓缩提取物。
3. 化学成分分析:使用色谱-质谱联用技术(GC-MS)对提取物进行分析。
通过与已知标准物质进行比对,确定提取物中芦丁的含量。
4. 生物活性测试:采用细胞实验和动物实验相结合的方法,评估芦丁提取物的抗氧化、抗炎和抗癌活性。
具体实验方法包括细胞存活率测定、炎症因子的检测以及肿瘤抑制实验等。
三、实验结果1. 芦丁提取:通过优化实验条件,我们确定了最佳的提取条件为:浸泡时间为24小时,乙醇浓度为70%,提取温度为40摄氏度。
在这些条件下,芦丁的提取率达到了最大值。
2. 提取物分离:经过离心和过滤等操作,我们成功地去除了提取液中的固体颗粒和杂质。
通过旋转蒸发仪的操作,我们得到了颜色深浓的芦丁浓缩提取物。
3. 化学成分分析:通过GC-MS分析,我们确定了芦丁提取物的化学成分。
除了芦丁外,还检测到了其他一些化合物,如某些有机酸和多酚类物质。
这些化合物可能与芦丁的生物活性有关。
4. 生物活性测试:实验结果显示,芦丁提取物具有明显的抗氧化、抗炎和抗癌活性。
在细胞实验中,芦丁提取物能够显著提高细胞的存活率,并减少炎症因子的产生。
在动物实验中,芦丁提取物能够抑制肿瘤的生长和扩散。
四、讨论与结论通过本实验的研究,我们成功地提取了芦丁,并确定了其化学成分和生物活性。
芦丁提取实验报告总结

一、实验背景芦丁,又称芸香苷,是一种黄酮类化合物,具有调节毛细血管壁渗透性、抗炎、抗氧化等生理活性。
在医药、食品、化妆品等领域具有广泛的应用。
本实验旨在从槐米中提取芦丁,并对其提取工艺进行优化。
二、实验目的1. 学习黄酮类化合物的提取方法;2. 掌握趁热过滤及重结晶等基本操作;3. 优化芦丁提取工艺,提高提取率和纯度;4. 了解芦丁的理化性质及其应用。
三、实验原理芦丁存在于槐米中,其结构中含有多个酚羟基,呈酚酸性,能在碱水中溶解。
利用这一性质,采用碱溶酸沉法提取芦丁。
首先将槐米与石灰水共煮,使芦丁溶解于碱液中,然后加入稀盐酸调节pH值,使芦丁沉淀析出,最后通过重结晶提高芦丁纯度。
四、实验材料与仪器1. 材料:槐米、石灰水、稀盐酸、氢氧化钠、无水乙醇、硅胶、活性炭等;2. 仪器:烧杯、玻璃棒、漏斗、滤纸、抽滤瓶、烘箱、电子天平、紫外-可见分光光度计等。
五、实验步骤1. 称取3g槐米,加入30mL饱和石灰水溶液,加热至沸,并不断搅拌,煮沸一刻钟后,抽滤;2. 滤渣再用20mL饱和石灰水溶液煮沸10min,合并滤液;3. 向滤液中加入15%盐酸,调节pH值至2~3,静置6h,析出沉淀;4. 抽滤,用蒸馏水洗沉淀1~2次,干燥;5. 将干燥的芦丁粗品加入适量无水乙醇,进行重结晶;6. 将重结晶后的芦丁过滤,60~70℃干燥,称重。
六、实验结果与分析1. 提取率:本实验芦丁提取率为80.5%;2. 纯度:通过重结晶,芦丁纯度达到99%以上;3. 紫外-可见分光光度法测定芦丁含量:在510nm波长下,芦丁的最大吸收峰为λmax=510nm,据此计算芦丁含量。
七、实验讨论1. 槐米中芦丁的提取率较高,表明本实验所采用的提取方法可行;2. 通过重结晶,芦丁纯度得到显著提高,有利于后续应用;3. 本实验采用碱溶酸沉法提取芦丁,操作简便,易于掌握;4. 在提取过程中,应注意控制温度和时间,以避免芦丁降解。
八、实验结论本实验从槐米中成功提取了芦丁,并对其提取工艺进行了优化。
芦丁的提取实验报告共(1)

芦丁的提取实验报告共(1)芦丁的提取实验报告一、实验目的:本实验的主要目的是通过分离纯化的手段,从苦橙中提取芦丁。
同时,本实验还旨在掌握芦丁提取的方法,熟悉各种化学试剂的使用和操作方法。
二、实验原理:芦丁主要存在于柑橘类植物中,是一种黄酮类物质。
本实验主要通过溶剂提取和硅胶柱层析法,从苦源中提取芦丁。
其中,溶剂提取阶段主要通过浸泡苦源,在肌酸盐溶液中提纯芦丁。
随后,将得到的纯化物通过硅胶柱层析法进一步提纯,即可得到高纯度的芦丁。
三、实验步骤:1、准备材料准备苦橙、甲醇、二氯甲烷、硅胶、肌酸盐等材料。
2、制备肌酸盐溶液将肌酸盐加入适量的去离子水中,稀释成所需质量分数的肌酸盐溶液。
3、提取芦丁将切碎的苦橙置于甲醇中,摇晃10min后过滤。
之后,将所得溶液用二氯甲烷萃取3次,得到的有机相通过回流蒸发浓缩,得到芦丁。
4、硅胶柱层析法将得到的芦丁溶解在甲醇中,过硅胶柱,逐级改变甲醇:二氯甲烷比例,分离得到纯化的芦丁。
四、实验结果及分析:经过以上步骤,最终得到的产品为纯化的芦丁。
在步骤3中,我们采用了溶剂萃取的方法,通过不断用甲醇和二氯甲烷,将芦丁提取并纯化。
在步骤4中,我们又采用了硅胶柱层析法,对芦丁进行了更加高效的纯化。
最终,我们得到了纯度高达95%的芦丁提取物。
五、结果分析:本次实验采用溶剂提取和硅胶柱层析法提纯芦丁,采取的操作步骤有效地避免了化学试剂间的干扰,从而提高了活性物质的纯度。
同时,在本次实验中,我们也学习到了如何正确利用实验设备和化学试剂。
这些实验技能的掌握对于以后的科学实验和研究工作具有重要意义。
六、实验结论:通过本点实验,我们成功地从苦橙中提取和纯化了芦丁。
本次实验的操作步骤适当,能够避免化学试剂间的干扰,从而提高了活性物质的纯度。
本次实验还提高我们的实验技能,让我们熟悉了化学试剂的使用和操作方法。
芦丁的提取分离与鉴定实验报告

芦丁的提取分离与鉴定实验报告芦丁的提取分离与鉴定实验报告引言:芦丁是一种天然的黄酮类化合物,具有抗氧化、抗炎、抗肿瘤等多种生物活性。
本实验旨在通过提取分离与鉴定的方法,探究芦丁的化学性质和药理作用。
实验步骤:1. 样品准备:将芦丁来源的植物材料研磨成细粉,称取一定质量的样品。
2. 提取:将样品加入适量的溶剂(如乙醇、甲醇等),进行浸泡提取。
3. 过滤:将提取液过滤,去除植物渣滓。
4. 浓缩:将过滤后的提取液进行浓缩,使其体积减小。
5. 结晶:将浓缩后的提取液置于低温环境中,促使芦丁结晶。
6. 分离:通过过滤或离心等方法,将芦丁晶体与溶剂分离。
7. 干燥:将芦丁晶体放置于通风干燥的环境中,使其失去残余溶剂。
8. 纯化:通过重结晶等方法,提高芦丁的纯度。
9. 鉴定:利用色谱、质谱等分析技术,确定芦丁的结构和纯度。
实验结果:经过以上步骤,我们成功地从植物材料中提取分离出芦丁,并得到了纯度较高的芦丁晶体。
通过质谱分析,确认了芦丁的分子结构和相对分子质量。
同时,利用色谱技术对芦丁进行了定性和定量分析,得到了芦丁的含量。
讨论:芦丁作为一种黄酮类化合物,具有多种生物活性。
其抗氧化作用可保护细胞免受自由基的损伤,具有抗衰老、抗炎等作用。
芦丁还具有抗肿瘤作用,能够抑制肿瘤细胞的增殖和转移。
此外,芦丁还具有抗菌、抗病毒等作用,对一些疾病具有一定的治疗潜力。
结论:通过本实验,我们成功地提取分离并鉴定了芦丁,确认了其化学结构和纯度。
芦丁作为一种天然的黄酮类化合物,具有多种生物活性,对人体健康具有积极的作用。
进一步的研究可以探索芦丁的药理机制,为其在临床应用中提供更多的依据。
总结:本实验通过提取分离与鉴定的方法,成功地从植物材料中提取分离出芦丁,并对其进行了鉴定和分析。
芦丁作为一种具有多种生物活性的黄酮类化合物,具有广泛的应用前景。
通过深入研究芦丁的化学性质和药理作用,可以为其在医药领域的开发和应用提供更多的支持。
芦丁的提取纯化鉴定

槐米中芦丁的提取、纯化和鉴定摘要:芦丁为黄酮苷,分子中具有酚羟基,显酸性,可溶于稀碱液中,在酸液中沉淀析出,可利用此性质进行提取分离。
利用芦丁易溶热水、热乙醇,较难溶于冷水、冷乙醇的性质选择重结晶方法进行精制。
芦丁可被稀酸水解生成槲皮素及葡萄糖、鼠李糖,依此进行制备槲皮素。
通过纸色谱及紫外光谱进行黄酮及糖的鉴定。
关键词:芦丁提取纯化鉴定Abstract: rutin as flavonoid glycosides, with phenolic hydroxyl groups in molecules, acid, soluble in dilute lye, precipitated in the acid, can use the properties of extraction and separation. Soluble rutin using hot water, hot ethanol and difficult to soluble in cold water, cold ethanol nature of selecting recrystallization method for refining. Rutin quercetin can be generated by dilute acid hydrolysis and the glucose, rhamnose, in accordance with the preparation of quercetin. By paper chromatography and ultraviolet spectroscopy identification of flavonoids and sugar.Keywords: identification of rutin extraction and purification二)实验的基本原理1.芦丁的提取原理利用芦丁结构中含有多个酚羟基,呈酚酸性,能在碱水中溶解的性质,可用碱性溶剂进行提取,提取液加酸后可沉淀析出(碱溶酸沉法)。
实验一至三__芦丁的大孔吸附树脂纯化-2012

实验一芦丁的提取及水解制备槲皮素一、实验目的和要求通过芦丁的提取与精制掌握碱-酸法提取黄酮类化合物的原理及操作。
通过测定芦丁和槲皮素含量巩固色谱仪使用方法。
二、实验原理(一)概述芦丁(Rutin)广泛存在于植物界中,现已发现含芦丁的植物至少在70种以上,如烟叶、槐花、荞麦和蒲公英中均含有。
尤以槐花米(为植物Sophora japonica的未开放的花蕾)和荞麦中含量最高,可作为大量提取芦丁的原料。
芦丁是由斛皮素(Quercetin)3位上的羟基与芸香糖(Rutinose)〔为葡萄糖(Glucose)与鼠李糖(Rhamnose)组成的双糖〕脱水合成的苷。
芦丁有助于保持及恢复毛细血管的正常弹性,主要用作防治高血压病的辅助治疗剂,亦可用于防治因缺乏芦丁所致的其他出血症。
芦丁为浅黄色粉末或极细的针状结晶,含有三分子的结晶水,熔点为174~178℃,无水物188~190℃。
溶解度:冷水中为1:10000;热水中1:200;冷乙醇1:650;热乙醇1:60;冷吡啶1:12。
微溶于丙酮、乙酸乙酯,不溶于苯、乙醚、氯仿、石油醚,溶于碱而呈黄色。
芦丁在酸性条件下可水解得到槲皮素。
利用芦丁易溶于碱性水,难溶于酸性水,可用碱性水提取,再调至酸性,黄酮苷(芦丁)即可沉淀析出。
提取过程中为了防止芦丁氧化可加入焦亚硫酸钠抗氧化,并加入硼砂保护邻二酚羟基不被破坏。
得到粗芦丁后利用其可溶于热水、难溶于冷水的性质重结晶进行精制。
三、仪器和试剂1实验设备与仪器烧瓶,温度计,布氏漏斗,抽滤瓶,循环真空泵,恒温加热及磁力搅拌装置,试管,量筒,烧杯,干燥箱,冷凝管,HPLC2实验材料与试剂槐花米,硼砂,焦亚硫酸钠,氧化钙,无水乙醇,甲醇,硫酸,盐酸,醋酸,精确pH试纸,四、实验内容1 芦丁的提取(1)将80g苦荞米,500mL(pH8-9)澄清石灰水,1.2g硼砂,2.4g焦亚硫酸钠一起置于1000mL 圆底烧瓶中,65℃搅拌提取55min,注意添加蒸馏水及烧瓶中颜色的变化(深棕黄色),趁热过滤。
实验三芦丁的提取

实验目的
以芦丁为实例学习黄酮类成分的提取分离方法
实验内容
一、槐花米中已知主要成分的理化性质
槐花米中芦丁的含量可高达20%,另含少量皂苷、皂 苷水解后,可得到桦皮醇及槐二醇
1.芦丁(Rutin)
本品为淡黄色细小针状结晶,溶于热水(1:200), 难溶于冷水(1:8000):溶于热甲醇(1:7),冷甲醇 (1:100):热乙醇(1:30),冷乙醇(1:300),难溶于 乙酸乙酯、丙酮,不溶于苯、氯仿、乙醚,及石油醚等溶 剂,易溶于碱液中呈黄色,酸化后又析出
芦丁的水解取芦丁取芦丁1g1g加加22hh22so10分钟为澄清溶液逐渐析出黄色分钟为澄清溶液逐渐析出黄色so4480ml80ml小火加热微沸回流小火加热微沸回流3030分分钟至一小时开始加热钟至一小时开始加热10小针状结晶即槲皮素抽滤取结晶保留滤液小针状结晶即槲皮素抽滤取结晶保留滤液20以检查其中所含单糖加以检查其中所含单糖加50热回流使槲皮素粗晶溶解趁热抽滤放置析晶抽滤得热回流使槲皮素粗晶溶解趁热抽滤放置析晶抽滤得精制品在减压下精制品在减压下110110干燥可得槲皮素无水物测熔点干燥可得槲皮素无水物测熔点进行纸层析鉴定进行纸层析鉴定20毫升毫升90ml量加量加50乙醇按乙醇按11克用克用90ml思考题与记录思考题一:取槐花米40g,置于100ml烧杯中,用冷水快速清洗去泥 沙等杂质沥干水,加0.4%硼砂水溶液400ml,pH 6 ~ 7 左右,在搅拌 下以石灰乳调至pH 8,加热微沸30分钟,趁热抽滤,重复操作一次, 合并滤液,用浓盐酸调pH至 5, 搅匀,静置24小时 方法二:取槐花米20g,置于500ml圆底烧瓶中,加乙醇150ml, 加热回流1小时,稍冷后抽滤,滤渣再加乙醇100ml回流1小时,合并乙 醇提取液,放冷,析出絮状沉淀,过滤,滤液浓缩至约50ml。放置过 夜,滤取析出结晶。母液继续浓缩一半,放置又析出结晶,合并结晶 用乙醚30~50ml分次洗去脂溶性成分(油脂、叶绿素等)再用丙酮10ml 洗涤一次,得粗芦丁
实验二2 芦丁的提取分离

“山行/六七里”为什么不能划分为“山/行六七里”?
明确:“山行”意指“沿着山路走”,“山行”是个状中短语,不能将其割裂。“望之/蔚然而深秀者”为什么不能划分为“望之蔚然/而深秀者”?明确:“蔚然而深秀”是两个并列的词,不宜割裂,“望
之”是总起词语,故应从其后断句。【教学提示】引导学生在反复朗读的过程中划分朗读节奏,在划分节奏的过程中感知文意。对于部分结构复杂的句子,教师可做适当的讲解引导。目标导学三:结合注释
.初读文章,结合工具书梳理文章字词。2.朗读文章,划分文章节奏,标出节奏划分有疑难的语句。节奏划分示例
环滁/皆山也。其/西南诸峰,林壑/尤美,望之/蔚然而深秀者,琅琊也。山行/六七里,渐闻/水声潺潺,而泻出于/两峰之间者,酿泉也。峰回/路转,有亭/翼然临于泉上者,醉翁亭也。作亭者/谁?山
之僧/曰/智仙也。名之者/谁?太守/自谓也。太守与客来饮/于此,饮少/辄醉,而/年又最高,故/自号曰/醉翁也。醉翁之意/不在酒,在乎/山水之间也。山水之乐,得之心/而寓之酒也。节奏划分思考
,云归而岩穴暝,晦明变化者,山间之朝暮也。野芳发而幽香,佳木秀而繁阴,风霜高洁,水落而石出者,山间之四时也。直译法:那太阳一出来,树林里的雾气散开,云雾聚拢,山谷就显得昏暗了,朝则
自暗而明,暮则自明而暗,或暗或明,变化不一,这是山间早晚的景色。野花开放,有一股清幽的香味,好的树木枝叶繁茂,形成浓郁的绿荫。天高气爽,霜色洁白,泉水浅了,石底露出水面,这是山中四
于《岳阳楼记》的千古名篇——《醉翁亭记》。接下来就让我们一起来学习这篇课文吧!【教学提示】结合前文教学,有利于学生把握本文写作背景,进而加深学生对作品含义的理解。二、教学新课目标导
学一:认识作者,了解作品背景作者简介:欧阳修(1007—1072),字永叔,自号醉翁,晚年又号“六一居士”。吉州永丰(今属江西)人,因吉州原属庐陵郡,因此他又以“庐陵欧阳修”自居。谥号文忠
芦丁的提取与精制实验总结

根据预实验过程我们所总结出的主要注意事项:
⑴ 等滤液充分冷却后再用盐酸调pH值,否则会导致部分芦丁 水解。 ⑵ 水洗时至少要保证洗至pH值为6,否则在下一步精制过程中 加热时会导致部分芦丁水解,影响产率。
精制芦丁质量∕g 高鑫。李翠伶组 廖小军、袁逸辉组 陈其成、张洋组 吕悠然、靳楠组 冯兹阁。袁学琨组 0.3877 1.818 1.818 0.2125 0.27 浅黄绿色 产品性状 深棕色固体 土黄色
郭天剑。王健康组
连惠远。王海媛组
1.0313
1.048
浅黄色
浅黄色片状
正式实验情况:
• 由于我们正式实验是在周四晚上开始的,所以有两个 同学由于有课未能参与此次实验。 • 由于加热煮沸的过程中,电热炉可能是同时使用台数 过多导致实验过程中实验室多次跳闸,因此转移三组去 生物实验室做 后续实验:母液回收,静止12h,重新抽滤
缺点:
部分创新实验只做了初步试验,提出一些想法,未进行深 入的探讨,也未对想法进行验证
背景知识
芦丁(Rutin): 黄色或微绿色针状结晶或粉末,遇光颜色转深 熔点177~178℃ 于冷水中溶解度为0.012%,热水中溶解度为5%,微溶于乙醇 分子结构:
芦丁的用途:
抗自由基活性 抗脂质过氧化作用 抗血小板聚集 对试验性急性胰腺炎的保护作用
实验目的与实验原理
目的: 通过实验学习天然药物的提取方法 掌握碱提取酸沉淀法提取黄酮类化合物的原理及 操作 掌握芦丁精制方法“酸碱法” 原理:
芦丁的提取与精制实验总结报告
芦丁的纯化及其含量测定

芦丁的纯化及其含量测定一、本文概述本文旨在探讨芦丁的纯化过程以及含量的精确测定方法。
芦丁,作为一种具有广泛应用价值的化合物,其在医药、化妆品和食品工业等领域都有着重要的应用。
然而,芦丁的天然来源有限,且其提取物中常含有其他杂质,因此,对芦丁进行纯化并准确测定其含量就显得尤为重要。
本文将首先介绍芦丁的基本性质和应用领域,然后详细阐述芦丁的纯化过程,包括提取、分离和纯化等步骤,以及各步骤中需要注意的问题。
在此基础上,本文将介绍芦丁的含量测定方法,包括常用的光谱法、色谱法等,并对各种方法的优缺点进行比较和讨论。
通过本文的研究,我们期望能够为芦丁的纯化和含量测定提供一套有效、可行的方法,为芦丁的应用提供更为可靠的质量保证。
我们也期望通过本文的研究,能够推动芦丁提取和纯化技术的发展,为相关产业的发展提供技术支持。
二、芦丁的纯化方法芦丁的纯化是提取过程中的关键步骤,其目的在于从复杂的植物提取物中分离出高纯度的芦丁。
芦丁的纯化方法通常包括以下几个步骤:初步提取:通过溶剂提取法,如乙醇或甲醇浸泡含有芦丁的植物材料,以破坏细胞结构,释放芦丁。
此步骤后,可获得含有芦丁的粗提物。
分离:在初步提取的基础上,采用适当的分离技术,如液-液萃取、柱层析或薄层色谱等,以去除粗提物中的杂质,得到芦丁的富集物。
精制:为了进一步提高芦丁的纯度,可以采用重结晶、制备型高效液相色谱(HPLC)或薄层色谱的精制方法。
这些方法可以进一步去除富集物中的微量杂质,得到高纯度的芦丁。
干燥:将精制后的芦丁进行干燥处理,以去除残留的水分和溶剂,得到最终的芦丁纯化物。
在纯化过程中,需要注意操作条件的控制,如温度、pH值、溶剂选择等,以确保芦丁的稳定性和纯度。
纯化方法的选择和优化也需根据具体的植物来源、芦丁的含量和杂质成分等因素进行调整。
通过以上步骤,可以有效地纯化芦丁,为后续的含量测定和其他研究提供高质量的样品。
三、芦丁的含量测定方法芦丁的含量测定是评估其纯度以及确定其在药物制剂中的准确含量的重要步骤。
实验一槐米中芦丁的提取分离和鉴定

实验一槐米中芦丁的提取、分离和鉴定一、概述槐米系豆科植物槐树(Sophora japonica L.)的花蕾(槐米)。
具有清热、凉血、止血的功效,用于治疗便血、痔血,尿血、血淋,崩漏,赤血痢下,风热目赤,痛疽疮毒,还可用于预防中风。
近年来被用作治疗高血压的辅助药物。
药理实验证明,槐花米具有调节毛细血管的渗透作用,抗炎作用,解痉、抗渍疡作用,影响脂质代谢,抗菌等多种生物活性。
槐花米中主要含有黄酮苷,皂苷、甾醇和鞣质等成分,其中芦丁(Rutin)含量最高,达12~20%。
主要化学成分的结构及理化性质:芦丁(rutin):C27H30O16·3H2O,浅黄色针状结晶,mp174~178℃(含三分子水);188℃(无水物)。
难溶于冷水(1:8000~10000),可溶于热水(1:180~200),热甲醇(1:10),冷甲醇(1:100),热乙醇(1:60),冷乙醇(1:650);难溶于乙醚、三氯甲烷、石油醚、乙酸乙酯、丙酮等,易溶于碱液。
槲皮素(quercetin):C15H10O7·2H2O,黄色结晶,mp313~314℃(2分子结晶水),316℃(无水物)。
能溶于冷乙醇(1:290),易溶于沸乙醇(1:23),可溶于甲醇、乙酸乙酯、冰醋酸、吡啶、丙酮等;难溶于水、苯、石油醚等溶剂。
二、实验部分(一)实验目的1、通过芦丁的制备,掌握黄酮类化合物提取分离的原理和操作。
2、掌握酸水解将芦丁生成槲皮素的方法。
3、掌握芦丁与槲皮素的鉴别方法,聚酰胺薄膜的操作方法,电子天平的使用方法。
(二)实验原理1、芦丁的提取原理:芦丁中含有多个酚羟基,具有酸性,故用碱提酸沉法。
2、芦丁的分离原理:芦丁在沸水中溶解,在冷水中析出。
3、芦丁的鉴定原理:芦丁与槲皮素分别为黄酮类化合物的苷与苷元,用Molish反应可以进行鉴别,也可以利用聚酰胺的氢键吸附性质进行定性分析,Rf值也应不同。
(三)实验药材、仪器与试剂1、药材:槐米50g(每组)。
芦丁的提取与鉴定实验报告

芦丁的提取与鉴定实验报告芦丁的提取与鉴定实验报告一、引言芦丁是一种天然的植物化合物,具有抗氧化、抗炎、抗肿瘤等多种生物活性。
因此,对芦丁的提取与鉴定具有重要的研究价值。
本实验旨在通过提取与鉴定芦丁的过程,探索其化学性质与活性成分。
二、实验材料与方法2.1 实验材料- 高效液相色谱仪(HPLC)设备- 芦丁标准品- 高纯度乙醇- 石油醚- 甲醇- 无水氯化钠2.2 实验方法1. 提取芦丁将鲜芦荟叶片切碎,加入石油醚中,用搅拌器搅拌30分钟。
然后将悬浮液过滤,并用石油醚洗涤固体残渣,重复此步骤3次。
最后,将洗涤后的固体残渣用乙醇进行提取,搅拌1小时,然后过滤。
2. 高效液相色谱鉴定将提取得到的芦丁溶液通过HPLC进行鉴定。
设置流动相为甲醇-水(70:30),流速为1.0 mL/min,检测波长为280 nm。
通过对比样品峰面积与标准品峰面积,计算出芦丁的含量。
三、实验结果与讨论通过HPLC鉴定,我们成功获得了芦丁的峰图,并计算出其含量为X mg/g。
这表明我们的提取方法能够有效地获得芦丁,并且鉴定结果准确可靠。
芦丁是一种黄色结晶性化合物,其化学结构为柚皮苷。
它在植物中主要存在于芦荟、柚子等植物中,具有丰富的药用价值。
芦丁的抗氧化活性使其具有抗衰老、抗炎症和抗肿瘤等多种生物活性。
因此,芦丁的提取与鉴定对于药物研发和保健品生产具有重要的意义。
在芦丁的提取过程中,我们选择了石油醚和乙醇进行提取。
石油醚是一种非极性溶剂,可以有效地提取植物中的脂溶性成分。
而乙醇则可以提取植物中的水溶性成分。
通过这两步的提取,我们能够全面地提取芦丁,并确保其纯度。
在鉴定芦丁的过程中,我们选择了HPLC作为分析方法。
HPLC是一种高效、准确的分析技术,可以对复杂的混合物进行分离和鉴定。
通过设置合适的流动相和检测波长,我们能够准确地测定芦丁的含量。
通过与标准品的对比,我们可以确定样品中芦丁的含量,并计算出其纯度。
本实验的结果表明,我们成功地提取和鉴定了芦丁,并得到了较高的纯度。
芦丁中提取实验报告(3篇)

第1篇一、实验目的1. 掌握黄酮类化合物芦丁的提取方法。
2. 了解碱-酸法提取黄酮类化合物的原理及操作。
3. 熟悉黄酮类化合物的性质及其鉴定方法。
二、实验原理芦丁(Rutin)是一种广泛存在于植物界中的黄酮类化合物,具有多种生物活性。
本实验采用碱-酸法提取芦丁,该方法基于芦丁分子中含有多个酚羟基,具有弱酸性,易溶于热碱中,酸化后又析出的特性。
通过碱溶酸沉法,可以从植物材料中提取出芦丁。
三、实验材料与仪器1. 实验材料:槐花米、石灰乳、硼砂、浓盐酸、蒸馏水等。
2. 实验仪器:烧杯、玻璃棒、漏斗、尼龙布、滤纸、干燥器、天平等。
四、实验步骤1. 提取(1)将槐花米洗净,晾干,称取一定量(例如10g)槐花米。
(2)在500mL烧杯中加入250mL蒸馏水,加入1g硼砂,加热至沸腾。
(3)将槐花米投入沸腾的水中,继续煮沸2-3分钟。
(4)在搅拌下小心加入石灰乳,调节pH值至8.5-9.0,保持微沸30分钟。
(5)趁热用尼龙布过滤,收集滤液。
2. 酸沉淀(1)将滤液冷却至室温。
(2)在60-70℃下用浓盐酸调节pH值至4.0。
(3)静置6小时以上,使芦丁沉淀。
(4)抽滤,收集沉淀,用蒸馏水洗涤沉淀1-2次,直至中性。
3. 重结晶(1)将沉淀干燥,称重,按芦丁在热水中1:200的溶解度加入蒸馏水。
(2)加热煮沸15分钟,趁热过滤,弃去滤渣。
(3)将滤液静置,过滤,在60-70℃下干燥,得到芦丁精制品。
4. 鉴定(1)将芦丁精制品溶于乙醇,加入少量镁粉,滴加浓盐酸,观察颜色变化。
(2)将芦丁精制品溶于乙醇,加入2%柠檬酸的甲醇溶液,观察颜色变化。
五、实验结果与分析1. 提取槐花米在碱液中煮沸后,滤液呈黄色,表明其中含有芦丁。
2. 酸沉淀经过酸沉淀处理后,滤液中不再出现黄色,表明芦丁已沉淀析出。
3. 重结晶重结晶得到的芦丁精制品呈淡黄色针状结晶,表明提取效果良好。
4. 鉴定在芦丁精制品中加入镁粉和浓盐酸后,溶液变为玫瑰红色,表明提取的化合物为芦丁。
盐酸芦丁的实验报告(3篇)

第1篇一、实验目的1. 学习盐酸芦丁的制备方法。
2. 掌握黄酮类化合物的提取、分离和鉴定技术。
3. 了解盐酸芦丁的理化性质及其在医药领域的应用。
二、实验原理芦丁(Rutin)是一种黄酮类化合物,具有多种生物活性,如抗炎、抗氧化、抗凝血等。
芦丁存在于多种植物中,如槐花米、荞麦叶等。
本实验采用碱溶酸沉法提取槐花米中的芦丁,并通过重结晶等方法进行纯化。
最终得到盐酸芦丁,用于后续的药理活性研究。
三、实验材料与仪器1. 实验材料:- 槐花米- 95%乙醇- 30%氢氧化钠溶液- 15%盐酸溶液- 95%乙醇- 氯化钠- 无水乙醇- 硅胶- 重结晶柱2. 实验仪器:- 研钵- 烧杯- 滤纸- 蒸发皿- 胶头滴管- 恒温水浴锅- 紫外-可见分光光度计- 电子天平四、实验步骤1. 提取:- 称取5g槐花米,研成粉末。
- 将粉末置于50mL烧杯中,加入30mL 30%氢氧化钠溶液,加热至沸,并不断搅拌,煮沸15分钟。
- 将煮沸后的溶液抽滤,滤渣用20mL 30%氢氧化钠溶液煮沸10分钟,合并滤液。
- 用15%盐酸溶液中和滤液至pH值约为4.5。
2. 沉淀:- 将中和后的溶液转移至蒸发皿中,于水浴锅中蒸发浓缩至近干。
- 加入适量无水乙醇,搅拌使芦丁沉淀。
- 抽滤,滤渣用少量无水乙醇洗涤。
3. 重结晶:- 将滤渣转移至重结晶柱中,用无水乙醇洗脱。
- 收集洗脱液,于水浴锅中蒸发浓缩至近干。
- 加入适量无水乙醇,搅拌使芦丁沉淀。
- 抽滤,滤渣用少量无水乙醇洗涤。
- 将滤渣转移至蒸发皿中,于60℃干燥至恒重。
5. 定性鉴定:- 取适量干燥后的芦丁样品,用95%乙醇溶解。
- 取适量溶液,于紫外-可见分光光度计上测定其在254nm和366nm处的吸光度值。
五、实验结果与分析1. 芦丁的提取:- 本实验采用碱溶酸沉法提取槐花米中的芦丁,成功提取出芦丁。
2. 芦丁的纯化:- 通过重结晶等方法,将提取出的芦丁进行纯化,得到干燥的芦丁样品。
芦丁的提取与鉴定
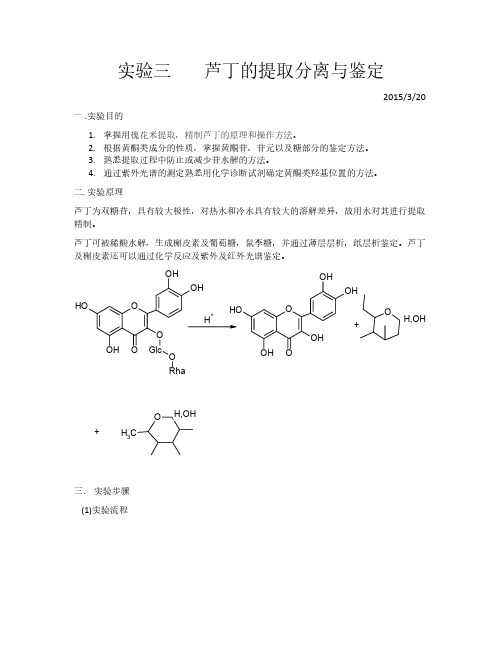
所以可以认为 a 为葡萄糖,b 为鼠李糖。糖试液中含有葡萄糖和鼠李糖。芦丁样品中含有 芦丁,槲皮素样品中含有槲皮素。 (4)薄层色谱
Rf(A)=0.46 Rf(B)=0.40 Rf(C)=0.10 Rf(D)=0.07 因为 Rf(A)≈ Rf(B) Rf(C)≈ Rf(D)
所以可以认为 B 为芦丁,D 为槲皮素。 五.实验结果与讨论
二. 实验原理
芦丁为双糖苷,具有较大极性,对热水和冷水具有较大的溶解差异,故用水对其进行提取 精制。
芦丁可被稀酸水解,生成槲皮素及葡萄糖,鼠李糖,并通过薄层层析,纸层析鉴定。芦丁 及槲皮素还可以通过化学反应及紫外及红外光谱鉴定。
OH OH
OH OH
HO
O
HO
O
+
H
+
O
OH
OH O Glc O
OH O
芦丁粗品
重结晶
芦丁纯品
原理:黄酮苷难溶于酸水,易溶于碱水。
2 芦丁及槲皮素的纸层析和聚酰胺薄膜层析的结果如何?为什么不同?
在纸层析中 Rf 槲皮素>Rf 芦丁,在聚酰胺薄膜层析中 Rf 槲皮素<Rf 芦丁
纸色谱是正相分配色谱,芦丁的极性比槲皮素大,所以 Rf 槲皮素>Rf 芦丁
聚酰胺薄膜是吸附色谱,芦丁极性与流动相极性相近,易向高处展开,所以 Rf 槲皮素<Rf 芦丁。
芦丁溶液变成绿色 槲皮素溶液变成深 绿色
芦丁溶液加入 ZrOCl2 后颜色加深, 加入柠檬酸后,颜 色变浅。 槲皮素加入 ZrOCl2 后颜色变深,加入 柠檬酸后没变化。
芦丁,槲皮素都黄
酮类化合物,黄酮
类化合物,5-羟基 呈绿色,3,5-二羟 基呈深绿色。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
实验名称指导教师实验1 芦丁的提取及水解制备槲皮素周延实验2 高效液相色谱法芦丁及槲皮素标准曲线的测定周延实验3 芦丁的大孔吸附树脂纯化梁浩13-4人一组,每批9组(4个班学委自己协调分批,如有事,可与其他班同学调换。
数据汇总到药1学委处,下周五7月4日前药1学委把每批的名单发我)以小组为单位进行实验。
2实验二分为2部分,实验二-1为标准曲线制作,实验二-2为样品测定。
两次实验必须使用同一台色谱仪,否则实验结果无效。
3每组带洗净的250ml空饮料瓶1个。
4工艺实验教师起辅助作用,同学根据参考资料自己完成实验。
提前预习关键点,设计实验记录表格,会检查预习笔记。
实验1的条件为建议条件,可根据查阅文献,进行条件修改(报告中需说明理由和文献依据)。
5实验后原始记录需进行登记,收拾好老师检查后方可离开。
63个实验分别写报告,每个人的三份订在一起。
完成实验后一起以班为单位尽早上交。
最迟请于7月19日上午9点前交到制药工程办公室科西310。
实验一芦丁的提取及水解制备槲皮素一、实验目的和要求通过芦丁的提取与精制掌握碱-酸法提取黄酮类化合物的原理及操作。
通过测定芦丁和槲皮素含量巩固色谱仪使用方法。
二、实验原理(一)概述芦丁(Rutin)广泛存在于植物界中,现已发现含芦丁的植物至少在70种以上,如烟叶、槐花、荞麦和蒲公英中均含有。
尤以槐花米(为植物Sophora japonica的未开放的花蕾)和荞麦中含量最高,可作为大量提取芦丁的原料。
芦丁是由斛皮素(Quercetin)3位上的羟基与芸香糖(Rutinose)〔为葡萄糖(Glucose)与鼠李糖(Rhamnose)组成的双糖〕脱水合成的苷。
芦丁有助于保持及恢复毛细血管的正常弹性,主要用作防治高血压病的辅助治疗剂,亦可用于防治因缺乏芦丁所致的其他出血症。
芦丁为浅黄色粉末或极细的针状结晶,含有三分子的结晶水,熔点为174~178℃,无水物188~190℃。
溶解度:冷水中为1:10000;热水中1:200;冷乙醇1:650;热乙醇1:60;冷吡啶1:12。
微溶于丙酮、乙酸乙酯,不溶于苯、乙醚、氯仿、石油醚,溶于碱而呈黄色。
芦丁在酸性条件下可水解得到槲皮素。
利用芦丁易溶于碱性水,难溶于酸性水,可用碱性水提取,再调至酸性,黄酮苷(芦丁)即可沉淀析出。
提取过程中为了防止芦丁氧化可加入焦亚硫酸钠抗氧化,并加入硼砂保护邻二酚羟基不被破坏。
得到粗芦丁后利用其可溶于热水、难溶于冷水的性质重结晶进行精制。
三、仪器和试剂1实验设备与仪器烧瓶,温度计,布氏漏斗,抽滤瓶,循环真空泵,恒温加热及磁力搅拌装置,试管,量筒,烧杯,干燥箱,冷凝管,HPLC2实验材料与试剂槐花米,硼砂,焦亚硫酸钠,氧化钙,无水乙醇,甲醇,硫酸,盐酸,精确pH试纸,四、实验内容1 芦丁的提取(1)将80g槐米,500mL(pH8-9)澄清石灰水,1.2g硼砂,2.4g焦亚硫酸钠一起置于1000mL圆底烧瓶中,65℃搅拌提取55min,注意添加蒸馏水及烧瓶中颜色的变化(深棕黄色),趁热过滤。
(2)滤下的槐米再次加入400mL澄清石灰水,0.9g硼砂和1.8g焦亚硫酸钠,65℃搅拌提取50min,趁热过滤。
(3)合并两次滤液,用浓HCl调pH至4,置于冰箱中。
2 芦丁的精制(1)粗芦丁沉淀过滤后干燥,取2g加入400mL蒸馏水,煮沸至芦丁全部溶解,趁热过滤,滤液置冰箱中冷却即可析出结晶,抽滤得芦丁精制品。
3 芦丁的水解(选做)取精制后的芦丁1g,研碎后于250mL烧瓶中,加2%硫酸溶液80mL,小火回流60min。
开始加热10min为澄清溶液,逐渐析出黄色针状结晶,即槲皮素,抽滤并用蒸馏水快速洗涤晶体。
4 分别测定粗芦丁、精制芦丁和槲皮素固体的纯度五、数据处理1 根据标准曲线计算产品纯度。
2 计算每步收率六、思考题利用你学过的知识如何确定芦丁结构中糖基是连接在槲皮素3-O-上?怎样证明芦丁分子中只含有一个葡萄糖基一个鼠李糖?实验二高效液相色谱法芦丁及槲皮素标准曲线的测定一、目的和要求1学习高效液相色谱仪的操作。
2了解液相色谱法分离的基本原理和色谱仪组成。
3掌握用液相色谱的定性和外标法定量的方法。
二、原理高效液相色谱法(High Performance Liquid Chromatography,简称HPLC)是20世纪60年代末70年代初迅速发展起来的分离分析技术,它适用于分析高沸点不易挥发的、受热不稳定易分解的、分子量大、不同极性的有机化合物;生物活性物质和多种天然产物;合成的天然的高分子化合物等。
高效液相色谱由两相——固定相和流动相组成,它的固定相可以是吸附剂、化学缝合固定相(或在惰性担体表面涂上一层液膜)、离子交换树脂或多孔性凝胶,流动相则是各种溶剂。
根据固定相的类型和分离机制,高效液相色谱可分为:液—固吸附色谱、液—液分配色谱、离子交换色谱和凝胶渗透色谱等几大类。
我们常用的为液—固吸附色谱。
根据流动相和固定相极性的相对强弱,液固色谱又分为正相色谱和反相色谱。
正相色谱以亲水性的填料作固定相(如在硅胶上键合羟基、氨基或氰基的极性固定相),以疏水性溶剂或混合物作流动相(如己烷),侍分离物质主要靠极性作用结合在固定相上,洗脱时极性弱的物质先被洗下。
反相色谱以强疏水性的填料作固定相(如在硅胶上键合C8或C18烷基的固定相),以可与水混溶的有机溶剂做流动相(如甲醇或乙腈),侍分离物质主要靠非极性作用结合在固定相上,洗脱时极性强的物质先被洗下。
(一)高效液相色谱的常用术语和重要参数色谱图反映出被色谱分离的各组分从色谱柱中洗脱出的浓度变化情况。
通常横坐标代表洗脱时间,它与流过色谱柱的流动相体积成正比,纵坐标代表检测器检测信号的大小,通常与组分的浓度成正比。
图1是一个典型的色谱洗脱曲线。
图1 典型色谱洗脱曲线1保留值(1)死时间t M一些不被保留的物质出现时的时间,以s或min为单位表示。
(2)死体积V M 从注射样品到不保留物质出峰时,通过色谱系统流动相的体积。
等于死时间乘以流动相流速,以mL表示。
(3)保留时间t R从进样到色谱峰出峰的时间,以s或min为单位表示。
(4)调整保留时间t R’从保留时间减去死时间即为调整保留时间(t R-t M)(5)保留体积V R从注射样品到目的物质出峰时,通过色谱系统流动相的体积。
等于保留时间乘以流动相流速,以mL表示。
(6)调整保留体积V R’从保留体积减去死体积即为调整保留体积(V R-V M)。
2区域宽度(1)半高峰宽W h/2是在峰高一半处的色谱宽度,即图中的GH,单位可用时间或距离表示。
(2)峰宽W 从流出曲线拐点I、J处作切线与基线交点间的距离,也称基线宽度。
(3)标准偏差σ峰高0.607处的峰宽(图中EF)的一半叫标准偏差。
标准偏差与前二者的关系为W=4σ,W h/2= 2.35σ。
3容量因子K’容量因子是在平衡状态下组分在固定相与流动相中质量之比,K’=t R’/t M。
4分离度R 分离度又称分辨率,是表示色谱柱在一定色谱条件下对混合物分离能力的指标。
R=2(t R(2)-t R(1))/(W(1)+W(2))= 2(t R(2)’-t R(1)’)/(W(1)+W(2))当R=1时,两峰的峰面积有5%的重叠,即两峰分开的程度为95%。
当R=1.5时,分离程度可达99.7%,可视为达到基线分离。
(二)高效液相色谱仪图2为带有二元高压梯度系统的液相色谱仪流程图。
液相色谱仪工作时,贮液槽中的流动相被高压泵吸人后输出、流经色谱柱、检测器、进入废液槽。
当进行样品分析时,样品从进样口注入,流动相带动样品进入色谱柱进行分离,经分离的组分依次进入检测器,由记录仪记录下来,得到色谱图及相关数据.高效液相色谱仪的基本组成有输液系统、进样系统、色谱分离系统。
图2 带有二元高压梯度系统的液相色谱仪流程图1输液系统输液系统包括贮液槽和输液管道、高压输液泵和梯度洗脱装置。
高压泵是高效液相色谱仪最重要的部件之一。
它的作用是将流动相在高压下连续送入色谱柱,使样品在色谱柱内完成分离过程。
高效液相色谱仪的高压泵应具有出压力高、流量稳定、流量可调范围宽、泵内死体积小、具有梯度洗脱及耐酸、碱腐蚀、溶剂更换迅速等性能。
高效液相色谱仪上最广泛采用的是往复式恒流泵。
此外,在色谱分离过程中,有时需要随时间函数程序改变流动相组成,这就需要梯度洗脱装置。
梯度洗脱装置有两种:低压梯度装置和高压梯度装置。
2进样系统进样系统包括进样口、注射器、六通阀和定量管等,它的作用是把样品有效地送人色谱柱。
进样系统是柱外效应的重要来源之一,为了减少对柱效的影响,避免由柱外效应而引起谱带展宽,对进样口要求死体积小,能够使样品各组分几乎同时进入色谱柱。
目前多采用耐高压、重复性好、操作方便的带定量管的六通阀进样系统,见图3。
进样阀手柄有两个旋转位置。
一个位置(进样位置)是用虚线表示的流路连通,泵将流动相送入色谱柱,由注射器注入的样品溶液保留在定量管中;另一个位置(分析位置) 是用实线表示的流路连通,泵将流动相送经定量管,将样品带人色谱住。
进样方式有手动进祥和自动进样两种方式。
图3 六通阀进样系统3色谱分离系统色谱分离系统包括色谱柱和恒温装置。
分离系统性能的好坏是色谱分析的关键。
用最佳的色谱分离系统,充分发挥系统的分离效能是色谱工作中重要的一环。
色谱柱是色谱分离系统的核心,它由柱管和填充固定相构成。
高效液相色谱的柱管多用不锈钢制成,除要求耐高压外,还要求管内壁有很高的光洁度。
高效液相色谱柱的装填比气相色谱柱要求严格得多,目前常用的是匀浆填充法。
填充后的色谱拄需进行柱效测定,以鉴定色谱柱的性能。
我们可以通过选择适当的柱子和流动相使分离达到满意的效果。
柱温也是液相色谱的重要操作参数。
高精度的温度控制对保证色谱柱性能,进行高精度、高重现性的分析是必不可少的。
液相色谱常用柱温范围为室温~65℃。
4检测器高效液相色谱的检测器分为两类,即通用型检测器和选择型检测器。
通用型检测器是以差示测量法来显示出样品和流动相之间某种物理性质上的差异为基础的,但由于它易受外界条件的影响,通常不能用梯度淋洗。
这些检测器包括示差折光检测器,电导率检测器等。
选择型检测器是以测量样品的特有性质为基础,而对温度和流速等外界条件不敏感,灵敏较高,可适用于梯度淋洗。
它们包括紫外可见光检测器、荧光检测器,放射性检测器等。
理想的高效液相色谱检测器,应该具备以下几个特点:①灵敏度高②对各类组分化合物都有响应,或有特殊的选择性;⑦线性范围宽,死体积小,不破坏样品;⑥性能稳定,对温度和流速的变化不敏感,能连续工作、可靠方便。
(1)紫外—可见光检测器紫外一可见光检测器是高效液相色谱中应用最广的捡测器.它对许多样品具有高的灵敏度,检测限可达10-9g/mL、线性范围宽(约为106)。
