初三化学物质检验鉴别专题(可直接打印)讲课稿
初三化学物质检验鉴别专题(可直接打印)
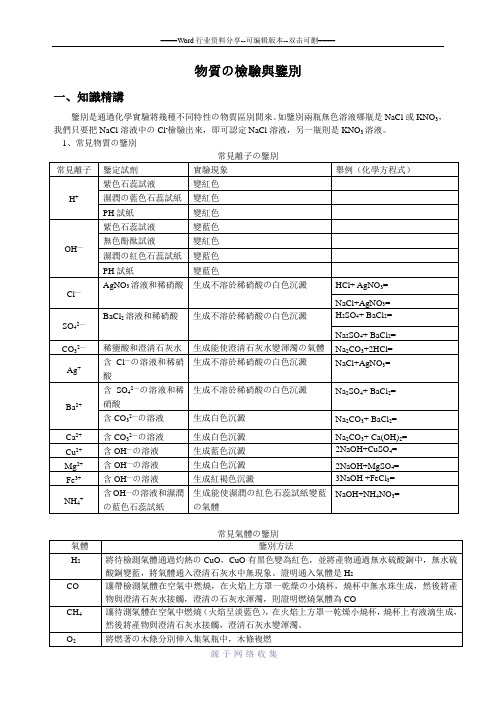
物質の檢驗與鑒別一、知識精講鑒別是通過化學實驗將幾種不同特性の物質區別開來。
如鑒別兩瓶無色溶液哪瓶是NaCl或KNO3,我們只要把NaCl溶液中のCl-檢驗出來,即可認定NaCl溶液,另一瓶則是KNO3溶液。
1、常見物質の鑒別)C、NaOH、CuSO4、NaCl、Ba(NO3)2D、FeCl3、NaOH、Na2SO4、KCl2、下列各組稀溶液中,利用組內物質相互反應,就能加以鑒別の是( )A、Na2CO3、H2SO4、HCl、KNO3B、CuSO4、KOH、NaCl、NaOHC、Na2SO4、Na2CO3、BaCl2、HNO3D、NaNO3、MgCl2、KCl、Ba(OH)23、下列各組溶液中,不用加其他試劑就不能鑒別出來の是()A、CuSO4、BaCl2、HNO3、NaOHB、Na2SO4、BaCl2、Na2CO3、HCl ,C、AgNO3、NaNO3、NaCl、HClD、FeCl3、NaOH、HNO3、Na2SO4,4、下列各種物質の溶液,不另加試劑就無法一一鑒別の是()A、CuSO4 HCl、NaOH、MgSO4B、Na2CO3、HCl、BaCl2、K2SO4C、HCl、CaCl2、NaOH、KNO3D、NH4NO3、H2SO4、NaOH、MgCl25、下列各組溶液,不用其他試劑就能區別出來の是()A、NaOH、HCl、NaClB、Na2CO3、HCl、BaCl2C、Na2CO3、Na2SO4、BaCl2D、AgNO3、HCl、NaCl6、下列各組物質の溶液,不用另加試劑就可以鑒別出來の是(不可加熱,且用化學方法)()A、Na2SO4、BaCl2、NaNO3、KNO3B、CuSO4、NaOH、NaNO3、KClC、NaCl、AgNO3、HCl、NaNO3D、K2CO3、K2SO4、H2SO4、Ba(NO3)27、下列幾組溶液不用其他任何試劑就可以鑒別の是()A、CaCl2、KNO3、Na2CO3、KClB、NaCl、BaCl2、Na2CO3、HCl.C、Na2SO4、Ba(OH)2、Na2CO3、NaNO3D、HNO3、Na2CO3、MgCl2、Ba(OH)2(二)、一次鑒別問題。
初三九年级 化学 复习专题 物质的检验、鉴别与分离、除杂课件

7.现有4种试剂:①紫色石蕊溶液②稀硫酸③碳酸钾溶
液④氯化钡溶液。能用来一次性鉴别稀盐酸、氢氧化钡
溶液、碳酸钠溶液的试剂有( )
A
A ②③ B ②④ C ①②③ D ② ③④
巩固提升
8.用括号内的物质不能区分的一组是 ( D)
A.NaCl、NaOH、NH4NO3 三种固体
(水)
B.K2CO3、Na2SO4、BaC12 三种溶液 (稀硫酸)
Hale Waihona Puke 离子依次检验出来,正确的实验操作顺序是:①滴加 Mg (NO3)2溶液 ②过滤 ③滴加AgNO3溶液 ④滴加Ba(NO3)2溶液( B )
A.①②④②③ C.③②①②④
B.④②①②③ D.④②③②①
常见离子的检验
知识储备
离子 H+
检验方法 滴加紫色石蕊溶液 使用蓝色石蕊试纸 使用pH试纸 加入锌粒等活泼金属(K、Ca、Na除外) 加入Na2CO3等碳酸盐,并将产生的气体通入澄清石灰水
CuO+ H2SO4
CuSO4+ H2O
链接中考
13.除去下列物质中少量的杂质,下列实验方案
能达到实验目的的是( )
C
看试剂 看用量 看操作
选项 A B C D
物质 (括号内为杂质)
CO2(HCl) CuCl2(FeCl2) MnO2(KCl)
NaCl(Na2CO3)
实验方案
先通过NaOH溶液,再通过浓硫酸干燥 先加足量水溶解,再加足量铁粉,过滤 先加足量水溶解,再过滤、洗涤、干燥 先加足量水溶解,再加足量稀硫酸,蒸 发结晶
二. 物质的分离、除杂
知识储备
物理除杂: 化学方法:主要是发生化学反应 除杂原则: (1)主不减:被提纯物质不能和加入的试剂反应。 (2)杂不增:不能引入新的杂质。 (3)易分离:使被提纯物质和杂质转化为不同状 态(气液固),易于分离。
初中九年级化学中考总复习专题物质的检验、鉴别、分离与除杂物质的检验与鉴别课件PPT

溶液变蓝
OH-
滴入少量无色酚酞溶液 用玻璃棒蘸取少量溶液滴在pH试纸上
加入可溶性铜盐
溶液变红 与标准比色卡对照,pH>7
有蓝色絮状沉淀生成
第三部分 专题综合强化
2
离子 - Cl - SO2 4
- CO2 3
Cu2+ + Fe3 Ca2+ NH+ 4 Ag+ Ba2+
检验方法 加入硝酸银溶液和稀硝酸 先加硝酸酸化,再加硝酸钡溶液 滴加稀盐酸,将生成的气体通入澄清 石灰水中 滴加 NaOH 溶液 滴加 NaOH 溶液 滴加可溶性碳酸盐溶液 取少量试剂滴加可溶性碱,加热,将 湿润的红色石蕊试纸放在试管口 滴加少量 NaCl 溶液和稀 HNO3 滴加少量 Na2SO4 溶液和稀 HNO3
2.硬水和软水的鉴别 生活中常用肥皂水来鉴别,加入肥皂水产生泡沫多、浮渣少的是软水,泡沫
少、浮渣多的是硬水。
第三部分 专题综合强化
6
3.化肥的鉴别
a.看外观:氮肥、钾肥都是白色晶体;磷肥是灰白色粉末。 b.加水:氮肥、钾肥都溶于水;磷肥大多不溶于水或微溶于水。
c.加熟石灰研磨:铵态氮肥(铵盐)能放出具有刺激性气味的氨气。
实验现象 生成白色沉淀且不溶解 先无变化,后生成白色沉淀 有气泡产生,石灰水变浑浊 生成蓝色沉淀 生成红褐色沉淀 有白色沉淀生成(可溶于稀硝酸) 有刺激性气味的气体产生,试纸变 蓝 生成白色沉淀且沉淀不溶解 生成白色沉淀且沉淀不溶解
第三部分ቤተ መጻሕፍቲ ባይዱ专题综合强化
3
二、常见气体的检验
气体
O2 CO2
检验方法
初中九年级化学中考总复习专题物质的检验、鉴别、 分离与除杂物质的检验与鉴别课件
第三部分 专题综合强化
1
中考化学 考点聚焦 第17讲 物质的检验与鉴别课件

察到有白色沉淀生成。
请回答下列问题:
硝酸铜、硫酸钠
(1)原固体中一定含有的物质是
。
( 2 ) 原 固 体 中 一 定 不 含 有 的 物 质 是 碳酸氢钠(tàn suān qīnɡ nà) , 证 据 是
__向__固__体__中__加__入__过__量__稀__盐__酸__时__,__无__气__泡___产__生__(_ch_ǎ_n_sh_ē_n_g_)(__或___在__步__骤__Ⅰ__中__未__观__察__到_____
12/12/2021
第十四页,共二十三页。
【方法指导】本题考查的是常见物质的鉴别,完成此题,可以依据已有的物质 的性质结合物质间反应的实验现象进行。根据题干提供的信息进行分析(fēnxī) :碳酸钠溶液既能与盐酸反应生成气体,又能与氯化钙溶液反应生成碳酸钙沉 淀,根据表格可以看出,A既能生成气体,也能生成沉淀。因此,“A”是解答 此题的突破口。由确定A是碳酸钠可依次推出B是盐酸,C是氯化钙,故D是氢氧
12/12/2021
第十一页,共二十三页。
Na2CO3溶液、Ca(OH)2溶液、盐酸、BaCl2溶液,Na2CO3溶液能够与另外 的三种(sān zhǒnɡ)物质产生两种白色沉淀[与Ca(OH)2溶液反应生成碳酸钙白色 沉淀,与BaCl2溶液反应生成碳酸钡白色沉淀]和一种气体(与盐酸反应生成二氧 化碳气体),盐酸能够与Na2CO3溶液反应产生无色气体,与BaCl2溶液不反应,无 明显现象,与Ca(OH)2溶液反应但没有显明现象,Ca(OH)2溶液和BaCl2溶液都 是只与Na2CO3溶液反应生成白色沉淀,与其他物质相遇没有明显现象,因此,不 加任何试剂无法鉴别,C错;CuO粉末、炭粉、铁粉三种黑色粉末可以用稀硫酸(或
中考化学复习专题物质的鉴别、检验、除杂PPT优秀课件

鉴别时常见的现象:
(1)物质的颜色、状态、气味、密度、硬度等 物理性质。
(2)化学反应时有生成气体。 (3)化学反应时生成沉淀。(不同颜色的沉淀也
是鉴别的依据) (4)溶液的酸碱度等。
命题角度:考试题型以填空与简答、实验 探究题型为主。以初中化学中常见物质作为 载体,对几种物质进行鉴别。
物质的除杂: 1.除杂原则 (1)不增:不能引入新杂质。 (2)不减:不能使被提纯的物质减少。 (3)易分:操作简单,易于分离。 2.除杂思路 使杂质转化为与被提纯物质状态不同的物质,然后采用过滤、蒸发 等操作得到 被提纯物质,或者使杂质转化为被提纯物质。
实验目的
实验设计
A
鉴别空气、氧气、二氧化碳
燃着的木条分别伸入集气瓶
B
区分氢氧化钠溶液和碳酸钠溶液 分别滴加无色酚酞溶液
C
鉴别稀盐酸和稀硫酸
D
鉴别稀盐酸和澄清石灰水
分别滴加BaCl2溶液 分别滴加紫色石蕊溶液
中考化学复习专题物质的鉴别、检验 、除杂P PT优秀 课件
中考化学复习专题物质的鉴别、检验 、除杂P PT优秀 课件
中考化学专题复习
检验、鉴别、除杂、分离
复习目标:
1掌握检验物质的基本方法和原理,学会应用常见方法鉴 别物质,了解应用最基本的除杂和分离方法。
2学会用物质的特征和特征反应来区别物质。
3掌握中考题中选择和试验题常考的知识点和方法。
物质鉴别的原理
物质的鉴别:就是利用物质的独特性质, 通过物理或化学方法后,物质会表现出的特 有的现象进行鉴别。 常见物质的鉴别 (1)鉴别硬水和软水用肥皂水。 (2)鉴别天然纤维和合成纤维用燃烧法。 (3)鉴别合金和纯金属用相互刻画法。 (4)鉴别热塑性塑料和热固性塑料用加热法。
九年级化学物质的检验与鉴别优秀课件

Ba(OH) 2
红色
HCl
紫色
NaCl
蓝色
Ba(OH)
2
〔2〕试剂法
HCl NaCl Ba(OH)
2
Na CO 23
气体
无变化
白色沉 淀
HCl NaCl Ba(OH)
2
4.只给你酚酞试液,请鉴别出HCl、NaCl 、Ba(OH) 三种无色溶液? 2
无色酚酞试液
装入C试管内的 液体是Ba(OH)2
物质鉴别与推断 专题复习
一.鉴别依据: 物质的性质特点
二. 知识要点: 三原四步五方法
A.三个根本原那么: 以最简便的方法、用最常见的试剂、看最明显的现象。
B.四个根本步骤〔含格式〕 :
辨色态 → 加试剂 → 看现象 →得结论
C.五个根本方法: 1、观察法〔物质的特殊色味态〕 2、试剂法〔用特殊试剂产生不同现象〕 3、指示剂法〔主要有石蕊、酚酞〕 4、灼烧法〔适用于有机物、金属离子〕 5、物理法〔常见的有加热、溶解、磁铁吸引等〕
H SO 24
HCl
红色消失
NaCl
没有变化
6.不用其他试剂,请你鉴别出CuSO4、 NaOH、 KNO3、MgCl2这四种溶液
白色沉淀 ↑
CuSO NaOH KNO MgCl
4
3
2
↓ 蓝色沉淀
课后提升:思考:题内涉及到哪些方法?
1.以下各组物质的区分方法中,不可行的是( ) A.硬水、软水——加肥皂水,搅拌观察泡 沫的多少 B.羊毛纤维、涤纶——灼烧,闻气味 C.氮气、二氧化碳——用燃着的木条检验, 观察燃烧的现象 D.氯化钾、氯化铵——加熟石灰,研磨, 闻气味
2.现有两瓶失去标签的无色溶液,分别是稀盐 酸(HCI)和(NaOH)烧碱溶液。要区别这两种溶 液,以下方法不能够到达目的的是〔 〕
中考化学专题复习:物质的检验与鉴别 课件

.
.
.
取少量样品于试 有气泡产生的是碳酸钠溶
管中,然后加入 液,无现象的是氢氧化钠
盐酸溶液
溶液
取样于试管中, 有沉淀产生的是碳酸钠溶
然后加入氯化钙 液,无现象的是氢氧化钠
溶液
溶液
链接中考:
(2014盐城):下列物质的鉴别方法不正确( ) A.用水鉴别氯化钠固体和硝酸铵固体 B.用闻气味的方法鉴别水和酒精 C.用磁铁吸引来区分铁丝和铝丝 D.用熟石灰来区分氯化铵和碳酸氢铵
现象
结论
O2 H2
CO
知识点:一、物质的检验
1、常见气体的检验:CO2、O2、 CO、H2等
气体 检验方法
现象
结论
CO2 通入澄清的石灰水中 澄清石灰水变 气体是CO2 浑浊
O2 用带火星的木条伸入集 木条复燃 气瓶中
气体是O2
H2 点燃气体,将干冷烧杯 烧杯内壁有出 气体是H2
罩在火焰上方
现_________
实验目的
方法
检验某固体是否是碳酸 加入稀盐酸,观察是否有气
盐
泡冒出
B
检验某溶液是否是碱性 滴加紫色石蕊试液,观察是
溶液
否变蓝
C
检验甲烷中是否有碳元 将燃烧产物通入澄清石灰水
素
中
D
检验某物质中是否含有 加氢氧化钠溶液,观察是否
铵根离子
有气泡冒出
归纳总结:物质的检验
1.依据:被检验物质的特性,选择 适当的试剂和方法 2.方法:步骤→现象→结论。
知识点:二、物质的鉴别:
氢氧化钠溶液、碳酸钠溶液的鉴别
试剂:酚酞溶液、二氧化碳、氢氧化钙溶液、
氯化钙溶液
常见 方案 步骤 物质
九年级化学复习课物质的鉴别公开课

九年级化学复习课:物质的鉴别(教案)知识与技能:通过三类题型解决方法的归纳总结,加深学生对离子的检验方法的理解,学会常见物质鉴别的基本方法,并能应用其解决生产生活中的实际问题。
过程与方法:1、通过学生分组讨论、比较、探索和归纳,使学生在探索中学会学习方法,发展求异思维,培养学生知识构建的能力和创新精神。
2、在小组合作中,让学生自主学习,培养自主探索能力和实验设计能力。
情感态度与价值观:通过探索活动,培养学生自主、探索、自信的学习态度及协作精神,激发学生学习化学的兴趣,感受化学知识的无穷魅力,提高科学素质。
[重点]:常见的离子的检验方法[难点]:运用物质鉴别方法解决实际问题[教学方法]:比较归纳法、探索法、讨论法[教具]:多媒体[教学过程]:1、总论:物质鉴别是根据物质之间的性质差异,将组内物质相互区别开,故重在区别,与鉴定某一种物质不彻底相同。
原则上要求操作简便易行,叙述时应按照操作→现象→结论的顺序。
2、方法:例1:鉴别酒精与白醋时,是利用了二者不同的性质。
小结:(1)物理方法:所给物质间有明显的物理性质的差异时,应先用来鉴别,如物质的颜色、气味、溶解性等,这些性质应用的方法很简便。
例2:鉴别下列物质稀HCl 、石灰水、NaCl 三种溶液小结:(2)化学方法:在用物理方法难以鉴别时就要利用组内物质化学性质间的差别来鉴别。
A 、酸碱性:同组内物质的溶液酸碱性若不同,可借助紫色石蕊试液或者酚酞试液来区分。
若物质较多,也可以借助指示剂先行分组,再在各组内鉴别。
例3:鉴别下列物质稀HCl 、NaOH 、Na2CO3、Na2SO4四种溶液B 、重要离子法:依据一些特殊离子发生反应的不同现象来鉴别,具体有: ,不溶于稀硝酸)(白色加AgCl 3AgNO ↓−−−→−-Cl较多)为避免混淆,往往用(白色加234B 24)Ba(NO ,SO 2BaSO a ↓−−→−+-阴离子 (特殊氨味)无色加铵盐等↑−−−→−-OH))或者稀(可溶于稀白色使澄清石灰水变浑浊(无色或者加加酸⎪⎩⎪⎨⎧↓−−−−−→−↑−−→−+-32H 23HNO HCl CO CO 22BaCl CaCl 小结:利用化学方法鉴别时,不管是根据酸碱性还是离子法,都是依据反应时现象的不同,如不同的颜色、产生沉淀、生成气体等加以鉴别。
九年级毕业会考化学专题复习物质的检验与鉴别

九年级毕业会考化学专题复习物质的检验与鉴别张家界市民族中学覃念[教学目标]1.知识与技能(1)学生通过实验归纳出物质的检验与鉴别的方法。
(2)学生通过学习能准确的、迅速的解题。
(3)学生通过学习能鉴别日常生活中的物质,能学以致用、辨别真伪。
2.过程与方法(1)通过对物质的检验与鉴别的实验探究,逐步提高学生的探究能力、动手操作能力。
(2)通过小组合作,培养学生的合作能力和语言表达能力。
(3)通过课堂练习,提高分析问题、解决问题能力。
3.情感态度与价值观(1)体验科学探究的过程,从探究中获得成功的喜悦。
(2)在设计实验的过程中,培养学生的创新精神、实践能力,以及严谨求实的科学态度。
[教学重点与难点]重点:物质的检验与鉴别难点:物质的检验与鉴别的方法以及实验步骤、现象、结论的表达。
[教学方法]实验探究教学法、分组讨论、归纳比较[教学准备]1.多媒体课件、教案、学生学案。
2.准备实验用品学生实验仪器:试管(每组6支)、标签(每组12个)、药匙(每组3把)、试管架(每组1个)、小烧杯(每组3个)、玻璃棒(每组3根)学生实验药品:硫酸铜溶液(不贴标签,在瓶上标①)、氢氧化钠溶液(不贴标签,在瓶上标②)、稀盐酸溶液(不贴标签,在瓶上标③)、生石灰粉末(不贴标签,在瓶上标④)、熟石灰粉末(不贴标签,在瓶上标⑤)、碳酸钙粉末(不贴标签,在瓶上标⑥)、酚酞溶液(贴标签)、蒸馏水(用塑料瓶盛装、贴标签)按每小组6人,将全班分成10小组。
[课型]复习课[板书设计]:专题复习物质的检验与鉴别一、初中常见离子的检验二、综合型鉴别题三、方法归纳1、物质检验的鉴别的依据(1)先根据物质的物理来检验和鉴别如看颜色、闻气味、测密度、溶解性等(2)再依据物质反应是时产生的特殊现象(即化学性质)如产生沉淀、放出气体、变色、燃烧产生的不同现象2、鉴别方法选择的原则:最简单的操作;最明显的现象;最明确的结论。
3、实验步骤:取样编号—加试剂—观察现象—得出结论。
(完整版)初三化学物质检验鉴别专题(可直接打印)
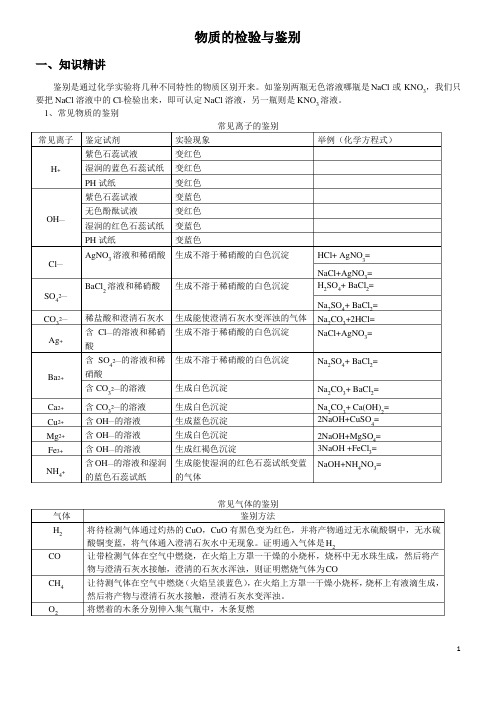
物质的检验与鉴别一、知识精讲鉴别是通过化学实验将几种不同特性的物质区别开来。
如鉴别两瓶无色溶液哪瓶是NaCl 或KNO 3,我们只要把NaCl 溶液中的Cl -检验出来,即可认定NaCl 溶液,另一瓶则是KNO 3溶液。
1、常见物质的鉴别常见离子的鉴别常见离子鉴定试剂实验现象举例(化学方程式)紫色石蕊试液变红色H +湿润的蓝色石蕊试纸变红色PH 试纸变红色紫色石蕊试液变蓝色OH —无色酚酞试液变红色湿润的红色石蕊试纸变蓝色PH 试纸变蓝色Cl —AgNO 3溶液和稀硝酸生成不溶于稀硝酸的白色沉淀HCl+ AgNO 3=NaCl+AgNO 3=2—BaCl 2溶液和稀硝酸生成不溶于稀硝酸的白色沉淀H 2SO 4+ BaCl 2=SO 4Na 2SO 4+ BaCl 2=CO 32—稀盐酸和澄清石灰水生成能使澄清石灰水变浑浊的气体Na 2CO 3+2HCl=Ag +含Cl —的溶液和稀硝生成不溶于稀硝酸的白色沉淀NaCl+AgNO 3=酸含SO 42—的溶液和稀生成不溶于稀硝酸的白色沉淀Na 2SO 4+ BaCl 2=Ba 2+硝酸含CO 32—的溶液生成白色沉淀Na 2CO 3+ BaCl 2=Ca 2+含CO 32—的溶液生成白色沉淀Na 2CO 3+ Ca(OH)2=Cu 2+含OH —的溶液生成蓝色沉淀2NaOH+CuSO 4=Mg 2+含OH —的溶液生成白色沉淀2NaOH+MgSO 4=Fe 3+含OH —的溶液生成红褐色沉淀3NaOH +FeCl 3=NH +含OH —的溶液和湿润生成能使湿润的红色石蕊试纸变蓝NaOH+NH 4NO 3=4的蓝色石蕊试纸的气体常见气体的鉴别气体鉴别方法H 2将待检测气体通过灼热的CuO ,CuO 有黑色变为红色,并将产物通过无水硫酸铜中,无水硫酸铜变蓝,将气体通入澄清石灰水中无现象。
证明通入气体是H 2CO 让带检测气体在空气中燃烧,在火焰上方罩一干燥的小烧杯,烧杯中无水珠生成,然后将产物与澄清石灰水接触,澄清的石灰水浑浊,则证明燃烧气体为COCH 4让待测气体在空气中燃烧(火焰呈淡蓝色),在火焰上方罩一干燥小烧杯,烧杯上有液滴生成,然后将产物与澄清石灰水接触,澄清石灰水变浑浊。
中考化学专题复习--物质的检验与鉴别课件(22张)

D.酚酞试液
【变式练习】 (202X·泰安新泰期末)实验室有一包白色固体由 K2CO3、K2SO4、KCl和 CuSO4中的一种或几种组成,实验记录如下: ①取该样品溶于水,得到无色溶液; ②取适量上述溶液加过量的BaCl2溶液,出现白色沉淀,过滤; ③向步骤②所得沉淀中加入过量的稀HNO3,沉淀全部消失并产生气泡。
物质 硬水和软水
检验试剂或方 法
棉花、羊毛、 合成纤维
NH4NO3和NaOH 固体
二氧化锰和氧 化铜
铵态氮肥的鉴 别
现象
常见物质的检验
物质
硬水和软水
棉花、羊毛、 合成纤维
NH4NO3和NaOH 固体 二氧化锰和氧 化铜 铵态氮肥的鉴 别
检验试剂或方 法
现象
肥皂水(等量) 出现泡沫多,浮渣少的是软水,反之是硬水
是(C )
选项
实验目的
实验方法
A 检验一瓶气体是否为氧气
将带火星的木条伸入瓶中
B
鉴别空气和氧气
C
鉴别食盐和白糖
将燃着的木炭放入集气瓶中 视察颜色进行区分
D 验证浓度对反应的影响 将燃着的木条分别伸入氧气和空气中
【变式训练】
如果要鉴别CO、H2、CH4三种气体,最好的方法( D)
A. 闻气味
B. 检验是否能让澄清的石灰水变浑浊
常见离子的检验
被检验 的离子
方法
H+
OH- CO32NH4+
现象
常见离子的检验
被检验 的离子
方法
1、石蕊溶液
H+
2、pH试纸 3、加入活泼金属(如Zn)
4、加入碳酸盐(Na2CO3或CaCO3)
1、石蕊溶液(或酚酞溶液) OH- 2、pH试纸
中考化学复习 专题三 物质的检验、鉴别、除杂与提纯课件

滴入可溶性的碳
有白色沉淀生
Ca2+ 酸盐(如Na2CO3)
成
Na2CO3+CaCl2===CaCO3↓+2NaCl
溶液
12/12/2021
第七页,共二十七页。
离子 检验方法
现象
原理举例(化学方程式)
滴入NaCl溶液和 Ag+
有白色沉淀生,该沉 AgNO3+NaCl===AgCl↓+NaNO3
稀硝酸
12/12/2021
第十一页,共二十七页。
高锰酸钾;黑色固体:铁粉、木炭、氧化铜、二氧化锰、四氧化三铁、 炭黑、活性炭。
b.常见溶液(róngyè)的颜色 蓝色溶液:含Cu2+的溶液;浅绿色溶液:含 Fe2+的溶液;黄色溶液:含Fe3+的溶液。
②根据气味的不同
常见的具有刺激性气味的气体有:HCl、SO2、NH3。 ③根据物质的溶解性不同 ④根据物质溶解时的吸放热现象:NaOH溶于水放出热量,温度升高;NaCl溶于 水温度保持不变;NH4NO3溶于水吸收热量,温度降低。
物质提纯的基本原则:1.不引入新的杂质。2.不减少被提纯物质。3.被 提纯物质与杂质易分离。4.被提纯物质易复原。
12/12/2021
第三页,共二十七页。
一、物质的检验(jiǎnyàn) 1.常见离子的检验
类型精讲
离子
检验方法
现象
原理举例(化学方程式)
①滴入紫色石蕊溶液 石蕊溶液变红
—
H+ ②pH试纸测酸碱度
Ca(OH)2+CO2=rá=n=)CaCO3↓+H2O
火焰呈淡蓝色,干燥的
点燃,在火焰上方罩一 烧杯内壁有水雾出现,
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初三化学物质检验鉴别专题(可直接打印)
物质的检验与鉴别
一、知识精讲
鉴别是通过化学实验将几种不同特性的物质区别开来。
如鉴别两瓶无色溶液哪瓶是NaCl或KNO3,我们只要把NaCl溶液中的Cl-检验出来,即可认定NaCl溶液,另一瓶则是KNO3溶液。
1、常见物质的鉴别
常见离子的鉴别
常见气体的鉴别
)
C、NaOH、CuSO4、NaCl、Ba(NO3)2
D、FeCl3、NaOH、 Na2SO4、 KCl
2、下列各组稀溶液中,利用组内物质相互反应,就能加以鉴别的是 ( )
A、Na2CO3、H2SO4、HCl、KNO3
B、CuSO4、KOH、NaCl、NaOH
C、Na2SO4、Na2CO3、BaCl2、HNO3
D、NaNO3、MgCl2、KCl、Ba(OH)2
3、下列各组溶液中,不用加其它试剂就不能鉴别出来的是()
A、CuSO4、BaCl2、HNO3、NaOH
B、Na2SO4、BaCl2、Na2CO3、HCl ,
C、AgNO3、NaNO3、NaCl、HCl
D、 FeCl3、NaOH、HNO3、Na2SO4,
4、下列各种物质的溶液,不另加试剂就无法一一鉴别的是()
A、CuSO4 HCl、NaOH、MgSO4
B、Na2CO3、HCl、BaCl2、K2SO4
C、HCl、CaCl2、NaOH、KNO3
D、NH4NO3、H2SO4、NaOH、MgCl2
5、下列各组溶液,不用其它试剂就能区别出来的是()
A、NaOH、HCl、NaCl
B、Na2CO3、HCl、BaCl2
C、Na2CO3、Na2SO4、BaCl2
D、AgNO3、HCl、NaCl
6、下列各组物质的溶液,不用另加试剂就可以鉴别出来的是(不可加热,且用化学方法)()
A、Na2SO4、BaCl2、NaNO3、KNO3
B、CuSO4、NaOH、NaNO3、KCl
C、NaCl、AgNO3、HCl、NaNO3
D、K2CO3、K2SO4、H2SO4、Ba(NO3)2
7、下列几组溶液不用其它任何试剂就可以鉴别的是()
A、CaCl2、KNO3、Na2CO3、KCl
B、NaCl、BaCl2、Na2CO3、HCl.
C、Na2SO4、Ba(OH)2、Na2CO3、NaNO3
D、HNO3、Na2CO3、MgCl2、Ba(OH)2
(二)、一次鉴别问题。
8、只用一种试剂就能将Na2CO3 NH4Cl 、NaCl 三种溶液区分开来的是()
A、澄清石灰水
B、CaCl2溶液
C、NaOH溶液
D、稀盐酸
9、只用一种试剂就可将Ba(OH)2、稀硫酸、KOH三种溶液鉴别出来的是()
A、K2CO3溶液
B、NaCl溶液
C、石蕊试液
D、酚酞试液
10、欲鉴别石灰水、稀盐酸、蒸馏水三瓶失去标签的无色液体,提供的试剂有:①纯碱溶液②紫色石蕊③酚酞试液。
只用一种试剂可将它们鉴别出来的是()
A、只有①
B、只有②
C、①或②
D、①或②或③
11、利用无色酚酞可以鉴别的一组溶液是()
A、BaCl2、H2SO4、HCl
B、NaOH 、KOH 、HCl
B、K2CO3、Na2CO3、HCl D、NaCl、NaOH 、HCl
12、只用一种试剂就能将(NH4)2SO4、NH4Cl、NaCl、Na2SO4四种溶液区分开来,这种试剂是()
A、AgNO3溶液
B、BaCl2溶液
C、NaOH溶液
D、 Ba(OH)2溶液
13、用一种试剂区别硫酸铜、氯化镁、氯化铁、氯化钠四种物质,这种试剂是()
A、硝酸银
B、氢氧化钠
C、氯化钡
D、盐酸
14、要鉴别NaCl、MgCl2、酚酞三瓶无色溶液,可选用下列试剂中的()
A、AgNO3溶液
B、HCl溶液
C、石蕊试液
D、NaOH溶液
(三)、鉴别顺序问题。
15、按下列添加试剂的先后顺序,即可将稀盐酸、稀硫酸、硫酸钾、氢氧化钠和硝酸钾五种无色
溶液鉴别开来的是()
A、石蕊试液、AgNO3溶液、HNO3
B、BaCl2溶液、酚酞试液、AgNO3溶液
C、石蕊试液、BaCl2溶液
D、酚酞试液、BaCl2溶液、AgNO3溶液
16、不用其它任何试剂鉴别下列5种物质的溶液:① NaOH ② MgSO4③Ba(NO3)2④ Cu(NO3)2⑤
KNO3,被鉴别出来的正确顺序是()
A、⑤④③②①
B、④③①②⑤
C、④①②③⑤
D、②③①④⑤
17、下列溶液,不用外加试剂(可组内结合)鉴别出来的先后顺序是 ( )
①氯化铁②硝酸钾③氯化镁④氢氧化钠
A、①②③④
B、①④③②
C、④①②③ C、①③④②
18、现有①NaOH ②Al2(SO4)3③Ba(NO3)2④FeCl3⑤NaCl 五种溶液,不用其它试剂,要用最简便的方法,被鉴别出来的物质顺序是()
A、①②③④⑤
B、④①②③⑤
C、②③①④⑤
D、④⑤②③①。
