【襄樊五中】第12章《烃》第3节《乙烯烯烃》第2课时
化学:5.3《乙烯 烯烃》第二课时课件(旧人教版必修2)

3. 既可以使溴水褪色 又可以使酸性高锰酸钾溶 既可以使溴水褪色,又可以使酸性高锰酸钾溶 液褪色的气体有 (
C)
B. CO2
A. CO
C. C2H4
D. C2H6
4. 乙烯发生的下列反应中 不属于加成反应 乙烯发生的下列反应中,不属于加成反应 的是 ( D ) A. 与氢气反应生成乙烷 B. 与水反应生成乙醇 C. 与溴水反应使之褪色 D. 与氧气反应生成二氧化碳和水
第三节
乙
烯
烯烃
第二课时
三. 乙烯的物理性质
通常情况下,乙烯是一种无色稍有气味的气体 通常情况下 乙烯是一种无色稍有气味的气体, 乙烯是一种无色稍有气味的气体 密度比空气略小,难溶于水 难溶于水. 密度比空气略小 难溶于水
四.乙烯的化学性质 乙烯的化学性质
乙烯分子的结构特点 C=C双键所具有的能量并不是 双键所具有的能量并不是C-C单键的 倍, 单键的2倍 双键所具有的能量并不是 单键的 而是小于2倍 双键的键长也不是C-C单键的 而是小于 倍;C=C双键的键长也不是 双键的键长也不是 单键的 一半,而是大于C-C单键的一半,所以乙烯分子中 单键的一半, 一半,而是大于 单键的一半 C=C双键中的两个键是不一样的,其中一个键容 双键中的两个键是不一样的, 双键中的两个键是不一样的 易断裂不稳定,乙烯的化学性质比乙烷活泼。 易断裂不稳定,乙烯的化学性质比乙烷活泼。
书写以下物质所发生的加聚反应 1、CH2=CHCH2CH2CH3 2、CH2=CHCH=CH2 3、CH2=CH2与CH2=CHCH3
如何确定加聚反应生成的高聚物的单体? 如何确定加聚反应生成的高聚物的单体? 高聚物的单体 小手缩回来,邻碳快牵上, 小手缩回来,邻碳快牵上, 若无双变单,单键就断掉。 若无双变单,单键就断掉。
高二化学教案-第三节乙烯烯烃002 最新
第三节 乙烯 烯烃[教学目标]1、使学生了解乙烯的物理性质和主要用途,掌握乙烯的化学性质和实验室制法。
2、使学生了解加成反应和聚合反应以及不饱和烃的概念。
3、使学生了解烯烃在组成、结构、重要的化学性质质上的共同点,以及物理性质随分子中碳原子数目的增加而变化的规律性。
[知识讲解]一、乙烯的分子结构 1、不饱和烃:断裂,这决定了乙烯的化学性质比较活泼。
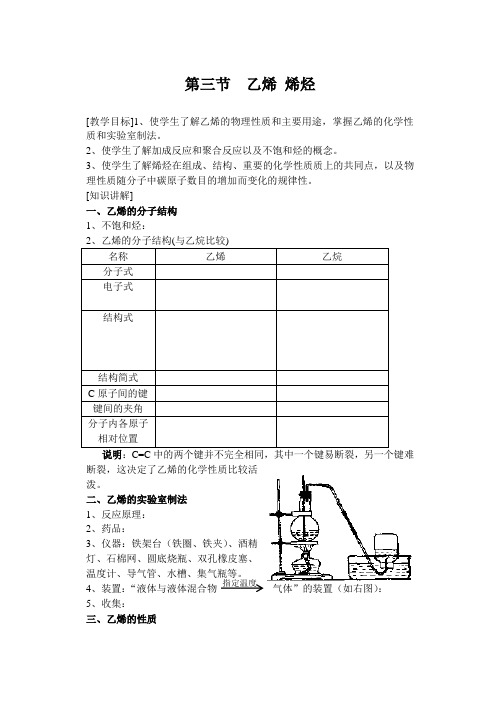
二、乙烯的实验室制法 1、反应原理: 2、药品:3、仪器:铁架台(铁圈、铁夹)、酒精灯、石棉网、圆底烧瓶、双孔橡皮塞、温度计、导气管、水槽、集气瓶等。
4、装置:“液体与液体混合物 气体”的装置(如右图):5、收集:三、乙烯的性质 指定温度1、物理性质:通常情况下,乙烯是无色、稍有气味的气体,密度与空气相近,难溶于水。
2、化学性质:1)氧化反应①易燃烧,燃烧时火焰明亮,产生黑烟。
完全燃烧时:②常温下易被氧化剂(如KMnO4溶液等)氧化。
可使酸性KMnO4溶液褪色。
此反应可用于烯烃与其它烷烃气体的鉴别。
2)加成反应:说明:①乙烯与溴水的反应常用于烷烃与烯烃的鉴别,也可用来除去混在气态烷烃中的气态烯烃。
②寻找出某些有机物的最适宜的制备途径。
如氯乙烷的制备,有乙烷与Cl2取代反应和乙烯与HCl的加成反应两条途径,显然前者会产生多种氯代产物,而后者产物单一,当然选择后一种方法好。
③加成反应的发生与否是不饱和烃与一般饱和烃在化学性质上最明显的差别,凡能发生加成反应的烃通常是不饱和烃。
3)聚合反应:四、乙烯的用途1、乙烯是石油化学工业最重要的基础原料。
主要用于制造塑料、合成纤维、有机溶剂等。
乙烯工业的发展水平,已成为衡量这个国家石油化学工业水平的重要标志之一。
2、乙烯是一种植物生长调节剂。
它可以催熟果实。
五、烯烃1、概念:2、通式:3、物理性质:碳原子数小于5的烯烃常温呈( )态。
一般地烯烃分子中碳原子数越多,其熔、沸点越( ),相对密度越( )。
4、化学性质1)氧化反应①易燃烧②使KMnO4溶液褪色2)加成反应——不饱和烃的共性3)加聚反应——烯烃的共性①一种单体:②二种单体:[典型例题]例1、下列混合气体中,比乙烯中碳质量分数高的是()A、甲烷+丙烯B、乙烯+丁烷C、乙炔+丙烯D、乙烯+丁烯例2、10mL某气态烃,在50mLO2里充分燃烧,得到液态水和体积为35mL的混合气体(所有气态体积都是在同温同压测定的)。
【襄樊五中】第12章《烃》第4节《乙炔炔烃》第2课时

高二化学第五章烃第四节乙炔炔烃(2课时)第二课时【说明】:本练习配套人教版化学读本,题目有一定的难度,适合省级示范高中或一些学校的优生使用,也可以作为高三第一轮复习的资料适用。
完成本练习的时间为30分钟,如果是高三第一轮复习,完成时间为20分钟。
后面有配套的标准答案,是经过认真审查的。
【练习题】1.据报道,1995年化学家合成了一种分子式为C200H200的含多个碳碳叁键(-C≡C-)的链状烃,其分子中含碳碳叁键最多可以是()A.49个B.50个C.51个D.100个2.下列关于分子组成为C x H y的烷、烯、炔烃的说法中不正确的是 [ ]A.当x≤4时,常温常压下均为气体B.y一定为偶数C.分别完全燃烧1mol时,耗氧(x+y/4)molD.在密闭的容器中完全燃烧时,150℃时测得的压强一定比燃烧前增加3.化学式为C5H7Cl的有机物,其结构不可能是()A、只含有一个双键的直链有机物B、只含有两个双键的直链有机物C、含有一个双键的环状有机物D、含有一个三键的直链有机物4.1体积某气态烃A最多和2体积HCl加成,生成氯代烷烃,1mol此氯代烷烃能和4molCl2发生取代反应,生成物只有碳、氯两种元素,则A的化学式为 [ ]A、C3H4B、C2H4C、C4H6D、C2H25.某烃W与溴水的加成反应产物是2,2,3,3—四溴丁烷,与W属同系物的是[]A.乙炔 B.2—丁烯 C.1,3—丁二烯 D.异戊二烯6.某炔烃氢化后得到的饱和烃如下:CH3-CH2-CH2-CH3,该烃可能的结构有()A.1种B.2种C.3种D.4种7.下列各组中的烃一定互为同系物的是()A.C3H4和C5H8B.C3H8和C5H12C.C3H6和C5H10D.C2H2和C2H48.1995年美国教授Lagow制得了磁碳的第四种同素异形体一一链式炔烃:…-C≡C-C≡C-C≡C-…该物质的一个分子中含300~500个碳原子,性质很活泼。
【襄樊五中】第13章《烃的衍生物》第1节《溴乙烷》第2课时

高二化学第六章烃的衍生物第一节溴乙烷卤代烃(2课时)第二课时【说明】:本练习配套人教版化学读本,题目有一定的难度,适合省级示范高中或一些学校的优生使用,也可以作为高三第一轮复习的资料适用。
完成本练习的时间为30分钟,如果是高三第一轮复习,完成时间为20分钟。
后面有配套的标准答案,是经过认真审查的。
【习题内容】1 常温下为气态的有机化合物是()A 一氯甲烷B 甲苯C 氯仿D 1—氯丙烷2 下列烃中,其一氯代物不止一种的是()A 新戊烷B 乙烷C 对二甲苯D 苯3 分子式为C4H9Cl的有机物有()A 2种B 3种C 4种D 5种4 2,3—二甲基丁烷的一氯代物有()A 2种B 3种C 4种D 5种5 对—二甲苯苯环上的二氯取代物有()A 2种B 3种C 4种D 5种6 组成为C3H2Cl6的卤代烃,可能存在的同分异构体有()A 3种B 4种C 5种D 6种7 臭氧层是地球的保护伞,它对紫外线有吸收和阻挡作用。
由于冰箱中致冷剂——氟利昂的泄漏,导致臭氧层破坏,使透射到地面的紫外线辐射增强,危及人类生存环境。
氟利昂是一种低沸点卤代烃,易挥发,进入大气层后,在紫外线作用下光解出Cl•它能促使O3转化成O2,其方程式为Cl•+ O3→ClO•+ O2,ClO•+ O→Cl•+ O2。
则Cl•在反应中充当()A.反应物 B.催化剂 C.媒介物 D.生成物8 一种新型的灭火剂叫“1211”,其分子式是CF2ClBr。
命名方法是按碳、氟、氯、溴的顺序分别以阿拉伯数字表示相应元素的原子数目(末尾的“0”可略去)按此原则,对下列几种新型灭火剂的命名不正确...的是()A CF3Br — 1301B CF2Br2— 122C C2F4Cl2— 242D C2ClBr2— 20129 六氯苯是被联合国有关公约禁止或限制使用的有毒物质之一。
下式中能表示六氯苯的是A BC D10 氯仿(CHCl3)可用作麻醉剂,但常因保存不慎而在光照下被空气中的氧氧化成剧毒的光气(COCl2)和氯化氢。
高二化学第三节 乙烯、烯烃人教版知识精讲

高二化学第三节 乙烯、烯烃人教版【本讲教育信息】一. 教学内容:第三节 乙烯、烯烃二. 教学目标:1. 了解乙烯的物理性质和用途,掌握乙烯的化学性质和制法。
2. 了解加成、聚合以及不饱和烃的概念。
3. 了解烯烃在组成结构、物理、化学性质上的异同。
三. 教学重点、难点:重点:乙烯的化学性质和实验室制法。
难点:聚合反应、乙烯的实验室制法。
四. 知识分析:1. 乙烯的分子结构和性质(1)结构:平面结构,键角为︒120,结构式是H HH —C ===C —H ,结构简式是22CH CH =。
(2)物理性质:无色、稍有气味,难溶于水,比空气略轻的气体。
(3)化学性质① 氧化反应O H CO O CH CH 22222223+−−→−+=点燃褪色−−−−→−=+)(422H KMnO CH CH② 加成反应⎪⎪⎩⎪⎪⎨⎧−−−→−→→−−−→−+=)(2322322233222制酒精催化剂催化剂OH CH CH O H ClCH CH HCl Br CH BrCH Br CH CH H CH CH③ 聚合反应---−−→−=n CH CH CH nCH ][2222催化剂聚乙烯2. 乙烯的制法和用途(1)工业制法以石油为原料制得(2)实验室制法药品:浓硫酸、酒精原理:O H CH CH OH CH CH CSOH 2224223170+↑=−−−→−︒浓 装置:与制取2Cl 、HCl 等的装置类似。
收集:排水法收集。
(3)用途重要的化工原料,可用于制造塑料、合成纤维、有机溶剂、植物生长调节剂等。
3. 烯烃(1)组成:通式是)2(2≥n H C n n(2)结构:链烃,分子中只含一个碳碳双键。
(3)性质① 物理性质相对密度增大熔点、沸点升高相对分子质量增大一系列烯烃分子组成与结构相似的−−−−−−−−−−−−−−→− ② 化学性质a . 能使酸性4KMnO 溶液褪色b . 能燃烧,燃烧通式为:O nH nCO O n H C n n 222223+−−→−+点燃 c . 加成反应,与2H 、2X 、HX 、O H 2等加成。
【襄樊五中】第12章《烃》第3节《乙烯烯烃》第1课时

高二化学第五章烃第三节乙烯烯烃(2课时)第一课时【说明】:本练习配套人教版化学读本,题目有一定的难度,适合省级示范高中或一些学校的优生使用,也可以作为高三第一轮复习的资料适用。
完成本练习的时间为30分钟,如果是高三第一轮复习,完成时间为20分钟。
后面有配套的标准答案,是经过认真审查的。
【练习题】1.下列反应属于取代反应的是 [ ]A、乙烯生成聚氯乙烯的反应B、乙醇与浓硫酸混合加热至170℃C、乙烯与氯化氢在一定条件下反应D、乙烷与氯气的混合物在光照条件下反应2.关于实验室制备乙烯的实验,下列说法正确的是 [ ]A、反应物是乙醇和过量的3mol/L硫酸的混和液B、温度计插入反应液面以下,以控制温度在140℃C、反应容器中应加入少许瓷片D、反应完毕先灭火再从水中取出导管3.下列物质中既能使溴水褪色又能使酸性高锰酸钾溶液褪色的是 [ ]A、SO3B、C2H4C、CH4D、HCl4.当前我国环保亟待解决的“白色污染”,通常所指的是 [ ]A、冶炼厂的白色烟尘B、石灰窑的白色粉尘C、聚乙烯等塑料垃圾D、白色建筑废料5.可以用来鉴别甲烷和乙烯, 又可以用来除去甲烷中混有的少量乙烯的操作方法是 [ ] A.混合气通过盛酸性高锰酸钾溶液的洗气瓶B.混合气通过盛足量溴水的洗气瓶C.混合气通过盛水的洗气瓶D.混合气跟氯化氢混合6.将15克甲烷与乙烯的混合气通入盛有溴水(足量)的洗气瓶, 反应后测得溴水增重7克, 则混合气中甲烷和乙烯的体积比为 [ ]A.2∶1 B.1∶2 C.3∶2 D.2∶37.下列物质中, 所有的原子都在同一平面上的分子是 [ ]A.氨气 B.乙烷 C.甲烷 D.乙烯8.乙烯发生的下列反应中,不属于加成反应的是 [ ]A.与氢气反应生成乙烷B.与水反应生成乙醇C.与溴水反应使之褪色D.与氧气反应生成二氧化碳和水9.关于乙烯分子结构的说法中,错误的是 [ ]A.乙烯分子里含有C=C双键B.乙烯分子里所有原子共平面C.乙烯分子中C=C双键键长和己烷分子中C-C单键的键长相等D.乙烯分子里各共价键之间夹角为120O10.实验室制取乙烯时,需要用到浓硫酸,它的作用是 [ ]①反应的原料②脱水剂③催化剂④干燥剂A 只有②B 只有②④C 只有①D 只有②③11.把1L含乙烯和氢气的混和气体通过镍催化剂,使乙烯和氢气发生加成反应,完全反应后,气体体积变为yL(气体体积均在同温同压下测定),若乙烯1L混和气体中的体积分数为x%,则x和y的关系一定不正确的是 [ ]A y=1·x%B y=(1-1·x%)C y=1·x%=0.5D y=(1-1·x%)<0.512.甲烷和乙烯混和气体完全燃烧时,消耗相同状况下的氧气是混和气体的2.4倍,则甲烷与乙烯的体积比是 [ ]A 3︰2B 1︰1C 2︰3D 1︰313.实验测得乙烯与氧气混和气体的密度与空气相同,可知其中乙烯的质量分数是 [ ]A 25.0%B 72.4%C 27.6%D 75.0%14.把mmol C2H4跟nmol H2 混合在密闭容器中,在适当条件下,反应达到平衡时生成pmolC2H6,若将所得平衡混和气体完全燃烧生成二氧化碳和水,需要氧气的量是 [ ]A (3m+n)molB (3m+n/2)molC (3m+3p+n/2)molD (3m+n/2-3p)mol15.(4分)有下列反应.①由乙烯制氯乙烷②乙烷在空气中燃烧③乙烯使溴水褪色④乙烯通入酸性高锰酸钾溶液⑤由乙烯制聚乙烯⑥乙烷与氯气光照其中属于取代反应的是________;属于氧化反应的是________;属于加成反应的是________;属于聚合反应的是__________16.将乙烯通入溴的四氯化碳溶液中,观察到的现象是;其反应方程式为。
2019-2020年高中化学《乙烯烯烃》第一课时教案 大纲人教版

2019-2020年高中化学《乙烯烯烃》第一课时教案大纲人教版●教学目标1.使学生了解乙烯的物理性质和主要用途,掌握乙烯的分子结构、化学性质和实验室制法,以培养学生分析思维、比较思维的能力;2.理解加成反应和聚合反应;3.了解不饱和烃的概念和烯烃在组成、结构、重要化学性质上的共同点,以及物理性质随分子中的碳原子数目的增加而变化的规律性;4.通过学习对比、体会物质结构与物质性质之间的“内因—外因”的辩证关系。
●教学重点1.乙烯的分子结构、化学性质及实验室制法;2.加成反应和聚合反应。
●教学难点乙烯的实验室制法。
●课时安排一课时●教学方法1.通过制作分子模型使学生认识和理解乙烯的分子结构特点;2.通过教学软件模拟使学生掌握实验室制乙烯的反应原理;3.通过实验演示使学生理解和掌握乙烯重要的化学性质;4.通过引导、投影显示、自学等方法使学生理解乙烯的聚合反应。
●教学用具投影仪、多媒体电脑、乙烯制备原理的教学课件、彩图两幅、塑料薄膜、球棍模型、乙烯分子的比例模型;铁架台、圆底烧瓶、温度计、双孔胶塞、导气管、带尖嘴的弯玻璃导管、石棉网、酒精灯、集气瓶、水槽、试管若干;酒精、浓硫酸、酸性KMnO4溶液、溴的四氯化碳溶液。
●教学过程[挂图展示]两幅彩图:图1为刚刚摘取不久的香蕉,颜色偏青;图2是将青香蕉与黄香蕉掺在一块放置几天后的结果,香蕉已全变黄。
[师]我们在买香蕉的时候是愿意买青香蕉还是黄香蕉?为什么?[生]当然原意买黄香蕉,因为黄香蕉成熟,好吃。
[设问]那么刚刚摘取不久的青香蕉何以与较熟的黄香蕉保存在一块就都变黄了呢?[师]这就是我们今天要学习的乙烯的功劳。
[板书]第三节乙烯烯烃[师]请大家写出乙烷分子的分子式,结构式和结构简式。
[生]按要求书写,并由一名学生上前板演:分子式结构式结构简式C2H6CH3CH3[师]请大家根据乙烷分子的结构式动手制作乙烷分子的球棍模型。
[学生活动]以小组为单位制作乙烷分子的球棍模型。
【襄樊五中】第13章《烃的衍生物》第2节《乙醇醇类》第1课时

高二化学第六章烃的衍生物第二节乙醇醇类(2课时)第一课时【说明】:本练习配套人教版化学读本,题目有一定的难度,适合省级示范高中或一些学校的优生使用,也可以作为高三第一轮复习的资料适用。
完成本练习的时间为30分钟,如果是高三第一轮复习,完成时间为20分钟。
后面有配套的标准答案,是经过认真审查的。
【习题内容】1 下列反应属于消去反应的是()A 乙醇在一定温度下与浓H2SO4反应制乙烯B 1—氯丙烷与NaOH水溶液共热C 乙醇与硫酸、溴化钾共热D 1—溴丙烷与NaOH乙醇溶液共热2 乙醇可以发生下列化学反应,在反应里乙醇分子断裂C—O键而失去羟基的是()A 乙醇在浓硫酸存在下发生消去反应B 乙醇与金属钠的反应C 乙醇在铜或银的存在下被氧化为乙醛D 乙醇与氢溴酸在一定条件下反应生成溴乙烷和水3 用浓 H2SO4跟乙醇和正丙醇的混合液反应,可能得到的醚有()A 1种B 2种C 3种D 4种4 下列反应属于取代反应的是()A 乙醇与浓硫酸混合加热到140℃B 乙醇与硫酸、溴化钠共热生成溴乙烷C 乙醇与氧气反应生成乙醛D 乙醇与浓硫酸共热至170℃5 检验无水乙醇是否含有水的方法是()A 加金属钠B 加入无水硫酸铜C 加热蒸馏D 加无水氯化钙6 现有组成为CH4O和C3H8O的混合物,在一定条件下进行脱水反应,可能生成有机物的种数为()A 5种B 6种C 7种D 8种7 下列两种醇的混合物8克,与足量的金属钠反应可生成标况下的H22.24升,则它们可能是()A.CH3OH和CH3CH2OH B.CH3OH和CH3CH2CH2OHC.C3H7OH和C4H9OH D.C4H9OH和C5H11OH8 下列物质既能发生消去反应又能氧化成醛或酮的是()A 2—甲基—1—丁醇B 2,2—二甲基—1—丁醇C 2—甲基—2—丁醇D 2,3—二甲基—1—丁醇9 下列醇不能发生消去反应而生成相应烯烃的是()A 甲醇B 2—甲基—2—丙醇C 2,2—二甲基—1—丙醇D 2—甲基—1—丙醇10 下列变化中属于消去反应的是()A 由乙醇制乙醚B 由乙醇制乙醛C 由乙醇制溴乙烷D 由乙醇制乙烯11 浓硫酸跟适量的乙醇共热到170℃,其反应的化学方程式是______________________,浓硫酸的作用是______________,把上面反应所得到的气态有机产物通入溴水中,其反应的方程式是_________________________________。
【襄樊五中】第12章《烃》第5节《苯》第2课时

高二化学 第五章 烃第五节 苯(2课时)第二课时【说明】:本练习配套人教版化学读本,题目有一定的难度,适合省级示范高中或一些学校的优生使用,也可以作为高三第一轮复习的资料适用。
完成本练习的时间为30分钟,如果是高三第一轮复习,完成时间为20分钟。
后面有配套的标准答案,是经过认真审查的。
【练习题】1.在15mL 苯中溶解560mL 乙炔,再加入75g 苯乙烯,所得混和液中碳元素的质量百分含量为 [ ]A 40%B 66.7%C 75%D 92.3%2.随着碳原子数的增多,碳元素的质量百分含量也增大的是 [ ]A 烷烃同系物B 烯烃同系物C 炔烃同系物D 苯的同系物3.下列各类烃中,碳氢两元素的质量比为定值的是 [ ]A 烷烃B 烯烃C 炔烃D 苯的同系物4.能用酸性高锰酸钾溶液鉴别的一组物质是( )A .乙烯、乙炔B .苯、己烷C .苯、甲苯D .己烷、环己烷5.苯环上有一个-C 4H 9和一个-C 3H 7两个取代基的有机物共有同分异构体( )A .12种B .4种C .8种D .24种6.下列说法中,正确的是 [ ]A 硝基苯和三硝基甲苯都是苯的衍生物B 硝基苯和三硝基甲苯互为同系物C 三硝基甲苯是一种烈性炸药,受热或撞击时会立即发生爆炸D 制取硝基苯和三硝基甲苯时,发生反应的类型相同7.已知分子式为C 12H 12的物质A 的结构简式为,A 苯环上的二溴代物有9种同分异构体,由此推断A 苯环上的四溴取代物的异构体的数目有[ ]A .9种B .10种C .11种D .12种8.在—CH =CH —C ≡C -CF 3分子中,位于同一平面的上的碳原子数最多有 [ ]A 8个B 9个C 10个D 11个9.已知C -C 可以绕键轴旋转,结构简式为右图的烃,下列说法正确的是 [ ]A 分子中至少有8个碳原子处于同一平面上B 分子中至少有9个碳原子处于同一平面上CH 3CH 3C 该烃的一氯取代物最多有4种D 该烃是苯的同系物10.已知有两种一氯取代物,则的一氯取代物有()A.3种B.4种C.6种D.8种11.将萘分子中的两个氢原子用一个氯原子和一个溴原子取代,所得卤代物的同分异构体的总数为 [ ]A 7种B 14种C 21种D 28种12.充分燃烧某液态芳香烃Χ,并收集产生的全部水,恢复到室温时,得到水的质量跟原芳香烃X的质量相等。
【襄樊五中】第12章《烃》第2节《烷烃》第2课时

高二化学第五章烃第二节烷烃(2课时)第二课时【说明】:本练习配套人教版化学读本,题目有一定的难度,适合省级示范高中或一些学校的优生使用,也可以作为高三第一轮复习的资料适用。
完成本练习的时间为30分钟,如果是高三第一轮复习,完成时间为20分钟。
后面有配套的标准答案,是经过认真审查的。
【练习题】1.现有一种烃,可表示为命名此化合物时,应该认定的主链上的碳原子数目 [ ]A.8 B.9 C.10 D.112.某烷烃的分子量为 72,跟氯气反应生成的一氯化物只有一种,这种烷烃是 [ ]A.2,2—二甲基丙烷 B.戊烷 C.2—甲基丙烷 D.2—甲基丁烷3.的名称是 [ ]A.2—甲基—3—乙基丁烷 B.2,3—二甲基戊烷C.2,3—二甲基—4—乙基丙烷 D.3,4—二甲基戊烷4.下列名称肯定错误的: [ ]A.2,2—二甲基戊烷 B.3—甲基—4—乙基己烷C.2,2—二甲基丙烷 D.2—乙基丁烷5.2,2,6,6-四甲基庚烷的一氯取代物的同分异构体共有 [ ]A 2种B 3种C 4种D 5种6.有机物:①正戊烷②异戊烷③新戊烷④正丁烷⑤异丁烷,它们的沸点按由高到低的顺序排列正确的是 [ ]A ①>②>③>④>⑤B ⑤>④>③>②>①C ①>②>④>③>⑤D ①>②>③>⑤>④7.下列有机物的命名正确的是 [ ]A.2,2—二甲基丁烷 B. 3,3—二甲基丁烷C.2—乙基丁烷 D.2,3,3—三甲基丁烷8.有A、B两种烃,含碳的质量分数相同,下列关于A和B的叙述中正确的是 [ ]A A和B一定是同分异构体B A和B不可能是同系物C A和B的最简式相同D A和B各1mol完全燃烧后生成的二氧化碳的质量一定相等9.下列化学性质烷烃不具备的是[ ]A.一定条件下发生分解反应 B.可以在空气中燃烧C.与氯气发生取代反应 D.能使高锰酸钾溶液褪色10.对己烷叙述正确的是: [ ]A.己烷的各同分异构体沸点都相同B.己烷有五种同分异构体C.己烷能溶于水,也能溶于有机溶剂D.己烷与2-甲基丁烷是同分异构体11.有一类组成最简单的有机硅化合物叫硅烷,它的分子组成与烷烃相似。
【襄樊五中】第12章《烃》第6节《石油煤》第1课时

高二化学第五章烃第六节石油煤(1课时)第一课时【说明】:本练习配套人教版化学读本,题目有一定的难度,适合省级示范高中或一些学校的优生使用,也可以作为高三第一轮复习的资料适用。
完成本练习的时间为30分钟,如果是高三第一轮复习,完成时间为20分钟。
后面有配套的标准答案,是经过认真审查的。
【练习题】1.已知天然气的主要成份CH4是一种会产生温室效应的气体,等物质的量的CH4和CO2产生的温室效应,前者大。
下面是有关天然气的几种叙述:①天然气与煤、柴油相比是较清洁的能源;②等质量的CH4和CO2产生的温室效应也是前者大;③燃烧天然气也是酸雨的成因之一。
其中正确的[ ]A 是①、②、③B 只有①C 是①和②D 只有③2.从石油分馏得到的固体石蜡,用氯气漂白后,燃烧时会产生含氯元素的气体,这是由于石蜡在漂白时与氯气发生过 [ ]A 加成反应B 取代反应C 聚合反应D 催化裂化反应3.乙烯的产量是衡量一个国家化学工业发展水平的重要标志之一。
为了;增加乙烯的产量,在石油加工时采用的措施是 [ ]A 减压分馏B 裂解C 热裂化D 催化裂化4.在相同条件下,对环境污染程度最小的燃料是 [ ]A 液化石油气B 煤油C 煤饼D 木柴5.下列关于石油及石油炼制的叙述中,错误的是 [ ]A 石油主要是烷烃、环烷烃、芳香烃组成的混和物B 石油分馏所得的馏分是纯净物C 为了防止重油进一步分馏时炭化结焦,常采用减压分馏D 石油裂化的原料是重油、石蜡等烃6.工业上获得苯主要通过 [ ]A 煤的干馏B 石油常压分馏C 石油减压分馏D 石油催化裂化7.石油裂解的目的是 [ ]A 提高轻质液体燃料的产量B 主要提高汽油的产量C 获得短链不饱和气态烃D 主要提高汽油的质量8.关于裂解与裂化的叙述不正确的是 [ ]A 裂解与裂化的产物中都含不饱和烃B 裂解与裂化都是为了得到气态烃C 裂解与裂化的原料都是石油分馏产品D 裂解与裂化都是使相对分子质量大的烃断裂为相对分子质量小的烃的过程9.对重油进行裂化的主要目的是 [ ]A 得到各种馏分的烃B 生成饱和及不饱和的气态烃C 提高汽油的产量和质量D 得到较多量的润滑油和凡士林10.下列有关煤的叙述,不正确的是 [ ]A 煤是工业上获得芳香烃的一种重要来源B 煤的干馏过程属于化学变化C 煤是由多种有机物组成的混合物D 煤除了主要含碳元素外,还含有少量的氢、氮、硫、氧等元素11.下列实验中,可以不用温度计的是 [ ]A 制乙烯B 制溴苯C 制硝基苯D 石油分馏12.丁烷被完全催化裂化后,所得混和气体的平均分子量是 [ ]A 58B 20C 29D 不能确定13.丁烷催化裂化时,如果有90%的丁烷发生裂化,且裂化生成的两种烯烃的质量相等,则裂化后得到的混和气体中分子量最小的气体在混和气体中的体积百分含量是()A.11% B.19% C.40% D.50%14.丙烷高温裂解生成甲烷和乙烯两种物质。
【襄樊五中】第12章《烃》第5节《苯》第1课时

高二化学第五章烃第五节苯(2课时)第一课时【说明】:本练习配套人教版化学读本,题目有一定的难度,适合省级示范高中或一些学校的优生使用,也可以作为高三第一轮复习的资料适用。
完成本练习的时间为30分钟,如果是高三第一轮复习,完成时间为20分钟。
后面有配套的标准答案,是经过认真审查的。
【练习题】1.能说明苯分子中的碳碳键不是单、双键交替的事实是 [ ]A、苯的一元取代物没有同分异构体B、苯的邻位二元取代物只有一种C、苯的间位二元取代物只有一种D、苯的对位二元取代物只有一种2.可以用分液漏斗分离的一组液体混和物是 [ ]A 溴和四氯化碳B 苯和溴苯C 汽油和苯D 硝基苯和水3.只用一种试剂就能将苯、己烯、CCl4、KI溶液鉴别开来,此试剂是 [ ]A、KMnO4溶液B、KI溶液C、溴水D、AgNO3溶液4.苯的二氯取代物有三种,那么苯的四氯取代物有 [ ]A 1种B 2种C 3种D 4种5.下列分子内各原子均在同一平面上的是①甲烷②乙烯③乙炔④苯 [ ]A 全部B 只有①C ②和③D ②③④6.以苯为原料,不能一步制得的是 [ ]A 环己烷B 苯磺酸钠C 溴苯D 硝基苯7.实验室里用苯与溴反应制取溴苯,反应后将所得液体倒入水中,分层后水底褐色的液体是 [ ]A 溴苯B 溶有溴的苯C 溶有溴的溴苯D 氢溴酸8.某烃结构式如下:-C≡C-CH=CH-CH3,有关其结构说法正确的是 [ ]A 所有原子可能在同一平面上B 所有原子可能在同一条直线上C 所有碳原子可能在同一平面上D 所有氢原子可能在同一平面上9.甲烷分子中的四个氢原子都可以被取代。
若甲烷分子中的四个氢原子都被苯基取代,则对取代后的分子(如图)的描述不正确的是 [ ]A 分子式为C25H20B 所有碳原子都在同一平面上C 此分子属非极性分子D 此物质属芳香烃类物质10.下列有机物注入水中振荡后分层且浮于水面的是 [ ]A 苯B 溴苯C 四氯化碳D 乙醇11.一氯代物有两种,两氯代物有四种的烃是 [ ]A 丙烷B 2-甲基丙烷C 丙烯D 苯12.有三种不同取代基-X,-Y,-Z,当它们同时取代苯分子中的3个氢原子,且每种取代产物中,只有两个取代基相邻时,取代产物有 [ ]A 2种B 4种C 6种D 8种13.通过实验事实的验证与讨论,认识苯的结构式。
【襄樊五中】第12章《烃》第1节《甲烷》第1课时

高二化学第五章烃第一节甲烷(1课时)第一课时【说明】:本练习配套人教版化学读本,题目有一定的难度,适合省级示范高中或一些学校的优生使用,也可以作为高三第一轮复习的资料适用。
完成本练习的时间为30分钟,如果是高三第一轮复习,完成时间为20分钟。
后面有配套的标准答案,是经过认真审查的。
【练习题】1.在人类已知的化合物中,品种最多的是 [ ]A.碱金属元素的化合物 B.卤族元素的化合物C.IVA族元素的化合物 D.VIA族元素的化合物2.下列物质中属于有机物的是 [ ]A.CH4 B. Na2CO3 C. CO2 D. Ca(HCO3)23.关于有机物的说法正确的是 [ ]A.只有在生物体内才能合成的物质B.指含碳元素的物质C.有机物都难溶于水,而易溶于有机溶剂D.有机物是指含碳元素的化合物4.下列物质的分子中,含有极性共价健且分子为正四面体结构的是 [ ]A.二氯甲烷 B.白磷 C.氨气 D.甲烷5.甲烷分子是以碳原子为中心的正四面体结构,理由是 [ ]A. CH3Cl不存在同分异构体 B.CH2Cl2不存在同分异构体C.CHCl3不存在同分异构体 D.CH4分子中四个价键间的键角和键长都相等6.在光照条件下,将等物质的量的甲烷和氯气充分反应,所得产物中物质的量最多的是 [ ]A.CH3Cl B.CH2Cl2 C.CHCl3 D.HCl7.光照对下列反应几乎没有影响的是 [ ]A.氯气和氢气反应 B.氯气跟甲烷反应C.甲烷跟氧气反应 D.次氯酸分解8.1mol甲烷完全与氯气发生取代反应,若生成相同物质的量的四种取代物,则消耗氯气的物质的量为[ ]A 1molB 2molC 2.5molD 4mol9.等物质的量的甲烷和氯气组成的混和气体,经较长时间的光照,最后得到的有机物是 [ ]①CH3Cl ②CH2Cl2③CHCl3④CCl4A 只有①B 只有②C 只有①②③D ①②③④10.瓦斯爆炸是空气中含甲烷5%~15%遇到火源所产生的爆炸。
【襄樊五中】第12章《烃》第4节《乙炔炔烃》第1课时

高二化学第五章烃第四节乙炔炔烃(2课时)第一课时【说明】:本练习配套人教版化学读本,题目有一定的难度,适合省级示范高中或一些学校的优生使用,也可以作为高三第一轮复习的资料适用。
完成本练习的时间为30分钟,如果是高三第一轮复习,完成时间为20分钟。
后面有配套的标准答案,是经过认真审查的。
【练习题】1.对于乙炔分子结构的叙述,正确的是[]A 乙炔分子是极性分子,其中只有极性键B 乙炔分子是非极性分子,其中只有非极性键C 乙炔分子是极性分子,其中既有极性键,又有非极性键D 乙炔分子是非极性分子,其中既有极性键,又有非极性键2.下列说法中正确的是[]A.乙烯和乙炔都能使溴水褪色,但与乙炔反应时消耗的溴要比等物质的量的乙烯反应消耗的多B.乙炔有特殊难闻的气味C.乙炔可用电石与水反应而制得,故实验里最好选用启普发生器为气体的发生装置D.乙炔含碳量比乙烯含碳量高,等物质的量的乙炔和乙烯燃烧时,乙炔所耗氧气多3.由乙炔为原料制取CHClBr—CH2Br,下列方法可行的是[]A、先与HBr加成后再与HCl加成B、先与H2加成后再与Cl2、Br2加成C、先与HCl加成后再与Br2加成D、先与Cl2加成后再与HBr加成4.CaC2和ZnC2、Al4C3、Mg2C3、Li2C2等都同属离子型碳化物。
请通过对CaC2制C2H2的反应的思考,从中得出必要的启示,判断下列反应产物正确的是()A.ZnC2水解生成乙烷(C2H6)B.Al4C3水解生成丙炔(C3H4)C.Mg2C3水解生成丙炔(C3H4)D.Li2C2水解生成乙烯(C2H4)5.含气体杂质的乙炔4.16g与H2加成生成饱和链烃,共用去4.48L(标准状况)H2,气体杂质不可能是[]A 乙烯B 丙炔C 丁二烯D 甲烷6.乙炔和乙烷的混和气体与同温同压下的空气密度相同,则该混和气体中乙炔的质量分数约是()A.22.4% B.25% C.67.2% D.75%7.乙炔与空气的混和气体(达爆炸极限)点燃时会爆炸,爆炸最剧烈时,乙炔在混和气中的体积分数是[]A 2.5%B 7.75%C 11.9%D 28.6%8.完全燃烧相同质量的下列各烃,消耗氧气最多的是[]A CH4B C2H4C C2H2D C6H149.两种气态烃组成的混合物共0.1mol,完全燃烧后得到3.85LCO2(标准状况)和3.6g水,下列说法正确的是[]A.一定有甲烷 B.一定有乙烷C.一定有乙烯D.一定有乙炔10.某气体是烯烃和炔烃的混合物,其密度是同温同压下氢气的13.5倍,则下列说法正确的是()A.混合气体一定有乙炔B.混合气体一定有乙烯C.混合气体可能由丙炔和乙烯组成D.混合气体一定由乙炔和乙烯组成11.下列混合气体比乙烯含碳百分率高的是[]A.甲烷+乙烯 B.乙烷+丁烯C.乙炔+丙烯 D.乙烷+丙烯12.某种烷烃和某种炔烃的混合气共50毫克在0℃.101105.⨯Pa时体积为50毫升,关于这混合气的叙述有:①能使溴水褪色②不可能有乙炔③肯定有甲烷④10毫升此状况下的混合气可跟状况下的氢气20毫升完全加成⑤可能有乙烷;以上叙述中不正确的是[]A.②③④ B.②④⑤ C.①②③ D.③④⑤13.相同条件下a升乙烯和乙炔的混合气完全燃烧,用去b升氧气,则原混合气中乙烯和乙炔体积比[]A.2a b3a b--B.5a b2b6a--C.2b5a6a2b--D.b2a3a2b--14.一定量的某烃完全燃烧后,将生成物通入足量的石灰水中,经过滤可以得到10克沉淀称其滤液质量时,其质量减少2.9克,此有机物可能是[]A.CH4 B.C2H2 C.C2H4 D.C2H615.现有CH4.C2H2.C2H4.C2H6.C3H6五种有机物,等质量的以上物质,在相同状况下体积最大的______;等质量的以上物质完全燃烧耗去氧气的量最多的是______;同状况同体积的以上物质完全燃烧耗去氧气的量最多的是_______;同质量的以上物质完全燃烧时,生成二氧化碳最多的_____生成水最多的是______.16.实验室制取的乙决气体中常混有少量H2S.CO2和水蒸气,为了得到干燥纯净的乙炔气体,选择最简便的实验方案有_______A.通过NaOH后,通过浓H2SO4,再通过石灰水B.通过CuSO4溶液后再通过石灰水C.通过五氧化磷,再通过无水CaCl2D.通过足量的碱石灰17.为探究乙炔与溴的加成反应,甲同学设计并进行了如下实验:先取一定量工业用电石与水反应,将生成的气体通入溴水中,发现溶液褪色,即证明乙炔与溴水发生了加成反应。
高二化学《乙烯 烯烃》课件

CH2=CH2+Br―Br
CH2Br-CH2Br
催化剂
CH2=CH2+H―H
CH3-CH3
CH2=CH2+H―X 催化剂 CH3-CH2X
现象 用途
CH2=CH2+H―OH 催化剂 CH3-CH2OH
3、聚合反应(选修5P30) 乙烯聚合过程
拓展: 氯乙烯聚合
单体
链节
聚合度
聚合反应:分子量小的化合物分子(单体)互相结合成
(一)工业制法:分离石油裂解气
(二)实验室制法
1、反应原理: 用浓硫酸作催化剂、脱水剂,加热到170℃左右,
使乙醇脱水产生乙烯。
CH2—CH2浓H2SO4
170℃
H OH
CH2=CH2 + H2O
CH3CH2OH浓1H702S℃O4 CH2=CH2 + H2O
2、发生装置: 液+液→△ 气(需控制温度)
以防止混合液受热沸腾时剧烈跳动。
4、为何要迅速升温到170℃,并控温在该温度?
①在浓硫酸作用下, 140℃时,乙醇发生分子间脱水,生成乙醚。 CH3—CH2—OH + HO—CH2—CH3 → C2H5—O—C2H5 + H2O
② 温度过高,不仅会产生大量气泡,同时会产生副反应,生成炭 黑等副产物,使反应难以顺利进行。乙烯中通常含有CO2、SO2等 杂质气体,要提纯可通过碱性物质。
5、温度计的位置? 温度计的水银球应在液面以下,但不接触瓶底。
三、乙烯的性质
(一)乙烯的物理性质
乙烯是 无 色 稍有 气味 的气体;在水中 难 (“易” 或“难”)溶于水;密度较空 气 略小 。
二、乙烯的化学性质
1、氧化反应:
高二化学乙烯烯烃课件 人教

分子式: 电子式: HH
C2H4 H ∶¨C ∷¨C∶H H
结构式: 结构简式: HH C C H CH2 CH2
分子几何构型: 六原子共平面
二、乙烯的实验室制法
1.药品:乙醇、浓硫酸
2.反应原理:
CH2 CH2
H
OH
乙醇
浓硫酸
170℃
CH2
乙烯
浓硫酸的作用:催化剂和脱水剂
CH2↑+H2O
讨论1.反应方程式中为什么要标明温度?
讨论10.一个完整的气体制备装置应包括几个部分?
发生 装置
净化 装置
收集 装置
尾气处 理装置
实验室制取乙烯发生装置与除杂装置连接顺序如何?
动画
三、乙烯的性质
1、物理性质 在通常状况下,乙烯是无色稍有气味的 气体,难溶于水。在标准状况时密度为1.25g/l与空气接 近
提问:用什么方法收集乙烯?点燃乙烯时,火焰与甲烷有
CH2 CH2
浓硫酸
170℃
H
OH
CH2 CH2↑+H2O
CH2 H
CH2 + CH2
OH
H
CH2
浓硫酸
140℃
C2H5OC2H5 +H2O
OH
讨论2.根据反应物的状态以及反应条件,请同学们思考: 实验室制取乙烯的装置与我们以前学过的哪一种气体的 发生装置类似?
固-液、液-液加热
液-液、固-液不加热
什么不同?
火焰明亮伴有黑烟
乙烯能否使酸性KMnO4(aq)或溴水褪色?
为什么?
2、化学性质
①氧化反应
与酸性KMnO4(aq):可被酸性KMnO4(aq)氧化(利用此反应 可以鉴别甲烷和乙烯)
最新-测控设计2021学年高中化学选修5课件:212烯烃 精品

单烯烃和环烷烃的通式都是CnH2n(n≥2),符合通式CnH2n(n≥2)的
烃一定是同系物吗?
提示:不一定。单烯烃和环烷烃的通式虽然都是CnH2n(n≥2),但
结构不同,不是同一类烃。含相同数目
碳原子的单烯烃和环烷烃是同分异构体,但烯烃和环烷烃不是同系
物。例如丙烯和环丙烷互为同分异构体,C2H4和C3H6不一定是同系
知识点1
知识点2
知识点3
A.品红溶液 B.NaOH溶液
C.浓硫酸
D.KMnO4酸性溶液
(2)能说明二氧化硫气体存在的现象是
。
(3)使用装置②的目的是 。
(4)使用装置③的目的是 。
(5)确定含有乙烯的现象是 。
解析:乙烯分子中含有碳碳双键,易与Br2发生加成反应及被
应时,有两种产物:
1,2-加成:1,3-丁二烯分子中一个双键断裂,两个氯原子分别与1号
碳原子和2号碳原子相连。化学方程式为
CH2 CH—CH CH2+Cl2
。
1,4-加成:1,3-丁二烯分子中两个双键断裂,两个氯原子分别与1号碳
原子和4号碳原子相连,在2号碳原子和3号碳原子之间形成一个新
的双键。化学方程式为
CH2 CH—CH CH2+Cl2
。
1,3-丁二烯的1,2-加成和1,4-加成是竞争反应,到底哪一种加成占优
势,取决于反应条件。
一
二
(4)加聚反应,如丙烯加聚反应的化学方程式为
nCH3—CH CH2
。
一
二
二、烯烃的顺反异构
1.顺反异构现象的产生
由于碳碳双键不能旋转而导致分子中原子或原子团在空间的排
物。
一
二
2.烯烃的物理性质
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高二化学第五章烃
第三节乙烯烯烃(2课时)
第二课时
【说明】:
本练习配套人教版化学读本,题目有一定的难度,适合省级示范高中或一些学校的优生使用,也可以作为高三第一轮复习的资料适用。
完成本练习的时间为30分钟,如果是高三第一轮复习,完成时间为20分钟。
后面有配套的标准答案,是经过认真审查的。
【练习题】
1、关于烷烃和烯烃的下列说法, 正确的是 [ ]
A.烷烃的通式是C n H2n+2, 符合这个通式的烃为烷烃
B.烯烃的通式是C n H2n, 符合这个通式的烃一定是烯烃
C.烷烃和烯烃都能与溴水反应
D.烯烃和二烯烃属于同系物
2.下列物质中与丁烯互为同系物的是 [ ]
A.CH3-CH2-CH2-CH3 B.CH2 = CH-CH3 C.C5H10 D.C2H2
3.下列反应属于加成反应的是 [ ]
A.由乙烯制乙醇 B.由甲烷制四氯化碳
C.由乙烯合成聚乙烯 D.由乙醇制乙烯
4.下列单体中在一定条件下发生加聚反应生成的是()
A.CH2 = CH2和CH4B.CH3-CH = CH2和CH2 = CH2
C.
D .
5.有二种烯烃和(—R表示烷基), 它们混合后进行加聚反应, 产物中不可能含有下列结构()
①②③④
A.②B.③④C.②④D.④
6.下列物质中与1—丁烯互为同分异构的是 [ ]
A.CH3-CH2-CH2-CH3 B.CH2 = CH-CH3
C. D.CH2 = CH-CH = CH2
7.C5H10的同分异构体属于烯烃和可能有 [ ]
A.4种 B.5种 C.8种 D.10种
8.某烯烃与H 2加成后的产物是, 则该烯烃的结构式可能有 [ ]
A.1种 B.2种 C.3种 D.4种
9.从烷烃(C n H2n+2),烯烃(C n H2n),二烯烃(C n H2n-2)的通式分析,得出碳氢原子的个数与分子中所含双键有一定关系,某种烃的分子式为C x H y,其中所含双键数目为 [ ]
A y/2
B (y-x)/2
C (y+2-x)/2
D (2x+2-y)/2
10.
常温常压下,一种气态烷烃与一种气态烯烃的混和物共1L,完全燃烧后,恢复到原状况,得到1.2L二氧化碳,则该混和气体中一定含有()A
A.甲烷B.乙烯C.乙烷D.环丙烷
11.某气态烃含碳85.7%,1mol该烃充分燃烧生成的二氧化碳恰好被1.5L、4mol/L的NaOH溶液吸收生成正盐,这种烃的分子式是 [ ]
A C2H6
B C3H6
C C4H8
D C6H14
12.
组成为C7H16的烷烃有九种,其中仅能由一种单烯烃加氢而制得的有()B
A.1种B.2种C.3种D.4种
13.
使1.0体积的某气态烷烃和烯烃的混合气体在足量空气中完全燃烧, 生成2.0体积的二氧化碳和2.2体积的水蒸气(均在120℃、1.01×105Pa条件下测定), 则混合气体中烷烃和烯烃的体积比为()B A.2∶3 B.1∶4 C.4∶1 D.3∶2
14、在相同条件下, 将x mol的乙烯和丙稀混合气体与y mol氧气混合, 使其恰好完全反应, 则原混合气体中乙稀和丙稀的体积比是 [ ]
A.9x2y
2y6x
-
-
B.
2y6x
9x2y
-
-
C.
2y9x
6x2y
-
-
D.
6x2y
2y9x
-
-
15.分子式为C6H12的某烯烃的所有的碳原子都在同一个平面上,则该烯烃的结构式为。
16.1mol某有机物A能与1mol氢气发生加成,反应的产物是2,2,3-三甲基戊烷,A可能是。
17、某烃A 0.2mol在氧气中充分燃烧后生成化合物B、C各1.2mol, 试回答:
(1)烃A的分子式________
(2)若取一定量的烃A完全燃烧后, 生成B、C各3mol, 则有________克烃A参加反应, 燃烧时消耗标准状况下的氧气________升
(3)若烃A不能使溴水褪色, 但在一定条件下, 能与氯气发生取代反应, 其一氯代物只有一种, 则此烃A 的结构简式为________
(4)若烃A能使溴水褪色, 在催化剂作用下与H2加成, 其加成产物经测定分子中含有4个甲基, 烃A可能有的结构简式为________
(5)比(4)中的烃A少2个碳原子的同系物有________种同分异构体
18.在一定条件下,将0.56g气态烃A在过量氧气中燃烧,将生成的气体通过浓硫酸后,溶液增重0.72g,再把剩余气体用碱石灰吸收,盛碱石灰的干燥管又增重1.76g,A与另一种气态烷烃等体积混和后,其平均分子量为22,求A的分子式及结构简式。
第二课时
1、A 2.B 3.A 4.B 5.D 6.C 7.D 8.C 9.D 10.A 11.B 12.B 13.B 14、A
15.
16.3,3-二甲基-2-乙基-1-丁烯、3,4,4-三甲基-2-戊烯、3,4,4-三甲基-1-戊烯
17、(1)C6H12 (2)42g 100.8L (3) (4)
(5)3种 18. CH2=CH2。
