CRISPR基因编辑技术教程课件
合集下载
crispr-cas基因编辑技术原理与应用PPT精选文档

力因子测试和MLST 基因型明显相关。
31
进展
2 在斑马鱼研究方面,通过注射两个 简单的体外合成的组件(即使用一个密 码子优化的Cas9 和单链向导 sgRNA) 到单细胞期胚胎中,使目标基因突变。 这种灵活的基因失活的方法为斑马鱼 基因功能和基因相互作用提供了一个 有效的方式。
32
进展
3 干细胞中的定点突变,包括引进或疾病患者特异性突变模 型的修正。然而,在人类胚胎干细胞中将一个报告基因整合成一 种内源性基因还需要漫长艰苦的两步:首先要正确识别目标然后 要排除耐药性。研究发现,tracrRNA 和crRNA 分开单独表达, 还能够提高切割的效率。这个发现让大家意识到:可以通过进一 步修改 sgRNA 的设计方案,让它与双 RNA 复合体的结构更加 相近,就能够进一步提高 Cas9 系统的基因组编辑效率。
缺陷
成本高,应用的物种有限,操纵的基因亦有限。
16
基因编辑功能应用
CRISPR-Cas9系统的基因编辑功能主要应用于在不同物种 的基因组产生需要的等位基因突变,来研究基因功能或建立疾病模 型。
如果CRISPR-Cas9系统的基因编辑功能如果真如研究者 报道那样强大的话,那该技术在先天性突变或获得突变所致疾病 的修复治疗中将有巨大的潜在价值。这一点还有待研究。
33
进展
4 在拟南芥研究方面,利用C RISPR/Cas 系统对分裂组织有 针对性地定点诱变产生遗传突变, 结果表明,在拟南芥中使用 CR ISPR/Cas系统为 RNA 引导的核 酸内切酶(RGEN)定点突变分裂组 织提供了一种有效的遗传基因工 程的方法。
34
进展
5 CRISPR/Cas 的 打 靶 效 率 比 较 高,最
缺陷:1、不能预期引入的ZFN蛋白是
31
进展
2 在斑马鱼研究方面,通过注射两个 简单的体外合成的组件(即使用一个密 码子优化的Cas9 和单链向导 sgRNA) 到单细胞期胚胎中,使目标基因突变。 这种灵活的基因失活的方法为斑马鱼 基因功能和基因相互作用提供了一个 有效的方式。
32
进展
3 干细胞中的定点突变,包括引进或疾病患者特异性突变模 型的修正。然而,在人类胚胎干细胞中将一个报告基因整合成一 种内源性基因还需要漫长艰苦的两步:首先要正确识别目标然后 要排除耐药性。研究发现,tracrRNA 和crRNA 分开单独表达, 还能够提高切割的效率。这个发现让大家意识到:可以通过进一 步修改 sgRNA 的设计方案,让它与双 RNA 复合体的结构更加 相近,就能够进一步提高 Cas9 系统的基因组编辑效率。
缺陷
成本高,应用的物种有限,操纵的基因亦有限。
16
基因编辑功能应用
CRISPR-Cas9系统的基因编辑功能主要应用于在不同物种 的基因组产生需要的等位基因突变,来研究基因功能或建立疾病模 型。
如果CRISPR-Cas9系统的基因编辑功能如果真如研究者 报道那样强大的话,那该技术在先天性突变或获得突变所致疾病 的修复治疗中将有巨大的潜在价值。这一点还有待研究。
33
进展
4 在拟南芥研究方面,利用C RISPR/Cas 系统对分裂组织有 针对性地定点诱变产生遗传突变, 结果表明,在拟南芥中使用 CR ISPR/Cas系统为 RNA 引导的核 酸内切酶(RGEN)定点突变分裂组 织提供了一种有效的遗传基因工 程的方法。
34
进展
5 CRISPR/Cas 的 打 靶 效 率 比 较 高,最
缺陷:1、不能预期引入的ZFN蛋白是
crispr cas9技术课件PPT

8
2.CRISPR/Cas9技术的缺点 1.脱靶效应
2021/3/10
7
CRISPR/技术的前景及优缺点
➢ 3.2 CRISPR-Cas9系统的应用前景 ➢ 1.在基因敲除方面具有绝对的优势 ➢ 2.可以用于因单基因突变造成的遗传病治疗 ➢ 3.在家畜及农业育种方面带来新的基因编辑技术
2021/3/10
1CRISPR-Cas9技术的优势
而且从实际应用的角度来说,CRISPRs比TALENs更容易操作,因为每一对TALENs都需要重 新合成,而用于CRISPR的gRNA只需要替换20个核苷酸就行。
只需合成一个sgRNA就能实现对基因的特异性修饰,Cas蛋白不具特异性。 编码sgRNA的序列不超过100bp,因此比构TALENs和ZFNs更简单方便。 较短的sgRNA序列也避免了超长、高度重复TALENs编码载体带来的并发症。
➢ 2005 年发现CRISPR 的间隔序列(spacer)与宿主菌的染色体外的遗传物质 高度同源,推测细菌可能通过CRISPR 系统可能以类似于真核生物的RNAi 方式抵抗外源遗传物质的入侵。
➢ 2013 年初,MIT 的研究组首次利用CRISPR/Cas9 系统对人293T 细胞
EMX1 和PVALB 基因以及小鼠Nero2A 细胞Th 基因实现了定点突变。
Cas蛋白是一种双链DNA核酸酶,能在guide RNA引 导下对靶位点进行切割。它与folk酶功能类似, 但是它并不需要形成二聚体才能发挥作用。
2021/3/10
3
CRISPR/cas9作用机理
1.CRISPR 的高度可变的间隔区的获得 首先识别入侵的核酸和扫描外源 DNA 潜在 的 PAM(NGG序列),将临近 PAM 的序列 作为候选protospacer;然后在 CRISPR 基 因座的5'端合成重复序列;最后新的间隔 序列整合到两个重复序列之间
基因编辑新技术课件-PPT精选文档17页

基因编辑新技术
组长:凌晨 组员:徐青蓝
刘明明 高阳 刘晨东
引言
2019年,CRISPRs 成为了生物技术圈的宠儿。 什么是CRISPRs? CRISPRs 全称为规律成簇间隔短回文重复。 这是一类广泛分布于细菌和古菌基因组中 的重复结构。这种基因组编辑技术能够重 编程一种CRISPR系统,其有潜力切割任何的 特异性DNA靶标。
讨论
5 热点
下一个挑战将是分析和解决可能出现的脱靶效应,提高 系统效率和特异性,扩大应用到其他生物体。
6 未来
CRISPR/Cas9在基础理论研究,临床治疗和农牧渔业等领
域必将有越来越有广阔的应用前景,并且产生深远的影响。
谢谢
谢谢你的阅读
知识就是财富 丰富你的人生
讨论
3 应用 A 干细胞的基因编辑 B 肿瘤、艾滋病等的治疗 C 重大传染病的基因治疗 D 生物工程中的巨大潜力
讨论
4 疑问 A .CRISPRs是否还有其他的功能?
B. 为什么自然界中的噬菌体大量存在,却只在 40%的细菌中存在CRISPRs基因座?
C. 既然细菌与噬菌体是一种共进化的关系, 是否可以猜测噬菌体中也存在着能够抵抗 CRISPRs系统的相关机制?
方法
3 .过程(以cas9为例)
结果
1.美国哈佛-麻省理工Broad 研究所、哈佛大学医学院和首尔
大学的三个独立研究小组设计出了双RNAs或 sgRNAs,当 研究人员在各种人类细胞系中表达这种“人源化” Cas9和导 向RNAs时,他们观察到靶DNA发生了预期的改变,介导了 双链断裂及随后的修复。
这种基因打靶成功率高达38%,只伴随有低水平的Cas9毒性。
结果
• 2 Hwang等人则使用单细胞斑马鱼胚胎进行了试
组长:凌晨 组员:徐青蓝
刘明明 高阳 刘晨东
引言
2019年,CRISPRs 成为了生物技术圈的宠儿。 什么是CRISPRs? CRISPRs 全称为规律成簇间隔短回文重复。 这是一类广泛分布于细菌和古菌基因组中 的重复结构。这种基因组编辑技术能够重 编程一种CRISPR系统,其有潜力切割任何的 特异性DNA靶标。
讨论
5 热点
下一个挑战将是分析和解决可能出现的脱靶效应,提高 系统效率和特异性,扩大应用到其他生物体。
6 未来
CRISPR/Cas9在基础理论研究,临床治疗和农牧渔业等领
域必将有越来越有广阔的应用前景,并且产生深远的影响。
谢谢
谢谢你的阅读
知识就是财富 丰富你的人生
讨论
3 应用 A 干细胞的基因编辑 B 肿瘤、艾滋病等的治疗 C 重大传染病的基因治疗 D 生物工程中的巨大潜力
讨论
4 疑问 A .CRISPRs是否还有其他的功能?
B. 为什么自然界中的噬菌体大量存在,却只在 40%的细菌中存在CRISPRs基因座?
C. 既然细菌与噬菌体是一种共进化的关系, 是否可以猜测噬菌体中也存在着能够抵抗 CRISPRs系统的相关机制?
方法
3 .过程(以cas9为例)
结果
1.美国哈佛-麻省理工Broad 研究所、哈佛大学医学院和首尔
大学的三个独立研究小组设计出了双RNAs或 sgRNAs,当 研究人员在各种人类细胞系中表达这种“人源化” Cas9和导 向RNAs时,他们观察到靶DNA发生了预期的改变,介导了 双链断裂及随后的修复。
这种基因打靶成功率高达38%,只伴随有低水平的Cas9毒性。
结果
• 2 Hwang等人则使用单细胞斑马鱼胚胎进行了试
crisprcas基因编辑技术原理与应用ppt课件

为了规范事业单位聘用关系,建立和 完善适 应社会 主义市 场经济 体制的 事业单 位工作 人员聘 用制度 ,保障 用人单 位和职 工的合 法权益
应用
Rudolf Jaenisch教授实验室采用CRISPR/Cas技术绕过了胚胎干细胞 操作过程,可快速而有效地建立携带多个基因突变的小鼠。这是 CRISPR/Cas技术首次被用于多细胞生物的基因操作。
目录
CRISPR/Cas基因编辑技术
发现 原理 应用 优点 缺点 发展 前景
为了规范事业单位聘用关系,建立和 完善适 应社会 主义市 场经济 体制的 事业单 位工作 人员聘 用制度 ,保障 用人单 位和职 工的合 法权益
发现
在1987年的一篇论文中,日本大阪大学的研究人员报告了一项表面上微不 足道的研究发现。他们在调查一种编码碱性磷酸酶的细菌基因序列时,发现 了邻近的一个不同寻常的DNA片段,这一DNA片段中间是一段短直接重复 核苷酸序列,两侧为短特异片段。他们当时指出“这些序列的生物学意义尚 不清楚”。在几乎过去快30年后,这一最初看起来不起眼的研究发现,现在 为简易操控大量生物体的基因组打开了大门。2000年,相似的重复序列在其 它真细菌和古细菌中被发现并被命名为短间隔重复序列(Short Regularly
What
01
Clustered regularly interspaced
shortpalindromic repeats (CRISPR)/CRISPR-
associated (Cas) systems
(常间回文重复序列丛集关联蛋白系统)
CRISPR表示成簇的规律间隔的短回文重复序列, 02 而Cas是一种和CRISPR系统相关联的蛋白质、
应用
基因打靶技术在基因功能研究中的应用、研制人类疾病动物 模型、改良动物品系和研制动物反应器等。
CRISPR基因编辑技术ppt课件
2007 年,Barrangou 等首次发现细菌可能利用CRSPR 系统抵抗噬菌体入 侵;2008 年,Marraffini 等发现细菌CRISPR 系统能阻止外源质粒的转 移,首次利用实验验证了CRISPR 系统的功能
2013 年初,MIT 的研究组首次利用CRISPR/Cas9 系统对人293T 细胞
23
CRISPR/Cas 9作用机理
24
CRISPR/Cas 9作用机理
PAM(NGG序列) 25
CRISPR/Cas 9系统靶向要求
最主要的要求:PAM(protospacer-adjacent motif)为NGG。在人 类基因组中,平均每8bp就出现一个NGG PAM。
26
CRISPR/Cas 9基因编辑实验流程图
• NI可以识别A
• NN可以识别G或A
通过这种特异性识别,将多个Tal蛋白组
装在一起,就可以构成可以识别目的片
段的Tale蛋白。Fra bibliotek13TALEN原理
TALEN的特异性打靶的原理:
一对可以特异性识别靶基因的TALE,定位到需要编辑的基因组区域; 然后非特异性核酸内切酶 FokI切断双链DNA从而造成DNA双链断裂(doublestrand break,DSB); 再通过DNA的自我修复,引起碱基的缺失或突变,从而引起基因突变。 FokI只有在形成二聚体的时候才有内切酶活性。
30
CRISPR/Cas 9系统的优势
操作简单,靶向精确性更高。sgRNA靶向序列和基因组序列 必须完全匹配,Cas9才会对DNA进行剪切。编码sgRNA 的序 列不超过100bp,因此比构建TALENs和ZENs更简单方便, 用于CRISPR的sgRNA识别序列仅需20个核苷酸。 CRISPR/Cas9系统是由RNA调控的对DNA的修饰,其基因修 饰可遗传。 基因修饰率高,CRISPRs基因敲入的效率为51%-79%, TALENs的效率为0%-34%。 基因调控方式多样,例如敲除、插入、抑制、激活等 无物种限制,可实现对靶基因多个位点同时敲除。 实验周期短,最快仅需2个月,节省大量时间和成本。(ZFNS 一个靶点成本6000$)
Crisper Cas 9技术介绍PPT课件

精选PPT课件
9
谢谢!
精选PPT课件
10
精选PPT课件
8
参考文献
[1]视频: 基因编辑CRISPR-Cas9原理-张锋参与制作 /v_show/id_XMTM4NTQ2ODU4NA.html [2]《细胞》特辑:CRISPR/Cas9技术 /newsf/20154/2015422151743416.htm [3]CRISPR/Cas9基因编辑器及其原理简介 /biowiki/t3170/
Crispr Cas9
61314104 张紫菡
精选PPT课件
1
CRISPR是什么?
•病毒能把自己的基因整合到细菌,利用细菌的细胞工具为自己的基因复 制服务。
•细菌为了将病毒的外来入侵基因清除,进化出CRISPR系统,利用这个系 统,细菌可以不动声色地把病毒基因从自己的染色体上切除,这是细菌 特有的免疫系统。
精选PPT课件
5
Crispr Cas9应用
•2013 年 1 月份,美国两个实验室在《Science》杂志发表 了基于 CRISPR-Cas9 技术在细胞系中进行基因敲除的新方 法,利用靶点特异性的 RNA 将 Cas9 核酸酶带到基因组上 的具体靶点,从而对特定基因位点进行切割导致突变,是一 种可靠、高效、快速的构建敲除动物模型的新方法。
精选PPT课件
目前发现的CRISPR/Cas系统有三种不同类型即I型、II型和III型,在II型系统中pre-
crRNA的加工由Cas家族中的Cas9单独参与。Cas9含有在氨基末端的RuvC和蛋
白质中部的HNH2个独特的活性位点,在crRNA成熟和双链DNA剪切中发挥作用。
精选PPT课件
4
Crispr Cas9 工作原理
CRISPR-Cas9-基因编辑技术简介ppt课件

CRISPR基因座的表达(包括转录 和转录后的成熟加工)
当该噬菌体再次入侵细菌时, CRISPR簇首先转录为长的crRNA 前体,然后逐步加工成小的成 熟的crRNA.
CRISPR/Cas系统活性的发 挥或外源遗传物质的干 扰
crRNA结合相关的Cas蛋白后,
形成NA-Cas蛋白复合体,
精选版课件ppt
5
2.CRISPR/Cas系统结构
2.2CRISPR结构:
CRISPR是一种特殊的DNA 重复序列家族,广泛分布于细菌 和古细菌基因组中。CRISPR位点通常由短的高度保守的重复序 列(repeats)组成,重复序列的长度通常为21--48bp,重复序列之 间被26--72bp间隔序列(spacer)隔开。CIRSPR通过这些间隔序列 (spacer)与靶基因进行识别。
沈彬,2015
精选版课件ppt
18
6.降低脱靶效应
添加同源臂(homology arm,HR)
Yu Hisano et al.2014
精选版课件ppt
19
6.降低脱靶效应
FoKI-dCas9
Nicolas Wyvekens et al.2015
精选版课件ppt
20
6.降低脱靶效应
CRISPR/Cpf1系统
精选版课件ppt
11
4.CRISPR/Cas9系统
酿脓链球菌
精选版课件ppt
12
4.CRISPR/Cas9系统
精选版课件ppt
13
4.CRISPR/Cas9系统
gRNA 在线设计工具:
CRISPR Design Tool: / E-CRISPR: ZiFiT: / Cas9 Design: http://cas9 /index.jsp Cas-OFFinder: /cas-offinder/ CCTop: http://crispr.cos.uni-heidelberg.de/
CRISPR-Cas9系统原理应用及发展ppt课件

CRISPR-Cas系统基因修饰技术
1
1 CRISPR-Cas概述
1987年,日本大阪大学(Osaka University)在对一种细菌 编码的碱性磷酸酶(alkaline phosphatase)基因进行研究时, 发现在这个基因编码区域的附近存在一小段不同寻常的DNA 片段,这些片段是由简单的重复序列组成的,而且在片段的 两端还存在一段不太长的特有的序列。
8
2 CRISPR-Cas系统的发现
9
2 CRISPR-Cas系统的发现
10
2 CRISPR-Cas系统的发现
CRISPR-Cas系统赋予原核细胞针对外源DNA特异性免 疫, 而这种特异性是由间隔序列(spacer)决定的。在宿主 防御噬菌体攻击中,针对自然界中庞大的噬菌体种群,细菌 进化了CRISPR 介导的适应性免疫。这种免疫功能的发挥是 由CRISPR 间隔序列的动态性变化,即通过增加或删除间隔 序列(spacer)来实现的。
15
3.1 dual-RNA:Cas介导编辑模板替换
2013年1月29日在《nature biotechnology》上发表的 《RNA-guided editing of bacterial genomes using CRISPR-Cas systems》一文中,作者利用CRISPR-Cas系 统用设计好的DNA模板替换的相应基因来达到基因的定向 修饰。
5
1.1 CRISPR结构
6
1.2 Cas家族
Cas(CRISPR associated): 存在于CRISPR位点附近,是一种双链DNA核酸酶,能在
guide RNA引导下对靶位点进行切割。它与folk酶功能类似, 但是它并不需要形成二聚体才能发挥作用。
1
1 CRISPR-Cas概述
1987年,日本大阪大学(Osaka University)在对一种细菌 编码的碱性磷酸酶(alkaline phosphatase)基因进行研究时, 发现在这个基因编码区域的附近存在一小段不同寻常的DNA 片段,这些片段是由简单的重复序列组成的,而且在片段的 两端还存在一段不太长的特有的序列。
8
2 CRISPR-Cas系统的发现
9
2 CRISPR-Cas系统的发现
10
2 CRISPR-Cas系统的发现
CRISPR-Cas系统赋予原核细胞针对外源DNA特异性免 疫, 而这种特异性是由间隔序列(spacer)决定的。在宿主 防御噬菌体攻击中,针对自然界中庞大的噬菌体种群,细菌 进化了CRISPR 介导的适应性免疫。这种免疫功能的发挥是 由CRISPR 间隔序列的动态性变化,即通过增加或删除间隔 序列(spacer)来实现的。
15
3.1 dual-RNA:Cas介导编辑模板替换
2013年1月29日在《nature biotechnology》上发表的 《RNA-guided editing of bacterial genomes using CRISPR-Cas systems》一文中,作者利用CRISPR-Cas系 统用设计好的DNA模板替换的相应基因来达到基因的定向 修饰。
5
1.1 CRISPR结构
6
1.2 Cas家族
Cas(CRISPR associated): 存在于CRISPR位点附近,是一种双链DNA核酸酶,能在
guide RNA引导下对靶位点进行切割。它与folk酶功能类似, 但是它并不需要形成二聚体才能发挥作用。
基因编辑技术比较CRISPR Cas9,casF,Cpf1 ppt
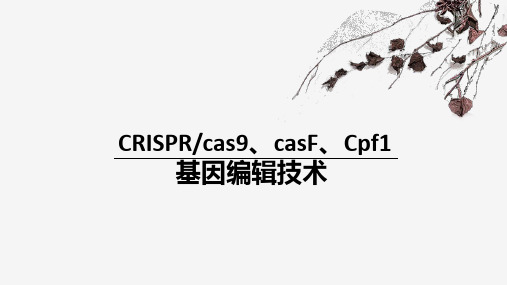
CRISPR-CPf1作用原理
cas9 / casF /cpF1总结
Part.4
Cpf1/Cas9比较
Cas9/ casF / Cpf1总结
谢谢观看
CRISPR:
CRISPR簇是一个广泛存在于细菌和古生菌基因组中 的特殊DNA重复序列家族,是成簇的规律间隔的短 回文重复序列。右图展示了完整的CRISPR位点的结 构。
CRISPR/cas9基因编辑原理
主要内容
crRNA ( CRISPR-derived RNA )通过碱基配对与 tracrRNA (trans-activatingRNA )结合形成 tracrRNA/crRNA复合物,此复合物引导核酸酶Cas9 蛋白在与crRNA配对的序列靶位点剪切双链DNA。
CRISPR/cas9、casF、Cpf1 基因编辑技术
ቤተ መጻሕፍቲ ባይዱ
➢ 1. CRISPR/cas9基因编辑技术 ➢ 2. CRISPR/casF基因编辑技术 ➢ 3. CRISPR/cpF1基因编辑技术 ➢ 4. cas9 / casF /cpF1总结
CRISPR/cas9的基本原理
Part.1
CRISPR/cas9基因编辑原理
CRISPR/casF基因编辑技术
Part.2
CRISPR/ casF基因编辑技术
原理: casF能切割与crRNA互补的DNA,并且使用单个RuvC活 性位点进行pre-crRNA加工和切割。 casF分子量:cas9蛋白的一半 Cas蛋白结构域:HNH、RuvC 向导RNA:crRNA pre-crRNA加工方式:casF蛋白加工 DNA识别区:富含T的PAM 序列(5′TBN 3′,B是G、T或C) 优点:分子量小、对PAM区要求低,有利于基于载体向细胞内 递送和更广泛的可靶向基因组序列范围
《crisprcas9技术》课件

CRISPR-Cas9的应用
基因组编辑及修补
CRISPR-Cas9技术可以精确的定位基因组中特定位点 进行编辑和修补,是医学、农业、工业等领域中重 要的基因体系。
基因靶向表达
利用CRISPR-Cas9技术的靶向控制基因表达可以实现 治疗疾病、生产有用生物制品等应用。
基因调控
CRISPR-Cas9技术可选择性、有 Nhomakorabea地进行基因调控,
应用前景
• CRISPR-Cas9技术未来将 广泛用于医疗、农业、 工业、环保等领域,成 为生物技术创新的重要
• 推基动于C力R。ISPR-Cas9技术的 新产品、新技术、新应 用也将成为未来投资的 热点领域。
2
编辑系统的工作原理
CRISPR-Cas9通过识别、结合、切割目标基因位点,进一步实现对基因组的编辑 和修补,使基因组发生特定改变,达到治疗或改良目的。
3
PAM序列的特点
PAM序列指的是Cas9靶序列的附近序列,是单导RNA结合Cas9蛋白并定位于靶点 上的关键信息之一,其特点包括长度和序列的多样性。
农业遗传改良
利用CRISPR-Cas9技术对商业作物进行精准改良是未
CRISPR-Cas9技术的局限和挑战
1 异源物质的干扰
2 细胞外的嵌合酶
CRISPR-Cas9技术会受到外部异源物质的干扰, 影响其在目标细胞内的有效性。
CRISPR-Cas9技术需要有效的嵌合酶才能达到 预期效果,因此嵌合酶的研究一直是制约该 技术发展的瓶颈之一。
应用领域
CRISPR-Cas9技术已广泛应用于基因组编辑、基因表达调控、疾病治疗和药物筛选等领域,且 应用前景广阔。
CRISPR-Cas9系统的构成和原理
基因编辑技术课件

Editas宣布的2017年人体实验激动人心之处在于,这有可能是首次体内(in vivo)基因编辑试验。这项研究成功的意义在于,将CRISPR基因编辑“工具”装载到病毒体内,再把病毒注射到患处,CRISPR可以自行对患病部位进行基因改造。那么以后治疗Layla那样的白血病,不用分离T细胞了,直接将改造好的病毒注射到骨髓,就直接将基因异常的骨髓修复了,或者是直接整合目标基因加强其战斗力。这样一来,很多大手术就会变成微创手术,带来的好处是难以估量的。
根据CRISPR/Cas 系统这一特性,将其用于设计人工的核酸内切酶(engineered endonuclease,EEN),用来对我们感兴趣的基因位点进行修饰. 三类 CRISPR/Cas 系统中TypeⅡ型系统的核糖核蛋白复合物相对简单,除crRNA 和tracrRNA 外,只有Cas9 一个蛋白.目前,产脓链球菌(Streptococcus pyogenes SF370)的TypeⅡ型系统是被改造的最为成功的人工核酸内切酶。
利用同源重组机制对基因进行定向失活是为基因功能评估提供信息的有力手段。但是这一技术的应用有几个限制因素,包括遗传工程组件插入目标位点的效率低、筛选过程费时费力、有可能产生不利的突变效应等。
RNAi基因靶向敲除技术给研究者提供了快捷、廉价而且可以开展高通量研究的新方法,但是, RNAi的基因敲除效果还不够彻底,每次试验以及每个实验室的试验结果都会有差异,另外还存在不可预知的脱靶情况,所以只能够用于需要暂时抑制基因功能的试验当中。
第一代人工核酸内切酶:锌指核酸内切酶(zinc finger endonuclease, ZFN ),锌指是一类能够结合DNA的蛋白质,人类细胞的转录因子中大约有一半含有锌指结构,ZFN是将锌指蛋白与核酸内切酶Fok I融合形成的核酸内切酶,利用它可以在各种复杂基因组的特定位置制造DNA的双链切口。
根据CRISPR/Cas 系统这一特性,将其用于设计人工的核酸内切酶(engineered endonuclease,EEN),用来对我们感兴趣的基因位点进行修饰. 三类 CRISPR/Cas 系统中TypeⅡ型系统的核糖核蛋白复合物相对简单,除crRNA 和tracrRNA 外,只有Cas9 一个蛋白.目前,产脓链球菌(Streptococcus pyogenes SF370)的TypeⅡ型系统是被改造的最为成功的人工核酸内切酶。
利用同源重组机制对基因进行定向失活是为基因功能评估提供信息的有力手段。但是这一技术的应用有几个限制因素,包括遗传工程组件插入目标位点的效率低、筛选过程费时费力、有可能产生不利的突变效应等。
RNAi基因靶向敲除技术给研究者提供了快捷、廉价而且可以开展高通量研究的新方法,但是, RNAi的基因敲除效果还不够彻底,每次试验以及每个实验室的试验结果都会有差异,另外还存在不可预知的脱靶情况,所以只能够用于需要暂时抑制基因功能的试验当中。
第一代人工核酸内切酶:锌指核酸内切酶(zinc finger endonuclease, ZFN ),锌指是一类能够结合DNA的蛋白质,人类细胞的转录因子中大约有一半含有锌指结构,ZFN是将锌指蛋白与核酸内切酶Fok I融合形成的核酸内切酶,利用它可以在各种复杂基因组的特定位置制造DNA的双链切口。
CRISPR基因编辑技术讲课稿

并引起一系列生物伦理的问题…
基因组编辑技术
• 基因组编辑技术(genome editing)是一种可以在基因 组水平上对DNA序列进行改造的遗传操作技术。也称为基 因打靶(Gene targeting)。
• 技术的原理是构建一个人工内切酶,在预定的基因组位置 切断DNA,切断的DNA在被细胞内的DNA修复系统修复 过程中会产生突变,从而达到定点改造基因组的目的。
TALEN
TALEN(Transcription activator -like effectors):一种源于植物致病菌 的靶向基因操作技术。
科学家发现,来自植物细菌Xanthomonas sp. (黄单胞菌) 的TAL蛋白的核 酸结合域的氨基酸序列与其靶位点的核酸序列有恒定的对应关系,一个模块 单元识别一个碱基,简单且特异性极好。
DNA识别域:由一系列TAL蛋白串联组成(一般20个左右),每个TAL蛋白识 别并结合一个对应的碱基。 核酸内切酶: 非特异性核酸内切酶FokI,形成二聚体时切割双链DNA
TALEN原理
全长为34aa的Tal 蛋白的第12、13位氨基 残基可以特异性识别核苷酸碱基。 • NG可以识别T • HD可以识别C • NI可以识别A • NN可以识别G或A 通过这种特异性识别,将多个Tal蛋白组 装在一起,就可以构成可以识别目的片 段的Tale蛋白。
• DNA识别域虽然具有较强的特异性识别能力,但是其识别的序列长度 比较有限。
• 因为ZFN剪切的过程不完全依赖同源二聚体的形成,所以一旦形成异 源二聚体,就很可能造成脱靶效应;
• 如果出现脱靶,可能导致DNA的错配和序列改变,产生较强的细胞毒 性。当这些不良影响积累过多,超过细胞修复机制承受的范围时,便 会引起细胞的凋亡。
CRISPRCas基因编辑技术简介 ppt课件

2.2CRISPR结构:
CRISPR是一种特殊的DNA 重复序列家族,广泛分布于细菌 和古细菌基因组中。CRISPR位点通常由短的高度保守的重复序 列(repeats)组成,重复序列的长度通常为21--48bp,重复序列之 间被26--72bp间隔序列(spacer)隔开。CIRSPR通过这些间隔序列 (spacer)与靶基因进行识别。
4.CRISPR/Cas9系统
Type Ⅱ 因其简单性及可操作性,被改造成有力的基因工程工具--
CRISPR/Cas9。现在广泛使用的CRISPR/Cas9系统来源于酿脓链球菌。
Type II系统具有以下特点:
在CRISPR/Cas基因座 上游会表达tracrRNA;
tracrRNA会参与 crRNA的加工,这个 工程亦需要RNaseIII 的参与;
tracrRNA会与crRNA形 成二聚体指导Cas对 双链DNA的切割。
4.CRISPR/Cas9系统
Cas9是一种核酸内切酶,其具有:RuvC和HNH两个内切酶活性中心 Jinek等发现Cas9在细菌和试管里对双链DNA具有强烈的切割能 力,但是这种切割能力需要的crRNA和tracrRNA介导。
4.CRISPR/Cas9系统
4.CRISPR/Cas9系统
CRISPR/Cas 作用: 基因 脱靶效应
2013年,研究者们发表多篇文章介绍CRISPR/Cas9系统,但CRISPR/Cas9 目前仍存在一个很严重且无法避免的问题,即潜在的脱靶效应不可消 除。
CRISPR基因座的表达(包括转 录和转录后的成熟加工)
当该噬菌体再次入侵细菌时, CRISPR簇首先转录为长的 crRNA前体,然后逐步加工成 小的成熟的crRNA.
CRISPR/Cas系统活性的发 挥或外源遗传物质的干 扰
CRISPR是一种特殊的DNA 重复序列家族,广泛分布于细菌 和古细菌基因组中。CRISPR位点通常由短的高度保守的重复序 列(repeats)组成,重复序列的长度通常为21--48bp,重复序列之 间被26--72bp间隔序列(spacer)隔开。CIRSPR通过这些间隔序列 (spacer)与靶基因进行识别。
4.CRISPR/Cas9系统
Type Ⅱ 因其简单性及可操作性,被改造成有力的基因工程工具--
CRISPR/Cas9。现在广泛使用的CRISPR/Cas9系统来源于酿脓链球菌。
Type II系统具有以下特点:
在CRISPR/Cas基因座 上游会表达tracrRNA;
tracrRNA会参与 crRNA的加工,这个 工程亦需要RNaseIII 的参与;
tracrRNA会与crRNA形 成二聚体指导Cas对 双链DNA的切割。
4.CRISPR/Cas9系统
Cas9是一种核酸内切酶,其具有:RuvC和HNH两个内切酶活性中心 Jinek等发现Cas9在细菌和试管里对双链DNA具有强烈的切割能 力,但是这种切割能力需要的crRNA和tracrRNA介导。
4.CRISPR/Cas9系统
4.CRISPR/Cas9系统
CRISPR/Cas 作用: 基因 脱靶效应
2013年,研究者们发表多篇文章介绍CRISPR/Cas9系统,但CRISPR/Cas9 目前仍存在一个很严重且无法避免的问题,即潜在的脱靶效应不可消 除。
CRISPR基因座的表达(包括转 录和转录后的成熟加工)
当该噬菌体再次入侵细菌时, CRISPR簇首先转录为长的 crRNA前体,然后逐步加工成 小的成熟的crRNA.
CRISPR/Cas系统活性的发 挥或外源遗传物质的干 扰
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
佳的工作空间。
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系本人改正。
ZFN技术的缺陷
• DNA识别域虽然具有较强的特异性识别能力,但是其识别的序列长度 比较有限。
• 因为ZFN剪切的过程不完全依赖同源二聚体的形成,所以一旦形成异 源二聚体,就很可能造成脱靶效应;
• 如果出现脱靶,可能导致DNA的错配和序列改变,产生较强的细胞毒 性。当这些不良影响积累过多,超过细胞修复机制承受的范围时,便 会引起细胞的凋亡。
• 另一方面,该手段在细胞内部操作的精确程度不足,则可能会引起相 关基因突变,引发癌症等。
• ZFN 作为基因治疗的手段之一,如果在生物体内使用,可能会引发免 疫反应。而现有的研究手段尚不能预测引入的ZNF蛋白是否会引起免 疫系统的进攻。
• 到目前为止,ZFN技术只能用于体外操作(in vitro),在对人体提取 的细胞进行处理之后,再导入回输到病人体内。
个锌指蛋白识别并请勿模仿;如有不当之处,请联系本人改正。
核酸内切酶: 非特异性核酸内切酶FokI,形成二聚体时切割双链DNA
两条ZFN之间具有被称为“间隔区”的spacer结构,该结构的长度以5~6bp 为宜,7bp也能正常工作,合理的“间隔区”设计才能保证ZFN二聚体拥有最 8
基因组巡航导弹,分子剪刀,DNA外科医生 定点突变,定点修饰(包括得到转基因),转录调控 基因治疗(如遗传病)
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系本人改正。
基因编辑的三大利器
• ZFN (Zinc-finger nucleases, ZFN) • TALEN(transcription activator-like effector nucleases) • CRISPR/Cas (clustered regulatory interspaced short
• 技术的原理是构建一个人工内切酶,在预定的基因组位置 切断DNA,切断的DNA在被细胞内的DNA修复系统修复 过程中会产生突变,从而达到定点改造基因组的目的。
基因组编辑技术 文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系本人改正。
历史
1993年前ZFN就已开始出现,迄今已发展了20多年才有今天的成就; 2009年底出现的TALEN似乎一夜之间呈现出取代ZFN的架势; 2012年底CRISPR/Cas已显现出取代TALEN的巨大潜力,在2013年成为现实。
荣誉
1. 2011年:ZFN, TALEN和Meganuclease—2011年度方法(Nature Methods) 2. 2012年:TALEN — 2012年十大突破(Science) 3. 2013年:CRISPR/Cas被认为是诺贝尔奖级别的成果,华人科学家张峰已
因此获得生物医学大奖。
应用
通过组合各类模块,可对任意核苷酸序列进行靶向特异性敲除或内源基因 的表达调控。
目前已在人、大鼠、小鼠、猪、羊、斑马鱼、拟南芥及酵母等多类物种中 得到成功应用。
TALEN原理 文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系本人改正。
典型的 TALEN由一个包含核定位信号(NLS)的N端结构域、一个包含可识别特定 DNA序列的典型串联TALE重复序列的中央结构域,以及一个具有FokI核酸内切酶 功能的C端结构域组成。
4. 难以稳定的遗传
同源重组技术:e.g. 传统的基因敲除小鼠 5. 费时费力费钱,难以大量应用
并引起一系列生物伦理的问题…
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系本人改正。
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系本人改正。
基因组编辑技术
• 基因组编辑技术(genome editing)是一种可以在基因 组水平上对DNA序列进行改造的遗传操作技术。也称为基 因打靶(Gene targeting)。
palindromic repeat /Cas-based RNA-guided DNA endonucleases)
特异性 DNA识别域
+
非特异性 核酸内切酶
ZFN原理 文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系本人改正。
ZFN=蛋白的DNA识别域+核酸内切酶
DNA识别域: 由一系列 Cys2-His2锌指蛋白(zinc-fingers)串联组成(一般3~4个),每
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系本人改正。
TALEN
TALEN(Transcription activator -like effectors):一种源于植物致病菌 的靶向基因操作技术。
科学家发现,来自植物细菌Xanthomonas sp. (黄单胞菌) 的TAL蛋白的核 酸结合域的氨基酸序列与其靶位点的核酸序列有恒定的对应关系,一个模块 单元识别一个碱基,简单且特异性极好。
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系本人改正。
现状
基因突变技术:物理诱变、化学诱变… 1. 无法控制突变位点
转基因技术:T-DNA插入
2. 不能精确控制外源基因插入位点
RNA干扰技术:dsRNA、Artificial miRNA 3. 对靶基因抑制不彻底、不特异
核外遗传技术:质粒、人工染色体
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系本人改正。
• 自从证明DNA是遗传物质以后,人类就开始了通 过改变DNA来改造生物体生理机理和功能的尝试。
➢ 1973年,斯坦利·N·科恩(Stanley N. Cohen)和赫伯特·W·博耶 (Herbert W. Boyer) 成功将蛙的DNA插入到细菌中。 ➢ 20世纪70年代,基因泰克(Genetech)公司对大肠杆菌进行基因改造, 使其带有一个人源基因(这个基因是人工合成的),最后生产出治疗糖尿 病的胰岛素。 ➢ 1974年,,加利福尼亚州索克生物研究所(Salk Institute for Biological Studies)的Rudolf Jaenisch通过将SV40 病毒的DNA注射到小鼠的囊胚中, 培育出了第一只转基因小鼠。
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系本人改正。
ZFN技术的缺陷
• DNA识别域虽然具有较强的特异性识别能力,但是其识别的序列长度 比较有限。
• 因为ZFN剪切的过程不完全依赖同源二聚体的形成,所以一旦形成异 源二聚体,就很可能造成脱靶效应;
• 如果出现脱靶,可能导致DNA的错配和序列改变,产生较强的细胞毒 性。当这些不良影响积累过多,超过细胞修复机制承受的范围时,便 会引起细胞的凋亡。
• 另一方面,该手段在细胞内部操作的精确程度不足,则可能会引起相 关基因突变,引发癌症等。
• ZFN 作为基因治疗的手段之一,如果在生物体内使用,可能会引发免 疫反应。而现有的研究手段尚不能预测引入的ZNF蛋白是否会引起免 疫系统的进攻。
• 到目前为止,ZFN技术只能用于体外操作(in vitro),在对人体提取 的细胞进行处理之后,再导入回输到病人体内。
个锌指蛋白识别并请勿模仿;如有不当之处,请联系本人改正。
核酸内切酶: 非特异性核酸内切酶FokI,形成二聚体时切割双链DNA
两条ZFN之间具有被称为“间隔区”的spacer结构,该结构的长度以5~6bp 为宜,7bp也能正常工作,合理的“间隔区”设计才能保证ZFN二聚体拥有最 8
基因组巡航导弹,分子剪刀,DNA外科医生 定点突变,定点修饰(包括得到转基因),转录调控 基因治疗(如遗传病)
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系本人改正。
基因编辑的三大利器
• ZFN (Zinc-finger nucleases, ZFN) • TALEN(transcription activator-like effector nucleases) • CRISPR/Cas (clustered regulatory interspaced short
• 技术的原理是构建一个人工内切酶,在预定的基因组位置 切断DNA,切断的DNA在被细胞内的DNA修复系统修复 过程中会产生突变,从而达到定点改造基因组的目的。
基因组编辑技术 文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系本人改正。
历史
1993年前ZFN就已开始出现,迄今已发展了20多年才有今天的成就; 2009年底出现的TALEN似乎一夜之间呈现出取代ZFN的架势; 2012年底CRISPR/Cas已显现出取代TALEN的巨大潜力,在2013年成为现实。
荣誉
1. 2011年:ZFN, TALEN和Meganuclease—2011年度方法(Nature Methods) 2. 2012年:TALEN — 2012年十大突破(Science) 3. 2013年:CRISPR/Cas被认为是诺贝尔奖级别的成果,华人科学家张峰已
因此获得生物医学大奖。
应用
通过组合各类模块,可对任意核苷酸序列进行靶向特异性敲除或内源基因 的表达调控。
目前已在人、大鼠、小鼠、猪、羊、斑马鱼、拟南芥及酵母等多类物种中 得到成功应用。
TALEN原理 文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系本人改正。
典型的 TALEN由一个包含核定位信号(NLS)的N端结构域、一个包含可识别特定 DNA序列的典型串联TALE重复序列的中央结构域,以及一个具有FokI核酸内切酶 功能的C端结构域组成。
4. 难以稳定的遗传
同源重组技术:e.g. 传统的基因敲除小鼠 5. 费时费力费钱,难以大量应用
并引起一系列生物伦理的问题…
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系本人改正。
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系本人改正。
基因组编辑技术
• 基因组编辑技术(genome editing)是一种可以在基因 组水平上对DNA序列进行改造的遗传操作技术。也称为基 因打靶(Gene targeting)。
palindromic repeat /Cas-based RNA-guided DNA endonucleases)
特异性 DNA识别域
+
非特异性 核酸内切酶
ZFN原理 文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系本人改正。
ZFN=蛋白的DNA识别域+核酸内切酶
DNA识别域: 由一系列 Cys2-His2锌指蛋白(zinc-fingers)串联组成(一般3~4个),每
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系本人改正。
TALEN
TALEN(Transcription activator -like effectors):一种源于植物致病菌 的靶向基因操作技术。
科学家发现,来自植物细菌Xanthomonas sp. (黄单胞菌) 的TAL蛋白的核 酸结合域的氨基酸序列与其靶位点的核酸序列有恒定的对应关系,一个模块 单元识别一个碱基,简单且特异性极好。
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系本人改正。
现状
基因突变技术:物理诱变、化学诱变… 1. 无法控制突变位点
转基因技术:T-DNA插入
2. 不能精确控制外源基因插入位点
RNA干扰技术:dsRNA、Artificial miRNA 3. 对靶基因抑制不彻底、不特异
核外遗传技术:质粒、人工染色体
文档仅供参考,不能作为科学依据,请勿模仿;如有不当之处,请联系本人改正。
• 自从证明DNA是遗传物质以后,人类就开始了通 过改变DNA来改造生物体生理机理和功能的尝试。
➢ 1973年,斯坦利·N·科恩(Stanley N. Cohen)和赫伯特·W·博耶 (Herbert W. Boyer) 成功将蛙的DNA插入到细菌中。 ➢ 20世纪70年代,基因泰克(Genetech)公司对大肠杆菌进行基因改造, 使其带有一个人源基因(这个基因是人工合成的),最后生产出治疗糖尿 病的胰岛素。 ➢ 1974年,,加利福尼亚州索克生物研究所(Salk Institute for Biological Studies)的Rudolf Jaenisch通过将SV40 病毒的DNA注射到小鼠的囊胚中, 培育出了第一只转基因小鼠。
