舒芬太尼在ICU镇痛中的应用
舒芬太尼ICU

舒芬太尼减轻ICU患者应激
NE ug/ml
700 600 500 400 300 舒芬太尼 芬太尼组
200
100 t0
t1
t2
t3
19
--高东艳,陈丽等.舒芬太尼对小儿心脏手术麻醉中血流动力学和应激反应的影响.中国药物与临床.2009.9(2)
躁动
70%ICU患者可能出现躁动
谵妄
机械通气患者谵妄发病率为70%-80%
睡眠障碍
ICU患者均有不同程度的睡眠障碍 研究表明:疼痛是以上症状的最主要原因!
--ICU病人镇痛镇静治疗指南(2006)
11
ICU镇痛药物选择
ICU临床用药特点
多种药物和手段合并使用,注意药物相互作用 镇痛镇静药物累积量大 药代/药效动力学不稳定 随时调整药物种类和剂量
舒芬太尼呼吸抑制轻
1
0.5
0
-0.5 舒芬太尼
-1
芬太尼
-1.5
0 100 200 300 400
20
--Bailey P.L, et al. Differences in magnitude and duration of opioid induced respiratory depression and analgesia with Fentanyl and sufentanil . Anesth Analg, 1990,70:pp.8-15.
200 0
对照 诱导后5 min 插管后1 min 插管后10 min
24 --Freye,E.and E.Hartung, Kardiovaskulare und zentralnervose Effekte unter Fentanyl versus sufentanil bei der Intubation herzchirurgischer Patienten . Anasthesie Aktuell,1993,9:pp3-14
瑞芬太尼、舒芬太尼用于ICU镇痛

100%
舒芬太尼缩短恢复时间
时间:min 800 芬太尼 舒芬太尼
700
600 500
400
300 200
100
0 苏醒时间 气管拔管时间 呼吸机使用时间
舒芬太尼与镇静催眠药的协同性高
δ波功率
1400
1200 δ芬太尼 1000 800 600 400 δ舒芬太尼
200 0
对照 诱导后5min 插管后1min 插管后10min
舒芬太尼在ICU的应用
安全用于脑外伤患者
舒芬太尼对大脑的血流动力学不产生影响,不增高颅 内压,可以安全用于脑外伤患者
机械通气患者的镇痛与镇静
持续输注舒芬太尼0.2-0.3ug/(kg*h)可达到良好的镇痛 镇静效果同时不影响患者的呼吸功能(潮气量、分钟通 气量、呼吸频率)及循环功能(血压、心率)。
5
儿科患者(=>2岁): 无需调整瑞芬太尼 的剂量,剂量与成 人相同。
使用瑞芬太尼的注意事项
注意事项
1.由于瑞芬太尼的特殊代谢方式——非特异性酯酶 代谢,所以瑞芬太尼不能与血液制品同一通道给 药;
2.瑞芬太尼不能与单胺氧化酶抑制剂合用;
3.因为瑞芬太尼中含有甘氨酸,所以不能硬膜外或 鞘内给药; 4.对芬太尼类药品过敏者禁用。
舒芬太尼在ICU的应用
舒芬太尼常用于ICU长时间镇静1
半衰期短于芬太尼 肝脏清除率高于芬太尼 停止术后后恢复时间比芬太尼短
例如
舒芬太尼0.125ug/(kg*h)或瑞芬太尼10ug/(kg*h)复合 咪达唑仑0.1mg /(kg*h)用于长时间使用呼吸机患者中 维持镇静镇痛,结果显示随时间延长舒芬太尼用量减 少,停药后撤机时间比瑞芬太尼长
静吸麻醉术后ICU老年患者应用舒芬太尼复合右美托咪定行静脉自控镇痛的效果

[4] 吴曼,邢桂英,于建设,等.硬膜外阻滞复合浅全麻用于老年高血压 病患者开胸手术[J].中国临床实用医学,2010,11(4):26-27.
河南外科学杂志 2018年 9月第 24卷第 5期 HENANJOURNALOFSURGERYSep.2018,Vol24,No5
·79·
10mL/kg,呼吸比 1∶2,通气频率 12~14次 /min,血氧饱 和度 >98%。间断静注丙泊酚 4~12mg/(kg· h),舒 芬太尼 02μg/(kg·h),顺阿曲库铵 007mg/kg。并 吸入 15% ~20%七氟醚麻醉维持。术毕前 30min停 用七氟醚、顺阿曲库铵及舒芬太尼,20min后停用丙泊 酚。术毕连接 PCIA入住 ICU。 1.2.1 自 控 静 脉 镇 痛 用 药 (1)对 照 组:舒 芬 太 尼 20μg/kg。(2)观察组:舒芬太尼 20μg/kg复合右美 托咪定 10μg/kg。2组均用生理盐水稀释至 200mL。 PCIA持续背景输出量设置为 2mL/h,单次给药剂量为 05mL,锁定时间为 15min。 1.3 评价 指 标 根 据 视 觉 模 拟 量 表 (VAS)[2]记 录 术 后各时点患者的 VAS评分(0分为无痛,10分为剧烈疼 痛。分值越高,表示疼痛越严重)。记录苏醒期躁动分 级[3](0级:无躁动及呻吟。1级:吸痰等刺激时轻度躁 动及呻 吟。2级:中 度 躁 动 及 持 续 呻 吟,无 需 按 压。3 级:剧烈躁动,需按压)、按压 PCIA次数和嗜睡、恶心呕 吐、心动过缓等不良反应。 1.4 统计学方法 数据采用 SPSS180统计学软件进 行分析。计量资料用均数 ±标准差 (x珋±s)表示,t检 验;计数资料 用 率 (%)表 示,卡 方 检 验。 P<005为 差 异具有统计学意义。 2 结果 2.1 VAS评分 观察组患者术后各时点 VAS评分明 显低于对照组,差异有统计学意义(P<005),见表 1。 观察组患者术后按压 PCIA(234±078)次,对照组为 (438±112)次,差异有统计学意义(P<005)。
舒芬ICU运用

注意事项
应有呼吸辅助设施。 应有呼吸辅助设施。 应有监测设备。 应有监测设备。 甲低,肺部疾病(COPD),肝、肾功能不全, 甲低,肺部疾病(COPD),肝 肾功能不全, (COPD), 肥胖和酒精中毒,体弱及老年患者应减量。 肥胖和酒精中毒,体弱及老年患者应减量。 哺乳期静脉使用舒芬太尼,24h后才能哺乳 后才能哺乳。 哺乳期静脉使用舒芬太尼,24h后才能哺乳。
血液动力学稳定性更好 呼吸抑制的比率小, 呼吸抑制的比率小, 术后恢复快 术后镇痛效果比芬太尼好, 术后镇痛效果比芬太尼好,持续时间比芬太尼长 恶心、呕吐、 恶心、呕吐、瘙痒等不良反应更少
舒芬太尼临床优势 舒芬太尼临床优势
更符合现代镇痛技术
长时间静脉持续输注无蓄积 可以得到非常稳定的血药浓度, 可以得到非常稳定的血药浓度,镇痛及镇静水平稳定 稳定的血流动力学 术后意识恢复的时间很快
舒芬太尼的临床应用
宜昌人福药业有限责任公司
舒芬太尼(Sufentainil) 是一种 舒芬太尼 (Sufentainil)是一种 强效的阿片类 是一种强效的阿片类 镇痛药,同时也是一种高选择u 激动剂。 镇痛药,同时也是一种高选择u-激动剂。镇 痛效应强与芬太尼、 吗啡。 痛效应强与芬太尼 、 吗啡 。 舒芬太尼与阿 片受体的结合具有饱和性、 片受体的结合具有饱和性 、 可逆性和特异 它与阿片受体的亲和力是芬太尼的 亲和力是芬太尼的7 性 。 它与阿片受体的 亲和力是芬太尼的 7.7 倍以上, 倍以上 , 而且具有良好的血液动力学稳定 同时保证足够的心肌氧供。 性,同时保证足够的心肌氧供。
舒芬太尼临床优势 舒芬太尼临床优势
镇痛作用更好
安全阈宽,治疗指数 ;(芬太尼 安全阈宽,治疗指数>25000;(芬太尼 ;(芬太尼270) ) 等效剂量下, 等效剂量下,只需芬太尼用量的十分之一 镇痛时间长,是芬太尼的 倍 镇痛时间长,是芬太尼的2倍 提高痛阈
舒芬太尼在ICU镇痛中的应用 县人民医院ICU

下丘脑-垂体-肾上腺皮质系统
机体创伤后,通过传人神经投射于蓝斑和下 丘脑,合成和分泌大量的促肾上腺皮质激素 释放激素,刺激垂体前叶释放促肾上腺皮质 激素,肾上腺皮质合成和释放糖皮质激素。
糖皮质激素的作用
1、促进蛋白质、脂肪分解,增强糖原异生,升高血糖,以保证重要器官的能量供应 2、提高心血管系统对儿茶酚胺的敏感性 3、降低毛细管的通透性,有利于血容量的维持 4、稳定溶酶体膜,防止或减轻组织损伤 5、抑制化学介质(白三烯、血栓素、前列腺素和 5~羟色胺等)的合成,减轻炎症反 应,减轻组织损伤 6、降低肾小球入球小动脉的阻力,增加肾小球的滤过率 7、抑制肥大细胞的脱颗粒反应,减少组胺释放
阿片类药物的临床应用史
◆我们应对芬太尼家族进行再认识!
●芬太尼的唯一优势:价格 ●瑞芬太尼: ①短小手术;②肝肾功能不全手术;③老年病人手术 ● 舒芬太尼: ①中长时间手术;②分娩镇痛;③术后镇痛; ④ICU气管插管病人的镇静和镇痛
芬太尼家族的特点
• 起效时间
– 量、强度、用药方式 – 起效-血脑平衡时间:瑞芬太尼1min;阿芬太尼 1min;芬太尼6.6min;舒芬太尼6.2min。 • 副作用 – 呼吸抑制 – 骨骼肌强直 – 恶心、呕吐、便秘
阿片类作用于阿片受体“膜电位超极化”
神经末梢的递质(P物质、Ach、NA、
DA等)释放减少“阻断神经冲动的传递”
产生各种效应
阿片类作用于CNS阿片受体,抑制P物质
的释放,产生镇痛作用。
痛觉传导及阿片类的镇痛作用
中 枢
P物质
脊髓接 受神经 元
脊髓后根 痛觉传入 神经元 脊髓中 间神经 元
舒芬太尼在ICU的用法用量查对表doc
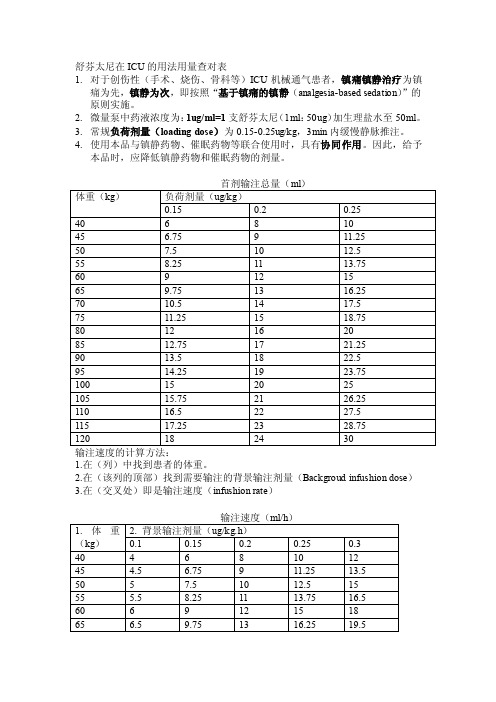
舒芬太尼在ICU的用法用量查对表
1.对于创伤性(手术、烧伤、骨科等)ICU机械通气患者,镇痛镇静治疗为镇
痛为先,镇静为次,即按照“基于镇痛的镇静(analgesia-based sedation)”的原则实施。
2.微量泵中药液浓度为:1ug/ml=1支舒芬太尼(1ml:50ug)加生理盐水至50ml。
3.常规负荷剂量(loading dose)为0.15-0.25ug/kg,3min内缓慢静脉推注。
4.使用本品与镇静药物、催眠药物等联合使用时,具有协同作用。
因此,给予
本品时,应降低镇静药物和催眠药物的剂量。
1.在(列)中找到患者的体重。
2.在(该列的顶部)找到需要输注的背景输注剂量(Backgroud infushion dose)
3.在(交叉处)即是输注速度(infushion rate)
整。
舒芬太尼在重症医学科患者镇痛治疗中的应用效果观察

舒芬太尼在重症医学科患者镇痛治疗中的应用效果观察摘要目的观察舒芬太尼在重症医学科患者镇痛治疗中的应用效果。
方法重症加强治疗病房收治的86例患者,随机分为观察组与对照组,各43例。
观察组给予咪达唑仑联合舒芬太尼镇痛治疗,对照组仅给予咪达唑仑镇痛治疗。
观察两组患者的临床疗效。
结果用药1 h后,观察组心率、呼吸频率、血氧饱和度及平均动脉压等均优于对照组,Ramsay评分(镇静评分)显著优于对照组,差异均具有统计学意义(P<0.05)。
结论舒芬太尼在重症医学科患者镇痛治疗的应用效果理想,值得在临床上推广。
关键词舒芬太尼;重症医学科;镇痛治疗;效果在重症加强治疗病房(ICU)患者中给予镇静、镇痛治疗是挽救患者生命、提高其生活质量的重要内容[1]。
为研究舒芬太尼在重症医学科患者镇痛治疗的应用效果,作者展开本次研究,现报告如下。
1 资料与方法1. 1 一般资料选取2014年6~12月本院重症加强治疗病房收治的患者86例,其中男49例,女37例,年龄23~77岁,平均年龄(51.4±6.4)岁;其中手术治疗74例,保守治疗12例;意识清醒者76例,意识不清醒者10例。
将其随机分为对照组与观察组,各43例。
两组患者基线资料比较差异无统计学意义(P>0.05),具有可比性。
1. 2 方法两组患者进行镇静、镇痛治疗前均根据具体病情给予营养支持、抗感染治疗及脏器功能保护等常规治疗。
对照组仅给予咪达唑仑治疗,将咪达唑仑注射液20 mg加入0.9%的氯化钠注射液20 ml中进行静脉滴注治疗,每隔2 h根据患者疼痛评分适当调整滴注速度。
观察组给予咪达唑仑联合舒芬太尼治疗,将50~100 mg舒芬太尼、20 mg咪达唑仑及50 ml浓度为0.9%生理盐水中稀释,使用微量注射泵以2~4 ml/h的速度进行持续静脉泵入。
用药期间需详细监测患者呼吸、血氧饱和度及平均动脉压等变化情况。
1. 3 观察指标及疗效评价标准[2,3] 治疗1 h后,详细记录两组患者心率、呼吸频率、血氧饱和度及平均动脉压等,以便进行效果评价。
研究舒芬太尼在重症医学科患者镇痛治疗中的疗效

研究舒芬太尼在重症医学科患者镇痛治疗中的疗效摘要】目的:客观了解重症医学科患者专业镇痛治疗中施以舒芬太尼疗法的价值。
方法:选取87例因患重症疾病而于2015年8月—2017年2月间入住我院重症医学科的患者,以镇痛疗法的不同进行分组:42例甲组病例行咪达唑仑疗法,而45例乙组病例则加行舒芬太尼疗法,分别统计两组病例镇痛质量,再作对比。
结果:42例甲组病例用药后Ramsay计(2.15±0.50)分,45例乙组病例是(3.60±0.40)分,(P<0.05);且用药1小时后,乙组病例脉动压值、心率值、血氧饱和度及其呼吸频率等显著优于甲组,(P<0.05)。
结论:对于接受镇痛治疗的重症医学科病例,通过施以舒芬太尼疗法,可充分提升机体镇痛质量,推荐选用。
【关键词】咪达唑仑疗法;重症医学科;舒芬太尼疗法;镇痛治疗;Ramsay计分【中图分类号】R614 【文献标识码】A 【文章编号】1007-8231(2017)05-0060-02重症医学科日常工作中,最为重要的环节之一即为镇痛治疗,通过改善机体疼痛感,在消除其躁动情绪、焦虑情绪的基础上,提升救治工作水平。
为了解舒芬太尼疗法在我院开展现状,在选取87例因患重症疾病而于2015年8月—2017年2月间入住我院重症医学科的患者的同时,分组施以不同镇痛疗法,旨在提升镇痛工作实践效率,实现对患者疼痛感的充分控制。
1.临床信息及方法1.1 临床信息选取87例因患重症疾病而于2015年8月—2017年2月间入住我院重症医学科的患者,以镇痛疗法的不同进行分组。
42例甲组,23岁~77岁,均值(42.2±3.33)岁;25例(男)/17例(女)。
45例乙组,24岁~76岁,均值(43.0±2.22)岁;27例(男)/18例(女),分别统计甲组、乙组病例信息,比较结果缺乏显著性,(P>0.05)。
1.2 方法42例甲组病例行咪达唑仑疗法:于氯化钠注射液(给药标准:20.0ml)中添加咪达唑仑(给药标准:20.0mg),使其充分融合后,给予患者用药,给药途径是静滴。
舒芬太尼在术后ICU患者镇静镇痛中的应用研究

舒芬太尼在术后ICU患者镇静镇痛中的应用研究作者:马冬璞李保林李成建杨彩浮来源:《中国当代医药》2013年第33期[摘要] 目的探讨舒芬太尼在术后ICU患者镇静镇痛中的临床有效性和安全性。
方法选择术后ICU患者60例,随机分为对照组和观察组,对照组患者采用芬太尼注射液镇静镇痛,观察组使用舒芬太尼注射液镇静镇痛。
比较观察两组患者治疗前及治疗后30 min、60 min、6 h、12 h、24 h、48 h的呼吸频率、脉搏血氧饱和度(SpO2)、氧合指数(PaO2/FiO2)。
结果两组患者在用药期间至观察结束呼吸频率差异无统计学意义(P>0.05),但观察组在镇痛24 h、48 h PaO2/FiO2、SpO2明显高于对照组,差异有统计学意义(P[关键词] 舒芬太尼;ICU患者;镇静镇痛[中图分类号] R971+.2 [文献标识码] A [文章编号] 1674-4721(2013)11(c)-0176-02Clinical reserch of sufentanil in sedatives and analgesics of the postoperative ICU patientsMA Dong-pu LI Bao-lin LI Cheng-jian YANG Cai-fuDepartment of Intensive Care Unit, Zhengzhou Central Hospital Affiliated to Zhengzhou University, Zhengzhou 450007, China[Abstract] Objective To explore clinical effect and safety of sufentanil in sedatives and analgesics of the postoperative ICU patients. Methods 60 postoperative ICU patients were randomly divided into two groups. The patients in the control group were intravenously treated with fentanyl,while patients in the observation group were intravenously given sufentanil. Then the respiratory frequency, pulse oxygen saturation (SpO2)and oxygenation index(PaO2/FiO2) were compared between the two groups before and 30 minutes, 60 minutes, 6 h, 12 h, 24 h and 48 h after treatment. Results The respiratory frequency shows no insignificant difference between the two groups before and after treatment (P>0.05). There were significant differences in SpO2 and PaO2/FiO2 between the two groups at 24, 48 h after treatment(P[Key words] Sufentanil; ICU patients; Sedatives and analgesics镇静镇痛对于术后ICU危重患者有重要意义,可调节或减轻应激反应,减少肺部并发症,促进患者及早活动,预防深静脉血栓形成等,已成为术后ICU患者治疗的重要组成部分。
舒芬太尼在术后ICU患者镇静镇痛中的应用研究

舒芬太尼在术后ICU患者镇静镇痛中的应用研究目的探讨舒芬太尼在术后ICU患者镇静镇痛中的临床有效性和安全性。
方法选择术后ICU患者60例,随机分为对照组和观察组,对照组患者采用芬太尼注射液镇静镇痛,观察组使用舒芬太尼注射液镇静镇痛。
比较观察两组患者治疗前及治疗后30 min、60 min、6 h、12 h、24 h、48 h的呼吸频率、脉搏血氧饱和度(SpO2)、氧合指数(PaO2/FiO2)。
结果两组患者在用药期间至观察结束呼吸频率差异无统计学意义(P>0.05),但观察组在镇痛24 h、48 h PaO2/FiO2、SpO2明显高于对照组,差异有统计学意义(P<0.05),观察组不良反应发生率明显低于对照组。
结论舒芬太尼用于术后ICU患者镇静镇痛有效性及安全性较高。
[Abstract] Objective To explore clinical effect and safety of sufentanil in sedatives and analgesics of the postoperative ICU patients. Methods 60 postoperative ICU patients were randomly divided into two groups. The patients in the control group were intravenously treated with fentanyl,while patients in the observation group were intravenously given sufentanil. Then the respiratory frequency,pulse oxygen saturation (SpO2)and oxygenation index(PaO2/FiO2)were compared between the two groups before and 30 minutes,60 minutes,6 h,12 h,24 h and 48 h after treatment. Results The respiratory frequency shows no insignificant difference between the two groups before and after treatment (P>0.05). There were significant differences in SpO2 and PaO2/FiO2 between the two groups at 24,48 h after treatment(P<0.05). The clinical adverse drug reaction rate in the observation group was lower than that in control group. Conclusion The sufentanil has better clinical effect and high safety in the sedatives and analgesics of postoperative ICU patients.[Key words] Sufentanil;ICU patients;Sedatives and analgesics镇静镇痛对于术后ICU危重患者有重要意义,可调节或减轻应激反应,减少肺部并发症,促进患者及早活动,预防深静脉血栓形成等,已成为术后ICU 患者治疗的重要组成部分。
舒芬太尼硬膜外持续输注用于ICU术后镇痛

舒芬太尼硬膜外持续输注用于ICU术后镇痛:与硬膜外芬太尼的比较摘要舒芬太尼是一种强效阿片类镇痛药,与芬太尼相比,具有更强的镇痛活性,适用人工呼吸气管内插管的全身麻醉,也作为复合麻醉的镇痛、全身麻醉大手术的麻醉诱导和维持用药,在术前、术中、术后及重症监护室内的镇静/镇痛都有广泛的应用。
舒芬太尼是一种芬太尼衍生物,它的特性使其比芬太尼更利于持续地硬膜外给药。
其效能是芬太尼的5-7倍,而半衰期较短(T1/2 α 1.4min;T1/2β17.1min)。
舒芬太尼有着高脂溶性和高的受体亲和力,致使其麻醉起效快,作用时间长关键词舒芬太尼芬太尼资料和方法试验对象为拟行择期上腹部手术并被SICU收治的40名患者,这些患者术前均存在一定的心肺疾病(其中有23例为血管疾病)。
本次试验征得了University of Cape Town 伦理委员会的同意。
术前,向患者解释数字评分法,并使其熟悉赖特呼吸计。
本试验采取双盲对照的方法,随机将试验对象分为试验组(舒芬太尼)和对照组(芬太尼),每组20名患者。
麻醉前给予;苯二氮卓类作为术前用药,术中的阿片类药只用芬太尼,并且用量限制为《3ug/kg/h。
在手术室进行肌松恢复。
术后由一名观察者于L2-3处置入硬膜外导管。
术后当患者刚开始诉说疼痛时,用数字评分法对其疼痛程度进行评估,并在硬膜外注入首量麻醉性镇痛药后开始持续输注。
对照组首先给于首量(5mg吗啡/10ml生理盐水),随后以0.5mg/h(20mg/200ml)的速度持续输注;试验组首量为50ug舒芬太尼/10ml生理盐水,继以5ug/h(200ug/200ml)的速度持续输注。
如果需要,可以辅助给予吗啡2-4mg静脉注射。
关于疼痛的评估由研究者对护士进行训练。
疼痛评估包括以下几点:1护士通过观察患者对刺激的反应如咳嗽、活动、吸痰、理疗进行评估(严重为1分、中等2分。
轻微3分、无痛4分);2 患者自己通过数字评分法进行评估(最严重的疼痛为10分,无痛为0分);3 通过对辅助吗啡的需要量进行评估;4 通过最大肺活量进行评估。
舒芬太尼在重症医学科患者镇痛治疗中的应用效果观察

舒芬太尼在重症医学科患者镇痛治疗中的应用效果观察【摘要】舒芬太尼是一种强效的阿片类镇痛药物,在重症医学科患者镇痛治疗中有着广泛的应用。
本研究旨在观察舒芬太尼在重症医学科患者中的镇痛效果,并探讨其应用的临床意义。
文中详细介绍了舒芬太尼的特点及作用机制,以及其在镇痛治疗中的临床应用情况。
通过对一定量的重症医学科患者进行舒芬太尼治疗,并观察其治疗效果,结果显示舒芬太尼在镇痛治疗中具有显著的疗效。
研究方法采用了XXXX,结果分析指出了XXXX。
结论部分总结了舒芬太尼在重症医学科患者镇痛治疗中的应用效果,并展望了未来研究方向。
本研究有助于提高重症医学科患者的镇痛治疗水平,促进患者的康复。
【关键词】舒芬太尼、重症医学科、患者、镇痛治疗、应用效果、观察、特点、作用机制、临床应用、研究方法、结果分析、展望未来、研究方向、结论总结。
1. 引言1.1 研究背景舒芬太尼是一种强效的合成阿片类药物,具有快速起效、作用持续时间短、镇痛效果好等特点。
在临床上,舒芬太尼主要用于手术麻醉和术后镇痛,常被用于重症医学科患者的疼痛治疗。
重症医学科患者往往需要接受多种治疗和操作,其中疼痛管理尤为重要。
目前关于舒芬太尼在重症医学科患者镇痛治疗中的应用效果的研究还比较有限。
随着重症医学科的发展和患者数量的增加,对镇痛治疗的需求也在不断增加。
深入研究舒芬太尼在重症医学科患者中的应用效果,可以为改善重症患者的疼痛管理提供更科学的依据。
对舒芬太尼的临床应用进行观察和总结,有助于进一步完善镇痛治疗方案,提高患者的舒适程度和治疗效果。
本研究旨在探讨舒芬太尼在重症医学科患者镇痛治疗中的应用效果,为临床实践提供参考和指导。
1.2 研究目的研究的目的是评估舒芬太尼在重症医学科患者镇痛治疗中的应用效果,探讨其对患者疼痛缓解和生命质量的影响。
通过观察舒芬太尼在临床实践中的效果,可以为重症医学科患者的镇痛治疗提供更有效的方法和指导,促进患者康复和病情的改善。
舒芬太尼

舒芬太尼摘要:本品为芬太尼的衍生物,药用其枸橼酸盐。
主要作用于μ阿片受体。
20世纪80年代欧美等国已开始舒芬太尼麻醉的临床研究。
随着研究不断深入,已证实舒芬太尼在许多方面优于芬太尼,其应用范围也不断扩大。
其在药效学、药理学与药代动力学方面有一定的特性,镇痛强度大,作用时间长,更平稳。
舒芬太尼在人工流产术、分娩镇痛、全身麻醉、椎管内阻滞等方面都有很好的临床应用。
下面对舒芬太尼进行详细的介绍。
1、药理学与药代动力学特性舒芬太尼(sufentanil,Suf)是芬太尼(Fentanyl,Fen)N-4位取代的衍生物,属苯基哌啶类,其化学名称为:N-{4-甲氧甲基-1-[2-(2-噻吩)乙基]-4-哌啶基}-N-苯基丙酰胺枸橼酸盐,其结构式为:舒芬太尼的脂溶性高,亲脂性约为芬太尼的2倍,极易透过血脑屏障,并能迅速在脑内达到有效浓度,因此,虽然其消除半减期较芬太尼短,但由于与阿片受体的亲和力较芬太尼强,故不仅镇痛强度大,约为芬太尼的5~10倍,而且作用持续时间也更长。
舒芬太尼的分布容积为1.7L/kg,而芬太尼为4.1L/kg,虽然舒芬太尼的亲脂性高于芬太尼,但其分布容积却比芬太尼小,可能原因包括:①舒芬太尼与血浆蛋白的结合率为92.5%,明显高于芬太尼,尤其是与α1酸性糖蛋白的结合率。
②芬太尼与α1酸性糖蛋白的结合较疏松,所以滞留于血浆中的量较少,易分布于组织,因此,分布容积增大。
舒芬太尼240min输注后时量相关半减期(C-ST1/2)为33.9min,在组织中无明显蓄积现象,在脂肪和肌肉组织易清除。
其经肝脏转化为N-去羟基和O-去甲基的代谢物,代谢产物从尿和胆汁排出,以原形从尿排除不到1%。
其中去甲基舒芬太尼也有药理活性,效价约为舒芬太尼的1/10,即相当于芬太尼,这也是舒芬太尼作用时间长的原因之一。
2、药效学特性舒芬太尼镇痛强度为芬太尼的5~10倍,作用时间为其2倍。
治疗指数(LD50/ED50)为25211,是阿片类中最安全的一个,对呼吸的抑制与芬太尼相似,主要表现为呼吸频率减慢,剂量较大时,潮气量也减少,直至呼吸抑制,对呼吸的抑制短于镇痛作用,且可被纳洛酮拮抗,对心血管的抑制也与芬太尼相似,表现为心率减慢,可用阿托品对抗,血压下降,但比芬太尼更平稳。
舒芬(icu)

阿片类镇痛药在ICU的应用
间断肌内注射 静脉连续输注 皮下连续输注
PCA 硬膜外置管
适用于患者局部灌注不良,效果不稳定 常用方法,需根据效果评估调整用量 急性镇痛不推荐
意识障碍,老年患者不能保证用药效果 应与局麻药合用
枸橼酸舒芬太尼
1974 成功研制
1976
1979
1984
2005
其化学及药 理特性被首 次报道
身体依赖
身体依赖为规律性给药的患者,停药或骤然减量导致停药反应,表现为焦 虑、易激怒、震颤、皮肤潮红、全身关节痛、出汗、卡他症状、发热、恶 心呕吐、腹痛腹泻等。逐步减量可避免身体依赖的发生。
热点问题—阿片类药物常见不良反应及应对措施
缩瞳
μ受体和κ受体激动剂兴奋动眼神经副交感核导致瞳孔缩小,长期使用阿 片类药物的患者可能发生耐受,但若增加剂量认可表现为瞳孔缩小。应注 意鉴别高碳酸血症和低氧血症也可改变瞳孔大小。
特点六:不良反应发生率低
结论:两组病例的术后镇痛效果差异无显著性 (P>0.05)。不良反应情况,舒芬 太尼组明显低于芬太尼组 (P<0.05)。
--孙静娴.舒芬太尼和芬太尼用于术后自控镇痛的临床观察.包头医学.2007.31(4)
舒芬太尼产品小结
简要说明书
【通用名】 【成 分】 【辅 料】 【性 状】 【适应症】 【包 装】 【贮 藏】 【有效期】
对重症学科疾病转归的认识
• 20th70s:损伤→感染→脓毒症(sepsis) → MOF • 20th90s:损伤→机体应激反应→ SIRS → MODS → MOF
-《实用重症医学》,第1版,人民卫生出版社
ICU中镇痛治疗的必要性
单纯镇静治疗
患者经常难于拔管(药物积累,过 度镇静),呼吸机相关肺炎的发生
舒芬太尼在分娩镇痛的应用北大医院
6
硬膜外舒芬太尼的最低有效剂量(4)
0.0625%bupi+adr1.25μg/ml+suf 0.5、0.75、 1μg/ml;6ml/h infusion。 结果:三组舒芬太尼镇痛效果无差异 ;皮肤搔痒 随剂量而增加51%、53%、65%。 结论:为减轻对母婴的不良反应,建议使用较低 的有效剂量。
Can J Anesth,1998,45:620-625
18
鞘注舒芬太尼对于胎心和宫缩的影响
比较硬膜外:0.125% bupi+0.75μg/ml suf,CSE: 2.5mg bupi+1.5μg suf, CSE:7.5μg suf 镇痛 60min内对于胎心和宫缩的影响。 结果:胎心异常:11%、12%、24%; 宫缩异常:2%、2%、12%; 严重低血压:7%、29%、12%; 镇痛起效:慢、快、快。 结论:CSE7.5μg suf导致较多胎心和宫缩异常。
Anesthesia, 2001, 56:526-529
9
布比卡因的有效镇痛剂量
序贯法,147例产妇,宫口<7cm。 随机分组: bupi+suf0、0.5、1、1.5μg/ml,硬膜 外首量均为20ml。 镇痛有效:30min时VAS<10mm。 结果:布比卡因的最低镇痛浓度0.104%,复合舒 芬太尼0.5、1、1.5μg/ml后,最低镇痛浓度分别为 0.048%、0.021%和0.009%(p<0.0001)。
清除率(ml/min/kg)
3-5
10-20
2.5-3.0
10-15
1
舒芬太尼的药代动力学(2)
脂溶性高,起效快; 镇痛性能最强,静脉用药是芬太尼的10倍,硬膜 外用药是芬太尼的4-6倍; 与阿片受体结合力强,无耐受性。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
神经末梢的递质(P物质、Ach、NA、
DA等)释放减少阻断神经冲动的传递
产生各种效应
阿片类作用于CNS阿片受体,抑制P物质
的释放,产生镇痛作用。
痛觉传导及阿片类的镇痛作用
中 枢
P物质
脊髓接 受神经 元
脊髓后根 痛觉传入 神经元 脊髓中 间神经 元
脑啡肽
【作用机制】
21
芬太尼家族镇痛作用
药物 效能 最低有效血浆浓度(ng/ml) 20 0.2 0.02 0.2
吗啡 1 芬太尼 100 舒芬太尼 1000 瑞芬太尼 134
舒芬太尼的药理特点
舒芬太尼的药理学特点
◆药效学
舒芬太尼(Sufentainil)是一种强效的阿片类镇痛药,同时也是一种高选择u-激动剂。 ●起效(min)快于芬太尼(2 vs 7) ●镇痛作用约比芬太尼强7-10倍 ●镇痛作用时间(h)比芬太尼长2倍(11 vs 4.5) ●小剂量使用有一定的镇静作用
阿片类药物的临床应用史
◆1806年→法国泽尔蒂纳从鸦片分离出睡眠之神Morpheus →吗啡→“临床新纪元”
●镇痛作用强,但思维和记忆障碍并出现幻觉→谵妄 ●呼吸抑制尤其是延迟性呼吸抑制→ 死亡 ●身体和心理上严重依赖→成瘾性
◆1960年→人工合成第一个芬太尼家族成员→芬太尼→“临床麻醉应用新纪元”
阿片类药物的临床应用史
●镇痛作用更强,但起效慢 ●但胸壁强直和剂量依赖性呼吸抑制 ●应激反应抑制不全和封顶效应 ●镇静作用弱且意识消失不完全
◆1974年→人工合成第二个芬太尼家族成员→“舒芬太尼”
●镇痛作用最强,起效快 ●镇静作用比芬太尼强,催眠效应 ●对循环和呼吸系统影响更小 ●镇痛作用最长
阿片类药物的临床应用史
●老年人:呼吸代偿功能差 ●缺血性心脏病患者:缺氧和二氧化碳蓄积 ●肝功能不全肾功能不全:维持剂量相应减少 ●一般情况较差者慎用
◆瑞芬太尼
临床应用
随机、对照、双盲研究 20位老年(年龄65-86岁),腹部大手术患者 fentanyl-nitrous oxide与sufentanil-nitrous oxide fentanyl:7ug/kg→ 3ug/kg/h; sufentanil:1ug/kg→ 0.4ug/kg/h 诱导、插管、手术 平均动脉压、心率、血儿茶酚胺浓度
吗啡曾经是最常用ICU镇痛剂,SCCM指南推荐应用,但是欧洲指南建议, 当镇痛剂应用时间超过24小时的情况下,不建议应用吗啡。
常用阿片类药物-药代动力学
吗啡
代谢部位 排泄部位 清除率 (ml/kg/min) 排泄半衰期 (min) 4h持续输注半 衰期(min) 蓄积率 肝脏(吗啡-6-葡 萄糖醛酸,2倍)
舒芬太尼的药理学特点
◆药物特点
●强脂溶性:亲脂性为芬太尼的2倍→易透过细胞膜和血脑屏障 ●离子化率低于芬太尼→易透过细胞膜和血脑屏障 ●与μ1受体高选择性、饱和性和可逆性结合 ●与μ1受体的亲和力显著高于芬太尼(7~8倍)
舒芬太尼的药理学特点
◆药代动力学
●血浆蛋白结合率(%)高于芬太尼(93 vs 84) ● 分布容积 (L/kg) 低于芬太尼(2.9 vs 4.1) ●肝生物转化完全,其最终代谢产物基本无活性,仅2%以原形排泄 ●给药后2h储存于体内量(%)显著少于芬太尼(3 vs 25) ●血浆消除半衰期 (min)短于芬太尼(160 vs 240) ●时量相关半衰期仅为芬太尼的1/7 →适合TCI和持续输注
阿片受体功能
在中枢和外周神经系统,内阿片肽可能作为神经递
质、神经调质或神经激素
内阿片肽+阿片受体——内源性痛觉调制系统; 调节心血管、胃肠、免役、内分泌功能。 μ受体激动药——镇痛最强 κ受体——与内脏化学刺激疼痛有关;参与吗啡依赖 δ 受体——参与吗啡的镇痛 σ受体激动——幻觉、烦躁
作用机制
舒芬太尼ICU镇痛镇静用药流程
①镇痛评估
对于创伤性(手术、 烧伤、骨科等)ICU 机械通气患者
首剂缓慢推注5ml(0.2μg/kg),观察患 者反应,持续静脉输注0.1μg/(kg· h)
舒芬太尼(1ml:50μg/kg)1支加生 理盐水至50ml(浓度为1μg/ml)
若CPOT>2 或BPS>4时 以0.05μg/(kg· h)的速 率增加舒芬的用量
1ห้องสมุดไป่ตู้2
3-6 0.1 -
常用阿片类药物-药代动力学
吗啡
血浆蛋白结合 率(%) a1-酸性蛋白 结合率(%) 辛醇/水比率 (%) 分布容积 (L/kg)
芬太尼 84 44 810
舒芬太尼 93 84 1750
瑞捷® 70-92 70 17.9(pH=7.4)
30 1.4
3.2-3.7
4.1
2.9
0.35
芬太尼
肝脏
舒芬太尼
肝脏(去甲舒芬太 尼,1/10)
瑞捷®
血浆酯酶 (RBC和组织 细胞)
多在肾脏、710%胆道
肾脏 13.3 240 260
易于胃壁和肺储存, 90min后第二次血峰
肾脏、胆汁,原 形从尿排泄1-2%
肾脏 2800 5-10 3-5 很少
120-180 -
12.7 160 30 少
舒芬太尼半衰期曲线
●作用时间长
● 蛋白结合率高 ●其代谢产物—去甲舒芬太尼有较强的镇痛作用,为舒芬太尼的1/10,与芬太尼相当
舒芬太尼的药理学特点
●呼吸影响小
● 对μ1受体具有高度选择性,对δ 和μ2受体的亲合力为μ1受体的1/100
●消除半衰期较芬太尼短,消除快
●时量相关半衰期仅为芬太尼的1/7 → 蓄积的危险性低
舒芬太尼的药理学特点---药代动力学
● 分布容积 (L/kg) 表观分布容积(apparent volume of distribution, Vd)是指体内药物总量待平衡后, 按测得的血浆药物浓度计算时所需的体液总容积。Vd可用L/kg体重表示 Vd是反映药物分布的广泛程度或与组织中大分子的结合程度 Vd越小,药物排泄越快,在体内存留时间越短;分布容积越大,药物排泄越慢, 在体内存留时间越长 舒芬太尼的分布容积 (L/kg) 低于芬太尼(2.9 vs 4.1) ● 时量相关半衰期 静脉恒速输注药物一段时间停药后,中央室药物浓度下降50%所需的时间 舒芬太尼时量相关半衰期仅为芬太尼的1/7
①全身肌肉强直,但发生率低于等效剂量的芬太尼和阿芬太尼 ②肌肉紧张性震挛 ③呼吸抑制,大多为一过性,与剂量有关,能够被纳洛酮迅速有效拮抗 ④大剂量静脉应用可导致心动过缓和低血压
⑤麻醉恢复期常常发生恶心呕吐
⑥ 椎管内应用时最常见的副作用是恶心、瘙痒、头晕,偶尔有尿潴留发生
舒芬太尼的临床应用安全
◆舒芬太尼临床应用的人群选择(药理特点决定)
– 成瘾性
常用阿片类药物-药效动力学
吗啡
作用部位 起效时间 (min) 最大效应时间 (min) 持续时间 (min) 等效剂量 治疗窗 (LD50/ED50)
芬太尼 µ 2-3
舒芬太尼 µ 1.3-3
瑞捷® µ 1
µ ,κ 20 3-4h 10 70-90
5-8
25-30 0.1 277
3-5
25-50 0.01 25211
舒芬太尼的临床应用—ICU镇痛
◆可用于ICU术后插管病人的镇静治疗
●静脉使用推荐剂量:0.2-1.0 g/kg/h ●适量复合应用咪唑安定
舒芬太尼的临床应用安全
◆与吗啡和芬太尼比较:相对安全
●受体选择性更强 ●等效剂量小 ●消除半衰期更短 ●药物储存更少
舒芬太尼的临床应用安全的再评估
◆舒芬太尼具有一般阿片类药物相似的副作用
阿片类药物的临床应用史
◆我们应对芬太尼家族进行再认识!
●芬太尼的唯一优势:价格 ●瑞芬太尼: ①短小手术;②肝肾功能不全手术;③老年病人手术 ● 舒芬太尼: ①中长时间手术;②分娩镇痛;③术后镇痛; ④ICU气管插管病人的镇静和镇痛
芬太尼家族的特点
• 起效时间
– 量、强度、用药方式 – 起效-血脑平衡时间:瑞芬太尼1min;阿芬太尼 1min;芬太尼6.6min;舒芬太尼6.2min。 • 副作用 – 呼吸抑制 – 骨骼肌强直 – 恶心、呕吐、便秘
●安全范围大!治疗指数(LD50/ED50) 显著高于芬太尼( 25000 vs 270)
●抑制诱导插管时的刺激反应和机体应激反应的作用强于芬太尼抑制
舒芬太尼的药理学特点
◆药效学
●循环系统:最稳定;对心肌抑制作用轻,不引起组胺释放 ●对呼吸影响:①与芬太尼相比呼吸抑制少而短; ②抑制呼吸的时间比镇痛时间短 ●恶心、呕吐、瘙痒等不良反应比芬太尼更少
舒芬太尼 血液动力学稳定性更好
血 压
17 16 15 14 13 12 11 10 9 8 入室 用药后 1min 15min 30min
SBP SBP DBP DBP MAP MAP
fen suf fen suf fen suf
105 100 95 90 85 80 75
HR F HR S
舒芬太尼组对 气管插管时血 流动力学的影 响较芬太尼组 稳定
每10min进行一次镇痛评分(Behavioral Pain Scal,BPS评分方法或Critical-Care Pain Observation Tool,CPOT重症监护疼 痛观察工具) 当CPOT≤2或BPS≤4时,进行SAS 评分
静 痛
镇 镇
ICU镇痛药物
ICU理想的镇痛药物
ICU临床用药特点
需多种药物和手段合并使用,应注 意药物相互作用 需随时调整药物种类和剂量 患者药代/药效动力学不稳定 患者镇痛镇静药物累积量大 镇痛强度高 易调控 安全性高 不良反应少 代谢产物蓄积少
