【2014合肥三模】安徽省合肥市2014届高三第三次教学质量检测化学试题 扫描版含答案
14届高三第三次联考化学(附答案)

安徽省安庆市六校2014届高三第三次联考化学试题7.化学与生产、生活密切相关。
下列说法正确的是A.大型制冷设备的液氨大量泄露不会对操作人员有损害B.铅蓄电池、锂电池、碱性锌锰电池都属于二次电池C.明矾和漂白粉常用于自来水的净化,两者的作用原理完全相同D.医疗上常用硫酸钡作为“钡餐”8.对于实验I〜IV的描述正确的是A.实验I :逐滴滴加稀盐酸时,试管中立即产生大量气泡B.实验II:充分振荡后静置,下层溶液为橙红色,上层无色C.实验III:从饱和食盐水中提取NaCl晶体D.装置IV:酸性KMnO4溶液中有气泡出现,且溶液颜色逐渐变浅乃至褪去9.常温下,下列各组离子在指定溶液中一定能大量共存的是( ) A.1.0 mol·L–1的KNO3溶液:H+、Fe2+、Cl-、SO42-B.甲基橙呈红色的溶液:NH4+、Ba2+、AlO2-、Cl-C.c(H+)=10–12 mol·L–1的溶液:K+、Ba2+、Cl-、Br-D.加入苯酚显紫色的溶液:K+、NH4+、Cl-、I-10.用N A表示阿伏加德罗常数的值。
下列叙述正确的是A.25°C时,1L pH=12的Ba(OH)2溶液中含有的OH-数目为0.02N A B.室温下,14.0g乙烯和丁烯的混合气体中含有的C-H键数目为2.0N A C.0.1mol Fe在0.1mol Cl2中充分燃烧,转移的电子数为0.3N AD.标准状况下,22.4LCCl4中含有的分子数目为N A11.N2O5是一种新型硝化剂,在一定温度下可发生以下反应:2N2O5(g) 4NO2 (g)+ O2(g) ΔH > 0T1温度时,向密闭容器中通入N2O5,部分实验数据见下表:下列说法中不正确...的是A.T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1<K2 B.500 s内N2O5分解速率为2.96╳10-3mol·L-1·s-1C.T1温度下的平衡常数为K1=125,平衡时N2O5的转化率为50%D.达平衡后其他条件不变,将容器的体积压缩到原来的1/2,则c(N2O5)> 5.00 mol·L-1 12.空间实验室“天宫一号”的供电系统中有再生氢氧燃料电池(RFC),RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充放电池。
安徽省淮南二中2014届高三下学期第三次模拟考试化学试题 Word版含答案.pdf

安徽省淮南二中2014届高三下学期第三次模拟考试理科综合化学试题 可能用到的相对原子质量:H 1 B 11 C 12 N 14 O 16 Na 23 S 32 Fe 56 第Ⅰ卷 7.已知过氧化铬CrO5)的结构式过氧化铬不稳定,溶于水生成过氧铬酸溶于酸生成铬(III)盐(绿色)并放出氧气,4CrO5+12H+=4Cr3++7O2+6H2O)。
下列有关说法正确的是( ) A. CrO5Cr元素的化合价为+10 B.过氧化铬C.过氧化铬 D.设NA为阿伏加德罗常数的值。
下列叙述正确的是A. NA B.CnH2n的链烃中含有的碳碳双键的数目一定为NA/n C.+数目为10-7NA D.NA 9.下列离子或分子组能大量共存,且满足相应要求的是( ) A.Na+、K+、Ag+、NO3— 要求:逐滴滴加氨水先有沉淀产生,后沉淀消失 B.Fe3+、NO3—、I—、HCO3— 要求:逐滴滴加盐酸立即有气体产生 C.K+、AlO2—、Cl—、MnO4— 要求:无色澄清溶液 D.NH4+、Al3+、SO42—、CH3COOH 要求:逐滴滴加NaOH溶液立刻有气体产生 10.下列实验现象对应的结论正确的是( ) ①气密性检查 ②气体性质检验 ③化学平衡的探究 ④喷泉实验 选项现象结论A①导管口冒气泡,手松开无现象装置的气密性良好B②中KMnO4溶液紫红色褪去SO2具有漂白性C③中关闭活塞K,气体颜色在热水中比在冷水中深NO2生成N2O4为吸热反应D④中烧瓶中形成喷泉Cl2易溶于CCl411.在新能领域中,氢能已经普遍被认为是一种最理想的新世纪无污染的绿色能21世纪是氢能的世纪电解尿素[ CO(NH2)2]的碱性溶液制氢的装置示意图如图(电解池中隔膜仅阻止气体通过,a、b极均为惰性电极)。
下列说法正确的是 A.电解时,b极是阴极放出H2,发生氧化反应 B.溶液中OH—逐渐向b极移动 C.解时,a极的电极反应式为: D.若在b极产生标况下224mL,则消耗尿素2g在体积为2 L的恒容密闭容器中发生反应xA(g)+yB(g)zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始的变化关系。
安徽省合肥市高三理综(化学部分)第三次教学质量检测试
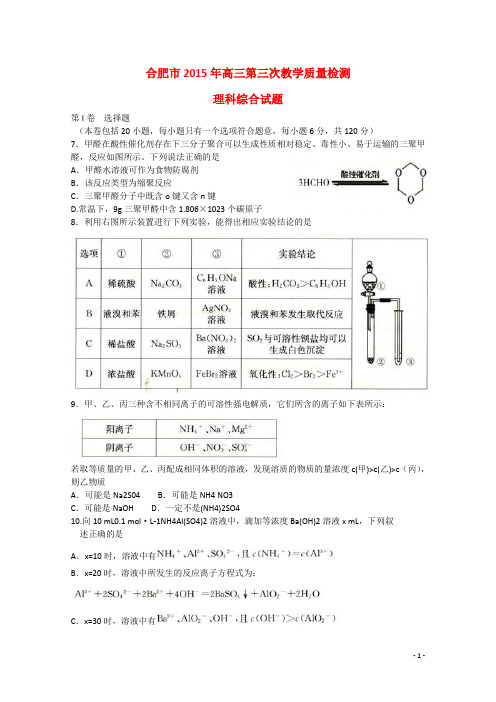
合肥市2015年高三第三次教学质量检测理科综合试题第I卷选择题(本卷包括20小题,每小题只有一个选项符合题意,每小题6分,共120分)7.甲醛在酸性催化剂存在下三分子聚合可以生成性质相对稳定、毒性小、易于运输的三聚甲醛,反应如图所示。
下列说法正确的是A.甲醛水溶液可作为食物防腐剂B.该反应类型为缩聚反应C.三聚甲醛分子中既含о键又含п键D.常温下,9g三聚甲醛中含1.806×1023个碳原子8.利用右图所示装置进行下列实验,能得出相应实验结论的是9.甲、乙、丙三种含不相同离子的可溶性强电解质,它们所含的离子如下表所示:若取等质量的甲、乙、丙配成相同体积的溶液,发现溶质的物质的量浓度c(甲)>c(乙)>c(丙),则乙物质A.可能是Na2S04 B.可能是NH4 NO3C.可能是NaOH D.一定不是(NH4)2SO410.向10 mL0.1 mol·L-1NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液x mL,下列叙述正确的是A.x=10时,溶液中有B.x=20时,溶液中所发生的反应离子方程式为:C.x=30时,溶液中有D.滴加过程中,生成沉淀的最大物质的量为0. 003 mol11.将KO2放人密闭的真空容器中,一定条件下,发生反应:达到平衡后,保持温度不变,缩小容器体积,重新达到平衡。
下列说法正确的是A.容器内压强增大B.KO2的量保持不变C.平衡常数减小D.氧气浓度不变12.如图所示,甲池的总反应式为。
下列说法正确的是A.甲池中负极上的电极反应式为B.乙池中石墨电极上发生的反应为C.甲池溶液pH增大,乙池溶液pH减小D.甲池中每消耗0. 1mol N2H4乙池电极上则会析出6.4g固体13.已知NaHC2O4溶液显弱酸性,向100 mL0.1 mol·L-1的NaHC2O4。
溶液中分别加入下列物质,有关说法正确的是A.加入少量H2 C2O4固体,促进水电离,溶液中c(H+)增大B.加入NaOH溶液至恰好完全反应,则溶液中:C.加入氨水至中性,则溶液中:D.加入0. 01 mol Na2 C2O4固体,则溶液中:25.(15分)已知前四周期五种元素X、Y、Z、W、T,它们的原子序数依次增大。
【2014合肥三模】安徽省合肥市2014届高三第三次教学质量检测化学试题 Word版含答案

安徽省合肥市2014届高三第三次教学质量检测理科综合能力化学试题(考试时间:150分钟满分:300分)注意事项:1.答题前,务必在答题卡和答题卷规定的地方填写自己的姓名、准考证号和座位号后两位。
2.答第I卷时,每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。
3.答第Ⅱ卷时,必须使用0.5毫米的黑色墨水签字笔在答题卷上书写,要求字体工整、笔迹清晰。
作图题可先用铅笔在答题卷规定的位置绘出,确认后再用0.5毫米的黑色墨水签字笔描清楚。
必须在题号所指示的答题区域作答,超出答题区域书写的答案无效,在试题卷、草稿纸上答题无效。
4.考试结束,务必将答题卡和答题卷一并上交。
可能用到的相对原子质量:H:l C:12 O:16 Mg:24 P:31 S:32 Cl:35.5第I卷选择题(本卷包括20小题,每小题只有一个选项符合题意,每小题6分,共120分)7.三硫化四磷用于制造火柴及火柴盒摩擦面,分子结构如下图所示。
下列有关三硫化四磷说法中正确的是A.该物质中磷元素的化合价为+3B.该物质分子中含有σ键和π键C.该物质的熔、沸点比食盐高D.该物质22g含硫原子的数目约为1.806×10238.常温下,下列离子或分子在指定溶液中能大量共存的一组是A.FeCl3饱和溶液:K+、I一、C l-、H+B.使紫色石蕊试液变蓝色的溶液:Na+、NO3-、Br一、NH3.H2OC.pH=l的溶液:Cr2O72-、K+、NO3-、C2H5OHD.能溶解Al2O3的溶液:Na+、Mg2+、HCO3-、C l-9.利用下列图表中的实验装置和试剂,能得出正确实验结论的是10.下列现象或事实可用同一原理解释的是A氯化铵晶体和碘晶体加热都产生气体B.明矾和液氯都可用于处理生活用水C.漂白粉和过氧化钠都可用于漂白有色织物D.常温下,铁和铜分别放在浓硫酸中都无明显现象11.-定条件下,在体积为VL的密闭容器中发生如下反应:一段时间后达到化学平衡状态。
安徽省2014届高考化学模拟试卷一新人教版

绝密★启用前安徽省2014届高三高考模拟化学试卷考试时间:100分钟;须知事项:1.答题前填写好自己的姓名、班级、考号等信息2.请将答案正确填写在答题卡上第I卷〔选择题〕请点击修改第I卷的文字说明一、选择题〔题型注释〕1.信息、材料、能源被称为新科技革命的“三大支柱〞。
如下观点或做法错误的答案是A.在即将到来的新能源时代,核能、太阳能、氢能将成为主要能源B.加大煤炭的开采速度,增加煤炭燃料的供给量,以缓解石油危机C.光缆在信息产业中有广泛应用,制造光缆的主要材料是二氧化硅D.高温结构陶瓷氮化硅〔Si3N4〕具有较高的硬度和耐磨性,可用于制造汽车发动机2.如下各组离子中,在给定条件下能够大量共存的是( )A.通入足量CO2后的溶液中:Na+、SiO32-、CH3COO-、CO32-B.无色溶液中:Mg2+、MnO4-、SO42-、K+C.c(H+)/c(OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl-D.c(ClO-)= 1.0 mol/L的溶液:Na+、SO32-、S2-、SO42-3.用如下实验别离装置进展相应实验,能达到实验目的的是〔〕A.用图Ⅰ所示装置除去CO2中含有的少量HClB.用图Ⅱ所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体C.用图Ⅲ所示装置别离NaCl和Na2SO4的混合溶液D.用图Ⅳ所示装置别离CCl4萃取碘水后已分层的有机层和水层4.如下表示正确的答案是A.由于Ksp(BaSO4)= 1.1 ×10-10 小于Ksp(BaCO3)= 5.1 ×10-9,如此不能使BaSO4沉淀转化为BaCO3沉淀B.在中和热测定的实验中,将NaOH溶液和盐酸混合反响后的最高温度作为末温度C.除去CH3COOC2H5中的CH3COOH先加足量的饱和Na2CO3溶液再蒸馏D.能使湿润的KI淀粉试纸变蓝的气体一定是Cl25.如下表格中的各种情况,可以用下面的图象曲线表示的是反响纵坐标甲乙A 等质量钾、钠分别与足量水反响H 2质量钠钾B 一样质量氨气,在同一容器中2NH3N2+3H2 ΔH >0 氨气的转化率500℃400℃C 在体积可变的恒压容器中,体积比1:3的N2、H2,N2+3H22NH3氨气的浓度活性一般的催化剂活性高的催化剂D 2molSO2与lmolO2,在一样温度下2SO2(g)+O2(g)2SO3(g) SO3物质的量2个大气压10个大气压6.如下有关原子结构与元素周期律的表示正确的答案是A.P、S、Cl的最高价含氧酸的酸性依次增强B.第ⅠA族元素铯的同位素137Cs比133Cs多4个质子C.第二周期元素从左到右,最高正价从+1递增到+7D.元素周期表位于金属与非金属分界限附近的元素属于过渡元素7.化学美无处不在,如下图是物质间发生化学反响的颜色变化,其中X是A.稀盐酸 B.Na2SO4溶液 C.稀硫酸 D.Na2CO3溶液第II卷〔非选择题〕请点击修改第II卷的文字说明8.A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料。
2014届高三第三次大联考(新课标卷)

2014届高三第三次大联考(全国新课标卷)理科综合能力测试相对原子质量:H 1 C 12 O 16 Na 237.化学无处不在,下列用品的有效成分及用途对应错误..的是() A.食盐既可以做调味剂,又可以做防腐剂B.纯碱既可以做清洗品,又可以做发酵粉C.漂白粉既可以做消毒剂,又可以做漂白剂D.酒精既可以做饮料,又可以做燃料8.某醇烯酸是合成香精的主要原料,其结构简式为:COOH OH下列有关某醇烯酸的叙述正确的是A.该醇烯酸的分子式为C7H8O3B.既可以通过加聚反应形成高分子,也可以通过缩聚反应形成高分子C.不能使酸性高锰酸钾溶液褪色D.分子内形成六元环的酯9.X、Y、Z、W的原子序数依次增大的短周期元素,其含氧酸根离子不能破坏水的电离平衡的是A.XO2-3B.YO-2C.ZO2-4D.WO—10.锂离子电池已经成为应用最广泛的可充电电池。
某种锂离子电池的结构示意图如下图所示,其中两极区间的隔膜只允许Li+通过。
电池充电时的总反应方程式为:LiCoO2==Li1-x CoO2+x Li。
关于该电池的推论错误的是()A.放电时,Li+主要从负极区通过隔膜移向正极区B.放电时,负极反应为x Li-x e-===x Li+C.电解质溶液不能是水溶液D.充电时,负极(C)上锂元素被氧化11.已知某苯的同系物C8H10,苯环上有两个侧链,其一氯取代物的种数是A.10 B.9 C.6 D.512.相同温度下,将足量氯化银固体分别放入:①50mL蒸馏水②40mL 0.1 mol·L-1盐酸③20mL 0.1 mol·L-1氯化镁溶液④30mL0.1 mol·L-1硝酸银溶液中,Ag+浓度:A.①>④=②>③B.④>①>②>③C.④=②>①>③D.①>④>②③13.用下列实验装置进行相应实验,能达到实验目的的是()。
26.(14分)雾霾含有大量的污染物SO 2、NO 。
合肥一中2013-2014高三年级段三考试

合肥一中2013-2014学年度高三年级12月份段考化学试卷相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Mg-24 Mn-55第I卷选择题(共50分)一、选择题(本题包括10小题,每小题2分,共20分。
每小题只有一个选项符合题意)1.化学与生产、生活及材料关系密切,下列说法正确的是()A.家庭燃气泄漏应开窗通风以避免发生爆炸B.低碳生活是一种时尚的生活理念,倡导减少CO2、CH4等常见的温室气体的排放C.明矾在水中生成Al(OH)3胶体,因此明矾厂用作净水剂和杀菌剂D.如果发生了氨气泄漏,可以用湿毛巾或蘸有食用醋的毛巾捂住口鼻撤离2.下列关于化学用语的理解正确的是()H Cl OA.HClO的电子式:B.碳酸氢钠溶液显碱性的原因:HCO3- + H2O −−→←−−H3O+ + CO32-C. 比例模型表示CH4分子或CCl4分子D.基态硫离子的核外电子排布式为:1s22s22p63s23p63. 类比类推是重要的学科思想,下列根据已知所进行的类比类推正确的是()A.根据(NH4)2CO3受热分解产生NH3,可推知所有铵盐受热分解一定产生NH3 B.根据主族元素最高正价与主族序数的关系,可推知卤族元素最高正价都是+7C.根据Na、K具有强还原性,钠在空气中加热生成Na2O2,可推知K再空气中加热产物更为复杂D.根据氢氧化铁溶于盐酸生成氯化铁和水,可推知氢氧化铁溶于氢碘酸生成水和碘化铁4. 设N A为阿佛加德罗常数的数值。
下列叙述正确的是()A.1L 0.1mol/L的Na2CO3溶液中,阴离子的数目小于0.1N AB.常温常压下,6.4g 氧气和抽样的混合气体中含氧原子总数为0.4 N AC.5.6g铁粉与一定量的稀硝酸完全反应,转移的电子数一定为0.3 N AD.在反应KIO3+6HI===3I2+KI+3H2O中,每生成3mol I2转移电子数为6 N A 5. 化学是以实验为基础的学科,下列各图示实验不合理的是()A.图1为证明非金属性强弱:S>C>SiB.图2为在铁制品表面镀铜C.图3可用于吸收氯化氢、溴化氢等气体D.图4为制备并收集少量NO2气体6.室温下,下列各组离子在指定的溶液中能大量共存的是()A.浓氨水中:NO3-、I-、Na+、Al3+B.室温下,pH =13的溶液中:Na+、K+、SiO32-、Cl-C.1.0mol·L-1的KNO3溶液:H+、Fe2+、Cl-、SO42-D.室温下,c(OH-)=1.0×10-1CH3mol/L 溶液中:CH3COO-、K+、SO42-、Br-7.下列离子方程式正确的是( )A.铜溶于稀硝酸中:Cu+4H++2NO3-Cu2++NO2B.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰使SO42-沉淀完全:Al3++2Ba2++2SO42-+4OH-2BaSO4↓+AlO2-+2H2OC.向碳酸钠溶液中逐滴加入与之等体积等物质的量浓度的稀醋酸:CO32-+CH3COOH CH3COO-+HCO3-D.硫酸氢铵溶液中滴加少量NaOH溶液:H++NH4++2OH-NH3.H20+H2O8.几种短周期元素的原子半径及主要化合物见下表:A.K、M两元素最高价氧化物对应的水化物不能发生化学反应B.在RCl2中,各原子最外层均满足8电子稳定结构C.K单质在T单质中燃烧所形成的化合物含有非极性共价键和离子键D.Q元素的最高价氧化物为电解质,其水溶液能够导电9. 意大利罗马大学的Funvio Cacace等人获得了极具理论研究意义的N4分子。
2014三模化学试题及答案(人教版)

2014年九年级三模考试化学试卷一.选择题:(16分)11.“烧不坏的手绢”是一个趣味实验,下列实验过程中主要发生化学变化的是:A.酒精和水形成混合液B.手绢浸入混合液中C.手绢上的酒精燃烧了D.手绢表面的水蒸发12.为了经久耐用,在灯泡中可填充的气体是:A.氧气 B.氮气 C.二氧化碳 D.二氧化硫13.下列肥料属于复合肥料的是:A.硫酸钾(K2SO4) B.碳酸氧铵(NH4HCO3) C.尿素[CO(NH2)2] D.磷酸二氧铵(NH4H2PO4)14.用打气筒将空气压入自行车胎内,主要是因为:A.气体分子很小 B.气体分子间距离较大 C.气体分子可分 D.气体分子在不断运动15.次氯酸钙[Ca(ClO)2]能起杀菌、消毒作用,其中钙元素的化合价为+2,氧元素的化合价为-2,则氯元素的化合价是:A.+l B.+3 C.+5 D.+716..为防止实验室意外事故的发生,下列预处理方法中错误..的是:17.在水中能大量共存的一组离子是:A.Ba2+、SO42-、K+ B.NH4+、Na+、OH-C.Na+、C1-、NO3-D.Cu2+、C1-、OH-则该草鱼能提供人类生命活动必需的营养素有:A.六大类B.五大类C.四大类D.三大类19.t℃时,有一杯接近饱和的硝酸钾溶液,下列做法一定不能使其变为饱和溶液的是:A.恒温蒸发溶剂B.降低溶液的温度C.向溶液中加入硝酸钾D.向溶液中加入t℃时硝酸钾的饱和溶液A 除去粗盐中的泥沙氯化钠和泥沙的溶解性不同B 将石油分馏得到石油产品石油中各成分的密度不同C 分离硝酸钾和氯化钠组成的混合物硝酸钾和氯化钠分解温度不同D 分离液态空气制取氧气利用氮气和氧气的熔点不同21.下列转化能一步完成的是:①CH4→CO2② HNO3→HCl ③ CaO→Ca(OH)2④ Ba(OH)2→NaOH ⑤ C→CuA. ①③④⑤B. ②③④⑤C.①②④⑤D.①②③④22.相同质量的Mg、Fe分别与稀盐酸作用,产生H2的质量m(H2)与加入稀盐酸的体积V(稀盐酸)关系如下图所示,其中正确的是:D二.填空题(每空1分,17分)34.(4分)请写出相应的化学符号或名称①2个磷原子;②+2价的锌元素;③2SO42-;④2 H2O 。
2014届合肥三模文科综合答案

合肥市2014年高三第三次教学质量检测文科综合试题参考答案及评分标准第Ⅰ卷(共132分,每小题4分)题号1234567891011答案B A C B C C B B C A D 题号1213141516171819202122答案C B A C B B B A D B C 题号2324252627282930313233答案C C B B D A A B B A D第Ⅱ卷(共168分)34.(共30分)(1)空气质量较好的城市主要分布在南方地区;集中分布在沿海地区㊁高原地区㊂(5分)空气质量较差的城市主要分布在北方地区;集中分布在华北地区㊁河谷地区㊂(5分)(2)舟山地处沿海地区,降水量较多,利于净化大气;风力较大,空气流动性好,利于大气中污染物的扩散;重污染企业较少㊂(5分)拉萨地处高原,城市规模较小,人口较少;工业发展较为落后,(或 第三产业比重较高 )污染物排放量少㊂(5分)(3)将污染大气的企业外迁;大气污染企业避开盛行风上风向(或 位于盛行风的下风向 ,或 位于与盛行风向垂直的郊外 ,或 位于最小风频的上风向 );城市规划保留入城的 通风口 ,便于污染物扩散;增加城市绿地面积,净化空气;在工业区和居住区之间建立卫生防护带㊂(每小点2分,满分10分)35.(共26分)(1)流量:裕溪河流量较杭埠河大,因为巢湖汇集上游水系(包括杭埠河)的大量来水,故径流量更大㊂高三文科综合试题答案㊀第1页(共4页)高三文科综合试题答案㊀第2页(共4页)水位变化:裕溪河水位(季节和年际)变化较杭埠河小,因为巢湖对裕溪河的径流具有调节(或 削峰补枯 )作用㊂流速:裕溪河流速较杭埠河小,因为裕溪河位于巢湖下游,落差较小,流速较慢,而杭埠河发源于大别山,落差较大,流速较快㊂含沙量:裕溪河含沙量较杭埠河小,因为巢湖支流进入巢湖,流速减慢,部分泥沙沉积㊂(任意答出3点即可,每点4分)或用表格回答裕溪河㊁杭埠河水文状况比较水文特征裕溪河杭埠河差异原因差异原因流㊀量较大汇集了上游来水较小流域面积较小水位(季节㊁年际)变化较小已经过巢湖调节较大未经过巢湖调节流㊀速较慢(下游)落差较小较快(上游)落差较大含沙量较小上游来的泥沙部分已在巢湖沉积较大落差较大,沉积作用不显著㊀㊀(列出 水文特征 中任意3项即可,每项4分㊂如用文字和列表两种方式回答,按前一种回答方式赋分)(2)风向变化规律:(6分)甲地白天盛行偏西风,夜晚盛行偏东风㊂7月风频变化最大的原因:(8分,任答2点即可)原因①:7月处于丰水期,湖面更宽广,湖水更深,湖陆热力性质差异更大㊂原因②:7月中下旬受副高控制,以晴朗天气为主,陆地昼夜温差更大,湖陆风更明显㊂原因③:7月中下旬大气环流整体以下沉气流为主,冬夏季风和锋面系统等对风向影响小㊂(其他回答,言之有理可酌情赋分)36.(共26分)(1)国家律令的监督和执行;纠察㊁弹劾不法官吏;维护封建礼仪㊂(6分)(2)实行三省六部制;建立谏诤制度;推行科举制度;提倡道德自律㊂(8分)(3)制度建设:建立中国共产党领导下的多党合作和政治协商制度;确立人民代表大会制度;实行民族区域自治制度;推行 村民自治制度 ,扩大基层民主㊂意义:有利于加强执政党的自身建设;有利于加强人民的监督;有利于完善社会主义民主与法制㊂(12分)37.(共30分)(1)社会状况:托拉斯成为美国普遍而典型的垄断组织形式,成为人们的议论焦点,政府一度实行遏制政策㊂(6分)势盛的原因:第二次工业革命使企业生产规模扩大,资本和生产不断集中;垄断组织有利于生产效率和管理水平的提高;资产阶级为追求利润,控制价格和市场㊂(9分)(2)现象:全球化时各国利益休戚相关;全球化造成利益分配不均;缺乏公正性的全球化难以为继㊂(6分)原因:商品㊁劳务㊁技术㊁资金在全球范围内流动和配置,使各国经济相互依赖㊁相互联系趋势更加密切;经济全球化是由发达国家主导的,其本质是资本在全球范围内的新一轮扩张;发展中国家在经济全球化过程中处于劣势和被动地位㊂(9分)38.(共28分)(1)①社会主义市场经济既具有市场经济的共性,又具有自己鲜明的特征,既可以发挥市场经济的长处,又可以发挥社会主义制度的优越性㊂(2分)②社会主义市场经济以共同富裕为根本目标㊂国家在促进经济发展的同时,注重民生的改善,提高人们的收入,逐步促进共同富裕目标的实现㊂(3分)③国家能够实行强有力的宏观调控㊂制定经济发展规划目标是国家运用经济手段加强宏观调控的重要体现,在社会主义市场经济条件下,国家能够集中人力㊁物力㊁财力办大事,能够把人民的当前利益与长远利益㊁局部利益与整体利益结合起来,并能够正确处理好政府与市场的关系,更加尊重市场规律,更好发挥政府作用㊂上述目标的实现充分说明了这一点㊂(3分)(2)生活与哲学:①任何事物都包含对立统一的两个方面,同一性和斗争性是矛盾的两个基本属性㊂(2分)②在国家财力一定的情况下,经济发展与民生改善存在着此消彼长的关系㊂这是矛盾斗争性的体现;(2分)③发展经济与改善民生是相互影响㊁相互促进的㊂发展经济为改善民生提供物质基础和保障;改善民生是发展经济的最终目的,并有利于扩大内需,促进经济平稳较快发展和经济发展方式的转变㊂这是矛盾同一性的体现㊂(2分)④矛盾双方既对立又统一,由此推动事物的运动变化和发展㊂要坚持一分为二的观点,全高三文科综合试题答案㊀第3页(共4页)面地看问题,在发展经济的同时,更加注重保障和改善民生,实现经济社会协调发展㊂(2分)政治生活:①政府要科学㊁民主决策,综合考虑经济发展形势㊁促进就业㊁改善民生等相关因素,科学确定经济发展目标㊂(3分)②政府应切实履行有效管理社会㊁提供优质公共服务的职能㊂在全面履行职能的同时,努力建设服务型政府,真正提高政府为经济社会发展服务㊁为人民服务的能力和水平㊂(3分)③政府及其工作人员在实际工作中要贯彻落实科学发展观,努力促进社会和谐,做到经济与社会协调发展㊂(3分)④政府及其工作人员要坚持对人民负责的原则,坚持权为民所用㊁情为民所系㊁利为民所谋,切实把改善民生作为发展经济的最终目的㊂(3分)39.(共28分)(1)①统筹城乡发展,以城带乡,各方面优势互补㊁良性互动,是贯彻落实科学发展观,促进经济发展方式转变的要求㊂(2分)②公有制为主体㊁多种所有制共同发展是我国的基本经济制度,形成上述文化产业格局,有利于解放和发展文化生产力㊂(2分)③统一开放㊁竞争有序的市场体系是市场合理配置资源的前提条件,形成上述文化市场格局有利于优化资源配置,激活文化发展的活力㊂(2分)④适应经济全球化和入世的新形势,必须坚持全面对外开放,形成上述文化开放格局,有利于充分利用国际国内两个市场㊁两种资源,加快我省文化发展㊂(2分)(2)①完善村级公共文化服务设施,提升农村基本公共文化服务水平,有利于大力发展公益性文化事业,保障村民的基本文化权益㊂(3分)②将相关文化遗存保护利用起来,不仅有利于展示文化多样性,也有利于促进和保护文化财富㊂(3分)③积极挖掘㊁传承和弘扬乡村特色文化和民间民俗文化,有利于继承和弘扬优秀传统文化㊂(3分)④文化对人的影响来自特定的文化环境和各种形式的文化活动㊂大力开展形式多样的文化活动,有利于营造良好的文化氛围,让群众在潜移默化中接受先进文化的熏陶㊂丰富精神世界,增强精神力量,促进全面发展㊂(3分)(3)①辨证法的发展观㊁革命批判精神和辨证否定观,要求我们要树立创新意识,坚持实践创新和理论创新㊂(2分)②创新能够促进社会生产力的发展㊂(2分)③创新能够促进生产关系和社会制度的变革㊂(2分)④创新能够促进人类思维和文化的发展㊂(2分)高三文科综合试题答案㊀第4页(共4页)。
合肥市2014年高三第三次教学质量检测试卷及答案

合肥市2014年高三第三次教学质量检测英语试题(考试时间:120分钟满分:150分)第I卷(三部分,共115分)第一部分:听力(共两节, 满分30分)第一节(共5小题; 每小题1. 5分, 满分7. 5分)听下面5段对话。
每段对话后有一个小题,从题中所给的A、B、C三个选项中选出最佳选项, 并标在答题卷的相应位置。
用答题卡的考生, 先把选出的最佳选项标在试卷的相应位置, 再转涂到答题卡上。
听完每段对话后, 你都有10秒钟的时间来回答有关小题和阅读下一小题。
每段对话仅读一遍。
1. How is the man going to Chicago?A. By bus.B. By train.C. By air.2. What do we know about the woman?A. She is excited.B. She is crazy.C. She feels stressed3. What's the woman worried about?A. The man's study.B. The man's efforts.C. The man's job.4. What is the boy's attitude towards taking a piano class?A. He is eager to take itB. He is unwilling to take it.C. He is hesitant to take it.5. Where does the conservation most probably take place?A. In a hotel.B. In a store.C. In a bank.第二节(共15小题,每小题1. 5分,满分22. 5分)听下面5段对话或独白。
每段对话或独白后有几个小题,从题中所给的A、B、C三个选项中选出最佳选项,并标在答题卷的相应位置。
高考化学复习安徽省合肥市高三第三次教学质量检测理综化学试题(解析版).docx

高中化学学习材料唐玲出品7.毒品可卡因又称古柯碱(分子结构如下图所示),是一种具有局部麻醉作用的天然生物碱,因其毒性大且易成瘾,现已被其他麻药所替代。
下面有关叙述正确的是A.古柯碱是高分子化合物B.古柯碱分子结构中不存在非极性键C.古柯碱难溶于水和盐酸D.0. 01mol古柯碱分子中含甲基约1.204×1022个8.下列离子在溶液中能大量共存,通入SO2气体后仍能大量共存的一组是A.NH4+、I-、Cl-、Ca2+ B.K+、Na+、ClO-、SO42-C.Fe3+、Na+、Cl-、SCN- D.K+、Al3+、NO3-、AlO2-9.下列实验能够达到预期目的的是A.①可用于表示:0.1mol·L-1的NaOH溶液滴定盐酸的滴定曲线B.②可用于证明:氧化性 Cl2>Br2>I2C.③可用于证明:K sp(AgCl)>K sp(AgBr)>K sp(Ag2S)D.④可用于证明:非金属性 Cl>C>Si10.汽车尾气净化中的一个反应如下:2NO(g)+2CO(g)N2(g)+2CO2(g) △H=-373.4kJ/mol 反应达到平衡后,改变某一个条件,下列示意图曲线①〜⑧中正确的是A.①⑥⑧B.①⑤⑦C.②③④D.③⑥⑦11.工业品氢氧化钾溶液中含有某些含氧酸根杂质,可用离子交换膜法电解提纯。
电解槽内装有阳离子交换膜(只允许阳离子通过),其工作原理如右图所示。
下列说法不正确的是A.阴极材料可以是Fe,含氧酸根杂质不参与电极上放电B.该电解槽的阳极反应式为:4OH―― 4e-== 2H2O+O2↑C.通电后,该电解槽阴极附近溶液pH会减小D.除去杂质后氢氧化钾溶液从出口B导出【答案】C【解析】12.已知磷酸分子结构中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换。
又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不能跟D2O发生氢交换。
安徽省2014届高三高考模拟化学试卷三 Word版含答案
绝密★启用前安徽省2014届高三高考模拟化学试题三1.答题前填写好自己的姓名、班级、考号等信息2.请将答案正确填写在答题卡上第I卷(选择题)请点击修改第I卷的文字说明1.科学家曾预言一种可用作炸药的物质,分子式为C(N3)4,其爆炸反应方程式为:C(N3)4=C+6N2↑,下列说法一定正确的是A.该物质为离子晶体B.该物质可通过C60吸附N2直接制得C.18g该物质完全分解产生13.44LN2D.C(N3)4中碳元素为正价2.常温下,下列各组离子或分子能大量共存的是()A.无色溶液中: K+、H+、I-、Cr2O72-B.使pH试纸显深蓝色的溶液中:Cu2+、Na+、CH3COOH、Cl-C.含Na2S 的水溶液中:K+、H2S 、NH4+、SO42-D.水电离的H+浓度为1×10-3mol/L的溶液中:Cl-、Al3+、NH4+、Na+3.科学工作者发现另一种“足球分子”N60,它的结构与C60相似。
下列说法正确的是A.N60和C60互为同素异形体 B.N60是一种新型化合物C.N60和N2是同系物 D.N60和14N都是氮的同系物4.在Cu2S+2Cu2O6Cu+SO2↑反应中,说法正确的是A.Cu2O在反应中被氧化 B.Cu2S在反应中既是氧化剂又是还原剂C.Cu既是氧化产物又是还原产物 D.若反应中转移12mol电子,则生成6molCu 5.下列实验装置进行的相应实验,能达到实验目的的是A.装置甲可用于检验有乙烯生成B.装置乙可用于收集和吸收氨气C.装置丙可用于除去CO2中混有的HCl气体D.装置丁可用于除去溴苯中的溴6.下列离子方程式正确的是2+--2-B.向偏铝酸钠溶液中通入过量二氧化碳气体:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-C.用稀硝酸溶解氢氧化亚铁: Fe(OH)2+2H+=Fe2+ +2H2OD.漂白粉溶液中通入足量二氧化硫气体:ClO-+SO2+H2O=HClO+HSO3-7.某温度时,在密闭容器中,X、Y、Z三种气体浓度的变化如图I所示,若其它条件不变,当温度分别为T1和T2时,Y的体积分数与时间关系如图Ⅱ所示。
安徽省合肥市高三化学第三次教学质量检测试卷

安徽省合肥市2007年高三化学第三次教学质量检测试卷6.下列说法不正确的是()①一种元素只有一种原子,但可能有多种离子;②阴离子或阳离子有可能既有氧化性也有还原性;③由同种元素组成的物质属于单质;④有新单质生成的化学反应不一定是氧化还原反应;⑤具有相同质子数的粒子都属于同种元素。
A.①③⑤B.①②③C.③④⑤D.①③④7.下列判断正确的是( )A.任何液溶胶加入可溶性电解质后都能使胶体粒子凝成较大颗粒形成沉淀析出B.丁达尔现象、布朗运动、电泳现、胶体凝聚中都只涉及到分散系的物理性质C.因为胶体粒子比溶液中溶质粒子大,所以胶体可以用过滤的方法把胶粒分离出来D.胶体与其它分散系的本质区别是分散质粒子直径在1nm--100nm之间8.下列混合物在物质的量一定时,组内各物质按任意比例混合,完全燃烧时消耗O2的量不变的是()A.甲烷、乙烯、甲醇B. 乙烯、乙醇、羟基丙酸C.乙炔、苯、苯乙烯D. 丙烯、2-丁烯、丁醛9. 下列说法正确的是( )A.室温下,HClO分子不可能存在于c(OH-)>c(H+)的溶液中B.室温下,在pH=7的溶液中,CH3COO-不可能大量存在C.漂白粉只有在酸的存在下生成次氯酸才具有漂白作用D.c(CH3COO-)=c(Na+)的CH3COOH和CH3COONa的混合溶液呈中性10.下列各组离子,一定能在指定溶液中大量共存的是( )A.使甲基橙变红的溶液中:Fe3+、Na+、NO3-、SO42-B.水电离出的c(H+)=10-12mol/L的溶液中:NH4+、Na+、NO3-、S2O32-C.加入碳酸氢铵能放出气体的溶液中:K+、Ca2+、I-、NO3-D.能使紫色石蕊试液变蓝的溶液中:Na+、Mg2+、Cl-、SO42-11.以氢氧化钾溶液、氢气、氧气组成的燃料电池,电解饱和硫酸钠溶液一段时间,假设电解时温度不变且用惰性电极,下列说法不正确的是()A.当电池负极消耗m g气体时,电解池阴极有m g气体生成B.电解池的阳极反应式为:4OH-- 4e-==2H2O + O2↑C.电解后,c(Na2SO4)不变,且溶液中有晶体析出D.电池中c(KOH)不变;电解池中溶液pH变大12.无色溶液可能由K2CO3、MgCl2、NaHCO3、BaCl2溶液中的一种或几种组成。
皖南八校2014届高三第三次联考化学试题及答案

皖南八校2014届高三第三次联考理综化学试题7.人们的生活,生产与化学息息相关,下列说法不正确的是( )A.在即将到来的新能源时代,核能、太阳能、氢能将成为主要能源B.地沟油经过处理后可作为汽车燃油,故地沟油主要成分是液态烃C.实施化石燃科脱硫,脱硝可以减少硫的氧化物和氮的氧化物的排放D.雾霾天气中的主要污染物是PM2.5,其中含氮的有机物和光发生化学作用,可形成光化学烟雾8.常温下,下列各组离子在指定溶液中一定能大量共存的是()A.能与Cu反应产生气体的溶液:Na+、Fe2+、Cl-、SO42-B.滴入甲基橙显红色的溶液:K+、Cu2+、NO3-、I-C.由水电离出的C (H+)·C(OH-)=10-24溶液:K+、Na+、NO3-、Cl-D.无色溶液:K+、Al3+、ClO-、SO42-9.下列装置能达到实验目的是( )A.用图①所示装置测定NaOH的浓度B.用图②所示装置分馏少量石油C.用图③所示装置在实验室制备收集氨气D.用图④所示装置鉴别碳酸钠和碳酸氢钠10选项实验操作实验目的或结论A 将混有Ca(OH)2杂质的Mg(OH)2样品,放入水中搅拌成浆状后,加入足量饱和氯化镁溶液充分搅拌、过滤,沉淀用蒸馏水洗涤。
除去Mg(OH)2样品中的Ca(OH)2B 取少量KClO3晶体溶于适量的蒸馏水,再加入硝酸酸化的AgNO3溶液。
检验KC1O3中的氯元素C 向某溶液中滴加Ba(NO3)2溶液产生白色沉淀,再加稀盐酸沉淀消失。
说明原溶液中一定含有CO32-或SO32-D向盛有1mL 0.01lmol·L-1AgNO3溶液的试管中滴加5滴0.0lmol·L-1NaCl溶液,有白色沉淀生成,再向其中滴加0.01 mol·L-1NaI溶液,产生黄色沉淀。
常温下,Ksp(AgCl)>Ksp(Agl)1136K4[Fe(CN)6]的混合溶液,下列说法不正确的是( )A.K+移向催化剂bB.催化剂a表面发生反应:Fe(CN)64――e-=Fe(CN)63-C. Fe(CN)63-在催化剂b表面被氧化D.电解质溶液中Fe(CN)63-和Fe(CN)64-浓度基本保持不变12.已知N2O4(g)⇌2NO2(g) △H>0且平衡体系的总质量(m总)与总物质的量(n总)之比在不同温度下随压强变化曲线如图所示,下列说法正确的是( )A.平衡常数K(a)=K(b)<K(c)B.反应速率:v a<v bC.温度:T2>T1D.13.常温下,将0.01 mol·L-1 Na2SO3溶液与0.01 mol·L-1 KHSO3溶液等体积混合,若忽略混合后溶液的体积的变化,则下列判断正确的量( )A.混合后溶液中存在有关系:C(K+)+C(Na+)+C(H+)=C(SO32-)+C(HSO3-)+C(OH-)B.混合后溶液中存在有关系:C(K+)+C(H2SO3)+C(H+)=C(SO32-)+C(OH-)C.混合后溶液中存在有关系:C(SO32-)+C(HSO3-)+C(H2SO3)=0.02 mol·L-1D.两溶液混合前,Na2SO3溶液中,水电离出C(H+)小于KHSO3溶液中水电离出C(H+)第II卷(非选择题共180分)25.(15分)已知A、B、C、D、E都是周期表中前四周期的元素,它们的核电荷数依次增加。
