王积涛著《有机化学》第二版课后习题答案--第十六章 碳负离子的缩合反应
《有机化学》(王积涛第二版_下册)学习笔记

+ CO 2
可见其酸性是大于水而小于碳酸的。 苯环上有吸电子基团时增强苯酚的酸性;间氯苯酚酸性大于对氯苯 酚,邻氯苯酚酸性较强,但是如果邻位有较大基团时影响溶剂化的作 用而使酸性减弱。
42
有机化学笔记
2Hale Waihona Puke 3、与 FeCl3 的显色反应 (具有烯醇式结构的都能发生显色反应) 。 醚的生成
由于酚氧键不易断裂,不能像醇那样发生分子间的脱水而成醚,但是 酚氧负离子可以作为亲核试剂与卤代烷反应,类似于醇解反应生成 醚。又由于苯酚是弱酸,即酚氧负离子为强碱,易于与卤代烷发生消 除反应,所以卤代烷只能是伯卤。
2-甲氧基戊烷
混合醚的命名将较小的烃或苯基写在前面。 多元醚首先写出多元醇的名称,在写出另一个部分烃基的名称。 CH3OCH2CH2OCH3 乙二醇二甲醚 CH3CH2OCH2CH2OH 乙二醇乙醚
醚无活泼氢,分子间不能形成氢键但能与水形成氢键。 醚的化学性质 醚是稳定的化合物,对碱、稀酸、金属钠、催化氢化、还原剂、氧化 剂等不反应。 1、 钅羊盐及络合物的形成 醚上有未公用电子对,是 Lewis 碱,与强酸作用形成钅羊盐,与 Lewis 酸作用络合
CH 3CH2OC H2 CH3 +
浓H 2SO 4
R BF3 R O
C H 3C H2OCH 2CH3 H BF3
+
HSO4
R
O
R
+
2、 醚键的断裂
46
有机化学笔记
与 HX 同热,醚键断裂。
R O R + HX R H O -X R Δ ROH + RX
醚键断裂的方向:
伯大 芳
O O
伯小 脂
伯
有机课后习题解答(王积涛版).ppt

OH 油层 油层 OH
操作:
弃去
NO2 O2N (2) NO2 O2N
NO2 OH 油层 NO2 CH3 Na2CO3 H2O 水层 O2N 分液 O2N NO2
CH3 NO2 NO2 油层 H3O 分液 O2N 水层 弃去
OH NO2
ONa NO2
NO2
4. 用简单的化学方法鉴别下列化合物
OH Br CH3 H3C C OH CH3 CH3CHCH2CH3 OH CH3CH2CH2CH2OH FeCl3 √(紫红色)
3 2 1
Br
(4) Br
5 6 7
4 3 2
(5) OH
H
OH 2-溴-1,4-对苯二酚 邻溴对苯二酚
8
1
CH3 5 CH2C6H5
4
5-氯-7-溴-2-萘酚 5-氯-7-溴-β -萘酚
(3R,4R)-4-甲基-5-苯基-1-戊烯-3-醇
2. 完成下列反应式。
OH (1) C CH3 HCl (主) CH3 Cl CH3 CH3 CH3 + CH3 Cl + CH3 CH3
D:
F:
CH3 CH3 O
10. 完成下列转化。
(1) CH2OH H2SO4 Br2 CCl4 B2H6 CH3 H2O2 OH CH3 Br Br NaOH EtOH TsCl OH CH3 EtONa EtOH CH3 OH CCH2CH3 CH3 OTs
(2) HO
H2SO4 CH3
(CH3)3COK (CH3)3COH CH3
OH 比较: C CH3 H2SO4 CH3
CH3 CH3 (主) +
CH3 CH3
OH 机理: C CH3 H CH3 CH3 CH3 Cl Cl CH3 CH3
《有机化学》第三版 王积涛 课后习题答案 南开大学 无水印版本
CH3 CH3CH-CH3
ci s-3-heptene
(
):
2-
1
(2) Cl2 (3) Br2
CH3 CH3-C=CH2
Cl2
CH3 CH3-C-CH2
Cl Cl
1, 2- -2-
CH3 CH3-C=CH2
Br2
CH3 CH3-C-CH2
BrBr
1, 2- -2-
(4) I2
CH3
I2
CH3-C=CH2
方向优先?
= =
O CH3 _ C _ CH3 + Na+
- NH2
O
CH3
_
C
_
CH
2
Na+
+
NH3
反
应优先向着生成弱酸、弱碱的方向进行。13、利用表 1-1 中 pK 的值,预测下 a
列反应的走向。
(1) HCN + CH3COONa pKa: 9.2
Na+ -CN + CH3COOH pKa: 4.72
(1)
H3Cδ+__
δBr
(2)
H3Cδ+__
δNH2
δ- δ+ (3) H3C __ Li
(4)
H2Nδ-__
δ+ H
(5)
δ+ H3C __
δOH
(6)
H3Cδ_- _
δ+ Mg
Br
10、H 2
N-是一个
比
HO-更强的碱,对它们的共轭
酸
NH3
和
H2O,哪个酸性更
强?
为什麽?
答:H O 的酸性更强。共轭碱的碱性弱,说明它保持负电荷的能力强,其相应的 2 共轭酸就更容易失去 H+而显示酸性。
高教第二版(徐寿昌)有机化学课后习题答案第16章
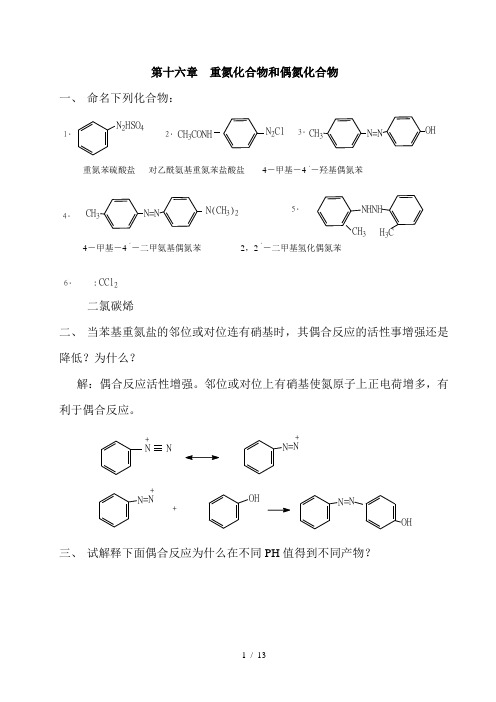
第十六章 重氮化合物和偶氮化合物一、 命名下列化合物:1.N 2HSO 42.CH 3CONHN 2Cl3.CH 3N=NOH4.6..CCl 2.二氯碳烯二、 当苯基重氮盐的邻位或对位连有硝基时,其偶合反应的活性事增强还是降低?为什么?解:偶合反应活性增强。
邻位或对位上有硝基使氮原子上正电荷增多,有利于偶合反应。
N N+N =N+N =N++OHN =NOH三、 试解释下面偶合反应为什么在不同PH 值得到不同产物?H 2NOH+C 6H5N 2+PH=5PH=9H 2NOHN=NC 6H 5H 2NOHN=NC 6H 5解:PH 等于5时,氨基供电子能力强于羟基,偶合反应在氨基的邻位发生。
PH 等于9时,为弱碱性,羟基以萘氧负离子形式存在,氧负离子供电子能力大于氨基,偶合反应发生在羟基的邻位。
四、 完成下列反应式:2.OHOCH 3+CH 2N 23.CH 33(CH 3)3COKCH 3Cl Cl 4.CH 3CH 2CH 2C=C CH 2CH 2CH 3H H+CH 2..CH 2CH 2CH 3CH 2CH 2CH 3H五、 指出下列偶氮染料的重氮组分和偶连组分。
解: 重氮组分 偶连组分1.N=NHSO 3N(CH 3)2HSO 3N 2+N(CH 3)22.N=NN=NOHN=NN 2+OH3.CH 3CONHN=NCH 3OH CH 3CONHN 2+HOCH 34.NaSO 3N=NHONaSO 3N 2+HO5.SO 3HNH 2N=N SO 3HN 2N=NNH 2SO 3HN 2++NH 2六、 完成下列合成:1.NO 2ClClClNO 2Cl ClNH 2NH 2N 2ClFe/HCl2ClClClNaNO 2,HClClCl ClH 3PO 2Cl2.CH 3CH 3Br BrCH 3CH 3CH 3CH 33H 2SO 4NO 2NH 2NH2Br[H]2BrBrCNCNNO 22NH 22N 2Cl N 2ClCNCNNaNO 2,HClKCN,CuCN3.NHCOCH 3OHBrNHCOCH 3Br NHCOCH 3Br BrBrNH 2N 2HSO 4H 2O,H+NaNO 2H 2SO450H SO OHBr4.5.CH 3CH 3NO 2CH 3CH 3CH 3NO 2NH 2NHCOCH 3[H]CH 3COClHNO H 2SO 4CH 3NO 2CH 3NHCOCH 3NO 2CH 3H O,H +NH 2N 2ClNaNO 2NO 2CH 3NO 2H PO6.NH 2NO 2BrBrNH 2CH 3COClNHCOCH 33H 2SO 4NHCOCH 3NO 2NHCOCH 3NO 2Br BrBrNO 2BrBr H O,H +NH 2NO 2BrBrNaNO2HClN2Cl NO 2BrBrH 3PO 27.NH 2BrCOOHBrNH 2NH2NH 2H 2SO 4SO 3H2BrBr NH2SO 3H H O,H +BrBr BrBrNaNO 2,HClN 2Cl KCN/CuCNBrBr BrBrCNCOOHH 2O,H +七、 以苯,甲苯,萘和小于或等于两个碳原子的有机化合物为原料合成下列化合物:1.(CH 3)2NN=N3H 2SO 4NO 2NH 2N(CH 3)23NH 2HNO 2N 2ClN(CH3)2N 2Cl+(CH 3)2N N=N2.CH 3N=NH 2NNH 2CH 3HNO 3H 2SO 4NO2CH 3CH3[H]NH 2CH3NaNO 2HClN 2Cl HNO 3H 2SO 42NO 2O 2NH 2NNH2[H]CH 3N 2ClCH 3N=NH 2NNH 23.CH 3N=N CH 3CH 3SO 3HCH3CH 3H SO NaOHONaCH 3H 3O +OHCH 3HNO 3H 2SO 4CH 3CH 3NO 2NO 2+CH 3NO 2[H]CH 3CH 3NH 2N 2Cl2HClCH 3+CH 3N=NCH 3N=N 4.HSO3OH NH2H SONH2SO3H 2SO3HN2Cl+H2SO4<65CSOOHOHSO3HN2Cl+N=NHSO3OH5.(CH3)2N N=NNO2NO2NH2NHCOCH3NO2NHCOCH3 NO2NO2NH2N2Cl2(CH3)2N N=N NO2 NH22CH3IN(CH3)2N=NCH 3CH3CH 3NO 22ZnNaOH/C 2H 5OHN=NCH 3CH 36.7.COONaN=N NaSO 3OH OH+CO 23OHCOONaN 2ClCOONaN=NNaSO 3OH 8.N=NCH 3HOCH 3OHCH 3+ClN 2CH 3N=NHO CH 3CH 3八、 推测下列化合物的结构:1,某芳烃分子式为C 6NO 2Fe,HClNaNO ,HClC H OHCl2OC 6H 3OHCl NO 2ClBrNO 22、某芳香性族化合物分子式为试根据下列反应确定其结构:C 6H 4NO 2CH 322+4O C OONO 2CH 3NH 2CH 3CH 3CH 3CH 3O C O OFe,HClNaNO 2,HCl N 2ClCuCN CN H 2O,H +COOH4COOH九、下列结构的偶氮染料,以氯化亚锡-盐酸溶液还原分解后,生成那些化合物?1.N=N(CH 3)2NSO 3H(CH 3)2N NH 2H 2N SO 3HSnCl 2,HClN=NSnCl 2,HClHSO 3NH 2SO 3H2.HSO 3NH 2NH 2SO 3HH 2N+N=N SnCl ,HClNH 2H 2N+3.CH 3OHCH 3OH十、某化合物以氯化亚锡盐酸还原可得对甲基苯胺和N,N -二甲基对苯二胺,试推测原化合物的结构,并以苯,甲苯及甲醇为原料合成之。
有机化学_第二版答案(全)

《有机化学》第二版习题参考答案第二章烷烃1、用系统命名法命名下列化合物(1)2,3,3,4-四甲基戊烷(2)3-甲基-4-异丙基庚烷(3)3,3,-二甲基戊烷(4)2,6-二甲基-3,6-二乙基辛烷(5)2,5-二甲基庚烷(6)2-甲基-3-乙基己烷(7)2,2,4-三甲基戊烷(8)2-甲基-3-乙基庚烷2、试写出下列化合物的结构式(1) (CH3)3CC(CH2)2CH2CH3(2) (CH3)2CHCH(CH3)CH2CH2CH2CH3(3) (CH3)3CCH2CH(CH3)2(4) (CH3)2CHCH2C(CH3)(C2H5)CH2CH2CH3(5)(CH3)2CHCH(C2H5)CH2CH2CH3(6)CH3CH2CH(C2H5)2(7) (CH3)2CHCH(CH3)CH2CH3(8)CH3CH(CH3)CH2CH(C2H5)C(CH3)33、略4、下列各化合物的系统命名对吗?如有错,指出错在哪里?试正确命名之。
均有错,正确命名如下:(1)3-甲基戊烷(2)2,4-二甲基己烷(3)3-甲基十一烷(4)4-异丙基辛烷(5)4,4-二甲基辛烷(6)2,2,4-三甲基己烷5、(3)>(2)>(5)>(1) >(4)6、略7、用纽曼投影式写出1,2-二溴乙烷最稳定及最不稳定的构象,并写出该构象的名称。
H交叉式最稳定重叠式最不稳定8、构象异构(1),(3)构造异构(4),(5)等同)2),(6)9、分子量为72的烷烃是戊烷及其异构体(1) C(CH3)4(2) CH3CH2CH2CH2CH3 (3) CH3CH(CH3)CH2CH3(4) 同(1)10、分子量为86的烷烃是己烷及其异构体(1)(CH3)2CHCH(CH3)CH3(2) CH3CH2CH2CH2CH2CH3 , (CH3)3CCH2CH3 (3)CH3CH2CH(CH3)CH2CH3(4)CH3CH2CH2CH(CH3)214、(4)>(2)>(3)>(1)第三章 烯烃1、略2、(1)CH 2=CH — (2)CH 3CH=CH — (3)CH 2=CHCH 2— CH 2CH CH 3M eH H i-P rE t M en-P rM e M e E t i-P rn-P r (4)(5)(6)(7)3、(1)2-乙基-1-戊烯 (2) 反-3,4-二甲基-3-庚烯 (或(E)-3,4-二甲基-3-庚烯 (3) (E)-2,4-二甲基-3-氯-3-己烯 (4) (Z)-1-氟-2-氯-2-溴-1-碘乙烯(5) 反-5-甲基-2-庚烯 或 (E)-5-甲基-2-庚烯 (6) 反-3,4-二甲基-5-乙基-3-庚烯 (7) (E) -3-甲基-4-异丙基-3-庚烯 (8) 反-3,4-二甲基-3-辛烯 4、略 5、略 6、CH 3CH 2CHC H 2CH 3CH 3CH 2CCHC H 3CH 3OH BrCH 3CH 2CCHC H3CH 3Cl ClCH 3CH 2C CHC H3CH 3OH OHCH 3CH 2CHCHC H 3CH 3OHCH 3CH 2COCH3CH 3CHOCH 3CH 2CHCHC H 3CH 3Br(1)(2)(3)(4)(5)(6)(7)7、活性中间体分别为:CH 3CH 2+ CH 3CH +CH 3 (CH 3)3C + 稳定性: CH 3CH 2+ > CH 3CH +CH 3 > (CH 3)3C + 反应速度: 异丁烯 > 丙烯 > 乙烯8、略9、(1)CH 3CH 2CH=CH 2 (2)CH 3CH 2C(CH 3)=CHCH 3 (有顺、反两种) (3)CH 3CH=CHCH 2CH=C(CH 3)2 (有、反两种)用KMnO 4氧化的产物: (1) CH 3CH 2COOH+CO 2+H 2O (2)CH 3CH 2COCH 3+CH 3COOH (3) CH 3COOH+HOOCCH 2COOH+CH 3COCH 310、(1)HBr ,无过氧化物 (2)HBr ,有过氧化物 (3)①H 2SO 4 ,②H 2O (4)B 2H 6/NaOH-H 2O 2 (5)① Cl 2,500℃ ② Cl 2,AlCl 3(6)① NH 3,O 2 ② 聚合,引发剂 (7)① Cl 2,500℃,② Cl 2,H 2O ③ NaOH 11、烯烃的结构式为:(CH 3)2C=CHCH 3 。
有机化学(第二版)课后答案

有机化学(第二版)课后答案第一章绪论1-1扼要解释下列术语.(1)有机化合物(2)键能、键的离解能(3)键长(4)极性键(5)σ键(6)π键(7)活性中间体(8)亲电试剂(9)亲核试剂(10)Lewi碱(11)溶剂化作用(12)诱导效应(13)动力学控制反应(14)热力学控制反应答:(1)有机化合物-碳氢化合物及其衍生物(2)键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所吸收的能量称为键能。
键的离解能:共价键断裂成两个原子所吸收的能量称为键能。
以双原子分子AB为例,将1mol气态的AB拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。
应注意的是,对于多原子分子,键能与键的离解能是不同的。
分子中多个同类型的键的离解能之平均值为键能E(kJ.mol-1)。
(3)键长:形成共价键的两个原子核之间距离称为键长。
(4)极性键:两个不同原子组成的共价键,由于两原子的电负性不同,成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有部分负电荷性质,另一端电子云密度较小具有部分正电荷性质,这种键具有极性,称为极性共价键。
(5)σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道,所形成的键叫σ键(6)π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键(7)活性中间体:通常是指高活泼性的物质,在反应中只以一种”短寿命”的中间物种存在,很难分离出来,,如碳正离子,碳负离子等。
(8)亲电试剂:在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。
(9)亲核试剂:在反应过程中,如果试剂把电子对给予有机化合物与它反应的那个原子并与之共有形成化学键,这种试剂叫亲核试剂。
(10)Lewi碱:能提供电子对的物种称为Lewi碱。
(11)溶剂化作用:在溶液中,溶质被溶剂分子所包围的现象称为溶剂化作用。
(12)诱导效应:由极性键的诱导作用而产生的沿其价键链传递的电子对偏移(非极性键变成极性键)效应称为诱导效应。
王积涛著《有机化学》第二版课后习题答案7立体化学共59页

(1)3-溴己烷
Br
CH3CH2 C CH2CH2CH3
H
C2H5
C2H5
H
Br Br
H
C3H7
S
C3H7
R
(2) 3-甲基-3-氯戊烷
CH3
CH3CH2 C CH2CH3
无手性
Cl
(3)1,3-二氯戊烷 CH2-CH2
Cl C2H5
H C CH2CH3 Cl
C2H5
SH
Cl
Cl
HR
CH2CH2Cl
(7)(1S,3S,4R)-3-甲基-4-乙基环己醇
C 2H 5 CH3
OH
6.写出下列化合物的所有立体异构体;并用(R,S 及Z,E)标明构型。
(1) 2,4-二溴戊烷
CH3
H
Br
H
H
H
Br
CH3
H
Br
H
H
Br H
CH3
Br H
H
H
H
Br
CH3
CH3
CH3
( 2 R ,4 S )
(2 S ,4 S )
(4)
C
D
C2H5
(5)
C
H
D
H
OH
Br CH3 C CH3
CH3
HO
H (S)
D C2H 5
H
D
(S )
C B r(C H 3)2
CH3
(6)
C
HO H
H OH
C CH3
Br
(7)
H
CH3
C 2H 5
Br
H
CH3
H
O H (S)
《有机化学》(王积涛第二版上册和下册)学习笔记_合并

酸是电子的受体,碱是电子的给体。
NH3 + BF3
碱酸
H3N- BF3
酸碱加和物
5
有机化学笔记
有机反应的类型:
按断键的方式分为均裂和异裂,此外还有协同
1 均裂反应-自由基反应
AB
AB
2 异裂反应-离子型反应
AB
3 协同反应-成键断键同步发生
≠ +
AB
第二章 烷烃(alkane)
开链饱和烷烃通式:CnH2n+2 同系列:结构相似,通式相同组成上差若干个 CH2 的一系列化合物 同系物:同系列的各化合物互为同系物 构造:分子中原子间相互连接的方式和次序 构象:由于键的旋转而产生的分子中原子或原子团在空间上的不同排 列方式(交叉式和重叠式是两种极限式) 命名法: 1 选最长的、取代基最多的为主链 2 从支链最近处开始编号 3 较优基团后列出 4 支链编号最小原则 较优基团的次序原则: 1 原子序数大较优
(SP、SP2、SP3) Br ö nsted 酸碱理论: 酸是质子的给体,碱是质子的受体。
HCl
H
Cl
酸Leabharlann 共轭碱NH3H
碱
N H4
共轭酸
酸强度用酸在水中的解离常数 Ka 来测定,碱也一样。
HA + H2O
H3O + A
Ka =
A
H3O
HA
PKa=-lgKa PKa<4 强 酸 PKa>4 弱
酸
Lewis 酸碱理论:
有机化学
王积涛第二版
课本笔记及自学心得
有机化学笔记
目录 引言................................................................................................. 2 第二章 烷烃(alkane).................................................................... 6 第三章 烯烃(alkene).................................................................... 9 第四章 炔烃和二烯烃(alkyne&alkadiene)......................... 15 第五章 脂环烃(alicylic hydrocarbon)................................... 19 第六章 芳烃(aromatic hydrocarbon)....................................... 22 第七章 立体化学(stereochemistry).........................................27 第八章 卤代烃(halide hydrocarbon)....................................... 29 第九章 醇和酚(alcohol&phenol).............................................35
王积涛著《有机化学》第二版课后习题答案--第十七章 胺

OH
CH3 CH3CH2CH=C-NO2
CH3 H2/Pt CH3CH2CH2-CH-NH2
(5)
CH3NO2 + 3HCHO
CH2OH OH HOCH2-C-NO2 CH2OH
(6)
(CH3)2CHNH2 +
(CH3)2CHNHCH2CH2OH O
(7)
NH + Br-(CH2)4 -Br
CH3 Ag2O H2O CH3 N
-
N
CH3 OH
Br+
CH3 N CH3 CH3
(8) N H
CH3I
N I过量 CH3 CH3
CH3
宁夏大学化学化工学院
7
CH3 (9) C-C-CH3 OH NH2
NaNO2 H+
O CH3-C-CH CH3
O Cl N-K+ O O + CH3-CH-C-OC2H5 CH3CHCO2C2H5
解:在0℃~5℃下分别加入NaNO2 ~HCl立即N2↑为D,温
度升高后放出N2的C,生成棕色油状物的是A,不与亚
硝酸反应的是B。 7、用化学方法分离下列混合物。 (1)、苄胺,N ~甲基环己胺,苯甲醇,对甲苯酚。 (2)、邻甲苯酚,水杨酸,N ~甲基苯胺,乙苯, 对甲基苯胺。
宁夏大学化学化工学院 13
解: (1) CH3
OH CH2NH2 NHCH3 CH2OH NaOH 水
水层
CH3
CO2 O Na CH3 H2O
+
OH
CH2NH2 油层 NHCH3 CH2OH HCl H2O
油层
CH2OH CH2NH2 NHCH3
水层
油层
王积涛著《有机化学》第二版课后习题答案--第四章 炔烃与二烯烃

2
(12)热的KMnO4水溶液
C H 3C H 2C ≡ C H
K Mn O 4
△
CH 3 C H 2 COOH +CO
2
5、用1,3-丁二烯代替1-丁炔进行4题中的反应, 如果有反应,写出反应式。 (1)1molH2,Ni;
H 2 (1 m o l)
CH 2 =C H -C H =CH
2
Ni
CH 3 -CH = CH - CH
CH 3—
CH3
— C = C— — C = C— CH3 — CH3 H
H—
反 ,反 -3 -甲 基 -2 ,4 -已 二 烯 (2 Z ,4 E )
CH 3—
H
顺 ,顺 (2 E ,4 Z )
-3 -甲 基 -2 ,4 -已 二 烯
CH3 — C = C— H— — C = C— H — CH3 H
CH3— H
— C = C— —
C H 2C H 2C H = C H 2 H
C H 3— H — C = C— — H C H 2C H 2C H =C H 2
顺-1,6-庚二烯
反-1,6-辛二烯
(2)无共轭、有顺反
顺-4-已烯-1-炔
反-4-已烯-1-炔
3
(3)有共轭、有顺反
C H 3—
— C = C— — H C = C— H— H
Cl HC ≡ CCH3
HCl
Cl
HI
H 2 C = C -C H 3
C H 3 -C -C H 3 I
—
C H 3C H 2C H 2 — (2 ) H C H 3C H = C H 2
— C = C—
CH3 H
高等有机概论

15.醚
R O R
,
C O
C
O CH 2 CH
CH 2
C H2
CH O CH 2 CH
CH 2
(1)醚氧原子上的反应 碱性、 盐的形成、醚键的断裂 (2)-碳上的反应—自动氧化 (3)1,2-环氧化合物的开环反应 亲电开环,亲核开环 (4)苯基烯丙醚及乙烯基烯丙醚的重排反应 ——Claisen重排
23. 季铵盐、季铵碱 季铵碱的Hofmann消除 24. 芳基重氮盐 (1)热分解及取代反应 (2)还原脱胺反应 (3)还原成肼 (4)偶联反应
H C C
+
N
+
Ar N 2 x
-
25. 偶氮化合物 (1)异构化反应 (2)还原及还原产物的联苯胺重排 (3)氧化反应 (4)热分解反应
26. 重氮甲烷
2. 高等有机化学的学习方法 (1)要重视这门课。 (2)要喜欢这门课。 (3)要注意这门课与相关课程的联系。
与物理、化学基本原理的联系:质量守恒、电荷守恒。 与无机、物化知识的联系:化学键理论、酸碱理论等。 与基础有机化学的联系:各类有机化合物的化学性质。
(4)看书时要动笔写写画画。
三、各类有机 化合物的结构 和化学性质
29. 吡啶 (1)亲电取代 (2)亲核取代 (3)碱性和亲核性 (4)侧链 - H的反应 (5)氧化和还原 30. 喹啉和异喹啉 (1)亲电取代 (2)亲核取代 (4)侧链 - H的反应 (5)氧化和还原
N ..
N
N
31. 单糖 (1)还原 (2)氧化 (3)成脎 (4)差相异构化 (5)醛糖的递升和递降 32. 氨基酸 (1)等电点 (2)与水合茚三酮的反应 (3)氨基和羧基的反应
19. 羧酸衍生物
王积涛著《有机化学》第二版课后习题答案--第二章 烷烃

3) 链终止
C C l C H C C H 3 3 3 + ︱ C H 3
C H C C H H C C H 3 3 +C 3 3 ︱ ︱ C H C H 3 3
C C l 3 ︱ C H C C H 3 3 ︱ C H 3
C H H C 3 3 ︱ ︱ C H C C C H 3 3 ︱ ︱ C H H C 3 3
2
CH3 3)CH CH ∣ 3 2CHCH2CH2CH3 H3C CH3 ∣ 4) CH ∣ CHCHCH CH
3 2 3
2019/2/16 宁夏大学化学化工学院
C H C H 3 3 5) ∣ ∣ C H C H C H C H C H 3 2 3
CH3 ∣ 6) CH3CCH2CH2CH3 ∣ CH3
他们是不同物质
15
8.叔丁基过氧化物是一个稳定而便于操作的液体,可作 为一个方便的自由基来源:
( C H ) C O O C ( C H ) 3 3 3 3 1 3 0 ℃ 2 ( C H ) C O 3 3 或 光
异丁烷和 CCl4 的混合物在 130-140℃时十分稳定。假如 加入少量叔丁基过氧化物就会发生反应,主要生成叔 丁基氯和氯仿,同时也有少量叔丁醇( CH3)3C-OH ,其 量相当于所加的过氧化物 ,试写出这个反应可能机理的 所有步骤。
C C l C C l 3+ 3
C C l C l C 3 3
2019/2/16
宁夏大学化学化工学院
18
2019/2/16
宁夏大学化学化工学院
16
1) 链引发
2) 链增长
C H 3
C H 3 ︱ H C C H ( C H ) C O+C ② 3 3 3 3 ︱ H
有机化学课后习题参考答案(全)

第一章绪论 (1)第二章饱和烃 (3)第三章不饱和烃 (7)第四章环烃 (14)第五章旋光异构 (22)第六章卤代烃 (27)第七章波谱分析 (33)第八章醇酚醚 (34)第九章醛、酮、醌 (41)第十章羧酸及其衍生物 (50)第十一章取代酸 (58)第十二种含氮化合物 (65)第十三章含硫和含磷有机化合物 (72)第十四章碳水化合物 (74)第十五章氨基酸、多肽与蛋白质 (78)第十六章类脂化合物 (82)第十七章杂环化合物 (88)第一章绪论1.1 扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
1.2是否相同?如将CH4 及CCl4各1mol混在一起,与CHCl3及CH3Cl各1mol的混合物是否相同?为什么?答案:NaCl与KBr各1mol与NaBr及KCl各1mol溶于水中所得溶液相同。
因为两者溶液中均为Na+ , K+ , Br-, Cl-离子各1mol。
由于CH4 与CCl4及CHCl3与CH3Cl在水中是以分子状态存在,所以是两组不同的混合物。
1.3 碳原子核外及氢原子核外各有几个电子?它们是怎样分布的?画出它们的轨道形状。
当四个氢原子与一个碳原子结合成甲烷(CH4)时,碳原子核外有几个电子是用来与氢成键的?画出它们的轨道形状及甲烷分子的形状。
答案:C+624HCCH 4中C 中有4个电子与氢成键为SP 3杂化轨道,正四面体结构CH 4SP 3杂化2p y2p z2p x2sH1.4 写出下列化合物的Lewis 电子式。
a. C 2H 4b. CH 3Clc. NH 3d. H 2Se. HNO 3f. HCHOg. H 3PO 4h. C 2H 6i. C 2H 2j. H 2SO 4答案:a.C C H H H HCC HH HH或 b.H C H H c.H N HHd.H S He.H O NO f.O C H Hg.O P O O H H Hh.H C C HHH H HO P O O H HH或i.H C C Hj.O S O HH OO H H或1.5 下列各化合物哪个有偶极矩?画出其方向。
有机化学第二版答案

有机化学第二版答案引言有机化学是研究碳基化合物的化学性质和反应机理的一门学科。
它在化学领域中占有重要的地位,涉及到药物、合成材料、能源等诸多领域。
本文档将提供《有机化学第二版》中各章节的答案,以帮助读者更好地学习和掌握有机化学的知识。
第一章:有机化学导论问题1:定义有机化学并描述其研究对象。
有机化学是研究碳元素相关的化合物的化学行为和反应机理的学科。
它主要研究有机物的结构、性质和合成方法。
问题2:简述有机化合物的特点。
有机化合物的主要特点包括:•含有碳元素,且通常与氢元素相连形成碳氢键;•可以形成多样的结构和化学键;•具有多样的物理性质,如熔点、沸点等。
问题3:列举常见的有机化合物。
常见的有机化合物包括烃类(烷烃、烯烃、炔烃)、醇、醚、酮、酸、酯、胺等。
第二章:有机化合物的结构和性质问题1:说明有机化合物的结构式表示法。
有机化合物的结构式表示法通过连接线、角标等方式来反映出分子中的原子之间的连接关系和空间构型。
问题2:解释分子式和结构式的区别。
分子式指的是表示化合物种类和组成的化学式,只能提供有机物的整体元素比例关系,不能提供具体的分子结构信息。
而结构式包括结构式式样(线角式、骨架式、立体式等)和结构式种类(分子式、简式、全式等),可以提供分子结构、空间构型等信息。
问题3:阐述立体化学的概念及其在有机化学中的重要性。
立体化学是研究分子或离子的三维空间构型及其对化学性质的影响的学科。
在有机化学中,分子的立体构型直接影响着其物理性质和化学反应。
例如,同分异构体的存在就是立体化学的重要概念之一。
第三章:烃类和可代替烃类问题1:列举并解释烃类的分类。
烃类可以分为以下几类:•烷烃:只含有碳碳单键的烃。
•烯烃:含有至少一个碳碳双键的烃。
•炔烃:含有至少一个碳碳三键的烃。
问题2:简述杂环烃的特点及其命名规则。
杂环烃是指由碳和非碳原子构成的环状化合物。
杂环烃的命名规则与脂环烃类似,不同原子的名字前面加上指示原子种类和数目的前缀,并用短划线连接。
王积涛著《有机化学》第二版课后习题答案--第十六章 碳负离子的缩合反应

O
O ① NaOC2H5 ②CH2—CH2 O
O CH3 O CH3C—C—C
O CH3 O
解:
CH3CCH-C-OC2H5 CH3
O
O CH3 O CH3-C-C C-OC2H5 CH2CH2-O-
CH2—CH2
CH3-C-C O C-OC2H5
O CH3 O CH3-C-C-C-OC2H5 H OC2H5 -OC2H5
吡咯烷
CH3 CHCH=C CH3
O (5) COCH3 C-CH3 O ① KOH ② H+
O C CH2 C O
宁夏大学化学化工学院
COC2H5 O
6
(6). C6H5CH2CHO
+
ClCHCO2C2H5 CH3
① Zn ② H /H2O
+
O C6H5CH-CH-COC2H5 OH CH3
为Reformatsky反应
解:
O
H+
‥ HOCH2CH(CH3)2
OCH2CH H CH3
质子迁移 HO O—H OCH2CH(CH3)2 -H+ H—O O C OCH2CH(CH3)2
OH
O 质子迁移 OCH2CH(CH3)2
-
O
H
OH OCH2CH(CH3)2 -H2O
O
OCH2CH(CH3)2
宁夏大学化学化工学院
15
①
-
OH CH2COOH
② H+, △ -CO2
(3).
O
COOH
① NaOC2H5 ② BrCH2Br ①
-
CH2—CH2 CH2 CH2—CH2
王积涛著《有机化学》第二版课后习题答案6芳烃

2020/6/17
宁夏大学化学化工学院
29
(3) 为什么反式的1,2-二苯基乙烯不能转变为顺式1,2二苯基乙烯?
解答: (1)反式更加稳定。因为形成e-Hσ键(放热)减去断
裂C=C(吸热)等于氢化热。氢化热数值意味着破 坏C=C需要更高的能量。
(2)导致转变的因素 : ①由氢化热值可以看出:反式比顺式稳定。 ②顺式中两个较大基团在双键同侧造成空间拥挤。
宁夏大学化学化工学院
35
( 2 ) O2,V2O5
O2 V2O5
( 3 ) Na, CH3CH2OH H
=
=
O O 邻笨二甲酸酐
O
H
2020/6/17
Na, C2H5OH 78℃
Na, C2H5OH 150℃
H
H
1,4-二氢化萘
宁夏大学化学化工学院
四氢萘
36
( 4 ) Na, C5H11OH
Na C5H11OH
16
(2) 苯;溴苯;硝基苯;甲苯 甲苯>苯>溴苯>硝基苯
COOH
CH3
(3)
COOH
CH3
COOH
COOH
CH3 >
CH3 >
COOH >
COOH
2020/6/17
COOH
宁夏大学化学化工学院
COOH
17
CHCl2 CCl3 (4)
CH2Cl CH3
CH3 >
CH2Cl >
CHCl2 >
CCl3
CH2Br +
CCl3
21
(2)反应中还分离出少量的HBr和C2Cl6.这些产物是怎样 形成的.
CH3
CH2
Br +
【推荐】有机化学第二版答案-推荐word版 (28页)

本文部分内容来自网络整理,本司不为其真实性负责,如有异议或侵权请及时联系,本司将立即删除!== 本文为word格式,下载后可方便编辑和修改! ==有机化学第二版答案篇一:有机化学 (第二版)课后答案有机化学(第二版)课后习题参考答案第一章绪论1-1 扼要解释下列术语.(1)有机化合物 (2) 键能、键的离解能 (3) 键长(4) 极性键 (5) σ键 (6)π键 (7) 活性中间体 (8) 亲电试剂(9) 亲核试剂(10)Lewis碱(11)溶剂化作用 (12) 诱导效应 (13)动力学控制反应 (14) 热力学控制反应答:(1)有机化合物-碳氢化合物及其衍生物(2) 键能:由原子形成共价键所放出的能量,或共价键断裂成两个原子所吸收的能量称为键能。
键的离解能:共价键断裂成两个原子所吸收的能量称为键能。
以双原子分子AB为例,将1mol气态的AB拆开成气态的A和B原子所需的能量,叫做A—B键的离解能。
应注意的是,对于多原子分子,键能与键的离解能是不同的。
分子中多个同类型的键的离解能之平均值为键能E(kJ.mol-1)。
(3) 键长:形成共价键的两个原子核之间距离称为键长。
(4) 极性键: 两个不同原子组成的共价键,由于两原子的电负性不同, 成键电子云非对称地分布在两原子核周围,在电负性大的原子一端电子云密度较大,具有部分负电荷性质,另一端电子云密度较小具有部分正电荷性质,这种键具有极性,称为极性共价键。
(5) σ键:原子轨道沿着轨道的对称轴的方向互相交叠时产生σ分子轨道,所形成的键叫σ键。
(6) π键:由原子轨道侧面交叠时而产生π分子轨道,所形成的键叫π键。
(7) 活性中间体:通常是指高活泼性的物质,在反应中只以一种”短寿命”的中间物种存在,很难分离出来,,如碳正离子, 碳负离子等。
(8) 亲电试剂:在反应过程中,如果试剂从有机化合物中与它反应的那个原子获得电子对并与之共有形成化学键,这种试剂叫亲电试剂。
有机化学第二版胡志强课后答案全解

有机化学第二版胡志强课后答案全解1、具有挥发性的生物碱是()[单选题] *A吗啡碱B麻黄碱(正确答案)C苦参碱D小檗碱2、浓缩速度快,又能保护不耐热成分的是()[单选题] *A水蒸汽蒸馏法B常压蒸馏法C减压蒸馏法(正确答案)D连续回流法3、牛蒡子属于()[单选题] *A香豆素类B木脂内酯(正确答案)C苯丙酸类D4、连续回流提取法与回流提取法比较,其优越性是()[单选题] *A节省时间且效率高B节省溶剂且效率高(正确答案)C受热时间短D提取量较大5、在溶剂提取法中,更换新鲜溶剂可以创造新的(),从而使有效成分能够继续被提取出来。
()[单选题] *A极性差B压力差C浓度差(正确答案)D体积差6、E何首乌(正确答案)下列不含蒽醌类成分的中药是()*A丹参(正确答案)B决明子C芦荟D紫草(正确答案)7、在高效液相色谱法中,常用的柱内填料是()[单选题] *A氧化铝B活性炭C十八烷基硅烷键和硅胶(正确答案)D羧甲基纤维素8、处方中厚朴主要化学成分厚朴酚,其结构类型是()[单选题] *A黄酮B香豆素C木脂素(正确答案)D三萜皂苷9、具有酚羟基或羧基的游离蒽醌类成分有一定酸性,可用的提取方法是()[单选题]* A酸溶碱沉法B碱溶酸沉法(正确答案)C水提醇沉法D醇提水沉法10、南五味子具有的主要化学成分是()[单选题] *A色原酮B胆汁酸C多糖D木脂素(正确答案)11、有机溶剂加热提取中药成分应采用()[单选题] * A回流装置(正确答案)B蒸馏装置C萃取装置D分馏装置12、在简单萃取法中,一般萃取几次即可()[单选题] * A3~4次(正确答案)B1~2次C4~5次D3~7次13、容易发霉变质的是()[单选题] *A中药水提取液(正确答案)B中药乙醇提取液C二者均是D二者均非14、碱水提取芦丁时,若PH过高会使()[单选题] *A产品质量降低B产品收率降低(正确答案)C苷键水解断裂D内酯环开环15、E连续回流提取法(正确答案)用乙醇作溶剂提取时,下列说法正确的是()* A对植物细胞壁穿透力强(正确答案)B溶解范围广,提取较全面(正确答案)C提取液中蛋白质、多糖等水溶性杂质少(正确答案)D有防腐作用,提取液不易发霉变质(正确答案)16、E易酶解苷类成分关于亲水性有机溶剂,说法正确的有()*A极性大(正确答案)B极性小C水不相溶D与水部分相溶17、具有挥发性的香豆素成分是()[单选题] *A游离小分子简单香豆素(正确答案)B香豆素苷C呋喃香豆素D双香豆素18、苯丙素类的基本母核是具有一个或数个()单元的天然化合物()[单选题] *AC6-C3基团(正确答案)BC6-C6基团CC5-C3基团DC8-C8基团19、能提取出中药中的大部分亲水性成分和绝大部分亲脂性成分的溶剂是()[单选题]* A乙醚B乙醇(正确答案)C水D苯20、用有机溶剂加热提取中药成分时,宜采用(多选)()*A浸渍法B渗漉法C煎煮法D回流提取法(正确答案)21、沉淀法的分类不包括以下哪一种方法()[单选题] *A水提醇沉法B碱提酸沉法C铅盐沉淀法D结晶法(正确答案)22、以下哪种方法是利用成分可以直接由固态加热变为气态的原理()A [单选题] * A升华法(正确答案)B分馏法C沉淀法D透析法23、七叶内酯的结构类型为()[单选题] *A简单香豆素(正确答案)B简单木脂素C呋喃香豆素D异香豆素24、在结晶溶剂的选择过程中首先要遵循的是()[单选题] *A成分的纯度(正确答案)B相似相容原理C冷却热饱和原理D以上都不对25、木脂素母核结构中的C6-C3单体数目为()[单选题] *A1个B2个(正确答案)C3个D4个26、挥发性成分的提取,常用的是()[单选题] *A溶剂提取法B水蒸气蒸馏法(正确答案)C超临界液体萃取法D超声提取法27、所有游离香豆素均可溶于热的氢氧化钠水溶液,是由于其结构中存在()[单选题] * A异戊烯基B酮基C内酯环(正确答案)D酚羟基对位活泼氢28、适用于队热及化学不稳定的成分、低极性成分的提取()[单选题] * A渗漉法B超声提取法C回流提取法D超临界流体提取法(正确答案)29、以下哪种分离方法是利用分子筛的原理的()[单选题] *A吸附色谱法B萃取法C沉淀法D透析法(正确答案)30、牛蒡子属于()[单选题] *A香豆素类B木脂内酯(正确答案)C苯丙酸类D黄酮类。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
CH3CH2-C-CH=CCH3 OCH3CH=CH-CH=C-CH3
‥ CH3CH=CHCHCCH3
碱性:
‥ CH3CH=CHCHCCH3
>
Cl (2). CHCO 2C2H5 ,
宁夏大学化学化工学院 2
CHCO 2C2H5
解: Cl ‥ CHCO2C2H5 Cl O CH-COC2H5 Cl OCH=C-OC2H5 Cl O CH-COC2H5 Cl O CH-COC2H5
习题与解答
宁夏大学化学化工学院
1
1. 写出下列负离子的共振结构式。分别比较两对离子的碱性。
O
O ,
-
O CH3CH=CHCHCCH3
O O
-
(1).
解:
CH3CCHCCH3
O
O O ‥ CH3CH2CCHCCH3 O
O
CH3CH2-C=CH-CCH3 O ‥ CH3CH-CH=CH-CCH3 O O O ‥ CH3CH2CCHCCH3
吡咯烷
CH3 CHCH=C CH3
O (5) COCH3 C-CH3 O ① KOH ② H+
O C CH2 C O
宁夏大学化学化工学院
COC2H5 O
6
(6). C6H5CH2CHO
+
ClCHCO2C2H5 CH3
① Zn ② H /H2O
+
O C6H5CH-CH-COC2H5 OH CH3
为Reformatsky反应
宁夏大学化学化工学院 8
(1) (CH3)2C=CHCH2CH2C(CH3)=CHCH2OH ① Mg/乙醚 ② CH2—CH2 O H+
SoCl2
(CH3)2C=CHCH2CH2C(CH3)=CHCH2Cl CrO3-吡啶 参P274 Ag+(NH3)2 C2H5OH H2SO4
(CH3)2C=CHCH2CH2C(CH3)=CHCH2-CH2CH2OH
5
宁夏大学化学化工学院
O NaOC2H5 O C2H5OC C O COC2H5
(2). CH2=CHCOCH=CH2
+
CH2(CO2C2H5)2
(3).
CO2H
2LiN[CH(CH3)2]2 Li
O CO-Li+
①CH3I ②H 2O
O COH CH3
CN
(4) . (CH3)2CHCHO
+
NCCH 2CO2C2H5
解: CH2(COC2H5)2 CH3 O
① NaOC2H5 ② CH2=CHCH2Cl ①
-
O CH2=CH-CH2-CH(COC2H5)2 OH CH3 CH2=CHCH2CHCO2H ① NaOC2H5 ② CH3I
CH2=CH-CH2-C - (COC2H5)2
② H+, △ -CO2
O (2). O 解: O CH2COH O O H
+ -
O OH
CH3-C-CH-C-OC2H5 CH3
CH3
CH2CH=C-CH2CH2-CH=C(CH3)2 ② H , △ -CO2
CH3CCH2-CH2CH=C-CH2CH2CH=C(CH3)2
7. 由丙二酸二乙酯或乙酰乙酸乙酯为起始原料合成:
CH3 (1). CH2=CHCH2CHCO2H
宁夏大学化学化工学院 9
(CH3)2C=CHCH2CH2C(CH3)=CHCH2-CH2CHO
O
(CH3)2C=CHCH2CH2C(CH3)=CHCH2CH2COC2H5
O
O NaOC2H5
O
O
(CH3)2C=CHCH2CH2C(CH3)=CHCH2Cl
(2). CH3CCH2COC2H5 O O
CH3CCH-CHOC2H5 ①
宁夏大学化学化工学院 7
O
O ① NaOC2H5 ②CH2—CH2 O
O CH3 O CH3C—C—C
O CH3 O
解:
CH3CCH-C-OC2H5 CH3
O
O CH3 O CH3-C-C C-OC2H5 CH2CH2-O-
CH2—CH2
CH3-C-C O C-OC2H5
O CH3 O CH3-C-C-C-OC2H5 H OC2H5 -OC2H5
‥ CHCO2C2H5 O CH-COC2H5
O CH-COC2H5 OCH=C-OC2H5
O CH-COC2H5
Cl 碱性: ‥ CHCO2C2H5 〉 ‥ CHCO2C2H5
宁夏大学化学化工学院
3
2. 按生成烯醇式难易程度排列下列化合物。
O CH2CH3 O O CH=CH2 O O O
A
O 解: CH=CH2 O
CH2—CH2 O
-
O CH3 CH-C-CH
C-OC2H5
-OC2H5
a CH3C—C—C
b O CH3 O O
O CH2CH2
6.设计合成路线 把牻牛儿醇转化为下列化合物。 (CH3)2C=CHCH2CH2C(CH3)=CHCH2OH
CH2—CH2 d c
牻牛儿醇
(1) (CH3)2C=CHCH2CH2C(CH3)=CHCH2CH2CO2C2H5 (2) (CH3)2C=CHCH2CH2C(CH3)=CHCH2CH2COCH3
(7). C H CH CHO 6 5 2 NaOC2H5 CH3 O CH2—CH—C—COC2H5 O
+ ClHCCO2C2H5 CH3
(8). O
O O + CH3CC6H5
O ① NaOC2H5 ② H+
O
CH2CH2CH2-C-CH2-C-C6H5 OH
5. 2-甲基-3-丁酮酸乙酯在乙醇中用乙醇钠处理后加入环氧乙烷得到一个化合物。这 个化合物的分子式为C7H10O3 它的1HNMR数据为δ1.7(三重峰,2H),δ1.3(单峰, 3H),δ2.1(单峰,3H),δ3.9(三重峰,2H)。写出这个化合物的结构式和反应机 理。
B
O
C
O CH2CH3 O
〉
A
〉
O
B
C
4
宁夏大学化学Biblioteka 工学院3. 3-环己烯酮在催化作用下与2-环己烯酮存在以下平衡, 写出它们相互转化的机理
O O H+
O O H+ -H6 H6 Hα -Hα + O H+
解:
4. 完成下列反应式:
(1). C5H6COCH2CH3 + HCO2C2H5 ①NaOC2H5 ②H+ O C6H5C-CH-CHO CH3
宁夏大学化学化工学院
O CH2COH O + O CH2(COC2H5)2 O C2H5OC O H
10
O
合成: C2H5O
O
O + O CH2=CHCH=O
NaOC2H5
O C2H5OC
O O
O ① NaOC2H5 ②CH2(CO2C2H5)2 C2H5O
O
O O
H
NaOC2H5
C2H5O O
CH(COC2H5)2
