高中化学原电池知识点总结教学内容
(完整word版)高中化学原电池知识点总结
(完满word 版)高中化学原电池知识点总结 1 / 1
选修四 第四章 电化学基础
第一节 原电池
1.定义:把化学能转变成电能的装置
2.实质:一个能自觉进行的氧化还原反应。
3.构成条件:
( 1)两个活性不同样的金属(其中一种可以为非金属,即作导体用)作电极。
( 2)两电极插入电解质溶液中。
( 3)形成闭合回路。
(两电极外线用导线连接,可以接用电器。
)
( 4)自觉地发生氧化还原反应
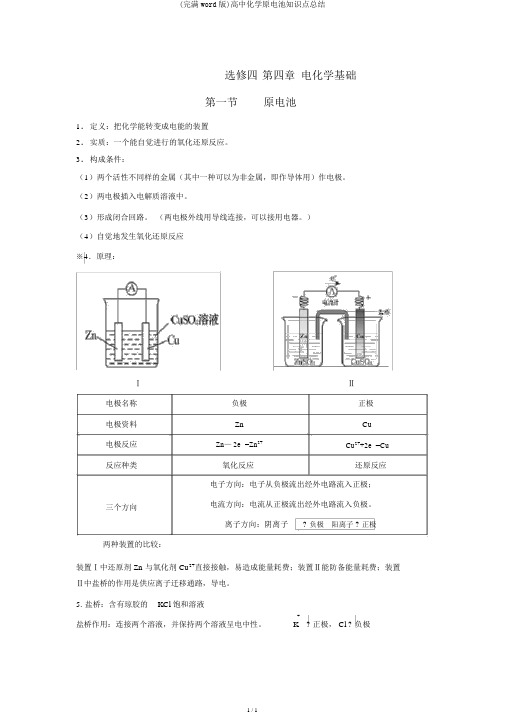
※ 4.原理:
Ⅰ
Ⅱ 电极名称
负极 正极 电极资料
Zn Cu 电极反应
Zn — 2e - =Zn 2+ Cu 2++2e - =Cu 反应种类
氧化反应 还原反应 电子方向:电子从负极流出经外电路流入正极;
三个方向 电流方向:电流从正极流出经外电路流入负极。
离子方向:阴离子
? 负极 阳离子 ? 正极 两种装置的比较:
装置Ⅰ中还原剂 Zn 与氧化剂 Cu 2+直接接触,易造成能量耗费;装置Ⅱ能防备能量耗费;装置Ⅱ中盐桥的作用是供应离子迁移通路,导电。
5. 盐桥:含有琼胶的 KCl 饱和溶液
盐桥作用:连接两个溶液,并保持两个溶液呈电中性。
+ - ? 负极
K ? 正极, Cl。
高中化学人教版选修四第41课《原电池》讲解稿

高中化学人教版选修四第41课《原电池》讲解稿一、引言本课我们将学习原电池的相关知识。
原电池是一种将化学能转化为电能的装置,广泛应用于我们的日常生活和工业生产中。
二、原电池的构成和工作原理原电池由两个半电池和电解质组成。
半电池分为阳极和阴极,电解质则负责传递离子。
当阳极和阴极通过电解质相连时,化学反应会导致电子在电路中流动,产生电流。
三、原电池的种类1. 干电池干电池是一种常见的原电池,它使用固态或半固态的电解质。
干电池具有体积小、重量轻、使用方便等特点,广泛应用于电子设备、玩具等领域。
2. 燃料电池燃料电池是一种利用化学能直接转化为电能的装置。
它使用可燃性物质(如氢气、甲醇等)作为燃料,通过与氧气发生反应产生电能。
燃料电池具有高能量转化效率、环保等优点,在汽车、航空航天等领域有着广泛的应用前景。
四、原电池的应用1. 电子设备原电池广泛应用于各种电子设备,如手持式电子产品、遥控器、闹钟等。
干电池由于便携性好且寿命较长,成为这些设备的常用电源。
2. 交通工具燃料电池作为一种新型的清洁能源装置,被广泛应用于汽车、船舶、飞机等交通工具。
燃料电池车辆具有零排放、低噪音等特点,有望成为未来交通工具的主流。
五、总结原电池作为一种将化学能转化为电能的装置,在我们的生活和工业生产中扮演着重要角色。
通过学习本课,我们了解了原电池的构成和工作原理,以及干电池和燃料电池的种类和应用领域。
希望同学们能够将所学知识应用到实际生活中,进一步加深对原电池的理解。
谢谢!。
高中化学《原电池和电解池》知识点总结!

高中化学《原电池和电解池》知识点总结!一、理解掌握原电池和电解池的构成条件和工作原理二、掌握电解反应产物及电解时溶液pH值的变化规律及有关电化学的计算1、要判断电解产物是什么必须理解溶液中离子放电顺序,阴极放电的总是溶液中的阳离子,与电极材料无关。
放电顺序是若是非惰性电极作阳极,则是电极本身失电子。
要明确溶液中阴阳离子的放电顺序,有时还需兼顾到溶液的离子浓度。
如果离子浓度相差十分悬殊的情况下,离子浓度大的有可能先放电。
如理论上H+的放电能力大于Fe2+、Zn2+,但在电解浓度大的硫酸亚铁或硫酸锌溶液时,由于溶液[Fe2+]或[Zn2+]>>[H+],则先在阴极上放电的是Fe2+或Zn2+,因此,阴极上的主要产物则为Fe和Zn。
但在水溶液中,Al3+、Mg2+、Na+等是不会在阴极上放电的。
2、电解时溶液pH值的变化规律电解质溶液在电解过程中,有时溶液pH值会发生变化。
判断电解质溶液的pH值变化,有时可以从电解产物上去看。
①若电解时阴极上产生H2,阳极上无O2产生,电解后溶液pH值增大;②若阴极上无H2,阳极上产生O2,则电解后溶液pH值减小;③若阴极上有H2,阳极上有O2,且,则有三种情况:a如果原溶液为中性溶液,则电解后pH值不变;b如果原溶液是酸溶液,则pH值变小;c如果原溶液为碱溶液,则pH值变大;④若阴极上无H2,阳极上无O2产生,电解后溶液的pH可能也会发生变化。
如电解CuCl2溶液(CuCl2溶液由于Cu2+水解显酸性),一旦CuCl2全部电解完,pH值会变大,成中性溶液。
3、进行有关电化学计算,如计算电极析出产物的质量或质量比,溶液pH值或推断金属原子量等时,一定要紧紧抓住阴阳极或正负极等电极反应中得失电子数相等这一规律。
三、理解金属腐蚀的本质及不同情况,了解用电化学原理在实际生活生产中的应用1、金属的腐蚀和防护(1)金属腐蚀的实质是铁等金属原子失去电子而被氧化成金属阳离子的过程,可分为化学腐蚀和电化学腐蚀。
高中化学原电池知识点归纳

高中化学原电池知识点归纳原电池是指在化学反应中产生电场和电势差,利用化学能转化为电能的一类电池。
原电池的基本特点是,所产生的电能依靠化学反应而非外界能源,因此具有自主性。
下面将介绍原电池的知识点。
1. 原电池的构成原电池由两种不同金属和一种离子溶解物组成。
其中,一种金属作为负极,另一种金属则作为正极,溶解物则是电解质。
另外还有一种被称作“盐桥”的物质,可以将电池内部的溶液连结起来,使其处于电中性状态。
2. 电解质电解质是指能支持正离子和负离子之间的化学反应,并与电子交换的物质。
在原电池中,电解质经过电解作用后将被氧化或还原,从而释放或吸收电子,最终导致电荷分离和电势差的产生。
3. 电动势电动势是指原电池在不连接外部电路时所能够产生的电势差。
在原电池中,电荷得以沿着电场线进行传递,而电电势则表示这些电荷在经过电路时所能够产生的功率与所消耗的能量之比。
这比值就是电势差。
4. 极性反转在某些原电池中,可能会出现极性反转的情况。
这是由于在电池反应中,正负极上生成的电荷有可能会被再次还原或氧化,从而导致原来的电势差发生逆转。
5. 电极反应在原电池中,电极反应是化学反应的本质。
它是指在电极表面,金属和离子之间发生的化学变化。
对于不同的原电池,电极反应也各不相同。
6. 阻滞电池当原电池中的一种电极和电解质发生反应时,有可能会形成一些难以传递的物质,从而影响电池的正常运行。
这种情况下,电池无法提供足够的电流,被称为阻滞电池。
7. 废旧电池的回收废旧电池中所含有的金属和化学物质对环境和人类健康都有一定的危害。
因此,对于废旧电池的回收和处理是必要的。
一般情况下,回收废旧电池的方法包括物理分拣、化学处理、电化学处理等。
总而言之,原电池是一种在化学反应中产生电场和电势差的电池,具有自主性。
它由两种不同金属和一种电解质组成,通过电极反应来产生电能。
废旧电池的回收和处理是非常重要的。
高中化学知识点总结3:电化学

高中化学知识点总结-----电化学一、原电池1.概念和反应本质:原电池是把化学能转化为电能的装置,其反应本质是氧化还原反应。
2.原电池的构成条件(1)一看反应:能自发进行的氧化还原反应(且为放热反应)。
(2)二看两电极:一般是活泼性不同的两电极。
(但在燃料电池中两电极都为Pt 铂电极,不参与反应,有很强的催化活性,起导电作用)(3)三看是否形成闭合回路,形成闭合回路需要两电极直接或用导线相连插入电解质溶液中。
(4)四看电解质溶液或熔融电解质;3.原电池的工作原理:以锌铜原电池为例(Cu-Zn-CuSO 4) 单液原电池、 双液原电池负极(锌片):Zn -2e -===Zn 2+(氧化反应)(1) 正极(铜片):Cu 2++2e -===Cu (还原反应)电池反应:Zn + CuSO 4 = Cu + ZnSO 4(2)电子流向:由负极(Zn 片)沿导线流向正极(Cu 片)(3)离子移向:正正负负(4)盐桥 ①盐桥中通常装有琼胶的KCl (KNO 3)饱和溶液。
②盐桥的作用:平衡电荷,形成闭合回路③盐桥中离子移向:正正负负。
可逆反应达到平衡时,v (正)=v (逆),电流表指针归0.(5)单液原电池的缺点:负极与电解液不可避免会接触反应,在负极析出Cu ,形成无数微小的Cu-Zn 原电池,造成原电池效率不高,电流在较短时间内就会衰减。
(6)双液原电池优点:把氧化反应和还原反应彻底分开,形成两个半电池,避免负极与电解液直接反应。
一般电极材料与相应容器中电解液的阳离子相同。
4、原电池正负极的判断方法强调:负极首先是能与电解液直接反应,其次为较活泼的一极。
如:Mg-Al-NaOH 原电池中,Al 作负极。
Al-Cu-浓HNO 3原电池中,Cu 作负极。
另外还可以根据:(1) 原电池的工作原理: 负失氧化阴移向,正得还原阳移向。
(2)根据现象判断。
金属溶解质量减轻的一极为负极,有金属析出质量增加或有气体产生的一极为正极。
高一下化学原电池知识点

高一下化学原电池知识点电池是我们日常生活中经常使用的电源装置之一,它能够将化学能转化为电能,并为我们的电子设备提供稳定可靠的能量。
而要了解电池的原理,就需要掌握一些基础的化学知识。
本文将为大家介绍高一下学期化学中关于原电池的知识点。
1. 电池的基本结构电池的基本结构包括两个电极和电解质。
其中正极是指能够供给电子的电极,通常由金属或其化合物构成;而负极则是指能够接受电子的电极,也可由金属或其化合物组成。
电解质则是指能够提供离子,并在电池中维持电中性的物质。
2. 氧化还原反应与电池电池的工作原理与氧化还原反应密切相关。
在电池中,正极发生氧化反应,负极发生还原反应。
通常情况下,正极的反应是氧化反应,而负极的反应则是还原反应。
这两个半反应之间通过电子流相连,形成了电路。
3. 电池的电动势电动势是电池输出电流的推动力,是衡量电池正负极之间电能转化效果的物理量。
它通常以电势差的形式进行表示,单位是伏特(V)。
电动势取决于电池中发生的化学反应特性,可以通过标准电极电势来计算。
4. 电池的使用寿命与容量电池的使用寿命是指电池能够持续供电的时间,取决于电池内的活性物质耗尽程度。
而容量则是指电池能够存储的电荷量,通常以安时(Ah)为单位。
一般来说,电池的容量越大,使用时间越长。
5. 常见的原电池在日常生活中,我们常见的原电池有铅酸蓄电池、锌-碳干电池和碱性电池。
铅酸蓄电池主要用于汽车起动等高功率设备;锌-碳干电池常用于手电筒、遥控器等低功率设备;碱性电池则是目前应用最广泛的一种常规电池,适用于各种电子设备。
6. 原电池的环保问题尽管原电池在我们的生活中发挥着重要的作用,但同时也产生了一系列的环保问题。
原电池中的重金属如铅、汞等对环境具有一定的污染作用,因此在使用后需要进行妥善处理,不可随意丢弃。
总结:原电池是常用的电源装置,利用氧化还原反应将化学能转化为电能。
了解电池的基本结构、电动势、使用寿命和容量等知识,对于我们合理使用和处理电池具有重要意义。
高二化学知识点总结(电化学)

高二化学知识点总结(电化学)(经典版)编制人:__________________审核人:__________________审批人:__________________编制单位:__________________编制时间:____年____月____日序言下载提示:该文档是本店铺精心编制而成的,希望大家下载后,能够帮助大家解决实际问题。
文档下载后可定制修改,请根据实际需要进行调整和使用,谢谢!并且,本店铺为大家提供各种类型的经典范文,如演讲稿、总结报告、合同协议、方案大全、工作计划、学习计划、条据书信、致辞讲话、教学资料、作文大全、其他范文等等,想了解不同范文格式和写法,敬请关注!Download tips: This document is carefully compiled by this editor. I hope that after you download it, it can help you solve practical problems. The document can be customized and modified after downloading, please adjust and use it according to actual needs, thank you!In addition, this shop provides you with various types of classic sample essays, such as speech drafts, summary reports, contract agreements, project plans, work plans, study plans, letter letters, speeches, teaching materials, essays, other sample essays, etc. Want to know the format and writing of different sample essays, so stay tuned!高二化学知识点总结(电化学)化学难在哪儿?面对三大突出特点,考试主要面临三大思维障碍。
高考化学原电池必背知识点

高考化学原电池必背知识点1. 电池的基本概念:电池是一种能够将化学能直接转化为电能的装置。
它由正极、负极和电解质构成。
在正极发生氧化反应产生电子,电子通过外部电路流向负极,在负极发生还原反应,与离子结合形成化合物。
这种电子的流动产生了电流,实现了能量的转化。
2. 电池的分类:根据正负极材料的性质,电池可分为原电池和储能电池。
原电池是一次性使用的,电池内的化学反应一旦停止,就无法再产生电流。
储能电池则可以通过充电和放电的循环来反复使用。
3. 原电池的基本原理:原电池是一种将金属与非金属之间的氧化还原反应转化为电能的装置。
它由两种电极(正极和负极)和电解质组成。
正极是一个易被氧化的物质,负极是一个易被还原的物质。
在电解质溶液中,正极发生氧化反应,产生电子并释放金属离子,负极接收电子,并与离子结合形成金属。
这样电池内就形成了一个电势差,电子会从正极流向负极,从而产生电流。
4. 原电池的电势差:原电池的电势差可以用标准电极电势来表示。
标准电极电势是指在标准条件下,某种物质在电解质溶液中发生氧化或还原反应时所释放或吸收的电能。
标准电极电势可以根据氧化还原反应的方程式计算得出,正极的标准电极电势减去负极的标准电极电势就是原电池的标准电动势。
5. 原电池的使用注意事项:(1) 为了保证原电池能够正常工作,应避免电池短路或过载。
(2) 储存和使用电池时,要避免受热或受潮,以免损坏电池。
(3) 在电池使用完后,应进行分类回收,以保护环境。
6. 常见的原电池:(1) 干电池:干电池是一种常见的原电池,它内部使用固体或半固体的电解质。
干电池常用于电子设备、遥控器等日常用品中。
(2) 锂离子电池:锂离子电池是一种高效、长寿命的原电池,因其高能量密度和较低自放电率而被广泛使用。
它常用于手机、电脑等电子设备中。
(3) 镍氢电池:镍氢电池是一种环保、经济的原电池,具有较长的使用寿命和较低的自放电率。
它常用于数码相机、电动工具等设备中。
高中化学原电池知识点总结

高中化学原电池知识点总结高中有关原电池知识点的一、构成原电池的条件构成原电池的条件有:(1)电极材料。
两种金属活动性不同的金属或金属和其它导电性(非金属或某些氧化物等);(2)两电极必须浸没在电解质溶液中;(3)两电极之间要用导线连接,形成闭合回路。
说明:①一般来说,能与电解质溶液中的某种成分发生氧化反应的是原电池的负极。
②很活泼的金属单质一般不作做原电池的负极,如K、Na、Ca等。
二、原电池正负极的判断(1)由组成原电池的两极材料判断:一般来说,较活泼的或能和电解质溶液反应的金属为负极,较不活泼的金属或能导电的非金属为正极。
但具体情况还要看电解质溶液,如镁、铝电极在稀硫酸在中构成原电池,镁为负极,铝为正极;但镁、铝电极在氢氧化钠溶液中形成原电池时,由于是铝和氢氧化钠溶液发生反应,失去电子,因此铝为负极,镁为正极。
(2)根据外电路电流的方向或电子的流向判断:在原电池的外电路,电流由正极流向负极,电子由负极流向正极。
(3)根据内电路离子的移动方向判断:在原电池电解质溶液中,阳离子移向正极,阴离子移向负极。
(4)根据原电池两极发生的化学反应判断:原电池中,负极总是发生氧化反应,正极总是发生还原反应。
因此可以根据总化学方程式中化合价的升降来判断。
(5)根据电极质量的变化判断:原电池工作后,若某一极质量增加,说明溶液中的阳离子在该电极得电子,该电极为正极,活泼性较弱;如果某一电极质量减轻,说明该电极溶解,电极为负极,活泼性较强。
(6)根据电极上产生的气体判断:原电池工作后,如果一电极上产生气体,通常是因为该电极发生了析出氢的反应,说明该电极为正极,活动性较弱。
(7)根据某电极附近pH的变化判断析氢或吸氧的电极反应发生后,均能使该电极附近电解质溶液的pH增大,因而原电池工作后,该电极附近的pH 增大了,说明该电极为正极,金属活动性较弱。
三、电极反应式的书写(1)准确判断原电池的正负极是书写电极反应的关键如果原电池的正负极判断失误,电极反应式的书写一定错误。
高中化学原电池和电解池全部知识点

高中化学原电池和电解池全部知识点
1. 定义:原电池是将两种不同的金属通过电解质连接起来,利用金属内部化学反应来产生电能的装置。
2. 构成:原电池由阳极、阴极和电解质三部分组成。
3. 电子流动方向:电子从阳极流向阴极,离子从阴极流向阳极。
4. 电位、电动势和电化学势:原电池产生的电动势取决于电极材料、电解质及其浓度等因素。
电动势表示成“标准电动势”,单位是伏(V)。
电动势越大,产生的电化学反应越强,电池反应速度越快。
5. 活性序列:金属的活性大小可以通过活性序列进行比较。
活性序列越靠前的金属,越容易氧化,即容易成为阳极;而活性序列靠后的金属越容易被还原,成为阴极。
电解池:
1. 定义:电解池是将电能转化为化学能的装置,可以将电能作用于电解质溶液中的离子,促使化学反应发生。
2. 构成:电解池由阳极、阴极和电解质三部分组成。
3. 电子流动方向:电子从外部电源流向阴极,离子从电解质中向阳极移动。
4. 电解质:电解质是指能在水溶液中分解成离子的化合物。
5. 电解反应:电解池中发生的反应取决于电解质种类和电压。
电解质中的阳离子被还原在阴极上,而阴离子则被氧化在阳极上。
6. 法拉第电解定律:电解过程中的物质电量与通过电解质的电量成正比,电量称为电容量,单位是库仑(C)。
高考化学原电池知识点归纳

高考化学原电池知识点归纳原电池也叫做原电池,是一种将化学能直接转化为电能的装置。
在原电池中,化学反应会使两种不同的金属发生电子转移,产生电流。
1. 原电池的构成:原电池由两个不同金属电极和电解质组成。
通常情况下,一个金属是阳极,即电子流动的起始点,另一个金属是阴极,即电子流动的终点。
电解质可以是固态、液态或者是溶液。
2. 原电池的工作原理:原电池中的化学反应会引发电子的流动。
在阳极处,金属会氧化并丧失电子,成为离子溶解在电解质中。
离子在电解质中移动到阴极处,与电解质中的离子结合,使得金属还原并收回电子。
电子在两个电极之间的外部电路中流动,从而形成了电流。
3. 原电池的电势差:原电池的电势差是指在开路状态下,两个电极之间的电位差。
电势差可以通过将电压计连接到电池的两个极端来测量。
4. 原电池的电动势:原电池的电动势是指在工作状态下,两个电极之间的电位差。
电动势可以通过将电压计连接到电池的两个极端并接通外部电路来测量。
5. 原电池的表示方法:原电池可以使用标准电动势表(如电池电势序列)来表示。
标准电动势是相对于标准氢电极的电势测量值。
6. 原电池的电源类型:根据电解质状态的不同,原电池可以分为干电池和湿电池。
干电池中,电解质是固体,而在湿电池中,电解质是液体或者溶液。
7. 原电池的应用:原电池广泛应用于日常生活和工业中,例如电池驱动的手电筒、遥控器、闹钟等。
它们还被用于电子设备、交通工具等领域。
8. 原电池的使用注意事项:在使用原电池时,需要注意保持电极清洁、避免电池反向连接、避免短路,以避免电池损坏或者发生危险。
以上是关于化学原电池的一些基本知识点的归纳总结。
了解以上知识点可以帮助我们更好地理解原电池的工作原理、鉴别标准以及使用方法。
在化学考试中掌握这些知识,也能够更好地回答相关的试题。
继续写:9. 原电池的化学反应:不同的原电池采用不同的化学反应。
常见的原电池包括锌-银电池、锌-铜电池、锌-锰电池等。
高中化学原电池知识点归纳

高中化学原电池知识点归纳原电池是指能够自行产生电能的电池,它的能量来自于化学反应。
在高中化学中,学生需要了解如何根据化学反应原理来设计和构造原电池,在实验中探究原电池的性质和应用。
1. 原电池的基本构造原电池主要由阳极、阴极和电解质三个部分构成。
阳极一般为金属,其在电化学反应中被氧化。
阴极一般为金属或还原剂,其在电化学反应中被还原。
电解质则是负责传递离子的介质,一般为电解质溶液或固体电解质。
2. 原电池的工作原理原电池的工作原理主要是通过化学反应将化学能转化为电能。
在阳极上进行氧化反应,产生电子并释放出阳离子;在阴极上进行还原反应,吸收电子并接受阴离子;电解质中的离子则负责在阳极和阴极之间传递电荷。
3. 原电池的电势差原电池电势差是指原电池输出电压的大小,其取决于原电池的反应物浓度、温度、压力、电极表面积和电极材质等因素。
一般来说,原电池的电势差越大,其输出电压越高,反应也越强烈。
4. 原电池的应用原电池广泛应用于各个领域,如电子产品、汽车、航空航天、医疗器械、农业、能源等。
其中,锂离子电池、铅酸电池、镍氢电池等原电池是目前应用最广泛的电池类型。
5. 原电池的分类原电池可以按照反应方式、工作方式和电解质状态等多种方式进行分类。
按照反应方式可以分为氧化还原电池、燃料电池、光电池等;按照工作方式可以分为干电池、湿电池、固体电池等;按照电解质状态可以分为液态电池、固态电池等。
6. 原电池的制备原电池的制备一般分为实验室制备和工业制备两种。
实验室制备一般采用简单的装置和操作步骤,通过控制反应条件来达到不同的反应效果。
工业制备则需要考虑生产效率、能源消耗、成本控制等因素,采用更加先进的设备和技术来提高制备效率和产品质量。
7. 原电池的环保问题原电池在使用过程中会产生一些有害物质,对环境造成一定的影响。
例如,铅酸电池会产生铅污染,锂离子电池会产生电池废弃物等。
因此,研究如何减少或处理电池废弃物是解决原电池环保问题的重要途径。
高中化学教案《原电池》

高中化学教案《原电池》主题:原电池
一、教学目标:
1. 理解原电池的构造和工作原理;
2. 掌握原电池中正负极的原理及其化学反应;
3. 能够解释原电池在电化学方面的应用。
二、教学重点:
1. 原电池的构造和工作原理;
2. 原电池中的正负极化学反应。
三、教学内容:
1. 原电池的定义及构造;
2. 原电池的工作原理;
3. 原电池中正负极的化学反应。
四、教学过程:
1. 导入新知识:介绍原电池的定义及其在生活中的应用;
2. 学习原电池的构造及工作原理;
3. 分析原电池中正负极的化学反应;
4. 进行小组讨论,探讨原电池的优缺点及改进方向;
5. 总结课程内容,做一些相关练习。
五、教学评估:
1. 参与小组讨论,展示对原电池的理解;
2. 完成相关练习,检测对知识的掌握情况。
六、扩展阅读:
1. 《物理化学原理》;
2. 《化学电源》杂志。
七、小结:
原电池在电化学领域中有着重要的应用,通过本节课的学习,相信同学们已经掌握了原电池的构造和工作原理,以及其中的化学反应。
希望同学们能够进一步深入学习,将知识应用到实际生活和工作中。
高二化学原电池知识点总结

原电池知识点归纳小结一、原电池1、原电池的形成条件原电池的工作原理原电池反应属于放热的氧化还原反应,但区别于一般的氧化还原反应的是,电子转移不是通过氧化剂和还原剂之间的有效碰撞完成的,而是还原剂在负极上失电子发生氧化反应,电子通过外电路输送到正极上,氧化剂在正极上得电子发生还原反应,从而完成还原剂和氧化剂之间电子的转移;两极之间溶液中离子的定向移动和外部导线中电子的定向移动构成了闭合回路,使两个电极反应不断进行,发生有序的电子转移过程,产生电流,实现化学能向电能的转化;从化学反应角度看,原电池的原理是氧化还原反应中的还原剂失去的电子经导线传递给氧化剂,使氧化还原反应分别在两个电极上进行;➢原电池的构成条件有三个:1电极材料由两种金属活动性不同的金属或由金属与其他导电的材料非金属或某些氧化物等组成;2两电极必须浸泡在电解质溶液中;3两电极之间有导线连接,形成闭合回路;只要具备以上三个条件就可构成原电池;而化学电源因为要求可以提供持续而稳定的电流,所以除了必须具备原电池的三个构成条件之外,还要求有自发进行的氧化还原反应;也就是说,化学电源必须是原电池,但原电池不一定都能做化学电池;4形成前提:总反应为自发的氧化还原反应➢电极的构成: a.活泼性不同的金属—锌铜原电池,锌作负极,铜作正极;b.金属和非金属非金属必须能导电—锌锰干电池,锌作负极,石墨作正极;c.金属与化合物—铅蓄电池,铅板作负极,二氧化铅作正极;d.惰性电极—氢氧燃料电池,电极均为铂;➢电解液的选择:电解液一般要能与负极材料发生自发的氧化还原反应;➢原电池正负极判断:负极发生氧化反应,失去电子;正极发生还原反应,得到电子;电子由负极流向正极,电流由正极流向负极; 溶液中,阳离子移向正极,阴离子移向负极2、电极反应方程式的书写正确书写电极反应式1列出正、负电极上的反应物质,在等式的两边分别写出反应物和生成物;2标明电子的得失;3使质量守恒;电极反应式书写时注意:①负极反应生成物的阳离子与电解质溶液中的阴离子是否共存;若不共存,则该电解质溶液中的阴离子应该写入负极反应式;②若正极上的反应物质是O2,且电解质溶液为中性或碱性,则H2O必须写入正极反应式,且生成物为OH-;若电解液为酸性,则H+必须写入反应式中,生成物为H2O;③电极反应式的书写必须遵循离子方程式的书写要求;4正负极反应式相加得到电池反应的总的化学方程式;若能写出总反应式,可以减去较易写出的电极反应式,从而写出较难书写的电极方程式;注意相加减时电子得失数目要相等;负极:活泼金属失电子,看阳离子能否在电解液中大量存在;如果金属阳离子不能与电解液中的离子共存,则进行进一步的反应;例:甲烷燃料电池中,电解液为KOH,负极甲烷失8个电子生成CO2和H2O,但CO2不能与OH-共存,要进一步反应生成碳酸根;正极:①当负极材料能与电解液直接反应时,溶液中的阳离子得电子;例:锌铜原电池中,电解液为HCl,正极H+得电子生成H2;②当负极材料不能与电解液反应时,溶解在电解液中的O2得电子;如果电解液呈酸性, O2+4e-+4H+==2H2O;如果电解液呈中性或碱性,O2+4e-+2H2O==4OH-;➢特殊情况:1、Mg-Al-NaOH,Al作负极;负极:Al-3e-+4OH- = AlO2-+2H2O;正极:2H2O+2e- = H2↑+2OH-2、Cu-Al-HNO3,Cu作负极;注意:Fe作负极时,氧化产物是Fe2+而不可能是Fe3+;肼N2H4和NH3的电池反应产物是H2O和N2无论是总反应,还是电极反应,都必须满足电子守恒、电荷守恒、质量守恒;➢pH变化规律a、电极周围:消耗OH-H+,则电极周围溶液的pH减小增大;反应生成OH-H+,则电极周围溶液的pH增大减小;b、溶液:若总反应的结果是消耗OH-H+,则溶液的pH减小增大;若总反应的结果是生成OH-H+,则溶液的pH增大减小;若总反应消耗和生成OH-H+的物质的量相等,则溶液的pH由溶液的酸碱性决定,溶液呈碱性则pH增大,溶液呈酸性则pH减小,溶液呈中性则pH不变;3、原电池表示方法原电池的组成用图示表达,未免过于麻烦;为书写简便,原电池的装置常用方便而科学的符号来表示;其写法习惯上遵循如下几点规定:1. 一般把负极电池符号表示式的左边,正极写在电池符号表示式的右边;2. 以化学式表示电池中各物质的组成,溶液要标上活度或浓度mol/L,若为气体物质应注明其分压Pa,还应标明当时的温度;如不写出,则温度为298.15K,气体分压为101.325kPa,溶液浓度为1mol/L;3. 以符号“∣”表示不同物相之间的接界,用“‖”表示盐桥;同一相中的不同物质之间用“,”隔开;4. 非金属或气体不导电,因此非金属元素在不同氧化值时构成的氧化还原电对作半电池时,需外加惰性导体如铂或石墨等做电极导体;其中,惰性导体不参与电极反应,只起导电输送或接送电子的作用,故称为“惰性”电极;按上述规定,Cu-Zn原电池可用如下电池符号表示:-Zns∣Zn2+C‖Cu2+C∣Cus +理论上,任何氧化还原反应都可以设计成原电池,例如反应: Cl2+ 2I-═ 2Cl-+I2此反应可分解为两个半电池反应:负极:2I-═ I2+ 2e-氧化反应正极:Cl2+2e-═ 2Cl-还原反应该原电池的符号为:-Pt∣I2s∣I- C‖Cl- C∣Cl2PCL2 ∣Pt+二两类原电池腐蚀1、吸氧腐蚀:金属在酸性很弱或中性溶液里,空气里的氧气溶解于金属表面水膜中而发生的电化腐蚀;例如钢铁在接近中性的潮湿的空气中腐蚀属于吸氧腐蚀,其电极反应如下:负极Fe:2Fe - 4e = 2Fe2+ 正极C:2H2O + O2+ 4e = 4OH-钢铁等金属的电化腐蚀主要是吸氧腐蚀.2、析氢腐蚀:在酸性较强的溶液中发生电化腐蚀时放出氢气的腐蚀;在钢铁制品中一般都含有碳;在潮湿空气中,钢铁表面会吸附水汽而形成一层薄薄的水膜;水膜中溶有二氧化碳后就变成一种电解质溶液,使水里的H+增多;是就构成无数个以铁为负极、碳为正极、酸性水膜为电解质溶液的微小原电池;这些原电池里发生的氧化还原反应是:负极铁:铁被氧化Fe-2e=Fe2+;正极碳:溶液中的H+被还原2H++2e=H2↑ 这样就形成无数的微小原电池;最后氢气在碳的表面放出,铁被腐蚀,所以叫析氢腐蚀;析氢腐蚀定义金属在酸性较强的溶液中发生电化腐蚀时放出氢气,这种腐蚀叫做析氢腐蚀;三、常用原电池方程式1.Cu─H2SO4─Zn原电池正极:2H++ 2e-→ H2↑ 负极:Zn - 2e-→ Zn2+总反应式:Zn + 2H+= Zn2++ H2↑ 2.Cu─FeCl3─C原电池正极:2Fe3++ 2e-→ 2Fe2+负极:Cu - 2e-→ Cu2+总反应式:2Fe3++ Cu =2Fe2++ Cu2+3.钢铁在潮湿的空气中发生吸氧腐蚀正极:O2+2H2O+4e-→4OH-负极:2Fe-4e- →2Fe2+总反应式:2Fe + O2+ 2H2O == 2FeOH2 4.Al─NaOH─Mg原电池正极:6H2O + 6e- → 3H2↑ + 6OH- 负极:2Al - 6e- + 8OH- → 2AlO2- + 4H2O总反应式:2Al+2OH-+2H2O==2AlO2- + 3H2↑5.熔融碳酸盐燃料电池Li2CO3和Na2CO3熔融盐作电解液,CO作燃料:正极:O2+ 2CO2+ 4e- → 2CO32- 持续补充CO2气体负极:2CO + 2CO32- - 4e- → 4CO2总反应式:2CO + O2= 2CO2四、几种常见的电池化学电源1、一次电池干电池放电之后不能充电,内部的氧化还原反应是不可逆的;碱性锌锰电池构成:负极是锌,正极是MnO2,电解质是KOH负极:Zn+2OH--2e-=ZnOH2;正极:2MnO2+2H2O+2e-=2MnOOH+2OH-总反应式:Zn+2MnO2+2H2O=2MnOOH+ZnOH22、二次电池①铅蓄电池放电电极反应:负极:Pbs+SO42-aq-2e-=PbSO4s;正极:PbO2s+4H+aq+SO42-aq+2e-=PbSO4s+2H2Ol总反应式:Pbs+PbO2s+2H2SO4aq=2PbSO4s+2H2Ol充电电极反应:阳极:PbSO4s+2H2Ol-2e-=PbO2s+4H+aq+SO42-aq;阴极:PbSO4s+2e-=Pbs+SO42-aq总反应:2PbSO4s+2H2Ol=Pbs+PbO2s+2H2SO4aq总反应方程式:Pb s+ PbO2s +2H2SO4aq 2PbSO4s +2H2Ol说明:a负极阴极正极阳极b电池的正负极分别和电源的正负极相连c各极的pH变化看各电极反应,电池的pH变化看电池总反应②镍一镉碱性蓄电池负极:Cd+2OH--2e-=CdOH2;正极:2NiOOH+2H2O+2e-=2NiOH2+2OH-总反应式:Cd +2NiOOH+2H2O 2NiOH2+ CdOH23、燃料电池电池电极反应酸性电解质碱性电解质氢氧燃料电池负极2H2-4e-=4H+2H2+4OH--4e-=4H2O 正极O2+4H++4e-=2H2O O2+2H2O+4e-=4OH-总反应2H2+O2=2H2O 2H2+O2=2H2O甲烷燃料电池负极CH4 + 2H2O-8e-=CO2 + 8H+CH4+10OH--8e-=CO32-+7H2O 正极2O2 + 8H+ + 8e-=4H2O 2O2+4H2O+8e-=8OH-总反应CH4 + 2O2 = CO2 + 2H2O CH4+2O2+2KOH=K2CO3+3H2O甲醇燃料电池负极2CH3OH + 2H2O-12e-= 2CO2 + 12H+2CH3OH +16OH--12e-=2CO32-+12H2O 正极3O2 +12H+ +12e-=6H2O 3O2+6H2O+12e-=12OH-总反应2CH3OH + 3O2 = 2CO2 + 4H2O 2CH3OH+3O2+4KOH=2K2CO3+6H2O。
高中化学选修4原电池教案

高中化学选修4原电池教案
一、教学内容
本课程主要介绍原电池的概念、原理、结构和工作原理,以及常见原电池的类型和应用。
二、教学目标
1. 了解原电池的概念和基本原理;
2. 掌握原电池的结构和工作原理;
3. 熟悉常见原电池的类型和应用。
三、教学重点和难点
1. 原电池的结构和工作原理;
2. 常见原电池的类型和应用。
四、教学方法
1. 教师讲解结合示例;
2. 实验观察;
3. 讨论交流。
五、教学过程安排
1. 前期准备:教师准备好所需实验器材和化学试剂,确保实验顺利进行。
2. 导入环节:通过展示各种常见原电池,引导学生思考原电池的作用和应用。
3. 理论讲解:介绍原电池的概念、原理、结构和工作原理。
4. 实验操作:让学生进行原电池的制作实验,观察实验现象并记录数据。
5. 分析总结:引导学生讨论实验结果,总结原电池的特点和应用。
6. 拓展延伸:介绍一些新型原电池的发展和应用领域。
7. 总结交流:对本节课内容进行总结,答疑并征求学生意见。
六、教学评价
1. 实验结果记录;
2. 课堂表现评价;
3. 课后作业评价。
七、教学资源
1. 化学实验器材和化学试剂;
2. PPT课件;
3. 教科书和参考书籍。
八、教学反思
本课程通过实验操作和理论讲解相结合的方式,引导学生深入了解原电池的结构和工作原理,拓展学生的化学知识面,激发学生的学习兴趣。
同时,通过讨论和交流,提高学生的分析和思考能力,培养学生的实验操作和解决问题的能力。
新人教版高中化学原电池知识点考点复习资料-经典版

原电池复习一、原电池基本知识:必须掌握(两套装置、一个原理、四种化学电源)单液原电池双液原电池基本装置构成条件两极一液一连接、自发的氧化还原反应。
两极两液双连接自发的氧化还原反应。
优点电流强度大(1)能量转化率高(氧化剂和还原剂不接触)(2)电流持续、稳定缺点(1)能量转化率低(氧化剂和还原剂直接接触)(2)电流不稳定。
电流强度小工作原理电极名称判断1、由电极材料判断(通常活泼金属做负极)2、由电极反应判断(通常由电极现象判断电极反应。
如:通常质量减小的电极为负极,质量增加或有气体产生的电极为正极)3、由工作原理判断(电子、电流、离子的移动方向)电极反应式的书写负极:氧化反应+后续反应正极:还原反应+后续反应总反应式书写应用设计化学电源:(必须掌握四种化学电源电极反应式的书写)(1)锌锰碱性干电池(2)银锌纽扣电池(3)氢氧燃料电池(酸性和碱性)(4)铅蓄电池加快反应速率金属的腐蚀和保护常见的电池一一次电池1.锌锰干电池电解液?MnO2、NH4Cl?以及ZnCl2和淀粉负极:Zn - 2e == Zn2+正极:2NH4+ + 2MnO2 + 2e == 2NH3 + Mn2O3 + H2O总反应:2NH4+ + 2MnO2 + Zn == Mn2O3 + Zn2+ + 2NH3 + H2O2.碱性锌锰电池(简称碱锰电池)用KOH电解质溶液代替上述NH4Cl溶液作电解质溶液,电池的能量和放电电流都能得到显著的提高。
负极:Zn + 2OH- - 2e == Zn(OH)2正极:2MnO2 + 2H2O + 2e - == 2MnO(OH) + 2OH-3.Ag-Zn原电池(电池)负极:Zn + 2OH- - 2e== ZnO + H2O正极:Ag2O + H2O + 2 e== 2Ag + 2OH-总反应:Zn + Ag2O == ZnO + 2Ag4.Zn-空气电池电解质:KOH溶液:2Zn + 4OH- -4e= 2ZnO + 2H2O正极:O2 + 2H2O + 4e = 4OH-二1.铅蓄电池负极:Pb + SO42- - 2e == PbSO4正极:PbO2 + 4H+ + SO42- + 2e == PbSO4 + 2H2O总反应:Pb + PbO2 + 4H+ +2SO42- == 2PbSO4 + 2H2O2.碱性镍镉电池负极材料:Cd;正极材料:NiO(OH);电解质溶液:KOH溶液负极:Cd + 2OH- - 2e - == Cd(OH)2正极:2NiO(OH) + 2H2O + 2e - == 2Ni (OH)2 + 2OH-总反应:Cd +2NiO(OH) + 2H2O == Cd(OH)2 + 2Ni (OH)23.氢镍课充电电池+ 2OH- - 2e - == 2H2O正极:2NiO(OH) + 2H2O + 2e - == 2Ni (OH)2 + 2OH-总反应:H2 +2NiO(OH) == 2Ni (OH)24.锂电池Li;正极材料:石墨电解质LiAlCl4、SOCl2负极:Li - 2e== Li+正极:SOCl2 + 4e - == 4Cl- + S + SO2总反应:4Li + 2SOCl2 == 4LiCl + S + SO2三燃料电池(连续电池)1.氢氧燃料电池2H2 + O2 == 2H2O酸式负极:2H2 - 4e== 4H+正极:O2 + 4H+ + 4e == 2H2O中性:负极:2H2 - 4e== 4H+正极:O2 + H2O + 4e - == 4OH-碱式负极:2H2 +OH- - 4e -== 4H2O正极:O2 + H2O + 4e - == 4OH-2.熔融盐燃料电池电解质Li2CO3,NiCO3混合物CO为极燃气,空气和CO2为极助燃气负极:2CO + 2CO32- - 4e == 4CO2正极:O2 + 2CO2 + 4e == 2CO32-总反应:2CO + O2 == 2CO23.甲醇-氧燃料电池电解质负极:CH3OH + H2O - 6e== CO2 + 6H+正极:1.5O2 + 6H+ + 6e== 3H2O总反应:CH3OH + 1.5O2 == CO2 + 2H2O四Al-空气-海水电池Al;正极材料:Pt、Fe网负极:4Al - 12e == 4Al3+?正极:3O2 + 6H2O + 12e == 12OH-总反应:4Al +3O2 + 6H2O == 4Al(OH)3五、电极反应书写方法1.根据电池的装置书写负极:(1)若负极材料本身被氧化,其电极反应式有两种情况:一种是负极金属失电子后生成的金属阳离子不与电解质溶液的成分反应,此时的电极反应可表示为M-ne -==Mn+;另一种是负极金属失去电子后生成的金属阳离子与电解质溶液的成分反应,此时的电极反应要将金属失电子的反应、金属阳离子与电解质溶液的反应叠加在一起,如:铅蓄电池的负极反应:Pb + SO42- - 2e - == PbSO4。
原电池基本知识点总结

原电池基本知识点总结1、原电池的基本情况(1)构成:两极、一液(电解质溶液)、一回路(闭合回路)、一反应(自发实行的氧化还原反应)。
(2)能量转化形式:化学能转化为电能。
(3)电极与电极反应:较活泼的一极是负极,发生氧化反应;较不活泼的一极是正极,发生还原反应。
(4)溶液中阴、阳离子的移动方向:阳离子移向正极;阴离子移向负极。
(5)电子流向:负极(通过导线)→正极;在电解质溶液中,靠阴、阳离子发生定向移动而导电。
2、原电池电极反应规律(1)负极反应(与电极材料相关)①若为活泼电极:金属失去电子生成金属离子(注意:Fe→Fe2+);②若为惰性电极(石墨、铂):通到正极上的H2、CH4等燃料发生氧化反应;②正极反应(与电极材料无关):阳离子放电(常见阳离子的放电顺序为: H+<Cu2+< Fe3+< Ag +)或通到正极上的O2、Cl2等氧化剂发生还原反应。
3、重要原电池的的电极反应式和电池总式(1)铜—锌—稀硫酸电池负极:Zn - 2e- == Zn2+ 正极:2H+ +2e- == H2↑总反应式:Zn+ 2H+ == Zn2+ + H2↑Zn+ H2SO4== ZnSO4+ H2↑(2)铜—锌—硫酸铜溶液电池负极:Zn - 2e- == Zn2+ 正极:Cu2+ + 2e- == Cu总反应式:Zn+ Cu2+ == Zn2+ + Cu Zn+ CuSO4 == ZnSO4+ Cu(3) 铜—石墨—FeCl3溶液电池负极:Cu - 2e- == Cu2+正极:2Fe3++ 2e- == 2Fe2+总反应式:2Fe3+ + Cu == 2Fe2+ + Cu2+ 2FeCl3 + Cu == 2FeCl2+ CuCl2*(4)铅蓄电池负极:Pb+SO42--2e- == PbSO4正极:PbO2+4H++SO42- +2e- == PbSO4+2H2O电池总反应:Pb+PbO2+2H2SO4=2PbSO4+2H2O(5)氢氧燃料电池①电解质溶液为KOH溶液负极:2H2+4OH--4e- =4H2O 正极:O2+2H2O+4e-=4OH-②电解质溶液为稀硫酸负极:2H2-4e- =4H+ 正极:O2+4H++4e-=2H2O电池总反应:2H2+ O2=2H2O(6)钢铁的电化学腐蚀①吸氧腐蚀负极:2Fe - 4e- == 2Fe2+ 正极:O2+2H2O+4e-=4OH-总反应式:2Fe + O2+2H2O=2Fe(OH)2②析氢腐蚀负极:Fe - 2e- == Fe2+ 正极:2H+ +2e- == H2↑总反应式:Fe+ 2H+ == Fe2+ + H2↑4、金属腐蚀(1)金属腐蚀的类型:化学腐蚀和电化学腐蚀。
高中原电池知识点总结

高中原电池知识点总结高中原电池知识点总结原电池是高一化学课本中的重要知识,同学们一定要牢记。
下面是小编为你收集整理的高一化学原电池的知识点归纳,一起来看看吧。
高一化学原电池知识点一、原电池、电解池的两极电子从负极通过导线流向正极,电子的定向移动形成电流,电流的方向是正极到负极,这是物理学规定的。
阴极、阳极是电化学规定的,失去电子的极即氧化极,也就是阳极;得到电子的极即还原极,也就是阴极。
原电池中阳极失去电子,电子由阳极通过导线流向阴极,阴极处发生得电子的反应,由于原电池是一种化学能转化为电能的装置,它作为电源,通常我们称其为负极和正极。
在电解池中,连着负极的一极是电解池的阴极,连着正极的一极是电解池的阳极,由于电解池是一种电能转化为化学能的装置,我们通常说明它的阳极和阴极。
二、原电池、电解池、电镀池的判断规律(1)若无外接电源,又具备组成原电池的三个条件。
①有活泼性不同的两个电极;②两极用导线互相连接成直接插入连通的电解质溶液里;③较活泼金属与电解质溶液能发生氧化还原反应(有时是与水电离产生的H+作用),只要同时具备这三个条件即为原电池。
(2)若有外接电源,两极插入电解质溶液中,则可能是电解池或电镀池;当阴极为金属,阳极亦为金属且与电解质溶液中的金属离子属同种元素时,则为电镀池。
(3)若多个单池相互串联,又有外接电源时,则与电源相连接的装置为电解池成电镀池。
若无外接电源时,先选较活泼金属电极为原电池的负极(电子输出极),有关装置为原电池,其余为电镀池或电解池。
三、分析电解应用的主要方法和思路1、电解质在通电前、通电后的关键点是:通电前:电解质溶液的电离(它包括了电解质的电离也包括了水的电离)。
通电后:离子才有定向的移动(阴离子移向阳极,阳离子移向阴极)。
2、在电解时离子的放电规律是:阳极:金属阳极>S2—>I—>Cl—>OH—>含氧酸根>F—阴极:Ag+>Fe3+>Cu2+>H+(浓)>Pb2+>Sn2+>Fe2+>Zn2+>H+>Al3+>Mg2+>Na+>Ca2 +>K+3、电解的`结果:溶液的浓度、酸碱性的变化溶液的离子浓度可能发生变化如:电解氯化铜、盐酸等离子浓度发生了变化。
高中化学 原电池、化学电源(含燃料电池)

课时28原电池、化学电源(含燃料电池)知识点一原电池的工作原理及应用【考必备·清单】1.原电池(1)概念:原电池是把化学能转化为电能的装置。
(2)构成条件电极两极为导体,且存在活动性差异溶液两极插入电解质溶液中回路形成闭合回路或两极直接接触本质看能否自发地发生氧化还原反应(3)工作原理(以锌、铜原电池为例)电极名称负极正极电极材料锌片铜片电极反应Zn-2e-===Zn2+Cu2++2e-===Cu 电极质量变化减小增大反应类型氧化反应还原反应电子流向由Zn沿导线流向Cu盐桥中离子移向盐桥含饱和KCl溶液,K+移向正极,Cl-移向负极a.连接内电路形成闭合回路。
盐桥作用b.维持两电极电势差(中和电荷),使电池能持续提供电流。
(4)负极与正极①负极:发生氧化反应或电子流出的电极。
②正极:发生还原反应或电子流入的电极。
(5)两个移动方向①电子定向移动方向和电流方向a.电子从负极流出经外电路流入正极;b.电流从正极流出经外电路流入负极;故电子定向移动方向与电流方向正好相反。
②离子移动方向阴离子向负极移动(如SO2-4),阳离子向正极移动(如Zn2+和H+,溶液中H+在正极上得电子形成氢气在铜片上冒出)。
[名师点拨]①自发发生的氧化还原反应并不一定是电极与电解质溶液反应,也可以是电极与溶解的O2等发生反应,如将铁与石墨相连插入食盐水中。
②无论是原电池还是电解池,电子均不能通过电解质溶液。
③双液铜、锌原电池(带盐桥)比单液原电池的最大优点是Zn与氧化剂(Cu2+)不直接接触,仅有化学能转化为电能,避免了能量损耗,故电流稳定,放电时间长。
2.原电池原理的四大应用(1)加快氧化还原反应的速率一个自发进行的氧化还原反应,形成原电池时会使反应速率加快。
例如,在Zn与稀H2SO4反应时加入少量CuSO4溶液置换出的Cu能与Zn形成原电池使产生H2的反应速率加快。
(2)比较金属活动性强弱如有两种金属A和B,用导线将A和B连接后,插入到稀硫酸中,一段时间后,若观察到A溶解,而B上有气体放出,则说明A作负极,B作正极,即可以断定金属活动性:A>B。
化学原电池知识点总结高二

化学原电池知识点总结高二化学原电池作为一种常见的电化学装置,广泛应用于我们的生活和工业生产中。
在高二的学习中,我们需要掌握关于化学原电池的基本概念、原理和应用。
下面是对化学原电池知识点的详细总结。
一、化学原电池的概念化学原电池是一种通过化学反应将化学能转化为电能的装置。
它由两个半电池组成,每个半电池都包含一个电解质溶液和一个电极。
其中,负极反应产生电子,正极反应接受电子,两个半电池通过外部电路连接,使电子在外部电路中流动,从而产生电流。
二、化学原电池的原理1. 电极反应在化学原电池中,负极受到氧化反应,正极受到还原反应。
负极被称为阳极,正极被称为阴极。
氧化反应发生在阳极,负极物质被氧化为离子和电子;还原反应发生在阴极,正极物质接受电子并发生还原反应。
2. 电解质溶液电解质溶液在化学原电池中起着重要的作用。
它提供了溶解的离子,在反应中扮演着载流子的角色,维持了电池中的电中性。
广义上,电解质溶液可分为酸性电解质溶液和碱性电解质溶液。
常见的酸性电解质溶液有硫酸、盐酸等,碱性电解质溶液有氢氧化钠、氢氧化钾等。
三、化学原电池的应用1. 储能装置化学原电池是重要的储能装置,被广泛应用于便携式设备、无线麦克风等。
通过将化学能转化为电能,化学原电池为我们的日常生活提供了方便。
2. 电化学实验通过化学原电池可以进行一系列重要的电化学实验,如电解水制氢、电镀、化学感应等。
这些实验不仅有助于我们的学习,还拓宽了我们的科学视野。
3. 工业应用化学原电池在工业生产中具有广泛的应用。
比如,电镀行业使用化学原电池进行金属表面的镀铬、镀镍等加工,提高了产品的质量和外观。
四、化学原电池的举例1. 锌铜电池锌铜电池是一种常见的化学原电池,也是高中化学实验中常用的电池之一。
其中,锌作为负极,在硫酸溶液中氧化形成离子和电子;铜作为正极,接受电子并发生还原反应。
2. 锂电池锂电池是一种高效的化学原电池,常用于电子设备和电动车中。
锂离子在锂电池中沿着电解质溶液中的离子通道来回移动,在负极经历一系列的化学反应,将化学能转化为电能。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
选修四 第四章 电化学基础
第一节 原电池
1.定义:把化学能转化为电能的装置
2.实质:一个能自发进行的氧化还原反应。
3.构成条件:
(1)两个活性不同的金属(其中一种可以为非金属,即作导体用)作电极。
(2)两电极插入电解质溶液中。
(3)形成闭合回路。
(两电极外线用导线连接,可以接用电器。
)
(4)自发地发生氧化还原反应
※4.原理:
Ⅰ Ⅱ
两种装置的比较:
装置Ⅰ中还原剂Zn与氧化剂Cu2+直接接触,易造成能量损耗;装置Ⅱ能避免能量损耗;装置Ⅱ中盐桥的作用是提供离子迁移通路,导电。
5.盐桥:含有琼胶的KCl饱和溶液
盐桥作用:连接两个溶液,并保持两个溶液呈电中性。
K+ ⇒正极,Cl -⇒负极。
