p初中科学化学方程式汇总
《科学》化学方程式集合

《科学》化学方程式(陈川)第四册S + O2点燃SO2(硫在氧气中燃烧,形成二氧化硫)3Fe + 2O2点燃Fe3O4(铁在氧气中燃烧,形成四氧化三铁)C6H12O6+ 6O2−→−酶6CO2+ 6H2O + 能量(呼吸作用的反应过程,葡萄糖C6H12O6为有机化合物)C6H12O6+ 6O2酶6CO2+ 6H2O + 能量2H2O2M n O22H2O + O2↑(二氧化锰MnO2是催化剂)C + O2点燃CO2↑(碳在氧气中燃烧)4P + 5O2点燃2P2O52H2O 通电2H2↑+ O2↑CO2+ Ca(OH)2 =CaCO3↓+ H2OCO2+ H2O =H2CO3H2CO3=H2O + CO2↑CO2+ Ca(OH)2 =CaCO3↓+ H2OO2紫外线2OO + O2=O3 (臭氧)“臭氧”分子式:O3第五册CaCO3 + HCl =CaCl2+ CO2↑+ H2OFe2O3+ 6HCl =2FeCl3+ 3H2OCuO + 2HCl =CuCl2 + H2OHCl + AgNO3=AgCl↓+ HNO3NaOH + HCl =NaCl + H2O2NaOH + H2SO4=Na2SO4+ 2H2OH2SO4(硫酸)、HCl(盐酸)、HNO3(硝酸)、H3PO4(磷酸)与NaOH(氢氧化钠)、Ca(OH)2 、Cu(OH)2 、Fe(OH)3的反应。
H2SO4+ 2NaOH =Na2SO4+ 2H2OH2SO4+ Ca(OH)2 =CaSO4+ 2H2OH2SO4+ Cu(OH)2 =Cu SO4+ 2H2O3H2SO4+ 2Fe(OH)3=Fe2(SO4)3+ 6H2OHCl + NaOH =NaCl + H2O2HCl + Ca(OH)2 =CaCl2+ 2H2O2HCl + Cu(OH)2 =CuCl2+ 2H2O3HCl + Fe(OH)3=Fe Cl3+ 3H2OHNO3+ NaOH =NaNO3+ H2O2HNO3+ Ca(OH)2 =Ca(NO3)2+ 2H2O2HNO3+ Cu(OH)2 =Cu(NO3)2+ 2H2O3HNO3+ Fe(OH)3=Fe(NO3)3+ 3H2OH3PO4+ 3NaOH =Na3PO4 + 3H2O2H3PO4+ 3Ca(OH)2 =Ca3(PO4)2+ 6H2O2H3PO4+ 3Cu(OH)2 =Cu3(PO4)2+ 6H2OH3PO4+ Fe(OH)3=FePO4+ 3H2OSO2+2NaOH=Na2SO3+H2O (Na2SO3 亚硫酸钠)Ca(OH)2 + H2CO3=CaCO3↓+ 2H2ONaCO3+ CaCl2=CaCO3↓+ 2NaClNH3+ H2O + CO2=NH4HCO3(碳铵)2NH3+ H2SO4=(NH4)2 SO4(硫铵)2Cu + O2∆2CuO2Mg + O2点燃2MgOMg + 2HCl =MgCl2+ H2↑Zn + 2HCl =ZnCl2+ H2↑Mg + H2SO4=MgSO4+ H2↑Zn + H2SO4=ZnSO4+ H2↑Fe + CuSO4=FeSO4+ CuZn + CuSO4=Cu + ZnSO4CH4+ 2O2点燃CO2+ 2H2OC + CO2高温2COCO + CuO ∆Cu + CO22KMnO4∆K2MnO4 + MnO2 + O2↑KMnO4高锰酸钾(又名“过锰酸钾”)制“氧”反应,K2MnO4是锰酸钾Na2CO3+ 2AgNO3=2NaNO3+ Ag2CO3↓Ag2CO3 + 2HNO3=2AgNO3+ H2O + CO2↑CuSO4+ Ba(OH)2=BaSO4↓+ Cu(OH)2↓CuSO4·5H2O ∆CuSO4+ 5H2O (CuSO4·5H2O俗称“胆矾”)Al(OH)3+ 3HCl =AlCl3+ 3H2OFe + 2HCl =FeCl2+ H2↑(FeCl2是“氯化亚铁”)Zn + H2SO4=ZnSO4+ H2↑Fe2O3+ 3H2SO4=Fe2(SO4)3+ 3H2OCuO + H2SO4=CuSO4+ H2OCu(OH)2+ H2SO4=CuSO4+ 2H2OBaCl2+ H2SO4=2HCl + BaSO4↓Ca(OH)2 + Na2CO3=2NaOH + CaCO3↓3Ca(OH)2+ 2FeCl3=3CaCl2+ 2Fe(OH)3↓化学方程归类整理一、化合反应C + O2点燃CO2↑(碳在氧气中燃烧)2C + O2(不足)点燃2CO↑S + O2点燃SO24P + 5O2点燃2P2O52H2+ O2点燃2H2O2Mg + O2点燃2MgO3Fe + 2O2点燃Fe2O3Cu + O2 2CuO4Al + 3O2点燃2Al2O3CO + O2点燃CO2CO2 + C 高温2CO2Na + Cl2点燃2NaClH2+ Cl2点燃2HClFe + S 点燃FeSCO2+ H2O H2CO3SO2+ H2O = H2SO3SO3+ H2O = H2SO4P2O5+ 3H2O(热)= 2H3PO4(H3PO4是“磷酸”,PO43—是磷酸根)CaO + H2O = Ca(OH)2 (生石灰加水生成熟石灰)Na2O + H2O = 2NaOHK2O + H2O = 2KOHBaO + H2O = Ba(OH)2MgO + SO3= MgSO4CaO + SiO2高温CaSiO3(CaSiO3是“硅酸钙”)二、分解反应2H2O 通电2H2↑+ O2↑2HgO ∆2Hg + O2↑H2CO3= H2O + CO2↑H2SO3= H2O + SO2↑H2SO4∆H2O + SO3Cu(OH)2 ∆CuO + H2O2Fe(OH)3 ∆Fe2O3+ 3H2OCaCO3高温CaO + CO2↑MgCO3高温MgO + CO2↑Ca(HCO3)2∆CaCO3↓+ H2O +CO2↑NH4HCO3∆H2O + NH3↑+CO2↑2KClO3M n O22KCl + 3O2↑(“二氧化锰”MnO2是催化剂)2KMnO4∆K2MnO4 + MnO2 + O2↑Cu2(OH)2CO3∆2CuO + H2O + CO2↑CuSO4·5H2O ∆CuSO4+ 5H2O (CuSO4·5H2O俗称“胆矾”)三、置换反应Mg + 2HCl = MgCl2+ H2↑Zn + 2HCl = ZnCl2+ H2↑Fe + 2HCl = FeCl2+ H2↑Mg + H2SO4(稀)= MgSO4+ H2↑Zn + H2SO4(稀)= ZnSO4+ H2↑Fe + H2SO4(稀)= FeSO4+ H2↑Fe + CuSO4= FeSO4+ CuZn + CuCl2= ZnCl2+ CuCu + Hg(NO3)2= Cu(NO3)2+ HgH2 + CuO ∆Cu + H2OH2 + PbO ∆Pb + H2O (PbO是“氧化铅”)C + 2CuO 高温2Cu + CO2↑四、复分解反应HCl + NaOH =NaCl + H2OH2SO4+ 2NaOH =Na2SO4+ 2H2OHNO3+ NaOH =NaNO3+ H2OCu(OH)2+ 2HCl =CuCl2+ 2H2O2Fe(OH)3+ 3H2SO4=Fe2(SO4)3+ 6H2O2HNO3+ Mg(OH)2 =Mg(NO3)2+ 2H2OCaCO3+ 2HCl =CaCl2+ H2O + CO2↑AgNO3+ HCl = AgCl↓+ HNO3Na2CO3+ 2HCl = 2NaCl + H2O + CO2↑BaCl2+ H2SO4=2HCl + BaSO4↓Ba(NO3)2+ H2SO4=2HNO3+ Ba SO4↓CuSO4+ 2NaOH = Na2SO4+ Cu(OH)2↓FeCl3+ 3NaOH = 3NaCl + Fe(OH)3↓Na2CO3+ Ca(OH)2= 2NaOH + CaCO3↓MgSO4+ 2NaOH = Na2SO4+ Mg(OH)2↓NaCl + AgNO3= NaNO3+ AgCl↓BaCl2+ 2AgNO3 = Ba(NO3)2+ 2AgCl↓BaCl2 + Na2SO4= 2NaCl + BaSO4↓Ba(NO3)2+ CuSO2= Cu(NO3)2+ BaSO4↓五、其他反应CO2+ Ca(OH)2 =CaCO3↓+ H2OSO2+ 2NaOH = Na2SO3+ H2O (Na2SO3是“亚硫酸钠”)CO2+ 2NaOH = Na2CO3+ H2OCuO + H2SO4 CuSO4+ H2OFe2O3+ 3H2SO4=Fe2(SO4)3+ 3H2OFe2O3+ 6HCl = 2FeCl3+ 3H2OZnO + 2HNO3= Zn(NO3)2+ H2OCaO + 2HNO3= Ca(NO3)2+ H2OCuO + CO 高温Cu + CO2Fe2O3+ 3CO 高温2Fe + 3CO2CH4+ 2O2点燃CO2+ H2O (CH4是“甲烷”,气体)2C2H2+ 5O2点燃4CO2+ 2H2O (C2H2是“乙炔”,气体)C2H5OH + 3O2点燃2CO2+ 3H2O(C2H5OH是“乙醇”,俗称“酒精”)。
初中化学方程式总结表

初中化学方程式总结表1、碳铵受热分解:NH4HCO3 = NH3↑+ H2O + CO2↑2、铜绿受热分解:Cu2(OH)2CO3 = 2CuO + H2O +CO2↑3、铜绿和稀盐酸反应:Cu2(OH)2CO3 + 4HCl = 2CuCl2 + 3H2O +CO2↑4、红磷或白磷燃烧:4 P + 5 O2 点燃 2 P2O5 (黄色火焰,放热,生成白色固体)5、硫燃烧:S + O2 点燃SO2(空气中淡蓝色火焰,氧气中蓝紫色火焰)6、镁燃烧:2 Mg + O2 点燃2MgO (放出耀眼的白光,放热,生成白色固体)7、铁丝燃烧:3 Fe + 2 O2 点燃Fe3O4 (剧烈燃烧,火星四射,放热,生成黑色固体)8、铜丝加热:2Cu + O2(紫红色固体变黑)9、氧气充足时碳燃烧: C + O2 点燃CO210、氧气不足时碳燃烧: 2 C + O2 点燃 2 CO11、实验室用高锰酸钾制氧气:2KMnO4 △K2MnO4 + MnO2 + O2↑12、实验室用氯酸钾制氧气:2KClO △2KCl + 3O2↑(MnO2作催化剂)13、实验室用过氧化氢溶液制氧气:2H2O2== 2H2O + O2↑(MnO2作催化剂) (反应放热)14、电解水:2 H2O 通电O2↑+ 2H2↑(正氧负氢,体积比1:2,质量比8:1)15、氢气燃烧(氢气爆炸):2 H2 + O2 点燃 2 H2O16、实验室制CO2:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑(药品:大理石/石灰石和稀盐酸)17、工业制二氧化碳:CaCO3 高温CaO + CO2 ↑18、二氧化碳的检验:CO2 + C a(O H)2= CaCO3↓+ H2O19、二氧化碳与水反应:CO2 + H2O = H2CO320、碳酸分解:H2CO3 = CO2↑+ H2O21、CO燃烧:2 CO + O2点燃 2 CO222、碳还原二氧化碳:C+CO2 高温 2 CO23、碳还原氧化铜:C+2 CuO 高温 2 Cu + CO2↑24、氢气还原氧化铜:H2 + CuO === Cu + H2O25、CO还原CuO:CO + CuO △Cu + CO226、CO还原Fe2O3:3CO + Fe2O3高温2Fe + 3CO2MnO227、CO还原Fe3O4:4CO + Fe3O4高温3Fe + 4CO228、甲烷燃烧:CH4 + 2O2 点燃CO2 + 2H2O29、乙醇(酒精)燃烧:C2H5OH + 3O2 点燃2CO2 + 3H2O30、氢气在氯气中燃烧:H2 + Cl2点燃2HCl31、浓盐酸和浓氨水相遇生成白烟:HCl + NH3 == NH4Cl酸+ 活泼金属→盐+ 氢气(反应放热)32、实验室制取氢气:Zn + 2HCl = ZnCl2 + H2↑Zn + H2S O4= ZnS O4+ H2↑33、镁和稀酸反应:Mg+ 2HCl =MgCl2 + H2↑Mg + H2SO4 = MgSO4 + H2↑34、铁和稀酸反应:Fe + 2HCl = FeCl2 + H2↑Fe + H2SO4 = FeSO4 + H2↑35、铝和稀酸反应:2Al+6HCl = 2AlCl3+3H2↑2Al+3H2SO4 =Al2(SO4)3 + 3 H2↑酸 + 金属氧化物→盐+ 水36、用酸去除铁锈:Fe2O3+6HCl==2FeCl3+3H2O Fe2O3+3H2SO4==Fe2(SO4)3+3H2O(红棕色固体消失,溶液由无色变成黄色)37、硫酸和氧化铜反应:CuO+H2SO4==CuSO4+H2O (黑色固体消失,溶液由无色变成蓝色)38、硝酸和氧化锌反应:ZnO+2HNO3==Zn(NO3)3+H2O39、硫酸和氧化铝反应:Al2O3 + 3H2SO4 == Al2(SO4)3 + 3H2O40、盐酸和氧化镁反应:MgO + 2HCl == MgCl2 + H2O酸 + 碱→盐+ 水(反应放热)41、烧碱和酸反应:NaOH+HCl==NaCl+H2O 2NaOH+H2SO4==Na2SO4+2H2O42、蓝色沉淀和酸的反应:Cu(OH)2+2HCl==CuCl2+2H2O Cu(OH)2+H2SO4==CuSO4+2H2O43、氢氧化钡和硫酸的反应:Ba(OH)2+H2SO4==BaSO4↓+2H2O44、石灰乳和稀盐酸的反应:Ca(OH)2+2HCl==CaCl2+2H2O45、氢氧化镁治疗胃酸过多:Mg(OH)2+2HCl==MgCl2+2H2O46、氨水和稀硫酸的反应:2NH3·H2O + H2SO4 == (NH4)2SO4 + 2H2O酸 + 盐→新酸+ 新盐(酸 + 碳酸盐→盐+ 水+ 二氧化碳)47、稀盐酸和硝酸银反应:HCl+AgNO3== AgCl↓+HNO348、稀硫酸和氯化钡反应:H2SO4+BaCl2==BaSO4↓+2HCl49、稀硫酸和硝酸钡反应:H2SO4 + Ba(NO3)2 ==BaSO4↓+2HNO350、纯碱和稀盐酸反应:Na2CO3+2HCl==2NaCl+H2O+CO2↑51、小苏打和稀盐酸反应:NaHCO3+HCl==NaCl+H2O+CO2↑碱 + 非金属氧化物→盐+ 水(非基本反应类型)52、火碱溶液吸收CO2:2NaOH + CO2 = Na2CO3 + H2O53、火碱溶液吸收SO2:2NaOH + SO2 = Na2SO3 + H2O54、石灰水吸收SO2:Ca(OH)2 + SO2 = CaSO3↓+ H2O碱 + 盐→新碱+ 新盐(碱 + 铵盐→新盐+ 水+ 氨气)55、配制波尔多液:CuSO4+Ca(OH)2==Cu(OH)2↓+CaSO456、纯碱制烧碱:Ca(OH)2+Na2CO3==CaCO3↓+2NaOH Ba(OH)2+Na2CO3==BaCO3↓+2NaOH57、氯化铁和烧碱混合:FeCl3+3NaOH==Fe(OH)3↓+3NaCl58、氯化镁和石灰水混合:MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl259、苛性钠和氯化铵混合加热:NaOH+NH4Cl==NaCl+NH3↑+H2O60、熟石灰和硫酸铵反应:Ca(OH)2+(NH4)2SO4==CaSO4+2NH3↑+2H2O61、硫酸镁和氢氧化钡反应:MgSO4 + Ba(OH)2 == BaSO4↓+ Mg(OH)2↓62、硫酸铵和氢氧化钡反应:(NH4)2SO4 + Ba(OH)2 == BaSO4↓ + 2NH3↑ + 2H2O金属 + 盐溶液→新金属+ 新盐63、湿法炼铜:Fe + CuSO4 = Cu + FeSO464、锌和硫酸亚铁反应:Zn + FeSO4 = Fe + ZnSO465、铜与硝酸银反应:2AgNO3 + Cu = 2Ag+ Cu(NO3)266、铝与硫酸铜反应: 2Al + 3CuSO4 = 3Cu + Al2(SO4)3盐1 + 盐2 →新盐1 + 新盐267、氯化钠和硝酸银反应:NaCl+AgNO3==AgCl↓+NaNO368、硫酸钠和氯化钡反应:Na2SO4+BaCl2==BaSO4↓+2NaCl69、纯碱和氯化钡反应:Na2CO3 + BaCl2 == BaCO3↓+2NaCl70、纯碱和氯化钙反应:Na2CO3 + CaCl2 ==CaCO3↓+2NaCl钙循环高温71、制取生石灰:CaCO3 == CaO + CO2↑72、生石灰制取熟石灰(反应放热):CaO + H2O = Ca(OH)273、熟石灰生成碳酸钙:CO 2 + C a (O H )2 = CaCO 3↓ + H 2O 常见的盐74、电解食盐水: 2NaCl + 2H 2O == 2NaOH + H 2↑ + Cl 2↑ 侯德榜制碱法75、NaCl + NH 3 +CO 2 + H 2O === NaHCO 3↓ + NH 4Cl(先通氨气,溶液呈碱性,有利于吸收CO2,提高产率) 76、2NaHCO 3 == Na 2CO 3 + H 2O +CO 2↑77、纯碱溶液中持续通入二氧化碳:Na 2CO 3 + H 2O +CO 2 == 2NaHCO 378、胆矾的生成:CuSO 4 + 5H 2O == CuSO 4·5H 2O (白色固体变蓝色)79、可燃冰完全燃烧:CH 4·nH 2O + 2O 2 == CO 2 + (2+n)H 2O80、光合作用: 6CO 2 + 6H 2O == C 6H 12O 6 + 6O 2 81、呼吸作用: C 6H 12O 6 + 6O 2 == 6CO 2 + 6H 2O82、硫酸型酸雨的形成:① 2SO 2 + O 2 == 2SO 3 SO 3 + H 2O == H 2SO 4② SO 2+H 2O == H 2SO 3 2H 2SO 3 + O 2 == 2H 2SO 4 通电点燃 光照 叶绿素 酶尘埃。
初中必背化学方程式汇总(最全)

初中必背化学方程式汇总(最全)下面是初中化学方程式的汇总:1.酸碱中和反应方程式:酸+碱→盐+水例如:HCl+NaOH→NaCl+H₂O2.金属与非金属氧化物的反应方程式:金属+氧气→金属氧化物例如:2Na+O₂→2Na₂O3.酸与金属的反应方程式:酸+金属→盐+氢气例如:2HCl+Zn→ZnCl₂+H₂4.金属与酸的反应方程式:金属+酸→盐+氢气例如:Mg+2HCl→MgCl₂+H₂5.非金属与氧气的反应方程式:非金属+氧气→非金属氧化物例如:C+O₂→CO₂6.金属与非金属的氧化还原反应方程式:金属+非金属氧化物→盐+水例如:Na+Cl₂O→NaCl+H₂O7.非金属与酸的反应方程式:非金属+酸→氧化物+水例如:2H₂SO₃+C→CO₂+2H₂O8.金属与非金属的酸碱中和反应方程式:金属氢氧化物+酸→盐+水例如:NaOH+HCl→NaCl+H₂O9.酸与酸碱指示剂的反应方程式:酸+碱性指示剂→锥色盐例如:HCl+NaOH+碱性指示剂→NaCl+H₂O+锥色盐10.非金属氧化物和水的反应方程式:非金属氧化物+水→酸例如:SO₃+H₂O→H₂SO₄11.非金属酸与金属碱的反应方程式:非金属酸+金属氢氧化物→盐+水例如:HCl+NaOH→NaCl+H₂O12.碱与金属氧化物的反应方程式:碱+金属氧化物→锹色盐+水例如:KOHa+CuO→Cu(OH)₂+K₂O13.铜与稀硫酸反应的反应方程式:Cu+H₂SO₄→CuSO₄+H₂14.金属与水的反应方程式:金属+水→金属氢氧化物+氢气例如:2Na+2H₂O→2NaOH+H₂15.铁与酸的反应方程式:Fe+2HCl→FeCl₂+H₂16.铁与水蒸气的反应方程式:3Fe+4H₂O→Fe₃O₄+4H₂17.碳酸氢盐分解反应方程式:碳酸氢盐→二氧化碳+水+相应金属氧化物例如:NaHCO₃→CO₂+H₂O+Na₂O18.金属氢氧化物分解反应方程式:金属氢氧化物→金属氧化物+水例如:Ca(OH)₂→CaO+H₂O以上是初中化学方程式的汇总,涵盖了酸碱中和、金属与非金属氧化物的反应、金属与酸的反应、非金属与氧气的反应、金属与非金属的氧化还原反应等常见反应类型。
八年级科学下化学方程式知识总结

四、 氧化还原反应:
1、CH4(甲烷)+2O2== CO2+2H2O 2、2C2H2(乙炔)+5O2== 4CO2+2H2O
3、CO+CuO == Cu+CO24、3CO+Fe2O3== 2Fe+3CO2(高炉炼铁原理)
五、复分解反应:
1、CO2+Ca (OH)2== CaCO3↓+H2O(澄清石灰水变浑浊,久置石灰水的试剂瓶有白膜原因)2、CaCO3+2HCl == CaCl2+CO2↑+H2O(实验室制二氧化碳的原理、除白膜的方程式)
3、Na2CO3+2HCl == 2NaCl+CO2↑+H2O(灭火器原理)
4、Na2CO3+H2SO4== Na2SO4+CO2↑+H2O(灭火器原理)
5、NaHCO3+2HCl == 2NaCl+CO2↑+H2O
六、金属活动性顺序表:
K、Ca、Na、Mg、Al、Zn、Fe、Sn(锡)、Pb(铅)(H)Cu、Hg、Ag、Pt(铂)、Au(金)
9、2Mg+O2== 2MgO 10、2C+O2== 2CO 11、C+CO2== 2CO
12、CO2+H2O == H2CO3(微溶于水.生成使紫色石蕊变பைடு நூலகம்色的碳酸.使试管内气压减小)
二、 分解反应:
1、2KClO3== 2KCl+3O2↑(实验室制氧气原理)
2、2KMnO4== K2MnO4+MnO2+O2↑(实验室制氧气原理)
3、2H2O == 2H2↑+O2↑4、NH4HCO3== NH3↑+CO2↑+H2O
初中科学化学方程式归纳
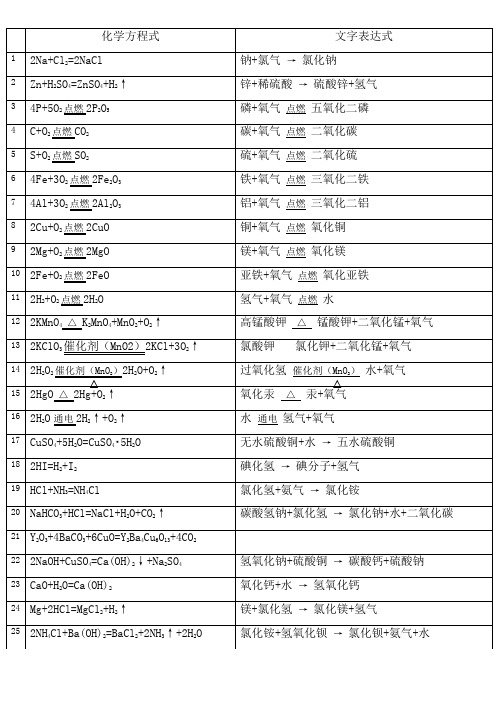
△ 15 2HgO △ 2Hg+O2↑
16 2H2O 通电 2H2↑+O2↑ 17 CuSO4+5H2O=CuSO4▪5H2O 18 2HI=H2+I2 19 HCl+NH3=NH4Cl 20 NaHCO3+HCl=NaCl+H2O+CO2↑ 21 Y2O3+4BaCO3+6CuO=Y2Ba4Cu6O13+4CO2 22 2NaOH+CuSO4=Ca(OH)2↓+Na2SO4 23 CaO+H2O=Ca(OH)2 24 Mg+2HCl=MgCl2+H2↑ 25 2NH4Cl+Ba(OH)2=BaCl2+2NH3↑+2H2O
26 CH4+Cl2=CH3Cl+HCl 27 3H2+Fe2O3=2Fe+3H2O 28 Cl+O3=ClO+O2 29 2ClO=Cl2O2 30 Cl2O2 阳光 2Cl+O2 31 2NO2+4CO 催化剂 4CO2+N2 32 CH4+2O2=CO2+2H2O 33 Ca(OH2)+CO2=CaCO3↓+H2O
九年级所有化学方程式总汇全

九年级所有化学方程式总汇全一、化学反应类型1. 置换反应金属置换反应:例如,铁与硫酸铜反应硫酸亚铁和铜。
Fe + CuSO₄ → FeSO₄ + Cu非金属置换反应:例如,氯气与溴化钠反应氯化钠和溴。
Cl₂ + 2NaBr → 2NaCl + Br₂2. 复分解反应中和反应:例如,氢氧化钠与盐酸反应氯化钠和水。
NaOH + HCl → NaCl + H₂O盐与盐的反应:例如,硫酸钠与氯化钡反应硫酸钡和氯化钠。
Na₂SO₄ + BaCl₂ → BaSO₄↓ + 2NaCl3. 分解反应热分解:例如,碳酸钙在高温下分解氧化钙和二氧化碳。
CaCO₃ → CaO + CO₂↑光解:例如,氯酸钾在光照下分解氯化钾和氧气。
2KClO₃ → 2KCl + 3O₂↑4. 合成反应燃烧反应:例如,碳与氧气反应二氧化碳。
C + O₂ → CO₂氢化反应:例如,氮气与氢气反应氨气。
N₂ + 3H₂ → 2NH₃二、化学方程式实例1. 氢气与氧气反应水2H₂ + O₂ → 2H₂O2. 铁与硫酸铜反应硫酸亚铁和铜Fe + CuSO₄ → FeSO₄ + Cu3. 氢氧化钠与盐酸反应氯化钠和水NaOH + HCl → NaCl + H₂O4. 碳酸钙在高温下分解氧化钙和二氧化碳 CaCO₃ → CaO + CO₂↑5. 氯酸钾在光照下分解氯化钾和氧气2KClO₃ → 2KCl + 3O₂↑6. 氮气与氢气反应氨气N₂ + 3H₂ → 2NH₃7. 碳与氧气反应二氧化碳C + O₂ → CO₂8. 氯气与溴化钠反应氯化钠和溴Cl₂ + 2NaBr → 2NaCl + Br₂9. 硫酸钠与氯化钡反应硫酸钡和氯化钠 Na₂SO₄ + BaCl₂ → BaSO₄↓ + 2NaCl 10. 氢气与氯气反应氯化氢H₂ + Cl₂ → 2HCl九年级所有化学方程式总汇全三、氧化还原反应1. 氧化反应例如,铁在氧气中燃烧四氧化三铁。
3Fe + 2O₂ → Fe₃O₄2. 还原反应例如,氧化铜在氢气中还原铜和水。
科学化学方程式

置换反应
• 该反应可以遵循以下公式 a+bc=b+ac(其中a是单质, bc是化合物,b是单质,ac是化合物) • 1、铁和硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu • 2、镁和稀盐酸反应:Mg+ 2HCl === MgCl2 + H2↑ • 3、氢气还原氧化铜:H2 + CuO 加热 Cu + H2O • 4、木炭还原氧化铜:C+ 2CuO 高温 2Cu + CO2↑ • 5、水蒸气通过灼热碳层:H2O + C 高温 H2 + CO • 6、焦炭还原氧化铁:3C+ 2Fe2O3 高温 4Fe + 3CO2↑ • 7、铁和稀盐酸反应:Fe+2HCl===FeCl2+H2↑ • 8、铁和稀硫酸反应:Fe+H2SO4===FeSO4+H2↑ • 9、氢气还原氧化铁:3H2+ Fe2O3 高温 2Fe + 3H2O • 10、活动顺序在前的金属置换在后的金属例如: 锌 和稀硫酸反应(实验室制氢气):Zn + H2SO4 == ZnSO4 + H2↑
相互关系③
(3)碱 + 盐 -------- 新碱 +新盐 1.氢氧化钠与硫酸铜:2NaOH + CuSO4 ==== Cu(OH)2↓ + Na2SO4 2.氢氧化钠与氯化铁:3NaOH + FeCl3 ==== Fe(OH)3↓ + 3NaCl 3.氢氧化钠与氯化镁:2NaOH + MgCl2 ==== Mg(OH)2↓ + 2NaCl 4. 氢氧化钠与氯化铜:2NaOH + CuCl2 ==== Cu(OH)2↓ + 2NaCl 5. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 === CaCO3↓+ 2NaOH
p初中科学化学方程式汇总

沿河二中初三化学方程式汇总1、与氧有关的化学方程式:2Mg+O2===2MgO 现象:燃烧、放出大量的热、同时放出耀眼的白光S+O2 ===SO2 现象:空气中是淡蓝色的火焰;纯氧中是蓝紫色的火焰;同时生成有刺激性气味的气体。
C+O2===CO2 现象:燃烧,淡蓝色火焰,生成能够让澄清石灰水浑浊的气体2C+O2===2CO 现象:燃烧,淡蓝色火焰4P+5O2===2P2O5 现象::生成白烟3Fe+2O2===Fe3O4 现象:剧烈燃烧、火星四射、生成黑色的固体2H2+O2===2H2O 现象:淡蓝色的火焰2H2O2===2H2O+O2↑现象:溶液里冒出大量的气泡2HgO===2Hg+O2↑现象:生成银白色的液体金属2KClO3===2KCl+3O2↑现象:生成能让带火星的木条复燃的气体2KMnO4==K2MnO4+MnO2+O2↑现象:同上,2、跟氢有关的化学方程式:2H2+O2===2H2O 现象:淡蓝色的火焰Zn+H2SO4==ZnSO4+H2↑现象:有可燃烧的气体生成Mg+H2SO4==MgSO4+H2↑现象:同上Fe+H2SO4 ==FeSO4+H2↑现象:变成浅绿色的溶液,同时放出气体2Al+3H2SO4 ==Al2(SO4)3+3H2↑现象:有气体生成Zn+2HCl==ZnCl2+H2↑现象:同上Mg+2HCl==MgCl2+H2↑现象:同上Fe+2HCl==FeCl2+H2↑现象:溶液变成浅绿色,同时放出气体2Al+6HCl==2AlCl3+3H2↑现象:有气体生成H2+CuO====Cu+H2O 现象:由黑色的固体变成红色的,同时有水珠生成2Fe2O3+3H2 ==2Fe+3H2O 现象:有水珠生成,固体颜色由红色变成银白色3、跟碳有关的化学方程式:C+O2==CO2(氧气充足的情况下) 现象:生成能让纯净的石灰水变浑浊的气体2C+O2===2CO(氧气不充足的情况下) 现象:不明显C+2CuO==2Cu+CO2↑现象:固体由黑色变成红色并减少,同时有能使纯净石灰水变浑浊的气体生成3C+2Fe2O3==4Fe+3CO2↑现象:固体由红色逐渐变成银白色,同时黑色的固体减少,有能使纯净的石灰水变浑浊的气体生成CO2+C===2CO 现象:黑色固体逐渐减少3C+2H2O=CH4+2CO 现象:生成的混和气体叫水煤气,都是可以燃烧的气体4、跟二氧化碳有关的化学方程式:C+O2点燃====CO2 现象:生成能使纯净的石灰水变浑浊的气体Ca(OH)2+CO2===CaCO3↓+H2O 现象:生成白色的沉淀,用于检验二氧化碳CaCO3+CO2+H2O===Ca(HCO3)2 现象:白色固体逐渐溶解Ca(HCO3)===CaCO3↓+CO2↑+H2O 现象:生成白色的沉淀,同时有能使纯净的石灰水变浑浊的气体生成Cu2(OH)2CO3=2CuO+H2O+CO2↑现象:固体由绿色逐渐变成黑色,同时有能使纯净石灰水变浑浊的气体生成2NaOH+CO2===Na2CO3+H2O(也可为KOH)现象:不明显CaCO3===CaO+CO2↑现象:有能使纯净石灰水变浑浊的气体生成跟一氧化碳有关的,但同时也跟二氧化碳有关:Fe3O4+4CO====3Fe+4CO2 现象:固体由黑色变成银白色,同时有能使纯净石灰水变浑浊的气体生成FeO+CO===Fe+CO2 现象:固体由黑色逐渐变成银白色,同时有能使纯净石灰水变浑浊的气体生成Fe2O3+3CO====2Fe+3CO2 现象:固体由红色逐渐变成银白色,同时有能使纯净石灰水变浑浊的气体生成CuO+CO====Cu+CO2 现象:固体由黑色变成红色,同时有能使纯净石灰水变浑浊的气体生成5、跟盐酸有关的化学方程式:NaOH(也可为KOH)+HCl==NaCl+H2O 现象:不明显HCl+AgNO3==AgCl↓+HNO3 现象:有白色沉淀生成,这个反应用于检验氯离子CaCO3+2HCl==CaCl2+H2O+CO2↑现象:百色固体溶解,生成能使纯净石灰水变浑浊的气体Na2CO3+2HCl==2NaCl+H2O+CO2↑现象:生成能使纯净石灰水变浑浊的气体NaHCO3+HCl==NaCl+H2O+CO2↑现象:生成能使纯净石灰水变浑浊的气体Fe2O3+6HCl==2FeCl3+3H2O 现象:红色固体逐渐溶解,形成黄色的溶液Fe(OH)3+3HCl==FeCl3+3H2O 现象:红棕色絮状沉淀溶解,形成了黄色的溶液Cu(OH)2+2HCl==CuCl2+2H2O 现象:蓝色沉淀溶解,形成黄绿色的溶液CuO+2HCl==CuCl2+H2O 现象:黑色固体溶解,生成黄绿色的溶液Zn+2HCl==ZnCl2+H2↑现象:同上Mg+2HCl==MgCl2+H2↑现象:同上Fe+2HCl==FeCl2+H2↑现象:溶液变成浅绿色,同时放出气体2Al+6HCl==2AlCl3+3H2↑现象:有气体生成6、跟硫酸有关的化学方程式:2NaOH(或KOH)+H2SO4==Na2SO4+2H2O 现象:不明显Fe2O3+3H2SO4==Fe2(SO4)3+3H2O 现象:红色固体溶解,生成黄色溶液CuO+H2SO4==CuSO4+H2O 现象:黑色固体溶解,生成蓝色溶液Cu(OH)2+H2SO4==CuSO4+2H2O 现象:蓝色沉淀溶解,生成蓝色溶液H2SO4+BaCl2==BaSO4↓+2HCl 现象:生成不溶于强酸的白色沉淀,用于检验硫酸根离子CaCO3+H2SO4==CaSO4+H2O+CO2↑Na2CO3+H2SO4==Na2SO4+H2O+CO2↑2NaHCO3+H2SO4==Na2SO4+2H2O+2CO2↑现象:这三个反应现象同与盐酸反应现象一致7、跟硝酸有关的化学方程式:Fe2O3+6HNO3==2Fe(NO3)3+3H2O 现象:红色固体溶解,生成黄色溶液CuO+2HNO3==Cu(NO3)2 +H2O 现象:黑色固体溶解,生成蓝色溶液Cu(OH)2+2HNO3==Cu(NO3)2+2H2O 现象:蓝色沉淀溶解,生成蓝色溶液NaOH(或KOH)+HNO3==NaNO3+H2O 现象:不明显Mg(OH)2+2HNO3==Mg(NO3)2+2H2O 现象:白色沉淀溶解CaCO3+2HNO3==Ca(NO3)2+H2O+CO2↑Na2CO3+2HNO3==2NaNO3+H2O+CO2↑NaHCO3+HNO3==NaNO3+H2O+CO2↑现象:以上三个反应现象同与盐酸反应现象一致8、跟碱有关的化学方程式:NaOH+HCl(或HNO3、H2SO4)==NaCl+H2O 现象:酸碱中和反应,现象不明显CaO+H2O==Ca(OH)2现象:放出大量的热NaOH(KOH)+FeCl3(Fe(NO3)3、Fe2(SO4)3)==Fe(OH)3↓+NaCl 现象:生成红棕色絮状沉淀,括号里面的反应过程相似,产物相对应就行了2NaOH(KOH)+FeCl2(Fe(NO3)2、FeSO4)==Fe(OH)2↓+2NaCl 现象:生成白色絮状沉淀,括号里面的反映过程相似,产物相对应就行了2NaOH(KOH)+CuCl2(Cu(NO3)2、CuSO4)==Cu(OH)2↓+2NaCl 现象:生成蓝色絮状沉淀,括号里面的反应过程相似,产物相对应就行了NH4Cl(NH4NO3、(NH4)2SO4)+NaOH(KOH)==NH3↑+H2O+NaCl 现象:有可以使石蕊试纸变蓝的气体生成MgCl2(Mg(NO3)2、MgSO4)+NaOH(KOH)==Mg(OH)2↓+NaCl 现象:生成白色沉淀,括号里面的反应过程相似,产物相对应就行了NaHCO3+NaOH==Na2CO3+H2O 现象:不明显此反应的Na换成K是一样的Ca(HCO3)2+2NaOH==CaCO3↓+Na2CO3+2H2O 现象:生成白色沉淀,此反应把Na换成K是一样的2NaOH+CO2==Na2CO3+H2O 现象:无明显现象此反应的Na换成K是一样的Ca(OH)2+CO2==CaCO3↓+H2O 现象:产生白色沉淀,此反应用于检验二氧化碳NaHSO4+NaOH==Na2SO4+H2O 现象:无明显现象2NaOH+SO2==Na2SO3+H2O 现象:无明显现象9、跟钡盐有关的化学方程式:BaCl2+Na2SO4==BaSO4↓+2NaCl 现象:有白色的不溶于强酸的沉淀生成BaCl2+Na2CO3==BaCO3↓+2NaCl 现象:有白色沉淀生成但可溶于盐酸和硝酸,其实也溶于硫酸,但生成硫酸钡沉淀,不容易看出来10、跟钙盐有关的化学方程式:CaCl2+Na2CO3==CaCO3↓+2NaCl 现象:生成白色沉淀CaCO3+CO2+H2O==Ca(HCO3)2 现象:固体逐渐溶解Ca(HCO3)2+Ca(OH)2==2CaCO3↓+2H2O 现象:生成白色沉淀11、跟几种金属及其盐有关的化学方程式:(1)铜:CuSO4•5H2O===CuSO4+5H2O↑现象:固体由蓝色变为白色CuO+CO====Cu+CO2 现象:固体由黑色逐渐变成红色,同时有能使纯净的石灰水变浑浊的气体生成H2+CuO====Cu+H2O 现象:固体由黑色逐渐变成红色,同时有水珠生成Cu+2AgNO3==Cu (NO3)2+2Ag 现象:铜表面慢慢生成了银白色金属CuCl2+2NaOH==Cu (OH) 2↓+2NaCl 现象:生成了蓝色絮状沉淀CuO+H 2SO 4==CuSO 4+H 2O 现象:黑色固体溶解,生成蓝色溶液 Cu (OH) 2+H 2SO 4==CuSO 4+2H 2O 现象:蓝色沉淀溶解,生成蓝色溶液 Fe(Zn)+CuSO 4==FeSO 4+Cu 现象:有红色金属生成 Cu 2(OH)2CO 3==2CuO+H 2O+CO 2↑ 现象:固体由绿色逐渐变成黑色,同时有能使纯净石灰水变浑浊的气体生成(2)铁:Fe+2HCl==FeCl 2+H 2 现象:铁粉慢慢减少,同时有气体生成,溶液呈浅绿色 FeCl 2+2NaOH==Fe(OH)2↓+NaCl 现象:有白色絮状沉淀生成 4Fe(OH)2+O 2+2H 2O==4Fe(OH)3 现象:氢氧化铁在空气中放置一段时间后,会变成红棕色 Fe (OH) 3+3HCl==FeCl 3+3H 2O 现象:红棕色絮状沉淀溶解,溶液呈黄色 Fe (OH) 2+2HCl==FeCl 2+2H 2O 现象:白色絮状沉淀溶解,溶液呈浅绿色 Fe+CuSO 4==FeSO 4+Cu 现象:铁溶解生成红色金属 Fe+AgNO 3==Fe(NO 3)2+Ag 现象:铁溶解生成银白色的金属 Fe 2O 3+6HCl==2FeCl 3+3H 2O 现象:红色固体溶解,生成黄色的溶液 23432Fe O Fe O 点燃= 现象:铁剧烈燃烧,火星四射,生成黑色的固体 Zn+FeCl 2==ZnCl 2+Fe 现象:锌粉慢慢溶解,生成铁(3)银:AgNO 3+HCl==AgCl ↓+HNO 3 现象:有白色沉淀生成,且不溶于强酸 AgNO 3+NaCl==AgCl ↓+NaNO 3 现象:有白色沉淀生成,且不溶于强酸 Cu+2AgNO 3==Cu(NO 3)2+2Ag 现象:红色的铜逐渐溶解,同时有银白色的金属生成 2AgNO 3+Na 2SO 4==Ag 2SO 4↓+2NaNO 3 现象:有白色沉淀生成(4)补充化学方程式: 3Ag+4HNO 3(稀)==3AgNO 3+NO ↑+2H 2O 现象:银逐渐溶解,生成气体遇空气变棕色 Ag+2HNO 3(浓)==AgNO3+NO 2↑+H 2O 现象:银逐渐溶解,生成棕色气体 Cu+2H 2SO4(浓)==CuSO 4+SO 2↑+2H 2O 现象:铜逐渐溶解,生成有刺激性气味的气体 2FeCl 3+Fe==3FeCl 2 现象:铁粉逐渐溶解,溶液由黄色变成浅绿色 2Na 2O 2(过氧化钠)+2H 2O=4NaOH+O 2 现象:有能使带火星的木条复燃的气体生成。
初中科学化学方程式大全

初中科学化学方程式大全一. 化合反应:1. 镁在空气中燃烧:2Mg + O 2 点燃 2MgO2. 铁在氧气中燃烧:3Fe + 2O 2 点燃 Fe 3O 43. 铜在空气中受热:2Cu + O 2 ≡≡≡ 2CuO4. 铝在空气中燃烧:4Al + 3O 2 点燃 2Al 2O 35.铝在空气中氧化:4Al + 3O 2 ===2Al 2O 36. 氢气中空气中燃烧:2H 2 + O 2 点燃 2H 2O7. 红磷在空气中燃烧:4P + 5O 2 点燃 2P 2O 5 8. 硫粉在空气中燃烧: S + O 2 点燃 SO 2 9. 碳在氧气中充分燃烧:C + O 2 点燃 CO 2 10. 碳在氧气不充分燃烧 2C + O 2 点燃 2CO11. 一氧化碳燃烧: 2CO + O 2 点燃 2CO 2 12. 碳与二氧化碳反应: CO 2+ C=== 2CO 13.二氧化碳溶于水:CO 2 + H 2O === H 2CO 3 14.三氧化硫溶于水: SO 3 + H 2O == H 2SO 415.生石灰与水反应:CaO + H 2O === Ca(OH)2二.分解反应: 16. 水在直流电的作用下分解: 2H 2O 通电 2H 2↑+ O 2 ↑ 17. 双氧水在二氧化锰作用下制取氧气 2H 2O 2 ===2H 2O+O 2↑ 18. 加热氯酸钾(二氧化锰作催化剂): 2KClO 3 ==== 2KCl + 3O 2 ↑ 19. 加热高锰酸钾: 2KMnO 4 == K 2MnO 4 + MnO 2 + O 2↑ 20. 碳酸不稳定:H 2CO 3 === H 2O + CO 2↑ 21. 高温煅烧石灰石:CaCO 3 高温 CaO + CO 2↑ 22.加热碱式碳酸铜: Cu 2(OH)2CO 3 = 2CuO + H 2O + CO 2↑ 23.加热碳酸氢铵 NH 4HCO 3 = NH 3 ↑+ H 2O + CO 2↑ 三.置换反应 24. 氢气还原氧化铜:H 2 + CuO Cu + H 2O25. 木炭还原氧化铜:C+ 2CuO 高温 2Cu + CO 2↑26. 焦炭还原氧化铁:3C+ 2Fe 2O 3 高温 4Fe + 3CO 2↑27. 焦炭还原四氧化三铁:2C+ Fe 3O 4 高温 3Fe + 2CO 2↑金属单质 + 酸 -------- 盐 + 氢气28. 稀硫酸制取氢气: Zn + H 2SO 4 = ZnSO 4 + H 2↑29. 铁和稀硫酸: Fe + H 2SO 4 = FeSO 4 + H 2↑30. 镁和稀硫酸: Mg + H 2SO 4 = MgSO 4 + H 2↑31. 铝和稀硫酸: 2Al +3H 2SO 4 = Al 2(SO 4)3 +3H 2↑32. 稀盐酸制取氢气: Zn + 2HCl === ZnCl 2 + H 2↑33. 铁和稀盐酸: Fe + 2HCl === FeCl 2 + H 2↑34. 镁和稀盐酸: Mg+ 2HCl === MgCl 2 + H 2↑35. 铝和稀盐酸: 2Al + 6HCl == 2AlCl 3 + 3H 2↑ 金属单质 + 盐(溶液) ------- 另一种金属 + 另一种盐36. 铁和硫酸铜溶液反应:Fe + CuSO 4 === FeSO 4 + Cu37. 铝和硫酸铜溶液反应:2Al + 3CuSO 4 === Al 2(SO 4)3 +3 Cu38. 铜和硝酸银溶液反应:Cu + 2AgNO 3=== Cu(NO 3)2 + 2Ag四、复分解反应 金属氧化物 +酸 -------- 盐 + 水39. 稀盐酸除铁锈: Fe 2O 3 + 6HCl === 2FeCl 3 + 3H 2O40. 稀硫酸除铁锈: Fe 2O 3 + 3H 2SO 4 === Fe 2(SO 4)3 + 3H 2O 41. 氧化铜和稀盐酸反应:CuO + 2HCl ==== CuCl 2 + H 2O 42. 氧化铜和稀硫酸反应:CuO + H 2SO 4 ==== CuSO 4 + H 2O △ △ △ △ MnO 2 高温 △ △ MnO 243. 稀硫酸腐蚀铝的表面: Al 2O 3 + 3H 2SO 4 === Al 2(SO 4)3 + 3H 2O(5)酸 + 碱 -------- 盐 + 水44.盐酸和烧碱起反应: HCl + NaOH ==== NaCl +H 2O45. 硫酸和氢氧化铜反应: H 2SO 4 + Cu(OH)2 ==== CuSO 4 + 2H 2O46. 盐酸和氢氧化钙反应: 2HCl + Ca(OH)2 ==== CaCl 2 + 2H 2O47. 盐酸和氢氧化铁反应: 3HCl + Fe(OH)3 ==== FeCl 3 + 3H 2O48. 氢氧化铝药物治疗胃酸过多: 3HCl + Al(OH)3 ==== AlCl 3 + 3H 2O49. 氢氧化镁药物治疗胃酸过多:2HCl + Mg(OH)2 ==== MgCl 2 + 2H 2O50. 硫酸和烧碱反应: H 2SO 4 + 2NaOH ==== Na 2SO 4 + 2H 2O51. 硝酸和烧碱反应: HNO 3+ NaOH ==== NaNO 3 +H 2O 酸 + 盐 -------- 另一种酸 + 另一种盐52.实验室制取二氧化碳: CaCO 3 + HCl === CaCl 2 + H 2O + CO 2↑53.苏打与稀盐酸反应: Na 2CO 3 + 2HCl === 2NaCl + H 2O + CO 2↑54.小苏打治疗胃酸过多: NaHCO 3 + HCl === NaCl + H 2O + CO 2↑55.盐酸和硝酸银溶液反应: HCl + AgNO 3 === AgCl↓ + HNO 356.硫酸和碳酸钠反应: Na 2CO 3 + H 2SO 4 === Na 2SO 4 + H 2O + CO 2↑57.硫酸和氯化钡溶液反应: H 2SO 4 + BaCl 2 ==== BaSO 4 ↓+ 2HCl58.硝酸和碳酸钡反应: BaCO 3 + 2HNO 3 === Ba (NO 3)2 + H 2O + CO 2↑碱 + 盐 -------- 另一种碱 + 另一种盐59.氢氧化钠与硫酸铜: 2NaOH + CuSO 4 ==== Cu(OH)2↓(蓝色) + Na 2SO 460.氢氧化钠与氯化铁: 3NaOH + FeCl 3 ==== Fe(OH)3↓ (红褐色)+ 3NaCl61.氢氧化钠与氯化镁: 2NaOH + MgCl 2 ==== Mg(OH)2↓(白色) + 2NaCl62. 纯碱与熟石灰制烧碱: Ca(OH)2 + Na 2CO 3 === CaCO 3↓(白色) + 2NaOH63. 碳酸钾与熟石灰: Ca(OH)2 + K 2CO 3 === CaCO 3↓(白色) + 2KOH盐 + 盐 ----- 两种新盐64.氯化钠溶液和硝酸银溶液: NaCl + AgNO 3 ==== AgCl↓ + NaNO 365.硫酸钠和硝酸钡: Na 2SO 4 + Ba (NO 3)2 ==== BaSO 4↓ + 2NaNO 366. 碳酸钠和氯化钙: Na 2CO 3 + CaCl 2 ==== CaCO 3↓ + 2Na Cl五.其它反应:67. 甲烷在空气中燃烧: CH 4 + 2O 2 点燃 CO 2 + 2H 2O68. 酒精在空气中燃烧: C 2H 5OH + 3O 2 点燃 2CO 2 + 3H 2O 69. 葡萄糖在体内缓慢氧化: C 6H 12O 6 + 6O 2 === 6CO 2 + 6H 2O 70. 一氧化碳还原氧化铜: CO+ CuO ===Cu + CO 271. 一氧化碳还原氧化铁: 3CO+ Fe 2O 3 高温 2Fe + 3CO 272. 一氧化碳还原四氧化三铁: 4CO+ Fe 3O 4 高温 3Fe + 4CO 2非金属氧化物 +碱 -------- 盐 + 水 (不是复分解反应) △ 酶73.苛性钠暴露在空气中变质:2NaOH + CO2 ==== Na2CO3 + H2O 74.苛性钠吸收二氧化硫气体:2NaOH + SO2 ==== Na2SO3 + H2O 75.苛性钠吸收三氧化硫气体:2NaOH + SO3 ==== Na2SO4 + H2O 76.石灰水检验二氧化碳:Ca(OH)2 + CO2 ==== CaCO3↓+ H2O 77. 石灰水吸收二氧化硫:Ca(OH)2 + SO2 ==== CaSO3↓+ H2O。
初中最重要的87个化学方程式

初中最重要的87个化学方程式化学是一门研究物质的性质、组成和变化的自然科学学科,对于初中生来说,化学方程式是学习化学知识的基础。
在初中阶段,学生需要掌握的化学方程式有很多,但其中有一些是最重要的,可以说是化学学习的重点。
下面我们就来详细介绍初中最重要的87个化学方程式。
首先,让我们来看看一些最基础的化学方程式。
其中最重要的有化学反应的基本概念,如生成氧气的反应:2KClO3→2KCl+3O2;生成氢气的反应:2H2O→2H2+O2;生成二氧化碳的反应:CO2+H2O→H2CO3。
这些简单的反应方程式,是学生学习化学的第一步。
接着是一些常见的酸碱中和反应的方程式。
学生需要了解酸与碱中和反应的化学方程,如盐酸与氢氧化钠的反应:HCl+NaOH→NaCl+H2O;硫酸与氢氧化钠的反应:H2SO4+2NaOH→Na2SO4+2H2O。
这些方程式是化学实验室中常见的反应,学生需要熟练掌握。
此外,学生还需要了解一些金属与非金属氧化物的反应。
比如金属氧化物与非金属氧化物的反应方程式:Fe2O3+2Al→2Fe+Al2O3;Na2O+H2O→2NaOH。
这些方程式是学生学习金属与非金属性质的重要参考。
另外,学生还需要了解一些氧化还原反应的方程式。
氧化还原反应是化学反应中的重要类型之一,学生需要明白氧化还原反应的基本概念。
比如氧化铁的还原反应:2Fe2O3+3C→4Fe+3CO2;铜与硝酸的反应:3Cu+8HNO3→3Cu(NO3)2+4H2O+2NO。
最后,学生还需要掌握一些单质与化合物反应、气体的制备和性质、实验室中的实际反应等内容。
这些方程式涵盖了化学学习的各个方面,是初中学生必须掌握的基本知识。
综上所述,初中最重要的87个化学方程式涵盖了化学学习的方方面面。
学生在学习这些方程式的过程中,不仅能够加深对化学知识的理解,还能够提高实验操作的能力。
因此,学生应该认真学习这些化学方程式,掌握好化学知识的基础,为今后的学习打下扎实的基础。
科学初中化学方程式大全完整版

科学初中化学方程式大全Document serial number【NL89WT-NY98YT-NC8CB-NNUUT-NUT108】【科学】初中化学方程式大全化学最重要的就是方程试了,所以一定要掌握化学方程式汇总 一.物质与氧气的反应: (1)单质与氧气的反应: 1.镁在空气中燃烧:2Mg+O 22MgO 2.铁在氧气中燃烧:3Fe+2O 2Fe 3O 4 3.铜在空气中受热:2Cu+O 22CuO 4.铝在空气中燃烧:4Al+3O 22Al 2O 3 5.氢气中空气中燃烧:2H 2+O 22H 2O 6.红磷在空气中燃烧:4P+5O 22P 2O 5 7.硫粉在空气中燃烧:S+O 2SO 2 8.碳在氧气中充分燃烧:C+O 2CO 2 9.碳在氧气中不充分燃烧:2C+O 22CO(2)化合物与氧气的反应: 10.一氧化碳在氧气中燃烧:2CO+O 22CO 211.甲烷在空气中燃烧:CH 4+2O 2CO2+2H 2O 12.酒精在空气中燃烧:C 2H 5OH+3O 22CO 2+3H 2O二.几个分解反应:13.水在直流电的作用下分解:2H 2O 2H 2↑+O 2↑ 14.加热碱式碳酸铜:Cu 2(OH)2CO 32CuO+H 2O+CO 2↑15.加热氯酸钾(有少量的二氧化锰):2KClO 3=2KCl+3O 2↑ 16.加热高锰酸钾:2KMnO 4K 2MnO 4+MnO 2+O 2↑17.碳酸不稳定而分解:H2CO3=H2O+CO2↑18.高温煅烧石灰石:CaCO3CaO+CO2↑三.几个氧化还原反应:19.氢气还原氧化铜:H2+CuO Cu+H2O20.木炭还原氧化铜:C+2CuO2Cu+CO2↑21.焦炭还原氧化铁:3C+2Fe2O34Fe+3CO2↑22.焦炭还原四氧化三铁:2C+Fe3O43Fe+2CO2↑23.一氧化碳还原氧化铜:CO+CuO Cu+CO224.一氧化碳还原氧化铁:3CO+Fe2O32Fe+3CO225.一氧化碳还原四氧化三铁:4CO+Fe3O43Fe+4CO2四.单质、氧化物、酸、碱、盐的相互关系(1)金属单质+酸=盐+氢气(置换反应)26.锌和稀硫酸Zn+H2SO4=ZnSO4+H2↑27.铁和稀硫酸Fe+H2SO4=FeSO4+H2↑28.镁和稀硫酸Mg+H2SO4=MgSO4+H2↑29.铝和稀硫酸2Al+3H2SO4=Al2(SO4)3+3H2↑30.锌和稀盐酸Zn+2HCl=ZnCl2+H2↑31.铁和稀盐酸Fe+2HCl=FeCl2+H2↑32.镁和稀盐酸Mg+2HCl=MgCl2+H2↑33.铝和稀盐酸2Al+6HCl=2AlCl3+3H2↑(2)金属单质+盐(溶液)=另一种金属+另一种盐34.铁和硫酸铜溶液反应:Fe+CuSO4=FeSO4+Cu35.锌和硫酸铜溶液反应:Zn+CuSO4=ZnSO4+Cu36.铜和硝酸汞溶液反应:Cu+Hg(NO3)2=Cu(NO3)2+Hg(3)碱性氧化物+酸=盐+水37.氧化铁和稀盐酸反应:Fe2O3+6HCl=2FeCl3+3H2O38.氧化铁和稀硫酸反应:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O39.氧化铜和稀盐酸反应:CuO+2HCl=CuCl2+H2O40.氧化铜和稀硫酸反应:CuO+H2SO4=CuSO4+H2O41.氧化镁和稀硫酸反应:MgO+H2SO4=MgSO4+H2O42.氧化钙和稀盐酸反应:CaO+2HCl=CaCl2+H2O(4)酸性氧化物+碱=盐+水43.苛性钠暴露在空气中变质:2NaOH+CO2=Na2CO3+H2O44.苛性钠吸收二氧化硫气体:2NaOH+SO2=Na2SO3+H2O45.苛性钠吸收三氧化硫气体:2NaOH+SO3=Na2SO4+H2O46.消石灰放在空气中变质:Ca(OH)2+CO2=CaCO3↓+H2O47.消石灰吸收二氧化硫:Ca(OH)2+SO2=CaSO3↓+H2O(5)酸+碱=盐+水48.盐酸和烧碱起反应:HCl+NaOH=NaCl+H2O49.盐酸和氢氧化钾反应:HCl+KOH=KCl+H2O50.盐酸和氢氧化铜反应:2HCl+Cu(OH)2=CuCl2+2H2O51.盐酸和氢氧化钙反应:2HCl+Ca(OH)2=CaCl2+2H2O52.盐酸和氢氧化铁反应:3HCl+Fe(OH)3=FeCl3+3H2O53.氢氧化铝药物治疗胃酸过多:3HCl+Al(OH)3=AlCl3+3H2O54.硫酸和烧碱反应:H2SO4+2NaOH=Na2SO4+2H2O55.硫酸和氢氧化钾反应:H2SO4+2KOH=K2SO4+2H2O56.硫酸和氢氧化铜反应:H 2SO 4+Cu(OH)2=CuSO 4+2H 2O 57.硫酸和氢氧化铁反应:3H 2SO 4+2Fe(OH)3=Fe 2(SO 4)3+6H 2O 58.硝酸和烧碱反应:HNO 3+NaOH=NaNO 3+H 2O (6)酸+盐=另一种酸+另一种盐59.大理石与稀盐酸反应:CaCO 3+2HCl=CaCl 2+H 2O+CO 2↑ 60.碳酸钠与稀盐酸反应:Na 2CO 3+2HCl=2NaCl+H2O+CO 2↑ 61.碳酸镁与稀盐酸反应:MgCO 3+2HCl=MgCl 2+H 2O+CO 2↑ 62.盐酸和硝酸银溶液反应:HCl+AgNO 3=AgCl↓+HNO 3 63.硫酸和碳酸钠反应:Na 2CO 3+H 2SO 4=Na 2SO 4+H 2O+CO 2↑ 64.硫酸和氯化钡溶液反应:H 2SO 4+BaCl 2=BaSO 4↓+2HCl (7)碱+盐=另一种碱+另一种盐65.氢氧化钠与硫酸铜:2NaOH+CuSO 4=Cu(OH)2↓+Na 2SO 4 66.氢氧化钠与氯化铁:3NaOH+FeCl 3=Fe(OH)3↓+3NaCl 67.氢氧化钠与氯化镁:2NaOH+MgCl 2=Mg(OH)2↓+2NaCl 68.氢氧化钠与氯化铜:2NaOH+CuCl 2=Cu(OH)2↓+2NaCl 69.氢氧化钙与碳酸钠:Ca(OH)2+Na 2CO 3=CaCO 3↓+2NaOH (8)盐+盐=两种新盐70.氯化钠溶液和硝酸银溶液:NaCl+AgNO 3=AgCl↓+NaNO 3 71.硫酸钠和氯化钡:Na 2SO 4+BaCl 2=BaSO 4↓+2NaCl 五.其它反应:72.二氧化碳溶解于水:CO 2+H 2O=H 2CO 3 73.生石灰溶于水:CaO+H 2O=Ca(OH)2 74.氧化钠溶于水:Na 2O+H 2O=2NaOH75.三氧化硫溶于水:SO3+H2O=H2SO476.硫酸铜晶体受热分解:CuSO45H2O加热CuSO4+5H2O77.无水硫酸铜作干燥剂:CuSO4+5H2O=CuSO4+5H2O。
初二科学化学方程式大全

科学化学式一、氧气的性质:(1)单质与氧气的反应:(化合反应)1.镁在空气中燃烧:2Mg+O2点燃2MgO2.铁在氧气中燃烧:3Fe+2O2点燃Fe3O43.铜在空气中受热:2Cu+O2加热2CuO4.铝在空气中燃烧:4Al+3O2点燃2Al2O35.氢气中空气中燃烧:2H2+O2点燃2H2O6.红磷在空气中燃烧(研究空气组成的实验):4P+5O2点燃2P2O57.硫粉在空气中燃烧:S+O2点燃SO28.碳在氧气中充分燃烧:C+O2点燃CO29.碳在氧气中不充分燃烧:2C+O2点燃2CO(2)化合物与氧气的反应:10.一氧化碳在氧气中燃烧:2CO+O2点燃2CO211.甲烷在空气中燃烧:CH4+2O2点燃CO2+2H2O12.酒精在空气中燃烧:C2H5OH+3O2点燃2CO2+3H2O(3)氧气的来源:13.玻义耳研究空气的成分实验2HgO加热Hg+O2↑14.加热高锰酸钾:2KMnO4加热K2MnO4+MnO2+O2↑(实验室制氧气原理1)15.过氧化氢在二氧化锰作催化剂条件下分解反应:H2O2MnO22H2O+O2↑(实验室制氧气原理2)二、自然界中的水:16.水在直流电的作用下分解(研究水的组成实验):2H2O通电2H2↑+O2↑17.生石灰溶于水:CaO+H2O==Ca(OH)218.二氧化碳可溶于水:H2O+CO2==H2CO3三、质量守恒定律:19.镁在空气中燃烧:2Mg+O2点燃2MgO20.铁和硫酸铜溶液反应:Fe+CuSO4===FeSO4+Cu21.氢气还原氧化铜:H2+CuO加热Cu+H2O22.镁还原氧化铜:Mg+CuO加热Cu+MgO四、碳和碳的氧化物:(1)碳的化学性质23.碳在氧气中充分燃烧:C+O2点燃CO224.木炭还原氧化铜:C+2CuO高温2Cu+CO2↑25.焦炭还原氧化铁:3C+2Fe2O3高温4Fe+3CO2↑(2)煤炉中发生的三个反应:(几个化合反应)26.煤炉的底层:C+O2点燃CO227.煤炉的中层:CO2+C高温2CO28.煤炉的上部蓝色火焰的产生:2CO+O2点燃2CO2(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应(实验室制二氧化碳):CaCO3+2HCl==CaCl2+H2O+CO2↑30.碳酸不稳定而分解:H2CO3==H2O+CO2↑31.二氧化碳可溶于水:H2O+CO2==H2CO332.高温煅烧石灰石(工业制二氧化碳):CaCO3高温CaO+CO2↑33.石灰水与二氧化碳反应(鉴别二氧化碳):Ca(OH)2+CO2===CaCO3↓+H2O(4)一氧化碳的性质:34.一氧化碳还原氧化铜:CO+CuO加热Cu+CO235.一氧化碳的可燃性:2CO+O2点燃2CO2其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理):Na2CO3+2HCl==2NaCl+H2O+CO2↑五、燃料及其利用:37.甲烷在空气中燃烧:CH4+2O2点燃CO2+2H2O38.酒精在空气中燃烧:C2H5OH+3O2点燃2CO2+3H2O39.氢气中空气中燃烧:2H2+O2点燃2H2O六、金属(1)金属与氧气反应:40.镁在空气中燃烧:2Mg+O2点燃2MgO41.铁在氧气中燃烧:3Fe+2O2点燃Fe3O413.铜在空气中受热:2Cu+O2加热2CuO14.铝在空气中形成氧化膜:4Al+3O2=2Al2O3(2)金属单质+酸--------盐+氢气(置换反应)15.锌和稀硫酸Zn+H2SO4=ZnSO4+H2↑16.铁和稀硫酸Fe+H2SO4=FeSO4+H2↑17.镁和稀硫酸Mg+H2SO4=MgSO4+H2↑18.铝和稀硫酸2Al+3H2SO4=Al2(SO4)3+3H2↑19.锌和稀盐酸Zn+2HCl==ZnCl2+H2↑20.铁和稀盐酸Fe+2HCl==FeCl2+H2↑21.镁和稀盐酸Mg+2HCl==MgCl2+H2↑51.铝和稀盐酸2Al+6HCl==2AlCl3+3H2↑(3)金属单质+盐(溶液)-------新金属+新盐24.铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu25.锌和硫酸铜溶液反应:Zn+CuSO4==ZnSO4+Cu26.铜和硝酸汞溶液反应:Cu+Hg(NO3)2==Cu(NO3)2+Hg(3)金属铁的治炼原理:55.3CO+2Fe2O3高温4Fe+3CO2↑。
人教版八年级科学化学方程式整理

13、电解水:2H2O=====2H2↑+O2↑
14、碳酸不稳定分解:H2CO3===H2O+CO2↑
15、高温煅烧石灰石:CaCO3=====CaO+CO2↑
16、硫酸铜晶体受热失去结晶水:CuSO4·5H2O====CuSO4+5H2O
7、氢气在氧气中燃烧:2H2+O2======2H2O
8、一氧化碳在空气中燃烧:2CO+O2=====2CO2
9、碳不充分燃烧:2C+O2(不充分)=====2CO
10、二氧化碳与水反应:CO2+H2O=====H2CO3
(二)分解反应:
11、氯酸钾与二氧化锰共热(实验室制O2):2KClO3======2KCl+3O2↑
17、过氧化氢(双氧水)分解:2H2O2=====2H2O+O2
(三)其他:
18、大理石和稀盐酸(实验室制CO2H2O+CO2↑
19、氢氧化钠和硫酸铜:2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
20、碳酸钠和盐酸(灭火器原理):Na2CO3+2HCl=2NaCl+H2O+CO2↑
八年级下册化学方程式整理
(一)化合反应:
1、木炭在氧气中燃烧:C+O2=====CO2
2、硫在氧气中燃烧:S+O2======SO2
3、镁在空气中燃烧:2Mg+O2=====2MgO
4、铁在氧气中燃烧:3Fe+2O2=====Fe3O4
5、磷在氧气中燃烧:4P+5O2=====2P2O5
初中化学方程式大全及现象总结

初中化学方程式大全及现象总结一、化合反应:1.金属与非金属元素的化合反应例如:2Mg+O2→2MgO现象:镁与氧气反应后生成氧化镁,并放出大量的热。
2.金属氧化物和非金属元素的化合反应例如:2CuO+C→2Cu+CO2现象:铜氧化物与碳反应后生成铜和二氧化碳,并放出大量的热。
3.非金属氧化物和非金属元素的化合反应例如:P4+5O2→P4O10现象:磷与氧气反应生成五氧化二磷,并放出大量热。
二、分解反应:1.金属氢化物的分解反应例如:2NaH→2Na+H2现象:金属氢化物加热分解生成金属和氢气。
2.金属碳酸盐的分解反应例如:CaCO3→CaO+CO2现象:金属碳酸盐加热分解生成金属氧化物和二氧化碳。
3.金属过氧化物和金属超氧化物的分解反应例如:2H2O2→2H2O+O2现象:过氧化氢加热分解生成水和氧气。
三、置换反应:1.单个活泼金属与酸反应的置换反应例如:2Al+6HCl→2AlCl3+3H2现象:活泼金属与酸反应生成相应的金属盐和氢气。
2.活泼金属与金属盐溶液反应的置换反应例如:2Ag+2HCl→2AgCl+H2现象:活泼金属与金属盐溶液反应生成相应的沉淀和氢气。
3.金属与酸酐反应的置换反应例如:2Na+S→Na2S现象:金属与酸酐反应生成相应的化合物。
四、双替换反应:1.酸与碱的双替换反应例如:HCl+NaOH→NaCl+H2O现象:酸与碱反应生成相应的盐和水。
2.氯化物与硝酸盐的双替换反应例如:2NaCl+H2SO4→2HCl+Na2SO4现象:氯化物与硝酸盐反应生成盐酸和硫酸钠。
五、氧化还原反应:1.单质与非金属氧化物的氧化还原反应例如:C+O2→CO2现象:碳与氧气反应生成二氧化碳。
2.单质与金属氧化物的氧化还原反应例如:2Fe+3O2→2Fe2O3现象:铁与氧气反应生成三氧化二铁。
初三化学必背知识点方程式

初三化学必背知识点方程式一、必背化学方程式。
1. 氧气的制取。
- 过氧化氢分解制取氧气。
- 化学方程式:2H_2O_2{MnO_2}{===}2H_2O + O_2↑- 反应原理:过氧化氢在二氧化锰作催化剂的条件下分解生成水和氧气。
- 氯酸钾分解制取氧气。
- 化学方程式:2KClO_3{MnO_2,}{===}2KCl+3O_2↑- 反应原理:氯酸钾在二氧化锰作催化剂并加热的条件下分解生成氯化钾和氧气。
- 高锰酸钾分解制取氧气。
- 化学方程式:2KMnO_4{}{===}K_2MnO_4+MnO_2+O_2↑- 反应原理:高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气。
2. 氢气的制取。
- 锌和稀硫酸反应制取氢气。
- 化学方程式:Zn + H_2SO_4===ZnSO_4+H_2↑- 反应原理:锌的活动性比氢强,能置换出稀硫酸中的氢元素生成氢气。
3. 二氧化碳的制取。
- 大理石(或石灰石)与稀盐酸反应制取二氧化碳。
- 化学方程式:CaCO_3+2HCl===CaCl_2+H_2O + CO_2↑- 反应原理:碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳。
大理石或石灰石的主要成分是碳酸钙。
4. 水的电解。
- 化学方程式:2H_2O{通电}{===}2H_2↑+O_2↑- 反应现象:电极上有气泡产生,正极产生的气体能使带火星的木条复燃(氧气),负极产生的气体能燃烧,产生淡蓝色火焰(氢气),氢气和氧气的体积比约为2:1。
5. 碳的化学性质相关方程式。
- 碳在氧气中充分燃烧。
- 化学方程式:C + O_2{点燃}{===}CO_2- 反应现象:发出白光,放出热量,生成能使澄清石灰水变浑浊的气体。
- 碳在氧气中不充分燃烧。
- 化学方程式:2C+O_2{点燃}{===}2CO- 碳还原氧化铜。
- 化学方程式:C + 2CuO{高温}{===}2Cu+CO_2↑- 反应现象:黑色固体逐渐变成红色,生成能使澄清石灰水变浑浊的气体。
p初中科学化学方程式汇总

沿河二中初三化学方程式汇总1、与氧有关的化学方程式:2Mg+O2===2MgO 现象:燃烧、放出大量的热、同时放出耀眼的白光S+O2 ===SO2 现象:空气中是淡蓝色的火焰;纯氧中是蓝紫色的火焰;同时生成有刺激性气味的气体。
C+O2===CO2 现象:燃烧,淡蓝色火焰,生成能够让澄清石灰水浑浊的气体2C+O2===2CO 现象:燃烧,淡蓝色火焰4P+5O2===2P2O5 现象::生成白烟3Fe+2O2===Fe3O4 现象:剧烈燃烧、火星四射、生成黑色的固体2H2+O2===2H2O 现象:淡蓝色的火焰2H2O2===2H2O+O2↑现象:溶液里冒出大量的气泡2HgO===2Hg+O2↑现象:生成银白色的液体金属2KClO3===2KCl+3O2↑现象:生成能让带火星的木条复燃的气体2KMnO4==K2MnO4+MnO2+O2↑现象:同上,2、跟氢有关的化学方程式:2H2+O2===2H2O 现象:淡蓝色的火焰Zn+H2SO4==ZnSO4+H2↑现象:有可燃烧的气体生成Mg+H2SO4==MgSO4+H2↑现象:同上Fe+H2SO4 ==FeSO4+H2↑现象:变成浅绿色的溶液,同时放出气体2Al+3H2SO4 ==Al2(SO4)3+3H2↑现象:有气体生成Zn+2HCl==ZnCl2+H2↑现象:同上Mg+2HCl==MgCl2+H2↑现象:同上Fe+2HCl==FeCl2+H2↑现象:溶液变成浅绿色,同时放出气体2Al+6HCl==2AlCl3+3H2↑现象:有气体生成H2+CuO====Cu+H2O 现象:由黑色的固体变成红色的,同时有水珠生成2Fe2O3+3H2 ==2Fe+3H2O 现象:有水珠生成,固体颜色由红色变成银白色3、跟碳有关的化学方程式:C+O2==CO2(氧气充足的情况下) 现象:生成能让纯净的石灰水变浑浊的气体2C+O2===2CO(氧气不充足的情况下) 现象:不明显C+2CuO==2Cu+CO2↑现象:固体由黑色变成红色并减少,同时有能使纯净石灰水变浑浊的气体生成3C+2Fe2O3==4Fe+3CO2↑现象:固体由红色逐渐变成银白色,同时黑色的固体减少,有能使纯净的石灰水变浑浊的气体生成CO2+C===2CO 现象:黑色固体逐渐减少3C+2H2O=CH4+2CO 现象:生成的混和气体叫水煤气,都是可以燃烧的气体4、跟二氧化碳有关的化学方程式:C+O2点燃====CO2 现象:生成能使纯净的石灰水变浑浊的气体Ca(OH)2+CO2===CaCO3↓+H2O 现象:生成白色的沉淀,用于检验二氧化碳CaCO3+CO2+H2O===Ca(HCO3)2 现象:白色固体逐渐溶解Ca(HCO3)===CaCO3↓+CO2↑+H2O 现象:生成白色的沉淀,同时有能使纯净的石灰水变浑浊的气体生成Cu2(OH)2CO3=2CuO+H2O+CO2↑现象:固体由绿色逐渐变成黑色,同时有能使纯净石灰水变浑浊的气体生成2NaOH+CO2===Na2CO3+H2O(也可为KOH)现象:不明显CaCO3===CaO+CO2↑现象:有能使纯净石灰水变浑浊的气体生成跟一氧化碳有关的,但同时也跟二氧化碳有关:Fe3O4+4CO====3Fe+4CO2 现象:固体由黑色变成银白色,同时有能使纯净石灰水变浑浊的气体生成FeO+CO===Fe+CO2 现象:固体由黑色逐渐变成银白色,同时有能使纯净石灰水变浑浊的气体生成Fe2O3+3CO====2Fe+3CO2 现象:固体由红色逐渐变成银白色,同时有能使纯净石灰水变浑浊的气体生成CuO+CO====Cu+CO2 现象:固体由黑色变成红色,同时有能使纯净石灰水变浑浊的气体生成5、跟盐酸有关的化学方程式:NaOH(也可为KOH)+HCl==NaCl+H2O 现象:不明显HCl+AgNO3==AgCl↓+HNO3 现象:有白色沉淀生成,这个反应用于检验氯离子CaCO3+2HCl==CaCl2+H2O+CO2↑现象:百色固体溶解,生成能使纯净石灰水变浑浊的气体Na2CO3+2HCl==2NaCl+H2O+CO2↑现象:生成能使纯净石灰水变浑浊的气体NaHCO3+HCl==NaCl+H2O+CO2↑现象:生成能使纯净石灰水变浑浊的气体Fe2O3+6HCl==2FeCl3+3H2O 现象:红色固体逐渐溶解,形成黄色的溶液Fe(OH)3+3HCl==FeCl3+3H2O 现象:红棕色絮状沉淀溶解,形成了黄色的溶液Cu(OH)2+2HCl==CuCl2+2H2O 现象:蓝色沉淀溶解,形成黄绿色的溶液CuO+2HCl==CuCl2+H2O 现象:黑色固体溶解,生成黄绿色的溶液Zn+2HCl==ZnCl2+H2↑现象:同上Mg+2HCl==MgCl2+H2↑现象:同上Fe+2HCl==FeCl2+H2↑现象:溶液变成浅绿色,同时放出气体2Al+6HCl==2AlCl3+3H2↑现象:有气体生成6、跟硫酸有关的化学方程式:2NaOH(或KOH)+H2SO4==Na2SO4+2H2O 现象:不明显Fe2O3+3H2SO4==Fe2(SO4)3+3H2O 现象:红色固体溶解,生成黄色溶液CuO+H2SO4==CuSO4+H2O 现象:黑色固体溶解,生成蓝色溶液Cu(OH)2+H2SO4==CuSO4+2H2O 现象:蓝色沉淀溶解,生成蓝色溶液H2SO4+BaCl2==BaSO4↓+2HCl 现象:生成不溶于强酸的白色沉淀,用于检验硫酸根离子CaCO3+H2SO4==CaSO4+H2O+CO2↑Na2CO3+H2SO4==Na2SO4+H2O+CO2↑2NaHCO3+H2SO4==Na2SO4+2H2O+2CO2↑现象:这三个反应现象同与盐酸反应现象一致7、跟硝酸有关的化学方程式:Fe2O3+6HNO3==2Fe(NO3)3+3H2O 现象:红色固体溶解,生成黄色溶液CuO+2HNO3==Cu(NO3)2 +H2O 现象:黑色固体溶解,生成蓝色溶液Cu(OH)2+2HNO3==Cu(NO3)2+2H2O 现象:蓝色沉淀溶解,生成蓝色溶液NaOH(或KOH)+HNO3==NaNO3+H2O 现象:不明显Mg(OH)2+2HNO3==Mg(NO3)2+2H2O 现象:白色沉淀溶解CaCO3+2HNO3==Ca(NO3)2+H2O+CO2↑Na2CO3+2HNO3==2NaNO3+H2O+CO2↑NaHCO3+HNO3==NaNO3+H2O+CO2↑现象:以上三个反应现象同与盐酸反应现象一致8、跟碱有关的化学方程式:NaOH+HCl(或HNO3、H2SO4)==NaCl+H2O 现象:酸碱中和反应,现象不明显CaO+H2O==Ca(OH)2现象:放出大量的热NaOH(KOH)+FeCl3(Fe(NO3)3、Fe2(SO4)3)==Fe(OH)3↓+NaCl 现象:生成红棕色絮状沉淀,括号里面的反应过程相似,产物相对应就行了2NaOH(KOH)+FeCl2(Fe(NO3)2、FeSO4)==Fe(OH)2↓+2NaCl 现象:生成白色絮状沉淀,括号里面的反映过程相似,产物相对应就行了2NaOH(KOH)+CuCl2(Cu(NO3)2、CuSO4)==Cu(OH)2↓+2NaCl 现象:生成蓝色絮状沉淀,括号里面的反应过程相似,产物相对应就行了NH4Cl(NH4NO3、(NH4)2SO4)+NaOH(KOH)==NH3↑+H2O+NaCl 现象:有可以使石蕊试纸变蓝的气体生成MgCl2(Mg(NO3)2、MgSO4)+NaOH(KOH)==Mg(OH)2↓+NaCl 现象:生成白色沉淀,括号里面的反应过程相似,产物相对应就行了NaHCO3+NaOH==Na2CO3+H2O 现象:不明显此反应的Na换成K是一样的Ca(HCO3)2+2NaOH==CaCO3↓+Na2CO3+2H2O 现象:生成白色沉淀,此反应把Na换成K是一样的2NaOH+CO2==Na2CO3+H2O 现象:无明显现象此反应的Na换成K是一样的Ca(OH)2+CO2==CaCO3↓+H2O 现象:产生白色沉淀,此反应用于检验二氧化碳NaHSO4+NaOH==Na2SO4+H2O 现象:无明显现象2NaOH+SO2==Na2SO3+H2O 现象:无明显现象9、跟钡盐有关的化学方程式:BaCl2+Na2SO4==BaSO4↓+2NaCl 现象:有白色的不溶于强酸的沉淀生成BaCl2+Na2CO3==BaCO3↓+2NaCl 现象:有白色沉淀生成但可溶于盐酸和硝酸,其实也溶于硫酸,但生成硫酸钡沉淀,不容易看出来10、跟钙盐有关的化学方程式:CaCl2+Na2CO3==CaCO3↓+2NaCl 现象:生成白色沉淀CaCO3+CO2+H2O==Ca(HCO3)2 现象:固体逐渐溶解Ca(HCO3)2+Ca(OH)2==2CaCO3↓+2H2O 现象:生成白色沉淀11、跟几种金属及其盐有关的化学方程式:(1)铜:CuSO4•5H2O===CuSO4+5H2O↑现象:固体由蓝色变为白色CuO+CO====Cu+CO2 现象:固体由黑色逐渐变成红色,同时有能使纯净的石灰水变浑浊的气体生成H2+CuO====Cu+H2O 现象:固体由黑色逐渐变成红色,同时有水珠生成Cu+2AgNO3==Cu (NO3)2+2Ag 现象:铜表面慢慢生成了银白色金属CuCl2+2NaOH==Cu (OH) 2↓+2NaCl 现象:生成了蓝色絮状沉淀CuO+H 2SO 4==CuSO 4+H 2O 现象:黑色固体溶解,生成蓝色溶液 Cu (OH) 2+H 2SO 4==CuSO 4+2H 2O 现象:蓝色沉淀溶解,生成蓝色溶液 Fe(Zn)+CuSO 4==FeSO 4+Cu 现象:有红色金属生成 Cu 2(OH)2CO 3==2CuO+H 2O+CO 2↑ 现象:固体由绿色逐渐变成黑色,同时有能使纯净石灰水变浑浊的气体生成(2)铁:Fe+2HCl==FeCl 2+H 2 现象:铁粉慢慢减少,同时有气体生成,溶液呈浅绿色 FeCl 2+2NaOH==Fe(OH)2↓+NaCl 现象:有白色絮状沉淀生成 4Fe(OH)2+O 2+2H 2O==4Fe(OH)3 现象:氢氧化铁在空气中放置一段时间后,会变成红棕色 Fe (OH) 3+3HCl==FeCl 3+3H 2O 现象:红棕色絮状沉淀溶解,溶液呈黄色 Fe (OH) 2+2HCl==FeCl 2+2H 2O 现象:白色絮状沉淀溶解,溶液呈浅绿色 Fe+CuSO 4==FeSO 4+Cu 现象:铁溶解生成红色金属 Fe+AgNO 3==Fe(NO 3)2+Ag 现象:铁溶解生成银白色的金属 Fe 2O 3+6HCl==2FeCl 3+3H 2O 现象:红色固体溶解,生成黄色的溶液 23432Fe O Fe O 点燃= 现象:铁剧烈燃烧,火星四射,生成黑色的固体 Zn+FeCl 2==ZnCl 2+Fe 现象:锌粉慢慢溶解,生成铁(3)银:AgNO 3+HCl==AgCl ↓+HNO 3 现象:有白色沉淀生成,且不溶于强酸 AgNO 3+NaCl==AgCl ↓+NaNO 3 现象:有白色沉淀生成,且不溶于强酸 Cu+2AgNO 3==Cu(NO 3)2+2Ag 现象:红色的铜逐渐溶解,同时有银白色的金属生成 2AgNO 3+Na 2SO 4==Ag 2SO 4↓+2NaNO 3 现象:有白色沉淀生成(4)补充化学方程式:3Ag+4HNO 3(稀)==3AgNO 3+NO ↑+2H 2O 现象:银逐渐溶解,生成气体遇空气变棕色 Ag+2HNO 3(浓)==AgNO3+NO 2↑+H 2O 现象:银逐渐溶解,生成棕色气体 Cu+2H 2SO4(浓)==CuSO 4+SO 2↑+2H 2O 现象:铜逐渐溶解,生成有刺激性气味的气体 2FeCl 3+Fe==3FeCl 2 现象:铁粉逐渐溶解,溶液由黄色变成浅绿色 2Na 2O 2(过氧化钠)+2H 2O=4NaOH+O 2 现象:有能使带火星的木条复燃的气体生成。
初中科学 常见的化学方程式

常见的化学方程式化合反应●红磷在空气中燃烧,产生白烟:4P+5O22P2O5白磷自燃:4P+5O2=2P2O5●木炭充分燃烧:C+O2CO2●木炭不充分燃烧:2C+O22CO●硫在空气(氧气)中燃烧:S+O2SO2●铁丝在氧气中燃烧:3Fe+2O2Fe3O4●铝在氧气中燃烧:4Al+3O22Al2O3铝不易生锈的原因:4Al+3O2=2Al2O3●镁在空气中燃烧:2Mg+O22MgO●铜在空气中加热:2Cu+O22CuO●氢气在氧气中燃烧:2H2+O22H2O●将CO2变成CO:C+CO22CO●二氧化碳溶于水形成碳酸:CO2+H2O=H2CO3●用生石灰制取熟石灰:CaO+H2O=Ca(OH)2●一氧化碳燃烧:2CO+O22CO2●向澄清的石灰水中通入过量的二氧化碳,变浑浊的石灰水又变澄清:CaCO3+CO2+H2O=Ca(HCO3)2●氢气在氯气中燃烧:H2+Cl22HCl钠在氯气中燃烧:2Na+Cl22NaCl镁在氮气中燃烧:3Mg+N2Mg3N2(注意氮元素的化合价)上面三个化学方程式给我们的启示是:燃烧不一定有氧气参与。
分解反应●汞在空气中加热:2Hg+O22HgO●氧化汞加强热:2HgO2Hg+O2↑●分解过氧化氢制取氧气(实验室制取氧气的反应原理之一):2H2O22H2O+O2↑加热高锰酸钾制取氧气(实验室制取氧气的反应原理之一):2KMnO4K2MnO4+MnO2+O2↑加热氯酸钾制取氧气(实验室制取氧气的反应原理之一):2KClO32KCl+3O2↑分解过氧化氢制取氧气符合绿色化学的观念,是三种方案中最安全、最节约资源的一种。
●电解水生成氢气和氧气:2H2O2H2↑+O2↑●工业制取生石灰和CO2的反应原理:CaCO3CaO+CO2↑●干粉灭火器的反应原理(碳酸氢钠受热分解):2NaHCO3Na2CO3+H2O+CO2↑●碱式碳酸铜受热分解:Cu2(OH)2CO32CuO+H2O+CO2↑●过氧化氢溶液不稳定,发生分解:2H2O2=2H2O+O2↑●碳酸不稳定,分解成水和二氧化碳:H2CO3=H2O+CO2↑●碳铵(碳酸氢铵)“消失”并发出刺激性气味:NH4HCO3=NH3↑+CO2↑+H2O●石笋、钟乳石的形成过程:CaCO3+CO2+H2O=Ca(HCO3)2 Ca(HCO3)2=CaCO3↓+CO2↑+H2O置换反应●氢气还原氧化铜:H2+CuO Cu+H2O●木炭还原氧化铜:C+2CuO2Cu+CO2↑●木炭还原氧化铁:3C+2Fe2O34Fe+3CO2↑●水煤气的形成:C+H2O H2+CO(注意没有气体生成符号↑)●实验室制取氢气的反应原理:Zn+H2SO4=ZnSO4+H2↑●金属与稀盐酸的反应⏹2X+2HCl=2X Cl+H2↑(X是+1价的金属,包括K、Na)⏹X+2HCl=X Cl2+H2↑(X是+2价的金属,包括Ca、Mg、Zn、Fe)⏹2Al+6HCl=2AlCl3+3H2↑●金属与稀硫酸的反应⏹2X+H2SO4=X2SO4+H2↑(X是+1价的金属,包括K、Na)⏹X+H2SO4=X SO4+H2↑(X是+2价的金属,包括Ca、Mg、Zn、Fe)⏹2Al+3H2SO4=Al2(SO4)3+3H2↑●金属与盐溶液的反应⏹镁◆3Mg+2AlCl3=3MgCl2+2Al3Mg+Al2(SO4)3=3MgSO4+2Al3Mg+2Al(NO3)3=3Mg(NO3)2+2Al◆Mg+X Cl2=MgCl2+X(X是+2价的金属,包括Zn、Fe、Cu)◆Mg+X SO4=MgSO4+X(X是+2价的金属,包括Zn、Fe、Cu)◆Mg+X(NO3)2=Mg(NO3)2+X(X是+2价的金属,包括Zn、Fe、Cu)◆Mg+2AgNO3=Mg(NO3)2+2Ag⏹铝◆2Al+3X Cl2=2AlCl3+3X(X是+2价的金属,包括Zn、Fe、Cu)◆2Al+3X SO4=Al2(SO4)3+3X(X是+2价的金属,包括Zn、Fe、Cu)◆2Al+3X(NO3)2=2Al(NO3)3+3X(X是+2价的金属,包括Zn、Fe、Cu)◆Al+3AgNO3=Al(NO3)3+3Ag⏹锌◆Zn+X Cl2=ZnCl2+X(X是+2价的金属,包括Fe、Cu)◆Zn+X SO4=ZnSO4+X(X是+2价的金属,包括Fe、Cu)◆Zn+X(NO3)2=Zn(NO3)2+X(X是+2价的金属,包括Fe、Cu)◆Zn+2AgNO3=Zn(NO3)2+2Ag⏹铁◆Fe+CuCl2=FeCl2+Cu◆Fe+CuSO4=FeSO4+Cu◆Fe+Cu(NO3)3=Fe(NO3)3+Cu◆Fe+2AgNO3=Fe(NO3)2+2Ag⏹铜:Cu+2AgNO3=Cu(NO3)2+2Ag⏹K、Ca、Na不遵循这样的置换反应,它们与盐溶液反应时,会先和水反应生成对应的碱,然后再和盐溶液反应。
初中科学化学方程式

初中科学化学方程式
嘿,朋友们!咱来聊聊初中科学里超重要的化学方程式吧!比如说氢气燃烧的方程式:2H₂ + O₂ → 2H₂O。
这就好像是氢气和氧气在跳一场欢快
的舞蹈,它们手牵手变成了水呀!你想想看,过年的时候放的烟花,那里面不就有氢气燃烧产生的美丽光芒嘛!
再看看铁和硫酸铜溶液反应的方程式:Fe + CuSO₄ → FeSO₄ + Cu。
就好像铁是个勇敢的战士,一下子就把硫酸铜里的铜给“抢”过来了自己身边,多厉害呀!这不,在我们生活中,铁制品用久了会生锈,就是因为铁和空气中的氧气等发生了类似这样的反应呢。
还有碳酸钙和盐酸反应:CaCO₃ + 2HCl → CaCl₂ + H₂O + CO₂↑。
这不就像是碳酸钙这个小家伙被盐酸刺激了,“噗”地放出了二氧化碳气体嘛!你去买瓶碳酸饮料,打开的时候“滋滋”冒气,那里面可就有类似这样的反应在发生哟!哈哈,化学方程式是不是很有趣呀?。
初二科学化学方程式大全

科学化学式一、氧气的性质:(1)单质与氧气的反应:(化合反应)1. 镁在空气中燃烧:2Mg + O2 点燃 2MgO2. 铁在氧气中燃烧:3Fe + 2O2 点燃 Fe3O43. 铜在空气中受热:2Cu + O2 加热 2CuO4. 铝在空气中燃烧:4Al + 3O2 点燃 2Al2O35. 氢气中空气中燃烧:2H2 + O2 点燃 2H2O6. 红磷在空气中燃烧(研究空气组成的实验):4P + 5O2 点燃 2P2O57. 硫粉在空气中燃烧: S + O2 点燃 SO28. 碳在氧气中充分燃烧:C + O2 点燃 CO29. 碳在氧气中不充分燃烧:2C + O2 点燃 2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO + O2 点燃 2CO211. 甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O12. 酒精在空气中燃烧:C2H5OH + 3O2 点燃 2CO2 + 3H2O(3)氧气的来源:13.玻义耳研究空气的成分实验 2HgO 加热 Hg+ O2 ↑14.加热高锰酸钾:2KMnO4 加热 K2MnO4 + MnO2 + O2↑(实验室制氧气原理1)15.过氧化氢在二氧化锰作催化剂条件下分解反应: H2O2 MnO22H2O+ O2 ↑(实验室制氧气原理2)二、自然界中的水:16.水在直流电的作用下分解(研究水的组成实验):2H2O 通电 2H2↑+ O2 ↑17.生石灰溶于水:CaO + H2O == Ca(OH)218.二氧化碳可溶于水: H2O + CO2==H2CO3三、质量守恒定律:19.镁在空气中燃烧:2Mg + O2 点燃 2MgO20.铁和硫酸铜溶液反应:Fe + CuSO4 === FeSO4 + Cu21.氢气还原氧化铜:H2 + CuO 加热 Cu + H2O22. 镁还原氧化铜:Mg + CuO 加热 Cu + MgO四、碳和碳的氧化物:(1)碳的化学性质23. 碳在氧气中充分燃烧:C + O2 点燃 CO224.木炭还原氧化铜:C+ 2CuO 高温 2Cu + CO2↑25.焦炭还原氧化铁:3C+ 2Fe2O3 高温 4Fe + 3CO2↑(2)煤炉中发生的三个反应:(几个化合反应)26.煤炉的底层:C + O2 点燃 CO227.煤炉的中层:CO2 + C 高温 2CO28.煤炉的上部蓝色火焰的产生:2CO + O2 点燃 2CO2(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应(实验室制二氧化碳):CaCO3 + 2HCl == CaCl2 + H2O + CO2↑30.碳酸不稳定而分解:H2CO3 == H2O + CO2↑31.二氧化碳可溶于水: H2O + CO2== H2CO332.高温煅烧石灰石(工业制二氧化碳):CaCO3 高温 CaO + CO2↑33.石灰水与二氧化碳反应(鉴别二氧化碳):Ca(OH)2 + CO2 === CaCO3 ↓+ H2O(4)一氧化碳的性质:34.一氧化碳还原氧化铜:CO+ CuO 加热 Cu + CO235.一氧化碳的可燃性:2CO + O2 点燃 2CO2其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理):Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑五、燃料及其利用:37.甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O38.酒精在空气中燃烧:C2H5OH + 3O2 点燃 2CO2 + 3H2O39.氢气中空气中燃烧:2H2 + O2 点燃 2H2O六、金属(1)金属与氧气反应:40.镁在空气中燃烧:2Mg + O2 点燃 2MgO41.铁在氧气中燃烧:3Fe + 2O2 点燃 Fe3O442. 铜在空气中受热:2Cu + O2 加热 2CuO43. 铝在空气中形成氧化膜:4Al + 3O2 = 2Al2O3(2)金属单质 + 酸 -------- 盐 + 氢气(置换反应)44. 锌和稀硫酸Zn + H2SO4 = ZnSO4 + H2↑45. 铁和稀硫酸Fe + H2SO4 = FeSO4 + H2↑46. 镁和稀硫酸Mg + H2SO4 = MgSO4 + H2↑47. 铝和稀硫酸2Al +3H2SO4 = Al2(SO4)3 +3 H2↑48. 锌和稀盐酸Zn + 2HCl == ZnCl2 + H2↑49. 铁和稀盐酸Fe + 2HCl == FeCl2 + H2↑50. 镁和稀盐酸Mg+ 2HCl == MgCl2 + H2↑51.铝和稀盐酸2Al + 6HCl == 2AlCl3 + 3 H2↑(3)金属单质 + 盐(溶液) ------- 新金属 + 新盐52. 铁和硫酸铜溶液反应:Fe + CuSO4 == FeSO4 + Cu53. 锌和硫酸铜溶液反应:Zn + CuSO4 ==ZnSO4 + Cu54. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 == Cu(NO3)2 + Hg (3)金属铁的治炼原理:55.3CO+ 2Fe2O3 高温 4Fe + 3CO2↑。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
沿河二中初三化学方程式汇总1、与氧有关的化学方程式:2Mg+O2===2MgO 现象:燃烧、放出大量的热、同时放出耀眼的白光S+O2 ===SO2 现象:空气中是淡蓝色的火焰;纯氧中是蓝紫色的火焰;同时生成有刺激性气味的气体。
C+O2===CO2 现象:燃烧,淡蓝色火焰,生成能够让澄清石灰水浑浊的气体2C+O2===2CO 现象:燃烧,淡蓝色火焰4P+5O2===2P2O5 现象::生成白烟3Fe+2O2===Fe3O4 现象:剧烈燃烧、火星四射、生成黑色的固体2H2+O2===2H2O 现象:淡蓝色的火焰2H2O2===2H2O+O2↑现象:溶液里冒出大量的气泡2HgO===2Hg+O2↑现象:生成银白色的液体金属2KClO3===2KCl+3O2↑现象:生成能让带火星的木条复燃的气体2KMnO4==K2MnO4+MnO2+O2↑现象:同上,2、跟氢有关的化学方程式:2H2+O2===2H2O 现象:淡蓝色的火焰Zn+H2SO4==ZnSO4+H2↑现象:有可燃烧的气体生成Mg+H2SO4==MgSO4+H2↑现象:同上Fe+H2SO4 ==FeSO4+H2↑现象:变成浅绿色的溶液,同时放出气体2Al+3H2SO4 ==Al2(SO4)3+3H2↑现象:有气体生成Zn+2HCl==ZnCl2+H2↑现象:同上Mg+2HCl==MgCl2+H2↑现象:同上Fe+2HCl==FeCl2+H2↑现象:溶液变成浅绿色,同时放出气体2Al+6HCl==2AlCl3+3H2↑现象:有气体生成H2+CuO====Cu+H2O 现象:由黑色的固体变成红色的,同时有水珠生成2Fe2O3+3H2 ==2Fe+3H2O 现象:有水珠生成,固体颜色由红色变成银白色3、跟碳有关的化学方程式:C+O2==CO2(氧气充足的情况下) 现象:生成能让纯净的石灰水变浑浊的气体2C+O2===2CO(氧气不充足的情况下) 现象:不明显C+2CuO==2Cu+CO2↑现象:固体由黑色变成红色并减少,同时有能使纯净石灰水变浑浊的气体生成3C+2Fe2O3==4Fe+3CO2↑现象:固体由红色逐渐变成银白色,同时黑色的固体减少,有能使纯净的石灰水变浑浊的气体生成CO2+C===2CO 现象:黑色固体逐渐减少3C+2H2O=CH4+2CO 现象:生成的混和气体叫水煤气,都是可以燃烧的气体4、跟二氧化碳有关的化学方程式:C+O2点燃====CO2 现象:生成能使纯净的石灰水变浑浊的气体Ca(OH)2+CO2===CaCO3↓+H2O 现象:生成白色的沉淀,用于检验二氧化碳CaCO3+CO2+H2O===Ca(HCO3)2 现象:白色固体逐渐溶解Ca(HCO3)===CaCO3↓+CO2↑+H2O 现象:生成白色的沉淀,同时有能使纯净的石灰水变浑浊的气体生成Cu2(OH)2CO3=2CuO+H2O+CO2↑现象:固体由绿色逐渐变成黑色,同时有能使纯净石灰水变浑浊的气体生成2NaOH+CO2===Na2CO3+H2O(也可为KOH)现象:不明显CaCO3===CaO+CO2↑现象:有能使纯净石灰水变浑浊的气体生成跟一氧化碳有关的,但同时也跟二氧化碳有关:Fe3O4+4CO====3Fe+4CO2 现象:固体由黑色变成银白色,同时有能使纯净石灰水变浑浊的气体生成FeO+CO===Fe+CO2 现象:固体由黑色逐渐变成银白色,同时有能使纯净石灰水变浑浊的气体生成Fe2O3+3CO====2Fe+3CO2 现象:固体由红色逐渐变成银白色,同时有能使纯净石灰水变浑浊的气体生成CuO+CO====Cu+CO2 现象:固体由黑色变成红色,同时有能使纯净石灰水变浑浊的气体生成5、跟盐酸有关的化学方程式:NaOH(也可为KOH)+HCl==NaCl+H2O 现象:不明显HCl+AgNO3==AgCl↓+HNO3 现象:有白色沉淀生成,这个反应用于检验氯离子CaCO3+2HCl==CaCl2+H2O+CO2↑现象:百色固体溶解,生成能使纯净石灰水变浑浊的气体Na2CO3+2HCl==2NaCl+H2O+CO2↑现象:生成能使纯净石灰水变浑浊的气体NaHCO3+HCl==NaCl+H2O+CO2↑现象:生成能使纯净石灰水变浑浊的气体Fe2O3+6HCl==2FeCl3+3H2O 现象:红色固体逐渐溶解,形成黄色的溶液Fe(OH)3+3HCl==FeCl3+3H2O 现象:红棕色絮状沉淀溶解,形成了黄色的溶液Cu(OH)2+2HCl==CuCl2+2H2O 现象:蓝色沉淀溶解,形成黄绿色的溶液CuO+2HCl==CuCl2+H2O 现象:黑色固体溶解,生成黄绿色的溶液Zn+2HCl==ZnCl2+H2↑现象:同上Mg+2HCl==MgCl2+H2↑现象:同上Fe+2HCl==FeCl2+H2↑现象:溶液变成浅绿色,同时放出气体2Al+6HCl==2AlCl3+3H2↑现象:有气体生成6、跟硫酸有关的化学方程式:2NaOH(或KOH)+H2SO4==Na2SO4+2H2O 现象:不明显Fe2O3+3H2SO4==Fe2(SO4)3+3H2O 现象:红色固体溶解,生成黄色溶液CuO+H2SO4==CuSO4+H2O 现象:黑色固体溶解,生成蓝色溶液Cu(OH)2+H2SO4==CuSO4+2H2O 现象:蓝色沉淀溶解,生成蓝色溶液H2SO4+BaCl2==BaSO4↓+2HCl 现象:生成不溶于强酸的白色沉淀,用于检验硫酸根离子CaCO3+H2SO4==CaSO4+H2O+CO2↑Na2CO3+H2SO4==Na2SO4+H2O+CO2↑2NaHCO3+H2SO4==Na2SO4+2H2O+2CO2↑现象:这三个反应现象同与盐酸反应现象一致7、跟硝酸有关的化学方程式:Fe2O3+6HNO3==2Fe(NO3)3+3H2O 现象:红色固体溶解,生成黄色溶液CuO+2HNO3==Cu(NO3)2 +H2O 现象:黑色固体溶解,生成蓝色溶液Cu(OH)2+2HNO3==Cu(NO3)2+2H2O 现象:蓝色沉淀溶解,生成蓝色溶液NaOH(或KOH)+HNO3==NaNO3+H2O 现象:不明显Mg(OH)2+2HNO3==Mg(NO3)2+2H2O 现象:白色沉淀溶解CaCO3+2HNO3==Ca(NO3)2+H2O+CO2↑Na2CO3+2HNO3==2NaNO3+H2O+CO2↑NaHCO3+HNO3==NaNO3+H2O+CO2↑现象:以上三个反应现象同与盐酸反应现象一致8、跟碱有关的化学方程式:NaOH+HCl(或HNO3、H2SO4)==NaCl+H2O 现象:酸碱中和反应,现象不明显CaO+H2O==Ca(OH)2现象:放出大量的热NaOH(KOH)+FeCl3(Fe(NO3)3、Fe2(SO4)3)==Fe(OH)3↓+NaCl 现象:生成红棕色絮状沉淀,括号里面的反应过程相似,产物相对应就行了2NaOH(KOH)+FeCl2(Fe(NO3)2、FeSO4)==Fe(OH)2↓+2NaCl 现象:生成白色絮状沉淀,括号里面的反映过程相似,产物相对应就行了2NaOH(KOH)+CuCl2(Cu(NO3)2、CuSO4)==Cu(OH)2↓+2NaCl 现象:生成蓝色絮状沉淀,括号里面的反应过程相似,产物相对应就行了NH4Cl(NH4NO3、(NH4)2SO4)+NaOH(KOH)==NH3↑+H2O+NaCl 现象:有可以使石蕊试纸变蓝的气体生成MgCl2(Mg(NO3)2、MgSO4)+NaOH(KOH)==Mg(OH)2↓+NaCl 现象:生成白色沉淀,括号里面的反应过程相似,产物相对应就行了NaHCO3+NaOH==Na2CO3+H2O 现象:不明显此反应的Na换成K是一样的Ca(HCO3)2+2NaOH==CaCO3↓+Na2CO3+2H2O 现象:生成白色沉淀,此反应把Na换成K是一样的2NaOH+CO2==Na2CO3+H2O 现象:无明显现象此反应的Na换成K是一样的Ca(OH)2+CO2==CaCO3↓+H2O 现象:产生白色沉淀,此反应用于检验二氧化碳NaHSO4+NaOH==Na2SO4+H2O 现象:无明显现象2NaOH+SO2==Na2SO3+H2O 现象:无明显现象9、跟钡盐有关的化学方程式:BaCl2+Na2SO4==BaSO4↓+2NaCl 现象:有白色的不溶于强酸的沉淀生成BaCl2+Na2CO3==BaCO3↓+2NaCl 现象:有白色沉淀生成但可溶于盐酸和硝酸,其实也溶于硫酸,但生成硫酸钡沉淀,不容易看出来10、跟钙盐有关的化学方程式:CaCl2+Na2CO3==CaCO3↓+2NaCl 现象:生成白色沉淀CaCO3+CO2+H2O==Ca(HCO3)2 现象:固体逐渐溶解Ca(HCO3)2+Ca(OH)2==2CaCO3↓+2H2O 现象:生成白色沉淀11、跟几种金属及其盐有关的化学方程式:(1)铜:CuSO4•5H2O===CuSO4+5H2O↑现象:固体由蓝色变为白色CuO+CO====Cu+CO2 现象:固体由黑色逐渐变成红色,同时有能使纯净的石灰水变浑浊的气体生成H2+CuO====Cu+H2O 现象:固体由黑色逐渐变成红色,同时有水珠生成Cu+2AgNO3==Cu (NO3)2+2Ag 现象:铜表面慢慢生成了银白色金属CuCl2+2NaOH==Cu (OH) 2↓+2NaCl 现象:生成了蓝色絮状沉淀CuO+H 2SO 4==CuSO 4+H 2O 现象:黑色固体溶解,生成蓝色溶液 Cu (OH) 2+H 2SO 4==CuSO 4+2H 2O 现象:蓝色沉淀溶解,生成蓝色溶液 Fe(Zn)+CuSO 4==FeSO 4+Cu 现象:有红色金属生成 Cu 2(OH)2CO 3==2CuO+H 2O+CO 2↑ 现象:固体由绿色逐渐变成黑色,同时有能使纯净石灰水变浑浊的气体生成(2)铁:Fe+2HCl==FeCl 2+H 2 现象:铁粉慢慢减少,同时有气体生成,溶液呈浅绿色 FeCl 2+2NaOH==Fe(OH)2↓+NaCl 现象:有白色絮状沉淀生成 4Fe(OH)2+O 2+2H 2O==4Fe(OH)3 现象:氢氧化铁在空气中放置一段时间后,会变成红棕色 Fe (OH) 3+3HCl==FeCl 3+3H 2O 现象:红棕色絮状沉淀溶解,溶液呈黄色 Fe (OH) 2+2HCl==FeCl 2+2H 2O 现象:白色絮状沉淀溶解,溶液呈浅绿色 Fe+CuSO 4==FeSO 4+Cu 现象:铁溶解生成红色金属 Fe+AgNO 3==Fe(NO 3)2+Ag 现象:铁溶解生成银白色的金属 Fe 2O 3+6HCl==2FeCl 3+3H 2O 现象:红色固体溶解,生成黄色的溶液 23432Fe O Fe O 点燃= 现象:铁剧烈燃烧,火星四射,生成黑色的固体 Zn+FeCl 2==ZnCl 2+Fe 现象:锌粉慢慢溶解,生成铁(3)银:AgNO 3+HCl==AgCl ↓+HNO 3 现象:有白色沉淀生成,且不溶于强酸 AgNO 3+NaCl==AgCl ↓+NaNO 3 现象:有白色沉淀生成,且不溶于强酸 Cu+2AgNO 3==Cu(NO 3)2+2Ag 现象:红色的铜逐渐溶解,同时有银白色的金属生成 2AgNO 3+Na 2SO 4==Ag 2SO 4↓+2NaNO 3 现象:有白色沉淀生成(4)补充化学方程式:3Ag+4HNO 3(稀)==3AgNO 3+NO ↑+2H 2O 现象:银逐渐溶解,生成气体遇空气变棕色 Ag+2HNO 3(浓)==AgNO3+NO 2↑+H 2O 现象:银逐渐溶解,生成棕色气体 Cu+2H 2SO4(浓)==CuSO 4+SO 2↑+2H 2O 现象:铜逐渐溶解,生成有刺激性气味的气体 2FeCl 3+Fe==3FeCl 2 现象:铁粉逐渐溶解,溶液由黄色变成浅绿色 2Na 2O 2(过氧化钠)+2H 2O=4NaOH+O 2 现象:有能使带火星的木条复燃的气体生成。
