GC-YL-40350黄蜀葵花检验操作规程
黄蜀葵种子品质检验及质量标准初步研究

2 方法
2 1净度 分析 .
采用 四分 法分别将 已抽取 的 3份样 品倒在 光洁 的 桌面上 ,把纯净种子 、废种子和杂质分 开。若样品混有 较大或 多量 的杂物时 ,要在样品称重后 ,在分取测定样 品前进行必要 的清理并称重 。重复 3 ,余同 。 次 j
21 00年 4月 第 l 2卷
第 4期
中国现代中药 M dm hns M dc e oe C iee eii n
威瞳糍
黄蜀 葵种 子 品质 检 验 及 质 量标 准 初 步研 究
朱华云 ,谈献和 ,杨卉 ,徐柏 颐 ,沈 小林
( 南京中医药大学,江苏 南京 2(t; 江苏苏中药业集团 1 . 1) 2 I6 股份有限公司,江苏 姜堰 25 0 2 0) 5
黄蜀葵 Ae ocu aio( . M dc为锦 葵科 bl shsm nhtL ) ei m 植物 ,全草人 药 ,能清热 ,凉血 ,解毒 ,其花 性 味甘 寒滑 ,无毒 ,具 有清利湿热 ,消炎 解毒 之 功效 ,内服 主治五淋 ,水肿 ;外 用 治 疗痈 疽 肿 毒 ,汤水 烫 伤 。 J 果实种子具有补脾健 胃,生 肌功 效功 能。治疗 消化 不 良、不思饮食 ,跌 打损伤等 。现代药 理学 证 明 ,黄 J
[ 摘要] 目的 :研究黄蜀葵种子的品质检验方法和质量分级标 准 ,为黄蜀 葵种子检 验规程及 质量标 准的制定
提供依据 。方法 :依据种子检验方法对 不同产地 、不 同年份 的黄蜀葵 种子 的品质进 行测定 。结果 与结论 :测定 了不 同产地黄蜀葵种子的千粒重 、含水 率 、生活力 、发芽率等 ,并初步制定 了黄蜀葵种子 的质量分级标准 。 [ 关键词 ] 黄蜀葵 ;种子 ;品质检 验 ;质量标准
GC-YL-40220旋覆花检验操作规程
题目:旋覆花原药材检验操作规程
编号:TS-GC-YL-40220-02
制定人:
制定日期:2017年 月 日
版本:2
页数:1/2
审核人:
审核日期:2017年 月 日
颁发部门:质 量 部
批准人:
批准日期:2017年 月 日
生效日期:2017年 月 日
目的:规范旋覆花原药材检验操作
范围:旋覆花原药材检验
(2)薄层鉴别
仪器与试剂:分析天平、硅胶G薄层板、回流装置、层析缸、锥形瓶、石油醚、乙酸乙酯、香草醛、硫酸等。
方法:取本品粉末2g,置具塞锥形瓶中,加石油醚(60~90℃)30ml,密塞,冷浸1小时,加热回流30分钟,放冷,滤过,滤液浓缩至近干,残渣加石油醚(60~90℃)2ml使溶解,作为供试品溶液。另取旋覆花对照药材2g,同法制成对照药材溶液。照薄层色谱法(通则0502)试验,吸取上述两种溶液各5μl,分别点于同一硅胶G薄层板上,以石油醚(60~90℃)-乙酸乙酯(5:1)为展开剂,展开,取出,晾干,喷以5%香草醛硫酸溶液,加热至斑点显色清晰。供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的主斑点。
【鉴别】
(1)显微鉴别
仪器与试剂:生物显微镜、酒精灯、水合氯醛等。
方法:取本品粉末适量,用水合氯醛装片,置显微镜下观察:本品表面观:苞片非腺毛1~8细胞,多细胞者基部膨大,顶端细胞特长;内层苞片另有2~3细胞并生的非腺毛。冠毛为多列性非腺毛,边缘细胞稍向外突出。子房表皮细胞含草酸钙柱晶,长约至48μm,直径2~5μm;子房非腺毛2列性,1列为单细胞,另列通常2细胞,长90~220μm。苞片、花冠腺毛棒槌状,头部多细胞,多排成2列,围有角质囊,柄部多细胞,2列。花粉粒类球形,直径22~33μm,外壁有刺,长约3μm,具3个萌发孔。
GC-YL-30650叶下珠检验操作规程
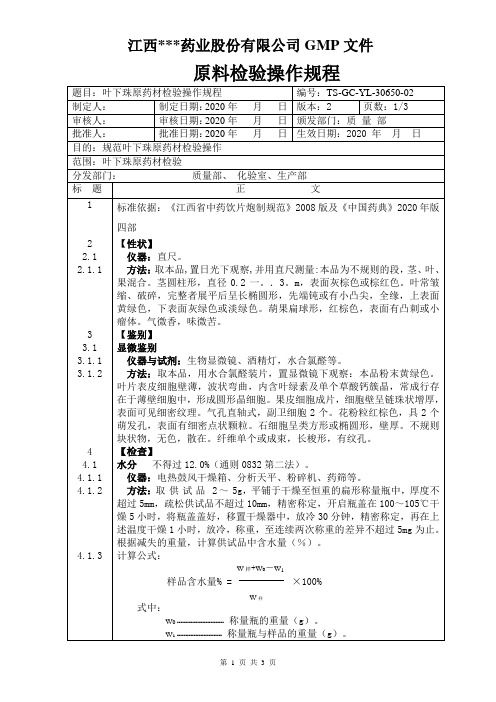
式中:
W0 ----------- 坩埚重量(g)。
W1----------- 坩埚与灰分的重量(g)。
W样----------- 样品的重量(g)。
酸不溶性灰分不得过3.0%(通则2302)。
仪器:粉碎机、药筛、分析天平、坩埚、箱式电阻炉等。
方法:取上述灰分,加入稀盐酸10ml,用表面皿覆盖坩埚,置水浴上加热10分钟,表面皿用热水5ml冲洗,洗液并入坩埚中,用无灰滤纸滤过,坩埚内的残渣用水洗于滤纸上,并洗涤至洗液不显氯化物反应为止,滤渣连同滤纸移至同一坩埚中,干燥,炽灼至恒重。根据残渣重量,计算供试品中酸不溶性灰分的含量(%)。
原料检验操作规程
题目:叶下珠原药材检验操作规程
编号:TS-GC-YL-30650-02
制定人:
制定日期:2020年月日
版本:2
页数:1/3
审核人:
审核日期:2020年月日
颁发部门:质 量 部
批准人:
批准日期:2020年月日
生效日期:2020 年 月 日
目的:规范叶下珠原药材检验操作
范围:叶下珠原药材检验
【性状】
仪器:直尺。
方法:取本品,置日光下观察,并用直尺测量:本品为不规则的段,茎、叶、果混合。茎圆柱形,直径0.2一。.3。m,表面灰棕色或棕红色。叶常皱缩、破碎,完整者展平后呈长椭圆形,先端钝或有小凸尖,全缘,上表面黄绿色,下表面灰绿色或淡绿色。葫果扁球形,红棕色,表面有凸刺或小瘤体。气微香,味微苦。
计算公式:
二氧化硫残留量(mg/kg)=(V供-V空)×C×0.032×106
W供
式中V供为供试品溶液消耗氢氧化钠滴定液的体积,ml;
V空为空白消耗氢氧化钠滴定液的体积,ml;
GC-YL-40300月季花检验操作规程
标 题
正 文
1
2
2.1
2.1.1
3
3.1
3.1.1
3.1.2
3.2
3.2.1
3.2.2
4
4.1
4.1.1
4.1.2
4.1.3
4.2
4.2.1
4.2.2
4.2.3
4.3
4.3.1
4.3.2
4.3.3
5
5.1
5.1.1
5.1.2
5.1.3
5.1.4
5.1.5
标准依据:《中国药典》2020年版一部及四部
【性状】
仪器:直尺。
方法:取本品,置日光下观察,并用直尺测量:本品呈类球形,直径1.5~2.5cm。花托长圆形,萼片5,暗绿色,先端尾尖;花瓣呈覆瓦状排列,有的散落,长圆形,紫红色或淡紫红色;雄蕊多数,黄色。体轻,质脆。气清香,味淡、微苦。
【鉴别】
(1)显微鉴别
仪器与试剂:生物显微镜、酒精灯,水合氯醛等。
【检查】
水分不得过12.0%(通则0832第二法)。
仪器:电热鼓风干燥箱、分析天平、粉碎机、药筛等。
方法:取供试品2~5g,平铺于干燥至恒重的扁形称量瓶中,厚度不超过5mm,疏松供试品不超过10mm,精密称定,开启瓶盖在100~105℃干燥5小时,将瓶盖盖好,移置干燥器中,放冷30分钟,精密称定,再在上述温度干燥1小时,放冷,称重,至连续两次称重的差异不超过5mg为止。根据减失的重量,计算供试品中含水量(%)。
【含量测定】 照高效液相色谱法(通则0512)测定。
仪器与试剂:电子分析天平、高效液相色谱仪、乙腈等。
GC-YL-40160金银花原料检验操作规程
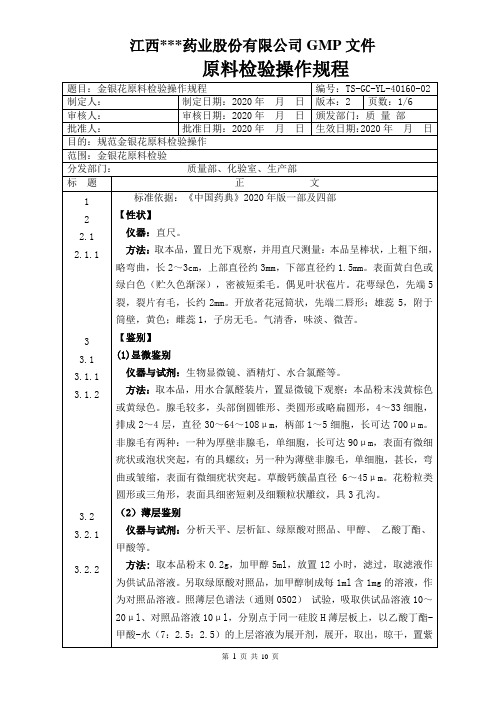
测定法精密吸取空白溶液与供试品溶液各10~20μ1,照标准曲线的制备项下方法测定吸光度(若供试品有干扰,可分别精密量取标准溶液、空白溶液和供试品溶液各1ml,精密加含1%磷酸二氢铵和0.2%硝酸镁的溶液0.5ml,混匀,依法测定),从标准曲线上读出供试品溶液中镉(Cd)的含量,计算,即得。
B法取供试品粗粉1g,精密称定,置凯氏烧瓶中,加硝酸-高氯酸(4:1)混合溶液5~10ml,混匀,瓶口加一小漏斗,浸泡过夜。置电热板上加热消解,保持微沸,若变棕黑色,再加硝酸-高氯酸(4:1)混合溶液适量,持续加热至溶液澄明后升高温度,继续加热至冒浓烟,直至白烟散尽,消解液呈无色透明或略带黄色,放冷,转入50ml量瓶中,用2%硝酸溶液洗涤容器,洗液合并于量瓶中,并稀释至刻度,摇匀,即得。同法同时制备试剂空白溶液。
计算公式:
含水量% =×100%
式中:
V ---------------检读数量ml。
W样---------------样品重量g。
总灰分不得过3.0%(通则2302)。
仪器:电阻炉、分析天平、粉碎机、药筛、坩埚等。
方法:取本品粉末约3g,过二号筛混合均匀后,置炽灼至恒重的坩埚中称定重量(准确至0.01g),缓缓炽热,注意避免燃烧,至完全炭化时,逐渐升高温度至500~600℃,使完全灰化至恒重。根据残渣重量,计算供试品中总灰分的含量(%)。
【检查】
水分不得过12.0%(通则0832第四法)。
仪器与试剂:水分测定装置、分析天平、圆底烧瓶、甲苯等。
方法:取供试品适量,精密称定,置圆底烧瓶中,加甲苯约200ml,必要时加入干燥、洁净的无釉小瓷片数片或玻璃珠数粒,连接仪器,自冷凝管顶端加入甲苯至充满水分测定管的狭细部分。将短颈圆底烧瓶置电热套中或用其他适宜方法缓缓加热,待甲苯开始沸腾时,调节温度,使每秒馏出2滴。待水分完全馏出,即测定管刻度部分的水量不再增加时,将冷凝管内部先用甲苯冲洗,再用饱蘸甲苯的长刷或其他适宜方法,将管壁上附着的甲苯推下,继续蒸馏5分钟,放冷至室温,拆卸装置,如有水黏附在水分测定管的管壁上,可用蘸甲苯的铜丝推下,放置使水分与甲苯完全分离(可加亚甲蓝粉末少量,使水染成蓝色,以便分离观察)。检读水量,并计算成供试品的含水量(%)。
黄蜀葵花总黄酮的质量标准及指纹图谱研究

·中药与天然药物·黄蜀葵花总黄酮的质量标准及指纹图谱研究张 俊1,3,章方臖2,宋必卫3(1 浙江中医药大学附属第二医院,浙江杭州310005;2 杭州市临安区第一人民医院,浙江杭州311300;3 浙江工业大学药学院,浙江杭州310014)摘要:目的 对黄蜀葵花总黄酮进行定性定量实验研究,建立黄蜀葵花总黄酮的质量标准及HPLC指纹图谱,为该有效部位的制剂开发提供参考。
方法 采用化学鉴别法和薄层色谱法对黄蜀葵花总黄酮进行定性鉴别;采用醋酸 醋酸钠 氢氧化铝法进行黄蜀葵花总黄酮含量测定;采用HITACHILaChromC18色谱柱(250mm×4 6mm,5μm),以乙腈 0 1%磷酸溶液作为流动相进行梯度洗脱,柱温30℃,检测波长360nm,流速1 0mL·min-1,进样量10μL,对10个不同批次提取物进行测定;采用HPLC DAD结合相似度评价建立黄蜀葵花总黄酮指纹图谱。
结果 拟定了黄蜀葵花总黄酮的质量标准草案,建立了黄蜀葵花总黄酮的指纹图谱,确定了11个共有峰。
结论 本研究建立的定性定量检测方法操作简便、准确可靠、专属性强、重复性好,可作为黄蜀葵花总黄酮的质量控制方法;建立的黄蜀葵花总黄酮HPLC指纹图谱可为该提取物的鉴别及质量控制提供参考。
关键词:黄蜀葵花;总黄酮;质量标准;指纹图谱中图分类号:R284 文献标识码:A 文章编号:1006 3765(2020) 07 0030 05作者简介:张 俊,硕士,药师,主要从事临床药理学及中药药理学。
E mail:junz128@163 com通讯作者:章方臖,硕士,药师。
E mail:zhangfj188@126 com基金项目:杭州市卫生科技计划项目(No 2018B067)StudyontheQualityStandardandFingerprintofTotalFlavonoidsfromAbelmoschlmanihotLmedicFlowersZHANGJun1,3,ZHANGFang jun2 ,SONGBi wei3(1 TheSecondAffiliatedHospitalofZhejiangChineseMedicalUniversity,Hangzhou310005,China;2 TheFirstPeople′sHospitalofLin′anDistrict,Hangzhou311300,China;3 CollegeofParmaceulticalScience,ZhejiangUniversityofTechnology,Hangzhou310014,China)ABSTRACT:OBJECTIVE ThequalitativeandquantitativeexperimentsontotalflavonoidsofAbelmoschlmanihotLmedicflowerswerecarriedouttoestablishthequalitystandardandHPLCfingerprintofthetotalflavonoidsofAbel moschlmanihotLmedicflowers,whichprovidedareferenceforthedevelopmentoftheeffectivepart METHODS First,thetotalflavonoidsofAbelmoschlmanihotLmedicflowerswerequalitativeidentifiedbychemicalidentificationandthin layerchromatographyanddeterminedbyAceticacid Sodiumacetate Aluminumhydroxidemethod The,10differentbatchesofextractwereanalyzedonaHITACHILaChromC18chromatographiccolumn(250mm×4 6mm,5μm),gradientelutionwithmobilephaseofacetonitrile 0 1%phosphoricacidsolutionandwaterflowingat1 0mL·min-1Andtheinjectionvolumewassetat10μLperinjectiondetectingat360nmin30℃ Last,HPLC DADcom binedwithsimilarityevaluationwasusedtoestablishthefingerprintofthetotalflavonoidsofAbelmoschlmanihotLmedicflowers RESULTS AdraftqualitystandardforthetotalflavonoidsofAbelmoschlmanihotLmedicflowerswasprepared,andthefingerprintofthetotalflavonoidsofAbelmoschlmanihotLmedicflowerswasestablished Itwasconfirmedthattherewere11commonpeaksinthese10batches CONCLUSION Theestablishedmethodinthisstudyissimple,accurate,reliable,specific,andreproducible,whichcanbeusedasaqualitycontrolmethodforthetotalflavonoidsofAbelmoschlmanihotLmedicflowers TheestablishedHPLCfingerprintofthetotalflavonoidsofAbelmoschlmanihotLmedicflowerscanprovidereferencefortheidentificationandqualitycontroloftheextract KEYWORDS:Totalflavonoids;AbelmoschlmanihotLmedicflowers;Qualitystandard;Fingerprint·03·海峡药学 2020年 第32卷第7期 黄蜀葵(AbelmoschlmanihotLmedic)又名秋葵、棉花葵、假阳桃、黄芙蓉等,为锦葵科植物,一年至多年生草本植物,原产于我国南方地区,常生于山谷草丛、田边或沟旁灌丛间,现除西北、东北等地外,全国大部分地区均有分布或栽培〔1〕。
GC-YL-40230密蒙花原料检验操作规程

(V供-V空)×C×0.032×106
二氧化硫残留量(mg/kg) =
W供
式中:
V供为供试品溶液消耗氢氧化钠滴定液的体积,ml;
V空为空白消耗氢氧化钠滴定液的体积,ml;
C为氢氧化钠滴定液的浓度,mol/L;
W供为供试品的重量,g。
0.032为lml氢氧化钠滴定液(lmol/L)相当的二氧化硫的质量,g
【检查】
二氧化硫残留量:照二氧化硫残留量测定法(通则 2331)测定,不得过150mg/kg
仪器与试剂:两颈圆底烧瓶、电热套、竖式回流冷凝管、磁力搅拌器、分析天平、甲基红乙醇溶液指示剂、氢氧化钠滴定液滴、盐酸溶液(6mol/L)等。
方法:测定法取药材或饮片细粉约10g(如二氧化硫残留量较髙,超过1000mg/kg,可适当减少取样量,但应不少于5g),精密称定,置两颈圆底烧瓶中,加水300〜400ml。打开回流冷凝管开关给水,将冷凝管的上端二氧化硫气体导出口处连接一橡胶导气管置于100ml锥形瓶底部。锥形瓶内加入3%过氧化氢溶液50ml作为吸收液(橡胶导气管的末端应在吸收液液面以下)。使用前,在吸收液中加人3滴甲基红乙醇溶液指示剂(2.5mg/ml),并用0.Olmol/L氢氧化钠滴定液滴定至黄色(即终点;如果超过终点,则应舍弃该吸收溶液)。开通氮气,使用流量计调节气体流量至约0.2L/min;打开分液漏斗的活塞,使盐酸溶液(6mol/L)10ml流入蒸馏瓶,立即加热两颈烧瓶内的溶液至沸,并保持微沸;烧瓶内的水沸腾1.5小时后,停止加热。吸收液放冷后,置于磁力搅拌器上不断搅拌,用氢氧化钠滴定(O.Olmol/L)滴定,至黄色持续时间20秒不褪,并将滴定的结果用空白实验校正。
【含量测定】照高效液相色谱法(通则0512)测定。
GC-YL-30430淫羊藿原料检验操作规程
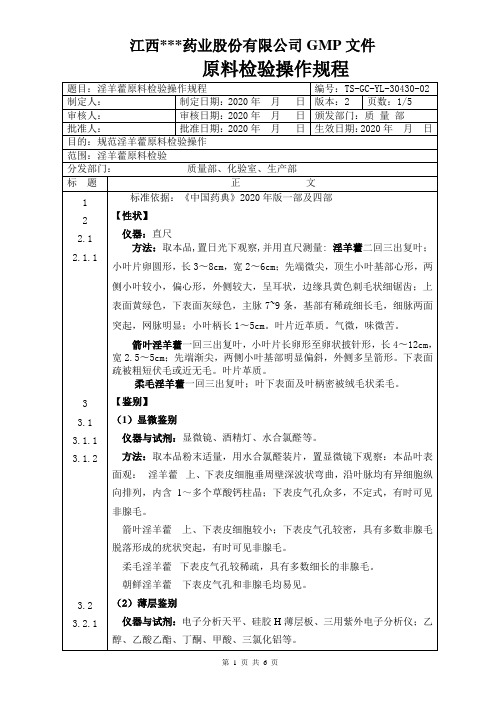
原料检验操作规程6.1.16.26.2.1总黄酮精密量取淫羊藿苷测定项下的供试品溶液0.5ml,置50ml 量瓶中,加甲醇至刻度,摇匀,作为供试品溶液。
另取淫羊藿苷对照品适量,精密称定,加甲醇制成每1ml含10μg的溶液,作为对照品溶液。
分别取供试品溶液和对照品溶液,以相应试剂为空白,照紫外-可见分光光度法(通则0401),在270nm波长处测定吸光度,计算,即得。
本品按干燥品计算,含总黄酮以淫羊藿苷(C33H40O15)计,不得少于5.0%。
总黄酮醇苷照高效液相色谱法(通则0512)测定。
色谱条件与系统适用性试验以十八烷基硅烷键合硅胶为填充剂(柱长为250mm,内径为4.6mm);以乙腈为流动相A,水为流动相B,按下表中的规定进行梯度洗脱;柱温为30℃;检测波长为270nmo理论板数按淫羊董苷峰计算应不低于8000。
对照品溶液的制备取淫羊薑苷对照品适量,精密称定,加甲醇制成每IE含40Mg的溶液,即得。
供试品溶液的制备取本品叶片,粉碎过三号筛,取约0.2g,精密称定,置具塞锥形瓶中,精密加入稀乙醇20ml,称定重量,超声处理(功率400W,频率50kHz)1小时,放冷,再称定重量,用稀乙醇补足减失的重量,摇匀,滤过,取续滤液,即得。
测定法分别精密吸取对照品溶液与供试品溶液各10μl,注入液相色谱仪,测定。
以淫羊鬣苷对照品为参照,以其相应的峰为S峰,计算朝霍定A、朝董定B、朝螯定C峰的相对保留时间,其相对保留时间应在规定值的±5%范围之内。
相对保留时间及校正因子见下表6.2.2以淫羊藿苷对照品为对照,分别乘以校正因子,计算朝藿定A、朝藿定E、朝藿定C和淫羊藿苷的含量。
本品按干燥品计算,叶片含朝藿定A (C39H50O20)、朝藿定B(C38H48O19).朝藿定C(C39H50O19)和淫羊藿^(C33H40O15)的总量,朝鲜淫羊藿不得少于0.50%;淫羊藿、柔毛淫羊藿、箭叶淫羊藿均不得少于1.5%计算公式:A样×C对×稀释倍数含量% =×100%式中:A样------------------------- 样品的面积。
GC-YL-30250垂盆草原料检验操作规程
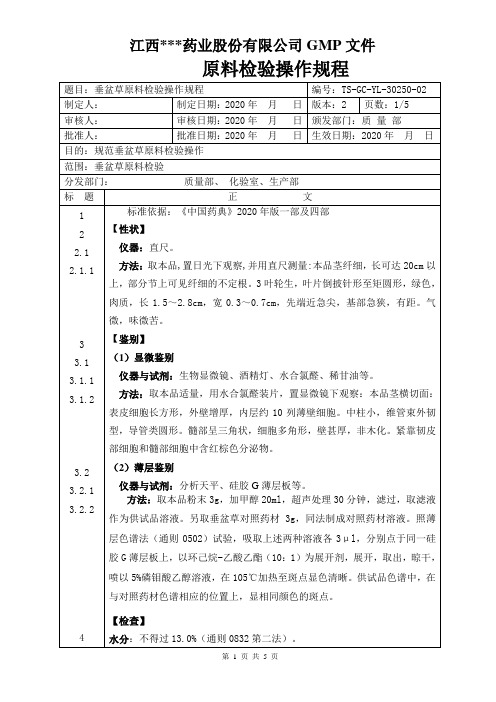
方法:取总灰分,加入稀盐酸10ml,用表面皿覆盖坩埚,置水浴上加热10分钟,表面皿用热水5ml冲洗,洗液并入坩埚中,用无灰滤纸滤过,坩埚内的残渣用水洗于滤纸上,并洗涤至洗液不显氯化物反应为止,滤渣连同滤纸移至同一坩埚中,干燥,炽灼至恒重。根据残渣重量,计算供试品中酸不溶性灰分的含量(%)。
计算公式:
(V供-V空)×C×0.032×106
二氧化硫残留量(mg/kg) =
W供
式中:
V供为供试品溶液消耗氢氧化钠滴定液的体积,ml;
V空为空白消耗氢氧化钠滴定液的体积,ml;
C为氢氧化钠滴定液的浓度,mol/L;
W供为供试品的重量,g。
0.032为lml氢氧化钠滴定液(lmol/L)相当的二氧化硫的质量,g。
方法:测定法取药材或饮片细粉约10g(如二氧化硫残留量较髙,超过1000mg/kg,可适当减少取样量,但应不少于5g),精密称定,置两颈圆底烧瓶中,加水300〜400ml。打开回流冷凝管开关给水,将冷凝管的上端二氧化硫气体导出口处连接一橡胶导气管置于100ml锥形瓶底部。锥形瓶内加入3%过氧化氢溶液50ml作为吸收液(橡胶导气管的末端应在吸收液液面以下)。使用前,在吸收液中加人3滴甲基红乙醇溶液指示剂(2.5mg/ml),并用0.Olmol/L氢氧化钠滴定液滴定至黄色(即终点;如果超过终点,则应舍弃该吸收溶液)。开通氮气,使用流量计调节气体流量至约0.2L/min;打开分液漏斗的活塞,使盐酸溶液(6mol/L)10ml流入蒸馏瓶,立即加热两颈烧瓶内的溶液至沸,并保持微沸;烧瓶内的水沸腾1.5小时后,停止加热。吸收液放冷后,置于磁力搅拌器上不断搅拌,用氢氧化钠滴定(O.Olmol/L)滴定,至黄色持续时间20秒不褪,并将滴定的结果用空白实验校正。
GC-YL-11230黄药子检验操作规程
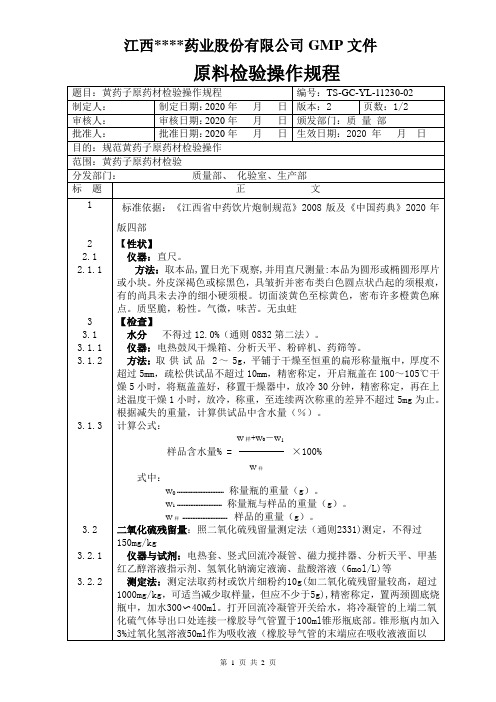
测定法:测定法取药材或饮片细粉约10g(如二氧化硫残留量较髙,超过1000mg/kg,可适当减少取样量,但应不少于5g),精密称定,置两颈圆底烧瓶中,加水300〜400ml。打开回流冷凝管开关给水,将冷凝管的上端二氧化硫气体导出口处连接一橡胶导气管置于100ml锥形瓶底部。锥形瓶内加入3%过氧化氢溶液50ml作为吸收液(橡胶导气管的末端应在吸收液液面以下)。使用前,在吸收液中加人3滴甲基红乙醇溶液指示剂(2.5mg/ml),并用0.Olmol/L氢氧化钠滴定液滴定至黄色(即终点;如果超过终点,则应舍弃该吸收溶液)。开通氮气,使用流量计调节气体流量至约0.2L/min;打开分液漏斗的活塞,使盐酸溶液(6mol/L)10ml流入蒸馏瓶,立即加热两颈烧瓶内的溶液至沸,并保持微沸;烧瓶内的水沸腾1.5小时后,停止加热。吸收液放冷后,置于磁力搅拌器上不断搅拌,用氢氧化钠滴定(O.Olmol/L)滴定,至黄色持续时间20秒不褪,并将滴定的结果用空白实验校正。
计算公式:
W样+W0-W1
样品含水量% =×100%
式中:
W0----------------------------称量瓶的重量(g)。
W1---------------------------称量瓶与样品的重量(g)。
W样---------------------------样品的重量(g)。
二氧化硫残留量:照二氧化硫残留量测定法(通则2331)测定,不得过150mg/kg
原料检验操作规程
题目:黄药子原药材检验操作规程
编号:TS-GC-YL-11230-02
制定人:
YL-50310通草原料检验操作规程

方法:取供试品2~3g,过二号筛混合均匀后,置炽灼至恒重的坩埚中称定重量,缓缓炽热,注意避免燃烧,至完全炭化时,逐渐升高温度至500~600℃,使完全灰化至恒重。根据残渣重量,计算供试品中总灰分的含量(%)。
计算公式:
W1-W0
总灰分% =×100%
检验操作规程
题目:通草原药材检验操作规程
编号:TS-GC-YL-50310-02
制定人:
制定日期2020 年 月 日
版本:2
页数:1/2
审核人:
审核日期2020 年 月 日
颁发部门:质 量 部
批准人:
批准日期2020年 月 日
生效日期2020 年 月 日
目的:规范通草原药材检验操作
范围:通草原药材检验
【鉴别】
显微鉴别
方法:取本品,用水合氯醛装片,置显微镜下观察:本品横切面:全部为薄壁细胞,椭圆形、类圆形或近多角形,外侧的细胞较小,纹孔明显,有的细胞含草酸钙簇晶,直径15~64μm。
【检查】
水分不得过16.0%(通则0832第二法)。
仪器:电热鼓风干燥箱、分析天平、粉碎机、药筛等。
方法:测定法取药材或饮片细粉约10g(如二氧化硫残留量较髙,超过1000mg/kg,可适当减少取样量,但应不少于5g),精密称定,置两颈圆底烧瓶中,加水300〜400ml。打开回流冷凝管开关给水,将冷凝管的上端二氧化硫气体导出口处连接一橡胶导气管置于100ml锥形瓶底部。锥形瓶内加入3%过氧化氢溶液50ml作为吸收液(橡胶导气管的末端应在吸收液液面以下)。使用前,在吸收液中加人3滴甲基红乙醇溶液指示剂(2.5mg/ml),并用0.Olmol/L氢氧化钠滴定液滴定至黄色(即终点;如果超过终点,则应舍弃该吸收溶液)。开通氮气,使用流量计调节气体流量至约0.2L/min;打开分液漏斗的活塞,使盐酸溶液(6mol/L)10ml流入蒸馏瓶,立即加热两颈烧瓶内的溶液至沸,并保持微沸;烧瓶内的水沸腾1.5小时后,停止加热。吸收液放冷后,置于磁力搅拌器上不断搅拌,用氢氧化钠滴定(O.Olmol/L)滴定,至黄色持续时间20秒不褪,并将滴定的结果用空白实验校正。
GC-YL-30410麻黄原料检验操作规程
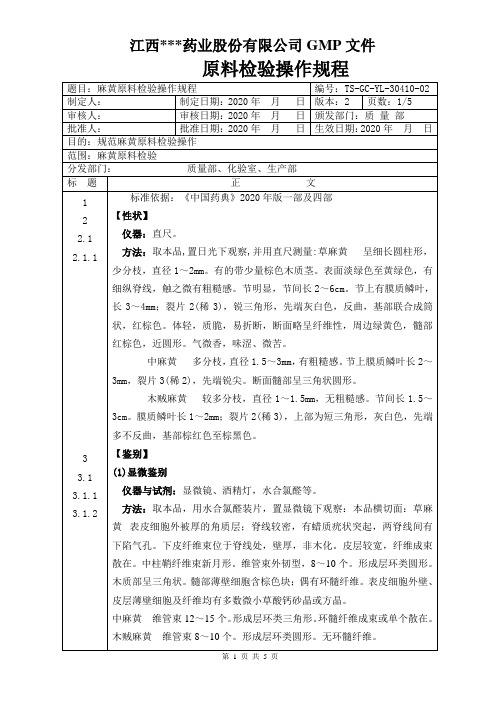
m-------------------------样品的重量(g)。
f-------------------------稀释体积。
方法:测定法取药材或饮片细粉约10g(如二氧化硫残留量较髙,超过1000mg/kg,可适当减少取样量,但应不少于5g),精密称定,置两颈圆底烧瓶中,加水300〜400ml。打开回流冷凝管开关给水,将冷凝管的上端二氧化硫气体导出口处连接一橡胶导气管置于100ml锥形瓶底部。锥形瓶内加入3%过氧化氢溶液50ml作为吸收液(橡胶导气管的末端应在吸收液液面以下)。使用前,在吸收液中加人3滴甲基红乙醇溶液指示剂(2.5mg/ml),并用0.Olmol/L氢氧化钠滴定液滴定至黄色(即终点;如果超过终点,则应舍弃该吸收溶液)。开通氮气,使用流量计调节气体流量至约0.2L/min;打开分液漏斗的活塞,使盐酸溶液(6mol/L)10ml流入蒸馏瓶,立即加热两颈烧瓶内的溶液至沸,并保持微沸;烧瓶内的水沸腾1.5小时后,停止加热。吸收液放冷后,置于磁力搅拌器上不断搅拌,用氢氧化钠滴定(O.Olmol/L)滴定,至黄色持续时间20秒不褪,并将滴定的结果用空白实验校正。
仪器与试剂:箱式电阻炉、分析天平、粉碎机、药筛、坩埚;稀盐酸等。
方法:取本品粉末2~3g(如须测定酸不溶性灰分,可取供试品3~5g),过二号筛混合均匀后,置炽灼至恒重的坩埚中称定重量(准确至0.01g),缓缓炽热,注意避免燃烧,至完全炭化时,逐渐升高温度至500~600℃,使完全灰化至恒重。根据残渣重量,计算供试品中总灰分的含量(%)。
分发部门: 质量部、化验室、生产部
标 题
正 文
1
2
2.1
2.1.1
高效液相色谱法测定黄蜀葵花总黄酮胶囊中的金丝桃苷和槲皮素-3'-葡萄糖苷

高效液相色谱法测定黄蜀葵花总黄酮胶囊中的金丝桃苷和槲皮素-3'-葡萄糖苷杜安全;周正华【摘要】建立高效液相色谱法测定黄蜀葵花总黄酮中金丝桃苷和槲皮素-3'-葡萄糖苷的含量.以乙腈-0.5%磷酸水溶液(22:78)为流动相,流量为1.0 mL/min,柱温为30℃,检测波长为360 nm.金丝桃苷和槲皮素-3'-葡萄糖苷的质量浓度分别在12.232~73.392μg/mL,11.044~66.264μg/mL范围内与色谱峰面积呈良好的线性关系,相关系数均为0.9999,检出限分别为200,180 ng/g.样品加标回收率分别为99.73%,100.78%,测定结果的相对标准偏差分别为0.86%,1.48%(n=6).该方法操作简单、快速,结果准确,重现性好,可为黄蜀葵花总黄酮胶囊的质量控制提供依据.【期刊名称】《化学分析计量》【年(卷),期】2019(028)003【总页数】3页(P104-106)【关键词】黄蜀葵花总黄酮胶囊;金丝桃苷;槲皮素-3'-葡萄糖苷;高效液相色谱法【作者】杜安全;周正华【作者单位】安徽省医学科学研究院,合肥 230061;安徽省医学科学研究院,合肥230061【正文语种】中文【中图分类】O657.7黄蜀葵花为锦葵科秋葵属植物黄蜀葵的干燥花,黄蜀葵花总黄酮是从黄蜀葵花中提取的总黄酮,其成分中含量较高的金丝桃苷、槲皮素-3’-葡萄糖苷[1]具有增加脑血流量、阻断脑缺血后脑细胞Ca2+内流、抗自由基和抑制 NO 生成等药理作用[2–5],对缺血性脑损伤有很好的保护作用。
因此黄蜀葵花总黄酮对脑血管疾病具有理想的疗效[6–10]。
由于黄蜀葵花总黄酮胶囊尚处于临床前阶段,目前还没有测定总黄酮中金丝桃苷、槲皮素-3’-葡萄糖苷含量的方法,只有用高效液相色谱法测定黄蜀葵花酒精浸膏中金丝桃苷含量的文献报道[11–15]。
为了制定该药质量标准,笔者建立了用高效液相色谱同时测定黄蜀葵花总黄酮中金丝桃苷、槲皮素-3’-葡萄糖苷含量的方法,该方法专属性强,精密度高,重复性好,为黄蜀葵花总黄酮胶囊质量标准的制定提供依据。
GC-YL-10200天葵子检验操作规程
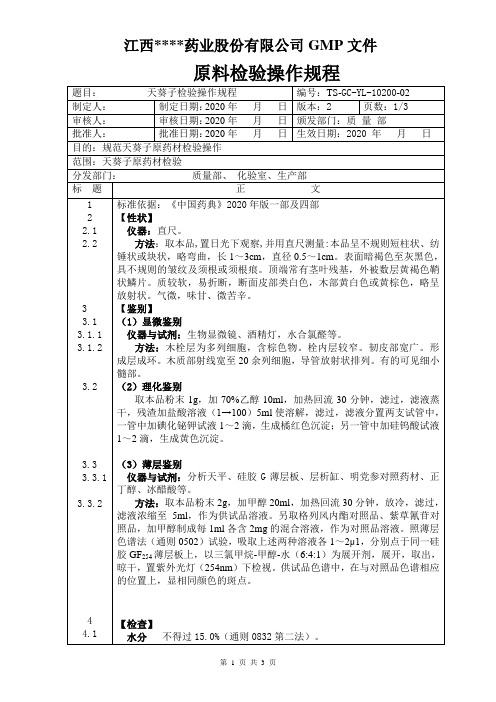
式中:
W0 ----------- 坩埚重量(g)。
W1----------- 坩埚与灰分的重量(g)。
W样----------- 样品的重量(g)。
二氧化硫残留量:照二氧化硫残留量测定法(通则2331)测定,不得过150mg/kg
仪器与试剂:电热套、竖式回流冷凝管、磁力搅拌器、分析天平、甲基红乙醇溶液指示剂、氢氧化钠滴定液滴、盐酸溶液(6mol/L)等
【鉴别】
(1)显微鉴别
仪器与试剂:生物显微镜、酒精灯,水合氯醛等。
方法:木栓层为多列细胞,含棕色物。栓内层较窄。韧皮部宽广。形成层成环。木质部射线宽至20余列细胞,导管放射状排列。有的可见细小髓部。
(2)理化鉴别
取本品粉末1g,加70%乙醇10ml,加热回流30分钟,滤过,滤液蒸干,残渣加盐酸溶液(1→100)5ml使溶解,滤过,滤液分置两支试管中,一管中加碘化铋钾试液1~2滴,生成橘红色沉淀;另一管中加硅钨酸试液1~2滴,生成黄色沉淀。
方法:取供试品约4g,精密称定,置250~300ml的锥形瓶中,精密加水100ml,密塞,冷浸,前6小时内时时振摇,再静置18小时,用干燥滤器迅速滤过,精密量取续滤液20ml,置已干燥至恒重的蒸发皿中,在水浴上蒸干后,于105℃干燥3小时,置干燥器中冷却30分钟,迅速精密称定重量。除另有规定外,以干燥品计算供试品中水溶性浸出物的含量(%)。
【检查】
水分不得过15.0%(通则0832第二法)。
仪器:电热鼓风干燥箱、分析天平、粉碎机、药筛等。
方法:取供试品2~5g,平铺于干燥至恒重的扁形称量瓶中,厚度不超过5mm,疏松供试品不超过10mm,精密称定,开启瓶盖在100~105℃干燥5小时,将瓶盖盖好,移置干燥器中,放冷30分钟,精密称定,再在上述温度干燥1小时,放冷,称重,至连续两次称重的差异不超过5mg为止。根据减失的重量,计算供试品中含水量(%)。
比色法测定黄蜀葵花总黄酮的含量

3 讨论3.1 本法可有效地测定丹参中原儿茶醛的含量,方法简便、重现性好、准确度高。
3.2 流动相的选择 将甲醇-乙腈-1%冰醋酸(10:2:88)、甲醇-0.5%冰醋酸(5:95)、甲醇-枸橼酸溶液-水(18:20:62)等作为流动相,分别进样后比较,发现甲醇-枸橼酸溶液-水(18:20:62)作为流动相时,较其它流动相原儿茶醛分离效果好、保留时间、峰形适当。
3.3 为防止原儿茶醛在酸性溶液中分解,调酸性后应立即用乙醚萃取。
3.4 比较不同来源丹参中原儿茶醛的含量,有显著性差异,以神农药店的较高。
参考文献[1] 郭洪柱,等.高效液相色谱法测定胰妇康胶囊中原儿茶醛含量[J].中国中药杂志.2000,25(10):609.[2] 潘英妮,等.HP LC法测定丹参类注射液中4种水溶性成分含量[J].沈阳药科大学学报,2004,21(3):196. [3] 李岳,薛贵平.复方丹参注射液的临床应用[J].张家口医学院学报,2002,19(3):32.[4] 凌海燕,等.丹参水溶性成分的研究概况[J].天然产物研究与开发,1999,11(1):75.比色法测定黄蜀葵花总黄酮的含量崔 燕,卢志强,景 瑞,赵春荣(山东省生物药物研究院,山东济南250108)摘 要:目的 采用紫外分光光度法测定黄蜀葵花中总黄酮的含量。
方法 用索氏提取法,以芦丁为对照品,以亚硝酸钠2硝酸铝2氢氧化钠为显色剂,检测波长为500nm。
结果 线性范围为0.012~0.072mgΠml,平均回收率为99.72%,相对标准偏差(RSD)为2.62%。
结论 本法为控制黄蜀葵花的内在质量提供了依据。
关键词:黄蜀葵花;比色法;索氏提取Colorimetric determination of the total content ofthe flavonoids in Abelmoschus manihotC UI Y an,LU Zhi2qiang,J I NG Rui,ZH AO Chun2rong(Institute o f Biopharmaceuticals o f Shandong Province,Jinan250108)Abstract:Objective T o analyze the total content of flav onoids in Abelm oschus manihot by colorimetric method.Meth2 od Abelmoschus manihot was distilled with S oxhlet extraction process,rutin was used as reference substance and the de2 tecting wavelength was500nm.R esult The linearity of flav onoids was fine in0.012~0.072mgΠml,average recovery rate 99.72%,RSD2.62%(n=5).Conclusion The method has laid the foundation for the control of the inherent quality in Abelmoschus manihot.K ey w ords:Abelmoschus manihot;colorimetry;s oxhlet extraction 黄蜀葵花为锦葵科植物黄蜀葵Abelmoschus manihot(L.)Medic的干燥花,主产于江苏、安徽等省。
农业综合开发公司化验室新鲜黄秋葵检验操作规程

农业综合开发公司化验室新鲜黄秋葵检
验操作规程
1.检验项目:感官
2.抽样方法:每批黄秋葵抽1.0kg.
3.适用范围: 本方法适用于各种各类蔬菜测定.
4.引用标准: QB/T 2076-1995 水果,蔬菜脆片技术要求
5感官要求
感官要求应符合下表:
项目要求
色泽各种水果、蔬菜脆片应具有与其原料相
应的色泽。
滋味和口感具有该品种特有的滋味,脂香、清香纯
正,口感酥脆
形态块状、片状,条状或该品种应有的整形
状。
各种形态应基本完好,同一品种的
产品厚度基本均匀,且基本无碎屑。
杂质无肉眼可见外来杂质
12.不合格措施:立即上报品质部、厂部,并通知仓库封存来料,不得投入生产。
13.填写记录《秋葵检验原始记录》。
对2010年版《中国药典》中黄蜀葵花含量测定方法的改进

对2010年版《中国药典》中黄蜀葵花含量测定方法的改进吕晓霞;陈宗良【期刊名称】《海峡药学》【年(卷),期】2015(027)010【摘要】目的研究改进《中国药典》黄蜀葵花的含量测定方法 ,并建立同时测定黄蜀葵花中金丝桃苷、槲皮苷含量的方法 . 方法采用月旭XB-C18(250mm×4.6mm,5μm)色谱柱,以乙腈-0.1%磷酸溶液进行梯度洗脱,检测波长360nm,柱温30℃,流速1.0mL· min -1. 结果对含量测定进行方法学考察,结果表明均符合含量测定要求,金丝桃苷进样量在0.21 ~6.31μg ( r =0.9998 )、槲皮苷进样量在0.21 ~6.38μg ( r =0.9995)范围内呈良好的线性关系,平均加样回收率分别为98.70%(RSD=0.92%)、97.46%(RSD=1.74%). 结论改进了《中国药典》黄蜀葵花的含量测定方法 ,解决金丝桃苷与相邻峰难以分离和分析时间过长的问题. 并建立了同时测定金丝桃苷、槲皮苷的方法 ,本方法结果准确,重现性好,专属性强,可用于黄蜀葵花的质量控制.%OBJECTIVE In this work,an improvement method of determination Flower of Sunset Abelmoschus in"Chinese Pharmacopoeia" was developed,and a new method for determination of hyperin and quercetin in Flower of Sunset Abelmoschus was established simultaneously.METHODS A Welch Ultimate? XB-C18 (25mm ×4.6mm,5μm) column was used for separation, with acetonitrile-0.1% phosphoric acid as mobile phase for gradient elu-tion.The detection wavelength was set at 360nm,column temperature was 30oC and flow rate was 1.0mL· min-1 .RESULTS The method showed very good reliability for Flower of SunsetAbelmoschus determination and it can acquire the requirements of determination very well.Hyperin injection quality at 0.21~6.31μg( r=0.9998 ) and quercetin injection quality at 0.21~6.38μg(r=0.9995) showed a good linear relationship,the average recovery were 98.70%( RSD =0.92%) and 97.46%( RSD =1.74%) .CONCLUSION The experiment improved the method for determination of Abelmoschus in"Chinese Pharmacopoeia";solved the problem of hyperoside with adja-cent peaks that was difficult to separate and need long analyze time.The method for simultaneous determination of hy-perin and Quercitrin was established and which showed high accurate and good reproducible, and can be used for quality control in the determination of Flower of Sunset Abelmoschus.【总页数】3页(P67-69)【作者】吕晓霞;陈宗良【作者单位】浙江省金华市金东区市场监督管理局金华 321000;浙江省金华市食品药品检验检测研究院金华 321000【正文语种】中文【中图分类】R927.2【相关文献】1.2005与2010年版《中国药典》肿节风中异秦皮啶含量测定方法的比较 [J], 王伏星;谢汝根;张运根;张大兴;刘玉军;马超2.《中国药典》2010年版二部注射用头孢哌酮钠舒巴坦钠含量测定方法探讨 [J], 雷成康;杨范莉3.关于《中国药典》2010年版枳实中辛弗林含量测定方法的商榷 [J], 刘海涛;孙楠;张进;郝静;齐耀东;孙鹤;郭治昕;张本刚;肖培根4.2010年版《中国药典》化橘红含量测定方法的商榷 [J], 刘群娣;徐新军;谢春燕;闫李丽;杨得坡5.抗生素含量测定方法在《中国药典》2010年版中的应用比较 [J], 彭莺因版权原因,仅展示原文概要,查看原文内容请购买。
紫外分光光度法测定黄蜀葵花总黄酮片中总黄酮的含量△

紫外分光光度法测定黄蜀葵花总黄酮片中总黄酮的含量△
邾枝花;黄平
【期刊名称】《北方药学》
【年(卷),期】2012(000)010
【摘要】目的:建立紫外分光光度法测定黄蜀葵花总黄酮片中总黄酮的含量.方法:样品加AlCl3溶液显色后,以金丝桃苷为对照品,在405nm处测定其吸光度.结果:
线性回归方程为:Y=0.0137X-0.0184,相关系数r=0.9994,黄蜀葵花总黄酮在
8.2032~41.0160μg·ml-1范围内具有良好的线性关系.平均回收率为97.24%,RSD 为1.23%.结论:该方法准确可靠,稳定性、重现性好,适用于黄蜀葵花总黄酮片的含量测定.
【总页数】2页(P3-3,4)
【作者】邾枝花;黄平
【作者单位】安徽医学高等专科学校合肥 230601;安徽医学高等专科学校合肥230601
【正文语种】中文
【中图分类】R927.2
【相关文献】
1.紫外分光光度法测定黄蜀葵花药材的总黄酮含量 [J], 曲延伟;张玲;尚立霞;张海
立
2.紫外分光光度法测定石淋通片中总黄酮含量 [J], 陈洁
3.紫外分光光度法测定心达康片中总黄酮苷元的含量 [J], 翁水旺;周继斌
4.紫外-可见分光光度法测定淫羊藿总黄酮胶囊中总黄酮的含量研究 [J], 张林
5.分光光度法测定复方刺五加片中总黄酮含量研究 [J], 杨赟
因版权原因,仅展示原文概要,查看原文内容请购买。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
式中:
A样-------------------------样品的面积。
A对------------------------ -对照品的面积。
C对-------------------------对照品的浓度(mg/ml)。
m-------------------------样品的重量(g)。
计算公式:
酸不溶性灰分% =
W样
式中:
W0----------- 坩埚重量(g)。
W1-----------酸不溶性灰分与坩埚的重量(g)。
W样----------- 样品的重量(g)。
【浸出物】照醇溶性浸出物测定法(通则2201)项下的冷浸法测定,用乙醇作溶剂,不得少于18.0%。
仪器与试剂:电热鼓风干燥箱、分析天平、蒸发皿、数显恒温水浴锅等。
方法:取供试品约4g,精密称定,置250~300ml的锥形瓶中,精密加水100ml,密塞,冷浸,前6小时内时时振摇,再静置18小时,用干燥滤器迅速滤过,精密量取续滤液20ml,置已干燥至恒重的蒸发皿中,在水浴上蒸干后,于105℃干燥3小时,置干燥器中冷却30分钟,迅速精密称定重量。除另有规定外,以干燥品计算供试品中水溶性浸出物的含量(%)。
【检查】
水分不得过12.0%(通则0832第二法)。
仪器:电热鼓风干燥箱、分析天平、粉碎机、药筛等。
方法:取供试品2~5g,平铺于干燥至恒重的扁形称量瓶中,厚度不超过5mm,疏松供试品不超过10mm,精密称定,开启瓶盖在100~105℃干燥5小时,将瓶盖盖好,移置干燥器中,放冷30分钟,精密称定,再在上述温度干燥1小时,放冷,称重,至连续两次称重的差异不超过5mg为止。根据减失的重量,计算供试品中含水量(%)。
测定法:测定法取药材或饮片细粉约10g(如二氧化硫残留量较髙,超过1000mg/kg,可适当减少取样量,但应不少于5g),精密称定,置两颈圆底烧瓶中,加水300〜400ml。打开回流冷凝管开关给水,将冷凝管的上端二氧化硫气体导出口处连接一橡胶导气管置于100ml锥形瓶底部。锥形瓶内加入3%过氧化氢溶液50ml作为吸收液(橡胶导气管的末端应在吸收液液面以下)。使用前,在吸收液中加人3滴甲基红乙醇溶液指示剂(2.5mg/ml),并用0.Olmol/L氢氧化钠滴定液滴定至黄色(即终点;如果超过终点,则应舍弃该吸收溶液)。开通氮气,使用流量计调节气体流量至约0.2L/min;打开分液漏斗的活塞,使盐酸溶液(6mol/L)10ml流入蒸馏瓶,立即加热两颈烧瓶内的溶液至沸,并保持微沸;烧瓶内的水沸腾1.5小时后,停止加热。吸收液放冷后,置于磁力搅拌器上不断搅拌,用氢氧化钠滴定(O.Olmol/L)滴定,至黄色持续时间20秒不褪,并将滴定的结果用空白实验校正。
W样
式中:
W0 ----------- 坩埚重量(g)。
W1----------- 坩埚与灰分的重量(g)。
W样----------- 样品的重量(g)。
二氧化硫残留量:照二氧化硫残留量测定法(通则2331)测定,不得过150mg/kg
仪器与试剂:电热套、竖式回流冷凝管、磁力搅拌器、分析天平、甲基红乙醇溶液指示剂、氢氧化钠滴定液滴、盐酸溶液(6mol/L)等
原料检验操作规程
题目: 黄蜀葵花检验操作规程
编号:TS-GC-YL-40350-02
制定人:
制定日期:2020年月日
版本:2
页数:1/3
审核人:
审核日期:2020年月日
颁发部门:质 量 部
批准人:
批准日期:2020年月日
生效日期:2020 年 月 日
目的:规范黄蜀葵花原药材检验操作
范围:黄蜀葵花原药材检验
分发部门: 质量部、 化验室、生产部
标 题
正 文
1
2
2.1
2.2
3
3.1
3.1.1
3.1.2
3.2
3.2.1
3.2.2
4
4.1
ቤተ መጻሕፍቲ ባይዱ4.1.1
4.1.2
4.1.3
4.2
4.2.1
4.2.2
4.2.3
4.3
4.3.1
4.3.2
4.3.3
4.4
4.4.1
4.4.2
4.4.3
5
5.1
5.1.1
5.1.2
6.1
6.1.1
酸不溶性灰分不得过2.0%(通则2302)。
仪器:粉碎机、药筛、分析天平、坩埚、箱式电阻炉等。
方法:取上述灰分,加入稀盐酸10ml,用表面皿覆盖坩埚,置水浴上加热10分钟,表面皿用热水5ml冲洗,洗液并入坩埚中,用无灰滤纸滤过,坩埚内的残渣用水洗于滤纸上,并洗涤至洗液不显氯化物反应为止,滤渣连同滤纸移至同一坩埚中,干燥,炽灼至恒重。根据残渣重量,计算供试品中酸不溶性灰分的含量(%)。
计算公式:
二氧化硫残留量(mg/kg)=(V供-V空)×C×0.032×106
W供
式中V供为供试品溶液消耗氢氧化钠滴定液的体积,ml;
V空为空白消耗氢氧化钠滴定液的体积,ml;
c 为氢氧化钠滴定液摩尔浓度,mol/L;
W供为供试品的重量,g。
0.032为lm l氢氧化钠滴定液(lmol/L)相当的二氧化硫的质量,g;
供试品溶液的制备取本品粉末(过四号筛)约0.2g,精密称定,置25ml量瓶中,加甲醇15ml,超声处理(功率250W,频率30kHZ)30分钟,放冷,加甲醇至刻度,摇匀,滤过,取续滤液,即得。
测定法分别精密吸取对照品溶液与供试品溶液各10μl,注入液相色谱仪,测定,即得。
计算公式:
A样×C对×f
含量% =×100%
计算公式:
W样+W0-W1
样品含水量% =×100%
式中:
W0----------------------------称量瓶的重量(g)。
W1---------------------------称量瓶与样品的重量(g)。
W样---------------------------样品的重量(g)。
总灰分不得过8.0%(通则2302)。
f-------------------------稀释体积。
仪器:粉碎机、药筛、分析天平、坩埚、箱式电阻炉等。
方法:取供试品2~3g,过二号筛混合均匀后,置炽灼至恒重的坩埚中称定重量,缓缓炽热,注意避免燃烧,至完全炭化时,逐渐升高温度至500~600℃,使完全灰化至恒重。根据残渣重量,计算供试品中总灰分的含量(%)。
计算公式:
W1-W0
总灰分% =×100%
仪器与试剂:高效液相色谱仪、数显恒温水浴锅等。
色谱条件与系统适用性试验以十八烷基硅烷键合硅胶为填充剂;以乙腈-0.1%磷酸溶液(15:85)为流动相;检测波长为360nm。理论板数按金丝桃苷峰计算应不低于10000。
对照品溶液的制备取金丝桃苷对照品适量,精密称定,加甲醇制成每1ml含0.1mg的溶液,即得。
计算公式:
醇溶性浸出物% =××100%
式中:
W0 ------- 蒸发皿的重量(g)。
W1 -------- 醇溶性浸出物与蒸发皿的重量(g)。
W样------- 样品的重量(g)。
【含量测定】照高效液相色谱法(通则0512)测定本品按干燥品计算,含金丝桃苷(C21H20O12)不得少于0.50%。
(2)薄层鉴别
仪器与试剂:分析天平、硅胶G薄层板、层析缸、明党参对照药材、正丁醇、冰醋酸等。
方法:取本品粉末1g,加0.18%盐酸乙醇溶液20ml,置水浴上加热回流1小时,趁热滤过,滤液浓缩至5ml,作为供试品溶液。另取槲皮素对照品,加乙醇制成每1ml含0.5mg的溶液,作为对照品溶液。照薄层色谱法(通则0502)试验,吸取两种溶液各1μl,分别点于同一用0.5%氢氧化钠溶液制备的硅胶G薄层板上,以甲苯-乙酸乙酯-甲酸(5:4:1)为展开剂,展开,取出,晾干,喷以三氯化铝试液,置紫外光(365nm)下检视。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的荧光斑点。
6.1.2
6.1.3
标准依据:《中国药典》2020年版一部及四部
【性状】
仪器:直尺。
方法:取本品,置日光下观察,并用直尺测量:本品多皱缩破碎,完整的花瓣呈三角状阔倒卵形,长7~10cm,宽7~12cm,表面有纵向脉纹,呈放射状,淡棕色,边缘浅波状;内面基部紫褐色。雄蕊多数,联合成管状,长1.5~2.5cm,花药近无柄。柱头紫黑色,匙状盘形,5裂。气微香,味甘淡。
【鉴别】
(1)显微鉴别
仪器与试剂:生物显微镜、酒精灯,水合氯醛等。
方法:取本品,用水合氯醛装片,置显微镜下观察:本品粉末淡黄色至褐黄色。花冠表皮细胞类长方形或不规则形,垂周壁微波状弯曲。花粉粒类圆形,直径约170μm,具散在孔,孔数约32~40,表面具刺。腺毛完整者长圆锥形,长510~770μm;腺头略呈长棒状,6~14细胞;腺柄3细胞,内含紫红色分泌物。非腺毛单细胞,长140~180μm,壁平滑。花粉囊内壁细胞,断面观类长方形,壁呈条状增厚;表面观类多角形,垂周壁连珠状增厚。草酸钙簇晶细小,直径9~19μm,棱角尖。
