甲基橙制备方法的改进_ 2015 刘婷婷
已改正有机化学实验十五甲基橙的制备

实验十五甲基橙的制备Preparation of methyl orange一.实验目的:1.了解偶联反应在有机合成中的应用。
2.掌握重氮盐和甲基橙的制备原理及方法。
学会用冰水浴控温,巩固抽滤、重结晶、干燥等操作。
二.实验重点和难点:1.甲基橙制备反应原理。
2.制备反应的操作方法。
实验类型:基础性实验学时:4学时三.实验装置和药品:主要实验仪器:烧杯酒精灯试管玻棒温度计抽滤瓶布氏漏斗主要化学试剂:对氨基苯磺酸晶体亚硝酸钠N,N--二甲苯胺浓盐酸氢氧化钠95%乙醇乙醚冰醋酸冰块淀粉---碘化钾试纸四.实验装置图:五.实验原理:甲基橙变色范围3.1—4.4(红---黄),橙红色鳞状晶体或粉末状,微溶于水,易溶于热水(1份溶于500份水中),不溶于乙醇,显碱性,0.1%的水溶液是常用的酸碱指示剂。
甲基橙是一种指示剂,它是由对氨基苯磺酸重氮盐与N,N--二甲基苯胺的醋酸盐。
在弱酸性介质中偶合得到的。
偶合首先得到的是嫩红色的酸式甲基橙,称为酸性黄。
在碱中酸性黄转变为橙黄色的钠盐,即甲基橙。
甲基橙的命名:4-{[4-(二甲氨基)苯]偶氮}苯磺酸钠盐或对二甲氨基偶氮苯磺酸钠本实验主要运用了芳香伯胺的重氮化反应及重氮盐的偶联反应。
由于原料对氨基苯磺酸本身能生成内盐,而不溶于无机酸,故采用倒重氮化法,即先将对氨基苯磺酸溶于氢氧化钠溶液,再加需要量的亚硝酸钠,然后加入稀盐酸。
六.实验內容及步骤:1.重氮盐的制备:在烧杯中放置10mL 5% NaOH 溶液及2.1g 对氨基苯磺酸晶体,温热使之溶解,然后冷却至室温。
另溶解0.8g NaNO2于6mL 水中,加入到上述烧杯内,用冰盐浴冷至0-50C。
在不断搅拌下,将3mL 浓盐酸与10mL 水配成的溶液缓缓滴加到上述混合液中,(观察现象),并控制温度在50C 以下,滴加完后,用淀粉---碘化钾试纸检验(注意观察现象)(如15-20秒内不变蓝,要补充NaNO2, NaNO2过量,可用尿素水溶液使其分解)。
甲基橙的制备

2.重氮化步骤中,对于1mol芳胺,酸的用量一般为2.5一3mo1,1mo1酸与亚硝酸钠反应产生亚硝酸,1mo1酸生成重氮盐,余下的过量的酸是为了维持溶液一定的酸度,防止重氮盐与未起反应的胺发生偶联。
酸的用量一般为2.5一3mo1,1mo1酸与亚硝酸钠反应产生亚硝酸,1mo1酸生成重氮盐,余下的过量的酸是为了维持溶液一定的酸度,防止重氮盐与未起反应的胺发生偶联。邻氨基苯甲酸重氮盐是个例外,由于重氮化后生成的内盐比较稳定,故不需要过量的酸。
重氮化反应还必须注意控制亚硝酸钠的用量,若亚硝酸钠过量,则生成多余的亚硝酸会使重氮盐氧化而降低产率。因而在滴加亚硝酸钠溶液时,必须及时用碘化钾一淀粉试纸试验至变蓝为止。
十二、参考文献
周志高编,《有机化学实验》,化学工业出版社,1998.10 p143-148
备注
实验设计者:章烨
首开实验时间:2007年5月
编写人:章烨
编写时间:2006年12月
三、实验示意图
重氮化盐制备
四、实验用主要仪器设备、消耗品
仪器设备名称
规格
消耗品名称
规格
烧杯
250ml
氢氧化钠
5%
滴液漏斗
100ml
对-氨基苯磺酸
CP
锥形瓶
250ml
亚硝酸钠
CP
布氏漏斗
常量
浓盐酸
CP
抽滤瓶
250ml
N,N-二甲基苯胺
CP
圆底烧瓶
实验4-4 甲基橙的制备

吉林工业职业技术学院 王文姣、初玉霞等制
实验4-4 甲基橙的制备
CONTENTS
目
01 02
录
03
04
05
06
目的要求 实验原理 实验用品 实验步骤 注意事项
思考题
【目的要求】
一
熟悉重氮化反应 及偶联反应的原 理与条件,掌握 甲基橙的制备方 法
二
熟悉低温操作 技术
【实验步骤】 重结晶
将上述粗产物用沸水进行重结晶(每克粗产物约需25 mL水)。 待结晶析出完全后,抽滤。滤饼依次用少量无水乙醇、乙醚进行洗涤,压紧 抽干。产品转移至表面皿上,于50 ℃以下自然晾干,称量质量,并计算产率。
性能试验
取少许产品溶解于水中,先加几滴稀盐酸溶液,再用稀氢氧化钠溶液中 和。观察溶液颜色变化,记录实验现象。
N(CH3)2 CH3COONa
H2O
【实验用品】
氢氧化钠溶液(5 %) 氯化钠溶液(饱和) 对氨基苯磺酸 N,N-二甲苯胺 淀粉-碘化钾试纸 无水乙醇 亚硝酸钠 浓盐酸
冰醋酸 氯化钠 乙醚 减压过滤装置 烧杯(100 mL、200 mL) 温度计(100 ℃) 水浴锅 表面皿
【实验步骤】
重氮化
【实验步骤】
偶联
试管中加入1.3 mL N,N-二甲苯胺和l mL冰醋酸,振荡混匀。不断搅拌下 将此溶液缓慢加到上述冷却的重氮盐溶液中(此间应始终保持低温操作)。 继续反应10 min,然后慢慢加入25mL 氢氧化钠溶液,此时反应液变为橙红 色,粗甲基橙呈细粒状沉淀析出。
盐析、抽滤
烧杯从冰盐水浴中取出恢复至室温。加入5 g氯化钠,搅拌并于沸水 浴中加热5 min,冷却至室温后再置于冰-水浴中冷却。待甲基橙晶体析 出完全后,抽滤。用少量饱和氯化钠溶液洗涤烧杯和滤饼,压紧抽干。
甲基橙制备方法微型化的探讨
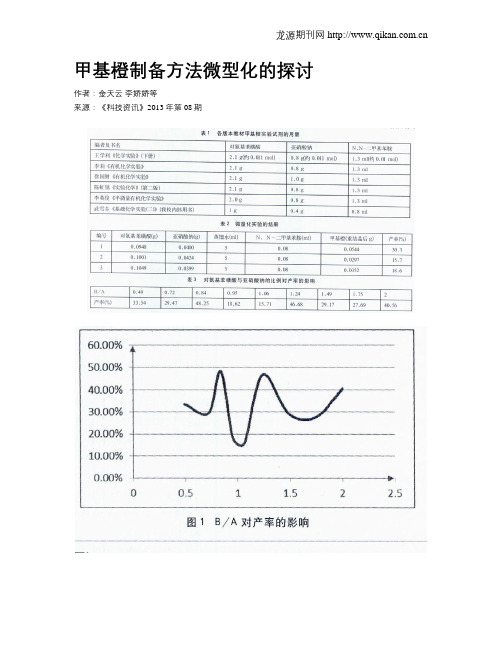
甲基橙制备方法微型化的探讨作者:金天云李娇娇等来源:《科技资讯》2013年第08期摘要:甲基橙是化学实验中常用的酸碱指示剂,其制备实验是大学基础化学实验中一种重要的合成实验,本文主要探讨甲基橙制备实验的微型化改革和甲基橙产率最大时的反应物比例关系。
关键词:甲基橙制备微量绿色化中图分类号:TQ421 文献标识码:A 文章编号:1672-3791(2013)03(b)-0210-02甲基橙是大学基础化学实验中最常用的化学试剂,被广大师生了解和熟悉,在无机化学测定溶液的酸碱性实验,有机化学甲基橙的合成实验,分析化学酸碱滴定等实验中,学生对甲基橙的性质和用法有了深刻的认识。
其中甲基橙制备实验是基础化学实验Ⅱ中重要的一组化学实验,实验中涉及到两类经典的胺类化合物特有的反应——重氮化反应和偶联反应,通过实验,学生能够很好地学习和掌握实验原理及胺类化合物的性质。
甲基橙制备实验所需实验仪器和设备普通,实验步骤和操作相对简单,实验效果明显,实验原理重要,具有代表性。
多数高校化学实验课都会涉及该实验。
1 甲基橙实验室制备方法的改进1.1 甲基橙制备实验改进的必要性我们知道,传统的教学方法很难起到一个完美的实验效果。
一些教师仅仅是为了教实验而“教”,学生仅仅是为了做实验而“做”,完全按照实验教科书上的内容去做[1],忽略了实验本身的价值和意义,没有认识到实验特有的性质。
因此对实验适当的改进是必要的。
1.2 甲基橙制备实验的改进方向近年来,毒奶粉,毒馒头,瘦肉精,假胶囊,地沟油等恶性事件直接威胁到人类自身的生存和发展,十八大以来,国家将生态文明建设推到了又一新的高度,“努力建设美丽中国”并不是一个空口号,对我们化学工作者来说,如何能达到理想的实验效果,实现实验的绿色化,低碳化,节约化,这是一个值得我们深入探讨和研究的课题。
绿色化学是一门新兴的学科,是当今国际化学研究的前沿[2],绿色化学是以最经济,最清洁,最安全的方法生产绿色化产品[3],符合化学实验的“12项”原则,要求我们进行对环境影响尽可能小的化学实验,做到原子经济性实验。
论文《甲基橙的制备》

论文《甲基橙的制备》长江大学工程技术学院文献检索与利用大作业系部:化工系专业:化学工程与工艺班级:化工 61101班级序号: 27学生姓名:罗磊1 前言19世纪50年代后,滴定分析法中采用了人工染料指示剂,1875年,德国人G.隆格合成了甲基橙。
甲基橙为小分子有机化合物,橙黄色粉末或结晶状鳞片,微溶于水,较易溶于热水,不溶于乙醇,显碱性,有毒。
它是实验室常用的酸碱指示剂(0.1%的水溶液),pH的变色范围为3.1(红色)-4.4(黄色)。
其用途非常广泛,可作为生物染色,生化研究,测定多数矿酸、强碱和水的碱度等其他用途,所以对于甲基橙的制备是很有意义的。
甲基橙的传统合成方法是“逆加法”,即先将对氨基苯磺酸碱化成水溶性较好的盐,然后在低温强酸性环境中发生重氮化反应,制得的重氮盐于醋酸环境中与N,N-二甲基苯胺偶联、碱化中和、重结晶制得。
所需的条件是低温,因为操作过程中要防止重氮盐的分解。
在偶联反应步骤,反应体系的反应物用量是导致实验失败的原因;在偶合反应过程中,反应体系过强是导致实验失败的关键,因此,本次试验讨论亚硝酸钠对甲基橙制备过程中有何影响。
为此在偶联反应步骤分别加入不同量的亚硝酸钠进行调节,取得了理想的实验结果。
此外再次验证了亚硝酸钠用量对产率的影响。
传统合成方法在重氮化时,埋没了对氨基苯磺酸。
本实验讨论亚硝酸钠量不同,对实验的影响。
我们通过不同实验操作过程和对实验中某些药品的替换,来探索提高甲基橙的产率,最终确定甲基橙的最佳制备方法。
甲基橙的制备2 实验2.1实验仪器和药品2.1.1实验仪器:烧杯(50ml、100ml),玻璃棒,温度计(200℃),胶头滴管,布氏漏斗,吸滤瓶,DF-101C型集热式恒温加热磁力搅拌器,SHZ-D(Ⅲ)循环水式真空泵,滤纸,天平,量筒(50ml、10ml),试管。
2.1.2药品:对氨基苯磺酸, N,N-二甲基苯胺,氢氧化钠(10%),亚硝酸钠,冰醋酸,浓盐酸(38%),硫酸(98%),磷酸(85%),乙醇,淀粉碘化钾试纸,PH试纸。
甲基橙合成的一种改进方法

第13卷 第1期2000年3月聊城师院学报(自然科学版)Journal of L iaochers U niversity(N at.Sci.)V o l.13N o.1M ar.2000甲基橙合成的一种改进方法α任树梅 李考真(聊城师范学院化学系,聊城252059)摘 要 介绍了一种在常温下由对氨基苯磺酸通过重氮化反应和N,N2二甲苯胺偶联反应一步合成甲基橙的方法.产率较高.关键词 甲基橙,常温合成,指示剂分类号 O621甲基橙是重要的酸碱指示剂经典的合成方法,是以对氨基苯磺酸为原料,采用逆加法,低温重氮化,其重氮盐在弱酸环境中再与N,N2二甲苯胺发生偶联反应制得.反应过程中为了要保持反应体系的酸碱性要多次加入酸或碱,并要控制温度不能超过5℃操作复杂,合成条件不易控制.对此我们进行了探索研究,在常温下一步合成甲基橙.实验中我们发现在水相介质中发生重氮化偶联反应时,无需加入酸或碱,即可高收率地得到产品,而在水2乙醇等体系中产品收率降低.1 不同反应介质对反应的影响在其他条件不变的情况下(即对氨基苯磺酸2.5g,N,N2二甲苯胺1.5mL,20%亚硝酸钠5mL),不同反应介质对甲基橙产量的影响.表1 氢氧化钠水溶液对产品的影响浓度(%)0.51.01.52.04.0体积(mL)11060403218产量(g)0.20.40.60.70.8产率(%)4.38.612.815.017.2 小结:该类溶液中所做的产品,色泽好,但产率太低.同时在溶解过程中有乳浊现象出现,对氨基苯磺酸全溶,搅拌完毕液面浮有一层油状物,表明反应不彻底.表2 碳酸氢钠水溶液对产品的影响浓度(%)1248体积(mL)6040188产量(g)2.72.01.51.3产率(%)57.542.631.927.7 小结:该类溶液中随溶液浓度的减小产率而升高,但最多达到57.5%.固体溶解完全.加碳酸氢钠过程中,冒出大量气泡.α收稿日期:1997207225表3 直接在水中发生反应时体积(mL )30406080100产量(g )33.23.54.04.2产率(%)62.967.273.385.287.8 小结:直接用水产品产率最高,对氨基苯磺酸不溶,而在反应过程中逐渐溶解,反应迅速,搅拌结束时,液面无油状物,表明反应彻底.表4 甲基橙在不同pH 下的变色范围pH 2345678颜色红红橙黄黄黄黄 文献值表明,甲基橙的变色范围:(红)3.1-橙-4.4(黄),实验结果与文献值相符.2 表征2.1 甲基橙、碱溶液中的变色试验取少量甲基橙产品,配成1%的水溶液,在不同酸、碱溶液中进行酸碱试验(见表4).2.2 红外光谱特征吸收我们以分析纯的甲基橙为基准样品,和我们所做的产品在相同条件下,分别作了红外光谱图,谱图表明基本一致.(图1).3 在水中常温合成甲基橙的最佳条件综上所述,我们认为在水中常温下合成甲基橙的最佳条件应为(1) 称取2.5g 对氨基苯磺酸,在100mL 烧杯中与1.5mLN ,N 2二甲苯胺混合均匀,加入60mL 蒸馏水.在强搅拌下滴加20%亚硝酸钠溶液5mL ,滴加完后为使反应完全继续搅拌20m in .调pH 值到碱性,加热至沸,冷却,过滤得甲基橙粗品.将粗品用2%氢氧化钠溶液60mL 重结晶,得纯甲基橙3.0~4.2g ,产率62.9%~87.8%.46聊城师院学报(自然科学版)第13卷(2) 按照以上提供的条件,我们在化学系九七级二班作了推广实验,结果如下:全班共计35人,分17个实验小组,3~3.9g 的共八组,4.0~4.2g 的九组.(3) 按照以上条件,我们进行了扩大实验,将所有原料扩大到原来的十倍,产量42g .产率87%.4 结束语在水中常温一步合成甲基橙,具有操作简便,产品产率高、纯度好的特点.并具有很高的推广和使用价值.参考文献1 曾昭琼.有机化学实验.北京:高等教育出版社,1987An I m p roved fo r P repa ring M e thyl O ra ngeR en Shum ei L i Kaozhen(D epartm ent of Chem istry ,L iaochengT eachers U niversity ,L iaocheng 252059)Abstract T he acidbase indicato r m ethyl o range w as syn thesized by the diazo tisati on of su lp han ilic acid and coap ling reacti on of the diazon iun sat w ith N ,N 2di m ethylan iline at room tem peratu re in one step .T he yield w as good .Key words M ethyl o range ,Room tem p eratu re ,Indicato r (上接第54页)Fa ult D e tec tion in the Chem ica l Rea c to rsUs ing A rtific ia l Neura l Ne tw o rksL iu M in(D epar m ent of Chem isty ,L iaocheng T eachers U niversity ,L iaocheng 252059)Abstract T h is Paper discu sses the fau lt detcti on in the chem ical reacto rs u sing B P algo rithm and revised Fah l m an algo rithm of the artificial neu ral netw o rk .T he advan tage of the latter can be seen by the com parison of the rate and p roperty of the iterati on of tw o algo rithm s .Key words N eu ral netw o rk ,Chem ical reacto r ,B P algo rithm ,R evised Fah l m an algo rithm 56第1期 任树梅等:甲基橙合成的一种改进方法 。
甲基橙制备方法的改进_ 2015 刘婷婷

氮盐的分解。故而对氨基苯磺酸能够在常温下重氮化,实验步
骤得以简化,减少了副反应,也缩短了反应时间。
2. 3 甲基橙的表征
2. 3. 1 甲基橙的变色实验 取少量甲基橙产品,配成 1% 的水溶液,在不同酸、碱溶
液中进行实验( 见表 2) 。
图 1 红外光谱图 Fig. 1 IR spectrum
3结论
[4] 中西香尔 P,索罗曼 H. 红外光谱分析 100 例[M]. 北京: 科学出版 社,1984: 41 - 42,61 - 68.
[5] 黄一石. 仪器分析[M]. 北京: 化学工业出版社,2002: 250 - 251.
为橙黄色的钠盐,即甲基橙。在常温反应时充分利用了对氨基
苯磺酸和 N,N - 二甲基苯胺自身的酸碱性来完成反应。重氮化
时,利用自身的酸碱两性就可以形成含阴离子的重氮内盐不用
外加强碱和强酸,降低了反应成本。
( 2)
低温时强酸中的重氮化反应,生成了 - NH(
CH3 )
+ 2
的
吸电子诱导作用,降低了苯环上的电子云密度,因此苯环很难
1. 2 常温一步法制备甲基橙的原理
常温一步法制备甲基橙,利用了原料自身的酸碱性来完成 反应,如 N,N - 二甲基苯胺呈碱性,可增大对氨基苯磺酸的溶 解性; 利用对氨基苯磺酸的酸性来进行重氮化,亚硝酸钠与之 等摩尔反应生成亚硝酸,可避免因亚硝酸过量引起的副反应, 无需再检验亚硝酸是否过量; 偶合反应与重氮化反应于同一容 器中,生成的中性内盐———重氮盐,立即与 N,N - 二甲基苯胺 偶合,从而减少了重氮盐分解的可能性。
* 基金项目: 徐州工程学院实验教学示范中心专项建设项目 ( 2013 - 2014) 。 第一作者: 刘婷婷,女,学生。 通讯作者: 石春玲 ( 1978 - ) ,女,副教授,主要从事有机合成方法研究。
《甲基橙的制备》论文[
摘要:甲基橙,亦称“金莲-D”,化学名是“对二甲氨基偶氮苯磺酸钠”。
【1】0.1%的水溶液是常用的酸碱指示剂;分光光度测定氯、溴和溴离子。
可与靛蓝二磺酸钠或溴甲酚绿组成混合指示剂,以缩短变色域和提高变色的锐灵性。
氧化还原指示剂,如用于溴酸钾滴定三价砷或锑。
【2】在偶联反应步骤,反应体系的反应物用量是导致实验失败的原因。
为此在偶联反应步骤分别加入不同量的亚硝酸钠进行调节,取得了理想的实验结果。
此外再次验证了亚硝酸钠用量对产率的影响。
关键词:对氨基苯磺酸二甲基苯胺甲基橙偶联反应重氮盐一、引言甲基橙为小分子有机化合物,橙黄色粉末或结晶状鳞片,与水配比即可得到甲基橙溶液,主要作为酸碱指示剂使用,测量的PH范围是3.1--4.4(由红至黄色)。
甲基橙的传统合成法是“逆加法”,即将对氨基苯磺酸碱化成水溶性较好的盐,然后在低温强酸性环境下发生重氮化反应,值得的重氮盐于醋酸环境下与N,N-二甲基苯胺偶联,碱化中和,重结晶制得。
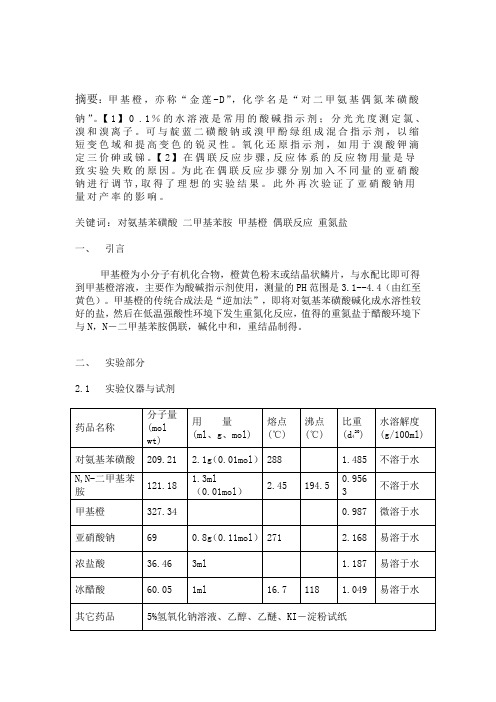
二、实验部分2.1实验仪器与试剂主要仪器:烧杯量筒温度计布氏漏斗抽滤瓶2.2 主要试剂物理性质2.3 实验原理将对氨基苯磺酸与氢氧化钠作用生成易溶于水的盐,再与硝酸重氮化,然后与N,N二甲基苯胺偶联得到粗产品,粗产品在%5的氢氧化钠溶液中重结晶,得到甲基橙产品。
2.4 实验步骤(1)、重氮盐的制备在50ml烧杯中、加入10ml 5%氢氧化钠溶液和2.1g对氨基苯磺酸晶体,温热使结晶溶解,用冰盐浴冷却至0℃以下。
另在一试管中配制0.8g亚硝酸钠和6ml水的溶液。
将此配制液也加入烧杯中。
维持温度0-5℃,在搅拌下,慢慢用滴管滴入3ml浓盐酸与10ml水配成的溶液,直至用淀粉-碘化钾试纸检测呈现蓝色为止,继续在冰盐浴中放置15分钟,使反应完全,这时往往有白色细小晶体析出。
【3】(2)、偶合反应在试管中加入1.3ml N,N-二甲基苯胺和1ml 冰醋酸,并混匀。
在搅拌下将此混合液缓慢加到上述冷却的重氮盐溶液中,加完后继续搅拌10min。
精细化工实验技术 实验四甲基橙的制备

染料
3.盐析、抽滤
将烧杯从冰盐水浴中取出,恢复至室温。加入5g氯化钠,搅拌并放 入沸水浴中加热使其全部溶解。冷至室温后置于冰水浴中冷却。待甲基 橙晶体完全析出后,抽滤。用少量饱和氯化钠水溶液洗涤烧杯和滤饼, 压紧抽干。
2.偶合反应
将l.3mL(0.01mol)N,N-二甲基苯胺与lmL冰醋酸混合,搅
拌下将此溶液加到上述重氮盐溶液中。加完后搅拌反应l0 min。 然后缓慢加入25mL 5%氢氧化钠溶液直至反应液变为橙色。若反应
物中尚存N,N-二甲基苯胺的醋酸盐,在加入氢氧化钠后,就有N, N-二甲基苯胺析出,影响产物的纯度。将橙色溶液在沸水浴上加
4.检验变色效果
把少许甲基橙晶体溶于水,加几滴盐酸,随后用稀氢氧化钠溶液中 和碱化,观察溶液颜色变化。
染料
六、实验记录与数据处理
1.实验记录:
碘化钾淀粉试纸若变蓝,则说明亚硝酸钠过量。此时加
g尿素搅拌后,碘化钾淀粉试纸刚好变成蓝色。
粗产物:
g;外观:
;纯度
%;
精制产物:
g;外观:
;纯度 %。
加盐酸后甲基橙溶液颜色:由 色变为 色;
将对氨基苯磺酸钠与亚硝酸钠的混合液在搅拌下慢慢倒 入冰冷的盐酸溶液中,用刚果红试纸检验,始终保持反应液 为酸性,并且控制反应温度在5℃以下。
染料
将反应混合物在冰盐浴中放置15 min,以保证反应全部完成。 对氨基苯磺酸的重氮盐在此时往往析出,这是因为重氮盐在水中 可电离,形成内盐,在低温下难溶于水而形成细小的晶体析出。 用碘化钾淀粉试纸检验溶液中是否有过量的亚硝酸。若碘化钾淀 粉试纸变蓝,则表明亚硝酸过量,可加入少量尿素分解。
甲基橙合成实验的改进

3 结 论
通过合成甲基橙的低温方法与常温方法的比 较得知 ,在常温下合成甲基橙可以充分利用对氨基
苯磺酸本身的酸性来完成重氮化 ,省去了外加酸 ,
减少了原料的消耗 ,降低了反应成本 ,操作时便于
控制温度 ,简化了实验步骤 ,缩短了实验时间 ,使收
3结论通过合成甲基橙的低温方法与常温方法的比较得知在常温下合成甲基橙可以充分利用对氨基苯磺酸本身的酸性来完成重氮化省去了外加酸减少了原料的消耗降低了反应成本操作时便于控制温度简化了实验步骤缩短了实验时间使收率由原来的67提高到85改进效果明显
2009年第 31卷第 1期
化学与黏合 CHEM ISTRY AND ADHESION
2 结果与讨论
2. 1 低温与常温制备甲基橙方法的对比
表 1 低温与常温合成甲基橙方法的对比
Table 1 Comparison between two methods of synthesizing methyl orange,
one is at room temperature and the other one is at low temperature
存在 ,由于 - N (CH3 ) 2 +的强供电子共轭效应 ,使二 甲基苯胺中苯环上的电子云密度增加 ,有利于重氮 离子对其进行亲电取代反应 。因此 ,重氮离子一但 生成 ,就 立 即 与 二 甲 基 苯 胺 发 生 偶 联 而 生 成 产 物 [3]。
实验证明对氨基苯磺酸可以在常温下进行重 氮化 ,并简化了实验步骤 ,缩短了合成时间 。
关键词 :甲基橙 ;常温合成 ;实验改进 中图分类号 : TQ 421. 3 文献标识码 : B 文章编号 : 1001 - 0017 (2009) 01 - 0075 - 03
关于甲基橙制备实验的两点意见

关于甲基橙制备实验的两点意见
索福喜
【期刊名称】《殷都学刊》
【年(卷),期】1992(000)004
【总页数】3页(P81-82,66)
【作者】索福喜
【作者单位】无
【正文语种】中文
【中图分类】O62-33
【相关文献】
1.甲基橙插层水滑石的制备及表征r——一个大学化学开放性实验设计 [J], 郭俊青;李佳;吕国伟;王海霞
2.关于甲基橙制备实验的两点意见 [J], 索福喜
3.石墨相氮化碳的制备及光催化降解甲基橙综合实验 [J], 刘文亮;温福山;楚雨格;苏畅;王有和;孙海翔
4.甲基橙制备实验的衍生与探索 [J], 王乾晓;李诗勉;王琨;周金梅;林丽榕
5.TiO2-锌卟啉催化剂的制备及光催化降解甲基橙实验设计 [J], 陈韶蕊;余旭东因版权原因,仅展示原文概要,查看原文内容请购买。
甲基橙制备

一、实验目的1.通过甲基橙的制备学习重氮化反应和偶合反应的实验操作;2.巩固盐析、重结晶和抽滤等操作。
二、实验原理1. 反应式:三、主要试剂及物理性质1.试剂:对氨基苯磺酸、N,N-二甲基苯胺、浓盐酸、5%NaOH、冰醋酸、10%NaOH、NaNO2、饱和NaCl溶液、乙醇2.试纸:淀粉-碘化钾试纸3.物理性质四、试剂用量规格五、仪器装置仪器:100ml烧杯、500ml烧杯、滴管、电磁炉、玻璃棒、吸滤瓶、布氏漏斗、表面皿、抽气泵、100ml量筒、10ml量筒六、实验步骤及现象七、实验结果理论结晶产量:2.00/173×327=3.78g实际结晶产量:3.40g (橙红色晶体,表面有银光色)产率:3.40/3.78×100%=89.95%八、问题讨论1、在本实验中,重氮盐的制备为什么要控制在0-5℃中进行?偶合反应为什么在弱酸性介质中进行?答:1>控制温度是因为重氮盐不稳定遇热易分解2>控制为弱酸性是因为此时重氮正离子的浓度大,且芳胺呈游离态,有利于偶联。
2、在制备重氮盐中加入氯化亚铜将出现什么样的结果?答:氨基磺酸是一个很稳定的溶剂,既能溶解又能防止试剂发生别的反应,氯化亚铜只是催化剂,使重氮盐分解成氯苯和氮气。
3、N,N-二甲基苯胺与重氮盐偶合为什么总是在俺记得对位上发生?答:重氮盐与三级芳胺偶联生成对氨基偶氮化合物,如果氨基对位有取代基,则偶联在邻位发生,因为氨基是很好的邻对位定位基团。
九、实验讨论结果分析:甲基橙产率较高,颜色相对较鲜红。
产率没有达到100%原因:1.冷却结晶时间不够,晶体没有完全析出;2.抽滤时玻璃棒、烧杯、滤纸上残留些许晶体;3.溶液PH值有点低,使得制备出来的甲基橙颜色较红。
操作要点:1.N,-N-二甲基苯胺有毒,致癌,实验时小心使用,接触后马上洗手;2.制备重氮盐时,温度应保持在5℃以下。
如果重氮盐的水溶液温度升高,重氮盐会水解生成酚,降低产率。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
关键词: 甲基橙; 常温制备; 改进方法
中图分类号: TQ421. 3
文献标志码: A
1. 3 实验步骤
在烧杯中加入 1. 8 g( 0. 01 mol) 无水对氨基苯磺酸、1. 2 g ( 0. 01 mol) N,N - 二甲基苯胺和 30 mL 水,加入搅拌子,用电 动搅拌器至固体完全溶解,在冷水浴下搅拌用恒压滴液漏斗滴 加亚硝酸钠水溶液( 0. 8 g 亚硝酸钠溶于 6 mL 水中) ,控制反应
亚硝酸钠 /g 5 mol / L 氢氧化钠 / mL
浓盐酸 / mL 冰醋酸 / mL
收率 /%
低温法 0 ~5
5 2. 1 1. 2 0. 8 35
3 1 76
常温法 20 ~ 25
2. 5 1. 8 1. 2 0. 8 4. 5
0 0 87
表 2 甲基橙在不同 pH 时的变色范围 Table 2 Color range of methyl orange in different pH
Key words: methyl orange; preparation at room temperature; improvement method
甲基橙是一种非常有用的酸碱指示剂,在生产和科学实验 中经常使用。目前的高等学校有机化学实验教材中[1],甲基橙 的制备大多使用的是经典三步法: 由对氨基苯磺酸、氢氧化 钠、亚硝酸钠和盐酸经过低温( 0 ~ 5 ℃ ) 重氮化反应生成重氮 盐,再与 N,N - 二甲基苯胺偶合,最后用氢氧化钠溶液进行重 结晶而制得。这种方法中低温控制比较困难,实验收率中等, 由于需在低温进行所需反应时间较长。因此参考相关文献,我 们将甲基橙的制备实验进行改进,使用常温一步法直接进行制 备。改进后的方法既丰富了有机化学实验的教学内容 ( 如用电 动搅拌、滴加反应物、减压抽滤等有机实验操作) ,且还降低 了反 应 的 能 耗、试 剂 的 耗 损,操 作 简 洁、条 件 易 行、时 间 减 少[2 - 3]。
1 实验部分
1. 1 仪器与试剂
烧杯; 电动搅拌器; 恒压滴液漏斗; 布氏漏斗; 抽滤瓶; 量筒; 天平; 真空循环水泵( SHZ - D) ,巩义英峪予华; 红外 光谱( R - 460) ,日本岛津。
对氨基苯磺酸; 亚硝酸; 氢氧化钠; 盐酸; N,N - 二甲基 苯胺; 乙醇; 乙醚; 均为化学纯。
第 43 卷第 1 期 2015 年 1 月
广州化工 Guangzhou Chemical Industry
Vol. 43 No. 1 Jan. 2015
甲基橙制备方法的改进*
刘婷婷,石春玲
( 徐州工程学院化学化工学院,江苏 徐州 221111)
摘 要: 实验室中甲基橙的经典制备方法是低温三步法,这种方法特点是反应条件难以控制、需要很长时间、收率较低等。
Abstract: The classical method of preparation methyl orange in the lab was three - step method at low temperature, which was difficult to control experimental condition,long reaction time and low yield. At room temperature,methyl orange can be prepared by one - step method. It was found that anhydrous p - aminobenzenesulfonic acid,N,N - dimethylaniline and water were added into the beaker at room temperature,while stirring and dissolving,sodium nitrite was slowly dropping at cold water,and the reaction should continue 25 min with stirring after dropping was finished,and the yield could reach about 87% . The yield was higher than that of the classical three - step method under low temperature
2. 2 讨 论
( 1) 高校有机化学实验书中,经典的低温三步法制备甲基
橙,其基本过程大同小异[2]。第一步,将对氨基苯磺酸用氢氧
化钠水溶液碱化成盐,再在低温( 0 ~ 5 ℃ ) 浓盐酸中进行重氮
化反应,得到重氮盐。第二步,在醋酸环境中与 N,N - 二甲基
苯胺偶联,得到酸性黄。第三步,在碱性条件下,酸性黄转变
为橙黄色的钠盐,即甲基橙。在常温反应时充分利用了对氨基
苯磺酸和 N,N - 二甲基苯胺自身的酸碱性来完成反应。重氮化
时,利用自身的酸碱两性就可以形成含阴离子的重氮内盐不用
外加强碱和强酸,降低了反应成本。
( 2)
低温时强酸中的重氮化反应,生成了 - NH(
பைடு நூலகம்
CH3 )
+ 2
的
吸电子诱导作用,降低了苯环上的电子云密度,因此苯环很难
进行亲电取代反应。而在常温环境且在同一容器中进行一步反
应,速度快,游离的 N,N - 二甲基苯胺由于 - N( CH3 ) 2 的强的
供电子共轭效应,使得 N,N - 二甲基苯胺苯环上的电子云密度
增加,有利于重氮离子对其进行亲电取代反应。所以,重氮离
子一旦形成立即与 N,N - 二甲基苯胺发生偶联反应,减少了重
1. 2 常温一步法制备甲基橙的原理
常温一步法制备甲基橙,利用了原料自身的酸碱性来完成 反应,如 N,N - 二甲基苯胺呈碱性,可增大对氨基苯磺酸的溶 解性; 利用对氨基苯磺酸的酸性来进行重氮化,亚硝酸钠与之 等摩尔反应生成亚硝酸,可避免因亚硝酸过量引起的副反应, 无需再检验亚硝酸是否过量; 偶合反应与重氮化反应于同一容 器中,生成的中性内盐———重氮盐,立即与 N,N - 二甲基苯胺 偶合,从而减少了重氮盐分解的可能性。
参考文献
[1] 李吉海,刘金庭. 基础化学实验( II) —有机化学实验. 2 版[M]. 北 京: 化学工业出版社,2007: 148 - 150.
[2] 张健,谭丹. 一步法合成甲基橙实验条件的优化[J]. 中南民族大学 学报: 自然科学版,2007( 4) : 26.
[3] 张建丽,闻质红. 常温合成甲基橙的新探索[J]. 中原工学院学报, 2010,21( 2) : 76 - 78.
氮盐的分解。故而对氨基苯磺酸能够在常温下重氮化,实验步
骤得以简化,减少了副反应,也缩短了反应时间。
2. 3 甲基橙的表征
2. 3. 1 甲基橙的变色实验 取少量甲基橙产品,配成 1% 的水溶液,在不同酸、碱溶
液中进行实验( 见表 2) 。
图 1 红外光谱图 Fig. 1 IR spectrum
3结论
* 基金项目: 徐州工程学院实验教学示范中心专项建设项目 ( 2013 - 2014) 。 第一作者: 刘婷婷,女,学生。 通讯作者: 石春玲 ( 1978 - ) ,女,副教授,主要从事有机合成方法研究。
第 43 卷第 1 期
刘婷婷,等: 甲基橙制备方法的改进
77
温度不超过 26 ℃ 。滴加完毕,继续搅拌 25 min,再滴入 5% 氢 氧化钠水溶液 4. 5 mL,搅拌,可加入适量水并加热促进溶解。 待结晶在冰水中完全析出后抽滤,沉淀依次用少量乙醇、乙醚 洗涤,得橙色片状晶体。干燥后称重,约 2. 84 g,产率 87% 。
pH
颜色
2
红
3
红
4
橙
5
黄
6
黄
7
黄
8
黄
文献中甲基橙变色范围: ( 红) 3. 1 ~ 4. 4( 黄) ,实验结果与 文献值相符。 2. 3. 2 红外光谱
以分析纯的甲基橙为基准样品,实验所得的产品在相同条 件下,分别作了红外光谱,谱图表明基本一致[4 - 5]( 图 1) 。
由表 1 中的数据说明,常温一步法制备甲基橙操作简便、 试剂损耗少、时间较短、收率较高。
[4] 中西香尔 P,索罗曼 H. 红外光谱分析 100 例[M]. 北京: 科学出版 社,1984: 41 - 42,61 - 68.
[5] 黄一石. 仪器分析[M]. 北京: 化学工业出版社,2002: 250 - 251.
文章编号: 1001 - 9677( 2015) 01 - 0076 - 02
Improvement of Methyl Orange Preparation*
LIU Ting - ting,SHI Chun - ling ( School of Chemistry and Chemical Engineering,Xuzhou Institute of Technology,Jiangsu Xuzhou 221111,China)
将常温一步法制备甲基橙与经典的低温三步法制备甲基橙 进行比较后得知,常温方法可以充分利用反应原料自身的酸碱 性促进反应的进行,如 N,N - 二甲基苯胺呈的碱性可增大对氨 基苯磺酸的溶解性; 偶合与重氮化反应在同一容器中,生成的 重氮盐立即与 N,N - 二甲基苯胺偶合,减少了重氮盐分解的可 能性; 利用对氨基苯磺酸的酸性完成重氮化,省去了外加碱和 酸,减少了原料的耗损,降低了反应成本,反应易于控制,实 验步骤简洁,时间大大缩短,产品收率得以提高,由 76% 提高 到 87% ,制备方法改进明显。
