高考化学复习专题课件:化学工艺流程-(共19张)
合集下载
高三工艺流程ppt课件

4
(2)分离提纯阶段的常见考点: ①调pH除杂:例如:若要除去Cu2+溶液中混有的Fe3+,可加入 CuO、Cu(OH)2、Cu2(OH)2CO3等物质来调节溶液的pH。 ②试剂除杂。 ③加热:加快反应速率或促进平衡向某个方向移动。如果在制备过 程中出现一些受热易分解的物质或产物,则要注意对温度的控制。如 NaHCO3、H2O2、Ca(HCO3)2、KMnO4、AgNO3、HNO3(浓)等物质。 ④降温:防止某物质在高温时会溶解(或分解)、使化学平衡向着题 目要求的方向移动。
蒸发浓缩, 冷却结晶,
④分液——互不相溶的液体间的分离
过滤,洗涤
⑤萃取——用一种溶剂将溶质从另一种溶剂中提取出来。
⑥升华——将可直接气化的固体分离出来。
⑦盐析——加无机盐使溶质的溶解度降低而析出
6
(4)获得产品阶段的其它考点: 趁热过滤:以防止某物质降温而析出; 洗涤(冰水、热水、醇洗):洗去晶体表面的杂质 离子,并减少晶体在洗涤过程中的溶解损耗。
2
▶高分策略,规范解题
(1)明确原始物质及目标物质。
(2)明确化工生产流程:原料→对原料的预处理→核心化学反应
→产品的提纯分离→目标产物。
(3)掌握主要的化工生产原理和绿色化学等。
(4)掌握常见的与化工生产有关的操作方法及作用。尤其要注
意对原料进行的预处理和控制反应条件的常用方法。
(2)原料与产品的简单计算(关系式法)。
5ቤተ መጻሕፍቲ ባይዱ
(3)获得产品阶段的常见考点:
①结晶——固体物质从溶液中析出的过程
a:蒸发结晶:提取溶解度随温度的变化而变化不大的溶质,如NaCl
b:冷却结晶:提取溶解度随温度的变化而变化较大的溶质、易水解
的溶质或结晶水合物,如 KNO3 、FeCL3 、CuSO4.5H2O ②过滤——固、液分离 ③蒸馏或分馏——液、液分离
(2)分离提纯阶段的常见考点: ①调pH除杂:例如:若要除去Cu2+溶液中混有的Fe3+,可加入 CuO、Cu(OH)2、Cu2(OH)2CO3等物质来调节溶液的pH。 ②试剂除杂。 ③加热:加快反应速率或促进平衡向某个方向移动。如果在制备过 程中出现一些受热易分解的物质或产物,则要注意对温度的控制。如 NaHCO3、H2O2、Ca(HCO3)2、KMnO4、AgNO3、HNO3(浓)等物质。 ④降温:防止某物质在高温时会溶解(或分解)、使化学平衡向着题 目要求的方向移动。
蒸发浓缩, 冷却结晶,
④分液——互不相溶的液体间的分离
过滤,洗涤
⑤萃取——用一种溶剂将溶质从另一种溶剂中提取出来。
⑥升华——将可直接气化的固体分离出来。
⑦盐析——加无机盐使溶质的溶解度降低而析出
6
(4)获得产品阶段的其它考点: 趁热过滤:以防止某物质降温而析出; 洗涤(冰水、热水、醇洗):洗去晶体表面的杂质 离子,并减少晶体在洗涤过程中的溶解损耗。
2
▶高分策略,规范解题
(1)明确原始物质及目标物质。
(2)明确化工生产流程:原料→对原料的预处理→核心化学反应
→产品的提纯分离→目标产物。
(3)掌握主要的化工生产原理和绿色化学等。
(4)掌握常见的与化工生产有关的操作方法及作用。尤其要注
意对原料进行的预处理和控制反应条件的常用方法。
(2)原料与产品的简单计算(关系式法)。
5ቤተ መጻሕፍቲ ባይዱ
(3)获得产品阶段的常见考点:
①结晶——固体物质从溶液中析出的过程
a:蒸发结晶:提取溶解度随温度的变化而变化不大的溶质,如NaCl
b:冷却结晶:提取溶解度随温度的变化而变化较大的溶质、易水解
的溶质或结晶水合物,如 KNO3 、FeCL3 、CuSO4.5H2O ②过滤——固、液分离 ③蒸馏或分馏——液、液分离
高考化学一轮复习化学工艺流程——物质的制备与提纯课件(50张)

_________________________________________________________。
[流程图解]流程图中各步主要转换如下:
[跟踪训练3] 某化学实验室以一种工业上的废渣(废渣主要含有
MgCO3、MgSiO3和少量Fe、Al的氧化物)为原料,制备MgCO3·3H2O。 实验流程如下图所示:
(4)利用上述表格数据,计算Ni(OH)2的Ksp=__×__(_10_-_1_4_)2_________(列 出计算式)。如果“转化”后的溶液中Ni2+浓度为1.0 mol·L-1,则 “调pH”应控制的pH范围是__~______。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正 极 材 料 的 NiOOH 。 写 出 该 反 应 的 离 子 方 程 式 __2_N_i_2+_+__C_l_O_-_+__4_O_H_-_=_=_=_2_N_iO__O_H_↓__+__C_l-_+__H_2_O____。
一元弱 将溶液中的硼元素转化为H3BO3,促进析出
溶浸 高温焙烧
微点拨 拆分流程图——“三看、二挖、一联” 【三看】 ①看原料成分和产物成分,如典例中的原料是Ni的氧化物,杂质是 油脂及Al、Fe的氧化物,需要除去。产物是硫酸镍晶体②看流程图中 物质的“进”和“出”,以及保留的中间产物、反应条件、实验操作
3.化工流程题中表述性词汇“八大答题方向” 化工生产流程和综合实验题中经常会出现一些表述性词语,这些表 述性词语就是隐性信息,它可以暗示我们所应考虑的答题角度。常见 的有 (1)“控制较低温度”——常考虑物质的挥发、物质的不稳定性和物 质的转化等。 (2)“加过量试剂”——常考虑反应完全或增大转化率、提高产率等。 (3)“能否加其他物质”——常考虑会不会引入杂质或是否影响产品 的纯度。
[流程图解]流程图中各步主要转换如下:
[跟踪训练3] 某化学实验室以一种工业上的废渣(废渣主要含有
MgCO3、MgSiO3和少量Fe、Al的氧化物)为原料,制备MgCO3·3H2O。 实验流程如下图所示:
(4)利用上述表格数据,计算Ni(OH)2的Ksp=__×__(_10_-_1_4_)2_________(列 出计算式)。如果“转化”后的溶液中Ni2+浓度为1.0 mol·L-1,则 “调pH”应控制的pH范围是__~______。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正 极 材 料 的 NiOOH 。 写 出 该 反 应 的 离 子 方 程 式 __2_N_i_2+_+__C_l_O_-_+__4_O_H_-_=_=_=_2_N_iO__O_H_↓__+__C_l-_+__H_2_O____。
一元弱 将溶液中的硼元素转化为H3BO3,促进析出
溶浸 高温焙烧
微点拨 拆分流程图——“三看、二挖、一联” 【三看】 ①看原料成分和产物成分,如典例中的原料是Ni的氧化物,杂质是 油脂及Al、Fe的氧化物,需要除去。产物是硫酸镍晶体②看流程图中 物质的“进”和“出”,以及保留的中间产物、反应条件、实验操作
3.化工流程题中表述性词汇“八大答题方向” 化工生产流程和综合实验题中经常会出现一些表述性词语,这些表 述性词语就是隐性信息,它可以暗示我们所应考虑的答题角度。常见 的有 (1)“控制较低温度”——常考虑物质的挥发、物质的不稳定性和物 质的转化等。 (2)“加过量试剂”——常考虑反应完全或增大转化率、提高产率等。 (3)“能否加其他物质”——常考虑会不会引入杂质或是否影响产品 的纯度。
2024届高三化学三轮复习专题工艺流程课件

⑥溶液配制、灼烧、蒸发、过滤用到的仪器⑦控制某反应的pH值使某些金属离子以氢 氧化物的形式沉淀(调节pH所用试剂为主要元素对应的氧化物、碳酸盐、碱,以避免 引入新的杂质;pH分离时的范围确定、范围过小的后果<导致某离子沉淀不完全>或过 大的后果<导致主要离子开始沉淀>)⑧减压蒸馏(减压蒸发)的原因:减小压强,使 液体沸点降低,防止(如H2O2、浓硝酸、NH4HCO3)受热分解\挥发⑨检验溶液中离 子是否沉淀完全的方法:将溶液静置一段时间后,向上层清夜中滴入沉淀剂,若无沉 淀生成,则离子沉淀完全⑩洗涤沉淀:沿玻璃棒往过滤器中加蒸馏水至浸没沉淀,待 水自然流下,重复操作2-3次
工艺流程题 答题策略
1 化工流程题的结构特点 2 化工流程答题思路 3 常见问题的答题策略 4 典例分析
目 录
1 化工流程题的结构特点
化工流程题的定义
就是将化工生产过程中的主要生产阶段即生产流程用框图形式表示出来,一般 都是以操作名称为主线,物质随着操作流程发生变化。
化工流程题的呈现方式
化工流程题的结构特点
的pH沉淀完全时
Al3+ 3.7
Fe3+ 2.2
Fe2+ 7.5
(c=1.0×10−5 mol∙L−1)的pH 8.7
4.7
3.2
9.0
回答下列问题:(1)“碱浸”中NaOH的两个作用分别是______________。为 回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离 子方程式______________。(2)“滤液②”中含有的金属离子是______________。 (3)“转化”中可替代H2O2的物质是______________。若工艺流程改为先“调 pH”后“转化”,即
高考化学工艺流程综合题讲解PPT精品课件

工艺流程综合题
考情 考法
分析
化学工艺流程题是高考的必考题型,题目综合性强,难 度大,通常以化工生产流程图的形式,以陌生元素或陌生化 合物知识为载体,综合考查元素化合物知识、氧化还原反应 方程式的书写、实验基本操作、实验步骤的分析、通过化工 原理的分析判断流程中残渣或废液的成分、反应条件的控制 与选择、产率的计算、Ksp的应用、绿色化学思想的体现等, 可以说是真正的学科内综合题,无所不考。
命题点 七
化学工艺流程题中的 绿色化学和循环使用
目的:提高原料的利用率,绿色化学
判断循环物质的方法: 箭头回头看 后面反应步骤的生成物,同为前面反应的步骤的反应物
注意:可逆反应中的物质
判断副产品的方法:支线产品,无毒无害
•
1. 中国人只要看到土地,就会想种点 什么。 而牛叉 的是, 这花花 草草庄 稼蔬菜 还就听 中国人 的话, 怎么种 怎么活 。
•
6.石壕吏和老妇人是诗中的主要人物 ,要立 于善于 运用想 像来刻 画他们 各自的 动作、 语言和 神态; 还要补 充一些 事实上 已经发 生却被 诗人隐 去的故 事情节 。
•
7.文学本身就是将自己生命的感动凝 固成文 字,去 唤醒那 沉睡的 情感, 饥渴的 灵魂, 也许已 是跨越 千年, 但那人 间的真 情却亘 古不变 ,故事 仿佛就 在昨日 一般亲 切,光 芒没有 丝毫的 暗淡减 损。
煅烧 改变结构,使一些物质能溶解,并使一些杂质在 高温下氧化、分解,如煅烧高岭土
命题点
二
化学工艺流程题中 物质的分离与提纯
(一) 物质分离、提纯的六 种物理方法
视频
(二) 分离提纯中的各种答题规范
1.判断沉淀剂过量的答题规范 取少量上层清液,置于一洁净的试管中,再滴加少量的沉 淀剂,若没有沉淀生成,则证明沉淀剂已过量。 2.洗涤沉淀时的答题规范 向过滤得到的沉淀上慢慢注入适量蒸馏水至刚好浸没沉 淀,然后静置,让其自然流下,重复以上操作 2~3 次,直至 洗涤干净。为了减少沉淀的溶解,可用冰水或有机溶剂洗涤。
考情 考法
分析
化学工艺流程题是高考的必考题型,题目综合性强,难 度大,通常以化工生产流程图的形式,以陌生元素或陌生化 合物知识为载体,综合考查元素化合物知识、氧化还原反应 方程式的书写、实验基本操作、实验步骤的分析、通过化工 原理的分析判断流程中残渣或废液的成分、反应条件的控制 与选择、产率的计算、Ksp的应用、绿色化学思想的体现等, 可以说是真正的学科内综合题,无所不考。
命题点 七
化学工艺流程题中的 绿色化学和循环使用
目的:提高原料的利用率,绿色化学
判断循环物质的方法: 箭头回头看 后面反应步骤的生成物,同为前面反应的步骤的反应物
注意:可逆反应中的物质
判断副产品的方法:支线产品,无毒无害
•
1. 中国人只要看到土地,就会想种点 什么。 而牛叉 的是, 这花花 草草庄 稼蔬菜 还就听 中国人 的话, 怎么种 怎么活 。
•
6.石壕吏和老妇人是诗中的主要人物 ,要立 于善于 运用想 像来刻 画他们 各自的 动作、 语言和 神态; 还要补 充一些 事实上 已经发 生却被 诗人隐 去的故 事情节 。
•
7.文学本身就是将自己生命的感动凝 固成文 字,去 唤醒那 沉睡的 情感, 饥渴的 灵魂, 也许已 是跨越 千年, 但那人 间的真 情却亘 古不变 ,故事 仿佛就 在昨日 一般亲 切,光 芒没有 丝毫的 暗淡减 损。
煅烧 改变结构,使一些物质能溶解,并使一些杂质在 高温下氧化、分解,如煅烧高岭土
命题点
二
化学工艺流程题中 物质的分离与提纯
(一) 物质分离、提纯的六 种物理方法
视频
(二) 分离提纯中的各种答题规范
1.判断沉淀剂过量的答题规范 取少量上层清液,置于一洁净的试管中,再滴加少量的沉 淀剂,若没有沉淀生成,则证明沉淀剂已过量。 2.洗涤沉淀时的答题规范 向过滤得到的沉淀上慢慢注入适量蒸馏水至刚好浸没沉 淀,然后静置,让其自然流下,重复以上操作 2~3 次,直至 洗涤干净。为了减少沉淀的溶解,可用冰水或有机溶剂洗涤。
化工流程(一)-云南省峨山彝族自治县第一中学高三化学复习课件(共19张PPT)

例1:以锂辉石(含有Li2Al2Si4O12和少量MgO、Fe2O3) 为原料制备Li2TiO3的工艺流程如图:
锂辉石 研磨
硫酸 酸溶 调pH 滤渣1 滤渣2
Na2CO3 反应 滤渣3
TiO2 煅烧
气体
Li2TiO3
滤渣1为 酸溶所得溶液主要阳离子为
• 例2.平板电视显示屏生产过程中产生大量的废玻璃粉 末,其中含有SiO2、Fe2O3、CeO2以及其他少量可溶于 稀酸的物质。二氧化铈(CeO2)是一种重要的稀土氧化物, 某课题组以此粉末为原料回收铈,设计实验流程如下:
MnS矿 MnO2 粉
H2SO
4
溶浸 滤渣1
MnO2 氧化
氨水 调pH 滤渣2
Na2S MnF2
除杂1 除杂2
滤渣3
滤渣4
NH4HCO3
沉锰
MnCO3
H2SO MnS4O4
(1)“滤渣1”含S和 SiO2(或不溶性;硅酸盐) 写出“溶浸”中二氧化锰与硫化锰反应的化学方程式
MnO2 + MnS + 2H2SO4 = 2MnSO4 + S + 2H2O
Ni2+
开始沉淀 8.1 6.3
1.5
3.4
8.9
6.2
6.9
沉淀完全 10.1 8.3
2.8
4.7
10.9 8.2
8.9
(3)“调pH”除铁和铝,溶液的pH范围调节为 4.7 ~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是
NiS、ZnS
(5)“除杂2”的目的是生成MgF2沉淀除去Mg2+,若溶液酸度过 高,Mg2+沉淀不完全,原因是
高考化学二轮复习化学工艺流程研究课件(84张)

(2)氯化过程中Cl2 转化为Ca(ClO3)2的总反应方程式为:6Ca(OH)2+6Cl2===Ca(ClO3)2 +5CaCl2+6H2O 氯化完成后过滤。 ①滤渣的主要成分为__________(填化学式)。 ②滤液中Ca(ClO3)2与CaCl2的物质的量之比n[Ca(ClO3)2] ∶n[CaCl2]________1∶5(填 “>”、“<”或“=”)。
[题型特点] 工艺流程题是江苏高考必考题型,工艺流程题的结构分题头、题干和题尾三部分。题 头一般是简单介绍该工艺生产的原材料和工艺生产的目的(包括副产品);题干主要用 流程图形式将原料到产品的主要生产工艺流程表示出来;题尾主要是根据生产过程中 涉及的化学知识设计成一系列问题,构成一道完整的化学试题。此类试题集综合性、 真实性、开放性于一体,包含必要的操作名称、化工术语或文字说明,考查知识面广、 综合性强、思维容量大。题干的呈现形式多为流程图、表格和图像;设问角度一般为 操作措施、物质成分、化学反应、条件控制的原因和产率计算等,能力考查侧重于获 取信息的能力、分析问题的能力、语言表达能力和计算能力;涉及到的化学知识有基 本理论、元素化合物和实验基础知识。
已知:多数金属硫酸盐的分解温度都高于 600 ℃ 硫去除率=1-焙 焙烧 烧后 前矿 矿粉 粉中 中硫 硫元 元素 素总 总质 质量 量×100% ①不添加 CaO 的矿粉在低于 500 ℃焙烧时,去除的硫元素主要来源于________。 ②700 ℃焙烧时,添加 1%CaO 的矿粉硫去除率比不添加 CaO 的矿粉硫去除率低, 其主要原因是________________________________________________________ ___________________________________________________________________。
2020届高三第一学期化学一轮复习专题课件---化学工艺流程(共88张PPT)

的措施是________________。
(2)步骤Ⅱ合成N2H4·H2O的装置如图1所示。NaClO 碱 性溶液与尿素水溶液在40 ℃以下反应一段时间后,再 迅速升温至110 ℃继续反应。实验中通过滴液漏斗滴 加的溶液是________;使用冷凝管的目的是________ _____。
(3)步骤Ⅳ用步骤Ⅲ得到的副产品Na2CO3制备无水 Na2SO3(水溶液中H2SO3、HSO3 、SO32 随pH的分布如图2 所示,Na2SO3的溶解度曲线如图3所示)。 ①边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液。 实验中确定何时停止通SO2的实验操作为______。
②边搅拌边向NaHSO3溶液中滴加NaOH溶液,测量溶液 pH,pH约为10时,停止滴加NaOH溶液,加热浓缩溶液至有 大量晶体析出,在高于34 ℃条件下趁热过滤
2.硝基苯(
可写成C6H5NO2)是一种剧毒化学品,具
有致畸、致突变和致癌性。处理含有硝基苯废水的方
法有很多,如图是铁、碳微电池法处理含硝基苯废水的
二、获得产品阶段的常见考查点 1.洗涤(冰水、热水):洗去晶体表面的杂质离子,并减 少晶体在洗涤过程中的溶解损耗;乙醇洗涤既可洗去晶 体表面的杂质,又可减少晶体溶解的损耗。 2.蒸发时的气体氛围抑制水解:如从溶液中析出FeCl3、 AlCl3、MgCl2等溶质时,应在HCl的气流中加热,以防其 水解。
样原理可除去NaCl中的少量KNO3。
【答题技法】
Байду номын сангаас1.化工流程题解题方法:
(1)解题策略
解题步骤
首尾呼应、 找出主线
解题策略
①对照原料和产品,确定核心反应和核 心辅料 ②依核心反应,明确流程主线、支线和 除杂任务
(2)步骤Ⅱ合成N2H4·H2O的装置如图1所示。NaClO 碱 性溶液与尿素水溶液在40 ℃以下反应一段时间后,再 迅速升温至110 ℃继续反应。实验中通过滴液漏斗滴 加的溶液是________;使用冷凝管的目的是________ _____。
(3)步骤Ⅳ用步骤Ⅲ得到的副产品Na2CO3制备无水 Na2SO3(水溶液中H2SO3、HSO3 、SO32 随pH的分布如图2 所示,Na2SO3的溶解度曲线如图3所示)。 ①边搅拌边向Na2CO3溶液中通入SO2制备NaHSO3溶液。 实验中确定何时停止通SO2的实验操作为______。
②边搅拌边向NaHSO3溶液中滴加NaOH溶液,测量溶液 pH,pH约为10时,停止滴加NaOH溶液,加热浓缩溶液至有 大量晶体析出,在高于34 ℃条件下趁热过滤
2.硝基苯(
可写成C6H5NO2)是一种剧毒化学品,具
有致畸、致突变和致癌性。处理含有硝基苯废水的方
法有很多,如图是铁、碳微电池法处理含硝基苯废水的
二、获得产品阶段的常见考查点 1.洗涤(冰水、热水):洗去晶体表面的杂质离子,并减 少晶体在洗涤过程中的溶解损耗;乙醇洗涤既可洗去晶 体表面的杂质,又可减少晶体溶解的损耗。 2.蒸发时的气体氛围抑制水解:如从溶液中析出FeCl3、 AlCl3、MgCl2等溶质时,应在HCl的气流中加热,以防其 水解。
样原理可除去NaCl中的少量KNO3。
【答题技法】
Байду номын сангаас1.化工流程题解题方法:
(1)解题策略
解题步骤
首尾呼应、 找出主线
解题策略
①对照原料和产品,确定核心反应和核 心辅料 ②依核心反应,明确流程主线、支线和 除杂任务
2021届高考化学工艺流程专题讲座(共20张PPT)

(3)“调pH”中发生反应的化学方程式为__________________。
【例2】[2018全国III27(2)]KIO3是一种重要的无机化合物,可作 为食盐中的补碘剂。利用“KClO3氧化法”制备KIO3工艺流程 如下图所示:
H2O
I2 KClO3 H2O
原料
酸
化逐
反
Cl2
应
KH(IO3)2、 Cl2、KCl
工艺流程专题讲座
存在问题 (1)
知识 储备 不足
存在问题 (2)
解 题 方 法 缺 乏
存在问题 (3)
计算 能力 有待 提高
学习目标:
(1)能说出工艺流程中的常见操作 (2)能初步掌握工艺流程题的分析方法
环节一:整体感知,构建框架
一、流程题的结构: 1.试题结构:
题干:原料、产品、新信息
流程图:生产(转化和除杂)过程
(3)溶液中的Cd2+可用锌粉除去,还原除杂工序中反应的离子方程式
为 Cd2++Zn===Cd+Zn2+
。
(4)电解硫酸锌溶液制备单质锌时,阴极的电极反应式为 Zn2++2e-===Z;n
沉积锌后的电解液可返回__溶__浸____工序继续使用。
环节三:方法指导,学以致用
【例2】[2018全国III27(2)]KIO3是一种重要的无机化合物,可作
【学生活动2】分组讨论以下问题: (1)原料预处理时常用酸浸,如何加快反应速率? (2)要除去Zn2+中混有的Fe3+,可加入什么物质?应调节 溶液的pH为多少?为什么不能加入NaOH溶液、氨水等? (3)为什么要趁热过滤? (4)为什么要用冰水洗涤晶体? (5)如何除去氯化钠中的少量硝酸钾?
(1)加快反应速率的方法:
高三化学高考备考二轮复习化学工艺流程课件

AgNO3
I2被进一步氧化
2AgI+Fe===2Ag+Fe2++2I- FeCl3、I2
(2) 以 NaIO3 为 原 料 制 备 I2 的 方 法 是 : 先 向 NaIO3 溶 液 中 加 入 计 量 的 NaHSO3,生成碘化物;再向混合溶液中加入NaIO3溶液,反应得到I2。 上 述 制 备 I2 的 总 反 应 的 离 子 方 程 式 为 ________________________________。
3.[2020·全国卷Ⅰ]钒具有广泛用途。黏土钒矿中,钒以+3、+4、 +5价的化合物存在,还包括钾、镁的铝硅酸盐,以及SiO2、Fe3O4。 采用以下工艺流程可由黏土钒矿制备NH4VO3。
该工艺条件下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所
示:
金属离子 Fe3+ Fe2+ Al3+ Mn2+
搅拌、适当升高温度(合理即可) Fe(OH)3、Al(OH)3 强化沉降Fe(OH)3和Al(OH)3
碱性
3.[2021·河北卷]绿色化学在推动社会可持续发展中发挥着重要作用。某 科研团队设计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消 耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了Cr -Fe-Al-Mg的深度利用和Na+内循环。工艺流程如下:
B.红色 C.紫色
D.绿色
(2)以重晶石(BaSO4)为原料,可按如下工艺生产立德粉:
①在回转炉中重晶石被过量焦炭还原为可溶性硫化钡,该过程的化
学方程式为_____________________________。回转炉尾气中含有有毒 气体,生产上可通过水蒸气变换反应将其转化为CO2和一种清洁能源
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正 极 材 料 的 NiOOH 。 写 出 该 反 应 的 离 子 方 程 式 _2_N_i_2_+_+_C_l_O_-_+__4_O_H_-__==_=_2_N_i_O_O_H__↓_+__C_l_-_+_____。 H(26O) 将 分 离 出 硫 酸 镍 晶 体 后 的 母 液 收 集 、 循 环 使 用 , 其 意 义 是 _提__高__镍_回__收__率__。
高中化学工业流程图专题(共9张PPT)

(3)第④步分离采用的方法是 0 ℃,HF的沸点是19.
(3)蒸发结晶:提取溶解度随温度的变化而变化不大的溶质,如NaCl。
________;第⑤步分离尾气中的HF、
(3)第④步分离采用的方法是________;
(1)箭头:箭头进入的是投料(即反应物)、出去的是生成物(包括主产物和副产物)。
HCl采用的方法是________。 工艺流程题就是生产流程用框图的形式表示出来,并根据物质生产流程中的有关化学知识步步设问,该类试题具有以下特点:
(5)蒸馏或分馏:分离沸点不同且互溶的液体混合物。
(6)冷却法:利用气体易液化的特点分离气体,如合成氨工业
采用冷却法分离氨气与氮气、氢气。
典例 ( 年高考安徽卷)LiPF6是锂离子电池中广泛应用的 电解质,某工厂用LiF、PCl5为原料,低温反应制备LiPF6,其 流程如下:
已知:HCl的沸点是-85.0 ℃,HF的沸点是19.5 ℃。
工艺流程题就是生产流程用框图的形式表示出来,并根据物质生产流程中的有关化学知识步步设问,该类试题具有以下特点:
为两种酸,写出PF 水解的化学方程 反应设备不能用玻璃材质的原因是________(用化学方程式表示)。
第⑤步分离尾气中的HF、HCl采用的方法5 是________。
式
:
_________________________。
(1)第①步反应中无水HF的作用是________、________。反应设备
不能用玻璃材质的原因是________(用化学方程式表示)。
(2) 步反应中 该流程需在无水条件下进行,第③ PF 极易水解,其产物 (2)三线:出线和进线均表示物料流向或操作流程,可逆线表示物质循环使用。
典例 ( 年高考安徽卷)LiPF6是锂离子电池中广泛应用的电解质,某工厂用LiF、PCl5为原料,低温反应5制备LiPF6,其流程如下:
高考化学复习讲义课件9 化学工艺流程

(5) “调 pH”中有沉淀生成,生成沉淀反应的化学方程式:N_a_A_l_O_2_+__H__C_l_+__H_2_O_=_=_=_ _N_a_C_l_+__A_l_(_O_H__)3_↓__或__N__a_[A__l(_O_H__)_4]_+__H_C__l=__=_=_N_a_C_l_+__A_l_(_O_H__)3_↓__+__H_2_O_________________。
(3) “中和沉淀”中,钒水解并沉淀为 V2O5·xH2O,随滤液②可除去金属离子 K+、
Mg2+、Na+、___________M__n_2+__________,以及部分的________F_e_3_+_、__A_l_3+________。
(4) “沉 淀转 溶”中 , V2O5·xH2O 转 化为 钒酸 盐溶 解。滤 渣 ③ 的主要 成分是 _________F__e_(O__H_)_3________。
(4) 在 “ 沉 镁 ” 中 生 成 Mg(OH)2·MgCO3 沉 淀 的 离 子 方 程 式 : _____________________________________________________ , 母 液 经 加 热 后 可 返 回 _____溶__浸_____工序循环使用。由碱式碳酸镁制备轻质氧化镁的方法是__高__温__焙__烧____。
时 c(Ni2+)=1.0×10-5mol/L,c(H+)=1.0×10-8.7mol/L,则 c(OH-)=cKHw+=1×10-
5.3mol/L.则 Ni(OH)2 的 Ksp=c(Ni2+)·c2(OH-)=1×10-15.6.如果“转化”后的溶液中 Ni2+
浓度为
1.0
mol/L,为避免镍离子沉淀,Ksp=
VO2 + 被 氧 化 成
2020届高三化学二轮复习——化学工艺流程(共23张PPT)
仗剑高考区
[2015·全国卷Ⅱ·36]苯酚和丙酮都是重要的化工原料,工业上可用异 丙苯氧化法生产苯酚和丙酮,其反应和工艺流程示意图如下:
(3)在分解釜C中加入的Y为少量浓硫酸,其作用
是
,优点是用量少,缺点是
。
(4)反应②为
(填“放热”或“吸热”)反应。反应温度应控
制在50~60℃,温度过高的安全隐患是
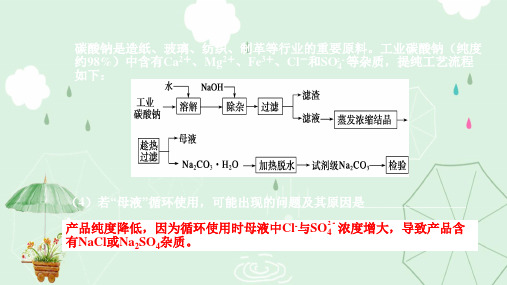
碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(纯度 约98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO24﹣等杂质,提纯工艺流程 如下:
(4)若“母液”循环使用,可能出现的问题及其原因是________________ 。 产品纯度降低,因为循环使用时母液中Cl-与SO42﹣浓度增大,导致产品含 有NaCl或Na2SO4杂质。
1、只要有坚强的意志力,就自然而然地会有能耐、机灵和知识。2、你们应该培养对自己,对自己的力量的信心,百这种信心是靠克服障碍,培养意志和锻炼意志而获得的。 3、坚强的信念能赢得强者的心,并使他们变得更坚强。4、天行健,君子以自强不息。5、有百折不挠的信念的所支持的人的意志,比那些似乎是无敌的物质力量有更强大 的威力。6、永远没有人力可以击退一个坚决强毅的希望。7、意大利有一句谚语:对一个歌手的要求,首先是嗓子、嗓子和嗓子……我现在按照这一公式拙劣地摹仿为:对 一个要成为不负于高尔基所声称的那种“人”的要求,首先是意志、意志和意志。8、执着追求并从中得到最大快乐的人,才是成功者。9、三军可夺帅也,匹夫不可夺志也。 10、发现者,尤其是一个初出茅庐的年轻发现者,需要勇气才能无视他人的冷漠和怀疑,才能坚持自己发现的意志,并把研究继续下去。11、我的本质不是我的意志的结果, 相反,我的意志是我的本质的结果,因为我先有存在,后有意志,存在可以没有意志,但是没有存在就没有意志。12、公共的利益,人类的福利,可以使可憎的工作变为可 贵,只有开明人士才能知道克服困难所需要的热忱。13、立志用功如种树然,方其根芽,犹未有干;及其有干,尚未有枝;枝而后叶,叶而后花。14、意志的出现不是对愿 望的否定,而是把愿望合并和提升到一个更高的意识水平上。15、无论是美女的歌声,还是鬓狗的狂吠,无论是鳄鱼的眼泪,还是恶狼的嚎叫,都不会使我动摇。16、即使 遇到了不幸的灾难,已经开始了的事情决不放弃。17、最可怕的敌人,就是没有坚强的信念。18、既然我已经踏上这条道路,那么,任何东西都不应妨碍我沿着这条路走下 去。19、意志若是屈从,不论程度如何,它都帮助了暴力。20、有了坚定的意志,就等于给双脚添了一对翅膀。21、意志坚强,就会战胜恶运。22、只有刚强的人,才有神 圣的意志,凡是战斗的人,才能取得胜利。23、卓越的人的一大优点是:在不利和艰难的遭遇里百折不挠。24、疼痛的强度,同自然赋于人类的意志和刚度成正比。25、能 够岿然不动,坚持正见,度过难关的人是不多的。26、钢是在烈火和急剧冷却里锻炼出来的,所以才能坚硬和什么也不怕。我们的一代也是这样的在斗争中和可怕的考验中 锻炼出来的,学习了不在生活面前屈服。27、只要持续地努力,不懈地奋斗,就没有征服不了的东西。28、立志不坚,终不济事。29、功崇惟志,业广惟勤。30、一个崇高 的目标,只要不渝地追求,就会居为壮举;在它纯洁的目光里,一切美德必将胜利。31、书不记,熟读可记;义不精,细思可精;惟有志不立,直是无着力处。32、您得相 信,有志者事竟成。古人告诫说:“天国是努力进入的”。只有当勉为其难地一步步向它走去的时候,才必须勉为其难地一步步走下去,才必须勉为其难地去达到它。33、 告诉你使我达到目标的奥秘吧,我唯一的力量就是我的坚持精神。34、成大事不在于力量的大小,而在于能坚持多久。35、一个人所能做的就是做出好榜样,要有勇气在风 言风语的社会中坚定地高举伦理的信念。36、即使在把眼睛盯着大地的时候,那超群的目光仍然保持着凝视太阳的能力。37、你既然期望辉煌伟大的一生,那么就应该从今 天起,以毫不动摇的决心和坚定不移的信念,凭自己的智慧和毅力,去创造你和人类的快乐。38、一个有决心的人,将会找到他的道路。39、在希望与失望的决斗中,如果 你用勇气与坚决的双手紧握着,胜利必属于希望。40、富贵不能淫,贫贱不能移,威武不能屈。41、生活的道路一旦选定,就要勇敢地走到底,决不回头。42、生命里最重 要的事情是要有个远大的目标,并借助才能与坚持来完成它。43、事业常成于坚忍,毁于急躁。我在沙漠中曾亲眼看见,匆忙的旅人落在从容的后边;疾驰的骏马落在后头, 缓步的骆驼继续向前。44、有志者事竟成。45、穷且益坚,不坠青云之志。46、意志目标不在自然中存在,而在生命中蕴藏。47、坚持意志伟大的事业需要始终不渝的精神。 48、思想的形成,首先是意志的形成。49、谁有历经千辛万苦的意志,谁就能达到任何目的。50、不作什么决定的意志不是现实的意志;无性格的人从来不做出决定。我终 生的等待,换不来你刹那的凝眸。最美的不是下雨天,是曾与你躲过雨的屋檐。征服畏惧、建立自信的最快最确实的方法,就是去做你害怕的事,直到你获得成功的经验。 真正的爱,应该超越生命的长度、心灵的宽度、灵魂的深度。生活真象这杯浓酒,不经三番五次的提炼呵,就不会这样可口!人格的完善是本,财富的确立是末能力可以慢 慢锻炼,经验可以慢慢积累,热情不可以没有。不管什么东西,总是觉得,别人的比自己的好!只有经历过地狱般的折磨,才有征服天堂的力量。只有流过血的手指才能弹 出世间的绝唱。对时间的价值没有没有深切认识的人,决不会坚韧勤勉。第一个青春是上帝给的;第二个的青春是靠自己努力的。不要因为寂寞而恋爱,孤独是为了幸福而 等待。每天清晨,当我睁开眼睛,我告诉自己:我今天快乐或是不快乐,并非由我所遭遇的事情造成的,而应该取决于我自己。我可以自己选择事情的发展方向。昨日已逝,
化学工艺流程ppt课件

PPT课件
23
①明确目的:从废钒催化剂中回收 V2O5,即除杂质提纯 V2O5。 ②明确原料:明确废钒催化剂的主要成分和杂质。 ③明确流程:该过程涉及酸浸、氧化、中和、过滤、淋洗、煅烧等,应明确 其含义。 核心反应:硫酸酸浸、KClO3 氧化、高 转化为 VO+ 2 ,反应前后钒元素的化合价不变,发生非氧化 还原反应, VO2+变为 VO+ 2 是氧化还原反应。 ⑤信息理解应用:可逆反应,平衡移动。 ⑥考查细节:前面加入了 KClO3 和 KOH。 ⑦关注细节:NH4VO3“煅烧”生成 V2O5,钒元素的化合价没有发生变化。
(3)TiO2·xH2O 沉淀与双氧水、氨水反应 40 min 所得实验结果如下表所示:
温度/℃
30 35 40 45 50
TiO2·xH2O 转化率/% 92 95 97 93 88
分析40 ℃时TiO2·xH2O转化率最高⑥的原因__________________________。
(4)Li2 Ti5O15 中 Ti 的化合价为+4,其中过氧键的数目为________。
PPT课件
13
(2)“酸浸”后,钛主要以TiOCl24-⑤形式存在,写出相应反应的离子方程式
_________________________________________________________________
________________________________________________________________。
剂,其氧化产物为 CO2,反应的化学方程式为 2FePO4+Li2CO3+H2C2O4===== 2LiFePO4+3CO2↑+H2O。
PPT课件
19
【答案】 (1)100 ℃、2 h,90 ℃、5 h (2)FeTiO3+4H++4Cl-===Fe2++TiOCl24-+2H2O (3)低于 40 ℃,TiO2·xH2O 转化反应速率随温度升高而增加;超过 40 ℃,双 氧水分解与氨气逸出导致 TiO2·xH2O 转化反应速率下降 (4)4 (5)Fe3+恰好沉淀完全时,c(PO34-)=11..30××1100--252 mol·L-1=1.3×10-17 mol·L-1, c3(Mg2+)·c2(PO34-)值为 0.013×(1.3×10-17)2≈1.7×10-40<Ksp[Mg3(PO4)2],因此 不会生成 Mg3(PO4)2 沉淀
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(2)酸溶及后续过程中均需保持盐酸过量,其目的
是
、
。
(3)通氯气氧化后时,发生的主要反应的离子方程式
为
;该过程产生的尾气可用碱溶液吸收,
尾气中污染空气的气体为 (写化学式 )。
一.探究思路
审题—关键
1.此流程的目的是什么? 2.流程中有哪些步骤? 3.流程中涉及哪些化学知识点,如何用化学
语言把你们获取的信息转化为答案呢?
因?①pH的控制 ②蒸发、反应时的气体氛围。
③改变温度 ④趁热过滤 ⑤冰水洗涤 ⑥有机物洗涤:
问题3.化工生产中的主要操作有哪些?
过滤、结晶、重结晶、洗涤、干燥、灼烧、分液
问题4.绿色化学生产有哪些理念?
①环境污染问题②原子的经济性③节约能源(包 括使用催化剂) ④原料应是可再生的(或者可循环使 用) ⑤工艺的安全性
3.大胆回答:考虑产物、环保、产量、成本等。
二.探究主线
交流讨论: 通过以上两个流程题你 能总结出工业生产流程题流程的主 线吗?
二.探究主线 (体现命题设问角度)
思考:试题通常会从哪些方面来设问?
三.探究设问点
问题1.原料预处理有哪些方法?
溶解,灼烧,煅烧,粉碎等
问题2.控制反应条件有哪些?有什么作用或原
你要思考 做什么?
用 制备
副产物
原料 产品
你要思考 做什么? 怎么做?
操作及步骤
你要思考
做什么? 怎么做? 为什么?
(2)酸溶及后续过程中均需保持盐酸过量, 其目的是 、 。
你要思考
做什么? 怎么做? 为什么?
(3)通氯气氧化后时,发生的主要反应的离子
方程式为 Cl2+2 Fe2+=2Cl-+2Fe3+;该过程
产生的尾气可用碱溶液吸收,尾气中污染空气的
气体为 HCl Cl2(写化学式 )。
一.探究思路
交流讨论:解答此类题目的基本思 路是什么?
一.解题思路
1.整体粗读 2.局部细读:
统览整体,截段分析
原料到产品:须除去什么元素,引进什么元素? 步骤与目的:加入试剂什么目的? 感觉与结果:有的步骤读不懂就看这一步结果 信息与迁移:所给信息一定有用,一定用
四.总结答题模式
结晶
蒸发浓缩、冷却结晶 蒸发结晶、趁热过滤
重结晶
有备而来 决胜高考
【流程概要】
【方法总结】
★解决无机化工题的关键为四个步骤:
流程懂目的
粗读
问题解意图
精读
【解题理念】
知信识 息解 有问用题 物尽其用
考虑环保 考虑成本 表达写答案
迁移
循环利用 考虑现规实范
高考专题复习
化学工艺流程题型研究
化学工艺流程顾名思义,就是将
化工生产中的主要生产阶段即生产 流程用框图的形式表现出来,并根 据生产流程中有关的化学知识步步 设问,形成与化工生产紧密联系的 化工工艺试题。
例题1以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶 体(FeCl3·6H2O)的工艺流程如下:
四.总结答题模式
有备而来 决胜高考
1.对原料预处理的方法和作用
研磨:增大固体与液体或气体间接触面积,
加快反应速率. 水浸:与水接触反属离子进入 溶液,不溶物通过过滤除去.
搅拌:加快反应(溶解)速率,使反应充分进行,
提高原料利用率. 灼烧:除去可燃性杂质或使原料初步转化.
四.总结答题模式
有备而来 决胜高考
2.常用的分离操作
过滤、萃取和分液、结晶、蒸馏和分馏等
趁热过滤:联系物质的溶解性考虑 检验沉淀是否完全的方法:静置向上层清液中继续
滴加原试剂,如出现… 沉淀洗涤: 乙醇洗涤:冰水、热水、乙醇(溶解性)
一是降低因溶质的溶解而引起的损耗 二是乙醇易挥发,利于干燥同时可防 止溶质与水反应 洗涤沉淀的方法: 检验沉淀是否洗净方法:
