亚硫酸钠与亚硫酸氢钠在不同的PH值的分配系数
基于aspen模拟的亚硫酸钠法烟气脱硫工艺研究

基于aspen 模拟的亚硫酸钠法烟气脱硫工艺研究侯向俊王剑锋郭佳(神华榆林能源化工有限公司,陕西榆林,719302)摘要:亚硫酸钠法烟气脱硫工艺是一种完全回收型的SO 2脱除工艺。
基于aspen 流程模拟软件,对工艺过程进行了基础研究和讨论。
吸收过程适宜的pH 值为6.0;空塔喷淋满足烟气降温和除尘要求;导向浮阀板式塔作为吸收塔,满足50mg/m 3的烟气脱硫精度要求;采用强制循环蒸发结晶过程,防止换热管的结晶;再生得到SO 2与蒸汽的混合气体通过真空汽提,可以得到89.3%浓度的SO 2原料气。
关键词:烟气脱硫亚硫酸钠法SO 2回收中图分类号:X701.3文献标识码:B 文章编号:2096-7691(2021)01-068-06作者简介:侯向俊(1982-)男,工程师,2006年毕业于中国石油大学(华东),现任神华榆林能源化工有限公司技术质量部工艺主管。
Tel:181****6067,E-mail:**********************.cn1研究背景我国是一个燃煤大国,煤炭燃烧产生的SO 2是大气污染的重要源头。
随着工业经济的迅速发展,大气中SO 2的排放量急剧增加,而烟气脱硫是控制SO 2排放的有效工艺技术手段,同时国家也在不断的提升大气污染物排放标准。
烟气脱硫技术,是指利用各种吸收剂或吸附剂,捕集烟气中的SO 2,并将其转化为较为稳定且易于机械分离的硫化合物或单质硫,从而达到脱硫的目的[1]。
煤炭和石油燃烧排放的烟气通常含有较低浓度的SO 2,由于燃料硫含量的不同,燃烧设施直接排放的烟气中SO 2浓度范围大约为10-4~10-3数量级[2]。
特点是SO 2的浓度低,烟气流量大,因此烟气脱硫设施的建设和运行费用通常十分昂贵。
烟气脱硫的方法按应用脱硫剂形态的不同分为湿法、干法和半干法,目前应用最多的是湿法脱硫。
按脱硫产物是否回收可以分为回收法和抛弃法。
抛弃法是将脱硫生成物当作固体废物抛弃掉,其处理方法简单、处理成本低,但不可避免地会出现二次污染问题,还会浪费大量土地来堆放固体废物。
亚硫酸盐在食品中的应用与标准规范

亚硫酸盐在食品中的应用与标准规范亚硫酸盐是食品工业广泛使用的漂白剂、防腐剂和抗氧化剂,通常是指二氧化硫及能够产生二氧化硫的无机性亚硫酸盐的统称,包括二氧化硫(SO2)、硫磺、亚硫酸(H2SO3)、亚硫酸盐(如Na2SO3)、亚硫酸氢盐(如NaHSO3)、焦亚硫酸盐(如Na2S2O5)、低亚硫酸盐(如Na2S2O4)[1-2],限制使用量通常为0-0.7mg/kg(以SO2计)。
在食品中,亚硫酸盐可以游离态、可逆结合态和不可逆结合态3种形态存在[3]。
常见的亚硫酸盐,无色、单斜晶体或粉末。
对眼睛、皮肤、粘膜有刺激作用,可污染水源。
受高热分解产生有毒的硫化物烟气。
碱金属的亚硫酸盐易溶于水,由于水解,溶液显碱性,其他金属的正盐均微溶于水,而所有的酸式亚硫酸盐都易溶于水。
亚硫酸盐受热容易分解。
亚硫酸钠是亚硫酸盐存在的最常见的形式,是优良的还原剂,用来清除氧。
1 亚硫酸盐的毒理作用2017年10月27日,世界卫生组织国际癌症研究机构公布的致癌物清单初步整理参考,亚硫酸盐在3类致癌物(对人类致癌性尚未归类)清单中。
目前对于二氧化硫的毒理学机制尚不完全清楚,但是SO2通过产生各种自由基引起组织氧化损伤被认为是其中的一种主要机制。
当机体摄入SO2以后,与体液形成亚硫酸盐和亚硫酸氢盐,亚硫酸盐极易通过电子氧化作用形成三氧化硫阴离子自由基(SO32-),而亚硫酸氢盐则可与氧迅速反应生成过氧自由基(O2·),其中未被灭活的自由基可攻击生物膜上的多不饱和脂肪酸,从而进一步激发自由基连锁反应,产生的有机过氧化物可攻击DNA、RNA及酶蛋白,引起基因突变和酶活性丧失,细胞代谢紊乱[4]。
同时,SO2还能降低抗氧化物酶(超氧化物歧化酶、过氧化氢酶等)的活性,减少非酶抗氧化物谷胱甘肽(GSH)水平,从而加剧过氧化自由基对组织的损伤[5]。
实验表明,亚硫酸盐可引起大鼠海马神经元、背根神经元钾、钠离子通道的变化,造成神经系统损伤。
13-亚硫酸氢钠化学品安全技术说明书(MSDS)

13-亚硫酸氢钠化学品安全技术说明书(MSDS)亚硫酸氢钠化学品安全技术说明书(MSDS)第一部分:化学品名称1.1 化学品中文名称:亚硫酸氢钠1.2 化学品英文名称: sodium bisulfite1.3中文名称2:酸式亚硫酸钠1.4 分子式:HNaO3S1.5 分子量:104.06第二部分:成分/组成信息2.1 主要成分:亚硫酸氢钠2.2 含量:纯品2.3 CAS No. 7631-90-5第三部分:危险性概述3.1 危险性类别:第8.1类酸性腐蚀品。
3.2 侵入途径:吸入、食入。
3.3健康危害:对皮肤、眼、呼吸道有刺激性,可引起过敏反应。
可引起角膜损害,导致失明。
可引起哮喘;大量口服引起恶心、腹痛、腹泻、循环衰竭、中枢神经抑制。
第四部分:急救措施4.1 皮肤接触:立即脱去污染的衣着,用大量流动清水冲洗。
如有不适感,就医。
4.2眼睛接触:立即提起眼睑,用大量流动清水或生理盐水彻底冲洗10~15分钟。
如有不适感,就医。
4.3吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
呼吸、心跳停止,立即进行心肺复苏术。
就医。
4.4 食入:用水漱口,给饮牛奶或蛋清。
就医。
第五部分:消防措施5.1危险特性:具有强还原性。
接触酸或酸气能产生有毒气体。
受高热分解放出有毒的气体。
具有腐蚀性。
5.2 有害燃烧产物:无意义。
5.3 灭火方法:本品不燃。
根据着火原因选择适当灭火剂灭火。
第六部分:泄漏应急处理6.1应急处理:隔离泄漏污染区,限制出入。
建议应急处理人员戴防尘口罩,穿防酸碱服。
穿上适当的防护服前严禁接触破裂的容器和泄漏物。
尽可能切断泄漏源。
用塑料布覆盖泄漏物,减少飞散。
勿使水进入包装容器内。
用洁净的铲子收集泄漏物,置于干净、干燥、盖子较松的容器中,将容器移离泄漏区。
第七部分:操作处置与储存7.1操作注意事项:密闭操作,局部排风。
防止粉尘释放到车间空气中。
操作人员必须经过专门培训,严格遵守操作规程。
等渗调节剂
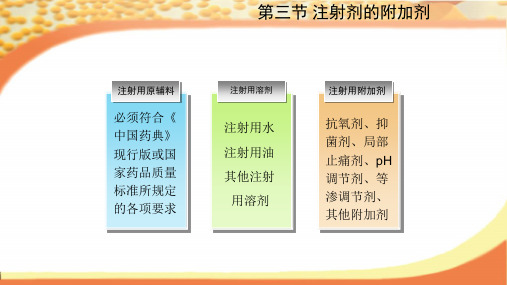
助悬剂
延效剂 止痛剂
1~ 2 0.3~0.5 1 0.5~1
【氯化钠等渗当量法】
与1g药物呈等渗效应的氯化钠量称为氯化钠等渗当量, 用E表示,计算公式为:
X=0.009v-EW总 X=0.009v-CVE
X:配成体积为v(ml)的等渗溶液需要加入氯化钠的量 V:欲配制溶液的体积 W:药物的重量 E:药物的氯化钠等渗当量
• 某注射液200ml,含硫酸阿托品为1.0%,盐酸吗啡为2.0%, 问需要氯化钠多少?才能使之成为等渗溶液? • X=0.009v-EW总 • X=0.009*200-(0.1*1%*200+0.15*2%*200)=1.0g
区别
• 高张液:无论是电解质或非电解质溶液,输入人体后,其药物微粒 不能进入或很少进入红细胞内,引起红细胞内渗透压相对降低,水 分随之外流,使细胞发生皱缩。 • 低张液:药物微粒过多进入红细胞内,使细胞内渗透压随之增高, 部分水分被吸入红细胞内,使之肿胀。 • 等张掖:当某种输入的溶液不引起红细胞形态和体积变化时。
注射剂的附加剂
【等渗调节剂】
注射剂常用的等渗调节剂 常用的等渗调节剂有氯化钠、葡萄糖等 渗透压调整方法和计算 :冰点降低数据法 氯化钠等渗当量法
注射剂的附加剂
【冰点数据降低法】冰点相同的稀溶液 都具有相等的渗透压血浆和泪 液的冰点均为-0.52
低渗溶液调整为等渗溶液,需加入等渗调节剂的量:
X 0.52 a b
第三节 注射剂的附加剂
注射用原辅料
注射用溶剂
注射用附加剂
必须符合《 中国药典》 现行版或国 家药品质量 标准所规定 的各项要求
注射用水
注射用油
其他注射
用溶剂
抗氧剂、抑 菌剂、局部 止痛剂、pH 调节剂、等 渗调节剂、 其他附加剂
铬的污水处理

•六价铬离子浓度的排放标准:0.5 毫克/ 升•酸液的排放标准:P H 值在6-9 之间•六价铬离子处理方案六价铬对人体有毒,含铬废水要经化学处理后才能排放,方法是用绿矾把废水中的六价铬还原为三价铬离子,再加入过量的石灰水,使铬离子转变为氢氧化铬沉淀。
其主要反应的化学方程式如下:现用上法处理含铬(+6 价)的废水(Cr 原子量52 ),试回答:(1 )处理后,沉淀物中除外,还有_______ ,________ (用化学式表示)。
(2 )需用绿矾多少千克?解答:(1 ),(2 )废水中含铬的物质的量需要绿矾的质量为即12.51kg 。
[ 解析] 与发生氧化还原反应生成及。
再加入后、均转化为、。
又与大量的形成沉淀。
4 、处理方案用石灰水来处理:+ = 沉淀•PH 值的处理方案用石灰水来处理直到PH 值在6-9 之间即可。
调整PH值到8左右,絮凝同时加NAOH沉淀,我现在在做一个6价铬的工程,就是这方法,出水能达1级排放钡盐就可以直接沉淀六价铬啊含六价铬的废液处理注意事项1).要戴防护眼镜、橡皮手套,在通风橱内进行操作。
2).把Cr(Ⅵ)还原成Cr(Ⅲ)后,也可以将其与其它的重金属废液一起处理。
3).铬酸混合液系强酸性物质,故要把它稀释到约1%的浓度之后才进行还原。
并且,待全部溶液被还原变成绿色时,查明确实不含六价铬后,才按操作步骤中从第四点开始进行处理。
处理方法[还原、中和法(亚硫酸氢钠法)][原理]Cr(Ⅵ)不管在酸性还是碱性条件下,总以稳定的铬酸根离子状态存在。
因此,可按照下式将Cr(Ⅵ)还原成Cr(Ⅲ)后进行中和,使之生成难溶性的Cr(OH)3沉淀而除去。
4H2CrO4+6NaHSO3+3H2SO4→2Cr2(SO4)3+3Na2SO4+10H2O (1)Cr2(SO4)3+6NaOH→2Cr(OH)3↓+3Na2SO4 (2)(1)式还原反应,若pH值在3以下,反应在短时间内即进行结束。
如果使(2)式中和反应pH在7.5~8.5范围内进行,则Cr(Ⅲ)即以Cr(OH)3形式沉淀析出.[操作步骤]1).于废液中加入H2SO4,充分搅拌,调整溶液pH在3以下(采用pH试纸或pH计测定。
亚硫酸氢钠 中国药典2010版

亚硫酸氢钠中国药典2010版亚硫酸氢钠中国药典2010版YaliusuanqingnaSodium BisulfiteNaHSO104.063[7631-90-5]本品为亚硫酸氢钠与焦亚硫酸钠的混合物。
按二氧化硫( SO)计算,应为58.5%~267.4%。
【性状】本品为白色颗粒或结晶性粉末;有二氧化硫的微臭。
本品在水中易溶,在乙醇或乙醚中几乎不溶。
【鉴别】 (1)本品的水溶液(1→20)呈酸性,显亚硫酸氢盐的鉴别反应(附录Ⅲ)。
(2)本品的水溶液显钠盐的鉴别反应(附录Ⅲ)。
【检查】溶液的澄清度与颜色取本品1.0g,加水10ml使溶解,溶液应澄清无色。
硫代硫酸盐取本品1.0g,加水15ml溶解后,加稀盐酸5ml,摇匀,静置5分钟,不得产生浑浊。
铁盐取本品1.0g,加盐酸2ml,置水浴上蒸干,加水适量溶解,依法检查(附录Ⅷ G),与标准铁溶液2.0ml制成的对照液比较,不得更深(0.002%)。
重金属取本品1.0g,依法检查(附录Ⅷ H第一法),含重金属不得过百万分之二十。
砷盐取本品0.5g,加水10ml溶解后,加硫酸1ml,置砂浴上蒸至白烟冒出,放冷,加水21ml与盐酸5ml,依法检查(附录Ⅷ J第二法),应符合规定(0.0004%)。
【含量测定】取本品约0.15g,精密称定,精密加碘滴定液(0.05mol/L)50ml,密塞,振摇使溶解,在暗处放置5分钟,用硫代硫酸钠滴定液(0.1mol//L)滴定,至近终点时,加淀粉指示液1ml,继续滴定至蓝色消失,并将滴定的结果用空白试。
验校正。
每1ml碘滴定液(0.05mol/L)相当于3.203mg的SO2【类别】药用辅料,抗氧剂。
【贮藏】遮光,密封保存。
思考题答案
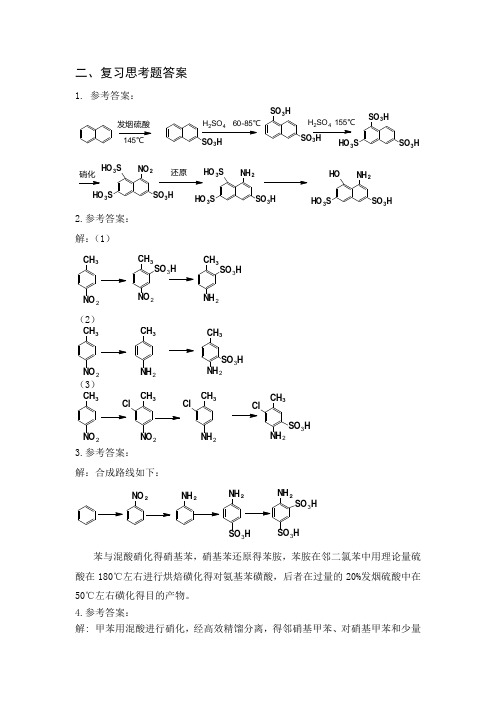
二、复习思考题答案1. 参考答案:SO3HHO3S SO3HSO3HSO3发烟硫酸145℃H SO155℃HO3SHO3S SO3HNO2硝化还原HO3SHO3S SO3HNH2HOHO3S SO3HNH22.参考答案:解:(1)CH32CH32SO3HCH3NO2SO3H(2)CH32CH32SO3HCH32(3)CH32CH32SO3HClCH32ClCH32Cl3.参考答案:解:合成路线如下:NH2SO3HNH2SO3HSO3H苯与混酸硝化得硝基苯,硝基苯还原得苯胺,苯胺在邻二氯苯中用理论量硫酸在180℃左右进行烘焙磺化得对氨基苯磺酸,后者在过量的20%发烟硫酸中在50℃左右磺化得目的产物。
4.参考答案:解: 甲苯用混酸进行硝化,经高效精馏分离,得邻硝基甲苯、对硝基甲苯和少量间硝基甲苯,将它们分别用氢气或二硫化钠将硝基还原成氨基,得邻甲苯胺,对甲苯胺和少量间甲苯胺。
(1)合成路线:CH 3NH 2CH 3NH 22将邻甲基苯胺在低温溶解于浓硫酸中,形成酸性硫酸盐,然后加入理论量的混酸、发烟硝酸或硝酸钠进行一硝化,然后放入水中稀释析出,得到目的产物。
(2)合成路线:CH 3NH 2CH 3NHCOCH 3CH 3NHCOCH 3O 2NCH 3NH 2O 2N间甲基苯胺用乙酐进行N-乙酰基化,得3-乙酰氨基甲苯,后者在浓硫酸中用理论量的发烟硝酸进行一硝化,得3-乙酰氨基-6-硝基甲苯,最后在氢氧化钠水溶液中或稀硫酸中加热,水解脱去乙酰基,得目的产物。
(3)合成路线:CH 32CH 32NO 2CH 3NO 2NHCOCH 3CH 33对甲苯胺在乙酸中用乙酸进行N- 乙酰化,生成4-乙酰氨基甲苯,接着加入理论量的混酸进行一硝化,得4-乙酰氧基-3-硝基甲苯,最后在氢氧化钠水溶液中或稀盐酸中加热,水解脱乙酰基,得到目的产物。
经过工艺改进,乙酰化法已经代替传统的对甲苯磺酰氯酰化法。
5.参考答案:解:合成路线如下ClNO2ClCl2Cl NH 2苯在铁催化剂的存在下,用理论量30%左右的氯气进行沸腾连续一氯化,精馏分离得氯苯。
工业碱渣生产亚硫酸钠的工艺研究与应用

工业碱渣生产亚硫酸钠的工艺研究与应用祥燕律(中盐株洲化工集团株洲 412004)摘要:本文通过对水合肼副产碱渣成份与亚硫酸钠性质的分析,以与碱液对二氧化硫吸收原理的研究,提出了一条利用水合肼副产十水碳酸钠制亚硫酸钠的生产方法,并将研究结果成功应用在工业生产上,具有投资少、成本低、操作方便等优点,为水合肼副碱渣提供了一条可靠的处理途径。
关键词:碱渣硫酸尾气亚硫酸钠尾气吸收The study and application of the technology about producting sodium sulfite by using by-product alkal of hydrazine hydrate to absorb the residue of sulfuric acid tail gasPeng Xiangyan ,Li Lv(Hunan Zhuzhou Chemical Industry Group Co.,Ltd.-CNSIC, Hunan Zhuzhou 412004,China) Abstract:Through studing the composition of the hydrazine hydrate’s alkaline residue and the properties of sodium sulfite , as well as absorption principle of the lye absorbing the sulfur dioxide exhaust gas , Put forward a production process of using hydrazine hydrate by-productNa2CO3·10H2O to product sodium sulfite, and the research results has been successfully applied in industrial production,the production process is less investment, low cost, easy to operate and so on, and provides a reliable way to deal with the hydrazine hydrate’s alkaline residueKey words: alkaline residue; sulfuric acid tail gas;sodium sulfite; absorptionof exhaust gas;背景目前国硫酸厂的SO2尾气大多采用氨液吸收后生成中间产品亚硫酸氢铵(NH4HSO3),然后通过加NH3通SO3制得固体硫铵外卖,SO2液化。
亚硫酸氢钠各元素化合价

亚硫酸氢钠各元素化合价亚硫酸氢钠(化学式NaHSO3)是一种常见的无机化合物,由钠离子(Na+)、亚硫酸根离子(HSO3-)和氢离子(H+)组成。
它在工业和实验室中广泛应用,具有多种有用的性质和特点。
本文将深入探讨亚硫酸氢钠中各元素的化合价以及与化学反应中的作用。
1. 亚硫酸氢钠的组成和结构亚硫酸氢钠是一种白色结晶性固体,常见形式是无水物(NaHSO3)和一水合物(NaHSO3·H2O)。
无水物是由一钠离子、一亚硫酸根离子和一个氢离子组成的晶体结构。
一水合物在其中添加了一个水分子,使其结构稍有不同。
亚硫酸氢钠在水中溶解时,会迅速离解为钠离子、亚硫酸根离子和氢离子。
2. 钠的化合价钠是一种碱金属元素,其化合价通常为+1。
在亚硫酸氢钠中,钠的化合价也是+1,它失去了一个电子,形成正离子。
这种离子在化学反应中起到平衡电荷的作用,并参与与其他离子或分子的相互作用。
3. 亚硫酸根离子的化合价亚硫酸根离子(HSO3-)是由亚硫酸(H2SO3)失去一个质子形成的。
亚硫酸是一种弱酸,所以亚硫酸根离子的化合价为-1。
它对整个化合物的性质和反应起着重要的作用。
亚硫酸根离子与其他离子或分子发生反应时,通常贡献一个氧原子给反应物。
4. 氢离子的化合价氢离子(H+)是亚硫酸氢钠中的另一个组成部分。
作为一价阳离子,其化合价为+1。
氢离子的主要作用是参与酸碱反应和中和反应,使反应物达到电中性。
5. 亚硫酸氢钠的化学反应亚硫酸氢钠作为一种有用的化合物,参与了多种化学反应。
以下是几个常见的反应示例:5.1 与强酸的反应:亚硫酸氢钠能够与强酸反应生成相应的盐和二氧化硫。
与盐酸反应可生成氯化钠和二氧化硫:NaHSO3 + HCl → NaCl + SO2 + H2O5.2 与还原剂的反应:亚硫酸氢钠可以作为还原剂与某些物质发生反应。
它与亚硫酸盐(如亚硫酸钠)反应生成硫酸:NaHSO3 + Na2SO3 → Na2SO4 + H2O + SO25.3 与氧化剂的反应:亚硫酸氢钠也可以被氧化剂氧化,生成相应的氧化产物。
亚硫酸氢钠危险化学品安全技术说明书

亚硫酸氢钠危险化学品安全技术说明书第一部分化学品名称化学品中文名称:亚硫酸氢钠化学品英文名称:sodium bisulfite中文名称2:酸式亚硫酸钠英文名称2:hydrogen sulfite sodium技术说明书编码:2909CAS No.:7631-90-5第二部分成分/组成信息第三部分危险性概述危险性类别:侵入途径:健康危害:对皮肤、眼、呼吸道有刺激性,可引起过敏反应。
可引起角膜损害,导致失明。
可引起哮喘;大量口服引起恶心、腹痛、腹泻、循环衰竭、中枢神经抑制。
环境危害:对环境有危害,对水体可造成污染。
燃爆危险:本品不燃,具腐蚀性,可致人体灼伤。
第四部分急救措施皮肤接触:立即脱去污染的衣着,用大量流动清水冲洗。
就医。
眼睛接触:立即提起眼睑,用大量流动清水或生理盐水彻底冲洗至少15分钟。
就医。
吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
如呼吸停止,立即进行人工呼吸。
就医。
食入:饮足量温水,催吐。
就医。
第五部分消防措施危险特性:具有强还原性。
接触酸或酸气能产生有毒气体。
受高热分解放出有毒的气体。
具有腐蚀性。
有害燃烧产物:氧化硫、氧化钠。
灭火方法:消防人员必须穿全身耐酸碱消防服。
灭火时尽可能将容器从火场移至空旷处。
然后根据着火原因选择适当灭火剂灭火。
第六部分泄漏应急处理应急处理:隔离泄漏污染区,限制出入。
建议应急处理人员戴防尘口罩,穿防酸服。
不要直接接触泄漏物。
小量泄漏:避免扬尘,小心扫起,收集于干燥、洁净、有盖的容器中。
大量泄漏:收集回收或运至废物处理场所处置。
第七部分操作处置与储存操作注意事项:密闭操作,局部排风。
防止粉尘释放到车间空气中。
操作人员必须经过专门培训,严格遵守操作规程。
建议操作人员佩戴自吸过滤式防尘口罩,戴化学安全防护眼镜,穿橡胶耐酸碱服,戴橡胶耐酸碱手套。
避免产生粉尘。
避免与氧化剂、酸类、碱类接触。
配备泄漏应急处理设备。
倒空的容器可能残留有害物。
储存注意事项:储存于阴凉、通风的库房。
亚硫酸氢钠

化学品安全技术说明书化学品中文名:亚硫酸氢钠; 酸式亚硫酸钠;重亚硫酸钠化学品英文名:sodium bisulfite; hydrogen sulfite sodium企业名称:生产企业地址:邮编: 传真:企业应急电话:电子邮件地址:技术说明书编码:√纯品混合物有害物成分浓度CAS No.亚硫酸氢钠7631-90-5危险性类别:第8.1类酸性腐蚀品侵入途径:吸入、食入健康危害:对皮肤、眼、呼吸道有刺激性,可引起过敏反应。
可引起角膜损害,导致失明。
可引起哮喘;大量口服引起恶心、腹痛、腹泻、循环衰竭、中枢神经抑制。
环境危害:对环境有害。
燃爆危险:不燃,无特殊燃爆特性。
皮肤接触:立即脱去污染的衣着,用大量流动清水冲洗。
如有不适感,就医。
眼睛接触:立即提起眼睑,用大量流动清水或生理盐水彻底冲洗10~15分钟。
如有不适感,就医。
吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
呼吸、心跳停止,立即进行心肺复苏术。
就医。
食入:用水漱口,给饮牛奶或蛋清。
就医。
危险特性:具有强还原性。
接触酸或酸气能产生有毒气体。
受高热分解放出有毒的气体。
具有腐蚀性。
有害燃烧产物:无意义。
灭火方法:本品不燃。
根据着火原因选择适当灭火剂灭火。
灭火注意事项及措施:消防人员必须穿全身耐酸碱消防服、佩戴空气呼吸器灭火。
尽可能将容器从火场移至空旷处。
喷水保持火场容器冷却,直至灭火结束。
应急行动:隔离泄漏污染区,限制出入。
建议应急处理人员戴防尘口罩,穿防酸碱服。
穿上适当的防护服前严禁接触破裂的容器和泄漏物。
尽可能切断泄漏源。
用塑料布覆盖泄漏物,减少飞散。
勿使水进入包装容器内。
用洁净的铲子收集泄漏物,置于干净、干燥、盖子较松的容器中,将容器移离泄漏区。
操作注意事项:密闭操作,局部排风。
防止粉尘释放到车间空气中。
操作人员必须经过专门培训,严格遵守操作规程。
建议操作人员佩戴自吸过滤式防尘口罩,戴化学安全防护眼镜,穿橡胶耐酸碱服,戴橡胶耐酸碱手套。
亚硫酸氢钠

亚硫酸氢钠(1)化学品及企业标识化学品中文名: 亚硫酸氢钠;酸式亚硫酸钠化学品英文名:sodium bisulfite ;hydrogen sulfite sodium分子式:NaHSO3相对分子量:104.06(2)成分/组成信息成分:纯品CAS No:7631-90-5(3)危险性概述危险性类别:第8.1 类酸性腐蚀品侵入途径:吸入、食入、经皮吸收健康危害:对皮肤、眼、呼吸道有刺激性,可引起过敏反应。
可引起角膜损害,导致失明。
可引起哮喘;大量口服引起恶心、腹痛、腹泻、循环衰竭、中枢神经抑制。
环境危害: 对环境有危害,对水体可造成污染。
燃爆危险: 本品不燃,具腐蚀性,可致人体灼伤。
(4)急救措施皮肤接触:脱去污染的衣着,用肥皂水和清水彻底冲洗皮肤。
如有不适感,就医眼睛接触: 提起眼睑,用流动清水或生理盐水冲洗。
如有不适感,就医吸入: 迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
如呼吸、心跳停止,立即进行人工呼吸。
就医。
食入:饮足量温水,催吐。
就医。
(5)消防措施危险特性:具有强还原性。
接触酸或酸气能产生有毒气体。
受高热分解放出有毒的气体。
具有腐蚀性。
有害燃烧产物: 氧化硫、氧化钠。
灭火方法:根据着火原因选择适当灭火剂灭火。
灭火注意事项及措施:消防人员必须穿全身耐酸碱消防服。
灭火时尽可能将容器从火场移至空旷处。
(6)泄漏应急处理应急行动:隔离泄漏污染区,限制出入。
建议应急处理人员戴防尘口罩,穿防酸服。
不要直接接触泄漏物。
小量泄漏:避免扬尘,小心扫起,收集于干燥、洁净、有盖的容器中。
大量泄漏:收集回收或运至废物处理场所处置。
(7)操作处置与储存操作注意事项:密闭操作,局部排风。
防止粉尘释放到车间空气中。
操作人员必须经过专门培训,严格遵守操作规程。
建议操作人员佩戴自吸过滤式防尘口罩,戴化学安全防护眼镜,穿橡胶耐酸碱服,戴橡胶耐酸碱手套。
避免产生粉尘。
避免与氧化剂、酸类、碱类接触。
配备泄漏应急处理设备。
实验五减水剂的制备与水泥净浆流动度测定

实验五减水剂的制备与水泥净浆流动度测定一、实验目的1.熟悉自由基聚合反应的特点;2.了解混凝土减水剂的特点,掌握制备方法;3.了解水泥净浆流动度的测定方法;二、实验原理三聚氰胺系减水剂是一种水溶性阴离子型高聚合物,它对水泥具有极强的吸附和分散作用,可增强砂浆与基层的黏附力,在混凝土拌合物中使用时具有与各种水泥的适应性好、与其它外加剂相容性好、不缓凝、早强效果突出等优点,是现有混凝土减水剂中综合指标较好的减水剂之一;由于三聚氰胺系减水剂产品还存在减水率低、保坍性不佳、生产成本较高等缺点使其应用受到限制;目前,市场上销售的三聚氰胺系减水剂产品主要是采用焦亚硫酸钠、氨基磺酸或对氨基苯磺酸对三聚氰胺甲醛树脂进行磺化反应制得,这些磺化剂价格较高;本试验以价格相对便宜的亚硫酸氢钠为磺化剂,以期制备出具有更高减水率、较好保坍性能及较低生产成本的三聚氰胺系减水剂;其合成原理与采用的原料单体有关;如由应用化学08级顾照照等同学开发成功并推向市场的三聚氰胺系减水剂产品之一的合成原理如下:1羟甲基化反应:在三聚氰胺的分子上有三个氨基—NH2,在酸催化下,羟甲基化后可生成3~6个不等的活性羟基,其产物特性与反应体系的pH、温度、反应物的比例以及反应时间直接相关;在酸性介质中极易生成不溶、不熔、质硬而脆的体型聚合物,一经形成便由水性体系中析出,发生不可逆沉降;而在中性或碱性介质中反应生成羟甲基三聚氰胺;因此,本文为了使反应容易控制,在这个阶段反应要在弱碱性中进行pH值约为8~9,温度控制在60℃~80℃,反应时间为90min,F:M=~:1三聚氰胺与甲醛在中性或弱碱性介质中发生加成反应,根据三聚氰胺与甲醛摩尔比的不同,可以分别得到三羟甲基三聚氰胺、四羟甲基三聚氰胺、五羟甲基三聚氰胺和六羟甲基三聚氰胺,反应方程式为:该反应为亲核加成反应,三聚氰胺在碱性条件下变为负电性,而甲醛碳原子带有偏正电荷,这里亲核的正电性碳原子进攻亲电的负电性氮原子,亲核反应机理如下:2磺化反应:磺化反应是磺酸基—SO3H对羟基—OH的亲核取代反应,先使其中的一个羟基被屏蔽,再进行缩合,同时磺酸基的引入大大改善了缩聚物的亲水性;影响磺化反应的重要因素是磺化剂的种类和用量;Aignesberger研究表明,焦亚硫酸钠、氨基磺酸、亚硫酸氢纳、氨基磺酸等都可以作磺化剂,但以焦亚硫酸钠最好;曾繁森对磺化剂的选择也做过研究,认为在相同时间内,焦亚硫酸钠比亚硫酸氢钠可以获得更高的磺化率,但当反应时间大于60分钟时,两者的磺化率几乎相同;本文采用亚硫酸氢钠作为磺化剂,反应在碱性介质中进行pH值在11~12,温度80℃~90℃,反应3h;S:M=~:反应方程式如下:3酸性缩聚:三聚氰胺甲基衍生物的缩聚反应,介质的pH值起决定作用;反应在pH值小于7的弱酸性介质中进行pH值在3~5,温度60℃~70℃,反应时间60min,羟甲基之间缩合成醚键;这种羟甲基三聚氰胺磺酸钠单体之间以醚键连接成线性树脂,得到三聚氰胺甲醛磺酸盐,即:4碱性中和重整:先用氢氧化钠溶液将体系调至pH=8~9,一定温度下T=70~90℃,反应;这步反应是SMF贮存稳定性的关键,这一过程并不发生化学反应,其主要作用是调整分子量,增大树脂稳定性,使之更易储存;反应之后SMF粘度下降,可能是由于介质使分子链的物理缠绕减少所致,另外被大分子包围的未反应的H+也可能会被OH-中和,从而大大降低缩聚物的反应活性,起到终止反应,调节反应产物分子量的作用;一般认为碱性重整反应只对树脂的稳定性有影响,而对树脂的性能没有影响;混凝土聚羧酸盐系高性能减水剂早在20世纪80年代中期由日本开发,并且很快就应用于混凝土工程,90年代在混凝土工程中大量使用;自1986年日本的触媒公司首次将聚羧酸系高性能减水剂产品打入市场以来,国内外的研究有了很大的进步,现已由第一代聚羧酸盐系减水剂甲基丙烯酸/烯酸甲酯共聚物、第二代聚羧酸盐系减水剂丙烯基醚共聚物发展到第三代聚羧酸盐系减水剂酸胺-酞亚胺型,并正在研发第四代聚酰胺-聚乙烯乙二醇支链的新型高效减水剂;其合成原理与采用的聚合单体有关;如由应用化学07级刘琰等同学开发成功并推向市场的聚羧酸减水剂产品之一的结构如下:20世纪90年代中期聚羧酸系减水剂在日本使用量就已经超过萘系减水剂;1998年底日本聚羧酸系列产品已占有高性能减水剂产品总数的60%以上,近年来其用量更是占到高性能减水剂的90%;目前,在日本生产的聚羧酸系减水剂品种、型号及品牌名目繁多,每年用此类减水剂的混凝土为1000万m3左右,并不断增多;同时,北美和欧洲也十分重视对聚羧酸系减水剂的研究,并已从萘系、蜜胺系减水剂向聚羧酸系减水剂发展;在国外目前比较着名的厂家有日本的花王、竹本油脂、日本制纸、腾泽药品等,北美和欧洲各国近几年在聚羧酸盐系高性能减水剂产品方面也推出一系列产品,如美国Grance公司的Adva系列,瑞士SIKA公司的Viscocrete3010等,均已经进入中国市场;目前我国减水剂品种主要是以第二代萘系产品为主体,但聚羧酸系减水剂在我国发展极为迅速,其研发水平与生产水平均获得了很大的提高,应用技术也不断完善;近年来,聚羧酸系减水剂的应用也从过去的重大工程重点部位的应用向一般重大工程、普通工程应用;现在,几乎所有国家重大、重点工程中,尤其在水利、水电桥梁等工程中广泛使用;目前在我国,聚羧酸系减水剂的工业化生产体系初步建立,主要包括原材料生产供应体系初步建立,国内如今对聚醚等原料的生产、供应不断发展,其生产厂家大多数都已形成工业化生产规模,有些公司的产品质量也已接近国外产品水平,并开始得到推广应用,相信在不久的将来,由于国内聚醚货源充足,价格相对国外的便宜再加上质量的提高,其市场供应能力将稳步提升;但是,生产聚羧酸盐系高性能减水剂的另一种原料甲基丙烯酸在国内由于其质量、生产规模的原因,预计在将来的几年里只能作为进口产品的补充;此外,生产酯化大单体的专业厂家也逐渐开始出现,这意味着国内外加剂企业可以把主要的精力放在如何保持质量稳定性等其他应用技术方面的研究上;其次,复配技术发展很快,自从减水剂问世以来,为了进一步改善它的性能,也为了降低一定的成本,通常采用不同的外加剂进行简单的复配使用,往往能得到出人意料的结果,我国混凝土外加剂的复配技术是世界领先的,随着聚羧酸系高性能减水剂的发展,复配技术也不断发展,几乎很少有聚羧酸系高性能减水剂产品没有复配就直接使用到混凝土工程的使用的;我国工程应用的数量在不断增多,质量也稳步提升,近年来,聚羧酸盐系高性能减水剂在高速铁路、港口码头、水电大坝、市政工程等许多重点工程中得到广泛应用,随着国家相关政策的出台,对高性能混凝土的要求不断严格,聚羧酸盐系高性能减水剂以其优越的性能将会得到越来越多的重视和研究;聚羧酸系减水剂在较低掺量下对水泥颗粒就具有强烈的分散作用,减水效果明显;分析其分散减水机理,主要包括以下方面;1.空间位阻斥力作用聚合物减水剂吸附在水泥颗粒表面,则在水泥颗粒表面形成一层有一定厚度的聚合物分子吸附层;当水泥颗粒相互靠近,吸附层开始重叠,即在颗粒之间产生斥力作用,重叠越多,斥力越大;这种由于聚合物吸附层靠近重叠而产生的阻止水泥颗粒接近的机械分离作用力,称之为空间位阻斥力;聚羧酸系高效减水剂在水泥颗粒表面呈梳状吸附,侧链进入液相形成较厚的聚合物分子吸附层,使水泥颗粒之间具有显着的空间位阻斥力作用;2.水化膜润滑作用减水剂分子吸附在水泥颗粒表面后,由于极性基的亲水作用,可使水泥颗粒表面形成一层具有一定机械强度的溶剂化水膜;水化膜的形成可破坏水泥颗粒的絮凝结构,释放包裹于其中的拌合水,使水泥颗粒充分分散,同时对水泥颗粒及骨料颗粒的相对运动起到润滑作用,宏观上表现为新拌混凝土流动性增大;聚羧酸系高效减水剂侧链上带有许多亲水性活性基团如-OH,-O-,-COO-等,使水泥颗粒与水的亲和力增大、溶剂化作用增强,水化膜增厚;因此,具有较强的水化膜润滑作用;3.静电斥力作用减水剂分子定向吸附在水泥颗粒表面,由于亲水性极性基团的电离作用,使得水泥颗粒表面带上电性相同的电荷,从而彼此间产生静电斥力,水泥颗粒絮凝结构解体,颗粒相互分散,拌合物流动性增大;聚羧酸系高效减水剂吸附在水泥颗粒表面,使水泥颗粒表面的ζ-负电位降低幅度较小,水泥颗粒间静电斥力作用也较小;此外,由于聚羧酸系减水剂分子中含有大量羟基、醚基及羧基,这些极性基团具有较强的液-气界面活性,因而这类减水剂还具有一定得引起隔离“滚珠”减水效应;三、实验用试剂药品与仪器装置试剂药品:三聚氰胺;甲醛溶液含量37-40%;亚硫酸氢钠;聚乙二醇;聚乙二醇单甲醚MPEG;烯丙基聚乙二醇APEG;甲基丙烯酸MAA;丙烯酸AA;丙烯酰胺AM;甲基丙烯磺酸钠SMAS;苯乙烯磺酸钠;马来酸酐;过硫酸铵;氢氧化钠;浓盐酸等;海螺水泥;砂、石均符合GB8076要求的集料;仪器装置:SJ-160双转双速水泥净浆搅拌机、数显恒温水浴锅、电动搅拌器、电热恒温干燥箱、pHS-3C型酸度计、电子天平、四口圆底烧瓶、球型冷凝等;四、实验步骤1.三聚氰胺系减水剂的制备1羟甲基化反应:在装有机械搅拌装置、温度计、酸度计及回流装置的四口烧瓶中加入计量的甲醛溶液和三聚氰胺,然后用NaOH溶液调节体系pH=,然后升温至70℃反应,即得到羟甲基化三聚氰胺溶液;2磺化反应:将计量的亚硫酸氢钠加入到羟甲基化三聚氰胺溶液中,用NaOH溶液调节体系pH=12,然后升温至80℃进行磺化反应3h,即得磺化羟甲基化三聚氰胺溶液;3酸性缩聚反应:将体系的温度降至60℃,用盐酸溶液调节体系pH=4,进行酸性缩聚反应1h,即得磺化三聚氰胺甲醛树脂溶液;4碱性重整反应:将体系的温度升至80℃后,用NaOH溶液调节体系pH=,进行碱性重整反应1h,即得三聚氰胺系减水剂产品;2.醚类聚羧酸减水剂的合成向装有温度计、机械搅拌装置、冷凝回流及恒压滴液装置的四口烧瓶中,先加入一定量的水和烯丙基聚乙二醇APEG,加热搅拌至反应温度80℃,同时滴加混合单体甲基丙烯酸、马来酸酐、丙烯酰胺和部分引发剂过硫酸铵水溶液,控制反应浓度为40%,滴加完毕后,再保持恒温反应6小时反应结束后中间加入余下的引发剂,降温至45℃后加入40%的氢氧化钠溶液进行中和,调节溶液至pH=7,冷却至室温,即制得APEG-MAA-AM三元共聚物高效减水剂;3.酯类聚羧酸减水剂的合成1丙烯酸聚乙二醇单甲醚大单体的制备在装有温度计、球形冷凝管、分水器和搅拌器的250ml四口烧瓶中加入一定量的聚乙二醇、聚乙二醇单甲醚MPEG,升温到85℃,使其溶解,再依次加入一定量的甲苯、丙烯酸AA、对苯二酚和对甲苯磺酸,搅拌,继续升温到120-125℃,反应一段时间,即得到丙烯酸聚乙二醇单甲醚大单体;2MPEGAA-AA-SMAS三元共聚物高效减水剂的制备将第一步酯化反应所得到的产物减压蒸馏除去溶剂甲苯后,冷却至50℃左右,加入一定量的蒸馏水,并加入一定量的甲基丙烯磺酸钠SMAS和苯乙烯磺酸钠,加热搅拌至反应温度85℃,恒温反应一段时间;再加入一定量的过硫酸钾,恒温反应一段时间;再加入剩余的过硫酸钾,恒温反应一段时间;然后冷却,降温至40℃左右时,再用40%的氢氧化钠溶液调节pH,直到调至pH为7~8;冷却至室温,即制得MPEGAA-MA-SMAS三元共聚物高效减水剂;五、水泥净浆流动度的测定1.仪器a净浆;b.截锥圆模:上口直径36mm,下口60mm,高度为60mm,内壁光滑无接缝的制品;c.板400×400mm,厚5mm;d.秒表;e.钢直尺,300mm;f.刮刀;2.实验步骤a.将玻璃板放置在水平位置,用湿布将玻璃板,截锥圆模,搅拌器及搅拌锅均匀擦过,使其表面湿而不带水渍;b.将截锥圆模放在玻璃板的中央,并用湿布覆盖待用;c.称取300g采用苏州杭达水泥制品有限公司生产的基准水泥,倒入搅拌锅内;d.加入掺量%的外加剂及87g水,先慢搅2min,再快搅1min;e.将拌好的净浆迅速注入截锥圆模内,用刮刀刮平,将截锥圆模按垂直方面提起,同时开启秒表计时,任水泥净浆在玻璃板上流动,至30s,用直尺量取流淌部分互相垂直的两个方向的最大直径,取平均值作为水泥净浆流动度;。
亚硫酸氢钠

亚硫酸氢钠(1)化学品及企业标识化学品中文名:亚硫酸氢钠;酸式亚硫酸钠化学品英文名:sodium bisulfite ;hydrogen sulfite sodium分子式:NaHSO3相对分子量:104.06(2)成分/组成信息成分:纯品CAS No:7631-90-5(3)危险性概述危险性类别:第8.1 类酸性腐蚀品侵入途径:吸入、食入、经皮吸收健康危害:对皮肤、眼、呼吸道有刺激性,可引起过敏反应。
可引起角膜损害,导致失明。
可引起哮喘;大量口服引起恶心、腹痛、腹泻、循环衰竭、中枢神经抑制。
环境危害:对环境有危害,对水体可造成污染。
燃爆危险:本品不燃,具腐蚀性,可致人体灼伤。
(4)急救措施皮肤接触:脱去污染的衣着,用肥皂水和清水彻底冲洗皮肤。
如有不适感,就医眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。
如有不适感,就医吸入:迅速脱离现场至空气新鲜处。
保持呼吸道通畅。
如呼吸困难,给输氧。
如呼吸、心跳停止,立即进行人工呼吸。
就医。
食入:饮足量温水,催吐。
就医。
(5)消防措施危险特性:具有强还原性。
接触酸或酸气能产生有毒气体。
受高热分解放出有毒的气体。
具有腐蚀性。
有害燃烧产物:氧化硫、氧化钠。
灭火方法:根据着火原因选择适当灭火剂灭火。
灭火注意事项及措施:消防人员必须穿全身耐酸碱消防服。
灭火时尽可能将容器从火场移至空旷处。
(6)泄漏应急处理应急行动:隔离泄漏污染区,限制出入。
建议应急处理人员戴防尘口罩,穿防酸服。
不要直接接触泄漏物。
小量泄漏:避免扬尘,小心扫起,收集于干燥、洁净、有盖的容器中。
大量泄漏:收集回收或运至废物处理场所处置。
(7)操作处置与储存操作注意事项:密闭操作,局部排风。
防止粉尘释放到车间空气中。
操作人员必须经过专门培训,严格遵守操作规程。
建议操作人员佩戴自吸过滤式防尘口罩,戴化学安全防护眼镜,穿橡胶耐酸碱服,戴橡胶耐酸碱手套。
避免产生粉尘。
避免与氧化剂、酸类、碱类接触。
配备泄漏应急处理设备。
亚硫酸溶液中加入亚硫酸氢钠固体ph的变化曲线

亚硫酸溶液中加入亚硫酸氢钠固体ph的变化曲线亚硫酸溶液中加入亚硫酸氢钠固体pH的变化曲线导言:pH值是衡量溶液酸碱性的重要指标之一。
当我们在亚硫酸溶液中加入亚硫酸氢钠固体时,会发生一系列化学反应,从而引起溶液pH值的变化。
本文将深入探讨这一过程,并介绍亚硫酸溶液中加入亚硫酸氢钠固体后pH值的变化曲线。
一、亚硫酸与亚硫酸氢钠的反应机制1.1 亚硫酸的性质亚硫酸(H2SO3)是一种无色、有刺激性气味的可溶于水的液体。
其具有酸性,是由亚硫酸酸根离子(HSO3-)和氢离子(H+)所组成的。
1.2 亚硫酸氢钠的性质亚硫酸氢钠(NaHSO3)也是一种无色的晶体固体。
当其溶解于水中时,会释放出亚硫酸酸根离子(HSO3-)和钠离子(Na+)。
1.3 反应机制当亚硫酸与亚硫酸氢钠发生反应时,亚硫酸酸根离子和氢离子会与亚硫酸氢钠中的钠离子结合,生成硫代硫酸盐和水。
二、亚硫酸溶液中pH值的变化曲线通过实验可以得出,在亚硫酸溶液中加入亚硫酸氢钠固体后,溶液的pH值呈现出一个特殊的变化曲线。
下面将逐步介绍这一曲线的特点。
2.1 初始状态当我们开始加入亚硫酸氢钠固体时,亚硫酸溶液中的pH值会保持在较低的酸性区域。
这是由于亚硫酸与亚硫酸氢钠反应后产生的硫代硫酸盐呈酸性的原因。
此时,溶液中存在着大量的亚硫酸酸根离子和氢离子。
2.2 过渡状态随着亚硫酸氢钠的加入,亚硫酸溶液开始在酸性到碱性之间进行一个过渡状态。
这是由于亚硫酸酸根离子和氢离子与亚硫酸氢钠中的钠离子结合生成的硫代硫酸盐和水,并将其中的氢离子中和掉。
溶液中的pH值逐渐升高。
2.3 平衡状态当亚硫酸氢钠完全溶解并与溶液中的氢离子发生完全中和后,溶液进入了一个平衡状态。
在这个阶段,亚硫酸酸根离子和亚硫酸氢钠中的钠离子已经完全转化为硫代硫酸盐,并且不再发生任何反应。
此时,溶液的pH值会停留在一个较高的碱性区域。
三、总结和回顾性内容通过本文的介绍,我们可以清晰地了解亚硫酸溶液中加入亚硫酸氢钠固体后pH值的变化曲线。
亚硫酸氢钠溶液中离子浓度大小排序

亚硫酸氢钠溶液中离子浓度大小排序嘿,朋友们!今天我们要聊聊一个听起来有点高深的化学话题——亚硫酸氢钠溶液中的离子浓度。
别担心,我会把它讲得简单易懂,让你听了心里倍儿爽!那么,亚硫酸氢钠是什么呢?简单来说,它就是我们常说的“酸性盐”,在水中溶解后,会分解成不同的离子。
这其中最主要的离子就是亚硫酸根离子(HSO₃⁻)、氢离子(H⁺)和钠离子(Na⁺)了。
听起来是不是有点复杂?没关系,我们一步一步来,确保你也能轻松get到!1. 亚硫酸氢钠的基本知识1.1 什么是亚硫酸氢钠?亚硫酸氢钠,化学式是NaHSO₃,名字虽然听上去很拗口,但其实它在日常生活中还是挺常见的。
比如,咱们在做一些食品保鲜的时候,亚硫酸氢钠就会派上用场。
它能帮助抑制细菌生长,防止食物变质。
真是个小能手呢!1.2 溶解后的离子当亚硫酸氢钠溶解在水里时,会分解成三种离子:钠离子(Na⁺)、氢离子(H⁺)和亚硫酸根离子(HSO₃⁻)。
这就像把一群好朋友放进一个聚会,大家都有各自的特点和作用。
钠离子可是个热情的人,总是和水分子打成一片;而氢离子嘛,那可就有点“火”了,专门制造酸性环境;至于亚硫酸根离子,它则在一旁默默支持,发挥着重要的作用。
2. 离子的浓度排序2.1 先来分析一下浓度好啦,接下来我们就要进入正题——如何排序这些离子的浓度。
一般情况下,当我们把亚硫酸氢钠溶解在水里的时候,钠离子的浓度是比较高的。
这是因为它在水里很容易分散,像个游泳健将一样畅游;而氢离子和亚硫酸根离子的浓度相对较低,尤其是氢离子,因为它们会与水分子结合,形成水合氢离子,导致浓度减少。
2.2 排序出来了所以,按照浓度从高到低来排序的话,结果是:钠离子(Na⁺)>亚硫酸根离子(HSO₃⁻)>氢离子(H⁺)。
这样一看,钠离子真的是个“高富帅”啊,稳稳的霸主地位,真让人佩服!3. 生活中的应用3.1 食品保鲜的好帮手说到亚硫酸氢钠,咱们不能不提它在生活中的应用。
尤其是在食品行业,它被广泛用作防腐剂和抗氧化剂。
亚硫酸氢盐转化原理

亚硫酸氢盐转化原理一、什么是亚硫酸氢盐?亚硫酸氢盐是一种化学物质,化学式为HSO3-。
由于其强还原性和氧化性较弱,被广泛应用于许多工业和化学领域。
亚硫酸氢盐常见的盐类有亚硫酸钠(NaHSO3)和亚硫酸钙(Ca(HSO3)2)。
二、亚硫酸氢盐的转化原理亚硫酸氢盐的转化原理主要涉及其在氧化还原反应和酸碱反应中的作用。
1. 氧化还原反应亚硫酸氢盐在氧化还原反应中常被用作强还原剂。
其自身可以被氧化为硫酸根离子(SO4-2),同时氧化物或金属离子(如Cu2+、Fe3+)被还原为较低的价态。
例如,亚硫酸氢钠与漂白粉(氯化钠)反应产生氯化钠、水和硫酸钠:2 NaHSO3 + NaClO → 2 NaCl + H2O + Na2SO4此反应中,亚硫酸氢钠(NaHSO3)被氯化钠(NaClO)氧化为硫酸钠(Na2SO4),氯化钠则被还原为氯化物(NaCl)。
2. 酸碱反应亚硫酸氢盐在酸碱反应中表现出良好的缓冲性质。
当亚硫酸氢盐与强碱反应时,会形成亚硫酸盐。
而当亚硫酸氢盐与强酸反应时,会形成二氧化硫和水。
例如,亚硫酸氢钙与氢氧化钠反应产生亚硫酸钙和水:Ca(HSO3)2 + 2 NaOH → CaSO3 + 2 H2O + 2 NaHSO3此反应中,亚硫酸氢钙(Ca(HSO3)2)与氢氧化钠(NaOH)发生中和反应,生成亚硫酸钙(CaSO3)、水和亚硫酸氢钠(NaHSO3)。
三、亚硫酸氢盐的应用由于亚硫酸氢盐具有还原性和缓冲性等特点,广泛应用于不同领域,下面列举了几个常见的应用领域:1.食品工业:亚硫酸氢盐可用作食品的食品添加剂,用于防止食品变色、腐败和氧化。
例如,在葡萄酒酿造过程中,亚硫酸氢盐可用于抑制细菌和酵母的生长,延长葡萄酒的保质期。
2.化学工业:亚硫酸氢盐可用作化学试剂,参与不同的反应过程。
例如,在某些有机合成反应中,亚硫酸氢盐可被用作还原剂,从而实现目标产物的合成。
3.环境保护:亚硫酸氢盐可以用于废水处理和脱硫过程。
亚硫酸氢钠 工业纯度

亚硫酸氢钠工业纯度亚硫酸氢钠是一种广泛应用于工业生产中的化学物质,其工业纯度是指该化学物质中所含杂质的含量非常低,可以满足各种工业生产的要求和标准。
下面将详细介绍亚硫酸氢钠工业纯度的相关内容。
一、亚硫酸氢钠的基本性质亚硫酸氢钠的化学式为NaHSO3,是一种白色结晶性粉末,在水中溶解度较大,呈弱酸性。
在常温下亚硫酸氢钠稳定,但在高温或强酸环境下会分解产生二氧化硫气体。
亚硫酸氢钠具有较强的还原性和抗氧化性,在食品、化妆品、医药等行业中具有广泛应用。
二、亚硫酸氢钠工业纯度的含义亚硫酸氢钠工业纯度是指该化学物质中所含杂质的含量非常低,可以满足各种工业生产的要求和标准。
其含量通常在99%以上,是一种高纯度的化学物质。
亚硫酸氢钠工业纯度的高低直接影响到其在工业生产中的应用效果和产品质量。
三、亚硫酸氢钠工业纯度的制备方法1. 硫磺和氢气反应制备:将硫磺和氢气按一定比例混合,通过催化剂反应生成亚硫酸氢钠。
该方法的优点是反应速度快,产物纯度高,但需要专业设备和技术支持。
2. 亚硫酸钠和酸反应制备:将亚硫酸钠和酸按一定比例混合反应,生成亚硫酸氢钠。
该方法的优点是操作简单,成本低,但产物纯度较低。
3. 亚硫酸钠和硫酸反应制备:将亚硫酸钠和硫酸按一定比例混合反应,生成亚硫酸氢钠。
该方法的优点是反应产物纯度高,但需要注意反应条件和环境污染问题。
四、亚硫酸氢钠工业纯度的应用领域亚硫酸氢钠工业纯度的应用领域非常广泛,主要包括以下几个方面:1. 食品行业:亚硫酸氢钠可以作为食品添加剂,用于保鲜、漂白、抗氧化等。
2. 化妆品行业:亚硫酸氢钠可以作为化妆品中的防腐剂、抗氧剂等。
3. 医药行业:亚硫酸氢钠可以作为医药制剂中的保护剂、抗氧化剂等。
4. 纺织行业:亚硫酸氢钠可以作为纺织品的漂白剂和染料还原剂。
5. 电子行业:亚硫酸氢钠可以作为电镀过程中的还原剂和清洗剂。
五、亚硫酸氢钠工业纯度的安全注意事项亚硫酸氢钠在使用过程中需要注意以下几个方面:1. 亚硫酸氢钠具有较强的还原性,与许多物质发生反应,使用时需要注意避免与其他化学物质混合。
