电解水制氢氧
电解水制氢,固碳合成甲醇 公式

电解水制氢,固碳合成甲醇公式
电解水制氢的化学反应方程式为:
2H₂O (l) → 2H₂ (g) + O₂ (g)
这个反应表示水在电解的条件下分解为氢气和氧气。
在实际的电解水制氢过程中,通常使用电解槽,通过电流将水分子分解为氢离子和氧离子,然后分别在阳极和阴极上得到氢气和氧气。
固碳合成甲醇的化学反应方程式为:
CO₂ (g) + 3H₂ (g) → CH₃OH (l) + H₂O (l)
这个反应表示二氧化碳和氢气在催化剂的作用下反应生成甲醇和水。
在固碳合成甲醇的过程中,通常使用催化剂来加速反应,同时需要控制反应条件(如温度、压力等)以获得较高的甲醇产率。
通过结合电解水制氢和固碳合成甲醇两个过程,可以实现将可再生能源(如太阳能、风能等)转化为化学能(甲醇)的目的,同时减少二氧化碳的排放,实现碳中和的目标。
这种技术被称为“绿色甲醇”或“可再生甲醇”生产技术。
电解水制氢

电解水
外文名
含义
水(H20)被电解生成氢气和氧气
方程式
2H2O——(通电)2H2t+O2t
历史
最早于1789年,杨-鲁道夫-德曼和阿德里安-派斯-范-特鲁斯维克通过静电装置发电利用 金电极把莱顿瓶中的水电解成气体。1800年,亚历山德罗-伏特发明了伏打电池,并于数
周后,被威廉-尼克森和安东尼-卡莱尔用于电解水。 解水逐渐引人关注,并成为一种廉价制氢的方法。
阳极:2H2O-4e-=O2t+4ht
阴极:4H++4e-=2H2t
反应遵循法拉第定律,气体产量与电流和通电时间成正比。
固体聚合物电解质,SPE电解水,最初用于向宇宙飞船或潜水艇供氧,或在实验室作
为氢气发生器(可用于气体色谱)。核电大规模发展以后,人们利用SPE技术在用电低谷电
解水产生氢,在供电高峰以SPE氢-氧燃料电池向外供电,使之成为能量贮存转换装置
通过直接电解纯水产生高纯氢气(不加碱),电解池只电解纯水即可产氢。通电后,
电解池阴极产氢气,阳极产氧气,氢气进入氢/水分离器。氧气排入大气。氢/水分离器将氢
气和水分离。氢气进入干燥器除湿后,经稳压阀、调节阀调整到额定压力(0.02〜0.45Mpa
可调)由出口输出。电解池的产氢压力由传感器控制在0.45Mpa左右,当压力达到设定值
时,电解池电源供应切断;压力下降,低于设定值时电源恢复供电。
3
在氯碱工业中副产多量较纯氢气,除供合成盐酸外还有剩余,也可经提纯生产普氢或
纯氢。像化工二厂用的氢气就是电解盐水的副产
电解水
水(H2O)被直流电电解生成氢气和 氧气的过程被称为电解水。电流通过水(H2O)时,在
阴极通过还原水形成氢气(H2),在阳极则通过氧化水形成氧气(O2)。氢气生成量大约是氧气 的两倍。电解水是取代蒸汽重整制氢的下一代制备氢燃料方法。
电解水制氢气和氧气的实验

连接方式:拧紧螺母,确保接触良好
电解液
添加标题
添加标题
添加标题
添加标题
作用:作为电解质,促进水电解反应
成分:氢氧化钠(NaOH)和氢氧化钾(KOH)
浓度:根据实验需求调整,一般控制在10%-30%
制备方法:将氢氧化钠和氢氧化钾按比例混合,加水溶解,搅拌均匀。
收集气体的装置
容量:根据实验需求选择适当容量
电解水制氢气和氧气的实验
汇报人:XX
目录
01
添加目录项标题
02
实验原理
03
实验器材和试剂
04
实验步骤
05
实验结果分析
06
实验注意事项
添加章节标题
1
实验原理
2
电解水反应原理
电解水反应:水分子被分解成氢气和氧气
反应方程式:2H2O → 2H2 + O2
反应产物:氢气和氧气
反应条件:通电
氢气和氧气的生成
实验误差分析
误差的减小:选择高精度仪器,改进操作方法,控制环境因素等
实验误差的来源:仪器误差、操作误差、环境误差等
误差的估计:通过多次测量取平均值,计算标准差
误差的影响:对实验结果的准确性和可靠性产生影响,需要认真对待和合理处理
实验结果的应用场景
添加标题
添加标题
添加标题
添加标题
氧气可以用于医疗、工业、航天等领域
装置名称:集气瓶
材质:玻璃或塑料
连接方式:与反应容器相连,用于收集产生的气体
使用方法:在集气瓶中装满水,将反应容器中的气体通过导管导入集气瓶中,气体会溶解在水中,形成气泡,便于观察和收集。
实验步骤
4
准备实验器材和试剂
电解水制氢实验

电解水制氢实验在人们不断探索可再生能源领域的同时,水电解制氢技术备受关注。
水电解制氢是一种利用电能将水分解成氧气和氢气的过程,其中氢气可以作为一种清洁能源的替代品。
本文将介绍电解水制氢的原理、实验过程和应用前景。
首先,让我们了解电解水制氢的原理。
该实验基于电解的原理,通过将水中的氢氧化物离子进行氧化还原反应,使其分解成氢气和氧气。
具体而言,当通入电流时,电子转移至阴极,同时水的氧化反应发生,产生氢气。
在阳极则发生氧化反应,生成氧气。
整个反应方程式为:2H2O(l) → 2H2(g)+O2(g)。
接下来,我们来进行电解水制氢的实验。
首先,我们需要准备一台电解槽、两根电极(通常为碳棒或铂丝)、蒸馏水和直流电源。
安装好电解槽后,将两根电极插入槽中,分别与正负电极相连。
然后,将电解槽中注入适量的蒸馏水,确保电极浸没在水中。
最后,将直流电源连接电解槽的两根电极,调节电流大小。
当电流通入后,我们可以观察到一些现象。
首先,在阴极处,我们会看到氢气以气泡形式释放,氧化反应发生在阳极处,会看到氧气以气泡形式释放。
这些气泡会逐渐上升到液面,并从液面逸出。
整个实验过程中,会伴随着一些电解槽内部电解液的变化,例如水的颜色可能会有所改变。
实验结束后,我们可以用氢气的可燃性和氧气的明亮燃烧性来确认产气。
电解水制氢具有广泛的应用前景。
首先,氢气可以作为一种清洁能源的替代品。
传统能源往往依赖石油、煤炭等化石燃料,而这些能源的使用会产生大量二氧化碳等温室气体,加剧气候变化。
因此,利用电解水制氢可以在一定程度上减少对传统能源的依赖,并降低碳排放。
此外,氢气还可以用作燃料电池的燃料,通过与氧气反应生成电能,以推动电动汽车等设备的运行。
这样的应用能够减少对有限的化石能源资源的需求,并减少空气污染。
此外,氢气还可以应用于航空航天、金属冶炼等领域,不仅为科学研究提供了新的动力,也拓宽了科技创新的广度。
综上所述,电解水制氢是一种重要的科学实验,通过电解水分解产生氢气和氧气。
电解水制氢实用工艺描述
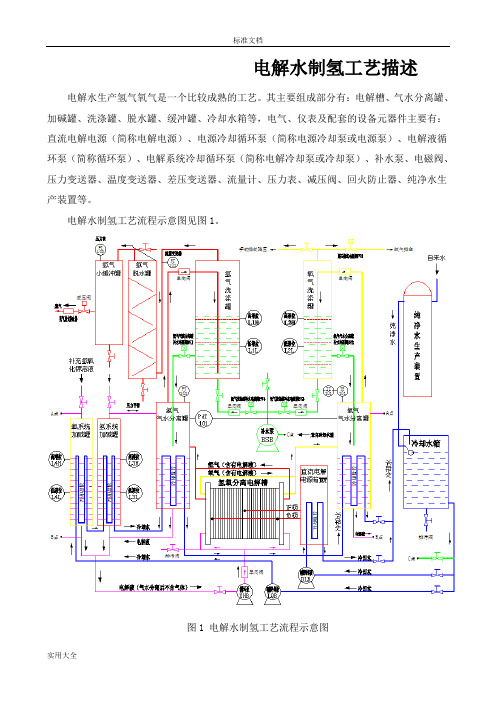
电解水制氢工艺描述电解水生产氢气氧气是一个比较成熟的工艺。
其主要组成部分有:电解槽、气水分离罐、加碱罐、洗涤罐、脱水罐、缓冲罐、冷却水箱等,电气、仪表及配套的设备元器件主要有:直流电解电源(简称电解电源)、电源冷却循环泵(简称电源冷却泵或电源泵)、电解液循环泵(简称循环泵)、电解系统冷却循环泵(简称电解冷却泵或冷却泵)、补水泵、电磁阀、压力变送器、温度变送器、差压变送器、流量计、压力表、减压阀、回火防止器、纯净水生产装置等。
电解水制氢工艺流程示意图见图1。
图1 电解水制氢工艺流程示意图压力的单位为Mpa,小数点后面保留3位。
差压的单位为kPa,小数点后面保留2位,流量单位为m3/h,小数点后面保留2位。
温度的单位为°C,小数点后面保留1位,累计流量的单位为m3,小数点后面保留1位,累计工作时间的单位为h,小数点后面保留1位。
所有的电磁阀均为电开阀,通电开启,断电关闭。
一、电解电源DDY、电源冷却泵DLB、循环泵XHB及冷却泵LQB控制表1 电解系统与冷却系统对应输入输出关系表1、氢气压力PH 由压力变送器PT101变送为4~20mA直流信号,根据氢气压力PH控制电解电源DDY(电解电源DDY由一个开关量信号控制运行与停止)、电源冷却泵DLB和循环泵XHB(电源冷却泵DLB和循环泵XHB与电解电源DDY同步受氢气压力PH控制)的通断,氢气压力可以在触摸屏上设置:○1氢气压力上限设定值(简称压力设定上限)PHH的设置范围0~3.00Mpa(参考值0.40Mpa);○2氢气压力下限设定值(简称压力设定下限)PHL的设置范围0~3.00MPa(参考值0.35Mpa)。
参考值就是第一次开机设置时(或者长时间断电数据丢失时)推荐使用的数值。
○3当氢气压力PH 高于压力设定上限PHH,PH>PHH,DO1输出为OFF,电解电源DDY、电源泵DLB和循环泵XHB停止运行;○4氢气压力PH 低于压力设定下限PHL,PH<PHL, DO1输出为ON,电解电源DDY、电源泵DLB和循环泵XHB通电运行。
电解水制氢技术的研究

电解水制氢技术的研究水是生命之源,而氢又是最简单的元素,它们的结合产生的水合氢对生命起到了重要的作用。
氢具有高能密度、清洁、可再生等优点,因此被认为是未来能源的重要替代品。
而电解水制氢技术作为一种可持续、清洁、低成本的制氢技术,正在逐渐受到人们的关注。
一、电解水制氢技术的原理电解水制氢技术的原理十分简单,就是利用电解作用将水分解成氢气和氧气。
其反应方程式如下:2H2O → 2H2 + O2在电解水过程中,电解池将水分子分解成氢离子和氧离子,并将它们分别吸收到阳极和阴极的表面上,这些离子在电极上接受电子的转移,从而形成氢和氧。
由于氧是一种强氧化剂,它会与阳极上的铜或钯等金属发生反应,因此在制氢反应中需要添加一些电解液将氧阴极化。
二、电解水制氢技术的优点1.清洁电解水制氢技术是一种清洁的制氢技术,根据其反应方程式,只产生水和氢气,在做好废水的处理后,反应过程中不会排放任何有害物质,因此不会污染环境。
2.低成本电解水制氢技术的原材料是水和电,相对于其他制氢技术,原材料成本很低,而且电解池设备简单,制氢的成本也比其他技术低。
3.可再生水可以说是可再生的,因此电解水制氢技术是一种可持续的制氢技术,可以长期使用。
三、电解水制氢技术的应用前景电解水制氢技术的应用前景十分广阔,氢燃料电池、天然气的储存、金属粉末制备等都可以采用该技术。
近年来,随着可再生能源的快速发展和氢能源政策的出台,电解水制氢技术也越来越受到重视。
在氢燃料电池领域,由于其能源密度高、无污染、低噪音、充电时间短等优点,越来越受到汽车制造商的关注。
汽车用氢燃料电池的推广,必将促进电解水制氢技术的发展。
除汽车之外,氢燃料电池还可以应用在其他领域,如大型交通工具、家用电器、发电机组等。
在金属粉末制备领域,由于金属粉末可用于3D打印、焊接、激光成型等领域,因此对电解水制氢技术的需求也越来越大。
四、电解水制氢技术的发展现状目前,电解水制氢技术已经越来越成熟。
pem电解水制氢原理

pem电解水制氢原理
PEM电解水制氢原理是基于质子交换膜技术的一种电解水制氢技术,其原理是将水分子分解成氢和氧气。
在PEM电解水制氢过程中,水被置于一个电解槽中,其中包含两个电极:一个阳极和一个阴极。
当电流通过电解槽时,阴极上的电子被氧化,而阳极上的电子被还原。
在这个过程中,水分子被分解成氧气和氢气。
质子交换膜用来分离氢气和氧气,同时允许质子通过。
因此,产生的氢气可以被收集和储存,以用于燃料电池等应用。
PEM电解水制氢技术具有高效、清洁和可靠的特点,因此已经成为了一种重要的氢气生产技术。
- 1 -。
电解水制氢 副产物

电解水制氢副产物
电解水制氢是通过将水分解成氢气和氧气的化学过程。
在这个
过程中,氢气是主要的产物,而氧气是副产物。
具体来说,当电流
通过水中时,水分子会被分解成氢气和氧气。
这是因为电流会导致
水中的氢离子在阴极处接受电子并生成氢气,而氧离子在阳极处失
去电子并生成氧气。
因此,在电解水制氢的过程中,氢气是我们希
望得到的主要产物,而氧气则是作为副产物同时生成的。
此外,除了氢气和氧气之外,电解水还可能产生一些其他的副
产物,这些副产物通常是由于水中的杂质或电解过程中的一些不完
全反应所致。
这些副产物可能包括氢氧化物、氢氧化钠或氢氧化钙等。
在实际的工业生产中,通常会对电解过程进行优化,以最大限
度地减少这些副产物的生成,以确保生产出高纯度的氢气和氧气。
总的来说,电解水制氢的主要产物是氢气,而氧气是其副产物。
在一些特定条件下,还会生成一些其他的副产物,但通常会通过优
化工艺来减少这些副产物的生成。
电解水制氢正负极反应

电解水制氢正负极反应一、引言电解水制氢是一种重要的氢气制备方式。
它通过电解水的过程,将水分解为氢气和氧气。
在这个过程中,正极和负极扮演着关键的角色。
本文将重点探讨电解水制氢过程中正极和负极的反应机制。
二、正极反应在电解水制氢过程中,正极是氢气的产生地。
正极一般采用铂或其他贵金属作为催化剂,以提高反应速率。
正极的反应可以表示为:2H2O + 2e- → H2 + 2OH-正极上的催化剂会促使水分子接受电子,并发生还原反应,生成氢气和氢氧根离子。
这个反应是一个非常重要的步骤,它决定了氢气的产量和纯度。
正极上的催化剂能够降低水的还原电位,加速水的电解过程。
三、负极反应负极是电解水制氢过程中的另一个关键部分。
负极一般采用铂或其他贵金属作为催化剂,同样是为了提高反应速率。
负极的反应可以表示为:4OH- → 2H2O + O2 + 4e-负极上的催化剂会促使氢氧根离子失去电子,并发生氧气的析出反应。
这个反应是一个重要的步骤,它防止了氢氧根离子在电解过程中堆积过多,同时也可以提供所需的电子供正极反应使用。
四、电解水制氢过程电解水制氢的过程是在电解槽中进行的。
电解槽通常由两个电极(正极和负极),以及一个电解质溶液组成。
正极和负极分别连接到电源的正负极端。
当电源通电时,电解质溶液中的水开始电离,产生氢气和氧气。
在正极上,水分子接受电子,并发生还原反应,生成氢气和氢氧根离子。
而在负极上,氢氧根离子失去电子,并发生氧气的析出反应。
这样,通过正极和负极的协同作用,水分解成氢气和氧气。
五、优化电解水制氢反应为了提高电解水制氢的效率和经济性,科学家们一直在寻求新的方法和材料。
他们研究了各种催化剂,以提高反应速率和降低能耗。
例如,一些研究表明,使用非贵金属催化剂也可以实现高效的电解水制氢。
调节电解质溶液的成分和浓度也可以改善反应效果。
通过优化反应条件,可以提高氢气的产量和纯度,减少能源消耗,从而推动电解水制氢技术的发展。
六、应用前景电解水制氢是一种可持续的氢气制备方式,具有广阔的应用前景。
电解水的制氢与制氧技术

电解水的制氢与制氧技术随着环保意识的不断提高,制氢与制氧技术逐渐被人们所熟知。
其中重要的一项技术是电解水的制氢与制氧技术。
这项技术以其环保、高效等特点,已经得到广泛应用。
一、电解水工艺基础电解水工艺是利用电能在电极上引发氧化还原反应,从而使水分解成氢气和氧气的技术。
该工艺利用的原理十分简单,将电流通过水中的电极,分别在阳极和阴极引发氧化还原反应,最终产生氢气和氧气。
这里需要注意的一点是,电解水的产物和电极材料的选择都会影响整个过程的效果和效率。
二、制氢技术的应用制氢技术应用非常广泛,特别是在工业领域和能源开发中发挥着关键作用。
比如说,制氢技术被广泛应用于氢燃料电池,其可以为汽车和其他机动设备提供安全、高效的能源。
制氢技术也被用于电力工程中,可以补充再生能源的储存和传输,未来也有可能为太空探索提供支持。
三、制氧技术的应用制氧技术同样受到广泛关注并得到应用。
制氧技术主要应用于工业化领域中的生产、医疗、冶金、生物和环境等领域。
在这些领域中,氧气是一种非常重要而且必不可少的气体,其具有一系列特殊的生理和化学特性,可以促进多种生物过程的顺利进行。
四、电解水制氢和制氧技术的优势与其他工艺相比,电解水的制氢和制氧技术具有许多显著的优势。
首先,这种工艺不会产生任何污染物,完全不会对环境造成损害。
其次,该工艺的效率非常高,产氢产氧比例可控,有很高的自动化程度。
第三,电解水工艺成本低,容易实现规模化应用,其工艺流程也相对简单。
五、未来的发展和前景随着环境保护和清洁能源的需求不断增加,电解水的制氢和制氧技术有着巨大的发展潜力。
未来,电解水的技术不仅可以为社会提供更清洁、高效、可持续的能源,而且有望为环境保护和可持续发展做出巨大的贡献。
总的来说,电解水的制氢和制氧技术十分重要而且有广泛的应用。
该技术具有许多优势,未来还有很大的发展前景。
我们相信,电解水的技术将会逐渐成为环保和科技领域中的重要支柱,为实现人与自然和谐共生的目标做出更大贡献。
电解水制氢的放热量

电解水制氢的放热量电解水制氢是一种常见的制氢方法,具有广泛的应用前景。
电解水制氢的基本原理是利用电解反应将水分解为氢气和氧气,其中电解过程是一个吸热反应,而产氢反应则是一个放热反应。
本文将从原理、实验和应用等方面介绍电解水制氢的放热量。
电解水制氢的基本原理是通过通电的方式将水分解为氢气和氧气。
在水中,氢原子与氧原子紧密连接在一起,通过加电解作用将它们分开,就可以得到氢气和氧气。
在电解水的过程中,需要提供能量作为电解反应的驱动力。
这个能量源可以是直流电源,如电池或太阳能电池板。
电解水制氢的过程可以用如下的方程式来表示:2H2O(l) -> 2H2(g) + O2(g)上述方程式表示了水在电解过程中分解为氧气和氢气的反应。
这个过程是一个吸热反应。
吸热反应是指反应物中的能量较高,而生成物中的能量较低。
因此,在电解水过程中,反应需要从外部吸收能量。
与此相反的是产氢反应。
产氢反应是指氢气生成的反应,这个过程是一个放热反应。
放热反应是指反应物中的能量较低,而生成物中的能量较高。
当水被电解分解成氢气和氧气时,氢气是放热的产物。
因此,在电解水制氢的过程中,能量会以热量的形式释放出来。
电解水制氢的实验通过一系列的操作来实现。
首先,要准备一个电解槽,将两个电极(通常是钢板)浸入水中。
一个电极称为阳极,另一个电极称为阴极。
然后,将直流电源连接到电解槽的两个电极上。
通电后,电解槽中的水开始分解,产生氢气和氧气。
实验过程中需要考虑一些因素,如电流的大小、电解槽的温度和反应的时间。
电流的大小直接影响到反应速度和产氢的效率。
较大的电流会加快反应速度,但也会使反应温度升高。
水的温度对反应速率有一定的影响,较高的温度可以使反应速率增加。
然而,过高的温度会导致氢气的泄漏和水的蒸发。
反应的时间也会影响到产氢的效率,一般情况下,较长的反应时间会有更高的产氢效率。
电解水制氢的放热量是一个重要的数据。
实验中可以通过测量反应容器的温度变化来获取放热量。
电解水制氢技术的应用前景

电解水制氢技术的应用前景随着科技的不断发展,人类对新能源的需求越来越迫切。
而氢能作为一种可再生、清洁、高效能源已经成为了人们研究的重点之一。
而要让氢能真正成为主流能源,需求首先解决的是氢的制备问题。
电解水制氢技术,作为氢能的核心技术之一,具有更加广泛的应用前景。
1. 电解水制氢技术的基本原理电解水制氢技术,顾名思义,就是利用电能将水分解成氢气和氧气的过程。
其基本原理是把电能作为动力,通过电解水的方式来把水分解成氢气和氧气。
在电解过程中,首先需要一个电解池。
电解池本身不会进行化学反应,而是提供一个粗略的分隔。
电解池中需要放置电解质,即能使水离子化的物质。
常见的电解质有NaOH、Na2SO4等。
然后,在电解池的两端需要放置电极。
一般选用铂电极或者是钢铁电极等。
在电解的过程中,在电解池的正极,会有氧气气体出现;在电解池的负极,会有氢气气体出现。
然后,通过把氢气气体收集起来,就可以得到用于制造氢能的氢气气体了。
2. 电解水制氢技术的应用前景(1)清洁能源电解水制氢不需要燃料,在这个过程中也不会产生任何有害的化学物质,因此,是一种十分干净的能源制备方式。
与传统的燃料制备方式不同的是,电解水制氢不会产生任何的废气、废液等污染物。
同时,对于氢能的应用,是一种无排放、无二噁英等污染物、无烟尘和噪音的清洁能源。
它对大气质量、城市噪声、生态环境等问题有着非常显著的改善作用。
因此,电解水制氢技术有很强的清洁生态性。
(2)可再生性电解水制氢技术的能源来源没有任何限制,可以使用任何方式提供电力,包括太阳能、风能、水能等等。
因此,电解水制氢具有非常显著的可再生性。
与非可再生的传统的燃料不同,电解水制氢的能源来源不会用完。
太阳能、风能、水能等等等能源是地球上不会用完的能源。
因此,电解水制氢具有不穷的发展前景。
(3)高效能源氢气燃烧的能量密度非常高,比传统的燃料更加高效。
同时,使用氢气作为燃料,体积质量比非常低。
因此,在航空航天、汽车运输等领域,氢气燃料系统是十分理想的选择。
电解水制氢的研究进展

电解水制氢的研究进展近年来,以氢能源为主要发展方向的研究逐渐受到人们的重视。
而电解水制氢技术便是其中重要的组成部分。
电解水制氢是指将水分子通过电解分解成氧气和氢气两种气体的过程。
这项技术包括两个主要步骤:水的电离和水分子中的氢离子和氧离子的电子还原。
这种制氢方式具有成本低廉、可再生能源、无污染等优点,未来有望成为氢能源的主要来源之一。
那么,电解水制氢的研究进展到底是怎么样的呢?一、电化学水制氢原理电化学水制氢,指电解水产生氢气和氧气的化学反应过程。
水的电解有两种方法:直接电解和间接电解。
1. 直接电解直接电解是指将水直接电解成氢气和氧气。
这种方法通常采用电解槽在其中放置两个电极,即阳极和阴极。
夹板水中的阴阳离子在电解过程中分别向着阴极和阳极移动。
在电解过程中,放置在阴极上的电子将水中的阳离子还原成氢气,而放置在阳极上的电子则将水中的阴离子氧化成氧气。
最终,氢气和氧气分别在两个电极上采集。
2. 间接电解间接电解法主要是将水和醇类化合物(如甲醇、乙醇等)混合,通过电氧化还原后,产生氢气和氧气。
该方法由于混合物中醇类化合物的存在,其电路贡献比电解水的电路更复杂,需要更高的电位才能开展反应,因此间接电解放电产生氢气比直接电解水消耗更多的电能。
二、电化学水制氢技术的研究进展1. 传统电解水制氢技术传统的电解水制氢技术,一般采用铂电极,在电解过程中,铂极表面会有氢气的附着形成氢化铂(Pt-H)阻碍其电势上升和促进氧还原反应附着的氧离子再生,从而帮助氧还原反应进行。
但这种方法的效率非常低,选择资料中指出该过程所需的能量成本非常高,甚至可能达到有害水平。
2. 贵金属代替技术近年来,由于铂、钯等贵金属价格昂贵,研究者对使用更加环保、经济的金属替代贵金属的方法更加关注。
新型电极材料具有较高的电催化活性和稳定性,被广泛地应用于制氢和电池等领域。
例如,钴纳米棒电极在电解水制氢时具有高的催化活性,被广泛应用;多组研究人员发现,铁基非贵金属电极对水分解具有催化作用。
电解水制氢方法

电解水制氢方法随着全球能源危机的加剧,清洁能源已经逐渐成为重要的选择。
氢作为一种纯净、无害的能源已经引起了人们的高度关注。
然而,如何将氢大规模生产成为一项着重研究的企业。
其中,电解水制氢方法成为目前最主流的一种选择。
电解水制氢方法的原理是利用电流解离水分子,得到氢气和氧气。
这里,我们来分步骤地阐述这一方法。
第一步,集氢气。
在电解水过程中,需要先准备一个集氢气的装置。
一般来说,可以利用玻璃瓶或者气球做容器,在容器底部开一个孔,接上橡胶管进行密封。
将另一端的橡胶管置于电解水中,开始电解。
电解的过程中,氢气会穿过橡胶管进入容器内,从而集中、保存在容器中。
第二步,连接电路。
连接起电解电路是制取氢气的关键之一。
电解的装置是一个简单的直流电路,由直流电源、两个带电极(阴极和阳极)、以及连接电解装置的电线组成。
将电线连接电解装置,再将电源连接至电解容器两端的两个带电极,就可以开始电解水制氢了。
第三步,电解水。
接着,需要利用电源令电解电路通电,开始电解水。
电源会将电荷分配给带正电的阳极和带负电的阴极,从而使水中的水分子发生分解,得到氢气和氧气。
电解过程中,需要注意电流大小和电解时间的掌控,以便得到预期的产量和效果。
第四步,收集氢气。
在电解过程中,氢气会在碱性电解液的作用下释放出来,溶解于水中,通过水分子的渗透逸出,穿过橡胶管进入到集氢气的容器中。
补充一点,由于电解过程同时伴随着有氧化反应的产生,也就是说在集氢气的过程中可能产生氮氧化物等杂质,因此取出氢气后要及时检测氢气是否纯净。
以上就是电解水制氢的四个步骤,当然,其中需要注意一些其他的细节问题。
例如,选择合适的电解液,保证电解液的温度等等。
但是总的来说,电解水制氢是目前比较实用的制氢方法之一,具有成本低、操作简单等优点,在未来将会得到越来越广泛的应用。
电解水制氢原理

电解水制氢原理
电解水制氢的原理是利用电解作用将水分解为氢气和氧气。
电解水的实验装置通常包括一个电解槽和两个电极,其中一个电极称为阴极,另一个电极称为阳极。
在电解水的过程中,将直流电源的正极与阳极连接,负极与阴极连接。
当通电时,阳极上的电子流向电源的负极,而阴极上的电子流向电源的正极。
这个过程称为电解。
在电解水的过程中,电解槽内的水分子受到电解的作用,发生水的电解反应。
具体来说,在阳极处发生氧气的电化学析出反应,即2H2O(液)→ O2(气)+ 4H+(液)+ 4e-;而在阴极处发生氢气的电化学析出反应,即4H+(液)+ 4e- → 2H2(气)。
因此,通过电解水,可以使水分子分解为氢气和氧气。
但需要注意的是,由于氢气具有易燃易爆的性质,制取氢气时应注意安全问题。
电解水制氢气化学方程式

电解水制氢气化学方程式
电解水制氢气是一种重要的电化学方法,主要通过电解水过程来生成氢气。
它可以通过这样的化学方程式来体现:
1、电解水:H2O(l)= H+ (aq) + OH- (aq)
2、产生还原氢气:2H+ (aq) + 2e- = H2(g)
3、产生氧化氢气:2OH- (aq) -2e- = H2O(l)
因此,电解水可以用下面的反应式表示:
H2O(l)= H2(g)+ H2O(l)
实现该反应所需要的实现电位(E),即电解槽分歧处半电位(H),必须大于1.23V。
而当处于稳定状态时,电解槽分歧处半电位(H)恒定在1.23V,正准确进行电解水。
电解水制氢期间,由于反应温度较低,反应速率较慢,这时需要相应的催化剂,如高锰酸钾、钛渣等,来加速反应的进行,以提高氢气的出口比。
此外,在电解水制氢过程中,电流的流向也是一个关键技术,一般情况下要求在电解液中的正极产生氢气,在负极产生水,这样就可以保证正反应的反应活性,同时可以有效降低水的消耗。
最后,电解水制氢气,必须保持反应室温度和湿度恒定,否则容易发生反应失灵和氢气污染等情况,而且,需要安装安全措施,以确保安全使用。
总之,电解水制氢气是一种值得推广和应用的可行的环保发电方式,既可以满足当前日益增长的能源需求,又能保护环境。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
1概述
氢能是一种二次能源,最丰富的含氢物质是水H2O,其次就是各种矿物燃料(煤、石油、天然气)及各种生物质等。
各种矿物燃料制氢,因其制氢成本较其它物质制氢成本低,是目前制氢的最主要方法。
但矿物燃料储量有限,且制氢过程会对环境造成污染。
从长远看以水为原料制取氢气是最有前途的方法,原料取之不尽,而且氢燃烧放出能量后又生成产物水,不造成环境污染。
以煤为燃料制气生产合成氨、甲醇等化工产品及生活煤气时,造气炉多以氧作为辅助气化剂。
氧气靠空分装置分离空气得到。
电解水制氢气、氧气,氧气供造气炉用,氢气作为合成气使用。
此流程能使氢、氧得到很好的使用。
2电解水制氢、氧
水分解制氢是目前应用较广且比较成熟的方法之一。
水为原料制氢过程是氢与氧燃烧生成水的逆过程,因此只要提供一定形式一定的能量,则可使水分解。
以水为原料制氢主要有:1热化学循环法、2光化学法、3电解法、4高温水热裂法制氢等。
热化学循环法制氢是利用太阳能或高温气冷堆原子能电站的热能,使反应不断循环进行,达到连续制氢的目的。
光化学制氢是以水为原料,光催化分解制取氢气的方法。
光催化过程是指含有催化剂的反应体系,在光照下由于有催化剂存在,促使水解制得氢气。
水电解制氢是一种
较为方便的方法。
在充满电解质的电解槽中通入直流电,水分子在电极上发生电化学反应,分解成氢气和氧气。
高温水热裂法制氢:将水蒸汽加热300K以上,使水分子热裂,直接分解成氢气和氧气。
水电解制氢是目前工业化制氢、氧所采用的最广泛的方法。
电解水制氢,关键是耗能问题。
以电能换氢能,成本很高。
日本开发了高温加压法,将电解水的效率提高到75%;美国建成一种SPE工业装置,能量效率达90%;我国研制了双反应器制氢工艺。
先进的PEM电解工艺,是一种可逆的电/氢转换装置,是燃料电池和产氢的电解槽的统一,总转换效率可达95%。
电解水制氢的电耗一般为4.5~5.5kwh/m3。
正在开发的新工艺有: 固体电解质电解水制氢,可简化流程,提高制氢效率和降低能耗;高温水蒸汽电解工艺,电耗可降低到3kwh/ m3。
电解水制氢气的投资成本与其规模成正比,大型碱电池制氢系统的单位投资成本一般为400-600美兀/kW,电解水的规模可以大到11万千瓦。
目前市场上的电解槽可以分为三种: (1)碱性电解槽(2) 质子交换膜电解槽(3)固体氧化物电解槽。
碱性电解槽是最早商业化的电解槽技术, 虽然其效率是三种电解槽中最低的, 但由于价格低廉, 目前仍然被广泛使用, 尤其是在大规模制氢工业中。
碱性电解槽的缺点是效率较低和使用石棉作为隔膜. 石棉具有致癌性, 很多国家已经提出要禁止石棉。
碱性电解槽中的使用。
质子交换膜电解槽由于转换
效率很高而成为很有发展前景的制氢装置. 由于采用很薄的固体电解质(PEM), 具有很好的机械强度和化学稳定性, 并且欧姆损失较小. 在日本, 效率达94.4%的质子交换膜电解槽已经研制成功 [11]. 但由于质子交换膜(目前常用的是由杜邦公司的Nafion)和使用铂电极催化剂, 价格昂贵, 制约了其广泛使用。
固体氧化物电解槽(Solid Oxide Electrolyzer)是另一种新兴的电解槽技术。
这种电解槽的缺点是工作在高温, 给材料的选择带来了一定限制. 优点是较高的反应温度使得电化学反应中,部分电能被热能代替, 从而效率较高, 尤其是当余热被汽轮机, 制冷系统等回收利用时, 系统效率可达90%。
目前三种电解槽的成本分别为: 碱性电解槽US$400-600/kW, PEM电解槽约US$2000/kW, 固体氧化物电解槽约US$1000-1500/kW。
电解水的规模可以大到11万千瓦。
考虑到投资成本及规模,本方案采用碱性电解槽。
3煤制氢、空分制氧
煤制氢是,煤为燃料,氧气、水蒸汽为气化剂,在造气炉中生成含氢、一氧化碳、甲烷、二氧化碳的粗煤气。
不同的造气炉各有优缺点。
以碎煤熔渣气化炉为例,5-40mm的煤以氧、蒸汽为气化剂,在1300-1350℃,3.0Mpa的条件下,生成的粗煤气中氢占33.4%,一氧化碳占33.5%,甲烷占7.3%。
根据生产工艺的要求,一氧化碳经变换制得到氢,甲烷经转化制得氢。
空分制氧是,空气经压缩、冷却、分离、精馏得到氧气和氮气。
4空分制氧与电解水制氧比较
4.1空分制氧
10000Nm3/(CO+H2)/h例,空分制氧供造气炉作为气化剂使用与电解水制氧供造气炉使用,氢作为合成气两方案比较如下。
空分制氧供造气炉作为气化剂使用,造气时10000Nm3/(CO+H2)/h需耗标煤6.2 t, 380V电400Kwh,低压蒸汽0.3 t,一次水10t,循环水100 t,氧2000 Nm3/(O2)。
空分生产2000 Nm3/O2需耗循环水500 t,中压蒸汽5.28 t, 6000V电32Kwh, 380V电19.2Kwh。
Ф3600mm气化炉的单炉生产(CO+H2)能力为40900Nm3/h。
造气装置投资按4千万计,运行15年,每年7200 h,每产生10000Nm3/(CO+H2)设备成本为90.56元。
25000空分装置投资按8千万计,运行15年,每年7200 h,每产生2000Nm3/O2设备成本为59.26元。
标煤按250元计,电价按0.25元计,循环水0.08元/ m3,一次水0.16元/ m3,中压蒸汽45元/ t,低压蒸汽38元/ t。
表一:煤制气造气成本估算(10000Nm3/CO+H2/h)
表二:空分生产2000Nm3/O2成本估算
含10000Nm3/(CO+H2)的粗煤气,经变换、净化成合成气的成本按300元考虑。
表三:空分制氧供煤制气,净化得到氢的成本估算:
4.2电解水制氧
电解水制氢设备成本按3850元/KW计,1 Nm3/H2用电5KW,产生2000Nm3/O2,同时产生4000Nm3/H2。
产生4000 Nm3/H2,装置投资7.7千万,每产生4000 Nm3/H2,设备拆旧费713元。
电价按0.25元计。
电解水制氢、氧成本估算(2000Nm3/O2、4000Nm3/H2)
表四:电解水制2000Nm3/O2、4000Nm3/H2成本估算
5小结
当电费0.25元时,电解水产生2000Nm3/O2、4000Nm3/H2,时费用5725.8元。
空分生产2000Nm3/O2成本349.66元,煤制气产生4000Nm3/H2成本824.64元,共计成本1174.3。
当电费为0.25元时电解水产生氢、氧的成本是煤制气的4.88倍。
当电费为X时,用电解水制氢、氧,氧气供造气炉中使用,氢气并入合成气中,用此流程产生14000 Nm3/H2成本是:
20000X+12.8+713+1761.6+300=20000X+2787.4
当电费为X时,空分制氧, 氧气供造气炉中使用,用此流程产生14000 Nm3/H2成本是:
(2411.2-112.8+451.2X)×1.4=3217.8+631.7X
当上述两种流程成本相当时:
20000X+2787.4=3217.8+631.7X
X=0.022
用现有的生产工艺,当电费低至0.022元时, 用电解水制氢、氧,氧气供造气炉中使用,氢气并入合成气中流程,与空分制氧, 氧气供
造气炉中使用流程生产成本相当。
考虑到现有的新工艺,电解效率从75%提到95%,电耗降至3kwh/ m3。
鞍山市水电解制氢项目组的技术人员研制出的制氢装置电耗低至2.51kwh/ m3。
当材料技术的发展,电解设备的成本进一步降,电解水制氢、氧,氧气供造气炉中使用,氢气并入合成气的方案是可行的。
