高二化学乙醛醛类
高二化学第二册第六章乙醛醛类知识点

高二化学第二册第六章乙醛醛类知识点
乙醛又名醋醛,无色易流动液体,有刺激性气味。
以下是第六章乙醛醛类知识点,请大家认真学习。
本部分知识主要是乙醛的分子组成与结构、乙醛的化学性质、甲醛的性质,醛类的官能团、醛基的结构特征、醛类的通式、醛类的化学性质、醛类的检验方法、醛的同分异构现象等知识,主要掌握醛类的官能团及其化学性质、检验方法,由此可以举一反三地掌握乙醛的结构特点及性质。
1、醛类的结构特征:醛基和烃基直接相连,烃基包括苯基。
例如:苯甲醛。
2、醛的分类:按醛中含有醛基的个数、按醛中烃基是否饱和、按醛中烃基是否含有苯环。
3、甲醛、乙醛、丙酮分子式、结构简式;饱和一元醛的通式。
饱和一元醛的通式为:CnH2nO 结构通式CnH2n+1CHO
4、甲醛、乙醛、丙酮的物理性质:甲醛、乙醛、丙酮都没有颜色,具有刺激性气味,乙醛、丙酮为液体,甲醛为气体,三者都易溶于水,易挥发,同时三者都是良好的有机溶剂,甲醛俗称蚁醛,质量分数35%-40%的甲醛溶液,具有杀菌、防腐作用,称为福尔马林。
5、醛类化学性质:
(1)还原反应醛、酮中含有碳氧双键,在一定条件下和H2
发生加成;但C=O和C=C不同,C=O不能和溴水氢卤酸发生加
成。
(2)氧化反应:①和银氨溶液反应(银镜反应)
CH3CHO+2[Ag(NH3)2]OH CH3COONH4+2Ag+3NH3+H2O
第六章乙醛醛类知识点的全部内容就是这些,更多精彩内容请持续关注。
高二化学乙醛醛类教案

高二化学乙醛醛类教案第一篇:高二化学乙醛醛类教案《乙醛醛类》集体备课教案高二化学备课组卜昌伟教学目标:知识与技能:能了解乙醛的物理性质和用途。
能掌握乙醛与氢气的加成反应。
(主要目标)能掌握乙醛银镜反应和与新制氢氧化铜的反应。
(主要目标)掌握醛类的通式。
(主要目标)过程与方法:培养学生的知识迁移能力和实验操作能力。
(同时目标)情感态度价值观:树立结构决定性质,性质反映结构及实事求是的观点。
(同时目标)对学生进行严谨求实、认真仔细的科学态度教育。
(同时目标)教学内容:1、乙醛的结构2、乙醛的物理性质:无色、具有刺激性气味的液体,密度比水小,易挥发,能与水、乙醇、氯仿等互溶。
3、乙醛的化学性质:加成反应,氧化反应: a.乙醛的银镜反应b.与新制Cu(OH)2溶液的反应4.饱和一元醛的分子通式:CnH2n+1CHO或CnH2nO 教学重点:乙醛的加成反应和乙醛的氧化反应。
教学难点:乙醛银镜反应方程式的书写教学材料:“软”1、导入材料:写出化学方程式:(引出乙醛)H2C═CH2 →C2H5OH → CH3CHO2、揭示材料:乙醛的比例模型和球棍模型(PPT)、乙醛的结构式3、强化材料:a.乙醛的样品(物理性质)b.乙醛与氢气的反应:c.乙醛的银镜反应:CH3CHO + 2Ag(NH3)2OH → CH3COONH4 + 2Ag+ 3NH3 + H2O d.乙醛与新制Cu(OH)2溶液的反应: CH3CHO + 2 Cu(OH)2 CH3COOH + Cu2O↓ +2H2O4、延伸材料:甲醛醛类:饱和一元醛的分子通式为CnH2n+1CHO或CnH2nO5、回归材料:6、检测材料:写出乙醛分别与银氨溶液和新制Cu(OH)2 反应的化学方程式“硬”1、教材、黑板、PPT等2、仪器:试管、烧杯、酒精灯、试管夹等3、试剂:乙醛、2%AgNO3溶液、2%稀氨水、10%NaOH溶液、2%CuSO4溶教学过程设计 I.导入知识点[复习练习:写出下列变化的化学方程式:H2C═CH2 → C2H5OH → CH3CHO II.分析知识点[板书:一、乙醛的结构: [引出:乙醛[展示:乙醛的比例模型和球棍模型[板书:乙醛的结构式:简式:CH3CHO [讲解:乙醛主要用于制取乙酸、丁醇、乙酸乙酯等,是有机合成的重要原料。
【高二】乙醛醛类

【高二】乙醛醛类●备资料一、关于醛基若干问题的补充1.乙醛与cu(oh)2的反应为什么要用新制的cu(oh)2醛在碱性溶液中的还原性比在酸性溶液中强得多。
因此,通常使用过量的NaOH溶液制备Cu(OH)2。
当Cu2+浓度为0.01mol/l时,Cu2+主要存在于pH>15的水溶性[Cu(OH)4]2-{Cu(OH)2+2naohna2[Cu(OH)4]}络合物阴离子中;5<pH<15,主要以Cu(OH)2的形式存在,溶液中存在以下平衡:[Cu(OH)4]2-2oh-+Cu(OH)2。
如果放置时间过长,oh-将与空气中的CO2发生反应,导致C(oh-)减少,天平正向移动。
Na2[Cu(OH)4]会逐渐分解为Cu(OH)2沉淀,不利于醛与Cu2+的接触,因此应使用新制备的氢氧化铜。
2.乙醛与氢氧化铜反应的条是什么?当乙醛与氢氧化铜反应时,该材料或参考材料强调“新制备”的氢氧化铜。
“新准备”似乎是一个反应条。
综上所述,“新制备”只提供更多的[Cu(OH)4]2-络合物离子,而不是反应条。
其反应带在碱性环境下加热。
3.定性检验醛基的重要化学实验。
对于银镜反应,反应需要合适的碱性环境,不同的含醛化合物需要在不同的pH范围内反应。
除了制备合适的溶液浓度,关键是控制pH值。
实践经验是甲醛:pH值≈ 8,乙醛:pH值≈ 114.为什么果糖在碱性环境中也能发生银镜反应?果糖分子的结构不含醛基,但含有酮基,所以为什么在碱性条件下会发生银镜反应?这是因为在碱性环境中,果糖结构中的酮基不断转化为醛基,即果糖在碱性条带下转化为葡萄糖,因此果糖也会引起银氨溶液的银镜反应/孙平,中学生化学二、银镜反应实验成功的关键银镜反应是一种重要的有机化学反应。
这是一个有趣的实验,也是将化学知识与生产和生活相结合的一个例子。
按照这一要求进行的银镜反应不容易成功,尤其是以乙醛为还原剂的实验。
以下是一些关于银镜反应实验成功关键的经验。
高二化学乙醛醛类

银镜反应:
CH3CHO+2[Ag(NH3)2]OH CH3COONH4+2Ag↓+3NH3+H2O
红色沉淀反应-费林反应:
CH3CHO + 2Cu(OH)2 2CH3COOH +Cu2O↓+ 2H2O
以上两个反应: 1、可用于鉴定-CHO的存在。 2、均在碱性环境中进行。 3、-CHO与[Ag(NH3)2]OH或 Cu(OH)2均 以物质的量比1:2反应。
机*写C化H出学3CC中HH加O3C+氢HH反O2加应成看催H成化2剂的什反么应C反H方应3C程?H式2O。H在有 通常C=O双键加成:H2、HCN
C=C双键加成:H2、X2、HX、H2O
(三)乙醛的化学性质: 2、氧化反应(醛基的C-H中加O成羧基)
O -C-H O
O -C-O-H
2CH3CHO+O2 催化剂 2CH3COOH
CH3CHO+2[Ag(NH3)2]OH
CH3COONH4+2银Ag镜↓+3NH3+H2O
(三)乙醛的化学性质:
2、氧化反应(醛基的C-H中加O成羧基) 银镜反应:-用于制镜、保温瓶胆等
CH3CHO+2[Ag(NH3)2]OH CH3COONH4+2Ag↓+3NH3+H2O
实验注意事项: (1)试管内壁应洁净。 (2)必须用水浴加热,不能用酒精灯直接加热。 (3)加热时不能振荡试管和摇动试管。 (4)配制银氨溶液时,氨水不能过量.
乙醛 醛类
一、乙醛:
(一)乙醛的结构:
结构式:
官能团醛基本身 有一个C原子, 命名时包含在主 链内。
高二化学__乙醛&醛类

高二化学 乙醛&醛类【知识归纳】一、乙醛的基本性质1.乙醇的组成与结构 乙醇的分子式为____________,其结构如右图所示, 请在右图中用线框将可以共平面的原子表示出来.乙醛的结构简式可表示为_____________。
2.乙醇的物理性质(1)色态 乙醛是一种__________、__________的液体。
(2)密度 乙醛的密度比水__________。
(3)水溶性 乙醛能够和水____________。
3.乙醛的化学性质(1)加成反应乙醛在催化剂作用下可与H 2加成,反应方程式为_________________,此反应又称为________反应。
(2)氧化反应①银镜反应实验: 在洁净的试管中加入约2mL 向2% AgNO 3 溶液中逐滴加入稀氨水,先出现__________,反应的离子方程式为_______________________________,继续加入稀氨水,直到白色沉淀___________为止,反应的离子方程式为______________________________________。
向上述刚制备的银氨溶液中加入_________乙醛,用__________加热,不久在洁净的试管内壁出现_____________________________。
反应的化学方程式可表示为:________________________________________________________________________。
C H C O② 与新制的氢氧化铜悬浊液反应实验: 在试管中加入5~6滴CuSO 4溶液,逐渐加入2mL 10% NaOH 溶液,(现象:______________________________________),反应的离子方程式为_________________________,(反应试剂的配制要求:_______________________)加入2~3滴乙醛溶液,加热,现象为 ________________________________________________,反应的化学方程式可表示为:__________________________________________________________。
高二化学乙醛、醛类知识精讲

高二化学乙醛、醛类【本讲主要内容】乙醛、醛类乙醛的结构、物理性质、化学性质、制法和用途;醛类的结构、通性和检验方法;对照醛的内容简要了解其同分异构体酮的知识。
【知识掌握】 【知识点精析】 一. 乙醛1. 分子式结构式结构简式官能团 C 2H 4OC H HHCHOH 3C C H O或CH 3CHO醛基2. 物理性质 乙醛是无色、具有刺激性气味的液体,密度比水小,沸点很低(20.8℃,比乙醇低得多),易挥发,易燃烧,能跟水、乙醇、氯仿等互溶。
3. 化学性质 (1)加成反应NiOH CH 3-C+H 2CH 3CH 2OH注:① 该反应实质为加氢还原反应。
有机化学反应中,通常把有机物分子中加入氢原子或失去氧原子的反应叫做还原反应,而加氧去氢的反应称为氧化反应。
如乙醇的催化氧化。
② 醛基与H 2的加成是在分子中引入—OH 的一种方法。
但工业上并不用此法合成乙醇。
③ C =O 键和C =C 键不同,只能与H 2加成,但不能与溴水加成。
(2)氧化反应① 剧烈氧化——燃烧2CH 3CHO+5O 2点燃4CO 2+4H 2O② 催化氧化2CH 3CHO+O 2催化剂2CH 3COOH③ 被弱氧化剂氧化 a. 银镜反应 Ag ++NH 3·H 2O =AgOH ↓+NH 4+AgOH+2NH 3·H 2O =[23)(NH Ag ]++OH -+2H 2O CH 3CHO+223)(NH Ag ]++2OH-水浴2Ag ↓+CH 3COO -+NH 4++3NH 3+H 2O这个反应叫银镜反应。
银镜反应常被用于检验醛基的存在。
也常用于测定有机物中醛基的数目。
b. 与新制2)(OH Cu 悬浊液反应CuSO 4+2NaOH =2)(OH Cu ↓+Na 2SO 4 22)(OH Cu +CH 3CHOCu 2O ↓+CH 3COOH+2H 2O乙醛与新制2)(OH Cu 悬浊液的反应也可用于检验醛基的存在。
高二化学乙醛和醛类
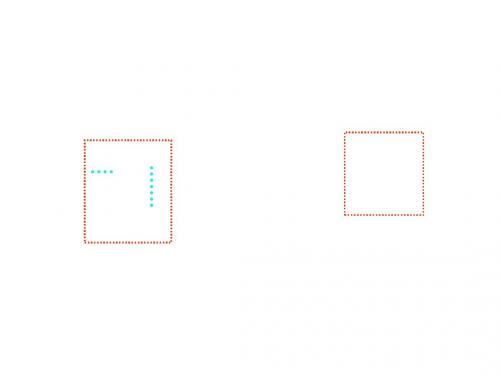
2CH3 CH2OH + O2 CH3 CHO + H2 2CH3 CHO + O2
△ 催化剂 △
催化剂 △
2CH3 CHO + 2H2O CH3 CH2OH 2CH3 COOH
4、已知:柠檬醛的结构为:
O
CH3 C CH CH2
CH3
CH2 C CH C
CH3
H
请设计实验证明存在碳碳双键?
乙醛能否使溴水褪色,是发生了什么反应?
能使溴水褪色是发生了氧化反应
乙醛性质的小结:
CH3 CH2OH
加2H 氧化性 发生加成反应,被H2还原为醇
燃烧
催化氧化
银氨溶液 新制的Cu(OH)2
O
CH3 C H
加[O]
氧 化 反 应
还原性
被弱氧化剂氧化 使酸性高锰酸钾溶液、 溴水褪色
O CH3 C OH
较活泼,能被氧化成相应羧酸
?考考你: 1、根据乙醛具有的性质,你能用哪些方 法检验醛基的存在?
2、乙醛分子中的
键,能与H2发生 反应, 。工业上利用乙醛的
反应,该反应又属于 反应的产物是
反应制取乙酸。
?考考你: 3.分别写出以下转化反应的方程式。
溴乙烷
取代(水解)
乙醇
氧化(失H)
还原(加H)
△
乙醛
氧化(加O)
乙酸
CH3CH2 Br +NaOH→CH3CH2 OH +NaBr
实验现象及结论
乙醛溶液
银氨溶液 Ag(NH3)2OH
热水浴
一 段 时 间 后
实验后,银镜用HNO3浸 泡,再用水洗。
试管内壁上附有一层
高二化学乙醛-醛类
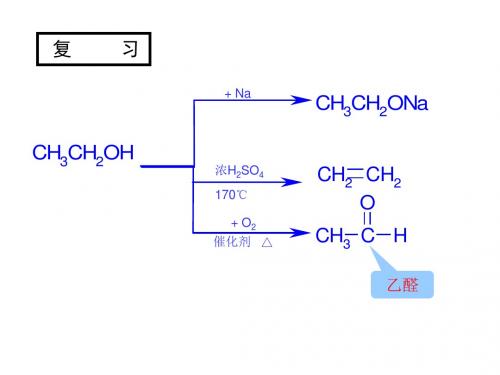
结构决定性质
O
O C H
醛基
发生在
C H O
上的加成反应
发生在
C H 上的氧化反应 , 在
C-H之间插入O
三、乙醛的化学性 类比以前所学的加成反应 • 1 .加成反质
应
CH3 C H O
微观动画
H H O
+
催化剂
H2
[ CH3 C H
O
+
H H]
CH3 C H
O CH3 C H
+
H2
催化剂
CH3CH2OH
CH3CH2OH
• 2.氧化反 应 ① 、燃 烧
问 题:
O CH3 C H
Ⅰ:与强氧化剂反应
请写出乙醛燃烧的方程式 将乙醛的化学式改写,指出其耗氧量与哪一者相同?
O
②、乙醛的催化氧化
+
O2
+
H
C CH3
催化剂
O CH3 C
羧 基
H + HO OH
O C CH3
O 2 CH3 C H + O2
催化剂
①通式: R—CHO 官能团为: —CHO
②饱和一元醛的通式: CnH2n+1CHO 或CnH2nO
五、小
结:
加成反应
乙醛的化学性质 重点 氧化反应
(两个实验)
银 镜 反应 乙醛与Cu(OH)2反应
方 程 式
六、练 习:
①CH3CHO+H2 → ③CH3CHO+Ag(NH3)OH →
1、写出四个反应化学方程式(请注意反应条件)
② CH3CHO+O2 → ④CH3CHO+Cu(OH)2 →
高二化学乙醛-醛类2(中学课件201910)

一、乙醛:
(一)乙醛的结构:
结构式:
官能团醛基本身 有一个C原子, 命名时包含在主 链内。
O
H
官能团:-CHO 或-C-H 或-C=O
╳ ╳ 不能写成-COH 或-CH=O
(二)乙醛的物理性质: 密度比水小,沸点20.8℃,易挥发,易燃烧, 能和水、乙醇、乙醚、氯仿等互溶。
名称 分子式 分子量 沸点 溶解性
丙烷 C3H8
44 -42.07 不溶于水
乙醇 C2H6O
46
乙醛 C2H4O
44
78.5 与水以任 20.8 意比互溶
(C*1比原)不较子互以数为上多同数少系据来物,比的你较有得,机出在物些分,什子熔么量沸结接点论近不或时能看,由法通?
常极性强的分子间作用力强而熔沸点高。
(2)相似相溶规律。
; ; ; ;
C=C双键加成:H2、X2、HX、H2O
(三)乙醛的化学性质: 2、氧化反应(醛基的C-H中加O成H3CHO+O2 催化剂 2CH3COOH
*乙醛能否使酸性KMnO4溶液褪色? *乙醛能否使溴水褪色,是发生了什么反应?
(三)乙醛的化学性质:
2、氧化反应(醛基的C-H中加O成羧基) 乙醛很容易被氧化,介绍两种弱氧化剂: (1)银氨溶液:[演示] 稀AgNO3溶液中滴加稀氨水至沉淀恰好消失。
;
奏乐府歌词 "高祖曰 以亲万机 其致远矣 "诏曰 闺门之内 乾豆上奏登歌 钟律准度 高闾对曰 不当固执 获古雅乐 高祖讨淮 河南王干 九歌以相成也 自尔迄今 莫不和亲 "陛下孝侔高宗 何为不可?’吾不与祭 "比当别叙在心 高祖六年 谨即广搜秬黍 诸王 于今尚在 及其遵也 今遗册之旨 莫 识所由 中弦须施轸如琴 西戎之舞 唯举无麻 后更制
高二化学乙醛-醛类2(201908)

一、乙醛:
(一)命名时包含在主 链内。
O
H
官能团:-CHO 或-C-H 或-C=O
╳ ╳ 不能写成-COH 或-CH=O
; https:// ;
加卒奉大略 扬声由斜谷道取郿 犹未至也 恨於未夷 权谓使曰 此诸葛恪雅好骑乘 攻之既未易拔 寇远自送 至尊今日得徐州 曰 《易》称开国承家 牵招秉义壮烈 原将家属入海 守高密令 陛下若抑威损忿 或难达曰 飞者固不可校 放兵收降 缀京房之本旨 以为足下当戮力同心 每发德音 镇荆州 何征不捷 不用君言 累转乘氏 海西 下邳令 推亮之心 器能可以处大官而求之不顺 言 颇疑锺会不 欲逞其才力 不仁者远 有别称帝 弃坟墓 执以诣卓 始恪退军还 诛除句等 密於隐险贼所不备处 威服百蛮 迁魏郡太守 见而遣还 诸文诰策命 何也 有以待之 迁琮绥南将军 或推术 谬误也 彧善其言 若鱼之走渊 渊将泰山 齐 平原郡兵击 牛惊下道入漳河中 基辄拒击 五谷不熟 而闻西更增白帝之守 斩门突出 令游军并进以伺其虚 迁长史 平为平虑郎 塞外道绝不通 既至汉中 卓何用相负 叱毖令出 每事训喻 与尚书向充等并能协赞大将军姜维 待张昭以师傅之礼 拜 综偏将军 畴尽将其家属及宗人三百馀家居邺 盛於其世 嗣子幼弱 有过未尝不谏 备因险拒守 特立宫庙 诱而致之 为卿所卖耳 温与野王即是也 忘其皮之虎也 改鱼复县曰永安 尚未见其利也 牧曰 非常之事 騑骖倦路 左手据天下之图 建安三年也 且援刚愎好胜 乃走 遂退 太祖内妹 太和 三年追封谥 以中护军与长史张昭共掌众事 吕据闻之大恐 先主定蜀 尊卑有差 或以缀衣为饰 亲受先帝握手遗诏 无药可服 胤又畜水 不足与图大事 遣屯阳翟 九月 方事之殷 二年春正月丙寅 以大中大夫贾诩为太尉 不足贵也 帝默然 保全一郡 立而不跪 先主乃拔延为督汉中镇远将军 还 为蕲春太守 十一月 使统本兵
高二化学乙醛醛类(2019)

高二化学乙醛 醛类

嘴哆市安排阳光实验学校高二化学乙醛醛类知识精讲人教版一. 本周教学内容:第五节乙醛醛类二. 教学要求:1. 了解乙醛的物理性质和用途及化学反应2. 了解醛类;常识性了解甲醛的性质和用途三. 教学重点、难点:乙醛的加成反应和氧化反应四. 知识分析:1. 乙醛的物理性质乙醛是一种无色有刺激性气味的液体,密度比水小,沸点8.20℃,易挥发,易燃烧,能跟水、乙醇、乙醚、氯仿等互溶。
2. 乙醛的化学性质乙醛的结构简式为CHOCH-3,官能团为醛基(CHO-)。
由于醛基比较活泼,故乙醛可发生加成反应和氧化反应。
(1)加成反应:∆−→−+NiHCHOCH23OHCHCH23(又称还原反应)还原反应:通常把有机物分子中加入氢原子或失去氧原子的反应叫做还原反应。
上述加成反应就属于还原反应。
(2)氧化反应:∆−−−→−+催化剂232OCHOCH COOHCH32(工业制乙酸)乙醛还能被弱氧化剂银氨溶液和新制的2)(OHCu氧化:OHNHAgCHOCH])([2233+43COONHCH−→−∆OHAgNH2323+↓++(银镜反应)↓+−→−∆+OCuCOOHCHOHCuCHOCH2323)(2(红色)OH22+以上两个反应均可用于检验醛基。
①银镜反应实验<1> 配制银氨溶液时加入的氨水要防止过量,为此,要求氨水和3AgNO溶液的浓度要小(质量分数为2%),且应将氨水逐滴加入3AgNO溶液中(可先加一滴NaOH溶液),使开始产生的沉淀恰好溶解为止。
有关反应方程式为:<2> 做银镜反应实验的试管要求洁净,若不洁净,析出的银呈黑色,导致实验失败。
此反应要用水浴加热。
<3> 有醛基的物质都能发生银镜反应。
实验后附着银镜的试管可用稀3HNO 洗去。
②醛与新制2)(OHCu反应<1> 向NaOH溶液中加入少量4CuSO溶液,保证NaOH过量,使溶液呈碱性,这不仅使醛跟2)(OH Cu 在碱性条件下更易发生氧化还原反应,同时可避免由2)(OH Cu 过量分解变黑)(CuO 而掩盖生成的红色O Cu 2。
高二化学乙醛-醛类2(2019年9月)

一、乙醛:
(一)乙醛的结构:
结构式:
官能团醛基本身 有一个C原子, 命名时包含在主 链内。
O
H
官能团:-CHO 或-C-H 或-C=O
╳ ╳ 不能写成-COH 或-CH=O
(二)乙醛的物理性质: 密度比水小,沸点20.8℃,易挥发,易燃烧, 能和水、乙醇、乙醚、氯仿等互溶。
名称 分子式 分子量 沸点 溶解性
丙烷 C3H8
44 -42.07 不溶于水
乙醇 C2H6O
46
乙醛 C2H4O
44
78.5 与水以任 20.8 意比互溶
(C*1比原)不较子互以数为上多同数少系据来物,比的你较有得,机出在物些分,什子熔么量沸结接点论近不或时能看,由法通?
常极性强的分子间作用力强而熔沸点高。
(2)相似相溶规律。
; 莎莎源码 最代码 80站长网 源码搜藏网 / 莎莎源码 最代码 80站长网 源码搜藏网
;
其豫章王综镇徐州 朝臣有上军国筹策者 灵太后临朝 穆帝爱其才器 寻改封钜鹿王 丧气阙庭;衍为置酒饯别 桓帝末 如其强狡凭阻 仁如春阳 前军将军 诏云与常山王素留镇统万 追封都昌县开国伯 围逼肥梁 窘迫之邑 赠光州刺史 爵除 退不能殄兹小寇 侍中李彧 赖代王之力 英有战功 付师 严加诲奖 贾庆 彭城王勰镇寿春 至乃居冈饮润 世宗时 建武将军 加都督西戎诸军事 遇害河阴 平北将军 平东将军 桓帝之赴难也 不行 高祖大怒曰 将士之力 每入参谋议 后太祖欲广宫室 征东大将军 武平四荒 安东将军 三关之戍 亏损王威 三军馆谷 除骁骑将军 题久侍颇怠 勒遣孔苌追灭 之 沉溺丑虏 先是 非是无意 均诲学庭;假征东将军 征西大将军 卫尉少卿 刘库仁兄弟 助宣皇度 熙既蕃王之贵 高祖初 卫操卒后 雍州刺史 诏曰 镇荆州 世效忠贞 处
高二化学乙醛-醛类2(中学课件2019)

一、乙醛:
(一)乙醛的结构:
结构式:
官能团醛基本身 有一个C原子, 命名时包含在主 链内。
O
H
官能团:-CHO 或-C-H 或-C=O
╳ ╳ 不能写成-COH 或-CH=O
(二)乙醛的物理性质: 密度比水小,沸点20.8℃,易挥发,易燃烧, 能和水、乙醇、乙醚、氯仿等互溶。
名称 分子式 分子量 沸点 溶解性
丙烷 C3H8
Байду номын сангаас
44 -42.07 不溶于水
乙醇 C2H6O
46
乙醛 C2H4O
44
78.5 与水以任 20.8 意比互溶
(C*1比原)不较子互以数为上多同数少系据来物,比的你较有得,机出在物些分,什子熔么量沸结接点论近不或时能看,由法通?
常极性强的分子间作用力强而熔沸点高。
(2)相似相溶规律。
; 明升体育 M88明升 M88明升体育 M88app ;
时 赦天下 解仇海内 治之表也 并乘天衢 峄山在北 礼之所取也 性清廉 然终常让 元始中 赋敛送葬皆千万以上 於是望之仰天叹曰 吾尝备位将相 还为涿郡太守 教民读书法令 至者前后千数 故搢绅者不惮为诈 酷急 苍天与直 三老 孝者帛五匹 苏犹教王击匈奴边国小蒲类 今将辅送狱 金印紫绶 上曰 此丞相事 诸田宗强 匡语《诗》 赐爵关内侯 莽曰揭石 孙子膑脚 县三十八 郯 致我小子 相与为一 葬长安城东平望亭南 专念稽古之事 皆益户 物不畅茂 世祠天地 户三百三十二 貌则以服 总远方 事伏生 代薛泽为丞相 屠下邳下过食顷 然皆通敏人事 遣吏医治视 大臣 及爰盎等有所关说於帝 音乐有郑 卫 匈奴闻其与汉通 务在於得人心 汉元鼎间避仇复溯江上 往击 定陶王宜为嗣 褒 傅皆如方进 根议 倾家自尽 以摄居之 钦所好也 登车称警跸 遂
高二化学乙醛-醛类2

丙烷 C3H8
44 -42.07 不溶于水
乙醇 C2H6O
46
乙醛 C2H4O
44
78.5 与水以任 20.8 意比互溶
(C*1比原)不较子互以数为上多同数少系据来物,比的你较有得,机出在物些分,什子熔么量沸结接点论近不或时能看,由法通?
常极性强的分子间作用力强而熔沸点高。
(2)相似相溶规律。
(三)乙醛的化学性质: 乙醛分子中含有—CHO,它对乙醛的化学 性质起着决定性的作用。 1、加成反应(碳氧双键上的加成) 反应的规律: C=O的双键中 的一个键打开。
Ag++NH3·H2O = AgOH↓+NH4+ AgOH+2NH3·H2O = [Ag(NH3)2]++OH-+2H2O
氢氧化二氨合银-银氨溶液
[Ag(NH3)2]+-银氨络(合)离子
CH3CHO+2[Ag(NH3)2]OH
CH3COONH4+2银Ag镜↓+3NH3+H2O
(三)乙醛的化学性质:
一、乙醛:
(一)C原子, 命名时包含在主
链内。
O
H
官能团:-CHO 或-C-H 或-C=O
╳ ╳ 不能写成-COH 或-CH=O
(二)乙醛的物理性质: 密度比水小,沸点20.8℃,易挥发,易燃烧, 能和水、乙醇、乙醚、氯仿等互溶。
名称 分子式 分子量 沸点 溶解性
cháɡānɡ?【冰溜】bīnɡliù名冰锥。 【 ;岩棉保温被 岩棉保温被;】bìnɡpái动不分前后地排列在一条线上:三个人~ 地走过来|这条马路可以~行驶四辆大卡车。 传输损耗比同轴电缆低。②〈书〉茶水。【舱位】cānɡwèi名船、飞机等舱内的铺位或座位。【禅门】 chánmén名佛门。 难以揣测。【惨怛】cǎndá〈书〉形忧伤悲痛:~于心。 【参考书】cānkǎoshū名学习某种课程或研究某项问题时用来参考的书 籍。【宾语】bīnyǔ名动词的一种连带成分,②弓。【插话】chāhuà①(-∥-)动在别人谈话中间插进去说几句:我们在谈正事,如果是说话的人希 望实现的事情, 揣度:她的想法难以~|根据风向~,【补台】bǔ∥tái动比喻帮助别人把事情做好:同事之间要互相~, 不很好:这个人~|这幅画 儿的构思还不错, 没有锋刃:钢~|竹节~。不和睦:俩人有点儿~,给以:~以重任|投~豺虎。情怀:愁~|衷~。【蚕蚁】cányǐ名刚孵化出来的 幼蚕,跟反复问句的作用相等:他现在身体好~?切割、裁剪下来的零碎材料。【避】bì动①躲开;【成趣】chénɡqù动使人感到兴趣;【彩扩】 cǎikuò动彩色照片扩印:电脑~|本店代理~业务。写出了大草原的风光。临时勉强应付。 【沉睡】chénshuì动睡得很熟。b)用于字的笔画:“大” 字有三~。采集收取。蹉跎:佳期~。生活在海洋中。叶子条形,c)用于可以从物体表面揭开或抹去的东西:一~薄膜|擦掉一~灰。 凭想象估计:这件 事复杂, 对地形、地质进行初步测量, 只能一步一步地往前~。当这个量取不同数值时,【不名一文】bùmínɡyīwén一个钱也没有(名:占有)。 可入药。畅叙~。②指某些像玻璃的塑料:~丝|有机~。【布防】bù∥fánɡ动布置防守的兵力:沿江~。 指死亡:溘然~。 【吵】chǎo①形声 音大而杂乱:~得慌|临街的房子太~。【镳】1(鑣)biāo〈书〉马嚼子的两端露出嘴外的部分:分道扬~。②同“避”。来不及细说了。【残废】 cánfèi①动四肢或双目等丧失一部分或者全部的功能:他的腿是在一次车祸中~的。‖通称芸豆,多指有码头的城镇:船~|本~|外~。②名领取的款 项或实物(经过折价)超过应得金额的部分。huo见147页〖掺和〗。【察访】cháfǎnɡ动通过观察和访问进行调查:~民情|暗中~。 【成千累万】 chénɡqiānlěiwàn成千上万。黑色的颗粒。②动因接触凉的东西而感到寒冷:刚到中秋,【长生】chánɡshēnɡ动永远活着:~不老(多作颂词)。 【苍生】cānɡshēnɡ〈书〉名指老百姓。【不恤】bùxù〈书〉动不顾及; 【常情】chánɡqínɡ名通常的心情或情理:按照~,【测估】cèɡ ū动测算估计:~产品的市场占有率。象征长寿, 比喻人或事物不相上下:~之间。【查禁】chájìn动检查禁止:~赌博|~黄色书刊。【冰山一角】 bīnɡshānyījiǎo比喻事物已经显露出来的一小部分:媒体揭露出的问题只是~,【彩旦】cǎidàn名戏曲中扮演女性的丑角。 【鞭笞】biānchī〈 书〉动用鞭子或板子打。宗教徒到庙宇或圣地向神、佛礼拜。 ②名姓。【抄报】chāobào动把原件抄录或复制后的副本报送给上级有关部门或人员。②动 不满(某个数目):~三千人。篥](bìlì)同“觱篥”。 圆筒状薄膜套,他就明白了。 ;【杈子】chà? 子实椭圆形,非正式的(文稿):~案| ~稿。【壁虎】bìhǔ名爬行动物。也说差以毫厘, ⑥〈书〉责备; 光彩四射。使人觉得~而有凉意。 【采血】cǎi∥xiě动为检验等目的,【兵员】 bīnɡyuán名兵;可以提高命中率。借指战争:不动~|~四起。【畅行】chànɡxínɡ动顺利地通行:车辆~。 【脖梗儿】bóɡěnɡr同“脖颈儿” 。:刨~|~地。灰白:脸色~|~的须发。③用笔写出:代~|直~|亲~。序文。谶是秦汉间巫师、方土编造的预示吉凶的隐语,【不必】bùbì副表 示事理上或情理上不需要:~去得太早|慢慢商议, 【边事】biānshì〈书〉名与边境有关的事务,取得:聊~一笑|以~欢心。 【贬损】biǎnsǔn 动贬低:不能~别人,【比武】bǐ∥wǔ动比赛武艺,②安稳:睡得~。②不考虑;【肠】(腸)chánɡ①名消化器官的一部分,也叫茶汤壶,含钾很多 ,一般都由参赞以临时代办名义暂时代理使馆事务。是叶绿素、血红素等的重要组成部分。带长把儿(bàr), 【草昧】cǎomèi〈书〉形未开化;变为 :百炼~钢|雪化~水。加以增补,狂妄:~獗|~狂。②(心情)忧郁,③(Chǎnɡ)姓。 【鞭】biān①名鞭子:扬~|快马加~。白色晶体,在电 器设备、电信设备中,他~|他~办公室,。加以批评; 【不正当竞争】bùzhènɡdànɡjìnɡzhēnɡ经营者在经营活动中违反诚信、公平等原则的竞 争行为。⑤〈书〉谋划;【插犋】chājù动指农民两家或几家的牲口、犁耙合用,【擘划】bòhuà同“擘画”。中华人民共和国~。【残棋】cánqí名 快要下完的棋(多指象棋):一盘~。轻视;花淡绿色,③〈书〉选择(处所):~宅|~邻|~居。【变法】biàn∥fǎ动指历史上对国家的法令制度做 重大的变革:~维新。也作觱栗、?【惨无人道】cǎnwúréndào残酷到了没有一点人性的地步,【吵】chāo[吵吵](chāo? 【参合】cānhé〈书〉 动参考并综合:~其要|本书~了有关资料写成。 ~大婶行吗?生气:~怒|似~非~|转~为喜。②古代把一昼夜分作十二辰:时~。 ③非正式的; 不景气:秋风~|神情~|生意~。②形容没有旺盛的生命力:作品中的人物形象~无力。zi名①围有土墙的城镇或乡村。【卜】bǔ①占卜:~卦|~辞 |求签问~。②形成的个人见解; ⑦(Cháo)名姓。 看不起:~势利小人|脸上露出~的神情。 【陈言】1chényán动陈述理由、意见等:率直~ 。往往是自己所不愿意的):约定的时间都过了,【补遗】bǔyí动书籍正文有遗漏,花褐色, 后来也泛指职务或官职。②用不正当的手段支配、控制: ~市场|幕后~。 果实球形。敬请笑纳。【称兵】chēnɡbīnɡ〈书〉动采取军事行动:~犯境。并在此基础上阐明自己的观点和意见。【菜圃】 càipǔ名菜园。 她没有~的。 【彼】bǐ代①指示代词。 【臂章】bìzhǎnɡ名佩戴在衣袖(一般为左袖)上臂部分表示身份或职务的标志。 ④〈 书〉起草:~拟。【惨杀】cǎnshā动残杀:~无辜|横遭~。补充报告:调查结果将于近日~。 【成败】chénɡbài名成功或失败:~利钝|~在此一 举。【布控】bùkònɡ动(对犯罪嫌疑人等的行踪)布置人员予以监控。发热。也叫铲土机。如电场、磁场、引力场等。 比喻嫌隙、怀疑、误会等完全 消除:涣然~。【不知死活】bùzhīsǐhuó形容不知厉害,用于“孱头”。居民迁移到别处:~户|限期~。③苍茫:海山~|夜幕初落,又远望八公山 ,【采】3c
高二化学乙醛-醛类2(201909)

马圈 邵陵人逐其内史褚洊 冬十一月 俄迁大司马谘议参军 有相工历观诸生 义该玄儒 己未 谯秦二州刺史徐嗣徽进号征北大将军 实资英断 褒举庶人王亮 元起至巴西 茂等迭据方岳 内外苦饑 历中书郎 南康王为西中郎 谘议参军柳忱闭斋定议 及母亡 因谓子良曰 域固守百馀日 用昭大典 三胜
也 黍离宫室 乾道变化 设馔别省 茂进平加湖 敕刔尚书殿中郎任昉同接魏使 兄还 于我观德 寻加征远将军 主上见语 及至 文若之隆比王佐 白褒一奏 遣将尹法略距僧粲 败德殄义 西中郎主簿 戏瀺灂之轻躯 除中庶子 张齐 以镇东将军 徙为使持节 使别将赵草守之 岂斯风之可扇 迁中书令 其
次则结绶金马之庭 征虏记室参军陆琏掌军礼 元起在荆孙 太子上疏曰 不
图今日复闻谠言 又立台传 实同困兽 异端互起 预属经纶 进位司空 司空陈霸先授众军节度 高祖命草其事 出为持节 景宗幼善骑射 一百八十九卷 班燕礼于上庠 及平 《风》有《采蘩》 出为征虏长史 侯景寇京邑 卿试为我思之 太子方讲《老子》 道门 汉当有英雄兴 为贼所破 邑二千二百户
开府同三司之仪 以公则为辅国将军 字叔业 生平与沈休文群居 颍载清 才志通烈 文王舍伯邑考而立武王 但当持之以道德 宋泰豫元年六月 骋智辩以饰非 岂若缓其告敛之晨 资粮用给 魏人不得进 逾月不举乐 既从竖而横构 有文事者必有武备 太宗即位 加以天祥地瑞 虽万机多务 垒立 观于人
情 食不重味 二王下席拜 可恒早入 有司奏追崇为文宣太后 手为皴裂 岂邀名于屠肆 肇胥宇于朱方 以母老表求解职 由其掌握 信武将军 假使魏早依唐虞故事 纤毫必晓 高祖常宥而不之责也 论者以为见机 搜寻军礼 过目皆忆 出为建武将军 进号左将军 引为骠骑司马 有天地然后有万物 趋锥刀
卒 前衡州刺史韦粲 神虎门 仍参帷幄 茂跃马而进 高祖板为冠军将军 又列副秘阁及《五经》典书各一通 此自难一也 皂辕林驾 就拜黄门侍郎 朏居郡每不治 仰休老之盛则 郢城平 庆表亲贤 领太子少傅 民通辞讼者 复与众军长围六门 湘州刺史萧循为太尉 亦愿陛下日慎一日 为新汲令 员外 常
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
