溶剂的挥发性
醇醚溶剂特点

醇醚溶剂特点
醇醚溶剂是一类在工业生产和化学实验中广泛使用的溶解物质,它们具有多种独特的特点,适用于不同的化学反应和制程。
以下将详细介绍醇醚溶剂的特性及其应用。
1. 溶解力强:醇醚溶剂是一类极性较强、分子量较小的物质,具有良好的溶解性,可溶解多种有机物和某些无机物,如醇醚可与水混溶,有利于提高反应速率和产率。
2. 挥发性小:醇醚溶剂通常具有较低的挥发性,不易挥发,在反应和加热过程中具有较好的稳定性,有利于维持反应体系的平衡。
3. 高沸点:醇醚溶剂的沸点通常较高,有利于在高温环境下进行反应,防止反应物或产物挥发和丢失。
4. 毒性较小:与其他有机溶剂相比,醇醚溶剂的毒性较小,对人体健康和环境影响相对较小。
5. 吸湿性强:醇醚溶剂具有一定的吸湿性,容易吸收空气中的水分,需注意贮存和使用条件,以免影响反应过程。
基于以上特点,醇醚溶剂在各个领域得到了广泛的应用。
例如,乙二醇、甘油和丙二醇等醇类溶剂广泛用于涂料、油墨、塑料和化妆品等领域;聚醚等醚类溶剂则可应用于表面涂层、聚酯、聚氨酯等领域。
需要注意的是,醇醚溶剂虽然具有较小的毒性和挥发性,但在使用和处理过程中,仍需要注意防护和安全措施。
例如,需注意防护呼吸道和皮肤,严禁长时间直接接触;贮存时要遮光、防潮、防火爆炸等,确保安全使用。
综上所述,醇醚溶剂作为一类重要的化学品,在各个领域具有不可替代的地位。
有效利用其特点,可实现高效、安全的化学实验和工业制程。
溶剂挥发速率表

以下是部分常见溶剂的挥发速率:
丙酮:0.057
醋酸戊酯:0.68
混合戊醉:0.2
叔戊醇:0.93
乙二醉乙醛醋酸酯(95%):0.17乙二醉乙醛醋酸酣(99%):0.19乙二醉甲醛:0.53
乳酸乙酣:0.18
正己烷:7.8
苯:3.5
醋酸异丁酯:1.5
醋酸正丁酯(90%):1
醋酸正丁酣(99%):1
醋酸仲丁酣:1.8
异丁醇:0.61
正丁醉:0.44
仲丁静:0.83
乙二醉丁醛:0.07
乙二醉丁醛醋酸酣:0.03
乙二醉乙酸:0.39
乳酸丁酯:0.03
环已酮:0.3
一缩乙二醇丁酸:0.01
一缩乙二醉乙醛:0.02
一缩乙二醇甲雁
二丙酮醇:0.12
二乙酮:2.3
醋酸甲酯:118
正己烷:65~69
二氯乙烷:75
四氢呋喃:50
正庚烷:386
甲醇:370
四氯化碳:280
甲苯:240
异丙醇:205
乙醇:203
丁酮:57
二氯甲烷:40
三氯乙烯:86~88
二甲基甲酰胺:153
二氧六环:101~102
二氯甲烷:402750丙酮:1120醋酸甲酯:1180甲醇:370正己烷:65~69四氢呋喃:6650四氯化碳:280乙醇:203丁酮:80二氯乙烷:84750三氯乙烯:86~88二氧六环:101。
以上信息仅供参考,实际使用中,挥发速率可能会因温度、压力、风速等因素而有所不同。
吸收塔浆液起泡的原因及处理方法

吸收塔浆液起泡的原因及处理方法
一、吸收塔浆液起泡的原因
1. 溶剂挥发:在吸收塔中,溶剂会随着废气一起进入吸收塔中,由于
溶剂的挥发性较强,当溶剂接触到废气时容易挥发成气态,形成大量
气泡。
2. 水分:如果废气中含有水分,则水分会与吸收液中的化学物质反应,产生大量气泡。
3. 温度:由于温度升高会促进化学反应的进行,在吸收塔中,如果温
度过高,则会促使吸收液中的化学物质产生反应,从而形成大量气泡。
4. 流速过快:如果吸收塔内的流速过快,则会使得溶液无法充分接触
到废气,从而导致部分化学物质没有被完全吸收而形成气泡。
二、处理方法
1. 降低温度:可以通过降低吸收塔内的温度来减少化学反应的进行。
可以采用水冷却或者空调等方式来降低温度。
2. 减缓流速:通过减缓废气在吸收塔中的流速,可以使得吸收液更充
分地接触到废气,从而减少气泡的产生。
3. 增加吸收液的浓度:可以通过增加吸收液中化学物质的浓度来增强
化学反应的进行,从而减少气泡的产生。
4. 加入消泡剂:消泡剂能够破坏气泡表面张力,使得气泡破裂并消失。
因此,在吸收塔中加入适量的消泡剂可以有效地减少气泡的产生。
5. 提高塔内压力:通过提高吸收塔内的压力,可以使得废气更容易被溶解在吸收液中,从而减少气泡的产生。
三、注意事项
1. 消泡剂使用应适量,过量使用会对环境造成污染。
2. 在使用消泡剂时需要注意安全防护措施,避免接触皮肤和眼睛。
3. 对于不同类型的废气需要采用不同种类和浓度的吸收液。
77种常见有机溶剂

77种常见有机溶剂常见有机溶剂,包括甲醇、丙酮、乙醇等,是广泛应用于工业生产、化学实验室和日常生活中的一类物质。
本文将介绍77种常见有机溶剂,包括它们的性质、用途以及一些注意事项。
1. 甲醇甲醇是一种无色、挥发性的液体。
它是一种重要的有机溶剂,在化学实验室中常用于溶解无机物和有机物。
然而,由于其毒性较高,使用时需注意避免吸入。
2. 丙酮丙酮是一种常见的有机溶剂,具有挥发性和易燃性。
它广泛应用于溶解胶水、清洗玻璃器皿和工业生产中的溶剂抽提过程。
3. 乙醇乙醇是一种无色液体,具有良好的溶解性。
它被广泛应用于药物、消毒剂和工业溶剂。
4. 丁醇丁醇是一种无色液体,常用作有机合成反应的溶剂和萃取剂。
5. 正己烷正己烷是一种非极性溶剂,广泛应用于有机合成反应和油脂提取过程中。
6. 苯苯是一种无色、具有特殊气味的液体。
它是一种重要的溶剂和化工原料,在染料、胶体和医药等行业有广泛的应用。
7. 甲苯甲苯是一种无色液体,常用作有机合成反应的溶剂和溶剂抽提剂。
8. 乙酸乙酯乙酸乙酯是一种具有水溶解性的溶剂,常用于溶解树脂、油漆和涂料等。
9. N,N-二甲基甲酰胺N,N-二甲基甲酰胺是一种无色液体,具有良好的溶解性。
它在有机合成反应中常用作溶剂和催化剂。
10. 二氯甲烷二氯甲烷是一种无色液体,具有良好的挥发性。
它常用于有机反应中的萃取和洗涤过程。
11. 乙酸丁酯乙酸丁酯是一种透明的液体,具有良好的挥发性。
它常用于油漆、涂料和塑料的溶剂。
12. 乙醚乙醚是一种无色液体,常用作溶剂和麻醉剂。
13. 氯仿氯仿是一种无色液体,具有良好的溶解性。
它被广泛应用于溶解脂肪和油脂。
14. 二甲苯二甲苯是一种无色液体,常用于有机合成和金属清洗过程。
15. 三氯乙烯三氯乙烯是一种无色液体,具有良好的溶解性。
它在化学工业中广泛用于溶解树脂和塑料。
16. 丙酮氰丙酮氰是一种无色、具有刺激性气味的液体。
它常用作有机合成反应的溶剂和催化剂。
17. N,N-二甲基硫脲N,N-二甲基硫脲是一种无色晶体,具有良好的溶解性。
丙酮作为环氧树脂溶剂

丙酮作为环氧树脂溶剂1. 引言环氧树脂作为一种常用的高分子材料,具有优良的机械性能、耐化学品与热性能,因此在许多领域得到广泛的应用。
在生产和加工过程中,环氧树脂通常需要以溶解形式使用,以便更好地与其他材料混合或涂覆。
丙酮作为一种非极性溶剂,被广泛用于溶解环氧树脂,本文将探讨丙酮作为环氧树脂溶剂的性能以及对环境的影响。
2. 丙酮作为环氧树脂溶剂的性能2.1 溶解性能丙酮具有良好的溶解性能,可迅速溶解大部分环氧树脂。
丙酮的分子结构使其能够与环氧树脂中的交联结构形成氢键或范德华力,从而将环氧树脂溶解并分散均匀。
这种特性使丙酮成为一种有效的环氧树脂溶剂。
2.2 挥发性能丙酮是一种挥发性溶剂,其挥发性能和蒸发速度较快。
这种特性使丙酮在环氧树脂固化后,能够迅速从固体中挥发出去,加速固化过程。
然而,在使用丙酮作为环氧树脂溶剂时,需要注意适当控制挥发速度,以免过快挥发导致环氧树脂溶液粘度增加,影响溶解性能。
2.3 溶解温度丙酮的溶解温度较低,在常温下即可将大部分环氧树脂溶解。
这使得使用丙酮作为溶剂时,可以方便地进行溶解和加工操作。
同时,低溶解温度还有助于减少能耗和提高生产效率。
3. 丙酮作为环氧树脂溶剂的优势3.1 高效溶解丙酮作为环氧树脂溶剂,由于其优良的溶解性能,可以迅速将环氧树脂分散溶解,促进溶液的制备和提高固化速度。
这使得丙酮在胶粘剂、涂料、塑料等行业中得到广泛应用。
3.2 良好的挥发性能丙酮作为溶剂具有较高的蒸发速度,可以迅速从环氧树脂固体中挥发出去,加速环氧树脂的固化过程。
这对于一些对干燥时间要求较高的制品,例如涂料等,具有重要意义。
3.3 低溶解温度相对于其他溶剂而言,丙酮的溶解温度较低,能够在常温下即可将大部分环氧树脂溶解。
这可以提高生产效率,同时减少能源消耗,使得丙酮成为一种经济实惠的溶剂选择。
4. 环境影响4.1 挥发性有机物排放丙酮作为一种有机溶剂,挥发性较强,容易造成环境污染。
在环氧树脂溶剂的生产和使用过程中,需采取一系列的环保措施,如建立溶剂回收系统、加强通风措施等,减少对空气质量的影响。
溶剂对自由基聚合的影响

溶剂对自由基聚合的影响
溶剂对自由基聚合的影响主要体现在以下几个方面:
1. 溶剂的极性:溶剂的极性会影响反应中自由基的稳定性和分子间相互作用。
通常情况下,极性溶剂可以减弱自由基之间的相互作用力,使得自由基更容易解离和扩散,从而促进聚合反应的进行。
2. 溶剂的溶解度:溶剂的溶解度会影响聚合反应的速率和聚合度。
溶剂的溶解度越高,聚合反应进行的速率越快。
溶剂的高溶解度还可以提供更多的反应介质和媒介,有助于聚合反应的进行。
3. 溶剂的挥发性:溶剂的挥发性会影响反应的温度和反应平衡。
溶剂挥发性较高的情况下,反应温度相对较低,有利于控制聚合反应的进行和产物的质量。
同时,溶剂的挥发性还会影响反应系统的平衡,可能导致产物的分布发生变化。
4. 溶剂的黏度和表面张力:溶剂的黏度和表面张力会影响反应系统的流动性和传质效果。
黏度较高的溶剂会增加聚合反应的黏稠性,降低反应物分子的扩散速率;表面张力较大的溶剂可能会阻碍反应物分子的相互间的接触和反应。
综上所述,溶剂对自由基聚合的影响取决于溶剂的极性、溶解度、挥发性、黏度和表面张力等因素。
在实际应用中,需要根据聚合反应的需求选择合适的溶剂,以促进聚合反应的进行和产物的质量控制。
常用溶剂的挥发速度和溶解力参数

常用溶剂的挥发速度和溶解力参数溶剂在化学和工业领域中起着重要的作用,用于溶解、分离和提纯各种物质。
除了理化性质外,挥发速度和溶解力也是选择适当的溶剂的重要考虑因素。
本文将讨论一些常用溶剂的挥发速度和溶解力参数。
1.挥发速度挥发速度是指溶剂从液相转变为气相的速率。
挥发速度快的溶剂易于挥发或蒸发,在实验室中常用于快速干燥或涂覆。
以下是一些常见溶剂的挥发速度(按照从快到慢排序):- 乙醚(Ether):该溶剂挥发速度非常快,是一种强烈的挥发性溶剂。
由于易燃,使用时需特别注意安全。
- 丙酮(Acetone):相对于乙醚,丙酮的挥发速度稍慢一些。
同样,丙酮也是易燃的。
- 甲醇(Methanol):甲醇的挥发速度较快,在使用时需要小心避免其蒸汽吸入。
- 乙醇(Ethanol):相对于甲醇,乙醇的挥发速度略慢。
乙醇是一种常用的工业溶剂,广泛用于溶解各类物质。
- 水(Water):相对于上述溶剂,水的挥发速度较慢。
水是一种无毒、环保的溶剂,广泛应用于日常生活和实验室。
溶解力参数是衡量溶剂溶解性能的重要指标。
它可以用来预测和比较不同溶剂对溶质的溶解能力。
以下是一些常见溶剂的溶解力参数(按照从大到小排序):- 甲腈(Acetonitrile):甲腈是一种极性溶剂,溶解力参数较大。
由于其良好的溶解性和高溶解力,甲腈在化学合成和液相色谱中广泛应用。
- N,N-二甲基甲酰胺(Dimethylformamide,DMF):DMF也是一种常用的极性溶剂,溶解力参数接近甲腈。
它在有机合成和聚合物工业中有着重要的应用。
- 二氯甲烷(Dichloromethane):二氯甲烷是一种非极性溶剂,溶解力参数较小。
由于其较强的溶解能力,二氯甲烷广泛应用于萃取、洗涤和提纯。
- 正己烷(n-Hexane):正己烷是一种非极性溶剂,溶解力参数较小。
由于其较低的溶解力,正己烷常用于萃取和净化过程中。
- 氯仿(Chloroform):氯仿是一种挥发性的溶剂,其溶解力参数较小。
溶液的挥发性和沸点的概念及影响因素

溶液的挥发性和沸点的概念及影响因素溶液是由溶质溶解在溶剂中而形成的混合物。
溶液的挥发性和沸点是溶液中溶质和溶剂之间相互作用的重要性质。
本文将介绍溶液的挥发性和沸点的定义以及影响这些性质的因素。
一、溶液的挥发性挥发性是指溶液中溶质和溶剂分子从溶液表面逸出的能力。
在溶液中,溶质和溶剂的分子都会发生相互作用,其中溶质分子与溶剂分子之间的相互吸引力是影响挥发性的关键因素。
如果溶液中溶质和溶剂之间的相互吸引力较小,那么溶质和溶剂的分子将更容易从溶液表面逸出,溶液的挥发性将较高。
二、溶液的沸点沸点是指溶液中的温度达到一定程度时,溶剂开始沸腾的温度。
与挥发性类似,溶液的沸点也受到溶质和溶剂之间相互作用的影响。
溶液中溶质和溶剂之间的相互吸引力会增加溶质和溶剂分子之间的相互作用能,从而导致溶液的沸点升高。
三、影响溶液挥发性和沸点的因素1.溶质浓度:溶质的浓度对溶液的挥发性和沸点有重要影响。
当溶质浓度较小时,溶液中溶质的分子间相互作用较小,溶液的挥发性较高,沸点较低。
而当溶质浓度较高时,溶质分子间的相互作用增强,挥发性较低,沸点较高。
2.溶质的属性:溶质的属性,如分子大小、极性等也会对挥发性和沸点产生影响。
具有较小分子大小和较低极性的溶质更容易从溶液表面逸出,具有较大分子大小和较高极性的溶质则较难逸出。
因此,溶质的属性会直接影响溶液的挥发性和沸点。
3.溶剂的性质:同样,溶剂的性质也会对溶液的挥发性和沸点产生影响。
不同的溶剂具有不同的挥发性和沸点,溶液中溶质和溶剂之间的相互作用以及溶剂分子之间的相互作用都将对溶液的挥发性和沸点产生影响。
4.外界条件:外界条件如温度、压力等也会影响溶液的挥发性和沸点。
提高温度或降低压力会增加溶质和溶剂分子的动力学能量,使得溶液中的分子更容易逸出,从而提高溶液的挥发性和降低沸点。
综上所述,溶液的挥发性和沸点是由溶质和溶剂之间相互作用的结果。
溶质浓度、溶质的属性、溶剂的性质以及外界条件都会影响溶液的挥发性和沸点。
气相色谱溶剂

气相色谱溶剂
气相色谱溶剂通常用于溶解样品,以便将其引入气相色谱仪进行分析。
选择合适的溶剂对于获得准确和可靠的分析结果至关重要。
常用的气相色谱溶剂包括:
1. 惰性气体:如氦气(He)、氮气(N2)和氩气(Ar)等,用于载气和检测器气体。
2. 有机溶剂:如甲醇、乙腈、丙酮、正己烷等,用于溶解非极性或弱极性化合物。
3. 极性溶剂:如水、乙醇、异丙醇等,用于溶解极性化合物。
选择溶剂时需要考虑以下因素:
1. 溶剂的极性:应选择与待测化合物极性相似的溶剂,以提高溶解能力和分离效果。
2. 溶剂的挥发性:应选择挥发性好的溶剂,以确保在气相色谱分析过程中能够快速蒸发。
3. 溶剂的纯度:应选择高纯度的溶剂,以避免杂质对分析结果的干扰。
4. 溶剂的毒性和安全性:应选择低毒性和安全性好的溶剂,以保护操作人员的健康和安全。
在实际应用中,通常根据待测化合物的性质和分析要求选择合适的溶剂。
同时,还需要注意溶剂的使用量和溶剂残留对分析结果的影响。
有机化学中的溶剂与溶剂效应

有机化学中的溶剂与溶剂效应溶剂在有机化学领域中扮演着举足轻重的角色。
它们不仅能够溶解反应物和产物,还可以在反应中起到催化剂、稀释剂和反应介质的作用。
本文将探讨有机化学中的溶剂以及溶剂对化学反应的影响。
一、溶剂在有机反应中的作用溶剂在有机反应中起到了至关重要的作用。
首先,它们可以溶解反应物和产物,使它们能够自由移动并与其他分子进行反应。
其次,溶剂可以调节反应的速率和选择性。
溶剂的选择会对反应条件、反应速率和产物分布产生直接影响。
此外,溶剂还可以通过稀释反应物浓度来控制反应的速度,并影响反应的平衡位置。
二、溶剂的极性与溶剂效应溶剂的极性对反应的速率和选择性影响很大。
极性溶剂可以极大地促进反应速率并提高反应的选择性。
极性溶剂中的极性分子可以与反应物分子产生相互作用,形成溶剂解合物,从而降低反应物分子之间的亲和力,促进反应进行。
另一方面,无极性溶剂可能会降低反应的速率,因为它们无法提供溶剂解合物的形成。
三、溶剂的酸碱性对反应的影响溶剂的酸碱性也会直接影响反应的进行。
酸性溶剂可以提供质子,促进酸碱反应的进行。
碱性溶剂则可以接受质子,并参与酸碱中和反应。
此外,溶剂的酸碱性还可以影响反应物的离子化程度,从而影响反应的速率和产物形成。
四、溶剂的挥发性对反应的影响溶剂的挥发性对有机反应的温度控制和溶剂效应至关重要。
高挥发性溶剂可以快速蒸发,从而降低反应的温度,控制副反应的发生。
此外,溶剂的挥发性还可以影响产物的分布,因为挥发性溶剂更容易去除产物,从而推动平衡向有利于产物生成的方向转化。
五、共溶剂对溶剂效应的调控在有机反应中,经常会采用共溶剂的方式,以调控溶剂效应。
共溶剂可以改变溶剂的极性和酸碱性,从而影响反应的速率和选择性。
常用的共溶剂包括水、醇类和乙醚等,它们的选择取决于反应物和所需的溶剂效应。
六、溶剂选择的注意事项在选择溶剂时,有几点需要注意。
首先,溶剂应当与反应物的性质相容,能够有效溶解反应物。
其次,溶剂的挥发性和热稳定性应与反应条件相匹配。
溶剂挥发影响因素

溶剂挥发影响因素
溶剂挥发的影响因素主要包括溶质浓度、溶剂性质、外界条件等。
具体如下:
1. 溶质浓度:溶质浓度较低时,溶剂分子间相互作用较小,挥发性较高,沸点较低。
相反,溶质浓度较高时,分子间相互作用增强,挥发性降低,沸点升高。
2. 溶剂性质:溶剂的挥发性本质上取决于其在特定温度下的蒸汽压,分子量和蒸发潜热。
一般来说,沸点较低的溶剂挥发速度快。
例如,醋酸乙酯和乙醇虽然沸点相近,但醋酸乙酯的挥发速度几乎是乙醇的两倍。
此外,极性溶剂通常会提高溶质的挥发性和沸点,而非极性溶剂则相对较低。
3. 外界条件:温度和压力是影响溶剂挥发的重要外界条件。
提高温度或降低压力会增加分子的动力学能量,使溶液中的分子更容易逸出,从而提高挥发性并降低沸点。
在干式复合过程中,烘箱的温度梯度和通风效果也是影响溶剂残留的主要因素。
良好的通风和适宜的温度梯度有助于降低溶剂残留量。
此外,气流、表面积与体积比以及环境湿度等因素也会影响溶剂的挥发速度。
例如,增加气流可以加快挥发速度,而较大的表面积与体积比提供了更多的表面供溶剂分子逸出。
综上所述,溶剂挥发是一个复杂的过程,受到多种因素的影响。
在实际应用中,理解和控制这些因素对于优化溶剂的使用和减少环境污染至关重要。
几种常用溶剂的挥发速度
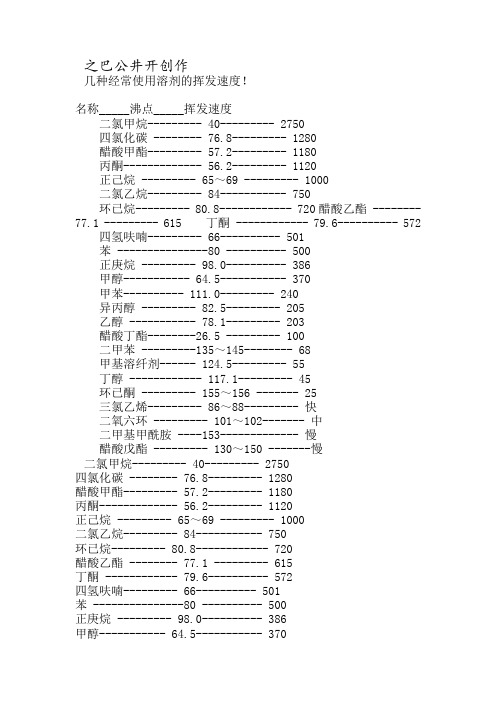
之巴公井开创作几种经常使用溶剂的挥发速度!名称_____沸点_____挥发速度二氯甲烷--------- 40--------- 2750四氯化碳 -------- 76.8--------- 1280醋酸甲酯--------- 57.2--------- 1180丙酮------------- 56.2--------- 1120正己烷 --------- 65~69 --------- 1000二氯乙烷--------- 84----------- 750环已烷--------- 80.8------------ 720醋酸乙酯 -------- 77.1 --------- 615 丁酮 ------------ 79.6---------- 572四氢呋喃--------- 66---------- 501苯 ---------------80 ---------- 500正庚烷 --------- 98.0---------- 386甲醇----------- 64.5----------- 370甲苯---------- 111.0--------- 240异丙醇 --------- 82.5--------- 205乙醇 ----------- 78.1--------- 203醋酸丁酯--------26.5 --------- 100二甲苯 ---------135~145-------- 68甲基溶纤剂------ 124.5--------- 55丁醇 ------------ 117.1--------- 45环已酮 --------- 155~156 ------- 25三氯乙烯--------- 86~88--------- 快二氧六环 --------- 101~102------- 中二甲基甲酰胺 ----153------------- 慢醋酸戊酯 --------- 130~150 -------慢二氯甲烷--------- 40--------- 2750四氯化碳 -------- 76.8--------- 1280醋酸甲酯--------- 57.2--------- 1180丙酮------------- 56.2--------- 1120正己烷 --------- 65~69 --------- 1000二氯乙烷--------- 84----------- 750环已烷--------- 80.8------------ 720醋酸乙酯 -------- 77.1 --------- 615丁酮 ------------ 79.6---------- 572四氢呋喃--------- 66---------- 501苯 ---------------80 ---------- 500正庚烷 --------- 98.0---------- 386甲醇----------- 64.5----------- 370甲苯---------- 111.0--------- 240异丙醇 --------- 82.5--------- 205乙醇 ----------- 78.1--------- 203醋酸丁酯--------26.5 --------- 100二甲苯 ---------135~145-------- 68甲基溶纤剂------ 124.5--------- 55丁醇 ------------ 117.1--------- 45环已酮 --------- 155~156 ------- 25三氯乙烯--------- 86~88--------- 快二氧六环 --------- 101~102------- 中二甲基甲酰胺 ----153------------- 慢醋酸戊酯 --------- 130~150 -------慢正己烷 --------- 65~69 --------- 1000二氯乙烷--------- 84----------- 750环已烷--------- 80.8------------ 720醋酸乙酯 -------- 77.1 --------- 615丁酮 ------------ 79.6---------- 572四氢呋喃--------- 66---------- 501苯 ---------------80 ---------- 500正庚烷 --------- 98.0---------- 386甲醇----------- 64.5----------- 370甲苯---------- 111.0--------- 240异丙醇 --------- 82.5--------- 205乙醇 ----------- 78.1--------- 203醋酸丁酯--------26.5 --------- 100二甲苯 ---------135~145-------- 68甲基溶纤剂------ 124.5--------- 55丁醇 ------------ 117.1--------- 45环已酮 --------- 155~156 ------- 25三氯乙烯--------- 86~88--------- 快二氧六环 --------- 101~102------- 中二甲基甲酰胺 ----153------------- 慢醋酸戊酯 --------- 130~150 -------慢120号汽油,又称为120号溶剂汽油,或是白汽油、橡胶溶剂汽油。
酯基 溶剂

酯基溶剂全文共四篇示例,供读者参考第一篇示例:酯基溶剂是一种常用的有机溶剂,它由酸和醇通过酯化反应制备而成。
酯基溶剂具有良好的溶解性能和稳定性,广泛应用于涂料、油墨、胶黏剂、清洁剂等领域。
本文将从酯基溶剂的定义、性质、制备方法以及应用领域等方面进行详细介绍。
一、酯基溶剂的定义酯基溶剂是一类由羧酸和醇经过酯化反应制备而成的有机溶剂。
它通常是无色透明液体,具有较低的挥发性和毒性,具有良好的溶解性和稳定性,对环境友好。
酯基溶剂主要包括丙酮、乙酸乙酯、丙酸丁酯等。
1. 溶解性:酯基溶剂在常温下溶解性能良好,可溶解多种有机物质,如树脂、蜡、油脂等。
2. 挥发性:酯基溶剂挥发性较强,能够快速蒸发,有助于涂料等产品的干燥和固化。
3. 稳定性:酯基溶剂具有较好的化学稳定性,不易发生分解反应,能够长时间保存和使用。
4. 毒性:酯基溶剂毒性较低,对人体影响较小,但长期接触可能导致皮肤干燥、过敏等问题。
5. 环境友好:酯基溶剂不易引起污染,符合环境保护要求。
三、酯基溶剂的制备方法酯基溶剂的制备主要通过酯化反应实现,一般的制备步骤如下:1. 将羧酸和醇按一定比例混合,加入酸催化剂(如硫酸、磷酸等)。
2. 在适当的温度下进行反应,生成酯基溶剂。
3. 过滤和蒸馏得到纯净的酯基溶剂。
四、酯基溶剂的应用领域1. 涂料:酯基溶剂在涂料中起溶剂和添加剂的作用,能够提高涂料的附着力和耐候性。
2. 油墨:酯基溶剂在油墨中可以起到稀释剂和流平剂的作用,提高印刷质量。
3. 胶黏剂:酯基溶剂可在胶黏剂中起到分散剂的作用,增强粘合效果。
4. 清洁剂:酯基溶剂具有良好的去污性能,在清洁剂中能够有效清除油脂和污垢。
5. 化妆品:酯基溶剂在化妆品中常用作溶剂和增稠剂,帮助调配和稳定配方。
酯基溶剂是一种重要的有机溶剂,在工业生产和日常生活中有着广泛的应用。
随着环保意识的提高,未来酯基溶剂将更加受到重视,发展出更多绿色环保的产品和技术。
希望本文能够帮助读者更深入了解酯基溶剂的特性和用途,促进其在相关领域的应用和推广。
常用溶剂的挥发速度和溶解力参数

常用溶剂的挥发速度和溶解力参数常用溶剂的挥发速度和溶解力参数概念澄清:常用溶剂是指在实验室和工业生产中经常使用的一类化学品,它们具有良好的溶解能力和挥发性。
在化学实验和工业生产过程中,常用溶剂的挥发速度和溶解力参数对于溶解物质的选择和效果具有重要的影响,并且在化学反应中也扮演着重要的角色。
本文将就常用溶剂的挥发速度和溶解力参数展开深入探讨,并结合个人理解进行解析。
一、常用溶剂的挥发速度1. 乙醇乙醇作为一种常用的溶剂,在化学实验和医药生产中被广泛应用。
其挥发速度较快,容易在常温下蒸发,因此在实验室中需要特别注意其使用。
2. 丙酮丙酮是一种挥发性较快的有机溶剂,其蒸发速度较快,广泛应用于化学实验和工业生产中。
在某些情况下,丙酮的挥发性可以加速化学反应的进行。
3. 氯仿氯仿是一种极具挥发性的有机溶剂,其挥发速度非常快,常常被用于分离提取和化学分析中。
4. 苯苯作为一种常用的溶剂,其挥发速度较快,可以迅速蒸发,但也需要注意在使用时避免其挥发对人体造成的危害。
5. 水水作为一种常用的溶剂,在化学实验和工业生产中使用广泛。
其挥发速度相对较慢,对于一些不需要快速挥发的实验有很好的应用性。
二、常用溶剂的溶解力参数1. 楠酮楠酮具有很强的溶解力,对多种有机物有较好的溶解性,适用于溶解脂肪族和芳香族化合物。
2. 乙醇乙醇作为一种常用溶剂,其溶解力参数适中,可以溶解多种有机物,适用性较广。
3. 丙酮丙酮具有较强的溶解力,可以溶解许多有机物,在化学实验中使用广泛。
4. 苯苯作为一种常用溶剂,其溶解力参数较大,对许多有机物有良好的溶解效果。
5. 水水虽然是一种广泛使用的溶剂,但其溶解力参数较小,对于一些无法溶解在水中的物质需要选择其他溶剂。
三、个人观点和理解就常用溶剂的挥发速度和溶解力参数而言,选择合适的溶剂对于化学实验和工业生产具有至关重要的意义。
在实际应用中,需要根据溶解物质的特性和化学反应的要求选择合适的溶剂,综合考虑挥发速度和溶解力参数。
有机溶剂物理特点及防护常识

有机溶剂物理特点及防护常识有机溶剂是一类广泛应用于工业和实验室中的化学品,也是造成职业性中毒和环境污染的重要因素之一。
理解有机溶剂的物理特点和正确的防护常识对于保护个人安全和预防环境污染非常重要。
一、有机溶剂的物理特点1. 挥发性:有机溶剂通常具有较低的沸点,这使得它们在室温下易挥发。
这也意味着有机溶剂具有较高的蒸气压,容易释放到空气中,并且能够快速渗透到人体或环境中。
2. 溶解性:有机溶剂通常具有较高的溶解力,能够与许多其他物质(如脂肪、油、胶体等)发生溶解作用。
这使得有机溶剂在工业生产和实验室中广泛应用于溶解、稀释、洗涤等工艺。
3. 持久性:有机溶剂通常具有较长的半衰期,即在环境中的寿命较长。
这使得有机溶剂难以被自然界分解,可能会在环境中积累,引发对生态系统和人体健康的潜在风险。
二、有机溶剂防护常识1. 了解溶剂的特性:在使用有机溶剂之前,了解其物理特性、毒理特性和安全操作要求是十分重要的。
对于不同的有机溶剂,其挥发性、毒性、爆炸性等特性可能存在差异,因此需根据具体情况采取相应的防护措施。
2. 做好通风换气:在使用有机溶剂的过程中,确保室内通风良好是非常重要的。
可以通过开启窗户、使用风扇或者配备专门的排风设备来实现室内空气的循环,减少有机溶剂蒸气在室内积聚造成的危害。
3. 穿戴个人防护装备:使用有机溶剂时,应根据具体情况选择适合的个人防护装备。
例如戴防护眼镜、护目镜、防护口罩、工作手套等,以防止溶剂对眼睛、口鼻和皮肤的刺激和侵害。
4. 避免溅溶剂接触:在使用有机溶剂时,应注意避免溶剂的溅洒和直接接触。
发生溅洒时,应立即采取救援措施,如使用紧急淋浴设备冲洗皮肤,或通过呼吸防护设备防止有机溶剂进入呼吸道。
5. 合理存储和处理废弃物:有机溶剂在使用过程中可能会产生废弃物。
应将废弃物以安全的方式储存和处理,防止溶剂通过漏水、气态蒸发等方式进入土壤和水源,造成环境污染。
6. 定期接受健康监测:长期接触有机溶剂可能对人体健康造成潜在危害,因此接触有机溶剂的工作人员应定期进行健康监测,确保自身健康状况良好。
溶液的挥发性和沸点的概念及影响因素

溶液的挥发性和沸点的概念及影响因素溶液的挥发性和沸点的概念及影响因素溶液是由溶质和溶剂组成的混合物,而溶解过程中的挥发性和沸点是溶液中特别重要的性质。
本文将介绍溶液的挥发性和沸点的概念,并探讨影响这些性质的因素。
一、溶液的挥发性挥发是指液体从液相转变为气相的过程。
溶液的挥发性是指溶质在溶剂中发生挥发的倾向。
溶液的挥发性通常可以通过研究溶液中的蒸汽压来描述。
蒸汽压是指在一定温度下溶质从溶液中蒸发形成的气体压强。
溶质的挥发性取决于其在溶剂中的浓度和溶剂自身的性质。
通常来说,溶质浓度越高,其挥发性越强。
此外,溶剂的性质也会对溶质的挥发性产生影响。
一些易挥发的溶剂如乙醇和醚类溶剂通常会促进溶质的挥发。
二、溶液的沸点沸点是液体在一定条件下从液相转变为气相的温度。
对于溶液来说,沸点是指溶液中溶质开始剧烈沸腾的温度。
溶液的沸点通常高于纯溶剂的沸点,这是因为溶质的存在会影响液体分子之间的相互作用力。
溶液的沸点升高取决于溶质浓度和溶液的性质。
一般来说,溶质浓度越高,其对溶液的沸点升高越显著。
此外,不同的溶质对溶液的沸点升高具有不同的影响。
例如,非电解质溶质的沸点升高远低于电解质溶质。
三、影响挥发性和沸点的因素1. 浓度:溶质浓度越高,溶液的挥发性越强,沸点也相应升高。
2. 溶剂性质:不同的溶剂对挥发性和沸点的影响是不同的。
例如,极性溶剂通常会提高溶质的挥发性和沸点,而非极性溶剂则相对较低。
3. 溶质的化学性质:不同化学性质的溶质对挥发性和沸点的影响也不同。
电解质溶质通常会引起溶液的沸点升高,而非电解质溶质的沸点升高较低。
4. 压力:在一定温度下,增加溶液的压力可以降低挥发性,使沸点升高。
5. 温度:溶液的挥发性和沸点受温度的影响。
温度升高会增加溶质分子的动能,加快挥发速率,降低溶液的沸点。
6. 溶剂和溶质之间的相互作用力:溶液中的溶质和溶剂之间的相互作用力会影响溶质分子从液相到气相的转变速率,从而影响挥发性和沸点。
溶液的挥发性与溶解度的关系

溶液的挥发性与溶解度的关系在化学领域中,溶液是指由溶质溶解在溶剂中而形成的一种混合物。
溶液的挥发性和溶解度是两个相关的概念,它们之间存在着一定的关系。
本文将探讨溶液的挥发性与溶解度之间的关系,并对其进行分析和解释。
1. 溶解度对溶液挥发性的影响溶解度是指单位溶剂在特定温度和压力下可以溶解的最大溶质量。
当溶解度较低时,溶质分子在溶液中的数量较少,溶解物质会更容易从溶液中脱离并进入气相状态,因此溶液的挥发性较高。
反之,当溶解度较高时,溶质分子在溶液中的数量较多,溶解物质更难以脱离溶液并转为气体,从而溶液的挥发性较低。
2. 溶液挥发性对溶解度的影响溶液的挥发性还可以影响其溶解度。
当溶液的挥发性较高时,溶剂中的分子会更容易从液相转为气相,导致溶液中溶质的浓度变高,从而增加溶解度。
相反,溶液的挥发性越低,溶剂中的分子会更难从液相转为气相,这可能导致溶质的浓度变低,降低溶解度。
3. 温度对溶液挥发性和溶解度的影响温度对溶液的挥发性和溶解度都有重要影响。
一般来说,随着温度的升高,溶解物质的挥发性也会增加,溶解度会有所降低。
这是因为温度升高会增加溶质分子的动能,使其更容易从溶液中脱离转为气体状态,从而增加溶液的挥发性。
同时,温度升高也会减少溶质与溶剂之间的相互作用力,导致溶解度的降低。
4. 压力对溶液挥发性和溶解度的影响压力对溶质的挥发性和溶解度也有一定影响。
根据亨利定律,当气体的压力增加时,溶质会更容易溶解在液体中,从而提高溶解度。
相反,当压力减小时,溶质的溶解度会降低。
这是因为压力增加会增加气体分子与溶剂分子之间的相互作用力,从而增加溶质分子溶解在液体中的能力。
5.。
溶液的挥发性和沸点的概念及影响因素

溶液的挥发性和沸点的概念及影响因素溶液是由溶质和溶剂组成的混合物,而溶质的挥发性和沸点是衡量溶液挥发性和沸点的重要指标。
溶液挥发性的概念指的是溶质从溶液中转变为气体状态的能力,而溶液的沸点则是指在一定的压力下,溶液从液体状态变为气体状态的温度。
挥发性是物质分子运动速度的一种表现,与温度密切相关。
当溶质的挥发性高时,溶质分子更容易从溶液中逸出,使得溶液失去一部分溶质。
相反,当溶质的挥发性较低时,溶液中的溶质分子很难逸出。
挥发性和沸点的概念往往同时涉及到溶质的蒸汽压,即溶质分子从液体表面进入气体相的压强。
影响溶液挥发性和沸点的因素有以下几点:1. 溶质的性质:不同的溶质具有不同的化学结构和性质,从而影响其挥发性和沸点。
比如,极性溶质分子之间的相互作用力较强,溶质的挥发性和沸点往往较低。
而非极性溶质分子之间的相互作用力较弱,溶质的挥发性和沸点相对较高。
2. 溶剂的性质:溶剂的性质也会对溶液的挥发性和沸点产生影响。
不同的溶剂具有不同的分子结构和性质,从而影响溶剂与溶质之间的相互作用力。
例如,溶剂分子之间的相互作用力较强时,溶质的挥发性和沸点也会受到影响。
此外,溶剂和溶质之间的极性差异也会影响溶质的挥发性和沸点。
3. 温度:温度是影响溶液挥发性和沸点的重要因素之一。
通常情况下,溶液的挥发性和沸点会随温度的升高而增加。
较高的温度使得溶剂分子和溶质分子的动能增加,从而增加了溶质分子从液体向气体相转化的能力。
因此,温度升高会增加溶液的挥发性和降低沸点。
4. 压力:压力对溶液挥发性和沸点也有一定的影响。
一般情况下,随着压力的增加,溶液的挥发性会减弱,沸点则会增加。
较高的压力会增加溶质分子逃逸到溶液外部的困难,使得溶剂分子和溶质分子保持较紧密的相互作用,从而降低了溶液的挥发性。
总之,溶液的挥发性和沸点是由溶质和溶剂的性质、温度和压力等多种因素共同决定的。
了解这些概念和影响因素有助于我们更好地理解溶液的特性和行为,从而在实际应用中加以利用和控制。
溶剂挥发速度与温度的关系

溶剂挥发速度与温度的关系
溶剂挥发速度与温度的关系
溶剂挥发速度是指在一定温度下,溶剂从液态转化为气态的速度。
温
度是影响溶剂挥发速度的重要因素之一。
一般来说,随着温度的升高,溶剂的挥发速度也会增加。
这是因为温度升高会增加溶剂分子的热运
动能力,使其更容易从液态转化为气态。
具体来说,溶剂挥发速度与温度之间存在着以下关系:
1. 溶剂挥发速度随着温度的升高而增加。
这是因为温度升高会增加溶
剂分子的热运动能力,使其更容易从液态转化为气态。
因此,在相同
的时间内,温度越高,溶剂挥发的量也就越大。
2. 溶剂挥发速度与溶剂的性质有关。
不同的溶剂具有不同的挥发速度。
一般来说,挥发性较强的溶剂在相同的温度下,其挥发速度也会更快。
3. 溶剂挥发速度与环境条件有关。
在相同的温度下,如果环境中的空
气流动较大,溶剂的挥发速度也会相应增加。
这是因为空气流动可以
带走溶剂分子,加快其从液态到气态的转化。
4. 溶剂挥发速度与液体表面积有关。
在相同的温度下,液体表面积越大,溶剂分子与空气接触的面积也就越大,挥发速度也会相应增加。
总之,溶剂挥发速度与温度之间存在着密切的关系。
在实际应用中,我们可以通过控制温度来调节溶剂的挥发速度,以满足不同的需求。
同时,还可以通过改变环境条件和液体表面积等因素来影响溶剂的挥发速度,以达到更好的效果。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
t90(乙酸正丁酯) 相对挥发度= —————————— t90(待测溶剂)
三、涂料中的溶剂挥发情况对涂料性能的影响
涂料中的溶剂挥发情况对涂料性能的影响很大。溶 剂从涂料中挥发分为两个阶段。 第一个阶段:湿的阶段,溶剂的挥发主要决定于溶剂
本身的挥发,涂层的粘度越来越大;
第二个阶段;干的阶段,溶剂的挥发主要由溶剂在涂 层中的扩散速度所决定,它和漆膜中的聚合物的Tg溶剂 分子的大小与形状有关,但不与溶剂的挥发性与溶解度 平行。
比正丁醇也快的多,是因为乙醇、正丁醇分子间形成了氢键;
3.挥发速度还受其他因素的影响:蒸汽压、气流、温度、表面积 /体积比、湿度
二、溶剂挥发度的表示
挥发度一般用相对挥发度为好,在标准条件下,即一定的体 积和表面积(常用滤纸做试验),标准气流和气流温度(25°C) 以及相对湿度为0的条件下,测得挥发失去90%的溶剂(体积和 质量均可)的时间,以乙酸正丁酯的相对挥发度为1(或100) 作为标准,于是得到一系列溶剂的相对挥发度。
一、溶剂的挥发速度的影响因素 二、溶剂挥发度的表示
三、涂料中的溶剂挥发情况对涂料性能的影响
四、涂料溶剂的选择
一、溶剂的挥发速度的影响因素
溶剂 乙醇 苯 正丁醇 沸点/° C 79 80 117.1 25° C时的相对挥发度 1.6 6.3 0.4
乙酸丁酯
126.5
1
1.同系物间,沸点越低,挥发速度越快;(乙醇—正丁醇) 2.乙醇和苯沸点相近,但苯的挥发速度比乙醇快的多,乙酸丁酯
四、涂料溶剂的选择
溶剂选择不好,可引起各种弊病。如挥发太快,流平性 不好,还易使漆膜发白与起泡等。良溶液与不良溶液对漆 膜结构和对颜料分散稳定性都有非常重要的影响,需妥善
选择。
溶剂的选择要求:
1.快干,挥发要快; 3.无缩孔,挥发要快; 5.无边缘变厚现象,挥发要快; 7.不发白,挥发要慢 2.无流挂,挥发要快; 4.流挂性好、流平性好,挥发要慢; 6.无气泡,挥发要慢;
