碱式硝酸铜的pdf卡片 理论说明以及概述
氨气沉淀法制备碱式硝酸铜及其形貌机理研究

第52卷第3期2023年3月人㊀工㊀晶㊀体㊀学㊀报JOURNAL OF SYNTHETIC CRYSTALS Vol.52㊀No.3March,2023氨气沉淀法制备碱式硝酸铜及其形貌机理研究王新安1,范天博1,2,3,赵一波1,刘㊀森1,郭洪范1,2,李㊀雪1,2,3(1.沈阳化工大学,辽宁省化工应用技术重点实验室,沈阳㊀110142;2.沈阳化工大学,辽宁省镁钙无机功能材料工程研究中心,沈阳㊀110142;3.沈阳化工大学,沈阳市镁钙资源利用技术重点实验室,沈阳㊀110142)摘要:本文以硝酸铜为原料,采用氨气沉淀法制备了多种形貌的碱式硝酸铜㊂研究了反应过程中温度㊁通氨时间和通氨速率对产品微观形貌和产品收率的影响,在最佳反应条件,即反应时间40min㊁反应温度90ħ㊁通氨速率500mL /min 时,产品收率达到50%,产品形貌为类六方片状,分散性好,粒径分布接近于正态分布㊂在产品中发现由纳米级碱式硝酸铜颗粒紧密排布而成的二维纳米网状结构,上面分布有纳米级微孔㊂采用Morphology 及CASTEP 程序对碱式硝酸铜生长习性进行理论分析,计算结果与实验吻合,由温度引起的(001)晶面显露程度变化是导致宏观形貌不规则的重要因素㊂关键词:硝酸铜;碱式硝酸铜;氨气沉淀法;纳米结构;形貌中图分类号:TQ131.2+1㊀㊀文献标志码:A ㊀㊀文章编号:1000-985X (2023)03-0536-10Preparation and Morphology Mechanism of Basic Copper Nitrate by Ammonia PrecipitationWANG Xin an 1,FAN Tianbo 1,2,3,ZHAO Yibo 1,LIU Sen 1,GUO Hongfan 1,2,LI Xue 1,2,3(1.Liaoning Key Laboratory of Chemical Application Technology,Shenyang University of Chemical Technology,Shenyang 110142,China;2.Liaoning Engineering Research Center for Magnesium and Calcium Inorganic Functional Materials,Shenyang University of Chemical Technology,Shenyang 110142,China;3.Shenyang Key Laboratory for the Utilization Technology of Magnesium and Calcium Resources,Shenyang University of Chemical Technology,Shenyang 110142,China)Abstract :Using copper nitrate as raw material,basic copper nitrate with various morphologies were prepared by ammonia precipitation method.The effects of temperature,ammonia-passing time and ammonia-passing rate on the microscopic morphology of the product and product yield during the reaction were studied.Under the optimal reaction conditions,that is,the reaction time of 40min,the reaction temperature of 90ħ,and the ammonia passing rate of 500mL /min,the product yield reaches 50%,and the product morphology is hexagonal flake-like,with good dispersibility and the particle size distribution is close to the normal distribution.It is found in the product that a two-dimensional nano-network structure formed by the close arrangement of nano-scale basic copper nitrate particles,with nano-scale micropores distributed in it.The Morphology and CASTEP program were used to theoretically analyze the growth habit of basic copper nitrate,the calculated results are consistent with the experimental results,the change of (001)crystal surface exposure caused by temperature is an important reason for the irregular macroscopic morphology.Key words :copper nitrate;basic copper nitrate;ammonia precipitation;nano-structure;morphology㊀㊀收稿日期:2022-11-21㊀㊀基金项目:国家自然科学基金(61102041);国家重点研发计划(2020YFC1909300);辽宁省教育厅项目(LJKZ0431,L2013169);辽宁省高校创新团队支撑计划(2013010);国家科技支撑计划(2013BAB09B01);辽宁省精细化工协同创新中心资助项目;辽宁省自然科学基金(201602582);辽宁省高等学校创新人才支持计划(LR2018078);辽宁省自然科学基金材料联合基金(20180510007);辽宁省自然科学基金指导计划(2019ZD0075);菱镁固废化工材料高值利用技术与基地集成示范(2020YFCI909300)㊀㊀作者简介:王新安(1998 ),男,辽宁省人,硕士研究生㊂E-mail:dxzya@ ㊀㊀通信作者:范天博,博士,副教授㊂E-mail:eftb@0㊀引㊀㊀言碱式硝酸铜(basic cupric nitrate)作为一种碱性铜盐,在无毒固体推进剂㊁点火组合物和汽车安全气㊀第3期王新安等:氨气沉淀法制备碱式硝酸铜及其形貌机理研究537㊀囊[1-2]中常被用作氧化剂,也可作为充电锂电池的高性能催化剂[3],同时也是制备Cu(OH)2和CuO的前驱体㊂由于具有小尺寸效应,纳米级碱式硝酸铜的杀菌性能[4]也大幅超过传统的波尔多液,已经在医药和农药[5]等方面广泛应用㊂在过去的几十年中,研究人员通过多种方法获得碱式硝酸铜晶体,Kratohvil等[6]通过CuO与Cu(NO3)2溶液反应,采用双喷射沉淀技术获得片状的碱式硝酸铜;Henrist等[7]将Cu(NO3)2㊃3H2O 溶解,然后在搅拌下加入NH4OH,最后加入NaOH获得叶片形状的碱式硝酸铜;Li等[8]从铜盐溶液和尿素中沉淀,并老化Cu(NO3)2溶液和NaOH溶液的混合物形成无定形颗粒产物㊂采用NH4OH和尿素做沉淀剂,溶液中氨浓度将随反应的进行而降低,导致pH值不稳定,产品形貌不够理想㊂持续通入氨气的氨气沉淀法具有反应时间快㊁一步反应㊁不用其他强化方法的优点㊂本课题组采用氨气沉淀法合成了空心球霰石碳酸钙[9]㊁六方片状氢氧化镁[10-11]㊂NH3-NH+4体系在制备Mg㊁Ca化学品过程中的优点在于当碱性镁㊁钙化合物成核结晶后,可以通过缓冲效应及时消除局部区域的OH-浓度差,迅速恢复到溶液平均水平,为新的结晶生成以及规则生长提供稳定的溶液环境,所以无须进行其他强化方法,仅进行反应温度和反应时间的控制就可以实现形貌控制制备㊂Zhan等[12]报道了在凝胶缓冲体系中制得长径比约为1ʒ1的六棱柱形貌的碳酸钙球霰石㊂Huang等[13]采用双壳类虹吸鞘,在凝胶体系中制备出六角形碳酸钙㊂可见,在缓冲体系中也可以合成出形貌较好的产物,可以得到在非缓冲体系不易得到的理想形貌㊂本文采用氨气沉淀法制备碱式硝酸铜,利用缓冲效应实现对产品形貌的控制,同时,拟采用Material Studio2020软件中Morphology程序对碱式硝酸铜的主要显露面族 (001)㊁(111)㊁(200)㊁(201)㊁(121)㊁(022)㊁(122)㊁(103)㊁(320)和(041)的形貌特征和相关的生长习性进行理论计算,对晶体微观形貌形成机理进行讨论㊂1㊀实㊀㊀验1.1㊀实验原料和制备方法硝酸铜,上海麦克林生化科技有限公司,分析纯;氨气,沈阳盛兴气体有限公司,分析纯㊂配制1mol/L的硝酸铜溶液,混合均匀㊂在一定的温度下,以500r/min搅拌,通过氨气质量流量控制器,通入氨气至适宜的时间,反应一定时间后结束实验,经陈化后抽滤,将滤饼放入烘箱干燥,得到蓝绿色的碱式硝酸铜㊂1.2㊀实验仪器德国Bruker公司的D8型X射线衍射仪,采用Cu Kα作为辐射源,2θ范围在0ʎ~70ʎ,0.05(ʎ)/step;北京尼高力公司的富里埃红外光谱分析仪,检测范围0~4000cm-1;日本JSM-6360LV扫描电子显微镜;丹东百特BT-9300H激光粒度仪;德国STA449C热重分析仪,分析环境为空气,从室温升至700ħ㊂2㊀结果与讨论2.1㊀产品结构及物性分析氨气沉淀法生成碱式硝酸铜的化学过程可表示为:4Cu(NO3)2+7H2O+6NH3ңCu4(NO3)2(OH)6㊃H2O+6NH4NO3(1)本文对产品进行了XRD表征,图1是在最佳条件:90ħ,通氨速率为500mL/min,通氨时间在40min 时制备的片状样品的XRD图谱,样品的衍射峰与国际衍射数据中心(ICDD)发布的PDF74-1749标准图谱一致,各特征峰尖锐且清晰,表明产物结晶良好,未见其他杂质如CuO等的特征峰,证明产品碱式硝酸铜纯度较好㊂在相同实验条件下产品的IR光谱如图2所示,其在1346和1046cm-1处表现出较强的吸收, 1046cm-1处的吸收是由于CuOH的弯曲振动㊂1346和878cm-1处的峰与NO3有关㊂并且,在400~800cm-1以不同间隔出现的峰是由于金属-氧键的存在㊂1422cm-1处的强峰显示了产物的良好结晶特征㊂此外,在1761和3400cm-1吸收带附近的区域与产物的OH基团和从空气中吸收的水分子有关㊂根538㊀研究论文人工晶体学报㊀㊀㊀㊀㊀㊀第52卷据上述分析,表明该产品可能是Cu 4(NO 3)2(OH)6㊃H 2O㊂图1㊀碱式硝酸铜的XRD 图谱Fig.1㊀XRD patterns of basic coppernitrate 图2㊀碱式硝酸铜的红外光谱图Fig.2㊀Infrared spectrum of basic copper nitrate 图3(a)㊁(b)是氨气沉淀法制备产品的SEM 照片,该产品有明显的棱角,大部分晶形完整,可以看到有类六方片状产物,制得的产品与气液冷凝法[14]制备的产品图3(c)㊁(d)相比分散性较高[15],产品尺寸均匀,厚度约为100nm,直径小于2μm,显露面平整无杂质㊂图3㊀碱式硝酸铜的SEM 照片Fig.3㊀SEM images of basic copper nitrate 对产物热重分析结果如图4所示㊂在产物的分解过程中有两个失重阶段㊂在40~210ħ的第一阶段失重是物理吸附水的解吸㊂在210~310ħ时,由于碱式硝酸铜微晶体的分解[16],曲线先迅速下降,后缓慢下降,在310ħ时趋于平缓,这是由硝酸铜氢氧化物分解引起的,原理为:2Cu 4(NO 3)2(OH)6㊃H 2O ң8CuO +4NO 2+8H 2O +O 2(2)实验数据失重率为39.52%,略高于理论失重率(39%),可以发现第二次失重时的起始分解温度比文献数据高约70ħ,这可能是由尺寸效应造成的[17]㊂图5是使用激光粒度仪对产品粒径测试结果,产品粒径分布较窄,粒径频率正态分布性好,且峰型尖锐,D 50为1.723μm,D 90为5.983μm,粒径分布集中,稳定性较为良好㊂㊀第3期王新安等:氨气沉淀法制备碱式硝酸铜及其形貌机理研究539㊀图4㊀碱式硝酸铜的热重曲线Fig.4㊀Thermogravimetric curve of basic coppernitrate 图5㊀碱式硝酸铜的粒径分布图Fig.5㊀Particle size distribution of basic copper nitrate 2.2㊀不同通氨速率对形貌的影响本文在温度为90ħ㊁通氨时间为40min,陈化时间在10min 的条件下,考察了3组不同通氨速率对碱式硝酸铜形貌的影响,所得实验结果如图6所示㊂当通氨速率在350mL /min 时,碱式硝酸铜产品大部分为团聚状态,当通氨速率在500mL /min 时,分散度得到了进一步的改善㊂图6㊀样品在不同通氨速率下的SEM 照片Fig.6㊀SEM images of the samples under different ammonia passing rates 当气态氨流速为200mL /min 时,大部分碱式硝酸铜产品处于团聚状态,但可以发现有罕见的纳米网结构㊂这种形貌的纳米网和文献[18-19]中的纳米网不同,文献报道的纳米网都是一种类似蜘蛛网的结构,从较为清晰的图7(b)可见,这种纳米网是由碱式硝酸铜纳米级颗粒排布而成的紧密二维结构,上面分布着纳图7㊀样品在通氨速率200mL /min 下的SEM 照片Fig.7㊀SEM images of the sample under the ammonia passing rate of 200mL /min米级的微孔,周围连接在体型较大的微米级结晶上㊂虽然还不清楚这种纳米网有哪些应用,但其网体本身肯定具有比三维结晶体更好的活性㊂该实验结果也印证了在NH 3-NH +4体系中,在缓冲效应的作用下能够获得一些较为理想甚至是罕见的形貌㊂如果通过进一步研究使这种二维结构从平方微米级扩大到平方毫米级,甚至更大,将对催化剂㊁新型材料㊁膜技术等领域产生重要影响㊂2.3㊀不同通氨时间对产品形貌的影响本实验在温度为90ħ㊁通氨气速度为500mL /min㊁陈化时间10min 条件下,考察了4组不同通氨时间对产品形貌的影响,所得实验结果如图8所示㊂540㊀研究论文人工晶体学报㊀㊀㊀㊀㊀㊀第52卷从图8中可看出,当反应时间低于40min 时,仅能见到叠拼在一起的片状物生成,分散性较差㊂通氨时间超过40min 时,产品为团聚的叶片插片㊂碱式硝酸铜产品收率随通氨时间呈先上升再下降的趋势,40min 为最佳通氨时间,产品收率可达50%(见图9)㊂收率下降的原因是当pHȡ13时,体系中的OH -浓度偏高,生成的碱式硝酸铜沉淀会以络离子的形式溶于过量的碱中,抽滤后的溶液中铜离子浓度增加,使铜离子回收不完全㊂图8㊀样品在不同通氨时间下的SEM 照片Fig.8㊀SEM images of the samples for different ammonia passingtime 图9㊀不同通氨时间下的产品收率Fig.9㊀Product yield for different ammonia passing time 2.4㊀反应温度对产品形貌的影响在不同温度下,氨气在溶液中的溶解度不同,OH -会随着温度升高而降低,但温度过高,产品的形貌会发生变化㊂从图10和图11中可以看出,当反应温度为90ħ时,所得产品收率最高,所得产品的形貌为长六方片,直径约为1μm㊂反应温度在50和70ħ的条件下形貌没有明显变化,产品分散性较差㊂反应温度>90ħ时,产品收率下降㊂从SEM 照片中也可以看出,在该温度下片状产物较之前减少,同时未见六方片状碱式硝酸铜产物生成㊂㊀第3期王新安等:氨气沉淀法制备碱式硝酸铜及其形貌机理研究541㊀图10㊀碱式硝酸铜在不同温度下的SEM 照片Fig.10㊀SEM images of basic copper nitrate at differenttemperatures 图11㊀不同反应温度下的产品收率Fig.11㊀Product yields at different reaction temperatures 3㊀生长机理分析3.1㊀计算模型与方法本文使用Material Studio 2020软件研究了碱式硝酸铜晶体形态形成的原因㊂碱式硝酸铜晶体数据来自无机晶体结构数据库(ICSD),序列号38152㊂碱式硝酸铜属于六方晶系,空间群为P 121/M 1,其晶胞参数为a =b =3.42,c =5.587,α=β=90ʎ,γ=90ʎ㊂构建了Cu 4(NO 3)2(OH)6㊃H 2O 的(001)㊁(111)㊁(200)㊁(201)㊁(121)㊁(022)㊁(122)㊁(103)㊁(320)和(041)面的真空slab 模型㊂计算采用CASTEP 程序中广义梯度近似(GGA)方法中的PBE 函数对Cu 4(NO 3)2(OH)6㊃H 2O 的(001)㊁(111)㊁(200)㊁(201)㊁(121)㊁(022)㊁(122)㊁(103)㊁(320)和(041)面进行结构优化㊂利用密度混合用于结构优化,波函数由BFGS 方法执行㊂计算考虑了准确性和效率㊂所有SCF tolerance 均设置为1.0ˑ10-4eV㊃atom -1,Energy cutoff 设置为260.00eV,Max.force 设置为0.05eV㊃Å-1,Max.displacement 设置为0.002Å(1Å=0.1nm),Max.stress 设置为0.1GPa㊂542㊀研究论文人工晶体学报㊀㊀㊀㊀㊀㊀第52卷3.2㊀形貌分析CASTEP 程序计算出碱式硝酸铜(001)㊁(111)㊁(200)㊁(201)㊁(121)㊁(022)㊁(122)㊁(103)㊁(320)和(041)面的理想生长形态如图12所示㊂由图12可见,碱式硝酸铜(001)面理想生长形貌为方片形,(111)面的理想生长形貌为长六方片形,(121)和(122)面的理想生长形貌为不规则六边形片状,可以预测出Cu 4(NO 3)2(OH)6㊃H 2O 结晶生长后的大部分会显露出长六方片形,但其中会夹杂一些不规则的六边形片形,这和图3所示的Cu 4(NO 3)2(OH)6㊃H 2O晶体的形貌基本一致㊂图12㊀碱式硝酸铜各真空slab 模型的生长习性Fig.12㊀Growth habit of each vacuum slab models of basic copper nitrate 3.3㊀碱式硝酸铜真空slab 模型的BFDH 计算本文主要采用Bravais-Friedel Donnay-Harker(BFDH)法[20-21]对晶体生长习性进行预测分析,通过该方法对Cu 4(NO 3)2(OH)6㊃H 2O 模型进行计算,结果如图13所示㊂计算得到的碱式硝酸铜(001)㊁(111)㊁(200)㊁(201)㊁(121)㊁(022)㊁(122)㊁(103)㊁(320)和(041)面的真空slab 模型主要生长晶面指数(hkl )㊁主要生长晶面的面积占晶面总面积的百分比(δ),以及晶体的生长原点和生长面间的中心距离(D )如表1所示㊂经过计算表明主要生长面为(001)㊁(001)㊁(100)㊁(100)㊁(010)和(010)㊂通过数据可以看出,主要生长晶面的面积占晶面总面积的百分比和生长原点和生长面间的中心距离成反比,这表明主要形貌为片状㊂(001)㊁(001)生长晶面在(001)㊁(111)晶面中的面积占晶面总面积的百分比最高,由此可以推出(001)㊁(111)为主要显露的晶面,主要生长形貌为六方片状,与图3(a)相符㊂为了进一步从电子结构的角度说明碱式硝酸铜晶体各晶面结构的稳定性差异,本文计算了Cu 4(NO 3)2(OH)6㊃H 2O (001)㊁(111)㊁(200)㊁(201)㊁(121)㊁(022)㊁(122)㊁(103)㊁(320)和(041)晶面态密度,结果如图13所示㊂由图13可以看出,碱式硝酸铜(001)㊁(111)㊁(200)㊁(201)㊁(121)㊁(022)㊁(122)㊁(103)㊁(320)和(041)面态密度图中每个能量分布范围有一定的差异性㊂电子密度主要由的s㊁p 和d 轨道态密度组成㊂大部分由d 轨道贡献,这是因为d 轨道位于价带的高能端,s 轨道在价带的最低能端,计算结果表明d 轨道在Cu 4(NO 3)2(OH)6㊃H 2O 的结构和稳定性中起主导作用㊂晶面原子层上的电荷密度在Cu 4(NO 3)2(OH)6㊃H 2O (001)面处最低,在Cu 4(NO 3)2(OH)6㊃H 2O (111)面处最高㊂可以看出,正是各晶面态密度的变化导致了Cu 4(NO 3)2(OH)6㊃H 2O 各结晶面结构稳定性的差别㊂从电子态密度图结合每个晶面的生长习性图来看,(001)面和(111)面相比其他晶面具有更多显现的优势,同时也在XRD 图谱中体现出碱式硝酸铜的宏观形态外观受(001)和(111)晶面影响较大㊂通过对比不同温度下的SEM 照片可以看出,随着温度的升高,逐渐形成类六方形,说明温度对(001)晶面有明显的影响㊂由于(001)面暴露相对较弱,一定程度上形成了以(111)面为主的长六方形片状及其他面的相应形貌㊂宏观㊀第3期王新安等:氨气沉淀法制备碱式硝酸铜及其形貌机理研究543㊀形态的非理想性是由非理想体系中不同形态晶面的不同程度重叠造成的㊂图13㊀碱式硝酸铜各真空slab 模型的态密度图Fig.13㊀Density of states of each vacuum slab models of basic copper nitrate544㊀研究论文人工晶体学报㊀㊀㊀㊀㊀㊀第52卷表1㊀碱式硝酸铜各真空slab模型的主要生长晶面指数(hkl)㊁主要生长晶面的面积占晶面总面积的百分比(δ),及生长原点和生长面间的中心距离(D)Table1㊀Main growth crystal plane indexes(hkl),the percentage of the area of the main growth crystal plane to the total crystal plane area(δ),and the center distance between the growth origin and the growth plane(D)ofeach vacuum slab models of basic copper nitrate(001)slab(111)slab(200)slab hklδ/%D/nm hklδ/%D/nm hklδ/%D/nm {001}28.21 5.93{001}21.327.51{001}18.627.83 {001}28.21 5.93{001}21.327.51{001}18.627.83 {010} 6.0616.49{010}8.2312.14{010} 6.9114.47 {010} 5.717.53{010}8.2312.14{010} 6.9114.47 {100} 5.5817.89{100}7.3813.54{011} 6.0716.45 {100} 5.5817.89{100}7.3813.54{011} 6.0716.45 {101} 5.318.85{011}7.3613.58{011} 6.0716.45 (201)slab(121)slab(022)slab hklδ/%D/nm hklδ/%D/nm hklδ/%D/nm {001}16.84 6.53{001}15.38.03{001}13.338.16 {001}16.84 6.53{001}15.38.03{001}13.318.16 {100}12.557.99{100}10.319.69{010}9.1710.89 {100}12.557.99{100}10.319.69{010}9.1710.89 {101}9.6810.32{010}9.0811{011}7.3413.61 {101}9.6810.32{010}9.0811{011}7.3413.61 {101}9.6810.32{101}7.9412.58{011}7.3413.61 (122)slab(103)slab(041)slab(320)slab hklδ/%D/nm hklδ/%D/nm hklδ/%D/nm hklδ/%D/nm {001}12.758.15{001}12.44 5.36{001}12.26 3.54{001}12.25 4.68 {001}12.758.15{001}12.44 5.36{001}12.26 3.54{001}12.25 4.68 {100}12.058.29{100}11.938.37{010}11.478.71{010}11.558.65 {100}12.058.29{100}11.938.37{010}11.478.71{010}11.558.65 {010}8.8611.27{101}10.059.94{011}10.629.41{011}10.169.83 {010}8.8611.27{101}10.059.94{01-1-}10.629.41{011}10.169.83 {101}8.5911.63{101}10.059.94{011}10.629.41{011}10.169.83 4㊀结㊀㊀论采用氨气沉淀法对碱式硝酸铜,对其生成条件㊁形貌和合成机理进行了研究,得出以下结论:1)采用氨气沉淀法制备多种形貌的微米级碱式硝酸铜,NH3-NH+4体系的存在对理想形貌的获得起重要作用㊂2)研究了通氨时间㊁通氨速率和反应温度对产品形貌和产品收率的影响,最佳反应条件为:通氨时间40min,反应温度90ħ,通氨速率500mL/min㊂得到的产品呈长六方片状结构,结晶对称性良好,宏观形貌较为理想㊂3)发现由纳米级碱式硝酸铜颗粒紧密排布而成的二维纳米网状结构,上面分布有纳米级微孔㊂4)采用BFDH法计算碱式硝酸铜的晶面微观性质,结果表明,主要生长面为(001)㊁(001)㊁(100)㊁(100)㊁(010)和(010)㊂另外,(001)面为主晶面,(111)面为经常出现的晶面,晶体呈六方形片状,与实验结果一致㊂态密度计算结果表明,d轨道对各晶面的结构稳定性起主导作用㊂参考文献[1]㊀戴良玉,吴望发,方遵华,等.新一代汽车安全气囊产气新材料-纳米体碱式硝酸铜[DB/OL].(2014-05-10).[2023-02-04].https:///KCMS/detail.aspx?dbname=SNAD&filename=SNAD000001584496.DAI L Y,WU W F,FANG Z H et al.A new generation of new-generation automotive airbag gas-producing materials-nanobody basic copper nitrate[DB/OL].(2014-05-10).[2023-02-04].https:///KCMS/detail.aspx?dbname=SNAD&filename= SNAD000001584496.㊀第3期王新安等:氨气沉淀法制备碱式硝酸铜及其形貌机理研究545㊀[2]㊀LIU Y,LIU Y,SHI H H,et al.Cobalt-copper layered double hydroxide nanosheets as high performance bifunctional catalysts for rechargeablelithium-air batteries[J].Journal of Alloys and Compounds,2016,688:380-387.[3]㊀石俊涛,王㊀妮,王秋雨.安全气囊气体发生剂用碱式硝酸铜的对比研究[J].化学推进剂与高分子材料,2017,15(1):56-59.SHI J T,WANG N,WANG Q Y.Contrastive study of basic copper nitrate for gas generating agent in safety airbag[J].Chemical Propellants& Polymeric Materials,2017,15(1):56-59(in Chinese).[4]㊀徐㊀爽.杀菌剂用纳米氢氧化铜的制备及应用性能研究[D].北京:中国科学院大学(中国科学院过程工程研究所),2018.XU S.Preparation and application performance of nano-copper hydroxide for bactericides[D].Beijing:Institute of Process Engineering,Chinese Academy of Sciences,2018(in Chinese).[5]㊀景志红,焦兆友,庞秋云,等.一种纳米氧化铜抗菌剂的制备方法:CN101273723[P].2008-10-01.JING Z H,JIAO Z Y,PANG Q Y,et al.A preparation method of nanometer copper oxide antibacterial agent:CN101273723[P].2008-10-01 (in Chinese).[6]㊀KRATOHVIL S,MATIJEVIC'E.Preparation of copper compounds of different compositions and particle morphologies[J].Journal of MaterialsResearch,1991,6(4):766-777.[7]㊀HENRIST C,TRANINA K,HUBERT C,et al.Study of the morphology of copper hydroxynitrate nanoplatelets obtained by controlled double jetprecipitation and urea hydrolysis[J].Journal of Crystal Growth,2003,254(1/2):176-187.[8]㊀LI B C,JECHAN L,EILHANNI K et al.2-dimensional nanoleaf-like porous copper nitrate hydroxide as an effective heterogeneous catalyst forselective oxidation of hydroxymethylfurfural to diformylfuran[J].Journal of the Taiwan Institute of Chemical Engineers,2021,126:189-196.[9]㊀范天博,贾晓辉,韩冬雪,等.以白云石为原料氨碱法制备球霰石及其生成机理研究[J].无机盐工业,2021,53(5):56-60.FAN T B,JIA X H,HAN D X,et al.Study on preparation of vaterite from dolomite by ammonia-alkali method and its mechanism[J].Inorganic Chemicals Industry,2021,53(5):56-60(in Chinese).[10]㊀范天博,姜㊀宇,刘露萍,等.一步水热法合成六方片状氢氧化镁及其生长习性分析的研究[J].人工晶体学报,2017,46(12):2319-2325.FAN T B,JIANG Y,LIU L P,et al.Crystal growth habit of hexagonal flake magnesium hydroxide synthesized by one-stepHydrothermal method[J].Journal of Synthetic Crystals,2017,46(12):2319-2325(in Chinese).[11]㊀周永红,范天博,刘露萍,等.六方片状氢氧化镁的合成及其第一性原理分析[J].化工学报,2016,67(9):3843-3849.ZHOU Y H,FAN T B,LIU L P,et al.Preparation of hexagonal plates of magnesium hydroxide and mechanism analysis with first principles[J].CIESC Journal,2016,67(9):3843-3849(in Chinese).[12]㊀ZHAN J,LIN H P,MOU C Y.Biomimetic formation of porous single-crystalline CaCO3via nanocrystal aggregation[J].Advanced Materials,2003,15(78):621-623.[13]㊀HUANG Z Q,ZHANG G S,TAN Y.Gelatinous siphon sheath templates the starfruit-shaped aragonite aggregate growth[J].Journal ofNanomaterials,2019,2019:1-9.[14]㊀DI L B,DUAN D Z,ZHAN Z B,et al.Nanosheets:gas-liquid cold plasma for synthesizing copper hydroxide nitrate nanosheets with highadsorption capacity[J].Advanced Materials Interfaces,2016,3(24):no.[15]㊀唐福兴.一种纳米体碱式硝酸铜的合成及应用研究[J].化工技术与开发,2018,47(8):25-27.TANG F X.Synthesis and application research of a new nanometer body alkali nitric acid copper[J].Technology&Development of Chemical Industry,2018,47(8):25-27(in Chinese).[16]㊀NIU H X,YANG Q,TANG K B.A new route to copper nitrate hydroxide microcrystals[J].Materials Science and Engineering:B,2006,135(2):172-175.[17]㊀姜慧娜,宋小军,刘伟景,等.纳米氧化铜尺寸效应对其湿度传感特性的影响[J].微纳电子技术,2018,55(9):630-634.JIANG H N,SONG X J,LIU W J,et al.Influence of the size effect of nanometer CuO on its humidity sensing property[J].Micronanoelectronic Technology,2018,55(9):630-634(in Chinese).[18]㊀NISTICÒR,NOVARA C,CHIADÒA,et al.Cysteine-mediated synthesis of silver nanonets and their use for surface enhanced raman scattering(SERS)[J].Materials Letters,2019,247:208-210.[19]㊀BERLY R,GOBI N.A concise review on electrospun nanofibres/nanonets for filtration of gaseous and solid constituents(PM2.5)from pollutedair[J].Colloid and Interface Science Communications,2020,37:100275.[20]㊀冯璐璐,曹端林,王建龙,等.1-甲基-2,4,5-三硝基咪唑的晶体形貌预测[J].含能材料,2015,23(5):443-449.FENG L L,CAO D L,WANG J L,et al.Prediction of crystal morphology of MTNI[J].Chinese Journal of Energetic Materials,2015,23(5): 443-449(in Chinese).[21]㊀王小军,秦㊀亮,何㊀丹,等.2,4,6-三硝基-2,4,6-三氮杂环己酮的晶体形貌预测[J].化学研究,2012,23(2):17-21.WANG X J,QIN L,HE D,et al.Prediction of crystal morphology of1-oxo-2,4,6-trinitro-2,4,6-triazacyclohexane[J].Chemical Research, 2012,23(2):17-21(in Chinese).。
碱式碳酸铜实验室制法的改进(无机某设计实验方案,有用的)

收稿日期:2002-05-05作者简介:魏兴国(1970-),男,山东陵县人,理学学士,德州学院化学系讲师,从事无机化学实验教学工作.第18卷第4期2002年12月德州学院学报Journal of Dezhou University Vol.18No.4Dec.2002碱式碳酸铜实验室制法的改进魏兴国,董岩,孟繁宗,刘新华(德州学院化学系,山东德州 253023)摘 要:通过对利用硝酸铜与碳酸氢铵制备碱式碳酸铜反应条件的测试,得到该制备的最佳实验步骤.并用化学平衡原理分析了该方法的理论依据及优势所在.关键词:碱式碳酸铜;制备;抽滤;物质的量中图分类号:O61-3 文献标识码:B 文章编号:1004-9444(2002)04-0036-03 碱式碳酸铜[CuCO 3・Cu (OH )2・xH 2O ]呈暗绿色或淡蓝绿色粉末状固体,是天然孔雀石的主要成分.易溶于稀酸和氨水,不溶于水,加热至200℃即分解,新制备的样品在沸水中就很易分解[1].主要用于固体荧光粉的激活剂和铜盐制造,油漆、颜料和烟火的配制等[2].通常由可溶性的铜盐和可溶性的碳酸盐制备.实验室中常用硫酸铜溶液和碳酸钠溶液进行复分解反应制备碱式碳酸铜[1].笔者据此进行了大量实验,发现该反应条件难以控制,且副产物较多,产率较低或以副产物为主.究其原因,碳酸钠溶液本身碱性较强,当硫酸铜与碳酸钠溶液混合时,则有三种不同的化合物生成,即水合碱式碳酸铜(形成大型沉淀),水合碱式硫酸铜及氢氧化铜.而三种产物的组成百分比与反应物配比和反应温度有很大关系.由于三种产物均为不溶或难溶物,故分离也有一定难度.另外,由于SO 42-离子体积较大,也易形成包合物,因此,笔者尝试利用硝酸铜与碳酸氢铵溶液反应制备碱式碳酸铜,取得了较好效果.1 实验1.1 实验条件的探求1)Cu (NO 3)2与N H 4HCO 3最佳物质的量比取5份0.5mol ・l -1的Cu (NO 3)2溶液10ml ,另分别取1.0mol ・l -1的N H 4HCO 3溶液6mL 、8mL 、10mL 、12mL 、14mL 于已经编号100mL 烧杯中.在室温条件下,依次将Cu (NO 3)2溶液分别倒入N H 4HCO 3溶液中,并不断搅拌.充分反应后,静置,抽滤,用蒸馏水洗涤2~3次,将产品在烘箱中于100℃烘干.冷至室温后称重,计算产率.实验结果列表1表1 硝酸铜与碳酸氢铵物质量比对反应产物的影响3V NH4HCO36mL 8mL 10mL 12mL 14mL 产率43.8%78.4%85.3%85.7%85.9%产物颜色翠绿色翠绿色翠绿色翠绿色翠绿色产物品质颗粒大颗粒大颗粒较大颗粒较大颗粒较大品质好品质好品质好品质好品质好 3Cu(NO3)2均为10mL0.5mol・l-1的溶液 由表1可以看出:在Cu(NO3)2与N H4HCO3的物质的量之比为1∶2(即N H4HCO3的体积为10mL时)时,产率已经开始趋于平衡,且产物品质较好,因此可以把此时的物质的量之比作为反应物的最佳配比。
碱式碳酸铜

碱式碳酸铜碱式碳酸铜碱式碳酸铜又称碳酸铜,呈孔雀绿颜色,所以又叫孔雀石,是一种名贵的矿物宝石。
它是铜与空气中的氧气、二氧化碳和水等物质反应产生的物质,又称铜锈,颜色翠绿。
在空气中加热会分解为氧化铜、水和二氧化碳。
溶于酸并生成相应的铜盐。
在自然界中以孔雀石的形式存在。
[1]中文名碱式碳酸铜英文名Copper carbonate basic别称碳酸铜、盐基性碳酸铜化学式Cu2(OH)2CO3分子量221.12CAS登录号12069-69-1EINECS登录号235-113-6熔点220oC水溶性不溶于水和醇。
密度 3.85g/mL外观孔雀绿色细小无定型粉末应用有机催化剂、烟火制造、颜料等目录1物化性质2制备方法3主要用途4计算化学数据5储运特性6危害说明毒理学数据生态学数据7安全信息安全术语风险术语1、物化性质性状:孔雀绿色细小无定型粉末。
不溶于水和醇。
溶于酸、氨水及氰化钾溶液。
[2]常温常压下稳定。
[2]碱式碳酸铜化学分子结构式2.避免的物料酸。
不溶于冷水和醇,在热水中分解,溶于酸而成相应铜盐。
溶于氰化物、氨水、铵盐和碱金属碳酸盐水溶液中,形成铜的络合物。
在碱金属碳酸盐溶液中煮沸时,形成褐色氧化铜。
对硫化氢不稳定。
加热至200℃分解黑色氧化铜、水和二氧化碳。
在硫化氢气氛中不稳定。
在水中的溶解度为0.0008%。
碳酸铜具有扬尘性,应避免与皮肤、眼睛等接触及吸入。
[2]3.不溶于水,溶于氨水中生成铜氨配离子。
加热到220℃时分解。
组成为2∶1的碱式碳酸铜为天蓝色的粉状结晶。
如在空气中长时间放置,则吸湿并放出部分二氧化碳,慢慢变成1∶1型碱式碳酸铜,不溶于水,但溶于氨水而形成铜氨配离子。
[2]2、制备方法1.硫酸铜法。
反应方程式:2CuSO4+4NaHCO3==CuCO3·Cu(OH)2↓+2Na2SO4+3CO2↑+H2O碱式碳酸铜操作方法:将小苏打配成相对密度1.05的溶液,先加入反应器中,于50℃时,在搅拌下加入经精制的硫酸铜溶液,控制反应温度在70~80℃,反应以沉淀变为孔雀绿色为度,pH值保持在8,反应后经静置、沉降,用70~80℃水或去离子水洗涤至洗液无SO2-4止,再经离心分离、干燥,制得碱式碳酸铜成品。
一种纳米体碱式硝酸铜的合成及应用研究

第 47 卷 第 8 期2018 年 8 月Vol.47 No.8Aug. 2018化工技术与开发Technology & Development of Chemical Industry一种纳米体碱式硝酸铜的合成及应用研究唐福兴1,2,3(1.三明医学科技职业学院轻纺工业系,福建 三明 365000;2.三明市火龙纺织化工有限公司,福建 三明 365000;3.三明东昇化工有限公司,福建 三明 365000)摘 要:本文研究了纳米体碱式硝酸铜的合成工艺路线、合成原理、工艺流程等,并采用电子隧道扫描显微成像仪对其形貌、比表面积、最可几孔径和粒度进行测试。
结果表明,采用本工艺生产的纳米体碱式硝酸铜,比表面积大,成本低,外观粒径可调可控,流散性好,颗粒均匀,有很强的燃烧催化性能,能满足汽车安全气囊产气剂材料的要求。
关键词:纳米体碱式硝酸铜;合成;应用研究中图分类号: O 614.121;TQ 567.8 文献标识码:A 文章编号:1671-9905(2018)08-0025-03作者简介:唐福兴(1964-),男,福建福州人,工程师,主要从事染整化学基础教学与科研。
E-mail: 361049035@ 收稿日期:2018-06-13新一代气囊气体发生剂的理论设计,要求碱式硝酸铜的比表面积大、成本低、外观粒径可调可控、流散性好、颗粒均匀,产品应具有很强的燃烧催化性能,可提高气囊的爆发速度。
我国汽车安全气囊研究开发工作还处在起步阶段,除少数科研人员在较早前开始对高比表面积和高燃烧速度的碱式硝酸铜进行理论研究和实验研究外,国内尚没有开展纳米体碱式硝酸铜的研发和在汽车安全气囊上的应用研究[1-3]。
目前国内外少数几家企业生产碱式硝酸铜的主要方法,是将普通硝酸铜和片碱采用合成工艺,生产D50小于1.5μm 的碱式硝酸铜,很难对产品的粒度分布进行有效控制。
这种普通碱式硝酸铜的比表面积小,很难达到产气材料理论配方对碱式硝酸铜的催化性能和燃烧速度的设计要求[4-6]。
碱式硝酸铜制备

碱式硝酸铜制备
碱式硝酸铜(Cu(NO3)2·3Cu(OH)2)可以通过硝酸铜与氢氧化钠反应制备。
制备步骤如下:
1. 首先将一定量的硝酸铜溶液慢慢加入氢氧化钠溶液中,同时搅拌。
反应过程中会观察到溶液逐渐变白。
2. 继续搅拌反应混合物,直到没有进一步的颜色变化。
3. 将反应混合物过滤,得到固体沉淀。
4. 用去离子水洗涤沉淀,以去除杂质。
5. 最后用醇溶剂洗涤沉淀,以去除溶液中的剩余离子。
6. 将沉淀过滤并晾干,得到碱式硝酸铜。
需要注意的是,在制备过程中,要保证反应物质量比为1:3,即硝酸铜与氢氧化钠的摩尔比为1:3。
此外,反应要在室温下进行,并搅拌均匀,以促进反应的进行。
碱面铜实验报告(3篇)

第1篇一、实验目的1. 观察碱面铜在加热过程中的颜色变化。
2. 了解碱面铜的制备方法。
3. 掌握实验室安全操作规程。
二、实验原理碱面铜是一种无机化合物,化学式为Cu(OH)2。
在加热过程中,碱面铜会分解生成氧化铜(CuO)和水(H2O)。
实验中,通过观察碱面铜加热过程中的颜色变化,可以了解其分解过程。
反应方程式如下:Cu(OH)2 → CuO + H2O三、实验材料与仪器1. 实验材料:碱面铜、酒精灯、镊子、试管、试管夹、滤纸、滴管、蒸馏水、氢氧化钠溶液、硫酸铜溶液、硝酸溶液、盐酸溶液。
2. 实验仪器:电子天平、研钵、烧杯、玻璃棒、移液管、容量瓶、滴定管、试管架、酒精灯、石棉网、烘箱。
四、实验步骤1. 准备工作:将碱面铜放入研钵中,用研棒研磨成粉末状,备用。
2. 取一小部分碱面铜粉末放入试管中,用滴管加入适量的蒸馏水,搅拌均匀。
3. 用酒精灯加热试管,观察碱面铜的颜色变化。
加热过程中,试管口应略微倾斜,避免水分过多蒸发。
4. 当碱面铜粉末开始变黑时,停止加热,用滤纸擦拭试管内壁,观察颜色变化。
5. 将试管中的黑色物质转移到另一个试管中,加入适量的氢氧化钠溶液,观察是否产生蓝色沉淀。
6. 若产生蓝色沉淀,说明黑色物质为氧化铜。
否则,为其他物质。
7. 用移液管取一定量的硫酸铜溶液,滴入黑色物质中,观察是否产生蓝色沉淀。
8. 若产生蓝色沉淀,说明黑色物质为氧化铜。
否则,为其他物质。
9. 将黑色物质放入烧杯中,加入适量的硝酸溶液,观察是否溶解。
10. 若黑色物质溶解,说明其中含有铜离子。
否则,为其他物质。
11. 将黑色物质过滤,用蒸馏水洗涤沉淀,烘干后称重,计算实验数据。
五、实验结果与分析1. 在加热过程中,碱面铜粉末由白色变为蓝色,最后变为黑色。
这表明碱面铜在加热过程中发生了分解,生成了氧化铜。
2. 加入氢氧化钠溶液后,黑色物质产生蓝色沉淀,说明其中含有铜离子。
3. 加入硫酸铜溶液后,黑色物质产生蓝色沉淀,进一步证实了其中含有氧化铜。
碱式硝酸铜对硝酸胍燃烧性能的影响

碱式硝酸铜对硝酸胍燃烧性能的影响摘要:本文以充气式发生器的气体发生剂为背景进行探索,研究了碱式硝酸铜比例分配对硝酸胍燃烧性能的影响。
通过实验分析,随着碱式硝酸铜质量百分含量的增加,配方的燃速得以增加。
关键词:燃烧性能气体发生剂碱式硝酸铜近年来,国民经济的快速发展推动了汽车的需求量急速扩张,加速了汽车产业的发展。
2011年我国汽车产销量达到1850万辆,相关产业创造的产值近4万亿元,汽车产业已成为国家支柱产业之一。
汽车产业的发展为汽车零部件提供了发展基础;作为汽车重要零部件的汽车安全气囊在国家政策的引导下,越来越普及,已成为乘用车的标准配件[1-4];随着生活水平的提高,促使人们越来越关心安全,为汽车安全气囊气体发生器提供了越来越广阔的市场空间。
安全气囊通常由传感器、控制器、气体发生器、气囊等部分组成[5]。
其中以气体发生器尤为重要,它是安全气囊气囊系统的核心部件,在汽车发生碰撞时,它能在50ms内迅速使气囊充气膨胀,保证乘员生命安全[6-8]。
气体发生器由气体发生剂和金属零部件组成。
气体发生剂是指燃烧后产生气体的各种物质,属于固体推进剂的一个种类[9],把气体发生剂装入气体发生器中,在车辆发生碰撞时引发,产生大量的气体,充满气囊的囊体。
汽车安全气囊气体发生剂前期主要是叠氮化钠类型的气体发生剂配方,具有燃烧稳定、燃温低、易点火、内压低、产气率高、残渣少等很多优点。
但是在生产过程中有许多缺陷,如易与重金属反应造成燃烧爆炸事故;同时叠氮化钠是剧毒物质,0.05g以上计量可致人死亡;最后是难于回收、易于泄露等环保问题。
这些缺陷导致在后期的气体发生剂研发过程中,很少或不使用叠氮配方。
目前,世界上各大气体发生器生产公司和研究机构纷纷在研究无毒型气体发生剂[10],无毒型气体发生剂也称为非叠氮类气体发生剂,主要使用的是高能量、低感度、大产气量、环保、价廉的物质。
最常用的是硝酸胍作为可燃物质的配方。
硝酸胍因为其本身便宜、感度低、安全性佳、产气量大、无毒等优点,成为目前国内外主流的气体发生剂物质。
碱的化学性质PPTPPT课件演示文稿

特点:(1)反应物、生成物均只有两种化
合物;
(2)发生反应的两种化合物相互交换 成分;
(3)各元素的化合价在反应前后均 不改变。
第18页,共22页。
碱溶液中含有相同的离子OH指示剂①
非金属氧化物 → 盐 + 水②
碱
酸 -中----和----反----应---→ 盐 + 水③ 盐 → ---------------- 盐 + 碱④
碱的化学性质PPTPPT课件演 示文稿
第1页,共22页。
(优质)碱的化 学性质PPTPPT课
件
第2页,共22页。
俗称
颜色 状态
氢氧化钠
烧碱、火碱、苛性 钠
白色片状固体
氢氧化钙
熟石灰、消 石灰
白色粉末 状固体
溶解性 易溶于水
微溶
腐蚀性
是否 潮解 溶解热 量变化
强腐蚀性 易潮解
溶解放热
有腐蚀性
不易潮解
4、在硫酸铜溶液中滴加石灰水。
CuSO4 + Ca(OH)2 = Cu(OH)2↓+ CaSO4
第7页,共22页。
3、碱跟非金属氧化物反应 [实验]: 向一支盛有澄清石灰水的试管中通入 二氧化碳,观察发生了什么现象:
澄清石灰水变浑浊。
化学反应方程式:
CO2 + Ca(OH)2 = CaCO3↓+ H2O 这一反应常用来检验二氧化碳的存在。
A.氢离子
B.氢氧根离子
C.金属离子
D.酸根离子
第22页,共22页。
在岁月
碱 + 盐→ 新盐 + 新碱
碱铜及其在家禽中的应用ppt实用资料

梁超博士 Micronutrients, Asia
1
目录
• 同质多晶现象与α 碱铜 • α 碱铜的作用机理 • α 碱铜对家禽的经济效益 • 铜元素:基本需求与最佳效益水平
2
化合物的同质异构现象
同分异构体
构型异构
(葡萄糖 VS 果糖)
几何异构
晶型异构
(钻石VS石墨)
非对映异构
conformations; the structures of seven
60只鸡×6(添加抗生素,一种大环类+一种四环素类) Peyer’s patch/ 肠道淋巴组织(GALT)
polymorphs (shown)
The simple molecule ROY forms at least ten polymorphs with different colors and molecular conformations; the structures of seven
虫药) ③ 对照+200ppm Cu (TBCC) ④ 空白对照+200ppm Cu (TBCC) ⑤ 每个处理: 200只鸡×6组
23
大白鸡饲养试验-效益分析
处理
体重(kg) 死亡率(%) FCR
对照
2.45
15.69
2.12
空白对照
2.55
14.13
2.10
对照+TBCC
2.61
12.99
2.01
4.3 小淋巴细胞 5. 单核细胞 6. 红细胞 7. 血小板
8. 浆细胞
9.核的残余
猪血
鸡血
猪血涂片 鸡血涂片
17
18
Peyer’s patch/ 肠道淋巴组织(GALT)
氢氧化钠和硝酸铜反应-概述说明以及解释

氢氧化钠和硝酸铜反应-概述说明以及解释1.引言1.1 概述氢氧化钠和硝酸铜是一种常见的化学反应体系,两者之间的反应在化学实验和工业生产中都具有重要意义。
氢氧化钠是一种碱性化合物,能够与酸性物质发生中和反应,而硝酸铜则是一种含有铜离子的盐类化合物。
本文将对氢氧化钠和硝酸铜的性质进行介绍,探讨它们之间的反应机理,并通过实验操作和结果观察来验证实验结论。
通过深入研究这一体系的化学反应过程,我们可以更好地了解这两种物质的性质和特点,为其在实际应用中的运用提供参考和指导。
1.2 文章结构:本文将分为引言、正文和结论三个部分。
在引言部分中,将介绍氢氧化钠和硝酸铜反应的背景和意义,以及本文的研究目的。
在正文部分,将详细探讨氢氧化钠和硝酸铜的性质,以及它们之间的反应机理。
同时,将介绍实验操作方法和结果观察。
最后,在结论部分将对实验结果进行分析总结,讨论反应的特点,并展望氢氧化钠和硝酸铜反应在潜在应用方面的可能性。
整篇文章将以科学严谨的态度进行论述,旨在为读者提供关于该反应的全面了解和深入探讨。
json"1.3 目的": {"目的": "本文旨在探究氢氧化钠和硝酸铜之间的化学反应,研究其反应机理和产物特性,为进一步理解这一反应提供参考和指导。
通过实验操作和结果观察,深入分析反应过程中的关键步骤,以期揭示该反应的特点和潜在应用领域。
"}"3.2 反应特点总结": {},"3.3 潜在应用和展望": {}}}}请编写文章1.3 目的部分的内容2.正文2.1 氢氧化钠和硝酸铜的性质氢氧化钠是一种无机化合物,化学式为NaOH,常见的固体形式为白色固体,是一种强碱性物质。
在水中溶解时会产生氢氧根离子和钠离子,使溶液呈现碱性。
氢氧化钠具有腐蚀性强、与蛋白质和脂肪反应等特点。
硝酸铜是一种含有铜离子和硝酸根离子的化合物,化学式为Cu(NO3)2,是一种深蓝色结晶固体。
硝酸铜安全技术说明书MSDS

第一部分化学品及企业标识化学品中文名:硝酸铜化学品英文名:cupricnitrateCASNo.:10031-43-3ECNo.:221-838-5分子式:Cu(NO3)2∙3(H2O)产品推荐及限制用途:工业及科研用途。
第二部分危险性概述紧急情况概述:固体。
跟可燃物质接触可能会引起火灾。
对水生物有剧毒,使用适当的容器,以预防污染环境。
对水生环境可能会引起长期有害作用。
使用适当的容器,以预防污染环境。
GHS危险性类别:根据《危险化学品分类信息表》(2015)危险性类别判定,该产品分类如下:氧化性固体,类别2;危害水生环境-急性毒性,类别1;危害水生环境-慢性毒性,类别1。
标签要素象形图:φ<t>警示词:危险危险信息:可能加剧燃烧;氧化剂,对水生生物毒性极大,对水生生物毒性极大并具有长期持续影响。
预防措施:远离热源、热表面、火花、明火以及其它点火源。
禁止吸烟。
远离服装和其他可燃材料P避免释放到环境中。
戴防护手套/穿防护服/戴防护眼罩/戴防护面具。
事故响应:收集溢出物。
安全储存:不适用。
废弃处置:按照地方/区域/国家/国际规章处置内装物/容器。
物理化学危险:跟可燃物质接触可能会引起火灾。
健康危害:吸入该物质可能会引起对健康有害的影响或呼吸道不适。
意外食入本品可能对个体健康有害。
通过割伤、擦伤或病变处进入血液,可能产生全身损伤的有害作用。
眼睛直接接触本品可导致暂时不适。
环境危害:本品对水生生物毒性极大。
本品对水生生物毒性极大并具有长期持续影响。
第三部分成分/组成信息。
物质混合物第四部分急救措施一般性建议:急救措施通常是需要的,请将本SDS出示给到达现场的医生。
皮肤接触:立即脱去污染的衣物。
用大量肥皂水和清水冲洗皮肤。
如有不适,就医。
眼睛接触:用大量水彻底冲洗至少15分钟。
如有不适,就医。
吸入:立即将患者移到新鲜空气处,保持呼吸畅通。
如果呼吸困难,给于吸氧。
如患者食入或吸入本物质,不得进行口对口人工呼吸。
硝酸铜和氢氧化钠的反应_概述说明以及解释

硝酸铜和氢氧化钠的反应概述说明以及解释1. 引言1.1 概述本文旨在探讨硝酸铜和氢氧化钠之间的反应,涉及到反应的概述、机理解释以及实际应用与意义等方面。
通过深入分析该反应的原理和特点,我们可以更好地理解其在工业领域和实验室中的应用,并进一步探讨与环境和生态问题相关的议题。
1.2 文章结构本文将按照以下结构展开对硝酸铜和氢氧化钠反应的讨论:- 引言:介绍文章主题,概述文章内容以及阐明研究目的。
- 反应概述:对硝酸铜和氢氧化钠反应进行简要介绍,包括反应方程式、反应条件和观察结果等方面的内容。
- 反应机理解释:阐述硝酸铜和氢氧化钠反应的离子反应机制分析、氧化还原反应解释以及沉淀生成反应机理说明等内容。
- 实际应用与意义:讨论硝酸铜和氢氧化钠反应在工业领域、实验室中的具体应用,并探讨其与环境和生态问题的相关性。
- 结论:总结本文主要内容并提出未来研究方向或深入研究建议,最后以结束语作为文章的收尾。
1.3 目的本文旨在提供关于硝酸铜和氢氧化钠反应的详细概述说明和解释,以便读者对该反应有一个全面而深入的理解。
通过分析该反应的机理和实际应用,我们可以认识到它在工业领域和实验室中的重要性,并进一步思考其对环境和生态问题可能产生的影响。
2. 反应概述2.1 硝酸铜和氢氧化钠的反应介绍硝酸铜和氢氧化钠之间发生的反应是一种典型的双替代反应。
在此次反应中,硝酸铜与氢氧化钠反应生成了沉淀和水。
该反应可以用于定性分析以及实验室合成中,也具有一定的工业领域应用。
2.2 反应方程式硝酸铜(Cu(NO3)2)与氢氧化钠(NaOH)反应时,生成了硫酸铜(Cu(OH)2)沉淀和水(H2O)。
其简化的化学方程式如下所示:Cu(NO3)2 + 2NaOH →Cu(OH)2 + 2NaNO32.3 反应条件和观察结果硝酸铜和氢氧化钠的反应通常在常温下进行。
当将两种溶液缓慢混合时,会观察到产生了一种蓝色沉淀物,并伴随着释放出部分热量。
这个蓝色沉淀物即为硫酸铜。
氢氧化钠和硝酸铜反应化学方程

氢氧化钠和硝酸铜反应化学方程2NaOH+Cu(NO3)2→Cu(OH)2+2NaNO3该化学方程式表示,当加入2 mol的氢氧化钠和1 mol的硝酸铜时,反应会发生,生成1 mol的氢氧化铜和2 mol的硝酸钠。
下面我将详细解释该反应的机理和反应条件。
首先,氢氧化钠(NaOH)和硝酸铜(Cu(NO3)2)是两种常见的化学物质。
氢氧化钠是一种白色、结晶性固体,其分子式为NaOH。
它是一种碱性物质,可以与酸反应生成盐和水。
硝酸铜是一种蓝色、结晶性固体,其分子式为Cu(NO3)2、它是一种金属盐,可溶于水。
由于氢氧化钠和硝酸铜具有不同的性质,它们可以通过反应生成不同的物质。
当氢氧化钠和硝酸铜混合时,发生了一系列的化学变化。
首先,溶解在水中的硝酸铜分子(Cu(NO3)2)会与氢氧化钠中的氢氧根离子(OH-)发生反应。
反应产生的产物中,一个氮原子和两个氧原子的组合形成了一个硝酸离子(NO3-),而铜(Cu)离子与水中的氢氧根离子结合形成了氢氧化铜物质(Cu(OH)2)。
在反应中,硝酸铜的亲电性较强,可以引发产物中的若干离子之间的反应。
这些离子的结合导致了新的物质的生成。
而氢氧化钠中的碱性氢氧根离子与铜离子结合形成了氢氧化铜。
氢氧化铜是一种浅蓝色的物质,具有一定的溶解度。
它在水中溶解时可以形成含有铜离子和氢氧根离子的溶液。
而硝酸钠是一个盐,具有较高的溶解度。
在这种反应中,溶液中的离子在化学反应中发生了重新组合,形成了新的物质。
总的来说,氢氧化钠和硝酸铜之间的反应是一种酸碱反应。
通过溶液中的离子间的相互作用,形成了具有新性质的物质。
这个反应是可逆的,可以通过改变反应条件来改变反应的进行程度。
在实际应用中,这种反应广泛用于制备和处理含有铜和氢氧化钠的化学材料,用于制备氢氧化铜和硝酸钠等物质。
总之,氢氧化钠和硝酸铜之间的反应可以用化学方程式2NaOH+Cu(NO3)2→Cu(OH)2+2NaNO3来表示。
这个反应是一种酸碱反应,通过溶液中的离子间的相互作用,形成了具有新性质的物质。
硝酸铜的理化性质和危险特性(表-)
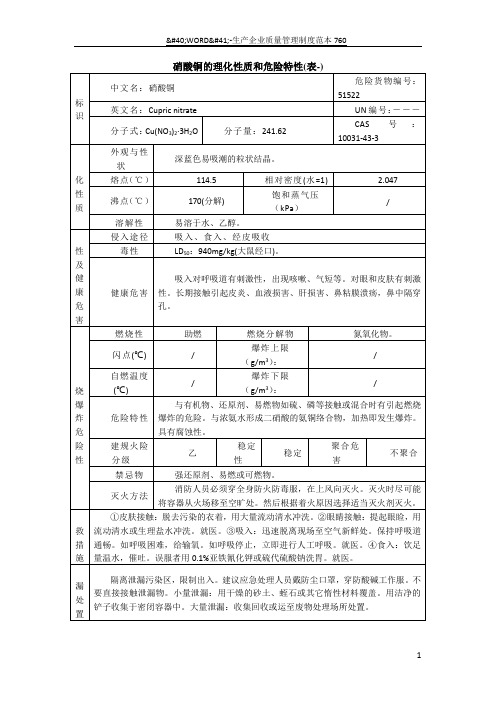
自燃温度(℃)
/
爆炸下限(g/m3):
/
危险特性
与有机物、还原剂、易燃物如硫、磷等接触或混合时有引起燃烧爆炸的危险。与浓氨水形成二硝酸的氨铜络合物,加热即发生爆炸。具有腐蚀性。
建规火险分级
乙
稳定性
稳定
聚合危害
不聚合
禁忌物
强还原剂、易燃或可燃物。
灭火方法
消防人员必须穿全身防火防毒服,在上风向灭火。灭火时尽可能将容器从火场移至空旷处。然后根据着火原因选择适当灭火剂灭火。
/
溶解性
易溶于水、乙醇。
毒性及健康危害
侵入途径
吸入、食入、经皮吸收
毒性
LD50:940mg/kg(大鼠经口)。
健康危害
吸入对呼吸道有刺激性,出现咳嗽、气短等。对眼和皮肤有刺激性。长期接触引起皮炎、血液损害、肝损害、鼻粘膜溃疡,鼻中隔穿孔。
燃烧爆炸危险性
燃烧性
助燃
燃烧分解物
氮氧化物。
闪点(℃)
/
爆炸上限(g/m3):
硝酸铜
标识
中文名:硝酸铜
危险货物编号:51522
英文名:Cupric nitrate
UN编号:―――
分子式:Cu(NO3)2·3H2O
分子量:241.62
CAS号:10031-43-3
理化性质
外观与性状
深蓝色易吸潮的粒状结晶。
熔点(℃)
114.5
相对密度(水=1)
2.047
沸点(℃)
170(分解)
饱和蒸气压(kPa)
隔离泄漏污染区,限制出入。建议应急处理人员戴防尘口罩,穿防酸碱工作服。不要直接接触泄漏物。小量泄漏:用干燥的砂土、蛭石或其它惰性材料覆盖。用洁净的铲子收集于密闭容器中。大量泄漏:收集回收或运至废物处理场所处置。
碱式硫酸铜ppt课件

2019
-
10
2019
-
11
二、含硫杀菌剂
• 硫 磺(Sulphur) • 有效成分:元素硫—S • 生物活性:防白粉病(杀螨,杀虫)
单质硫主要有单斜 硫和斜方硫两种形 式.但斜方硫是室温
下唯一稳定的硫的 存在形式
2019
-
12
石硫合剂(Lime Sulphur)
CaS·Sx
2019
-
13
性质:褐色,臭蛋味,碱性,易被氧化。 使用:白粉病、锈病、炭疽病。 药害:幼嫩组织 配制:石灰:硫磺:水=1:2:13 石灰乳液 煮沸 加硫磺粉 继续煮45分钟
多与选择性杀菌剂混合使用.
2019
-
26
三氯甲硫基(Cl3CS--)
Captan N-三氯甲硫基-4-环己烯-1,2-二甲酰亚胺
2019
-
27
理化性质:工业品为黄棕色,略带臭味。在中性或酸 性条件下稳定,在高温和磁性条件下易水解 50%克菌丹可湿性粉剂。 广谱性杀菌剂,兼有保护和治疗作用。 防治多种蔬菜的霜霉病、白粉病、炭疽病,西红柿 和马铃薯早疫病、晚疫病,500-800倍液喷 雾 ;0.75g/m2处理苗床 防治立枯病、猝倒病 .
2019
-
23
丙森锌(propineb)
2019
-
24
福美双 化学名称:四甲基秋兰姆二硫化物
2019
-
25
理化性质:难溶于水,遇酸分解。 LD50:865mg/kg 剂型:50% WP 作用特点:保护作用。500~800倍叶面喷雾防治葡萄 灰霉病,果实黑星病,油料作物菌核病等。
A.i0.25%种子处理或2.5g/m2防治腐霉菌引起的猝 倒病和镰刀菌引起的其他病害。
碱式硝酸铜标准

碱式硝酸铜标准
碱式硝酸铜的标准可能因具体的产品和应用场景而有所不同。
一般来说,碱式硝酸铜是一种分子量为480.22的化工产品,其分子式有多种,取决于形成过程中碱性环境的强弱,即硝酸根与氢氧根的比例可以调整。
在工业应用中,碱式硝酸铜的CAS号为12158-75-7,天然合成来源为合成,提取来源为1-2μm级别。
其纯度规格为51.8%,保存条件为干燥通风,外观为浅蓝粉状,天然合成来源为合成,含量为51.8%。
在保存和运输时,需注意理化属性为40公斤/纸板桶,类别为医药原料,行业为化工,领域为强氧化剂。
此外,碱式硝酸铜的用途可能因具体的产品和标准而有所不同。
例如,它可以作为某些化学反应的催化剂、燃料电池的电极材料、颜料和涂料的添加剂等。
在使用碱式硝酸铜时,需严格遵守相应的安全规范和使用说明,以确保安全和有效性。
硝酸铜安全使用说明书

硝酸铜安全使用说明书
(一)理化性状和用途
蓝绿色,有潮解性的大型斜方晶系结晶。
密度:2.05,熔点114.5℃。
用于感光纸,纺织品染色的媒染剂,氧化剂,铝的光泽剂,促进有机反应用的催化剂、医药、杀虫剂等
(二)毒性
本品有毒,对皮肤、粘膜的刺激性强。
(三)短期过量暴露的影响
硝酸根在肠内被还原生成亚硝酸盐时,则成为血液毒,引起贫血及肾脏障碍。
大量经口摄入。
可引起眩晕、腹部痉挛、呕吐、便血、全身衰弱、全身痉挛、昏迷等症状,有时可致死。
高温时,会分释出毒的氮氢化合物。
(四)长期暴露的影响
产生与上相同的症状。
火场中能助任何燃烧物火势。
着火时,可用水扑救。
(六)化学反应性
能与易氧化物强烈反应,引起燃烧或爆炸。
与有机物、硫、磷等混合,有引起燃烧或爆炸的危险。
(七)人身防护
吸入:着火时,消防人员须穿供氧气放毒面具。
以防中毒。
皮肤:使用手套、工作服和工作鞋,工作场所应备有可用的安全沐浴和眼睛冲洗器具。
(八)急救
吸入:使吸入毒气的患者脱离污染区,安置休息并保暖。
眼睛皮肤接触:用大量水冲洗。
口服:误服立即漱口,急送医院医治。
(九)储藏和运输
储存于阴暗、干燥处,防止受潮。
与可燃物、有机物、还原剂、易氧化物隔离储运。
储装方法:(I )类。
(十)安全和处理
对泄漏物须立即清除。
用沙土混合,倒至空旷地方掩埋,被污染地面用肥皂或洗涤剂刷洗,经稀释的污水排入废水系统。
载铜氮化碳纳米片对单质汞的吸附脱除特性

载铜氮化碳纳米片对单质汞的吸附脱除特性刘东京;张禛;吴江【摘要】用简易热剥离法合成了氮化碳纳米片(CNNS),再通过等体积浸渍法将铜负载于CNNS表面合成了载铜CNNS吸附剂,用于低温下吸附脱除气态单质汞(Hg0).利用氮气吸附-脱附、X射线衍射(XRD)、扫描电子显微镜(SEM)、透射电子显微镜(TEM)、X射线光电子能谱(XPS)等手段对吸附剂进行表征.结果表明:CNNS 对Hg0具有良好的吸附性能,吸附温度为120℃时,脱汞效率约为54.2%;载铜修饰可极大提高CNNS的脱汞活性,脱汞效率在40~240℃温度范围内均大于82.3%,这归因于铜与氮化碳间的紧密接触.煅烧温度对载铜CNNS的脱汞活性影响较大,最佳煅烧温度为200℃.通过载铜修饰可有效活化CNNS,提高其对Hg0的氧化能力,这可能归因于铜离子与氮化碳之间的莫特-肖特基电子转移效应.SO2和水蒸气对载铜CNNS的脱汞性能有抑制作用.【期刊名称】《中国环境科学》【年(卷),期】2019(039)005【总页数】7页(P1862-1868)【关键词】单质汞;氮化碳;铜修饰;莫特-肖特基效应【作者】刘东京;张禛;吴江【作者单位】江苏大学能源与动力工程学院,江苏镇江 212013;上海电力大学能源与机械工程学院,上海 200090;上海电力大学能源与机械工程学院,上海 200090【正文语种】中文【中图分类】X701汞是一种可以在生物体内和食物链中永久积累的有毒物质,如果排放到大气中,对环境与人类会造成很大危害,近年来逐渐引起人们的广泛关注[1].在汞排放的所有来源中,燃煤汞排放已经成为最主要的人为汞污染源[2].煤在燃烧过程中,通常会产生3种形态的汞,即氧化态汞(Hg2+或Hg+)、易于吸附于飞灰上的颗粒态汞(Hgp)和气态单质汞(Hg0)[3].其中,氧化态汞易溶于水,可较容易地被湿法脱硫装置吸收脱除,颗粒态汞也可以被除尘装置脱除.而气态单质汞(占比为20%~50%),由于其高挥发性和难溶于水的特性,很难被现有的污染物控制装置有效脱除 [4].因此,燃煤烟气中气态单质汞的有效脱除是脱汞领域的一大难题.固体吸附剂法是一种可行的燃煤烟气汞脱除方法,研究发现多种碳基(活性炭[5]、焦炭[6]等)及非碳基吸附剂(飞灰[7]、凹凸棒[8]等)均可用于气态单质汞的吸附脱除,但这些吸附剂普遍存在脱汞效率低与吸附容量小的缺点[9].因此,开发具有高脱汞效率与大吸附容量特性的汞吸附剂日益成为国内外研究的重点.石墨相氮化碳(g-C3N4)是氮化碳同素异形体中最稳定的一种晶相,具有像石墨一样的二维层状结构,非常利于电子的传输[10].同时,g-C3N4具有稳定性高、耐酸碱、孔隙结构丰富且易于制备等优点[11].近年来,g-C3N4被广泛应用于多相催化[12]、气体吸附[13]、光催化[14]等领域,将g-C3N4用作燃煤烟气单质汞吸附剂的研究还鲜见报道.本文以热氧化刻蚀剥离法合成了g-C3N4纳米片(CNNS),通过等体积浸渍法对其进行载铜修饰改性,然后,在固定床反应器中测试了其在低温条件下对单质汞的吸附脱除性能.同时,研究了煅烧温度、反应温度、SO2和水蒸气对载铜CNNS脱汞性能的影响,为g-C3N4在燃煤烟气脱汞领域的应用提供必要的理论基础.称取10g三聚氰胺于加盖氧化铝坩埚中,放入马弗炉中,在静止空气中以5℃/min 升温速率升至550℃并保持2h,然后冷却至室温.将得到的黄色块状固体研磨成粉末,即为g-C3N4.称取5g上述制得的g-C3N4于敞口坩埚中,并再次放入马弗炉中以5℃/ min升温速率升至550℃并保持3h,然后冷却至室温,即得淡黄色CNNS粉末[15].称取0.1g Cu(NO3)2×3H2O粉末溶解于0.5g去离子水中,然后加入0.3g CNNS,搅拌混合均匀后放入70℃烘箱中干燥12h.将获得的干燥混合物置于敞口坩埚中,然后放入马弗炉中,在静止空气中以5℃/min升温速率分别升至160,200,240℃并保持2h,然后冷却至室温,即得载铜CNNS(Cu原子的质量分数为8%).所合成的载铜CNNS命名为Cux/CNNS,其中x表示煅烧温度.采用X射线衍射仪(XRD,Bruker D8Advance)测试样品的物相结构,入射线源为铜靶Kα(Ni滤波),管电压40kV,管电流50mA,λ=0.15406nm.晶粒大小由谢乐公式(Scherrer equation)计算获得:式中:D为晶粒尺寸,nm;λ为X射线波长,nm;β为特征峰半峰宽,无因次;θ为X射线半衍射角度,rad.通过扫描电子显微镜(SEM,Phillips FEI XL30FEG)和透射电镜(TEM,Phillips Model CM200)测定样品表面微观形貌与结构特征.通过贝士德(Beishide)3H- 2000PS4型比表面及孔径检测仪测定样品的氮气吸附-脱附等温线,根据Brunauer-Emmett-Teller(BET)方程计算样品的比表面积,根据Barrett-Joyner- Halenda(BJH)模型分析样品的孔体积和孔径分布情况.X射线光电子能谱(XPS)在PHI-5000C ESCA 系统上测定完成,测试条件为铝/镁靶,高压14.0kV,功率250W.单质汞吸附实验装置主要由气路系统、汞蒸气发生器、固定床反应器、气态汞在线监测仪及尾气处理装置组成[16].实验中的汞发生器(PS Analytical)在50℃持续加热下产生一定浓度的汞蒸气,以氮气为载气将汞蒸气携带出来与另一管路的气体混合后进入固定床反应器进行吸附脱汞实验.利用Lumex(RA-915-M)在线汞蒸气分析仪测试管路系统中的汞蒸气浓度.利用质量流量计设置管路气体总流量为1.2L/min(载气路流量为0.2L/min),吸附剂用量为50mg(商用竹炭基活性炭用量为0.4g),反应器为石英玻璃管(内径为8mm,长度为700mm),采用管式电阻炉加热.单质汞脱除效率计算方法如式(2)所示,式中:η为脱汞效率,%;Cin、Cout分别表示反应器进口和出口单质汞的浓度,μg/m3.单质汞吸附量计算方法如式(3)所示,式中:qt为t时刻吸附剂的汞吸附量,μg/g;V为气体流速,m3/h;m为吸附剂质量,g;t 为反应时间,h;Dt为数据记录间隔时间,h.从图1可以看出,CNNS为片状多孔形貌,其厚度和长度分别约为30nm和1.5μm.此外,在CNNS片状结构表面能很清晰地看到大量的孔隙结构.载铜修饰后,CNNS 表面变得较为光滑和致密,导致其比表面积和孔体积显著降低.从图2可以看出, CNNS呈现出大尺度透明特征,表明CNNS为超薄纳米片形貌,其厚度和横向尺寸分别约为几十纳米和几个微米.对于Cu200/CNNS,晶面间距为0.232,0.250,0.270nm的晶格条纹分别对应于CuO的(111), (-111)和(-110)晶面[17].从图2b可以看出,g-C3N4和CuO晶粒相互间紧密结合形成了稳定的p-n型异质结构.图3为CNNS和载铜CNNS的XRD图谱. CNNS有2个特征峰,分别位于2θ为27.5°和12.7°处.其中,27.5°附近的强衍射峰为芳香物层间堆积的特征峰,对应于(002)晶面.而12.7°附近的弱衍射峰为平面层内重复单元3-s-三嗪结构的特征峰,对应于(001)晶面[18].载铜修饰后,在27.5°处的衍射峰强度增强,且位置向右移动,原因可能是Cu的引入改变了g-C3N4层状结构的层间距[19]. Cu200/CNNS和Cu240/CNNS在35.4,38.7,48.8°处的特征峰是CuO [PDF#65-2309]的衍射信号,分别对应于(-111), (111),(-202)晶面. Cu160/CNNS在12.8,25.7,33.5, 36.3°处的特征峰为碱式硝酸铜(Cu2(OH)3NO3) [PDF#15-0014]的特征信号,分别对应于(001), (002),(120),(121)晶面,在Cu160/CNNS的XRD图谱中,没有检测到CuO 的特征信号,说明只有当煅烧温度大于或等于200℃时,在CNNS表面可以生成CuO颗粒.根据谢乐公式,基于CuO(111)晶面和Cu2(OH)3NO3(001)晶面分别计算的CuO和Cu2(OH)3NO3的晶粒尺寸如表1所示. Cu240/CNNS的晶粒尺寸(26.20nm)明显大于Cu200/CNNS的晶粒尺寸(13.90nm),原因可能是CuO晶粒会随着温度的升高逐渐长大.而Cu160/CNNS中Cu2(OH)3NO3的晶粒大小为28.45nm,明显大于Cu200/CNNS和Cu240/CNNS的晶粒尺寸.CNNS和载铜CNNS的氮气吸附-脱附等温线和孔径分布分别如图4和图5所示.从图4可以看出,CNNS在较高相对压力处出现明显的滞后回环,表明CNNS表面存在较多介孔结构[20],从图5也可以确认CNNS表面具有孔径为4,20,35nm的介孔结构.CNNS比表面积和孔体积分别为109m2/g和0.456cm3/g(表1).载铜修饰后,吸附剂氮气吸附量明显降低,比表面积和孔体积也显著减小,但其平均孔径变化不大依然保持在20nm左右.为探究载铜CNNS对单质汞的吸附机理,以XPS表征手段分析了单质汞吸附前后Cu200/ CNNS表面化学组分的变化情况(图6). C 1s有2个特征吸收峰,位于结合能287.6~288.2eV处的吸收峰对应于N—C=N中C的衍射信号,而位于结合能284.8~ 285.2eV处的吸收峰对应于石墨相C—C键中C的衍射信号[21]. N 1s可拟合成3个特征吸收峰,位于结合能399.6~400.2eV处的吸收峰对应于氨基(-NH2)中N的特征信号,结合能位于398.4~ 399.1eV处的吸收峰属于石墨相氮(C—(N)3)的特征信号,结合能位于397.4~398.1eV处的吸收峰属于吡啶氮(C—N=C)的特征信号[22].吸附单质汞后,C 1s和N 1s的结合能向低数值方向移动,原因可能是g-C3N4从Hg0接收了2个电子导致C、N原子电子云密度增大、结合能降低[23]. O 1s可以拟合成2个特征吸收峰,结合能位于约531.9eV处的吸收峰为化学吸附氧(Oα)的特征信号,而结合能位于533.2~534.6eV处的吸收峰为吸附剂表面吸附的H2O或CO2分子中的氧(Oβ)[24].脱汞反应后,吸附剂表面化学吸附氧含量从46.5%增加至65.9%,原因可能是CuO中部分晶格氧在单质汞吸附反应过程中转变成了化学吸附氧. Cu 2p也可以拟合为2个特征峰,结合能位于932.6~933.4eV和952.6~ 953.6eV处的2个吸收峰分别属于CuO中Cu2+离子的特征信号[25].脱汞反应后,Cu 2p的结合能向低数值方向移动,表明CuO可能部分被还原成了低价态的铜氧化物. Hg 4f在104.4, 101.6eV结合能处的吸收峰分别对应于氧化态汞(HgO)Hg 4f 5/2和Hg 4f 7/2电子轨道的特征信号[26],说明单质汞被氧化成了二价汞形态而被吸附脱除.不同反应温度下CNNS和Cu200/CNNS的单质汞吸附特性曲线如图7所示. CNNS的脱汞效率随着温度的升高,基本上呈先增大后减小的趋势,最佳反应温度为120℃,脱汞效率为54.2%,说明CNNS对单质汞的吸附主要以物理吸附为主.载铜修饰可以显著提升CNNS的脱汞性能,脱汞效率在40~200℃范围内均增加了40%以上,脱汞效率均高于82.3%,原因主要有以下2个:(1)载铜修饰给CNNS引入了新的汞吸附活性位(CuO);(2)由于CuO与g-C3N4紧密结合形成了p-n型异质结,在CuO与g-C3N4的接触界面存在良好的莫特-肖特基电子转移效应[27], 载铜CNNS可以被肖特基能垒活化而具有更高的电子接收能力,从而促进单质汞的吸附脱除[28].但当反应温度升高至240℃时,Cu200/CNNS的脱汞效率下降至82.3%,原因是在较高反应温度下,吸附剂表面发生的氧化反应会发生可逆转变,部分氧化反应产物(HgO)可能会被CuO催化分解成单质汞(2HgO→ 2Hg+O2),导致脱汞效率下降[29].Cux/CNNS在120℃时的单质汞吸附特性曲线如图8所示.汞吸附速率随着煅烧温度的上升,先增大后减小,煅烧温度为200℃时,Cu200/CNNS的汞吸附速率最大,脱汞效率也高达98.6%,原因是200℃煅烧时生成了晶粒最小的CuO组分,有利于g-C3N4与CuO间的紧密接触.当煅烧温度为160,240℃时,脱汞效率分别降低至97.1%和91.5%.原因可能是分别生成了晶粒较大的氧化铜和碱式硝酸铜.图9为商用活性碳(AC)和Cu200/CNNS在120℃时连续12h内的单质汞吸附特性曲线.Cu200/CNNS具有十分稳定的单质汞吸附活性,在吸附反应2h后即可达到100%的脱汞效率,而且反应12h后依然能够保持在这一水平,汞吸附量为1051μg/g.AC在吸附反应5min后脱汞效率为76.5%,然后逐渐下降最后稳定在约68%左右,汞吸附量为103μg/g. Cu200/CNNS的脱汞活性和汞吸附量均显著高于AC.从图10中可以看出,SO2和水蒸气对Cu200/ CNNS的脱汞性能均有明显的抑制作用,脱汞效率分别由97.2%下降至80.5%和73.2%,这是因为SO2、水蒸气与Hg0的竞争吸附使单质汞吸附活性位减少,导致Cu200/CNNS脱汞性能下降[30].3.1 CNNS对单质汞具有很好的低温吸附脱除能力.载铜修饰后,CuO与g-C3N4形成了p-n型异质结构,可显著提高CNNS的脱汞活性,脱汞效率在40~240℃范围内均大于82.3%.3.2 煅烧温度对载铜CNNS的脱汞活性影响较大,Cux/CNNS的最佳煅烧温度为200℃.3.3 载铜CNNS表现出优异的脱汞性能,主要归因于铜离子与g-C3N4间的莫特-肖特基电子转移效应.3.4 在脱汞反应过程中,单质汞(Hg0)向CuO和g-C3N4给出两个电子被氧化成HgO而吸附脱除.3.5 SO2和水蒸气对Cu200/CNNS的脱汞性能均有抑制作用,脱汞效率分别下降了16.7%和24.3%,水蒸气与Hg0的竞争吸附抑制作用更为显著.[1] Liu D J, Lu C, Wu J. Gaseous mercury capture by copper-activated nanoporous carbon nitride [J]. Energy & Fuels, 2018, 32(8):8287– 8295. [2] Xie J, Qu Z, Yan N, et al. Novel regenerable sorbent based on Zr–Mn binary metal oxides for flue gas mercury retention and recovery [J]. Journal of Hazardous Materials, 2013,261:206–213.[3] Yao H, Luo G, Xu M, et al. Mercury emission and species duringcombustion of coal and waste [J]. Energy & Fuels, 2006,20(5):1946– 1950.[4] Li H, Wu C, Li Y, et al. Superior activity of MnOx-CeO2/TiO2 catalyst for catalytic oxidation of elemental mercury at low flue gas temperatures [J]. Applied Catalysis B Environmental, 2012,111:381– 388.[5] Liu Z, Adewuyi Y G, Shi S, et al. Removal of gaseous Hg0 using novel seaweed biomass-based activated carbon [J]. Chemical Engineering Journal, 2019, 366:41–49.[6] Xu W, Adewuyi Y, Liu Y, et al. Removal of elemental mercury from flue gas using CuOx and CeO2 modified rice straw chars enhanced by ultrasound [J]. Fuel Processing Technology, 2018,170:21–31.[7] Wang S, Zhang Y, Gu Y, et al. Using modified fly ash for mercury emission control for coal-fired power plant applications in China [J]. Fuel, 2016,181:1230–1237.[8] 左海清,徐东耀,但海均,等.凹凸棒石烟气脱汞吸附剂的研究进展 [J]. 化工进展, 2017,36(10):3533–3539. Zuo H Q, Xu D Y, Dan H J, et al.Research progress in attapulgite absorbents for mercury removal from flue gases.Chemical Industry and Engineering Progress (in Chinese), 2017,36(10):3533–3539. [9] Jampaiah D, Ippolito S J, Sabri Y M, et al. Ceria-zirconia modified mnox catalysts for gaseous elemental mercury oxidation and adsorption [J]. Catalysis Science & Technology, 2016,6(6):1792- 1803.[10] 王悦,蒋权,尚介坤,等.介孔氮化碳材料合成的研究进展 [J]. 物理化学学报, 2016,32(8):1913–1928. Wang Y, Jiang Q, Shang J K, et al.Advances in the Synthesis of Mesoporous Carbon Nitride Materials.Acta Physico–Chimica Sinica (in Chinese), 2016,32(8):1913–1928.[11] Wang X, Blechert S, Antonietti M. Polymeric graphitic carbon nitride for heterogeneous photocatalysis [J]. ACS Catalysis, 2012,2:1596– 1606. [12] Zhu J, Wei Y, Chen W, et al. Graphitic carbon nitride as a metal-free catalyst for NO decomposition [J]. Chemical Communications, 2010,46:6965–6967.[13] Koh G, Zhang Y W, Pan H. First-principles study on hydrogen storage by graphitic carbon nitride nanotubes [J]. International Journal of Hydrogen Energy, 2012,37(5):4170–4178.[14] Xiao J, Xie Y, Nawaz F, et al. Dramatic coupling of visible light with ozone on honeycomb–like porous g–C3N4 towards superior oxidation of water pollutants [J]. Applied Catalysis B Environmental, 2016,183: 417–425.[15] Xiao J, Han Q, Xie Y, et al. Is C3N4 chemically stable toward reactive oxygen species in sunlight–driven water treatment [J]. Environmental Science & Technology, 2017,51:13380–13387.[16] Liu D, Zhou W, Wu J. Effect of Ce and La on the activity of CuO/ ZSM-5and MnOx/ZSM-5composites for elemental mercury removal at low temperature [J]. Fuel, 2017,194(4):115-122.[17] Svintsitskiy D A, Kardash T Y, Stonkus O A, et al. In situ XRD, XPS, TEM, and TPR study of highly active in CO oxidation CuO nanopowders [J]. Journal of Physical Chemistry C, 2013,117(117): 14588–14599.[18] Ren H T, Jia S Y, Wu Y, et al. Improved photochemical reactivities of Ag2O/g–C3N4 in phenol degradation under UV and visible light [J]. Industrial & Engineering Chemistry Research, 2014,53:17645–17653. [19] Liu D J, Zhang Z, Wu J. Elemental mercury removal by MnO2nanoparticle decorated carbon nitride nanosheet [J]. Energy & Fuels, 2019, 33(4):3089–3097.[20] Dong F, Sun Y, Wu L, et al. Facile transformation of low cost thiourea into nitrogen–rich graphitic carbon nitride nanocatalyst with high visible light photocatalytic performance [J]. Catalysis Science & Technology, 2012,2:332–1335.[21] Bian J, Li Q, Huang C, et al. Thermal vapor condensation of uniform graphitic carbon nitride films with remarkable photocurrent density for photoelectrochemical applications [J]. Nano Energy, 2015,15:353– 361. [22] Yan S, Li Z, Zou Z. Photodegradation of rhodamine B and methyl orange over boron-doped g-C3N4under visible light irradiation [J]. Langmuir, 2010,26:3894–390.[23] Wang X, Blechert S, Antonietti M. Polymeric graphitic carbon nitride for heterogeneous photocatalysis [J]. ACS Catalysis, 2012,2:1596– 1606. [24] Li H, Wu S, Li L, et al. CuO–CeO2/TiO2 catalyst for simultaneous NO and Hg0 oxidation at low temperatures [J]. Catalysis Science & Technology, 2015,5:5129–5138.[25] Zhang Q, Xu L, Ning P, et al. Surface characterization studies of CuO–CeO2–ZrO2 catalysts for selective catalytic reduction of NO with NH3 [J]. Applied Surface Science, 2014,317:955–961.[26] Sasmaz E, Kirchofer A, Jew A D, et al. Mercury chemistry on brominated activated carbon [J]. Fuel, 2012,99:188–196.[27] Chen T, Guo S, Yang J, et al. In situ activated nitrogen-doped carbon by embeded nickel via Mott-Schottky effect for oxygen reduction reaction[J]. ChemPhysChem, 2017,18:3454–3461.[28] Fu T, Wang M, Cai W, et al. Acid-resistant catalysis without use of noble metals: carbon nitride with underlying nickel [J]. ACS Catalysis, 2014,4:2536–2543.[29] Khedr M H, Abdel Halim K S, Nasr M I, et al. Effect of temperature on the catalytic oxidation of CO over nano-sized iron oxide [J]. Materials Science and Engineering A, 2006,430(1/2):40-45.[30] Liu H, Zhang H, Yang H. Photocatalytic removal of nitric oxide by multi-walled carbon nanotubes-supported TiO2 [J]. Chinese Journal of Catalysis, 2014,35:66-77.【相关文献】[1] Liu D J, Lu C, Wu J. Gaseous mercury capture by copper-activated nanoporous carbon nitride [J]. Energy & Fuels, 2018, 32(8):8287– 8295.[2] Xie J, Qu Z, Yan N, et al. Novel regenerable sorbent based on Zr–Mn binary metal oxides for flue gas mercury retention and recovery [J]. Journal of Hazardous Materials, 2013,261:206–213.[3] Yao H, Luo G, Xu M, et al. Mercury emission and species during combustion of coal and waste [J]. Energy & Fuels, 2006,20(5):1946– 1950.[4] Li H, Wu C, Li Y, et al. Superior activity of MnOx-CeO2/TiO2 catalyst for catalytic oxidation of elemental mercury at low flue gas temperatures [J]. Applied Catalysis B Environmental, 2012,111:381– 388.[5] Liu Z, Adewuyi Y G, Shi S, et al. Removal of gaseous Hg0 using novel seaweed biomass-based activated carbon [J]. Chemical Engineering Journal, 2019, 366:41–49. [6] Xu W, Adewuyi Y, Liu Y, et al. Removal of elemental mercury from flue gas using CuOx and CeO2 modified rice straw chars enhanced by ultrasound [J]. Fuel Processing Technology, 2018,170:21–31.[7] Wang S, Zhang Y, Gu Y, et al. Using modified fly ash for mercury emission control for coal-fired power plant applications in China [J]. Fuel, 2016,181:1230–1237.[8] 左海清,徐东耀,但海均,等.凹凸棒石烟气脱汞吸附剂的研究进展 [J]. 化工进展,2017,36(10):3533–3539. Zuo H Q, Xu D Y, Dan H J, et al.Research progress in attapulgiteabsorbents for mercury removal from flue gases.Chemical Industry and Engineering Progress (in Chinese), 2017,36(10):3533–3539.[9] Jampaiah D, Ippolito S J, Sabri Y M, et al. Ceria-zirconia modified mnox catalysts for gaseous elemental mercury oxidation and adsorption [J]. Catalysis Science & Technology, 2016,6(6):1792- 1803.[10] 王悦,蒋权,尚介坤,等.介孔氮化碳材料合成的研究进展 [J]. 物理化学学报,2016,32(8):1913–1928. Wang Y, Jiang Q, Shang J K, et al.Advances in the Synthesis of Mesoporous Carbon Nitride Materials.Acta Physico–Chimica Sinica (in Chinese),2016,32(8):1913–1928.[11] Wang X, Blechert S, Antonietti M. Polymeric graphitic carbon nitride for heterogeneous photocatalysis [J]. ACS Catalysis, 2012,2:1596– 1606.[12] Zhu J, Wei Y, Chen W, et al. Graphitic carbon nitride as a metal-free catalyst for NO decomposition [J]. Chemical Communications, 2010, 46:6965–6967.[13] Koh G, Zhang Y W, Pan H. First-principles study on hydrogen storage by graphitic carbon nitride nanotubes [J]. International Journal of Hydrogen Energy, 2012,37(5):4170–4178.[14] Xiao J, Xie Y, Nawaz F, et al. Dramatic coupling of visible light with ozone on honeycomb–like porous g–C3N4 towards superior oxidation of water pollutants [J]. Applied Catalysis B Environmental, 2016,183: 417–425.[15] Xiao J, Han Q, Xie Y, et al. Is C3N4 chemically stable toward reactive oxygen species in sunlight–driven water treatment [J]. Environmental Science & Technology,2017,51:13380–13387.[16] Liu D, Zhou W, Wu J. Effect of Ce and La on the activity of CuO/ ZSM-5andMnOx/ZSM-5composites for elemental mercury removal at low temperature [J]. Fuel, 2017,194(4):115-122.[17] Svintsitskiy D A, Kardash T Y, Stonkus O A, et al. In situ XRD, XPS, TEM, and TPR study of highly active in CO oxidation CuO nanopowders [J]. Journal of Physical Chemistry C, 2013,117(117): 14588–14599.[18] Ren H T, Jia S Y, Wu Y, et al. Improved photochemical reactivities of Ag2O/g–C3N4 in phenol degradation under UV and visible light [J]. Industrial & Engineering Chemistry Research, 2014,53:17645–17653.[19] Liu D J, Zhang Z, Wu J. Elemental mercury removal by MnO2 nanoparticle decorated carbon nitride nanosheet [J]. Energy & Fuels, 2019, 33(4):3089–3097.[20] Dong F, Sun Y, Wu L, et al. Facile transformation of low cost thiourea into nitrogen–rich graphitic carbon nitride nanocatalyst with high visible light photocatalytic performance [J]. Catalysis Science & Technology, 2012,2:332–1335.[21] Bian J, Li Q, Huang C, et al. Thermal vapor condensation of uniform graphitic carbonnitride films with remarkable photocurrent density for photoelectrochemical applications [J]. Nano Energy, 2015,15:353– 361.[22] Yan S, Li Z, Zou Z. Photodegradation of rhodamine B and methyl orange over boron-doped g-C3N4under visible light irradiation [J]. Langmuir, 2010,26:3894–390. [23] Wang X, Blechert S, Antonietti M. Polymeric graphitic carbon nitride for heterogeneous photocatalysis [J]. ACS Catalysis, 2012,2:1596– 1606.[24] Li H, Wu S, Li L, et al. CuO–CeO2/TiO2 catalyst for simultaneous NO and Hg0 oxidation at low temperatures [J]. Catalysis Science & Technology, 2015,5:5129–5138. [25] Zhang Q, Xu L, Ning P, et al. Surface characterization studies of CuO–CeO2–ZrO2 catalysts for selective catalytic reduction of NO with NH3 [J]. Applied Surface Science, 2014,317:955–961.[26] Sasmaz E, Kirchofer A, Jew A D, et al. Mercury chemistry on brominated activated carbon [J]. Fuel, 2012,99:188–196.[27] Chen T, Guo S, Yang J, et al. In situ activated nitrogen-doped carbon by embeded nickel via Mott-Schottky effect for oxygen reduction reaction [J]. ChemPhysChem, 2017,18:3454–3461.[28] Fu T, Wang M, Cai W, et al. Acid-resistant catalysis without use of noble metals: carbon nitride with underlying nickel [J]. ACS Catalysis, 2014,4:2536–2543.[29] Khedr M H, Abdel Halim K S, Nasr M I, et al. Effect of temperature on the catalytic oxidation of CO over nano-sized iron oxide [J]. Materials Science and Engineering A, 2006,430(1/2):40-45.[30] Liu H, Zhang H, Yang H. Photocatalytic removal of nitric oxide by multi-walled carbon nanotubes-supported TiO2 [J]. Chinese Journal of Catalysis, 2014,35:66-77. Adsorption removal of elemental mercury on Cu-loaded carbon nitride nanosheet.。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
碱式硝酸铜的pdf卡片理论说明以及概述1. 引言1.1 概述本文将对碱式硝酸铜的pdf卡片进行理论说明和概述。
碱式硝酸铜作为一种重要的化学物质,在不同领域具有广泛的应用前景。
通过使用pdf卡片技术,我们可以更好地了解和研究碱式硝酸铜的性质、制备方法以及其在光催化、电化学储能和生物医学领域中的应用。
1.2 文章结构本文主要包括五个部分。
首先,在引言部分,我们将对文章的背景和目的进行简要介绍。
然后,在第二部分,我们将对碱式硝酸铜进行概述,并详细阐述其制备方法和基本性质。
接下来,第三部分将介绍碱式硝酸铜的pdf卡片实验步骤,包括实验器材和试剂准备、实验步骤详解以及实验结果与分析。
在第四部分中,我们将探讨碱式硝酸铜在光催化、电化学储能和生物医学领域中的应用潜力,并展望其未来发展前景。
最后,在第五部分中,我们将总结文章的主要内容并提出相应的结论。
1.3 目的本文的主要目的是通过对碱式硝酸铜的pdf卡片进行理论说明和概述,在读者中提高对该化学物质的认识和理解。
同时,本文还旨在探索碱式硝酸铜在光催化、电化学储能和生物医学领域等应用领域的发展前景,并为相关研究工作提供参考和启示。
通过深入了解碱式硝酸铜及其应用,我们可以为进一步推动科学研究和创新做出贡献。
2. 碱式硝酸铜的pdf卡片理论说明2.1 碱式硝酸铜概述碱式硝酸铜(Cu(OH)NO3)是一种重要的无机化合物。
它是由硝酸铜和氢氧化钠反应得到的沉淀物。
其化学式表达为Cu(OH)NO3,其分子量为141.57 g/mol。
2.2 硝酸铜的制备方法和性质硝酸铜(Cu(NO3)2)可以通过将铜粉溶于稀硝酸中得到。
其化学式表达为Cu(NO3)2,其分子量为187.55 g/mol。
硝酸铜呈现出蓝色晶体或结晶性粉末的形态。
它在常温下易溶于水,并能与氨水、乙二胺等配位体形成络合物。
2.3 pdf卡片的使用及特点PDF卡片是一种采用PDF格式制作的电子学习材料,以卡片为基本单元进行组织和展示。
在碱式硝酸铜方面,PDF卡片可以包括理论知识、实验步骤、应用领域等相关内容。
使用PDF卡片有以下特点:1. 高度可视化:PDF卡片可以通过插入图片、图表和动画等多媒体元素,直观地展示碱式硝酸铜的相关知识和实验过程。
2. 便携性强:PDF卡片可以在各种电子设备上进行阅读,如电脑、平板电脑和手机等,方便学习者进行随时随地的学习。
3. 整理性好:通过将相关内容整理成PDF卡片的形式,可以清晰地呈现出知识结构和逻辑关系,有助于学习者系统地学习碱式硝酸铜。
总结而言,采用PDF卡片作为学习工具能够提供高度可视化的展示效果,并具备便携性和整理性好的特点。
这种学习方式能够帮助读者更加深入地理解和掌握碱式硝酸铜相关的理论知识和实验操作。
3. 碱式硝酸铜的pdf卡片实验步骤:3.1 实验器材和试剂准备:在进行碱式硝酸铜的pdf卡片实验之前,需要准备以下实验器材和试剂:- 透明玻璃片:用于制作pdf卡片的基板。
- 对氨基苯甲酸:用作碱性沉淀剂。
- 硝酸铜:作为反应原料。
- 氨水:用于调节溶液中的pH值。
- 高锰酸钾:用于清洗实验器皿。
- 塑料滴管和玻璃搅拌棒:用于操作溶液。
另外,还需要准备一些常见的实验仪器,例如移液管、量筒和热板等。
确保所有的器材都是清洁且无任何污染物。
3.2 实验步骤详解:步骤1: 准备溶液先取一定比例的硝酸铜溶液放入一个容量瓶内,然后使用适量的氨水调节溶液pH值至约为8.5。
注意在调节过程中需要小心加入氨水,并进行充分搅拌以确保均匀混合。
步骤2: 沉淀反应将对氨基苯甲酸溶液加入到调节好pH值的硝酸铜溶液中,发生沉淀反应。
需要注意的是,加入沉淀剂时要缓慢滴加,并且边滴加边轻轻搅拌溶液,以避免沉淀堆积。
继续搅拌数分钟,让沉淀充分形成。
步骤3: 过滤和洗涤使用过滤纸或者玻璃纤维滤膜将溶液中的沉淀分离出来。
将过滤得到的固体用去离子水进行洗涤,重复此步骤几次以去除杂质和未反应的试剂。
步骤4: 干燥将洗净的沉淀放入干燥箱中进行干燥。
温度和时间可以根据具体情况进行调整,一般在80-100摄氏度下持续几个小时。
步骤5: 制作pdf卡片将得到的干燥产物粉末均匀撒在透明玻璃片上,并利用塑料滴管将少量去离子水滴在上面,使其湿润。
然后使用玻璃搅拌棒轻轻搅拌,使粉末均匀分布并形成薄膜。
等待薄膜干燥后,即可得到碱式硝酸铜的pdf卡片。
3.3 实验结果与分析:制备完成的碱式硝酸铜的pdf卡片可以在光照下观察到不同颜色的反射和吸收特性。
通过对卡片进行光谱分析,可以进一步研究其红外和可见光区域的吸收峰值和波长范围。
这些结果可以帮助了解碱式硝酸铜在光催化应用等领域中的潜在性能,并为其进一步应用提供参考。
在实验过程中应该注意控制实验条件,确保理想的沉淀反应和洗涤效果。
此外,在制备pdf卡片时,要仔细处理材料以避免任何污染或损坏。
实验后还需要对所得结果进行系统记录和数据分析,以便于后续的相关讨论与研究。
以上是关于"碱式硝酸铜的pdf卡片实验步骤"的详细内容。
通过此实验步骤的描述,读者可以更好地了解和掌握制备碱式硝酸铜pdf卡片的过程,并了解其在光学和化学领域中的应用前景。
4. 碱式硝酸铜应用领域探讨4.1 光催化应用研究进展碱式硝酸铜作为一种具有光催化活性的材料,在光催化应用方面显示出潜力。
近年来,许多研究人员对碱式硝酸铜进行了深入研究,并探索了其在环境净化、水分解、有机合成等领域的应用。
首先,在环境净化方面,碱式硝酸铜可以通过光催化降解有机污染物。
研究表明,碱式硝酸铜可以有效地吸收可见光,并产生活性氧物种(ROS),如羟基自由基和超氧阴离子自由基。
这些ROS能够高效地降解有害物质,如重金属离子和有机染料,因此被广泛研究和应用于实际的废水处理中。
其次,在水分解方面,碱式硝酸铜也被广泛研究并应用于光电转换器件中。
使用碱式硝酸铜作为光阳极材料,可以将太阳能转化为可用的电能。
光电转换器件通常采用水作为氢源,并通过碱式硝酸铜的光催化活性将水分解为氢和氧气,从而产生可再生的燃料。
此外,在有机合成领域,碱式硝酸铜也展示了其催化有机反应的能力。
例如,碱式硝酸铜可以用于有机合成中的偶联反应、C-H活化和环加成等反应。
由于其良好的催化活性和选择性,碱式硝酸铜在有机合成中具有广泛的应用前景,并受到了业界和学术界的关注。
4.2 电化学储能领域中的应用潜力分析在电化学储能领域,碱式硝酸铜被认为是一种潜在的正极材料候选者。
其原因在于,碱式硝酸铜具有良好的导电性和良好的离子传导性能。
实验结果显示,碱式硝酸铜具有较高的比容量和较长的循环寿命,这使得它成为一种理想的正极材料。
另外,由于其相对较低的成本和丰富的来源,碱式硝酸铜也具有一定的经济优势。
这使得它在商业应用中具有潜力,尤其是在大规模储能系统中。
然而,需要注意的是,碱式硝酸铜在电化学储能领域的应用还处于早期阶段,并面临着一些挑战和限制。
例如,碱式硝酸铜与电解质溶液之间的相互作用仍需进一步研究和改进,以提高其在电池中的性能。
4.3 生物医学领域中的应用前景展望最近的研究表明,碱式硝酸铜也显示出在生物医学领域中的应用潜力。
一方面,碱式硝酸铜可以作为抗菌剂使用,具有抗菌活性和对抗生物膜形成能力。
这使得碱式硝酸铜成为一种可替代传统抗菌药物且不易引起细菌耐药性问题的新型材料。
另一方面,在生物成像方面,由于其特殊光学性质和较好的生物相容性,碱式硝酸铜也被认为是潜在的生物标记物料。
碱式硝酸铜纳米颗粒可以通过特定的修饰和包覆方法,用于生物体内的成像技术,并有望在诊断和治疗方面发挥重要作用。
然而,目前关于碱式硝酸铜在生物医学领域中应用的研究仍处于初级阶段,还需要进一步的研究和验证其效果。
对于其毒性和长期使用中可能存在的潜在风险也需要进行更深入的评估。
综上所述,碱式硝酸铜作为一种具有广泛应用潜力的材料,在光催化、电化学储能以及生物医学领域均展现出了良好的前景。
随着科学技术的不断发展和深入研究对其特性和应用机制的理解加深,相信碱式硝酸铜将会进一步推动相关领域的发展并得到更广泛应用。
5 结论通过本文的研究和概述,可以得出以下几个结论:首先,碱式硝酸铜是一种具有广泛应用前景的重要化合物。
其在光催化领域、电化学储能领域和生物医学领域等多个方面都具有潜在的应用价值。
其次,硝酸铜作为碱式硝酸铜的前身,在制备方法和性质方面已有较为成熟的研究。
利用不同的制备方法可以得到不同性质的碱式硝酸铜,并应用于各种领域中。
再次,pdf卡片作为一种新型的材料形态,具有许多特点和优势。
它可以提供大量信息存储空间,并且易于保存、传输和随身携带。
在碱式硝酸铜方面,pdf卡片可应用于实验记录、数据分析等方面,并在科研教育中起到重要作用。
此外,在实验步骤部分详解了使用pdf卡片制备碱式硝酸铜的实验流程,并对实验结果进行了分析。
实验证明了该方法可行且效果良好。
最后,在探讨碱式硝酸铜的应用领域时,本文重点关注了光催化、电化学储能和生物医学三个方面。
目前在这些领域中已经取得了一些研究进展,并且展望了未来可能的应用前景。
综上所述,通过对碱式硝酸铜的pdf卡片理论说明和实验步骤的详细分析,可以看出该化合物具有潜在的广泛应用价值。
未来随着科学技术的不断发展,相信碱式硝酸铜将在更多领域中发挥其重要作用。
