药品养护汇总分析报表
药品养护管理制度_药品养护管理制度范本

药品养护管理制度_药品养护管理制度范本药品养护管理制度篇1一.本制度根据《药品管理法》、《药品经营质量管理规范》、《药品经营质量管理规范实施细则》等有关规定制定。
二.本医院设置兼职药品养护员,由具有药师职称的技术人员负责。
三.药品养护人员做到认真检查在库药品的储藏条件,配合保管人员进行库房温湿度的检测管理。
每日上午9~10时、下午2~3时各一次,定时对库房的温湿度进行记录。
温度:常温库(0~30℃)、阴凉库(20℃以下)、冷库(2~10℃),湿度在45%~75%之间,超出规定范围及时采取调控措施,并予以记录。
四、对陈列和储藏的药品根据流转情况定期进行养护和检查,并做好记录。
一般药品每季度检查一次,重点品种包括近效期在一年以内的药品,贵细药品、二类精神药品、易霉变、易潮解药品,已发现质量问题药品的相邻批号药品和储存时间较长的药品视情况缩短检查周期,每月或每周检查一次。
对质量有疑问及储存日久的药品及时抽样送检。
对近效期的药品,按月填报效期表。
五、中药材和中药饮片按其特征,采取干燥、降氧、熏蒸等方法养护,并做好记录。
六、药品养护人员定期汇总、分析和上报养护检查情况以及近效期或长时间储存的药品等质量信息。
七、药品养护人员具体负责养护仪器、设备(如除湿机、排风扇、空调)、冷藏设备、温湿度和监控仪器、仓库使用计量仪器及器具等管理工作,检查养护设备的运行情况。
八、养护中发现质量问题,应悬挂明显标志和暂停发货,并尽快通知质量管理负责人予以处理。
九、药品养护人员负责建立药品养护档案,定时记录温湿度,维修、保养仓储养护设施,按月填报效期报表。
十、本制度负责人为药品养护人员。
十一、本制度每季度考核一次。
药品养护管理制度篇2为确保所陈列和储存药品质量稳定,避免药品发生质量问题制定本制度。
1 药品养护工作的职责是:安全储存,降低损耗,保证质量,避免事故。
2 依据陈列和储存药品的流转情况,制定养护计划,进行循环的质量检查;对质量有疑问的或储存日久的品种,应有计划抽样送检。
药品储存保管与养护的基本工作职责是

. 药品储存保管与养护的基本工作职责是:安全储存、降低损耗、科学养护、保证质量、收发迅速、避免事故。
2. 仓库保管人员的基本职责:2.1 按照药品不同自然属性分类进行科学储存,防止差错、混淆、变质;2.2 做到数量准确,帐目清楚,帐、货、卡相符。
3. 药品仓储保管应执行《药品储存控制程序》,并按《主要剂型的储存保管与养护要点》做好在库药品的储存保管。
3.1 药品应按储藏温、湿度要求,分别储存于阴凉库或常温库、冷藏库内。
3.1.1阴凉库:温度不高于20℃;3.1.2常温库:温度保持在0℃~30℃;3.1.3 冷库:温度保持在2℃~10℃3.1.4相对湿度:各库房相对湿度保持在45%~75%之间。
3.2 药品应依据药品性质,按分库、分类存放的原则进行储存保管,其中:3.2.1药品与非药品(指不具备药品生产批准文号的物品)应分库存放;3.2.2内服药与外用药应分库或分区存放;3.2.3品种与外包装容易混淆的品种应分区或隔垛存放;3.2.4易串味的药品、中药材、中药饮片、化学原料药以及性质相互影响的药品应分库存放;危险品应与其他药品分库存放;3.2.5药品中的危险品应存放于危险品专库;3.2.6 处方药与非处方药分开存放;3.2.7不合格品应存放在不合格品区内,按《不合格药品管理规定》进行管理;3.2.8退货药品应存放在退货区在,经质量验收并确认为合格品后再移入合格品区;经质量验收为不合格的入不合格品区;3.2.9药品按品种、规格、批号、生产日期及效期远近依次或分开堆垛,如混批堆码,每一垛的混批时限为:药品的产品批号或生产日期间隔应不超过一个月;3.2.10近效期药品即有效期不足一年时,应按月填报近效期药品催销月报表;3.2.11近效期药品应挂近效期标志;3.2.12经营特殊管理药品(即麻、精、毒、放类药品),按其相应的管理制度执行。
3.3 在搬运和堆垛等作业中均应严格按药品外包装图示标志的要求搬运存放,规范操作。
gsp需要的表格-Microsoft-Word-文档-(9)

新版GSP认证零售药店需要哪些记录表格?一、质量管理体系文件1 文件发放回收记录……………………………… ZD—WJ—01—012 文件变更履历表………………………………… ZD—WJ—01—023 文件销毁申请单………………………………… ZD—WJ—01—034 文件销毁记录…………………………………… ZD—WJ—01—045 文件制作申请单………………………………… GC—WJ—02—016 文件会审单……………………………………… GC—WJ—02—02二、质量管理7 质量信息处理审批单…………………………… ZD—ZG—03—018 质量信息汇总表………………………………… ZD—ZG—03—029 现场调查记录…………………………………… ZD—ZG—04—0110 质量事故报告…………………………………… ZD—ZG—04—0211 质量查询函……………………………………… ZD—ZG—05—0112 质量查询及处理记录…………………………… ZD—ZG—05—0213 药品不良反应报告表…………………………… ZD—ZG—06—0114 归档资料凭单…………………………………… ZD—ZG—08—0115 档案资料借阅登记簿…………………………… ZD—ZG—08—0216 档案资料销毁审批表…………………………… ZD—ZG—08—0317 档案资料销毁记录……………………………… ZD—ZG—08—0418 质量制度检查考核记录………………………… ZD—ZG—09—0119 供货单位质量管理体系评价表………………… ZD—ZG—10—0120 供货单位质量管理体系评价报告表…………… ZD—ZG—10—0221 购货单位质量管理体系评价表(生产、经营) ZD—ZG—11—0122 购货单位质量管理体系评价表(医疗机构)… ZD—ZG—11—0223 药品质量评审计划…………………………… ZD—ZG—12—01 序号记录名称记录编号24 药品购进情况质量评审表……………………… ZD—ZG—12—0225 药品质量评审报告……………………………… ZD—ZG—12—0326 质量管理体系内部审核计划………………………GC—ZG—01—0127 质量管理体系内部审核实施方案……………… GC—ZG—01—0228 质量管理体系内部审核检查表……………………GC—ZG—01—0329 纠正/预防措施跟踪记录表………………………GC—ZG—01—0430 质量管理体系内部审核会议记录…………………GC—ZG—01—0531 质量管理体系内部审核报告………………………GC—ZG—01—0632 参加会议人员签到表………………………………GC—ZG—01—0733 公司质量方针、目标实施情况检查表……………GC—ZG—02—0134 部门质量方针、目标实施情况自查表……………GC—ZG—02—0235 质量方针、目标实施情况评价汇总表……………GC—ZG—02—0336 质量投诉调查处理记录……………………………GC—ZG—03—0137 质量投诉处理结果反馈与跟踪记录………………GC—ZG—03—0238 药品经营各环节质量风险管理评价与控制表……GC—ZG—04—0139 质量风险评估表……………………………………GC—ZG—04—0240 质量风险控制表……………………………………GC—ZG—04—0341 质量风险审核表……………………………………GC—ZG—04—0442 管理评审计划………………………………………GC—ZG—05—0143 管理评审报告………………………………………GC—ZG—05—0244 管理评审改进跟踪验证表…………………………GC—ZG—05—03三、人员与培训45 职工教育培训计划…………………………………ZD—RP—01—0146 培训方案……………………………………………ZD—RP—01—0247 培训签到表…………………………………………ZD—RP—01—0348 个人培训考核记录…………………………………ZD—RP—01—0449 培训考核汇总表……………………………………ZD—RP—01—05 序号记录名称记录编号50 培训汇总表…………………………………………ZD—RP—01—0651 外出培训登记表……………………………………ZD—RP—01—0752 健康检查工作安排…………………………………ZD—RP—02—0153 员工健康档案表……………………………………ZD—RP—02—0254 体检汇总表…………………………………………ZD—RP—02—0355 员工健康异常情况报告单…………………………ZD—RP—02—0456 企业员工花名册……………………………………ZD—RP—03—0157 应聘登记表…………………………………………ZD—RP—03—02四、设施设备58 设施设备台帐…………………………………… ZD—SS—01—0159 设备检查记录…………………………………… ZD—SS—01—0260 设备保养记录…………………………………… ZD—SS—01—0361 设备维修记录…………………………………… ZD—SS—01—0462 设施设备档案…………………………………… ZD—SS—01—05五、校准与验证63 检定、校准与验证计划………………………… ZD—JY—01—01六、计算机64 计算机系统操作权限授权审批表…………………ZD—JX—02—01七、采购65 首营企业审批表………………………………… ZD—CG—02—0166 首营品种审批表………………………………… ZD—CG—03—0167 销售员资格验证记录卡………………………… ZD—CG—04—0168 药品采购计划…………………………………… GC—CG—01—0169 中药材采购计划………………………………… GC—CG—01—0270 中药饮片采购计划……………………………… GC—CG—01—0371 药品采购记录…………………………………… GC—CG—01—0472 中药材采购记录………………………………… GC—CG—01—05 序号记录名称记录编号73 中药饮片采购记录……………………………… GC—CG—01—0674 专门管理药品采购记录………………………… GC—CG—01—0775 冷藏、冷冻药品采购记录……………………… GC—CG—01—0876 直调药品采购记录……………………………… GC—CG—01—0977 购进药品退出通知单…………………………… GC—CG—01—1078 购进药品退出记录……………………………… GC—CG—01—1179 购进专门管理药品退出记录…………………… GC—CG—01—1280 购进中药材退出记录…………………………… GC—CG—01—1381 购进中药饮片退出记录………………………… GC—CG—01—14八、收货与验收82 药品收货记录…………………………………… GC—SY—01—0183 中药材收货记录………………………………… GC—SY—01—0284 中药饮片收货记录……………………………… GC—SY—01—0385 冷藏、冷冻药品收货记录……………………… GC—SY—01—0486 专门管理药品收货记录………………………… GC—SY—01—0587 药品到货拒收记录……………………………… GC—SY—01—0688 中药材到货拒收记录…………………………… GC—SY—01—0789 中药饮片到货拒收记录………………………… GC—SY—01—0890 冷藏、冷冻药品到货拒收记录………………… GC—SY—01—0991 专门管理药品到货拒收记录…………………… GC—SY—01—1092 委托运输药品收货记录………………………… GC—SY—01—1193 委托运输中药材收货记录……………………… GC—SY—01—1294 委托运输中药饮片收货记录…………………… GC—SY—01—1395 委托运输冷藏、冷冻药品收货记录…………… GC—SY—01—1496 委托运输专门管理药品收货记录……………… GC—SY—01—1597 药品到货拒收单……………………………………GC—SY—01—1698 销后退回药品收货记录………………………… GC—SY—01—17序号记录名称记录编号99 销后退回中药材收货记录…………………………GC—SY—01—18 100 销后退回中药饮片收货记录………………………GC—SY—01—19 101 销后退回冷藏、冷冻药品收货记录………………GC—SY—01—20 102 销后退回专门管理药品收货记录…………………GC—SY—01—21 103 销后退回药品到货拒收单…………………………GC—SY—01—22 104 销后退回药品到货拒收记录………………………GC—SY—01—23 105 销后退回中药材到货拒收记录……………………GC—SY—01—24 106 销后退回中药饮片到货拒收记录…………………GC—SY—01—25 107 销后退回冷藏、冷冻药品到货拒收记录…………GC—SY—01—26 108 销后退回专门管理药品到货拒收记录……………GC—SY—01—27 109 药品验收记录…………………………………… GC—SY—02—01 110 中药材验收记录………………………………… GC—SY—02—02 111 中药饮片验收记录……………………………… GC—SY—02—03 112 专门管理药品验收记录………………………… GC—SY—02—04 113 冷藏、冷冻药品验收记录……………………… GC—SY—02—05 114 销后退回药品验收记录………………………… GC—SY—02—06 115 销后退回中药材验收记录……………………… GC—SY—02—07 116 销后退回中药饮片验收记录………………………GC—SY—02—08 117 销后退回专门管理药品验收记录…………………GC—SY—02—09 118 销后退回冷藏、冷冻药品验收记录………………GC—SY—02—10119 直调药品验收记录…………………………………GC—SY—02—11 120 药品验收拒收单…………………………………GC—SY—02—12 121 药品验收拒收记录…………………………………GC—SY—02—13 122 中药材验收拒收记录………………………………GC—SY—02—14 123 中药饮片验收拒收记录……………………………GC—SY—02—15 124 专门管理药品验收拒收记录………………………GC—SY—02—16 125 冷藏、冷冻药品验收拒收记录……………………GC—SY—02—17 序号记录名称记录编号126 销后退回药品验收拒收单………………………GC—SY—02—18 127 销后退回药品验收拒收记录……………………GC—SY—02—19 128 销后退回中药材验收拒收记录……………………GC—SY—02—20 129 销后退回中药饮片验收拒收记录…………………GC—SY—02—21 130 销后退回专门管理药品验收拒收记录……………GC—SY—02—22 131 销后退回冷藏、冷冻药品验收拒收记录…………GC—SY—02—23 九、储存与养护132 近效期药品催销月报表…………………………ZD—CY—03—01 133 外来人员进出库房登记表…………………………ZD—CY—05—01 134 药品库存记录……………………………………GC—CY—01—01 135 专门管理药品库存记录………………………… GC—CY—01—02 136 中药材库存记录………………………………… GC—CY—01—03 137 中药饮片库存记录……………………………… GC—CY—01—04 138 冷藏、冷冻药品库存记录……………………… GC—CY—01—05 139 库房巡检记录…………………………………… GC—CY—01—06 140 药品养护计划…………………………………… GC—CY—02—01 141 重点养护药品养护计划………………………… GC—CY—02—02 142 药品养护记录……………………………………GC—CY—02—03 143 中药材养护记录…………………………………GC—CY—02—04 144 中药饮片养护记录………………………………GC—CY—02—05 145 重点养护药品养护记录…………………………GC—CY—02—06 146 重点养护中药材养护记录………………………GC—CY—02—07 147 重点养护中药饮片养护记录……………………GC—CY—02—08 148 设施设备、环境、卫生养护检查记录…………GC—CY—02—09 149 药品养护分析报告表……………………………GC—CY—02—10 150 不合格药品库存记录……………………………GC—CY—03—01 151 不合格药品销毁审批表…………………………GC—CY—03—02 序号记录名称记录编号152 不合格药品报损审批表…………………………GC—CY—03—03 153 不合格药品报损记录…………………………… GC—CY—03—04 154 不合格药品销毁记录…………………………… GC—CY—03—05 155 不合格药品情况汇总分析表…………………… GC—CY—03—06 156 可疑药品报告确认表………………………………GC—CY—03—07 157 库存盘点报表…………………………………… GC—CY—04—01 158 盘点情况原因分析及处理报告………………… GC—CY—04—02 159 直接入库单……………………………………… GC—CY—04—03160 直接出库单……………………………………… GC—CY—04—04 161 直接入库记录…………………………………… GC—CY—04—05 162 直接出库记录…………………………………… GC—CY—04—06 163 库存不合格药品盘点报表……………………… GC—CY—04—07 164 温湿度监测记录………………………………… GC—CY—05—01 十、销售165 购货单位资格审批表…………………………… ZD—XS—01—01 166 药品销售单……………………………………… GC—XS—01—01 167 药品销售记录…………………………………… GC—XS—01—02 168 专门管理药品销售记录………………………… GC—XS—01—03 169 冷藏、冷冻药品销售记录……………………… GC—XS—01—04 170 中药材销售记录………………………………… GC—XS—01—05 171 中药饮片销售记录……………………………… GC—XS—01—06 172 直调药品销售记录……………………………… GC—XS—01—07 173 药品抽样检查出库单…………………………… GC—XS—01—08 174 药品抽样检查出库记录。
药店GSP管理表格-全套
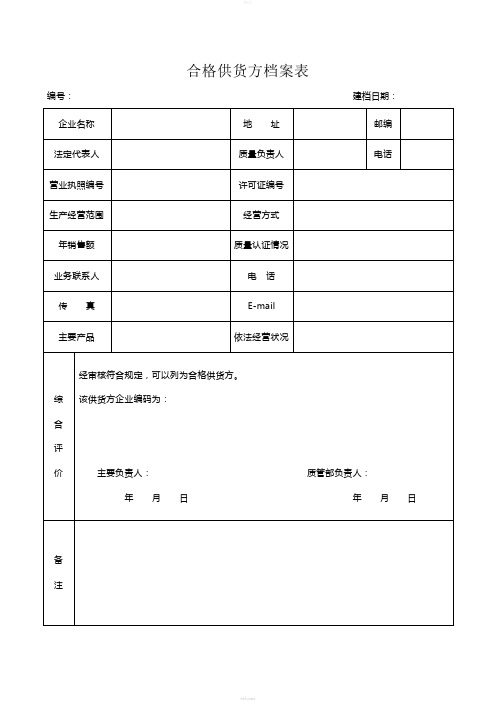
商品名称
外文名称
有效期
规格
批准文号
剂型
GMP认证
生产企业
地址
邮编
用途
建档目的
检验项目
性状
包装情况
内:
储存条件
中:
外:体积:
养
护
质
量
问
题
摘
要
时间
生产批号
质量问题饮片装斗复核记录
日期
品名
规格
生产日期
生产厂商
装斗数量
操作人
质量状况
复核人
备注
药品拆零销售记录表
药品通用名称:商品名称:
药品通用名称
商品名称
品种类别
剂型
规格
有效期
批准文号
储存条件
生产企业
GMP证书号
供货联系人
电话
传真
质量状况
综
合
评
价
经审核符合规定,可以列为合格经营品种。
该药品品种编码为:
主要负责人:质管部负责人:
年月日年月日
备
注
附:1.药品质量标准、2.药品外包装、3.药品说明书
首营企业审批表
编号:
企业名称
进货数量
验收人员
验收日期
不合格数量
不合格情况发现地点
不合格情况发现日期
不合格原因
保管员:年月日
不合格情况复查
负责人:年月日
质量管理部意见
负责人:年月日
主管负责人审批意见
负责人:年月日
备注
不合格药品台帐
编号:
日期
通用
名称
商品
名称
生产
96药品储存养护信息汇总分析报表

日期:年月日
普通养护质量情况
本季度共养护在库药品品种批次,品种未发现有质量异常现象。
重点养护品种质量情况
本季度重点养护品种药品品种批次,品种,经重点检查未发现有质量异常现象。
养护用仪器、设备质量情况
仓库用养护设施、设备的质量情况
对库房的排风扇、温湿度测定仪、照明设施等检查,异常现象。
仓库温湿度情况观察
Hale Waihona Puke 近效期药品及长期储存药品情况1、本季度在库近效期药品个品种,未发现有质量异常现象。
2、本季度长时间储存药品共个品种,在养护过程中,未发现有质量异常现象。
库房管理情况检查
汇总分析
储运部门意见
负责人:
质管部门意见
负责人:
药品质量养护信息汇总报表

填报单位:昆明泰和医药业有限公司
养护员:
注:1.总购进金额内包括纯购、调入和进口,总销售金额内包括纯销售、调出、总购进金额、季末库存金额与总销售金额均以统计数字为准。
2.计算:(1)总购金额%为入库验收有质量问题金额占本季总购进金额百分比。
(2)占库存金额%为在库检查有质量问题金额占季末库存金额百分比。
(3)占总销金额%为售后查询(结案)有质量问题金额占本季总销金额百分比。
昆明泰和医药有限公司
_________年_______季度药品质量养护信息汇总表
填报日期: 年 月 日金额单位:万元。
新GSP内审检查表--储存与养护

检查项目
责任人
整改时限
*08604
8605
养护人员应当按照养护计划对库 存药品的外观、包装等质量状况 进行检查,并建立养护记录。
8606
养护人员应当对储存条件有特殊 要求的或者有效期较短的品种进 行重点养护。 养护人员发现有问题的药品应当 及 时 在 计 算 机 系 统中 锁定 和记 录,并通知质量管理部门处理。
8609
养护人员应当定期汇总、分析养 护信息。
*08701
企业应当采用计算机系统对库存 药品的有效期进行自动跟踪和控 制,采取近效期预警及超过有效 期自动锁定等措施,防止过期药 品销售。
8801
药品因破损而导致液体、气体、 粉末泄漏时,应当迅速采取安全 处理措施,防止对储存环境和其 他药品造成污染。 对质量可疑的药品应当立即采取 停售措施,并在计算机系统中锁 定,同时报告质量管理部门确认 。 对存在质量问题的药品应当存放 于标志明显的专用场所,并有效 隔离,不得销售。 怀疑为假药的,及时报告药品监 督管理部门。
储存药品的货架、托盘等设施设 2.有货架、托盘等储存设施设备的检查、维护记录。 备应当保持清洁,无破损和杂物 3.货架、托盘等储存设施设备应清洁、无杂物堆放,保证药品不 堆放。 受污染。 4.货架、托盘等储存设施设备应完好无损,保证药品储存、摆放 安全。 1.有储存作业区人员出入管理制度,人员必须经过授权方可进出 未经批准的人员不得进入储存作 药品库房。 2.应采用门禁系统、人员登记等方式对库房进出人员实行可控管 业区。 理,防止药品被盗、替换或者混入假药。 储存作业区内的人员不得有影响 药品质量和安全的行为。 药品储存作业区内不得存放与储 存管理无关的物品。 储存作业区内的人员不得有不得有洗漱、就餐、饮酒员的日常生活用品,打扫卫生的 工具等。 1.有药品养护管理制度或规程,有养护岗位职责。
药品养护员工作总结

药品养护员工作总结篇一:药品养护工作总结20XX 年养护工作总结 20XX 年药品养护工作按照“药品经营质量管理规范”的指导方向,结合公司经营品种多的特点,在质管部领导、监督、指导下不断地完善、总结养护工作:一、从严要求,认真学习。
积极参与质管部组织的培训课程。
认真学习、严格执行公司制定的药品养护管理制度。
二、分库贮存,保障药品合理贮存。
严格按药品特性进行分库、分类贮存,并对库房的温湿度进行监控、记录。
发现异常及时调节。
确保药品在合理的贮存环境中,确保药品在库质量。
二、突出重点,养护有序。
1 、按照 GSP 要求,对合格品库的药品进行防潮、防虫和温湿度控制,中药库药品注重防霉变、防潮和防泛油。
发现问题采取相应措施,如日晒或者阴干处理。
2 、结合公司经营品种多的特点,对所有在库品种均按季度按”三三四”原则进行养护、检查一次,并按季汇总建养护总结 .3 、按照“三三四”原则,对在库药品按照货柜每个季度全部巡检养护一次,并作好记录。
公司在经营过程中,从未出现有关药品质量方面的问题。
20XX 年12 月 31 日 20XX 年第一季度养护工作总结20XX 年药品养护工作按照“药品经营质量管理规范”的指导方向,结合公司经营品种多的特点,在质管部领导、监督、指导下不断地完善、总结养护工作:一、从严要求,认真学习。
篇二:药店营业员工作总结药店营业员工作总结10.养护员:10-1、坚持“质量为本”的原则,负责在库药品的养护和检查工作,对在库药品的质量负有主要责任。
10-2、负责指导保管员对库存药品进行合理科学储存,并按时做好库内、外温湿度调控管理。
10-3、对库存药品应定期进行循环检查和养护,一般药品一季一次,重点养护品种应增加次数,并做好记录。
10-4、对由于异常原因可能出现问题的药品、易变质药品、已发现质量问题药品的相邻批号药品、储存时间较长的药品,应加强养护;检查中发现质量问题的药品应及时抽样送质量管理部复验,并挂黄牌暂停发货。
药品养护管理制度

药品养护管理制度1、药品养护员应指导保管员对药品进行合理储存,营业员对陈列药品进行规范陈列,并负责做好库房、营业厅温、湿度监测和管理,每日上午(10:00左右)、下午(16:00左右)各一次对库房、营业厅的温、湿度进行记录,超出规定范围时,应及时采取调控措施,并予以记录。
2、药品养护员应每季度对在库药品进行一次检查养护(循环检查),对近效期药品、易霉变、易潮解的药品应每月进行一次养护检查;对陈列药品应按月进行检查并记录.养护检查中发现有质量疑问的药品,不得上柜销售,养护人员应立即通知质量管理人员进行处理。
3、养护人员应根据季节变化对药品进行养护,做好降温、防潮、通风工作.4、养护人员应负责养护用仪器、设备、温、湿度检查和监控仪器、仓库在用计量仪器及器具等的管理工作,建立养护设备档案。
每月对养护设备进行检查、维护,以确保其能正常运行.检查、维护应做好记录.5、养护设备的使用应有使用记录。
6、养护人员应每季度汇总、分析养护检查、近效期或长期储存。
(储存)时间2年以上,其余同)药品质量信息,报质量管理员。
7、质量管理员负责对养护工作进行监督和指导,包括审核重点养护品种等养护工作计划,处理药品养护过程中发现的药品质量问题。
药品养护“三部曲”药品养护是指在药品在药品储存过程中,对药品进行科学保养的技术性工作,是保证药品在储存期间保持质量完好的一项重要措施,也是减少损耗、确保企业经济效益的重要手段。
由于药品从验收合格入库后一直到销售出去,整个在企业滞留期间的质量,都需要依靠养护工作提出充分的保证,因此,药品养护工作的重要性是不言而喻的。
药品在库期间,如果储存不当或者储存条件、养护设施和检测仪器运行不当都容易导致药品发生质量变化,再加上养护检查工作又不到位,就完全可能导致辞不合格药品销售给顾客,造成危害。
因此药品养护不仅是一项重要工作,更是一各责任。
药品经营企业应如何开展药品养护工作:配备专业人才,制定操作规范,开展药品养护工作,首先必须建立与经营规模相适应的养护组织,配备养护专职人员。
药品体系文件目录(201710)

目录一质量职责1. 质量管理领导小组职责 (4)2. 企业负责人质量职责 (5)3. 业务副总经理质量职责 (6)4. 质量负责人质量职责 (7)5. 质量管理部质量职责 (8)6. 质量管理部负责人质量职责 (10)7. 质量管理员质量职责 (12)8. 质量验收员质量职责 (13)9. 养护员质量职责 (14)10. 采购部质量职责 (15)11. 采购部经理质量职责 (16)12. 采购员质量职责 (17)13. 采购内勤质量职责 (18)14. 销售部质量职责 (19)15. 销售部经理质量职责 (20)16. 开票员质量职责 (21)17. 销售业务员质量职责 (22)18. 物流部质量职责 (23)19. 物流部经理质量职责 (25)20. 保管员质量职责 (26)21. 复核员质量职责 (27)22. 收货员质量职责 (28)23. 运输组长质量职责 (29)24. 药品运输员(送货员)质量职责 (30)25. 送货车辆驾驶员质量职责 (31)26. 财务部质量职责 (33)27. 财务部经理质量职责 (35)28. 会计质量职责 (36)29. 出纳质量职责 (37)30. 综合部质量职责 (38)31. 综合部经理质量职责 (39)32. 系统管理员质量职责 (40)33. 客户服务人员质量职责 (41)34. 第二类精神药品管理机构及人员职责 (42)35. 蛋白同化制剂、肽类激素经营管理部门及人员职责 (49)36. 收银员质量职责 (56)二质量管理制度1. 质量管理体系内审制度 (58)2. 质量否决制度 (61)3. 质量管理体系文件管理制度 (63)4. 质量方针目标管理制度 (67)5. 质量风险管理制度 (70)6. 质量管理制度检查考核制度 (73)7. 质量信息管理制度 (75)8. 供货单位资质审核制度 (77)9. 供货单位销售人员资格审核制度 (80)10. 购货单位资格审核制度 (82)11. 购货单位采购人员资格审核制度 (85)12. 首营企业审核制度 (87)13. 首营品种审核制度 (89)14. 药品采购管理制度 (91)15. 药品收货管理制度 (93)16. 药品质量验收管理制度 (95)17. 药品储存管理制度 (98)18. 药品养护管理制度 (101)19. 药品销售管理制度 (103)20. 药品出库复核制度 (106)21. 药品运输管理制度 (109)22. 药品效期管理制度 (111)23. 不合格药品和销毁管理制度 (113)24. 药品采购退出管理制度 (115)25. 药品销后退回管理制度 (117)26. 药品召回管理制度 (119)27. 药品质量查询管理制度 (121)28. 质量事故报告制度 (123)29. 质量投诉管理制度 (126)30. 药品不良反应报告管理制度 (128)31. 药品售后服务及客户访问管理制度 (130)32. 药品追回管理制度 (132)33. 环境卫生和人员健康管理制度 (134)34. 员工个人卫生管理制度 (136)35. 质量教育、培训管理制度 (137)36. 校准管理制度 (139)37. 设施设备验证管理制度 (141)38. 人员出入库管理制度 (145)40. 冷藏药品管理制度 (149)41. 设施设备管理制度 (152)42. 质量记录和凭证管理制度 (154)43. 计算机信息系统管理制度 (156)44. 计算机系统数据安全及数据备份管理制度 (158)45. 计算机系统数据维护管理制度 (160)46. 药品追溯体系管理制度 (163)47. 药品电子监管管理制度 (167)48. 质量基础数据编码规则及标准管理制度 (170)49. 直调药品管理制度 (177)50. 人员资质及档案管理制度 (179)51. 第二类精神药品管理制度 (181)52. 蛋白同化制剂、肽类激素管理制度 (185)53. 终止妊娠药品管理制度 (189)54. 含特殊药品复方制剂管理制度 (191)55. 考勤管理制度 (194)56. 发票管理办法 (196)57. 销售管理结算办法 (198)三质量操作程序1. 药品采购程序 (201)2. 首营企业审核程序 (203)3. 首营品种审核程序 (205)4. 供应商质量管理体系评审程序 (207)5. 药品收货程序 (210)6. 药品质量验收程序 (212)7. 药品入库储存保管程序 (215)8. 药品养护程序 (217)9. 库存药品盘点程序 (218)10. 药品销售程序 (220)11. 药品出库复核程序 (221)12. 药品运输程序 (222)13. 药品拆零和拼装发货程序 (224)14. 计算机系统操作程序 (225)15. 购货方质量管理体系评审程序 (227)16. 药品召回程序 (230)17. 药品售后服务及用户访问程序 (232)18. 质量投诉处理程序 (233)19. 不合格药品确认和处理程序 (234)20. 药品质量风险管理操作程序 (236)21. 冷库操作程序 (239)22. 冰排、保温箱操作程序 (240)23. 冷藏车操作程序 (242)24. 红外测温仪操作程序 (244)25. 备用发电机操作程序 (245)26. 冷藏药品收货、验收操作程序 (250)27. 冷藏药品储存、养护操作程序 (252)28. 冷藏药品出库复核、装箱操作程序 (254)29. 冷藏药品运输操作程序 (255)30. 冷藏药品储存和运输应急预案 (257)31. 温湿度自动监测系统操作程序 (260)32.温湿度检测终端校准操作程序 (262)四质量记录1. 内审计划表 (266)2. 内审检查表 (267)3. 质量管理体系内审报告 (268)4. 限期整改通知单 (269)5. 停售通知 (270)6. 解除停售通知 (271)7. 文件编码登记表 (272)8. 文件修订申请表 (273)9. 文件发放记录 (274)10. 文件回收记录 (275)11. 文件销毁审批记录 (276)12. 质量目标展开图 (277)13. 质量目标检查表 (278)14. 药品经营质量风险点排查表 (279)15. 质量风险点报告表 (280)16. 质量风险评估、沟通、审核记录 (281)17. 风险控制后未消除项目表 (282)18. 质量管理制度执行情况检查表 (283)19. 商品质量信息分析处理表 (284)20. 商品质量信息汇总分析报表 (288)21. 基础信息修改申请单 (286)22. 客户资质审核表 (287)23. 供货单位质量体系实地考察审核表 (288)24. 首营企业审批表 (289)25. 合格供货方档案表 (290)26. 首营品种审批表 (291)27. 药品质量档案表 (292)28. 采购合同 (293)29. 药品采购记录 (294)30.供货方供货情况评审表 (295)31.药品收货记录 (296)32.冷藏、冷冻药品收货记录 (297)33.药品拒收报告单 (298)34.销后退回药品收货记录 (299)35.药品质量验收记录 (300)36.药品采购入库单 (301)37.销货退回申请单 (302)38.药品销后退回验收记录 (303)40.药品质量验收复原标签 (305)41.药品入库记录 (306)42.盘点表 (307)43.盘点差错明细及处理审批表 (308)44.药品养护记录 (309)45.重点养护品种确定表 (310)46.药品养护档案表 (311)47.药品养护检查情况汇总分析表 (312)48.药品质量复查报告单 (313)49.药品销售合同 (314)50.销售记录 (315)51.销售结算单 (316)52.随货同行(出库复核)单 (317)53.药品出库复核记录 (318)54.药品拼箱清单 (319)55.药品拼箱标签 (320)56.药品运输记录 (321)57.冷藏、冷冻药品运输交接单 (322)58.冷藏、冷冻药品运输记录 (323)59.承运方运输药品质量保障能力审计表 (324)60.委托运输记录 (325)61.近效期药品预警表 (326)62.不合格药品台账 (327)63.不合格药品报损审批表(附清单) (328)64.不合格药品销毁记录 (329)65.不合格药品销毁清单 (330)66.不合格药品处理情况汇总分析 (331)67.药品采购退出单 (332)68.药品采购退出记录 (333)69.药品销后退回记录 (334)70.药品召回确认函 (335)71.药品召回通知(客户) (336)72.药品召回记录 (337)73.药品质量查询函 (338)74.药品质量查询记录 (339)75.质量事故报告单 (340)76.质量事故纠正和预防措施报告 (341)77.药品质量投诉登记处理表 (342)78.药品不良反应报告表 (343)80.药品群体不良事件基本信息表 (345)81.客户意见及投诉受理卡 (346)82.商品质量、服务质量征询意见书 (347)83.客户访问档案 (348)84.药品追回记录 (349)85.员工健康检查汇总表 (350)86.员工健康档案表 (351)87.企业员工年度质量培训计划表 (352)88.培训签到记录 (353)89.员工培训记录统计表 (354)90.培训效果调查表 (355)91.员工个人培训教育档案 (356)92.计量器具定期检定计划 (357)93.强制检定计量器具检定记录卡 (358)94.非强制检定计量器具检定卡 (359)95.验证控制数据及结论汇总表 (360)96.出入库登记表 (361)97.库房安全巡查记录表 (362)98.冰柜温度记录 (363)99.保温箱、冰排使用记录 (364)100.冷藏、冷冻药品装箱出库记录 (365)101.设施设备管理台帐 (366)102.设施设备维护维修记录 (367)103.设施设备使用记录 (368)104.计算机信息系统权限审批表 (369)105.计算机数据修改申请表 (370)106.直调药品申请表 (371)107.直调药品采购记录 (372)108.直调药品验收记录 (373)109.直调药品销售记录 (374)110.员工简历表 (375)111.特殊管理及专管药品验收记录 (376)112.特殊管理及专管药品管理台帐 (377)113.购买特殊药品及专管药品购买方经办人员身份证明核实登记表 (378)114.特殊管理及专管药品出库复核记录 (379)115.甘肃省麻醉药品和精神药品销毁处置单 (380)116.特殊管理药品及专管药品到货核实记录 (381)117. 进货拼箱标签 (382)118. 报损品种具体分析表 (383)。
GSP表格
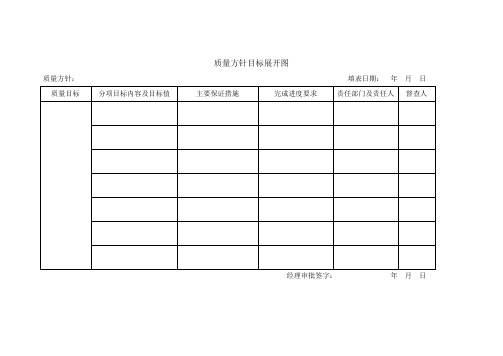
质量方针目标展开图质量方针:填表日期:年月日经理审批签字:年月日质量方针目标检查表质量方针:填表日期:年月日总经理:主管副总经理:质管部负责人:记录人:年度质量培训计划表编号:审批人:人力资源部:质量管理部:员工培训记录表编号:培训主题:培训时间:员工培训考核表编号:填表日期:主管领导:人力资源:质量管理部:填表人:员工培训效果调查表编号:填表日期:员工个人培训教育档案档案编号:年度企业员工健康检查汇总表编号:员工健康档案编号:建档时间:注:应将历次体检结果证明文件存入档案。
文件编码登记表页码:文件发放、回收记录编号:编号:编号:文件销毁审批记录编号:信息联系处理单编号:本单一式三份:信息发出部门、接收部门、质量管理部门各一份编号:建档时间:编号:药品购货计划表(年第季度)编号:制表日期:制表人:业务部门经理:质管部:财务部:总经理/副总经理:18编号:填表日期:编号:注:附药品生产企业许可证、营业执照、批准文件、质量标准、出厂检验报告、样品、价格批文、GMP证书及临床总结报告等资料。
药品购进记录编号:药品到货请验通知单验收组:现有以下购进/退回药品到货,请给予验收。
购进药品验收记录编号:销后退回药品验收记录编号:药品验收入库通知××××药品仓储保管组:以下购进/退回药品经质量检查验收合格,请予办理入库手续。
编号:验收员:保管员:入库日期:药品拒收报告单编号:药品停售通知单年第号名有关部门:以下药品因质量问题决定停售,请按有关规定采取有效措施停止出售,等等处理。
药品通用名称规格产品批号有效期生产日期生产企业质量管理部年月日(一式四联:一联质管部留存,二联仓储部,三联业务部门,四联必要时送外联客户)解除停售通知单年第号各有关部门:以下药品经质量复查结果合格,撤消年第号“药品停售通知单”,请恢复正常出库发货及销售,特此告知。
药品通用名称规格产品批号有效期生产日期生产企业质量管理部年月日(一式四联:一联质管部留存,二联仓储部,三联业务部门,四联必要时送外联客户)药品质量复查报告单编号:说明:本表一式三联,一联申请复查部门留存,二联质量管理部门复查后留存,三联复查后返回申请部门。
药品养护操作规程

1、目的:确保药品储存过程的质量,规范药品养护。
2、依据:药品管理法、药品经营质量管理规范等法律法规规章。
3、适用范围:所经营药品的在库养护、检查及其他养护工作。
4、责任人:养护员。
5、操作规程:5.1 检查药品储存作业是否合理:5.1.1 是否按药品的储存管理要求分库或分区,标识是否明显;5.1.2 药品储存的温湿度是否符合要求;5.1.3 药品是否按批号堆码,不同批号药品有无混垛,垛间距、药品与内墙、顶、温湿度调控设备及管道间距、与地面间距是否符合规定;5.1.4 药品是否有倒置;5.1.5 储存运输人员放置药品是否轻拿轻放。
5.2 设施设备是否正常运转:5.2.1 是否有效采取避光、遮光、防鼠、防虫等措施;5.2.2 每日检查库内卫生环境是否清洁;5.2.3 检查各类设备有无异常。
5.3 库房温湿度监测:5.3.1 自动监测系统是否运转正常并按规定记录;5.3.2 温湿度超出范围时应排查原因;5.3.3 出现温湿度超标及时采取措施并记录5.4药品养护:541确定重点品种:近效期药品、冷藏或有特殊温度要求的重点养护;5.4.2养护原则:一般药品每季度循环检查一次,重点品种每月养护检查一次;成的计划,进行药品包装和外观检查,并记录,养护抽样按验收抽样原则执行;5.4.3.1片剂有无裂片,变色;543.2丸剂是否圆整均匀,蜜丸软硬适中;543.3颗粒剂、散剂应干燥,无吸潮、软化、结块等;5.4.3.4锭剂、栓剂无变形;5.4.3.5合剂、口服液应澄清,无酸败、异臭等;5.4.3.6胶囊剂无粘结、无变形、无破裂等;5.4.3.7酒剂应澄清,可有少量轻摇易散的沉淀;5.4.3.9 膏剂(黑膏药)应乌黑油亮,老嫩适度,无红斑、无飞边;5.4. 3每月末按系5.4.3.8酊剂应澄清;5.4.3.10 橡胶膏剂应无脱膏;5.4.3.11 注射剂应无明显可见异物;5.4.3.12 软膏剂无酸败、异臭、变色、变硬等;5.4.3.13 糖浆剂应澄清,无酸败、异臭等变质现象,含药材提取物的可有少量轻摇易散的沉淀。
药品养护管理制度

药品养护管理制度1.养护员指导并协助保管员对药品进行合理储存,每日上班每间隔1小时在电脑上查看一次温湿度自动记录仪的显示情况。
2.发现温、湿度超标要采取相应调控措施,如:打开空调、换气扇、拖把加湿拖地等,进行除湿、通风、降温、保湿、恒温处理措施。
确保库房温、湿度控制在规定范围内,并将处理过程和结果记录在《养护设备使用记录》上,以备后查。
3.养护员每季度应将库内所有品种按30%、40%的比例循检一遍。
随机抽取3件药品打开外包装箱,从中间和底部各取出一盒(瓶)药品检查其外观质量,摇晃声音是否异常、中包装盒是否破损等,若药品完好无损应恢复原样。
4.每月对重点品种进行养护。
重点包括:首营品种、新品种、主营品种、质量不稳定品种、药监部门重点检测品种、近效期品种的养护。
检查药品外包装是否符合标准、药品有无短缺、破损,外观质量有无异常等。
发现问题及时悬挂“停售”黄牌,填写药品《停售通知单》,通知保管员暂停发货,并在养护系统中反映该问题药品,通知开票员暂停开票,同时上报质量管理部复查处理.5.养护员每季度将仓库进货总批次、养护批次、养护情况等记录汇总,对养护中的不合格药品的原因进行分析,提出改进建议,并上报质量管理部。
每季度将“重点养护药品确定表”、“药品质量养护检查记录”存档。
每年将养护设施、设备使用检查记录存档管理。
以上存档记录和养护检查档案至少保存三年。
药品温湿度管理制度为了加强仓库的温湿度管理,满足药品贮存条件的要求,保证药品质量,保障人民用药安全,特制定以下制度:一、库内温湿度应严格控制在规定的范围内:常温库:温度10~30℃相对湿度45% ~75%阴凉库:温度不高于相对湿度45% ~75%冷库:温度2~10℃相对湿度45% ~75%二、养护组成员负责督促各库保管员每天上午9:30,下午3:30两次对各库温湿度进行记录;三、养护员必须每天对各库的温湿度进行检测,针对超标的实际情况,结合库外环境状况,组织相关人员采取开关门窗、洒水增湿、启动空调等相应措施,使之达到各库温湿度的要求,并对采取的措施及调控后的结果进行记录;四、双休日及法定节假日由领导指定专人对温湿度进行监测记录;五、室外的温湿度记录工作由养护员完成,各库的温湿度记录表每月底由养护组统一收集整理归档。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
□重点检查发现有质量异常现象药品品种_______________________
养护用设施设备质量状况
仓库养护用设施设备的质量状况:对库房的托盘、货架、温湿度监测系统、空调(及滤网)、制冷机组、排气扇、照明设施、灭火器或消防栓、老鼠夹、粘鼠板、电子猫、防鼠板、灭蝇灯、干燥剂、加湿器、除湿机、吸尘器、电子称等检查
养护员意见
质管部门
意见
如有侵权请联系告知删除,感谢你们的配合!
2、本季度库龄较长药品共_______个品种
□未发现有质量异常现象□发现有质量异常现象药品________________□货位整齐□堆码规范□五距适当□色标明显□卫生较好□门窗结构严密
汇总分析
通过对本季度在库药品的养护(一般养护和重点养护),总体情况□符合□不符合GSP条款要求,针对近效期的______个品种,及库龄较长的_____个品种,共计____个品种填写药品催销表进行催销,并加强养护,保证药品质量不受影响。建议公司领导通过对各品种销售情况的分析,结合仓库库存及库容,加强进货计划的审核力度,以保证在库药品不积压,不滞销,合理利用库容,对销量小或不稳定的品种,采取少进货或不进货的方式,以减少在库品种积压的情况。
药品储存养护信息汇总分析报表
______年第____季度
日期:年月日
已检查药品
质量状况
本季度养护在库药品品种________批次,中药饮片________批次。
□未发现有质量异常现象
□发现有质量异常现象药品品种______________________________
重点养护品种质量状况
本季度重点养护药品品种_______批次(其中麻精药品______批次,国家有专门管理要求的药品______批次,冷藏冷冻药品______批次,近效期药品_______批次,库龄较长品种_______批次),中药饮片________批次。
□未发现有质量异常现象
□发现有质量异常现象__________________________
仓库温湿度
情况
仓库
最高温度
最低温度
平均温度
最高湿度
最低湿度
平均湿度
常温库
阴凉库
麻精库
中药饮片库
冷库
近效期药品
及库龄较长
药品情况
1、本季度近效期药品______个品种
□未发现有质量异常现象□发现有质量异常现象药品___________________
