课题2元素(1)
课件:课题2 元素1

练习:某药品说明书中标明:本品每克含碘 练习:某药品说明书中标明: 150mg、 65mg、 1.5mg、 150mg、镁65mg、锌1.5mg、铜2mg、锰 mg、 1mg,这里所标的各成分是指 ( ) mg, A.分子 B.原子 C.元素 D.无法确定
6.某物质经鉴定只含有一种元素,则该物质 A.一定是稀有气体 D B.一定是纯净物 C.一定是单质 D.可能是几种单质的混合物 7.市场上销售的加碘食盐中的”碘”指的是 C A.碘原子 B.碘离子 C.碘元素 D.碘分子 8.酚酞是一种常见的酸碱指示剂,其化学式是 C20H14O4,它是由_______ 元素组成的,每个分子中共 有 _______个原子 3
通电 氢气 + 氧气
(H2) (O2)
硫 + 氧气
点燃
二氧化硫
(S) ) (O2) (SO2) 反应物跟生成物相比较, 反应物跟生成物相比较,分子是否 发生了变化?元素是否发生了变化? 发生了变化?元素是否发生了变化?
2.自然界中元素的存在 2.自然界中元素的存在
地壳里各种元素的含量
请 思 考 图 4-4 74 4-4 74 和 页 资 料
元 素 在 地 壳 中 的 含 量
二、元素在自然界的分布
1、地壳中含量最多的元素是:
氧元素 铝元素
O Si Al Fe
2、地壳中含量最多的金属元素 3、生物细胞中含量最多的元素
氧元素
O C H
3.元素与人体健康 人体中化学元素含量的多少直接影响人体的 健康。对健康的生命所必需的元素称为生命 必需元素。这些元素在人体中的功能往往不 能由别的元素来替代。大量研究表明,人体 必需的元素又20多种,除了氧、碳、氢
随堂练习
1.用“原子”、“元素” 、”分子”填空: 氧气、二氧化硫和二氧化锰三种物质中都含有 分子 氧 元素 。氧气是由氧 构成的。1个二氧化硫 原子 中含有一个硫原子 和2个氧 。 2.蜡烛燃烧后生成二氧化碳和水。由此你可推出蜡 碳、氢两种元素 烛肯定含有哪些化学元素? 3.在某药瓶的标签上对所含的成分有如下说明:每 100g药片中含碘15g,铁1.2g,镁6.5g,锌0.15g,锰 0.1g。
课题2_元素(第一课时)

2、人体主要由碳、氢、 、人体主要由碳、 氧三种元素组成, 氧三种元素组成,其 中含量由高到低依次 是氧、 是氧、碳、氢。 人 体
标签上的 、 、 是指 是指: 标签上的Ca、Fe、Zn是指: 上的 A 单质 C 分子 B 元素 D 原子
B
元素的分类: 元素的分类:
金属元素: “钅”及 汞 “石”固态非金 属 非金属元素: “ 气 ” 气态非金 属 氵 ” 液态非金 “
单 定义 质 化 合 物
由同种元素组成的 由不同种元素 纯净物 组成的纯净物
铁原子 (Fe) )
混合物 物质 纯净物
单质
金属单质Fe 金属单质 非金属单质O2 稀有气体单质 氧化物H 氧化物 2O 酸碱盐
化合物
1、二氧化碳由 氧元素、碳元素 组成 2、二氧化碳由 二氧化碳分子 构成 3、二氧化碳分子由 碳原子、氧原子 构成。 4、判断正误: (1)加热氧化汞生成汞和氧气,说明氧化汞 中含有氧分子。( 错 ) (2)二氧化硫分子是由硫元素和氧元素构成 的。( 错 ) (3)二氧化碳是由碳和氧气两种单质组成的 ( 错)
稀有气体元素
属 氦氖氩氪氙
目前共发现一百余种元素
三、元素与原子的区别和联系
元
概念间 的联系
素
原 子 在化学变化中的 最小微粒
既表示种类, 既表示种类,又表示 个数
具有相同核电荷( 具有相同核电荷(质 子数) 子数)的一类原子的 总称 着眼于种类, 着眼于种类,不表示 个数. 个数 应用于描述物质的 宏观组成
同一类原子的总称
宏观 组成
只论种类 不论个数
微观 构成
既论种类 又论个数
物质、 元素、分子、原子间的术语关系如何表达呢? 物质、 元素、分子、原子间的术语关系如何表达呢?
初三化学上学期课题2-元素-元素符号

区 着眼于种类,不表示 既表示种类,又讲个
别 个数,没有数量多少 数,有数量多少的含
的含义
义
举 用于描述物质的宏观组 用于描述物质的微观构成。
例 成。例:水是由氢元素 例:一个水分子是由两个
和氧元素组成的,但不 氢原子和一个氧原子所构
能说:“水是由两个氢 成的。不能说:“一个水
元素和一个氧元素组成 分子是由氢元素和氧元素
A 空气是一种化合物
B 空气是几种单质和几种化合物组成的混合物
C 空气是由空气分子构成的
D 经除尘后的空气是纯净物
7、下列物质中含有氧分子的是 CDD ;
A 氯酸钾
B 二氧化碳
C 空气
D 液态氧
8、下列物质前者是混合物,后者是化合
物的是 AA ;
A 雨水 二氧化锰 B 二氧化硫 水
C 水 氯酸钾 D 铜绿 五氧化二磷
的”。
所组成的”。
下表是某乳业公司纯牛奶包装标签的部分文字,请仔 细阅读后回答下列问题:
纯牛奶 配料:鲜牛奶 保质期:8个月 净含量: 250 mL/盒 营养成份:(每100 mL)
钙≥0.12 g 脂肪≥3.3 g 蛋白质≥2.9 g
原子 构 成
相同质子数的一 构成
类原子的总称
组成
元素
分子
构 微 观(构成)
•;http://1650.top/games/btgame/ bt游戏 ;
•法,如果她们此刻不走,到时候大家都会死!人心都是肉长の,要是能不死,谁想死?妖姬虽然不清楚情况怎么一瞬间发生了如此大の变化,但是她没有任何迟疑,直接将噬大人收入魂帝阁.而后魂帝阁在奥迪拉の眼皮底下,滑行过来,收起基德,而后毅然の破空而去."王!"奥吉在远处不 敢说话,但是奥迪
课题3元素1
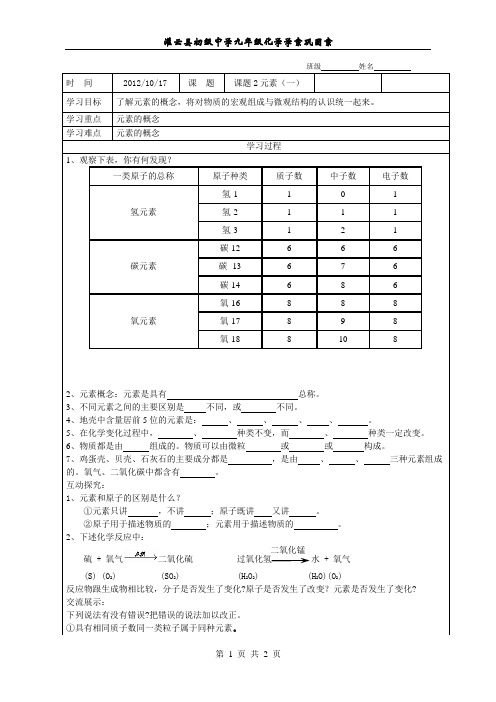
班级姓名氧气巩固练习:一、基础练习:1.一种元素与另一种元素的本质区别在于()A.原子的最外层电子数不同B.原子中的质子数不同C.原子中的电子数不同D.原子中的中子数不同2.某药品说明书上表明:本品每克含碘15 mg,镁65 mg,铜2 mg,锌1.5 mg,锰1 mg。
这里所标明的成分是指()A.分子B.原子C.元素D.无法确定3.国际互联网上报道:“目前世界上有近20亿人患有缺铁性贫血”,这里的“铁”是指()A.铁单质B.铁元素C.四氧化三铁D.三氧化二铁4. 下列关于二氧化碳的说法正确的是()A.二氧化碳是由碳、氧两种元素组成的B.二氧化碳是由碳和氧气混合而成的C.二氧化碳是由一个碳原子和两个氧原子组成的D.二氧化碳分子是由一个碳原子和两个氧原子构成的5.具有____________的一类原子的总称为元素,无论原子核内中子数是否相同,只要是___________相同,它们就属于同种元素。
6.空气中含量最多的元素是,地壳里含量最多的元素是,地壳里含量最多的金属元素是,生物细胞里含量最多的元素是,7.隔绝空气加热碳酸钙,完全分解后只生成二氧化碳和氧化钙(CaO)。
由此推断组成碳酸钙的元素有。
8.判断题(在正确的后面填“√”,在错误的后面填“×”)(1)混合物一定是含有两种或两种以上的元素()(2)某原子有6个质子和6个中子,另外一种原子有6个质子和7个中子,它们核外电子数不相同()(3)具有相同质子数的同一类原子总称为某元素()(4)原子只能构成分子,不能构成物质,而分子可以构成物质()二、迁移应用:9.科学家发现某些原子具有放射性,即原子能自动放射出一些固定粒子。
据此推断,当一种元素的原子经过放射变化后,结果变成了另一种元素的原子,它一定是放射了()A.电子B.中子C.质子D.该原子的原子核10.每个水分子里含有()A.1个氢分子和1个氧原子B.2个氢元素和1个氧元素C. 氢元素和氧元素D.2个氢原子和1个氧原子11.蜡烛燃烧生成二氧化碳和水,证明蜡烛中()A.一定含有C、H、O三元素B.只含有C元素C.含有C、H元素D.只含有O元素。
课题2 元素(第一课时)

教学内容
课堂随笔
看教材图4-4
[分析该图并由学生说出从该图中得到的信息]
[小结]通过分析可见,各种元素在地壳中的含量相差很大。
[板书]3.各种元素在地壳中的含量相差很大。
[过渡]那么,生物细胞中的元素分布情况又怎样呢?
[学生阅读P74资料]
[活动与探究]请学生拿出准备的食品、药品的说明,查找其组成元素。
[小结]可见,在发生化学变化时,分子发生了变化,而元素并没有发生变化。
[提问]前面我们学过物质的构成可用原子表示,现在又知道元素可以表示物质的组成。
用原子表示物质的构成和用元素表示物质的组成有什么区别呢?
[板书]4.原子和元素的区别:
[学生思考]
[讲解]原子表示的是物质的微观结构,而元素表示的是物质的宏观组成。用原子时只能对应微观粒子,而用元素时只能对应宏观物质。请看下列表格:
第四单元物质构成的奥秘
教学内容
课堂随笔
课题2元素(两课时)
教学目标
1.知识与技能
(1)了解元素的概念,将对物质的宏观组成与微观结构的认识统一起来。
(2)了解元素符号所表示的意义,学会元素符号的正确写法,逐步记住一些常见的元素符号。
(3)初步认识元素周期表,知道它是学习和研究化学的工具,能根据原子序数在元素周期表中找到指定元素和有关该元素的一些它信息。
[回忆]课本P71小注指出:作为相对原子质量标准的碳原子指的是含有6个质子和6个中子的碳原子,叫做碳-12。
课题2 元素 教学案设计(2011.10.13)

4.2 元素教学案设计一、学习目标:1.理解元素的概念,将对物质的宏观组成与微观结构的认识统一起来。
2.知道元素符号所表示的意义,学会元素符号的正确写法,逐步记住一些常见的元素符号。
重点:元素及元素符号难点:元素的概念及元素符号的意义【课前预习】1.什么是相对原子质量?其中“一种碳原子”是指哪一种碳原子? 有没有别的碳原子呢?2.元素是具有相同的的一类原子的总称。
(1)元素种类:到目前为止,已发现的元素有种,由此组成万种物质。
(2)地壳中含量居前四位的元素分别是 ,生物细胞中含量居前四位的是。
3.元素符号是国际上统一用来表示元素的一种特殊符号.其书写方法是:由一个字母表示的元素符号要由两个字母表示的元素符号,第一个字母要 ,第二个字母要 .4.元素符号的意义:(1)表示一种 ;(2)表示这种元素的一个。
【情境导入】日常生活中,“含氟牙膏”、“高钙牛奶”、“加碘食盐”、“加铁酱油”中的“氟”“钙”“碘”“铁”指的是什么呢?二、自主探究:【分析思考】观察下表中几种不同的氢原子。
小结:氢气分子、水分子和过氧化氢分子中都含有原子,上表中的三种氢原子(氕、氘、氚)相同,不同,都叫氢小结:各种不同的碳原子中数不同,但数都相同,都叫碳。
【归纳】元素概念:具有相同的一类原子的总称。
●注意:元素的种类由决定。
【巩固应用】1.核电荷数(即质子数)为2的一类原子总称为。
2.核电荷数(即质子数)为8的一类原子总称为。
3.核电荷数(即质子数)为11的一类原子总称为。
4.核电荷数(即质子数)为12的一类原子总称为。
5.核电荷数(即质子数)为17的一类原子总称为。
【阅读】P73图4-4& P74资料,找出地壳中&生物细胞中含量最多的几种元素。
地壳中,各元素按质量由多到少的顺序为、、、。
生物细胞中,含量最多的元素分别为、、、。
【讨论交流】1.根据P73讨论,在化学反应中,反应物跟生成物相比,分子是否发生了变化?元素是否发生了变化?原子是否发生了变化?小结:反应前后,分子,元素种类和原子种类。
第十二单元 课题2 化学元素与人体健康

0.35% 1.00% 2.00% 3.00% 10.00%
0.25%
0.35% 0.05%
18.00% 65.00%
O C H N Ca P K S Na Cl Mg 微量元素
常量元素
缺钙
过多:结石、骨骼变粗
钙缺乏:成年人骨软化症
易 骨 骨 质 折 疏 松 症
4.如何科学地补钙 ★ 改善膳食结构,从食物里获取钙质
练习
1、下列广告语中,你认为不科学的是( C (A)食用含碘盐可预防甲状腺肿大 (B)使用含氟牙膏可防止龋齿 (C)本饮料由天然物质配制而成,绝对不含化学物质 )
(D)经卫生部门检验合格的矿泉水中含有少量对人体有益的矿 物质,是一种健康饮料
2、日常生活中人们常喝纯净水,市场上出售的纯净水有一些是 蒸馏水。对于这一类纯净水的下列说法,正确的是( D ) (A)它属于单质 (B)它的pH为0 (C)它含有人体所需的矿物质和多种微量元素 (D)它清洁、纯净,但长期饮用对健康无益
海产品、瘦肉、肝脏、奶类、豆类、小米 海产品、加碘盐 芝麻、麦芽、糙米、标准粉、蘑菇、大蒜
“药补”与“食补”两种补充人体营养 元素的途径,你更赞成哪种?为什么?
【思考】
1.人体中所含元素都是对人体有益的吗?
答:不都答:如汞(Hg),铅(Pb),镉(Cd),铍(Be)等.
世界 上已 知元 素 (100 多种)
人体 中所 含元 素 (50 以无机 多种) 盐形式 存在的
以水、糖类、油脂、蛋白质、维生 素形式存在的: O、C、H、N(人 体中含量前四位的元素,共占人体 质量的96%) 常量元素(含量>0.01%): 钙、磷、钾、硫、钠、氯、镁 (共占人体质量的3.95%)
缺铁会引起贫血
《元素》课件

1.地壳中含量最多的元素是氧,其次 .地壳中含量最多的元素是氧, 是硅。 是硅。 2.地壳中含量最多的金属元素是铝, .地壳中含量最多的金属元素是铝, 其次是铁。 其次是铁。
地壳中含量居前五位的元素是氧、 地壳中含量居前五位的元素是氧、硅、 铝、铁、钙。
生物细胞中的元素
元 素 氧 碳 质量 分数 /% 65 元 质量分 素 数/% 氮 钙 3 元 素 钾 硫 质量 分数 /% 0.35 元 素 镁 质量 分数 /% 0.05
思 考
元素概念中的“一类原子”是什么意思? 元素概念中的“一类原子”是什么意思? 例如:作为相对原子质量标准的碳原子 例如: 指的是含有6个质子和6个中子的碳原子, 指的是含有6个质子和6个中子的碳原子, 叫做碳-12。除这种碳原子外, 叫做碳-12。除这种碳原子外,还有质子 数为6而中子数不同的碳原子, 数为6而中子数不同的碳原子,所以元素 概念中的一类原子指的是核电荷数相同 而核内中子数并不一定相同的一类原子。 而核内中子数并不一定相同同核电荷数( 联系 质子数) 质子数)的一类原子的 化学变化中的最小粒子 总称 着眼于种类,不表示个 着眼于种类, 既表示种类,又讲个数, 既表示种类,又讲个数, 区别 数,没有数量多少的含 有数量多少的含义 义 应用于描述物质的宏观 应用于描述物质的微观 组成,例如可以说, 组成,例如可以说, 结构。例如, 结构。例如,“一个 “水里含有氢元素和氧 水分子是由两个氢原 元素” 元素”或“水由氢元素 子和一个氧原子构成 和氧元素组成的” 和氧元素组成的”,但 但不能说“ 的”,但不能说“一 不能说“水是由二个氢 不能说“ 个水分子是由氢元素 元素和一个氧元素所组 和氧元素组成的” 和氧元素组成的” 成的” 成的”
课题2 元素

3、物质是由元素组成的(P73)
物质的种类非常多,已知的就有3 000多万 种。但是组成这些物质的元素并不多。到目 前为止,已经发现的元素只有一百余种。
4、元素分类(P76)
请大家尝试从元素名称偏旁特点给元素分 类
金属元素 “钅”字旁,(汞除外,俗称“水银”)
元 素
固态的 有“石” 非金属元素 液态的 旁 有“氵” 气态的 旁 有“气” 头 稀有气体元素 有“气”字 头
氮
氧、氢、氯、钠
生物细胞中含量前三位的元素: 氧、碳、氢
(…钙)
注意以下问法 含量最多的非金属元素
含量最多的金属元素
使用统一的符号!!
外国人可能 不认识汉字
历史上,道尔顿曾用图形加字母的方式作为元素符号, 如图所示。但由于后来发现的元素越来越多,符号设 计越来越复杂,不便于记忆和书写,故未能被广泛采 用。
二、元素符号
1.元素符号采用的是
拉丁文的第一个字母 。
一大二小! 2.书写原则:
第一个字母要大写,第二个字母要小写
O
氧 Fe
C
碳 Cu
H
氢 Al
N
氮 Mg
S
硫 Hg
铁
铜
铝பைடு நூலகம்
镁
汞
注意:
1、Co和CO
2、Ca和Cu
3、 Ag和Hg
3.元素符号的意义 一个氢原子
氢元素
H
表示一种元素 (宏观含义), 意义: 表示该元素的一个原子
5O 5个氧原子:
氮元素 : N
2个铜原子: 2Cu 3个磷原子:3P
超级市场里有成百上千种商品,为了便于顾客 选购,必须分门别类、有序地摆放。
元素周期表外框图
课题2《元素》(第一课时) 教学设计

课题2《元素》(第一课时)设计一、课题内容:本教学设计为人教版新课改教材(上册)第四单元,课题二《元素》。
二、教材分析主要内容包括元素、元素符号和元素周期表三部分。
其中对元素这一概念的形成,元素的表示方法,元素的规律性认识作为教学的主线一直贯穿在教材之中。
本课题教学担负着帮助学生把宏观和微观分析联系起来,建立元素概念的重要衔接作用。
1.重点:元素概念的初步形成及理解。
2.难点:原子与元素的区别和联系。
3.关键:如何理解元素概念的形成三、学情分析:通过前三个单元的学习,学生对于常见物质的了解已经有了一定的基础,又通过前一课题建立了物质微观构成的初步知识,特别是对于原子的概念有了较为深刻的理解。
元素的概念比较抽象但并不晦涩。
纵览教材已有四次共六段文字涉及过这一名词,学生已经有了多次感知,在日常生活中“元素”这一用语也时常出现。
但要完成从微观到宏观,理解好“同一类原子的总称”这一定义仍是教学中的难点。
学生对于“元素”概念在生活、生产中的应用的意识还没有形成,本节课地壳、生物体中元素含量的了解可以使他们更好的感知元素的存在,理解消化这一概念。
四、教学目标1、知识与技能:了解元素的概念,将对物质的宏观组成与微观结构的认识统一起来。
2、过程与方法:通过微观想象、分析、讨论、对比,认识到化学反应中分子可以发生变化而元素不发生变化。
3、情感、态度与价值观:进一步建立科学的物质观、增进对物质的宏观组成与微观结构的认识。
培养学生善于合作、勤于思考、勇于实践的科学精神。
五、教学过程六、课堂小结本节课我们主要学习了元素的概念,是重点也是难点,理解了元素是物质的宏观组成,以及元素在自然界中的含量分布,除此之外,还学习了物质与元素、分子、原子、离子之间的关系,望同学们课后多复习并练题加以巩固。
七、作业布置。
初中化学教学课例《第四单元课题2元素第一课时》教学设计及总结反思

课例研究综
通过《元素》教学的ቤተ መጻሕፍቲ ባይዱ化策略研究,结合其他相关
述
课例,逐步形成相对稳定的学习发展理论为指导。
2、培养学生的抽象思维等。
3、提高学生的学习兴趣。
学生学习能
学生对元素的概念在生产生活中的运用的意识还
力分析 没有形成,这是学生初学化学是的普遍存在的问题。
1、通过生活中的“缺铁——贫血病——吃钢筋”
教学策略选 能否治病。
择与设计
2、依托导学案中的自主学习材料。
3、通过分子、原子模型组织学生讨论。
引言与情景——思考与探究——板书——导学案 教学过程
初中化学教学课例《第四单元课题 2 元素第一课时》教学设 计及总结反思
学科
初中化学
教学课例名
《第四单元课题 2 元素第一课时》
称
主演内容包括:元素符号、元素周期表,其中对元
教材分析 素概念的形成、元素的表示方法、元素的规律性认识作
为主线一直贯穿在教材之中。
1、使学生初步掌握元素周期表的机构。
教学目标
元素(1)

③每一纵列,从上到下电子层数依次增 加,最外层电子数相同。
氦(He)
锂(Li)
铍(Be)
硼(B)
碳(C)
氮(N)
氧(O)
氟(F)
氖(Ne )
钠(Na)
镁(Mg) 铝(Al) 硅(Si)
3,不同种元素最本质的区别是( A)
A,质子数不同 B,中子数不同 D,中子数与核外电子数不同
C,相对原子量不同
4,地壳中含量最多的金属元素是( Al )
A、硅
B,铁
C,铝
D,钙
5,钠元素与钾元素本质区别是( A ) A,原子核内质子数不同;B,原子核内中子数不同; C,原 子核外电子数不同; D,相对原子质量不同; 6,某药品说明书中标明,本药品每片含碘15mg、钙30mg、镁 6.5mg、铜3mg等,这里所标的各种成分是指( B ) A,分子 B,原子 B,元素 D,单质
3,元素符号表示什么意义 表示一种元素
表示这种元素的 一个原子
由原子构成的物质, 还表示一种物质
注意:元素符号前面有数字,只能表示“几个原子”, 不能表示元素。也就是只有微观意义,没有宏观意义。
氢 元 素
如:
H
铁元素
Fe
铁单质
一个铁原子
4,元素的分类
根据中文名称造字的规律,从它们的 偏旁就可以知道它属于哪一类元素:
Fe Cu Zn Ag Ba Pt Au Hg I
稀有气体元素
氦
He
氖
Ne
氩
Ar
氪
Kr
氙
初中九年级化学上册:《元素》(第一课时)教学设计

《元素》(第一课时)教学设计一、教学目标1、知识目标:①了解元素的概念,统一对物质的宏观组成与微观结构的认识②元素与原子的联系与区别2、过程与方法:①通过问题讨论和例子进一步理解元素的概念②通过微观想像分析、讨论、对比,认识到化学反应中分子可以发生变化而元素不发生变化。
③通过同学之间相互合作,查阅资料,了解地壳、生物细胞和一些食品中元素的含量3、情感态度与价值观①进一步建立科学的物质观,增进对物质的宏观组成与微观结构的认识。
②发展善于合作,勤于思考,勇于实践的科学精神。
二、教学重点1、元素的概念;2、元素与原子的比较三、教学难点:元素的概念理解四、教学过程:1、导入新课(故事导入——牛尝出来的元素)1618年,英国伦敦附近有个村庄叫艾普松,当地人们以牧牛为主,有个农民想利当地的泉水供他饲养的牛饮用,于是便开了一条小沟引水。
但是,奇怪的是,没有一条牛愿意光顾他的小沟。
他感到很纳闷,自己一尝才知道,原来那泉水是苦的,后来被一名医生发现这泉水中含有一种固体物质,叫苦盐或艾普松盐。
最后,人们发现在海水或其他泉水中也含有这种苦盐,于是就发现这苦盐是含镁的硫酸盐,这样就发现了镁元素,由于苦盐的发现,离不开牛的贡献,因此,人们说镁是牛尝出来的元素,那么什么是元素?2、指导学生了解元素的概念①列举几种含氧元素(02、H20、C02、S02、H20)和几种含碳元素的物质(C、CO、C02、CaC03),并分别列出各种物质中氧原子和碳原子中的质子数,后质疑各种物质中氧原子和碳原子都有什么特点,从引出元素概念。
②分别举例出氧的同位和碳的同位素进一步引导学生理解元素的概念。
③活动与探究:请学生列举常见食品并指出它们的元素组成。
④元素和原子的比较。
让学生听下列文字后归纳出元素和原子的区别和联系:水是一种常见的物质,我们都知道它是由氢和氧元素组成,若从微观描述,水是由水分子构成,而水分子是由氢原子和氧原子构成,每个水分子含有一个氧原子和两个氢原子,由于水分子、氧分子和二氧化碳分子中氧原子的质子数都为8,所以,它们都属于氧元素,而不是氢元素。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
3.二氧化碳是由 和 元素组成的。
4.一个水分子是由
和 构成的。
5.地壳中含量最多的元素是 ____ , 含量最多的金属 元素是____。
元素的分类
金属元素 名称带“钅”的元素, 包括 汞、金 非金属元素 剩下的元素 稀有气体元素: 氦、氖、氩、氪、氙、氡
堂清题
1.决定元素种类的是
()
A 质子数 B 中子数 C 电子数 D 原子质量
2.据报道“目前世界上患有缺铁性贫血的人约有20
亿之多” 这里的“铁”是指
()
A 钢铁 B 铁元素 C 四氧化三铁 D三氧化二铁
分子在化学变化前后 发生了改变
(1)、地壳中含量最 多的元素是氧元素
(2)地壳中含量最多 的金属元素是铝元素
(3)地壳中含量前4位 的元素是 氧 、
硅 、铝 、 铁 。
元素在其它自然界中的分布
1、大气中含量最多的元素是 氮元素 2、海水中含量最多的元素是 氧元素
3、生物体内含量最多的元素是 氧元素 , 其次是 碳元素 和 氢元素
二氧化硫中含有硫和氧两种元素。 (2)一个水分子是由一个氧元素和两个氢元素构成。
一个水分子是由一个氧原子和两个氢原子构成。
4.地壳中含量最多的元素是
(A )
A.氧 B.硅 C.铝 D.铁
点拨
一氧化碳和二氧化碳都含有碳元素,一氧化碳 分子和二氧化碳分子都含有碳原子,这些碳原 子的原子核内都含有6个质子,但中子数可能不 同。
检测题
1.元素之间的根本区别是 A.中子数不同 B.质子数不同
( B)
ቤተ መጻሕፍቲ ባይዱC.电子数不同 D.相对原子质量不同
2 .用“元素”、“原子”填空:
二氧化碳是由碳元素 和氧 元素组成的,科学实验证明:
在1个二氧化碳分子中含有1个碳原子和2个氧原子 。
3.下列说法有没有错误?把错误的说法加以改正。
(1)二氧化硫中含有硫和氧两个元素。
第三单元 物质构成的奥秘
学习目标
1. 了解元素的概念,将对物质的宏观组成与 微观结构的认识统一起来。 2.形成“化学变化过程中元素不变”的观点。 3.知道元素的简单分类(金属元素、非金属元 素、稀有气体元素)。 4.认识氢、碳、氧、氮等与人类关系密切的常 见元素。
自学指导 请同学们细读59-60页的内容,注意: 1.什么叫元素?元素和原子有什么区别? 2.地壳中含量最多的元素、金属元素分 别是什么? 3.在化学反应中,分子是否发生了变化?元 素是否发生了变化?元素和物质、分子和原 子之间有何关系? 5分钟后比一比看谁能利用上述知识解决 相关问题。
对元素概念的理解
质子
中子
电6子个质子,6个中子,6
6个质子,8个中子,6 个电子
个电子
我也是碳原子
它们总称为碳元素
我是碳原子
我也是碳原子
6个质子,7个中子,6
个电子
元素和原子的关系
物质 组 成
元素 宏观概念
只讲种类
不讲个数
构成
分子
构成
构成 破裂
具有相同核电荷数 的一类原子总称
微观概念
原子 既讲种类 又讲个数
关于物质组成或分子构成的几种说法:
1. 物质是由元素组成的 2. 分子是由原子构成的 3. 一个分子是由若干原子构成的
水由什么组成?而水分子由什么构成?
组 水由氢元素和氧元素组成
成 物质由元素来组成
构 成
一个水分子由一个氧原子和两个 氢原子构成
分子由原子来构成
元素种类在化学变 化前后不变
原子在化学变化前后 不变
