体外诊断试剂干扰因素及其消除方法
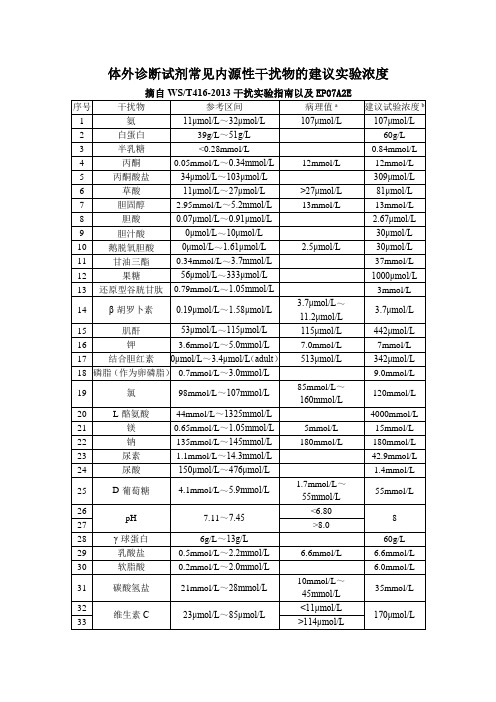
体外诊断试剂常见内源性干扰物的建议实验浓度摘自WST416-2013干扰实验指南以及EP07A2E
39
硬脂酸
0.1mmol/L
-
0.4mmol/L
40
油酸
<0.4mmol/L
-
1.4mmol/L
41
游离甘油
0.032mmol/L~0.232mmol/L
-
0.696mmol/L
42
总蛋白
60g/L~80g/L
<60g/L
120g/L
43
>90g/L
44
总钙
1.90mmol/L~2.55mmol/L
8
胆酸
0.07μmol/L~0.91μmol/L
-
2.67μmol/L
9
胆汁酸
0μmol/L~10μmol/L
-
30μmol/L
10
鹅脱氧胆酸
0μmol/L~1.61μmol/L
2.5μmol/L
30μmol/L
11
甘油三酯
0.34mmol/L~3.7mmol/L
-
37mmol/L
12
果糖
56μmol/L~333μmol/L
4
丙酮
0.05mmol/L~0.34mmmol/L
5
丙酮酸盐
34μmol/L~103μmol/L
-
309μmol/L
6
草酸
11μmol/L~27μmol/L
>27μmol/L
81μmol/L
7
胆固醇
2.95mmol/L~5.2mmol/L
13mmol/L
13mmol/L
120mmol/L
20
L-酪氨酸
44mmol/L~1325mmol/L
ELISA检测的干扰因素与方法

ELISA检测的干扰因素与方法ELISA应用最广,但这种固相测定技术非完美无缺,把握实验过程中每一个可能出现差错的关键性问题,采取相应的举措,才有可能使实验性误(漏)诊减少到最低限度。
1. 表面效应首先必须明确指出的是,:“固相”ELISA与传统的“液相”血清学试验的最大.最本质的区别是有一个预先固相抗原或抗体到载体表面的步骤,以及抗原与抗体结合反应由液态环境移到了固相载体表面进行。
蛋白质分子在吸附过程中,为了克服与固相载体之间的排斥力,需要重新分布其表面的功能性基因,使疏水性基因充分暴露,然后,局部接触区域的偶极分子脱氢,再通过范德瓦尔斯力吸引而固相到载体表面。
表面效应可直接影响抗原,抗体的构象和功能。
此外,表面效应亦影响抗原和抗体结合反应的动力学过程。
(1)固相导致抗原的变化为了测定抗体水平,需预先将抗原固相(包被)到极性和水性的聚苯乙烯(PS)或聚氯乙烯(PVC)酶标板上。
用直接物理吸附方法固相蛋白抗原及DNA等,导致的变化是多方面的,可引起分子构象和抗原性发生改变。
酶活性测定时可消失。
牛血清白蛋白固相之后,其抗原价可由5价降为1价。
此外,发现被动吸附方法固相铁蛋白,呈团串状,不均一的随机分布,这种影响质控的情况具有普遍性。
最后,大多数小分子半抗原不易直接吸附到载体表面。
解决这一难题的方法,一般是采用在小分子抗原上,先偶联上葡聚糖,明胶等手臂后再进行固相包被。
对于有多重表达抗原决定簇的大分子抗原,用抗体桥式包被法可避免表面效应的影响。
将蛋白抗原吸附于胶体AI(OH)3后再固相也可以避免蛋白变性。
用Y射线辐照(400GY)PS板,不但可增加蛋白抗原吸附能力,而且还有降低抗体测定本底的作用。
(2)固相对抗体的影响直接吸附固相抗体(Igs)分子,除了呈团串状,不均分布和易解吸等一般不利因素之外,Igs分子摊开在载体表面,不但构象发生改变,而且影响抗体的活性,如IgG的结合价减少,可由2价变为1价,甚至完全失活。
生物学实验中干扰性因素分析及其排除

生物学实验中干扰性因素分析及其排除无论是实验设计,还是实验实施和实验分析,分析和排除实验中干扰性因素是科学实验中的一项基础性工作,也是实验教学中要加以重视的一项重要实验技能。
本文从学生实验设计方案中出现的错误案例说起,以中学生物学典型试题为例,探讨和总结实验中干扰性因素的一般来源及其常见排除方法。
一、从学生作业中的错误说起试题1:血糖含量的相对恒定是保证动物机体进行正常生理活动的重要条件,一旦机体内血糖含量过低,细胞的正常活动则受到影响,动物会出现惊厥、昏迷等现象。
为了验证“胰岛素具有降低血糖的生理作用”,请以小白鼠为实验对象设计实验步骤,预测实验应出现的结果,并写出实验结论。
(一)实验材料和用具:小白鼠4只;鼠笼2个;胰岛素溶液;50%葡萄糖溶液;生理盐水;注射器若干个。
(二)实验步骤:(实验提示:采用腹腔注射给药,给药剂量不作实验设计要求)第一步:将4只小白鼠分为实验和对照两组,每组2只。
……实验结论:学生作业答案:第二步:在实验组小鼠腹腔下注射适量的胰岛素,在对照组小鼠腹腔下注射等量的生理盐水,置于30℃~37℃相同环境中;观察并记录小鼠活动状况。
第三步:给两组小鼠均注射等量的葡萄糖溶液;观察并记录小鼠活动状况。
实验现象:实验组小鼠被注射胰岛素后出现惊厥、昏迷等现象,在注射葡萄糖溶液后恢复正常;而对照组小鼠被先后注射生理盐水、葡萄糖溶液后均正常。
实验结论:实验鼠出现惊厥、昏迷是因为血糖降低引起的,血糖降低是胰岛素作用的结果。
试题2:利用下列装置(见图1),设计一个验证呼吸作用产生CO2的装置图。
错误分析:通过以上两道试题的学生答案,我们不难看出,由于实验中的干扰性因素没有排除,因此按照学生的思考和设计,是不能达到理想且科学的实验效果的。
试题1中,由于在注射胰岛素之前,没有对“两组小白鼠饥饿处理18~24h”,因此小白鼠肝脏中贮存的肝糖元等因素会在一定程度上影响胰岛素作用的发挥,使实验的现象不明显或不发生;试题2中,学生没有考虑到“空气中含有CO2”,因此没有排除空气中CO2,实验的结果和结论都没有说服力,从而缺乏实验的科学性。
免疫学检测中的干扰因素

免疫检测技术- 标记物
免疫测定技术均是以标记物示踪作为基 础,同位素、荧光素、酶是经典的三大标记 免疫测定技术。这三大标记技术发展了各种 各样的免疫测定方法,如RIA、ELISA、荧光 免疫测定、免疫化学发光测定等,目前应用 这三大标记技术的检测试剂盒在临床广为应 用。近年来,作为免疫测定发展方向的非同 位素标记技术以其敏感、安全等倍受关注。
免疫学检测方法中的 干扰因素和对策
第二军医大学附属长海医院实验诊断科
沈 茜
随着基础免疫学研究的深入和现代免 疫学理论的建立,使大量免疫学检测技术 被不断地创新、发明;在临床疾病诊治的 应用中也不断地推陈出新。目前应用免疫 学原理检测的检验项目占到三级综合医院 检验科全部检验项目的1/4,医疗收入约 占1/3。这就要求检验人员不断掌握最新 的临床免疫学知识和各种新的检验方法, 了解检验项目的基本原理。
干扰因素和对策- 类风湿因子
收集10份RF31~>1000IU/L的患者血清, 在美国和欧洲66各临床实验室进行74个项目 的免疫竞争法或免疫夹心法检测,仪器和试 剂均配套。3445个结果中8.7%为假阳性。错 误高值结果中的21%(所有结果的1.8%)引 起了临床的错误诊断,在使用RF吸附剂后再 检测,错误结果得到纠正。39%的假阳性结 果也可在使用RF吸附剂后降低。
干扰因素和对策- 外源性物质
冻存后融解的标本,蛋白质局部浓缩, 分布不均,应充分混合后再测定,但混匀时 应轻柔,不可强烈振荡。标本的反复冻融所 产生的机械剪切力将对标本中的蛋白等分子 产生破坏作用,从而引起假阴性结果。
操作流程不当-造成结果的改变
我们对HBV血清标志物五项指标仅抗HBc总抗体单阳性的血清实行了严格的复检 措施,发现初、复检结果的符合率<50%。 偏差如此之大是无法用实验人员操作不当解 释的。抗-HBc总抗体采用竞争抑制ELISA法 检测, 日常工作中无论标本多少,必然是先 加完血清标本后再加抗-HBc-HRP。这样, 血清中的抗-HBc与抗-HBc-HRP存在着明显 的‚不公平竞争‛。
1体外诊断试剂研发包被标记检测等详细步骤注意点影响因素

1体外诊断试剂研发包被标记检测等详细步骤注意点影响因素一、抗体包被详细步骤:用包被缓冲液将抗体稀释至蛋白质含量为1~10μg/mL。
在每个聚苯乙烯板的反应孔中加0.1mL,4℃过夜。
次日,平衡至室温弃去孔内溶液,用洗涤缓冲液洗3次,每次1分钟。
加入封阻液200uL,37℃温浴2-3h,用洗涤缓冲液洗3次,每次1分钟。
加入200uL含5%蔗糖的PBS缓冲液,37℃温浴1h,甩干后37℃烘干1h后自封袋封存(含干燥剂)。
包被缓冲液:10mM PBS;pH7.420mM Tris-HCL;pH7.2-8.050mM碳酸盐缓冲液;pH9.6洗涤缓冲液:10mM PBST(含有0.05%吐温)pH7.4封阻液:10mM PBS缓冲液ph7.4,含1%BSA二、过碘酸钠氧化法标记步骤:称0.5mg HRP,溶于0.25ml纯化水,入20uL新配的0.1M NaIO4,温避光反应20min(15-30min)。
1mM醋酸钠缓冲液透析,4度过夜,加入50ul0.16M乙二醇,混匀静置30min,加入5ul0.2M CBS。
立即加入0.5mg抗体,室温避光轻混2-4h,加入10ul新配的4mg/ml NaBH4,4度避光2h。
对PBS透析过夜调浓度,甘油对半稀释,-20冻存。
三、具体操作步骤1.配制稀释液(PBS,pH7.2~7.4,含2%BSA);2.取1块预包被板,平衡至室温(大概时间20min);3.取CA125抗原一支(冻干品,500U/支0.5mL纯水复溶)复溶混匀;4.加入稀释液,配制浓度为12U/mL,50U/mL的抗原液作为校准品;5.将-20℃酶标抗体(冻存浓度为500ug/mL)室温快速溶解(可以用手温或37℃水浴溶解),加入稀释液中,酶使用浓度为1ug/mL;6.酶反应底物配置,完成后用锡箔纸避光,使用之前必须平衡至室温(至少20min)7.所有试剂使用前平衡至室温(大概20min,液体较多则平衡至30min)8.每个孔加样100ul(垂直悬空加入,切勿碰到孔壁)盖上封板膜37℃孵育1h,和90min,注意边缘效应,边缘数值一般较高;9.沿弧线甩干液体,移液枪小心加入300uL PBST(0.05%吐温)洗涤液,不要流出孔外,放置到微量振荡器振荡1min,重复洗涤四次。
体外诊断试剂稳定性研究的影响因素和评价要求

体外诊断试剂稳定性研究的影响因素和评价要求摘要:体外诊断试剂是指在疾病的预测、预防、诊断、治疗监测、预后观察和健康状态评价的过程中,用于人体样本体外检测的试剂、试剂盒、校准品、质控品等产品,可单独使用,也可与仪器、器具、设备或系统组合使用。
其中,用于血源筛查的体外诊断试剂和采用放射性核素标记的体外诊断试剂按照药品进行管理,其他体外诊断试剂按照医疗器械进行管理。
体外诊断试剂稳定性是指产品在生产企业规定的条件下储存,在规定的时间内保持其性能特性的能力,主要包括实时稳定性、运输稳定性、开瓶稳定性、冻融稳定性、机载稳定性、复溶稳定性(冻干产品)等。
稳定性作为评价体外诊断试剂保持产品性能的重要指标,对产品的研发、生产、运输、保存和使用等环节具有重要意义,通过稳定性研究可以评价和调整产品组方、工艺、包装材料等,确定产品的保存期限和开封后保存期限,明确产品的运输、储存和开封后的保存条件,并可在产品保存期限和储存条件等发生变更时,验证变更后的产品稳定性。
关键词:体外诊断试剂稳定性;影响因素;评价要求引言GB/T29791.1-2013明确定义了体外诊断试剂的稳定性:体外诊断医疗器械将性能特性保持在制造商规定的限度内的能力。
该标准规定了三种适用稳定性的情况:第一种情况涉及按照制造商规定的条件储存、运输和使用体外诊断试剂、校准器或调节器;二是按照制造商的指示从封闭容器中提取、配制、使用和储存的溶解干燥材料、工作液和材料;第三,这些是校准仪器或测量系统,其稳定性通常是在体外诊断试剂时测量的。
稳定性是保持产品作为体外诊断试剂的安全性和有效性的重要指标,也是指导产品生产、运输、保存和使用的重要指标。
1开展体外诊断试剂稳定性研究的目的体外诊断试剂可根据成分结构和反应原理分为不同类别,不同产品的成分比较复杂,许多体外诊断试剂本身就是生物制剂。
一些活性体外诊断试剂基质具有不同的化学不稳定性趋势,易发生水解、酶解和氧化等反应,影响试剂的质量和稳定性。
临床检验试剂间相互干扰类型、部分已知常用试剂间相互干扰、干扰排查和发现及干扰消除

临床检验试剂间相互干扰类型、部分已知常用试剂间相互干扰、干扰排查和发现及干扰消除试剂间相互干扰类型试剂中含有下一个检测所要测定的底物,或是含有的某种试剂成分与下一反应的底物有作用,直接干扰下一反应的测定结果。
另一种原因是该试剂所引导的反应对下一个项目的反应进程带来间接的干扰,因为在有试剂污染的情况下,下一个测试所测定的是前后两个项目反应的综合作用结果。
部分已知常用试剂间产生相互干扰1、pH值改变试剂中反应缓冲液之间因仪器携带污染而使下一反应的pH值改变,使下一反应达不到最佳状态。
如双缩脲法测血清总蛋白,若其他条件相同,反应在碱性(pH值8-9)条件时,蛋白肽键(—CONH)才都能与碱性铜溶液作用生成紫色反应,完全测出血清蛋白的总量。
若pH<8时,总蛋白测定结果偏低,直接影响球蛋白、白蛋白/球蛋白的结果。
酶活力测定在最适pH值时,反应最快,灵敏度最高,但是因为缓冲能力有限,可因携带污染使酶促反应出现无效值。
大多数酶反应pH值在6.0-7.5之间;ALP、γ-GT、LDH须在碱性条件下最适宜。
2、TG、T-CH、UA、MG试剂中含有胆酸盐,对循环酶法测定胆汁酸能产生严重干扰。
3、ALT(IFCC)、AST(IFCC)试剂中含有高活力LD成分,有可能会对LD的测定带来干扰。
4、CK(NAC-activated)、CK-MB(NAC-activated)试剂中含有Glu成分,其分析方法的原理中包含Glu的已糖激酶(HK)反应过程,因此可能对Glu测定带来干扰,尤其对Glu的HK法测定可能带来严重干扰。
5、Glu(HK)、CK(NAC-activated)、CK-MB(NAC-activated)、TG、HDL-C、LDL-C(直接法)等试剂中使用了镁盐,可能会对其后的Mg2+ 测定带来干扰[2];TP试剂中高浓度的Cu2+对Mg2+测定也会产生干扰。
6、ALT、AST、LDH、CK、CK-MB、UA、r-GT、TP,LDH等试剂由于试剂中含有K+,与K+的酶法测定有相同或相反的进程,对K+的酶法测定产生干扰。
体外诊断试剂干扰因素及其消除方法

体外诊断试剂干扰因素及其消除方法1、非特异性干扰1)疏水作用原理:反应环境中存在的疏水性的物质,如样本中的脂肪/细菌/细胞碎片……与Ag/Ab 或胶乳通过疏水作用结合,产生假阳。
处理方式:表面活性剂或亲水聚合物分解。
2)补体补体(complement, C)是存在于正常人和动物血清与组织液中的一组活化后具有酶活性的蛋白质。
原理:Ab的Fc段与C1q补体结合位点暴露,激活血清中的补体分子与包被或标记Ab 结合,产生假阳。
处理方式:通过EDTA(络合剂)处理样本。
3)类风湿因子类风湿因子(rheumatoid factor,RF)是针对IgG Fc片段上抗原表位的一类自抗体,一般为IgG和IgM。
原理:人血清中的类风湿因子(RF)与包被或标记Ab的Fc片段结合产生假阳。
处理方式:使用无Fc片段的Fab片段抗体动物IgG中和。
2、异噬性抗体异嗜性抗体是指能够结合动物抗体而干扰免疫分析的所有人源抗体。
包括:① 人抗鼠抗体(Human Anti-More Antibodles HAMA )②人抗山羊抗体(HAGA)③人抗兔抗体(HARA)异嗜性抗体从何而来a 动物接触(驯兽师、兽医)b 动物产品接触(烹饪)c 动物辅助治疗(胸腺细胞、羊细胞、胚胎细胞)d 食物(奶酪)e 注射疫苗f输血g自身免疫性疾病h母婴传递I心脏病变秘方药物异嗜性抗体干扰的原理3、什么是阻断剂阻断剂是一种可结合异嗜性抗体,从而有效防止异嗜性抗体介导的免疫分析干扰的生物制剂。
1)阻断剂类型a被动阻断剂:非特异性物质(鼠IgG等),结合异嗜性抗体的亲和力弱。
b主动阻断剂:能特异性结合人类异嗜性抗体,结合异嗜性抗体的亲和力强。
2)常见的阻断剂厂家阻断剂系列Roche MAK33系列Scan tibodies HBR系列/鼠IgGMillipore ChemiBlock 系列Biodesig n A66800H菲鹏HIER系列万孚鼠IgG4、怎样确认干扰1)同一样本采用不同检测方法,若结果不一致说明可能存在干扰物。
全自动生化分析仪常用试剂间的相互干扰和应对措施

不 断 的提 高 , 由于共 用吸样 针 、 但 试剂 针 、 拌 棒 以及 比色杯 , 搅 当生化 仪 长期 及 其前一个 项 目单独 复检 又恢 复 正常 , 是 由于 发生 试 剂问 交叉 污 染所 致 。 多 由于试 剂 中化 学 成分 非 常复 杂 , 各种 稳 定 剂 、 反应 物 质 、 冲体 系共 缓 使 用致其 清洗 能力 下降 、 比色杯老 化后 引起 吸 附 力增 加 、 生化 仪 内 污垢 的 积 但 是 , 聚 、 试顺 序安 排不 当 , 常规 清 洗不 能 有 效 消 除 交叉 污染 时 , 会 增 加 试 存 , 各品种 、 厂商 的 试剂 内含 物 均 不 同 , 测 且 就 且 各 因此 试 剂 间 的化 学 污染 往 往较 剂 间化学 污染 的可 能性 , 测定 结果不 准确 J 引起 。 难判 别 。 日常工 作 中往往 是仪 器评估 没 问 题 , 用户 使 用时存 有 污染 ; 而 质控 1 1 试 剂 针 污染 : . 目前 大多 数 全 自动生 化 分 析 仪 采 用 双 试剂 检测 样 品 和 Wet r sa g d法则 不起 作用 , 质控 往 往 在控 ; 染 具有 偶 然 性 , 不 是 每次 污 并 8 J 本 , 剂 R 、2的吸取 与吐 出 , 试 lR 一般分 别 只配有 一 套试 剂针 。 当试剂 针在 清 都 出现 _ 。这就导 致 了判别 此类 污染 的 困难 性 。事 实上各 个厂 家所 提供 的 洗不 完全 , 黏 附 力 增 加 时 , 留 试 剂 可 能 会 对 下 一 相 临 检 测 结 果 造 成 产 品说明 书常不 能够 全面 反 映试 剂 组 成 的情 况 , 或 残 而生 化 反应 的影 响 因素 又 影响。 是相 当复杂 的 。因此 , 过实 验 发 现试 剂 交 叉 污染 可 能 带来 的干 扰 显得 更 通 12 搅拌 棒 污染 : . 在试剂 与样 本混 合后 , 往需 要 搅 拌棒 加 以混 匀 , 往 而 加 重要 。具 体可 以 通 过 以下 几 个 试 验 来 排 查 和 发 现 试 剂 问 可 能 发 生 的 搅拌 绑若 清洗不 完全 , 黏附力 增加 时 , 留试 剂 可 能会 对 下 一相 临 检测 结 干扰 。 或 残 果造 成影 响 。 3 1 可 以在清 洗保养 完 全 自动 生化 分 析 仪后 , 者 在 日常 工 作 中 , . 或 以 13 比色杯 污染 : . 生化 分析 仪 的 比色 杯一 般 是 循 环 使 用 的 , 每个 比色 三管蒸馏 水作 标本 , 行 每 个 项 目单 独 测 定 和 连 续测 定 , 管 测定 重 复 三 进 每 杯检 测完 毕后 , 清洗 , 继续 下一 个 检 测项 目的检 测 。 当某 个 比色 杯 次 , 算 出结果 经统 计学 处理 有无统 计 学意义 , 进行 然后 计 分析 交叉污 染发 生的环 节 。 清洗 不完全 时 , 附在 比色杯上 的上一 个 项 目的残 留 试剂 , 能会 对 在这 个 吸 可 32 用 定标 液 做标本 , 于定 标 液 造 价 比较 高 , 以我 们 只采 用 一 管 . 由 所 比色 杯 中进 行 的下一个 项 目的检测 结果造 成 影响 。 重 复三次 所得 的结 果 , 三个 结果 做 比较 , 每个 结果 同定标 值 傲 比较 。做 出交 以上 3 可 能的污染 , 比色杯污 染 最为 严重 , 种 以 因此 比 色杯 最难 以清 洗 叉 污染 的结论 。 干净 , 在实 际工作 中难 以 判 断该 比色 杯 上 一 测 试 的项 目 ; 剂 针 吸 量 较 且 试 大 , 以清洗 干净 。 亦难 2 常 用试剂 间相 互干扰 的类型 . 试 剂 中含 有 下一个 检测所 要 测 定 的底 物 , 是 含 有 的某 种 试 剂 成 分 与 或 下一 反应 的底物 有作用 , 因而直 接干扰 下 一反 应 的测 定 结 果 ; 一 种原 因 是 另 该 试 剂所引 导 的反应对 下一 个 项 目的 反应 进 程 带 来 间 接 的 干扰 , 因为 在 有 试 剂 污染 的情 况 下 , 下一个 测 试所 测定 的是 前 后 两 个 项 目反 应 的综 合 作 用 结 果 。部分 已知 的常用 试剂 间可能 产生 的相互 干扰 如 下 : 2 1 p 改变 : 剂 中反 应缓 冲液 之 间 因仪 器 携带 污 染 而 使 下 一反 . H值 试 应的 p H值改变, 使下一反应达不到最佳状态。如双缩脲法测血清总蛋 白, 若其他条件相 同, 反应在碱性( H值 8~9 条件时 , p ) 蛋白肽键(一C N 才 O H) 都 能与 碱性铜 溶液作 用生 成紫 色反应 , 全测 出 血清蛋 白的 总量 。若 p < 完 H 8 时 , 蛋 白测定结 果偏 低 , 总 直接影 响球 蛋 白 、 白蛋 8/ 蛋 白的 结果 。酶 活力 球 测 定在 最适 p{ 时 , 最快 , 度最 高 , 是 因为 缓 冲能 力 有限 , 因 I值 反应 灵敏 但 可 携 带污 染使 酶促 反应 出 现无效 值 。大 多数 酶 反应 pt 在 6 0—75之 间 ; I值 . . A P 一G 、D L、 T L H须 在碱性 条件下 最适 宜 J 。 22 T T—C U . G、 H、 A试剂 中含 有 胆酸 盐 , 对循 环 酶 法 测 定 胆 汁 酸 能产 生 严重 干扰 [ 。 33 用 自制 混合 血清 做 标 本 , . 先将 混 合 血 清 做试 剂 无 交叉 污 染 的试 验, 方法: 单项输入、 连续性测定评估项 目, 混合标本 l 0管求 出平均值。而 后做交叉污染试验, 方法基本同3 1将 自制的混合血清代替蒸馏水。分析 ., 结 果时采 用方法 3 1和方 法 3 2同 时进行 。这样 统计 学 处 理 的结果 比较全 。 .
理化检验中常见干扰源和应对方法

理化检验中常见干扰源和应对方法发布时间:2023-03-03T02:13:08.246Z 来源:《中国医学人文》11月11期作者:李元[导读]理化检验中常见干扰源和应对方法李元(邛崃市疾病预防控制中心;四川成都611530)近年来,我国卫生检验方面逐渐以经验科学向理论科学方向发展,理化检验与物理和化学方面的知识联系得更加紧密。
在医学检验的工作中,同样对于物理化学方面的要求也随之日益增高,在具体的项目检测中,也越来越多地会采用先进仪器分析的方法,而仪器方法在实质上指的就是研究物理化学性质方法的快速手段。
比如常见的原子吸收仪、气相色谱仪、原子荧光仪、GC-MS、HC-MS、ICP-MS、自动生化仪等等仪器就是广泛应用在我们平时的生活饮用水、空气、土壤、化妆品、食品、血液、细胞液以及组织液等样品理化检验中。
在日常的理化检验工作中,如果我们稍有不慎,便会造成各种干扰源对检验结果的影响,而在临床检验工作中同样会遇到相似或特异的干扰源影响其检测结果,对患者的后续治疗方案制定也会有一定的影响,因而临床上也会采用相应的措施或是应对方法来避免检测结果受到影响。
现本文就以理化检验中常见的干扰源和相应的应对方法进行拓展性讨论,具体如下。
一、什么是理化检验所谓理化检验其实就是一种质量检验的手段,其主要就是借助样品的物理和化学性质进行分析的技术手段,并使用相应的某类测量工具或是仪器设备如比色仪、PH仪、显微镜等对所采集的样本进行相应检验的方法。
而目前理化检验实行的条件大多必须在实验室的环境条件下,且主要是用来检验样品的成分、结构、物理性质以及化学性质和安全性、卫生性、环境污染性和破坏性的相关工作,其与常规的检验相比较而言,理化检验的结果可以采用定性和数据定量来进行表示,结果也相对的较为准确和客观。
理化检验不仅对仪器设备和检验条件有一定的要求,对于检测人员的知识丰富程度和特定的操作技术也有特定的要求,有时检验者的工作经验也很重要。
免疫检测中的干扰因素及排除方法

二、内源性干扰因素及对策——生物素
生物素: 生物素又被称为维生素B7或维生素H,是一种水溶性B族维生素。生物素亲和素系统是发展起来的一种新型生物反应放大系统。现被广泛应用于医 学领域,在体外诊断的实际应用中具有很大的优越性,生物素可以和几乎 所有生物大分子结合,亲和力高,结合稳定,灵敏度高,具有多级放大作 用。 生物素干扰存在于使用生物素-亲和素系统或生物素-抗生物素系统的检测中, 与仪器厂家、仪器型号、发光底物无关,同一厂家不同项目包被方式也可 能不同。生物素对化学发光干扰需要一定的浓度,不同项目/试剂抗生素干 扰的能力不同。生物素干扰可能产生假阳性,也可能产生假阴性。一般来 说,夹心法产生假阴性,竞争法产生假阳性。
三、外源性干扰因素及对策——溶血
溶血: 要注意避免严重溶血,血红蛋白中含有血红素基团,其有类似过氧化物的 活性,因此,在以HRP为标记酶的ELISA测定中,如血清标本中血红蛋白 浓度高,则其就很容易在温育过程中吸附于固相,从而与后面加入的HRP 底物反应显色。另外,机械强力震荡、突然反复冻融、低渗溶液、过酸、 过碱,以及酒精、乙醚、皂碱、胆碱盐等均可以起溶血。
临床免疫检测中的干 扰因素及对策
目录
一、概述 二、内源性干扰因素及对策 三、外源性干扰因素及对策 四、总结
一、概述
伴随着免疫检验技术的飞速发展,免疫学检验发展已取 得了从定性到定量;从常量分析到微量、超微量分析;从手 工检测到全自动化检测;从单标本检测到高通量检测等重大 的进步。应用范围遍及医学和其他生物学检验的各个领域。 经典的免疫检验技术(如凝集试验、沉淀反应等)由于仅能 定性或简单定量,灵敏度低,耗时费力,不能自动化。逐渐 被高敏感度和高特异性的现代免疫学检验方法 (如RIA、 ELISA、荧光免疫测定、免疫化学发光测定等)所取代,而这 些又主要是源于抗原抗体特异性结合及各种不同标记物的使 用,加上免疫检测系统也实现自动化、集成化和微型化,也 将有助于实验操作的规范化和标准化,提高检验结果的准确 性和重复性。
【精品】体外诊断试剂干扰实验评估指南

体外诊断试剂干扰评估指南-EP7A郑金来20110105目录 前言干扰物及其机理干扰的标准干扰评估干扰筛选及其效果评价用病人标本评价干扰效果 临床实验室验证总结前言NCCLS:国家临床化学实验室标准化委员会。
NCCLS是一家国际性的、各学科间的、非盈利性的标准制定和教育组织,推动在医疗团体间发展和使用自愿性一致的标准和指南。
NCCLS已经得到了全球广泛的认可NCCLS基于的原理为一致性是一个有效并经济的手段来提高患者测定和医疗服务。
,EMAIL:exoffice@08年11月NCCLS已经更名为CLSI前言NCCLS文件以标准、指南或委员会报告的形式发表 标准:通过一致性程序发展出来的一项文件,以一种未经修饰的形式、清楚地确定材料、方法学或使用惯例的特定以及必须的要求指南:根据一致性程序发展出来的一项文件,描述某个一般性操作惯例、程序或材料的标准,供用户自愿使用。
使用指南时,可由用户根据其特定需要草拟或进行修改报告:还没有提交进行一致性回顾的一种文件,由董事会发布。
前言NCCLS的标准和指南代表了有关良好医疗实践的一致性意见。
反映了实质上受到影响的有资质的以及有兴趣的各方根据NCCLS建立的一致性程序得到的实质协定。
即使符合自愿性一致文件,但用户仍有自认适合法规的要求。
用户的意见对于一致性程序时必要的,任何人都可以向委员会提出自己的意见。
前言干扰物质是体外诊断试剂使用过程中造成测量误差的一个主要原因,针对体外诊断试剂进行的干扰实验是指通过实验查找出对体外诊断试剂测量结果产生影响的物质的过程。
干扰实验评估资料是评价拟上市产品有效性的重要依据,也是产品注册所需的重要申报资料之一CLSI EP-7A的范围生产商:通过科学的实验设计、指定干扰物浓度和类型以及合适的结果分析,帮助生产商或实验程序的开发者明确程序对干扰物的易感性。
用户:通过系统的调查策略、指定数据收集和分析要求以及促进生产商和用户更好的合作,帮助临床实验室调查因干扰引起的有差异的结果,以便最终能够坚定、发现并评估新的干扰物。
体外诊断试剂干扰试验研究资料-分析性能评估

体外诊断试剂干扰物质研究资料1干扰试验评估方案1.1概述血脂是指体内脂肪在血液中脂质的总称,包括总胆固醇、甘油三酯、低密度脂蛋白(极低密度脂蛋白)、高密度脂蛋白等。
为了检验高血脂样本对本试剂的影响,本公司采用两个不同浓度的样本,然后加入不同浓度的甘油三脂,以评估高血脂样品对检测结果的影响;引起黄疸的物质叫胆红素,呈橙黄色,当待检样本中的胆红素浓度超出一定的值时,它会影响样本测定效果,从而影响检测的性能。
为了检验黄疸样本对本试剂的影响,本公司采用两个不同浓度的样本,然后加入不同浓度的胆红素,以评估黄疸样品对检测结果的影响。
另参考文献报道,WBC(白细胞计数)和PLT(血小板计数)可能对血红蛋白检测结果产生影响,对WBC(4×109/L~20×109/L)、PLT(100×109/L~700×109/L)对对血红蛋白检测结果的干扰性进行了研究。
为考察含胆红素、甘油三酯、WBC(白细胞计数)、PLT(血小板计数)样本对检测结果产生影响,对样本中的干扰物质进行分析,确定干扰物的浓度。
本次实验考察的干扰物浓度如下:胆红素:25μmol/L、50μmol/L、75μmol/L、100μmol/L;甘油三酯:1.0mmol/L、1.5mmol/L、2.0mmol/L、3.0mmol/L;WBC(白细胞计数):4×109/L、10×109/L、15×109/L、20×109/L;PLT(血小板计数):100×109/L、250×109/L、500×109/L、700×109/L。
同时,为考察同一干扰物质在不同浓度下对不同抗凝剂抗凝标本的检测结果是否存在差异,对相关结果按下表整理后(示例)进行方差分析,不同标本类型的检测结果应不存在显著差异。
批号2181016干扰物质甘油三酯被测物浓度45g/L序号干扰浓度mmol/L标本抗凝剂类型EDTA-Na EDTA-K枸橼酸钠肝素钠1044.5443.6644.5944.79 2145.2646.1944.6245.08 3 1.543.9444.0544.0143.35 4244.3144.9645.6244.995344.6443.3145.0646.38本试验所用的样本为全血(EDTA-Na抗凝、EDTA-K抗凝、枸橼酸钠抗凝、肝素钠抗凝)。
免疫学检测方法中的干扰因素和对策

干扰因素和对策- 补体
免疫检测系统中捕获抗体在向固相包被 中和标记抗体的标记过程中,抗体分子发生 变构,其Fc段的补体C1q分子结合位点被暴 露出来,使C1q 可以将二者连接起来,从而 造成假阳性。一些公司为了增加检测的敏感 性,使用链霉亲和素包被固相,将捕获抗体 用亲和素标记,此过程也可引起捕获抗体的 构象发生改变 ,造成假阳性或假性升高。
Clinical Chemistry 2002;48(11):2008~2016
RF的干扰-对策
捕获抗体用F(ab`)2替代完整的IgG
标本用连有热变性(63℃,10 min)IgG的
固相吸附剂(Euroimmune公司)处理(将 热变性IgG加入到标本稀释液或血清中同样 有效),4℃过夜离心后在检测;
检测抗原时,可以用终浓度0.1mol/L 2-巯 基乙醇(2- ME)等加入到标本稀释液或标本 中,使RF(IgM型)降解。
干扰因素和对策- 嗜异性抗体
嗜异性抗体通常是指与其他种类动物的 免疫球蛋白产生反应的人类抗体,具有广泛 的种特异性。免疫检测系统中大量使用单克 隆抗体,嗜异性抗体可与啮齿类动物IgG的 Fc段结合。这样嗜异性抗体既可与检测系 统中的捕获抗体结合、又可和标记抗体结合, 造成检测结果假阳性或假性升高。嗜异性抗 体干扰的程度、频率与患者的疾病状态、年 龄、性别等无关。
干扰因素和对策- 外源性物质
冻存后融解的标本,蛋白质局部浓缩, 分布不均,应充分混合后再测定,但混匀时 应轻柔,不可强烈振荡。标本的反复冻融所 产生的机械剪切力将对标本中的蛋白等分子 产生破坏作用,从而引起假阴性结果。
操作流程不当-造成结果的改变
探讨临床体外诊断试剂抗干扰能力验证方案的建立

探讨临床体外诊断试剂抗干扰能力验证方案的建立摘要】目的:以四川新健康成生物股份有限公司的同型半胱氨酸测定试剂盒(酶循环法)为例探讨临床体外诊断试剂抗干扰能力验证方案的建立,以确保临床试剂选择的正确性。
方法:参照NCCLS EP7-A2文件的评价方法,选择同型半胱氨酸测定结果正常的临床样本和异常的临床样本各一份作为基准样本,先将其分成3N+1份,每N份分别加入不同浓度的同种干扰物质,另1份作为每个干扰物质的基准对照组,即加入的干扰物质浓度为0,重复测定三次各样本,计算每个浓度干扰组测定均值与基准组测定均值相对偏差,对结果进行分析。
结果:当样本中血红蛋白浓度为1.5g/L时,|相对偏差|≤12.80%;当样本中胆红素浓度为342μmol/L时,|相对偏差|≤12.80%;当样本中甘油三酯浓度为11.3mmol/L时,|相对偏差|≤14.40%。
结论:该公司的同型半胱氨酸测定试剂盒(酶循环法)的抗干扰能力为满足临床抗干扰能力要求。
临床使用机构应该建立正确的体外诊断试剂抗干扰能力验证方案,确保使用产品符合质量要求,保障医院和患者的合法利益。
【关键词】抗干扰能力;相对偏差;体外诊断试剂【中图分类号】R44 【文献标识码】A 【文章编号】1007-8231(2017)03-0086-03To explore the pian’ establi shment of the anti interference ability verification of the clinical in vitro diagnostic reagentsLi Jingjing, Ding Xianping.College of life sciences scihuan university , Sichuan, 610064, China【Abstract】Objective Taking the Sichuan Xincheng Biologica l Co., LTD’ Homocysteine assay kit by enzyme cycle method for example to explore the pian’ establishment of the anti interference ability verification of the clinical in vitro diagnostic reagents, so as to ensure the correctness of the selection.Method Referencing the evaluation method of the EP7-A2 NCCLS document, choosing the normal clinical samples and abnormal clinical samples each one of the Homocysteine testing results for the reference sample and which were divided into3N+1 parts,different concentrations of the same interfering substances were added to each N and nothing for the other one, then testing these samples three times perserving, calculated relative deviation between the interference group means and reference group mean, analysis of the results. Results When the hemoglobin concentration was 1.5g/L, the absolute value of relative deviation was not exceeding 12.80%. When the bilirubin concentration was 342μmol/L, the absolute value of relative deviation was not exceeding 12.80%. When the triglyceride concentration was 11.3mmol/L, the absolute value of relative deviation was not exceeding14.40%.Conclusion The anti interference ability of the company's homocysteine test kit (enzymatic cycling method) to meet the requirements of clinical anti interference ability. Clinical institutions should establish a correct in vitro diagnostic reagent anti-interference ability to verify the program, to ensure that the use of products to meet the quality requirements, to protect the legitimate interests of hospitals and patients.【Key words】Anti interference ability verification;Relative deviation;In vitro diagnostic reagents随着中国卫生医疗事业发展,我国体外诊断试剂生产厂家越来越多,目前约300~400家,其中规模以上企业近200家,但年销售过亿元的企业仅有20家左右,相对于国外成熟市场,国内厂家普遍规模小、品种少[1]。
体外诊断试剂不合格品控制与纠正和预防措施

体外诊断试剂不合格品控制与纠正和预防措施
1.应制定对不合格品控制的有关职责、权限的规定。
2.对不合格品进行标识、隔离、专区存放,防止不合格品非预期使用,并按照不合格品控制程序进行及时处理并保存记录。
(奥咨达医疗器械咨询)
3.质量管理部门应会同相关部门对不合格品进行评审,确认产品不合格原因,并采取相应的纠正和预防措施。
应保存评审和纠正和预防措施的记录,并在采取纠正或预防措施之后应验证其有效性。
产品销售与客户服务控制
1.企业应建立销售记录。
根据销售记录能追查每批产品的销售情况,必要时应能及时全部召回。
销售记录内容至少应包括:品名、批号、效期、数量、收货单位和地址、联系人、发货日期、运输方式。
销售记录应保存至产品有效期后一年。
(只专注于医疗器械领域)
2.应指定部门负责调查、接收、评价和处理顾客反馈意见,保持记录并定期汇总和分析用户反馈信息,及时通报相关部门,采取必要的纠正和预防措施。
3.生产企业应建立产品退货和召回的程序,并保存记录。
退货和召回记录内容应包括:品名、批号、规格、效期、数量、退货和召回单位及地址、退货和召回原因及日期、处理意见。
因质量原因退货和召回的产品,应在质量管理部门监督下销毁。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
体外诊断试剂干扰因素及其消除方法
1、非特异性干扰
1)疏水作用
原理:反应环境中存在的疏水性的物质,如样本中的脂肪/细菌/细胞碎片……与Ag/Ab或胶乳通过疏水作用结合,产生假阳。
处理方式:表面活性剂或亲水聚合物分解。
2)补体
补体(complement,C)就是存在于正常人与动物血清与组织液中的一组活化后具有酶活性的蛋白质。
原理:Ab的Fc段与C1q补体结合位点暴露,激活血清中的补体分子与包被或标记Ab结合,产生假阳。
处理方式:通过EDTA(络合剂)处理样本。
3)类风湿因子
类风湿因子(rheumatoid factor,RF)就是针对IgG Fc片段上抗原表位的一类自抗体,一般为IgG与IgM。
原理:人血清中的类风湿因子(RF)与包被或标记Ab的Fc片段结合产生假阳。
处理方式:使用无Fc片段的Fab片段抗体动物IgG中与。
2、异噬性抗体
异嗜性抗体就是指能够结合动物抗体而干扰免疫分析的所有人源抗体。
包括:①人抗鼠抗体(Human Anti-More Antibodles HAMA)
②人抗山羊抗体(HAGA)
③人抗兔抗体(HARA)
异嗜性抗体从何而来?
a动物接触(驯兽师、兽医)
b动物产品接触(烹饪)
c动物辅助治疗(胸腺细胞、羊细胞、胚胎细胞)
d食物(奶酪)
e注射疫苗
f输血
g自身免疫性疾病
h母婴传递
I心脏病变秘方药物
异嗜性抗体干扰的原理
3、什么就是阻断剂
阻断剂就是一种可结合异嗜性抗体,从而有效防止异嗜性抗体介导的免疫分析干扰的生物制剂。
1)阻断剂类型
a被动阻断剂:非特异性物质(鼠IgG等),结合异嗜性抗体的亲与力弱。
b主动阻断剂:能特异性结合人类异嗜性抗体,结合异嗜性抗体的亲与力强。
2)常见的阻断剂
4、怎样确认干扰
1)同一样本采用不同检测方法,若结果不一致说明可能存在干扰物。
2)将样本倍数稀释后再检测,若检测值呈非线性,说明存在干扰物。
3)同一样本添加阻断剂与为添加阻断剂的检测结果不一致,说明存在干扰物。
4)同一样本56℃灭活半小时与不灭活检测结果不一致,说明可能存在不补体干扰。
